Introducción
La aplicación de fuerzas ortodóncicas (FO) sobre las piezas dentarias, aún cuando sean bien controladas (FOC), produce en la mayoría de los casos una serie de alteraciones en la pulpa dental. En su histórico trabajo de 1954, Massler y Malone 1 consideran que este problema se agrava todavía más cuando las FO no son controladas (FONC) y pasan a ser excesivas (FOE), especialmente si no se procura un período de reposo luego de que el movimiento de la pieza haya sido realizado. La aplicación de FO es universalmente considerada un tipo de trauma, por lo que no es extraño que la pulpa, la estructura radicular y los tejidos de soporte sufran cambios que, en el peor de los casos, pueden ser irreversibles. 2
En el presente trabajo se analizan el impacto de las FOE en relación con diferentes factores tales como la salud pulpar y el grado de reabsorción radicular (RR) —tanto en dientes con pulpa vital como en aquellos que han recibido un tratamiento endo-dóntico o un traumatismo previo— y el rol que puede desempeñar el tratamiento endodóntico en la posible resolución de las diferentes patologías provocadas.
Desarrollo
Impacto de las FOE sobre la pulpa dental
La alteración de los tejidos pulpares es una consecuencia constante de la aplicación de FOE sobre los dientes, y la gravedad de las lesiones resultantes se incrementa de forma proporcional al aumento de la intensidad de las fuerzas. Estas lesiones se producen fundamentalmente por la alteración del sistema neu-rovascular, que propicia la liberación de neurotrans-misores específicos (neuropéptidos). 3 Los neuropép-tidos influyen a su vez en la circulación sanguínea y el metabolismo celular. 4 , 5 La ruptura de los vasos sanguíneos provenientes del periodonto que irrigan la pulpa a través del foramen apical es, en última instancia, el factor más influyente sobre el futuro de la salud pulpar. En una etapa inmediatamente anterior a la ruptura, la compresión de los vasos durante el movimiento de la pieza dentaria hace que disminuyan los niveles de respiración (hipoxia) de las células pulpares y se reduzca la formación y la liberación de la fosfatasa alcalina. 5 La tasa de respiración celular se reduce a casi un 27% durante la aplicación de FOC y aún más en presencia de FOE. 5 Esto ocurre con cierta frecuencia en dientes con ápices completamente desarrollados, mientras que en los dientes con ápices inmaduros la actividad dentinogénica no experimenta cambios importantes, siempre y cuando no reciban FOE y se mantengan los períodos de reposo necesarios para la estabilización de los tejidos luego de efectuado el desplazamiento de la pieza dentaria. 6 En ese sentido, parecería que el grado de maduración dentaria juega un rol preponderante respecto de la tasa respiratoria de las células pulpares durante la aplicación tanto de FOC como de FOE. 5 La reducción de la tasa respiratoria se produce a partir de la alteración neurovascular mencionada, que conlleva a la destrucción progresiva de las mitocondrias en los odontoblastos y otras células pulpares. Las mitocon-drias son orgánulos pertenecientes al citoplasma celular, responsables de la producción de más del 90% de la energía necesaria para la actividad respiratoria de las células. Durante el proceso respiratorio, las mitocondrias producen la combustión de sustratos metabólicos provenientes de los hidratos de carbono y los ácidos grasos mediante un ciclo denominado “cadena transportadora de electrones y fosforilación oxidativa”. De esta manera, utilizan la glucosa y el oxígeno corporal para convertirlos y liberarlos como dióxido de carbono y ATP (energía). 4-8 Su actividad también es esencial en los procesos de termogénesis y en la regulación de los niveles del calcio intracelu-lar. La respuesta de la pulpa a la injuria producida por las FOE puede variar según la intensidad de estas. Tobon et al. 9 observaron, en pulpas de pacientes jóvenes, que la aplicación de FOE produce inicialmente la vacuolización y la degeneración de los odonto-blastos y de los tejidos pulpares (fig. 1A). Nixon et al. 10 y, más recientemente, Shameshima et al. 11 describen diferentes patologías progresivas tales como hiperemia inicial, dilatación y ruptura de vasos sanguíneos (microhemorragias) (fig. 1B), pulpitis irreversible, reabsorción dentinaria interna (fig. 1C-E), necrosis y RR. Los autores consideran que el grado de compromiso pulpar depende de factores como la intensidad, el punto de aplicación y la duración de las fuerzas. Todos estos procesos pueden estar exacerbados cuando preexisten patologías como caries, maloclusiones traumatizantes o diferentes grados de compromiso periodontal. Veberiene y Smailieneb 12 analizaron el efecto de las FOE sobre el estado de salud pulpar. Por su parte, Derringer y Lindem 13 informaron acerca de la presencia del factor de crecimiento derivado de plaquetas (PDGF), derivado del componente plaquetario y del factor de crecimiento epidérmico (EGF), ambos claramente detectables durante el movimiento ortodóncico, y sugieren que estos podrían participar activamente en la respuesta angiogénica de la pulpa durante la aplicación de FOE sobre las piezas dentarias.

Figura 1 A: Sección histológica de un premolar inferior extraído por razones ortodóncicas luego de 9 meses de iniciado el tratamiento, en la que se observa vacuolización y degeneración odontoblástica a nivel de la unión de los tercios coronario y medio (flecha) (p: pulpa; d: dentina; hematoxilina y eosina; magnificación original X100). B: Sección histológica de la pulpa de una pieza dentaria. Se puede observar la presencia de un vaso sanguíneo (flecha blanca) y un área hemorrágica (microhe-morragia) (flecha negra) (o: odontoblastos; d: dentina; hematoxilina y eosina; magnificación original X400). C-D: Radiografías de piezas dentarias con tratamiento ortodóncico, en las que se observan áreas de reabsorción dentinaria interna (flechas) detectadas 12 y 20 meses, respectivamente, después de iniciado el tratamiento. E: Sección histológica de una pieza dentaria a nivel del tercio medio de la raíz. Se pueden observar importantes áreas de reabsorción dentinaria interna con la presencia de dentinoclastos (flechas) (d: dentina; hematoxilina y eosina; magnificación original X1000).
En los casos en los que tanto las FOC como las FOE se apliquen de forma prolongada, sin períodos de reposo, resulta muy frecuente observar diferentes grados de calcificación de la pulpa. 8-18 Este fenómeno se denomina metamorfosis calcificante (MC) y aparece casi siempre como una aposición excesiva de dentina terciaria, generalmente acompañada por masas intrapulpares de calcificaciones distróficas que pueden incluso producir una obstrucción parcial o total del espacio del conducto radicular. 14 Bajo estas condiciones, este tipo de calcificación —aunque asintomática— es considerada patológica, y en los controles radiográficos de rutina suele observarse como la pérdida progresiva de la luz de la cámara pulpar y del conducto radicular (fig. 2A-E). La atrofia celular —mencionada anteriormente— reduce la capacidad reaccional reparativa de la pulpa y aumenta su susceptibilidad a las infecciones. Frente a la acción de FOE o de cualquier otro tipo de actividad traumática, e independientemente de la aposición de dentina terciaria sobre las paredes dentinarias, la aposición de tejido calcificado en el seno del tejido pulpar se produce a lo largo de las fibras colágenas o adyacentes a las paredes de los vasos sanguíneos (fig. 3A), lo cual la identifica con su origen neurovascu-lar y sostiene la teoría de que la dentina terciaria se forma a partir de células indiferenciadas perivascu-lares, e incluso a partir de algunas células endotelia-les, como una acción defensiva ante la aplicación de fuerzas traumáticas. 19 Aun en casos de obstrucciones de gran tamaño (fig. 3B-D), se ha comprobado que suele quedar un mínimo espacio del conducto (no de-tectable en las radiografías) con pulpa vital (fig. 3E), que a lo largo del tiempo evoluciona hacia la necrosis. 14 , 15 En los períodos iniciales, la MC coexiste con un aumento desproporcionado del colágeno; al ser asintomática, muchos investigadores tienden a minimizar la importancia de este fenómeno, y recién determinan la necesidad de tratamiento endodóntico cuando la radiografía evidencia la presencia de un área radiolúcida perirradicular que podría indicar necrosis en la pulpa, generalmente no aséptica. Rock y Lundi 19 recomiendan realizar el tratamiento no bien se detecte en los controles a distancia que la luz del conducto comienza a reducirse, y sugieren no dilatar su ejecución mientras sea posible acceder a la cámara y al conducto radicular sin dificultades. 16-19 Los resultados del tratamiento endodóntico en dientes con MC suelen ser muy alentadores. Sobre una cohorte de 54 pacientes en los que el estudio radiográfico reveló que la MC de incisivos superiores había avanzado abruptamente disminuyendo el espacio del conducto radicular y la presencia de áreas radiolúcidas perirra-diculares, Cvek et al. 20 informaron 80,4% de tratamientos exitosos realizados de manera preventiva.

Figura 2 A: Fotografía clínica de un paciente de 10 años con tratamiento ortodóncico. A los 14 meses posoperatorios el paciente discontinuó el tratamiento. B: Radiografía de control en la que se observa un inicio de estrechamiento de la luz del conducto radicular de la pieza 11. C: Una radiografía de control a los 20 meses posoperatorios muestra la calcificación progresiva del espacio del conducto (flecha). D: Radiografía de control a los 28 meses posoperatorios, en la que la luz del conducto radicular ha quedado prácticamente anulada. Se puede observar la presencia de una pequeña área radiolúcida apical (flecha). E: Sección histológica de una pieza dentaria con una calcificación casi total del espacio del conducto radicular (flecha negra) con la persistencia de algunas células inflamatorias (flecha blanca) (d: dentina; hematoxilina y eosina; magnificación original X800).
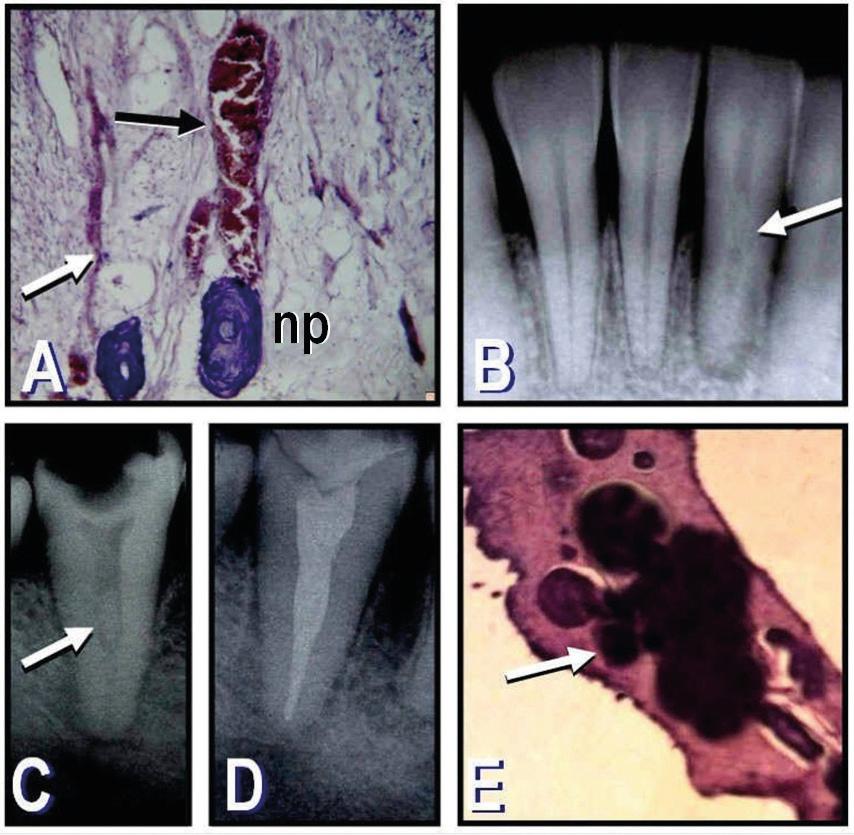
Figura 3 A: Sección histológica de la pulpa coronaria de un incisivo central superior obtenida durante un tratamiento en-dodóntico. Se observa un nódulo pulpar (np) en íntima relación con la pared de un vaso sanguíneo de gran tamaño (flecha negra). Se puede ver también un segundo nódulo en contacto con un vaso de menor calibre (flecha blanca) (hematoxilina y eosina; magnificación original X400). B: Radiografía de control de la pieza dentaria 32 asintomática obtenida luego de 2 meses de finalizado un movimiento ortodóncico. Se observa la anulación del espacio del conducto radicular a nivel del tercio medio (flecha), la presencia de un área radiolúcida perirradicular y el ensanchamiento del ligamento periodontal a nivel de la cresta ósea. C: Radiografía periapical de un molar inferior luego de dos años de finalizado un tratamiento ortodóncico. Se nota la presencia de una masa radiopaca (no observada en las radiografías preoperatorias) compatible con un nódulo pulpar de gran tamaño a nivel del tercio medio (flecha). D: Radiografía posoperatoria inmediata luego de realizado el tratamiento endo-dóntico. E: Sección histológica parcial de la pulpa extraída durante el tratamiento. Se observa la presencia de una gran masa calcificada formada por la unión de varios nódulos pulpares (flecha) (hematoxilina y eosina; magnificación original X1000).
Impacto de las FOE sobre el grado de RR
La reabsorción cemento-dentinaria externa de carácter fisiológico es permanente, tanto en el ser humano como en los demás mamíferos, y se manifiesta como respuesta a las presiones naturales ejercidas por la masticación y otros movimientos funcionales.
Por lo tanto, debe ser netamente diferenciada de la RR de tipo patológico producida por traumatismos o la aplicación de FOE durante el tratamiento ortodón-cico, generalmente acompañada de un cuadro inflamatorio del ligamento periodontal (fig. 4A). La RR que responde a mecanismos fisiológicos es en realidad un proceso combinado continuo de reabsorción y neoformación de cemento compensatorio (fig. 4B), siempre que la dentina no haya sido afectada. Cuando la dentina es afectada durante la aplicación de FO continuas sin suficientes períodos de reposo, la RR puede transformarse en un proceso claramente patológico 2 (fig. 4C). La inflamación periodontal y la frecuente contaminación bacteriana de los conductillos dentinarios favorecen la continuación progresiva e irreversible de la RR. En los casos en los que la reabsorción se manifiesta en la zona cervical, la invasión bacteriana es casi una norma a causa de la pérdida de adherencia epitelial. Esto favorece la persistencia de la reacción inflamatoria e impide la aposición de nuevo cemento. 21 En esa situación, la exposición de la dentina a las células clásticas constituye el punto de partida para el desarrollo de la RR patológica. El impacto de las FOE sobre la RR ha sido ampliamente analizado por diferentes investigadores. 21, 22 En ese sentido, se ha demostrado que existe una correlación definida entre el grado de RR y la intensidad de las fuerzas. Durante la aplicación de FOC se pueden perder aproximadamente 0,5-2 mm de longitud del tercio apical, mientras que en el caso de las FOE la pérdida radicular puede superar los 4 mm de longitud, muchas veces de manera conjunta con pérdida de cemento y dentina en la superficie mesial y/o distal de la raíz. 21 Es interesante comprobar que el manejo adecuado de las FO disminuye significativamente este problema. Por el contrario, el 80% de los pacientes que reciben FOE desarrollan una RR de importancia. 23 El tipo de aparatología utilizada y el tiempo durante el que se aplican las fuerzas también influyen significativamente. Jiang et al. 21 observaron que factores como el rango etario, el género o el tipo de pieza dentaria no parecen tener una influencia significativa en la RR. Sin embargo, también comprobaron que las FOE producen diferentes grados de reabsorción, generalmente graves, sobre la estructura radicular y ósea, en especial en dientes que han sufrido algún tipo de traumatismo o recibido un tratamiento endodóntico. Con respecto a esto, la literatura relacionada es escasa. Si una pieza dentaria ha experimentado un traumatismo previamente y desarrolla una RR, el cuadro clínico resulta aún más complicado. Wickwire et al . 23 comprobaron que los dientes que han recibido un tratamiento endodóntico son más proclives a sufrir una RR ante las FONC. Iglesias-Linares et al. 22 demostraron que en dientes con pulpa vital esta cumple un rol defensivo importante gracias a la actividad del grupo de la interleu-quina-1, un mediador proinflamatorio implicado en el movimiento ortodóncico de las piezas dentarias, y que las variaciones genéticas que puede sufrir la interleuquina-ip en el periodonto predisponen a una mayor proporción de RR en los dientes con tratamiento endodóntico previo (incluso en aquellos sin patología perirradicular), en comparación con los dientes con pulpa vital utilizados como control. Sin embargo, la incidencia de RR en dientes con o sin tratamiento endodóntico previo sigue siendo tema de discusión. 24 El consenso general entre los especialistas es que los dientes con tratamiento endodóntico sufren RR con mayor intensidad cuando han recibido algún tipo de traumatismo previo. Más aun, la mayoría de los investigadores piensan que si la pulpa mantiene su vitalidad y no existe infección no se indicaría tratamiento endodóntico. En estos casos, el control de la vitalidad pulpar a lo largo del tratamiento ortodóncico resulta fundamental, ya que bajo la acción de FOE y/o en ausencia de períodos adecuados de reposo la pulpa suele evolucionar a una necrosis, lo cual hace necesarios el tratamiento endodóntico y la suspensión de las fuerzas aplicadas sobre la/s pieza/s dentaria/s afectada/s por un período de tiempo razonable. 24 , 25 Durante el movimiento de un diente, tanto las FOC como las FOE producen microtraumatismos sobre el ligamento periodontal en la zona de compresión, donde inicialmente se desarrolla una zona hialina y posteriormente necrosis, poniendo en marcha finalmente la función de células inflamatorias y la liberación de factores activadores de células clásticas (cementoclastos y osteoclastos). 26 En casos de FOC, los períodos de reposo entre una y otra activación de fuerzas permiten la reorganización del ligamento periodontal y el restablecimiento del flujo sanguíneo. 26 , 27 Por el contrario, la persistencia de la acción de las FOE y la ausencia de períodos de reposo impiden la restauración mencionada; por lo tanto, la tasa de RR aumenta significativamente y se transforma en un problema netamente iatrogéni-co. 27 Ante este tipo de situación, Villa et al. 28 han experimentado con la prescripción de una medicación antiinflamatoria, pero los resultados no fueron concluyentes. Las radiografías panorámica y periapical son elementos de uso frecuente para el diagnóstico y la detección de la RR. Sin embargo, se ha demostrado que la tomografía computarizada de haz cónico (CBCT) es mucho más sensible para la detección de estos cambios patológicos. 29 , 30
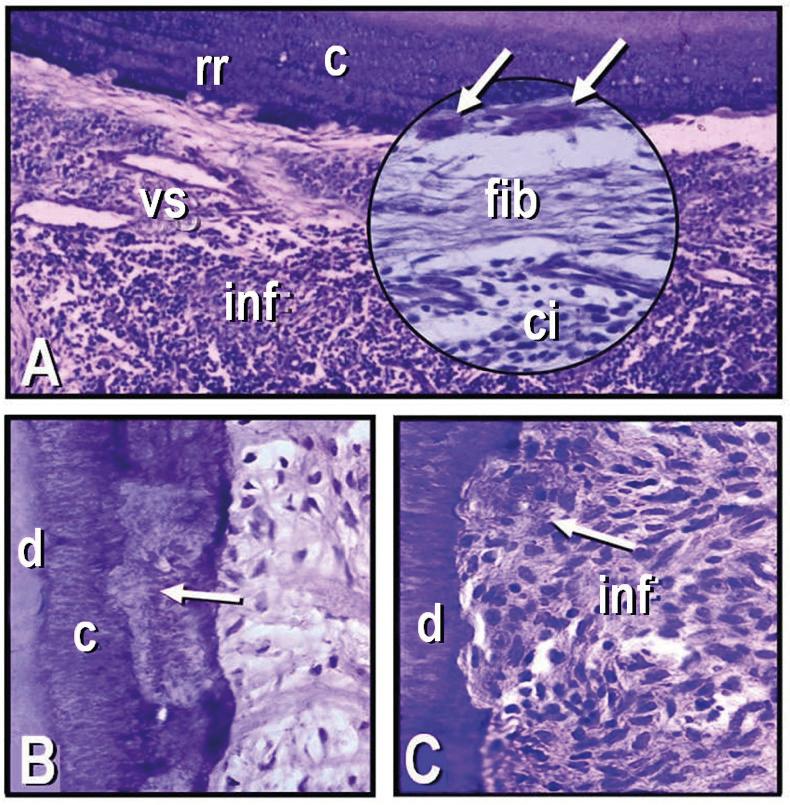
Figura 4 A: Sección histológica de un premolar superior extraído luego de 12 meses de iniciado un tratamiento ortodóncico. Se puede observar el cemento radicular (c), áreas de reabsorción radicular (rr), vasos sanguíneos (vs) y gran concentración de células inflamatorias en el ligamento periodontal (inf) (hematoxilina y eosina; magnificación original X100). Dentro del círculo y a mayor aumento, se observan dos cementoclastos linderos a un área de RR (flechas), fibroblastos (fib) y células inflamatorias (ci) (hematoxilina y eosina; magnificación original X400). B: Sección histológica de una pieza dentaria en la que se observa un área de reabsorción que solo involucró al cemento radicular (c), compensada por la aposición de nuevo cemento (flecha) (d: dentina; hematoxilina y eosina; magnificación original X1000). C: Sección histológica de un área de reabsorción cemento-dentinaria externa. El ligamento periodontal contiene una gran concentración de células inflamatorias (inf) y una célula clástica de gran tamaño (flecha), además de macrófagos y otras células inflamatorias linderas al área de reabsorción (d: dentina; hematoxilina y eosina; magnificación original X1000).
Estrategias de tratamiento
Las RR asociadas a un tratamiento ortodóncico
constituyen un verdadero desafío para el especialista. Para estos casos, se han propuesto diferentes modalidades de tratamiento. En términos generales, es necesario disponer de una historia clínica completa, un diagnóstico y el análisis del tipo y el grado de RR, además de datos de importancia como higiene, edad, género, historia previa de estrés o traumatismos, vitalidad pulpar, determinación de la proximidad de la raíz a la cortical alveolar, densidad del tejido óseo (mediante CBCT), maloclusión, presencia de áreas radiolúcidas perirradiculares, y considerar también las posibilidades futuras de supervivencia de cada caso en particular. Los factores sistémicos como diabetes, 11 alergias 31 e hiperparatiroidismo secundario 32 son de suma importancia, por lo que deben ser considerados. Jilka et al. 32 demostraron que el aumento de los valores normales de la hormona paratiroidea (PTH) acelera significativamente los procesos de reabsorción ósea y radicular bajo la aplicación de FO, y aún más cuando se ejercen FOE. La preparación y la desinfección del sistema de conductos radiculares debe ser minuciosa y su obturación, realizada con materiales que promuevan y estimulen la reparación mediante la aposición de tejido calcificado. Una de las opciones tradicionales sugeridas por Murata et al ., 31 Tronstad et al. 33 y Fuss et al. 34 es el empleo de una medicación intraconducto con hidróxido de calcio y un adecuado sellado de la cavidad de acceso para evitar la posterior invasión bacteriana. El pH alcalino del material produce necrosis aséptica, inhibiendo la acción de las células clásticas, limitando la de los lipopolisacáridos y favoreciendo la de la fosfatasa al-calina. 33 , 34 El inconveniente del hidróxido de calcio es su acción autolimitante, además de que se solubiliza y reabsorbe con facilidad. Por esa razón, se necesita realizar recambios frecuentes del material, cuando radiográficamente se aprecie que se ha iniciado el proceso de reparación o se encuentra en una etapa avanzada. Es entonces el momento adecuado para realizar la obturación con un compuesto de trióxidos minerales (MTA, MTA Plus) u otros biocerámicos de última generación. 35 Otro inconveniente muy común en relación con esta opción de tratamiento es la falta de constancia de algunos pacientes para concurrir a las sesiones intermedias para los recambios del material. Por el contrario, la ventaja de utilizar el hidróxido de calcio radica en la facilidad con que se puede reingresar en el conducto radicular para realizar el retratamiento en el caso de un fracaso a distancia. Otros autores prefieren obturar con MTA de forma inmediata o bien hacerlo luego de una medicación intraconducto con hidróxido de calcio por 7 días. 36 El inconveniente de este procedimiento es que, ante la posibilidad de un fracaso a distancia, la extrema microdureza del material hace muy difícil —y a veces imposible— reingresar en el conducto radicular para removerlo. 37-40
En cualquiera de las opciones de tratamiento sugeridas, la tasa de éxito suele ser de 75-80%. 3, 22-24 En otros casos, la gravedad de la lesión, una obturación y un sellado coronario defectuosos, la presencia de alteraciones sistémicas u otros factores externos difíciles de controlar hacen que el fracaso a distancia sea más frecuente. 31 , 32
Conclusiones
Las FO ejercidas sobre las piezas dentarias son causantes de alteraciones pulpares de tipo degenerativo o inflamatorio, especialmente en dientes con ápices completamente formados. Estas alteraciones están íntimamente relacionadas con el sistema neu-rovascular, en el que la liberación de neuropéptidos influye negativamente sobre la circulación sanguínea y el metabolismo pulpar por la reducción o la eliminación de la respiración celular. Además, pueden favorecer el desarrollo de RR, tanto durante la aplicación de FOC como de FOE.
Los dientes con tratamiento endodóntico están expuestos a una mínima proporción de RR durante el tratamiento ortodóncico con FOC, siempre y cuando no hayan recibido traumatismos previos. En el caso de que haya habido episodios traumáticos anteriores al tratamiento ortodóncico, los dientes pueden ser sometidos a un desplazamiento si la pulpa se mantiene vital y sin contaminación bacteriana. En el caso contrario, el tratamiento endodóntico está indicado previamente a la aplicación de FOC, las que no deberían iniciarse o reiniciarse hasta que no se compruebe, mediante controles clínicos y radiográficos a distancia, que el proceso de reparación se completó y se encuentra estable. La mayoría de los investigadores sugieren iniciar o reiniciar el tratamiento mediante la aplicación de fuerzas de baja intensidad, bien controladas y con períodos de reposo que permitan la reparación de los tejidos periodontal y óseo, así como del cemento radicular después de cada desplazamiento dentario.














