INTRODUCCIÓN
Las mejoras en las tecnologías endovasculares y el desarrollo de endoprótesis estándares o a medida nos permiten, actualmente, tratar lesiones aórticas complejas, como disecciones o aneurismas toracoabdominales. 1,2,3 Estos avances están conduciendo a un aumento en la complejidad de los procedimientos endovasculares, lo que implica la necesidad de una mayor precisión y calidad de imágenes, largos tiempos de procedimiento y altos niveles de exposición a la radiación. 4,5. A su vez, se ejerce presión sobre los profesionales dedicados a la cirugía vascular para mostrar habilidades intervencionistas y prácticas radiológicas cada vez más eficientes.
En este contexto, la tecnología de imagen avanzada representa un pilar sólido en la caja de herramientas destinadas a brindar la mejor atención con el menor riesgo.
Apoyados en esa tecnología, presentamos en este artículo nuestra experiencia inicial con la reparación de aneurismas aórticos complejos mediante la colocación endovascular de endoprótesis fenestradas construidas a medida en quirófano, empleando moldes de impresión tridimensional.
Dividimos la presentación en dos apartados: planeamiento y procedimiento.
Tecnologías de imágenes para el planeamiento quirúrgico
Tomografía de energía dual
La tomografía computarizada con tecnología de energía dual consiste en la adquisición de imágenes a través de niveles variables de energía de rayos X y su comparación. Dependiendo de la tecnología utilizada, la adquisición podrá ser a través de la emisión por dos fuentes de rayos X, una sola fuente emisora con switching de Kv o con tecnología espectral de detectores que permite aprovechar los rayos X de mayor y menor energía en una sola exploración.
El conocer cómo se comporta una sustancia en particular ante dos energías diferentes de rayos X puede proveer información acerca de la composición tisular, más allá de la que se puede inferir con técnicas que emplean un solo nivel de energía de rayos X. La nueva tomografía de energía dual (TC espectral) se ha convertido en una herramienta prometedora, con múltiples aplicaciones clínicas. 3,4,5,6. Con su capacidad de caracterización de elementos sobre la base de la comparación entre el efecto fotoeléctrico y el efecto Compton, permite la atenuación diferencial de tejidos y materiales pudiendo ayudar a identificar la composición de estructuras, entre las cuales podemos contar la diferenciación entre yodo intravascular de placas ateroscleróticas calcificadas o materiales quirúrgicos sobre la base de sus valores de atenuación diferencial. Además, la TC de energía dual es capaz de reducir sustancialmente los artefactos causados por las prótesis metálicas, eliminar el calcio de placas ateroscleróticas calcificadas mejorando la evaluación del grado de estenosis.
Al aumentar la visibilidad del yodo, la TC de energía dual con contraste puede hacer que un endoleak sea más evidente en comparación con la TC convencional, distinguiéndolo de materiales quirúrgicos (coils o stents). Una ventaja adicional de la reconstrucción de bajo KeV es que también se puede usar para amplificar la densidad del material de contraste EV en estudios angiográficos con opacificación subóptima de la luz vascular, ya sea por pacientes con mala función ventricular, cuando hay falla en el bolo o extravasación parcial del material de contraste, o en pacientes en los cuales se utiliza poco material de contraste en relación a condiciones médicas preexistentes. Finalmente, reduce sustancialmente la dosis de radiación administrada al paciente, al eliminar la necesidad de una primera adquisición sin contraste.
Reparación endovascular de aneurismas complejos mediante endoprótesis fenestradas construidas en quirófano por impresión tridimensional
La reparación endovascular de aneurismas mediante endoprótesis fenestradas se utiliza con frecuencia para los aneurismas aórticos yuxtarrenales, pararrenales y toracoabdominales. En la actualidad, tras un análisis profundo de la anatomía arterial, se construyen industrialmente dispositivos que, mediante fenestraciones (orificios), permiten incorporar el segmento visceral de la aorta dentro del territorio a recubrir. Lamentablemente, es necesario esperar entre 8 y 10 semanas para contar con estos dispositivos, lo que hace impracticable su utilización en casos urgentes. 6,7 Como solución a dicho problema, se pueden implantar endoprótesis modificadas por el médico en el quirófano a partir de un injerto estándar, confeccionando las fenestraciones de acuerdo con la anatomía del paciente. Pero esto requiere de una planificación precisa. A pesar de la experiencia, siempre existe un margen de error. La posibilidad de desalineación entre la fenestración y el ostium del vaso a respetar, puede conducir a un mayor tiempo de canulación y complicaciones en el momento de colocar el stent, incluida la pérdida del vaso.
Por otro lado, reconocemos que la incorporación relativamente lenta de la tecnología de endoprótesis fenestradas se relaciona, al menos en parte, con la planificación del caso y la complejidad del procedimiento. Una evaluación crítica de la aplicabilidad de esta técnica requiere comprender cómo, por ejemplo, la angulación aórtica afecta las mediciones de la distancia entre fenestraciones. La planificación de las fenestraciones en la anatomía aórtica con una leve angulación es bastante sencilla, y los resultados deben ser similares entre la planificación del software convencional y el plan generado por una reproducción anatómica 3D de la aorta del paciente. Sin embargo, la mayoría de los pacientes con aneurismas yuxtarrenales tienen aortas viscerales anguladas, de hasta 60 grados o más. Nosotros hemos aprendido que es importante tener en cuenta la alteración en el eje aórtico, que significa la colocación de una guía rígida y el introductor con la endoprótesis adentro y la aorta angulada. No realizar este ajuste en la línea central conduce a errores significativos en las mediciones de distancia requeridas para ubicar correctamente las fenestraciones. Como consecuencia, dicho error conduce a una difícil canulación de la rama durante la colocación del implante. Con aneurismas yuxtarrenales con gran angulación, aparecen dichas discrepancias de fenestración de 1 a 3 mm entre el plano convencional y la plantilla impresa en 3D. Resulta así tentador imprimir una réplica exacta de la aorta visceral con fines de planificación, introduciendo la angulación aórtica, para alinear correctamente los orificios de la endoprótesis a la arteria que se debe respetar.
La impresión aórtica tridimensional se ha descrito ampliamente en medicina para simulación, entrenamiento y planificación quirúrgica. 8,9
Describimos una técnica eficaz que utiliza un software de diseño asistido por computadora para crear un modelo 3D aórtico real 1:1, que se puede imprimir con facilidad y esterilizar rápidamente. Para tal fin, un proveedor externo (MIRAI 3D, Buenos Aires) asociado a nuestras instituciones realizó el modelado y la impresión. Para generar un modelo 3D para el molde de la prótesis, se parte de una tomografía computarizada con contraste arterial. Usando software de segmentación de estructuras anatómicas, se hace un barrido de contraste en la tomografía del paciente, dejando visibles solamente la aorta y sus ramas. Sobre este modelo se aplica un suavizado con un software de modelado 3D orgánico. Usando la aorta como base, se colocan guías normales a las salidas de las arterias renales, la arteria mesentérica superior y el tronco celíaco. Al extruir las paredes de la aorta se genera el molde, que luego será impreso. Se hace el recorte de las salidas de las arterias. Una vez generados los moldes, se opta por la tecnología de estereolitografía para la impresión de los modelos, ya que esta brinda una terminación superior a las tecnologías de FDM (modelado por deposición fundida). Se utiliza la impresora Form 2 de la empresa Formlabs, empleando la resina “Clear” para los modelos rígidos, y la resina “Elastic” (con una dureza de 50A Shore y elongación del 160%) para los modelos flexibles. Se crea, entonces, una plantilla personalizada que sirve como guía específica del paciente para la fenestración del injerto. Se esteriliza por plasma de peróxido de hidrógeno en un equipo Sterrad, con un ciclo exprés, que permite la rápida esterilización de materiales delicados. Con la impresión ya preparada, la endoprótesis estándar se coloca dentro del modelo, se despliega, y las ubicaciones de las aberturas del modelo (fenestraciones) se marcan con una pluma estéril sobre la endoprótesis. Las fenestraciones se confeccionan con un dispositivo de electrocauterización y se refuerzan con un material resistente y radiopaco, para permitir la visualización con los RX (Figura 1).
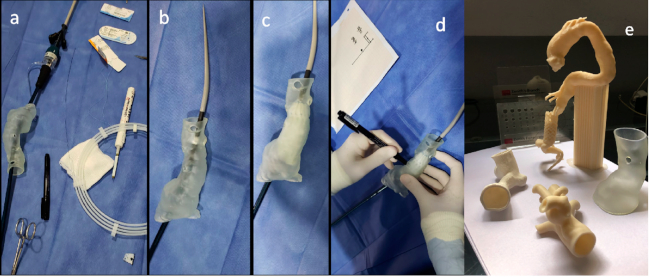
Fig. 1 Distintos materiales y pasos necesarios para confeccionar una fenestración en un paciente con las arterias renales a nivel del cuello proximal, en plan de colocación de una endoprótesis fenestrada (a-d). Algunos modelos de impresión 3D (e), fabricados con distintas finalidades (fenestraciones, información a pacientes, táctica quirúrgica).
Este modelo aórtico es utilizado para crear una endoprótesis fenestrada de manera precisa, con la potencialidad de generar procedimientos más cortos y seguros. Si bien se trata de una experiencia inicial, distintas publicaciones han mostrado a la impresión 3D como una herramienta valiosa para planificar, diseñar y crear dispositivos con mayor exactitud.
También es una herramienta eficaz para la enseñanza y el entrenamiento de médicos en procedimientos complejos, lo que permite reducir la curva de aprendizaje. Simular todos los pasos quirúrgicos complicados por adelantado, usando modelos prototipo, puede ayudar a prever complicaciones intra- y posoperatorias. Este es otro uso, que, conjuntamente con las tecnologías de videoconferencias, se viene desarrollando en nuestro medio. Algunos estudios muestran cómo la visualización 3D, en lugar de la pantalla 2D, ha ayudado en la preplanificación operativa, tanto para elegir el camino como para modificar una decisión tomada anteriormente. La impresión 3D, en estos casos, se utiliza para mejorar la visualización. Para eso, también diseñamos modelos, con la finalidad de mostrar distintas alternativas técnicas y tácticas para tratamientos complejos. Mediante impresiones 3D de casos reales, estamos capacitando a distancia sobre detalles técnicos finos en colocación de endoprótesis. Dichos modelos 3D reales, que replican la anatomía exacta de la aorta enferma, con una imagen clara del proceso patológico (Figura 2).

Fig. 2 Imagen tomográfica (a) de la cual se extrae la impresión 3D (b). Se utiliza dicha impresión para el entrenamiento en colocación de endoprótesis ramificada ilíaca (c).
Por último, mediante el uso de la impresión 3D, los cirujanos podemos explicar más fácilmente a los pacientes su situación clínica y el tipo de cirugía a la que se someterán. Publicaciones recientes han demostrado que el uso de la impresión 3D contribuye positivamente a fortalecer la decisión que toman los pacientes y aumenta su “consenso” para el tratamiento quirúrgico (Figura 2)
Tecnologías de imágenes útiles durante el procedimiento
Durante la implantación de una endoprótesis hay cuatro herramientas imagenológicas que nos son fundamentales para obtener un buen resultado y a la vez cuidar al paciente y al equipo tratante. Las imágenes desempeñan un papel fundamental en todas las fases del tratamiento endovascular del aneurisma de aorta, desde la planificación, pasando por la colocación y terminando en el seguimiento. Mientras que las modalidades de imágenes avanzadas se han convertido en una rutina para las fases de planificación y seguimiento después de procedimientos complejos, en particular, la angiografía y la fluoroscopía han seguido siendo las técnicas de imagen intraoperatorias de elección durante muchos años. La introducción de imágenes intraoperatorias avanzadas para la guía y el control del procedimiento tiene el potencial de reducir el uso perioperatorio de contraste y radiación, de mejorar el éxito intraoperatorio y de disminuir la necesidad de intervenciones secundarias posoperatorias. La aplicación de estas técnicas requiere, obviamente, de equipos de imagen avanzados dentro del quirófano.
Sistemas de imágenes de baja radiación
Los equipos modernos poseen un flat panel de 48 pulgadas como detector, que captura información con una resolución cuatro veces mayor que los sistemas convencionales de rayos X, con visualización de imágenes, acceso multimodal, monitoreo hemodinámico e informes integrados. Generan una amplia visualización en 3D de patologías a partir de una sola angiografía rotacional realizada en unos pocos segundos. Pero, probablemente, el más importante de estos adelantos sea la tecnología ClarityIQ, que es el último avance en reducción de la exposición a la radiación para los pacientes y el personal médico. Esta tecnología mantiene una calidad de imagen equivalente, con un nivel de dosis radicalmente menor. Esto ayuda a reducir la dosis de radiación como una barrera para los nuevos y más complejos procedimientos y técnicas.
Vessel Navigator o fusión de imágenes
Nuestras modernas salas están equipadas con una amplia gama de nuevas aplicaciones de imágenes, como imágenes de fusión y tomografía computarizada de haz cónico (CBCT). Estas tecnologías contribuyen a reducir la radiación mediante un software que permite realizar procedimientos endovasculares complejos, seguros y eficientes. Una de las mayores virtudes de esta tecnología es la fusión de imágenes. Mediante un software especialmente diseñado se pueden fusionar las imágenes de tomografía capturadas previamente, con las imágenes en vivo, que, por radioscopía, se obtienen en la sala quirúrgica. En otras palabras, sin inyectar contraste se puede saber cuál es el lugar donde debe ser desplegada la endoprótesis, o dónde es el nacimiento de la arteria renal sobre la cual hay que dejar su respectiva fenestración. 8,9,10,11 La imagen de fusión implica cuatro pasos para lograr una óptima ubicación intraoperatoria: el procesamiento de la angiotomografía (ATC) preoperatoria, la selección de los puntos de referencia en la ATC preoperatoria, la adquisición de un volumen intraoperatorio usando la CBCT y la fusión entre la imagen obtenida intraoperatoriamente (CBCT) y la ATC preoperatoria. De esta manera, se acorta significativamente el tiempo de la cirugía y se reduce la cantidad de sustancia de contraste y la dosis de radiación (Figura 3).
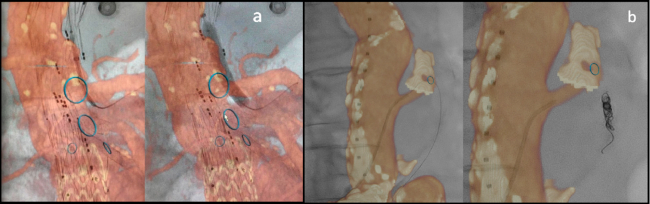
Fig. 3 Dos secuencias en las que se utilizó fusión de imágenes. En la de la izquierda (a), la imagen en tonos naranja, que corresponde a la angio-TC previa, se fusiona con la imagen en tonos de gris, correspondiente a la imagen angiográfica en vivo. Se canula el tronco celíaco en el caso de una endoprótesis ramificada. En la imagen de la derecha (b), el anillo celeste muestra el origen de la arteria mesentérica inferior que va a ser embolizada con coils para evitar un endoleak tipo II.
Ultrasonografía intravascular
La ultrasonografía intravascular (IVUS) permite obtener imágenes en tiempo real del vaso y es ideal para intervenciones aórticas. El IVUS proporciona información precisa para evaluar las vías de acceso, la ubicación y las distancias entre ramas de la aorta, así como el tamaño del vaso, para determinar el tamaño del injerto o lesiones asociadas, lo que facilita la realización de procedimientos endovasculares aórticos complejos. Por otra parte, el uso de IVUS reduce la necesidad de dosis altas de contraste y radiación en la mayoría de los procedimientos, ya que reemplaza la angiografía en muchas instancias. El IVUS nos da la seguridad de navegar en la luz verdadera, en el caso de disecciones tanto agudas como crónicas (Figura 4). Junto con la hoja de ruta en 3D basada en técnicas de fusión, el IVUS puede ubicar los tears de entrada y reentrada, el flujo en la falsa luz y el tamaño de las respectivas luces, incluso antes de la fluoroscopía. Estas imágenes, que también se pueden guardar, pueden usarse como guía (sobre la base de puntos de referencia óseos) para el despliegue correcto de la endoprótesis. 12,13
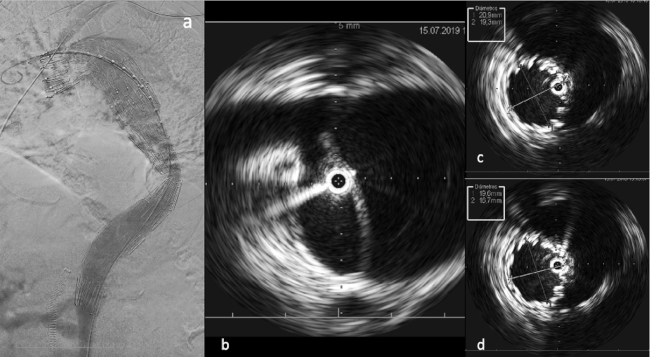
Fig. 4 Imagen de ecografía intravascular. Angiografía final que demuestra la exclusión de la falsa luz en un paciente con una disección aórtica tipo B (a). Las imágenes por IVUS muestran, que la guía por donde debe viajar la endoprótesis, se encuentra en la luz verdadera (b) y además, que la luz verdadera se expande a lo largo de varios segmentos segmentos de la aorta, luego de colocada la endoprótesis que ocluye el orificio de entrada de la disección (c-d).
CBCT intraoperatoria
Una angiografía final a veces puede tener dificultades para detectar estenosis en las extremidades ilíacas de una endoprótesis, o la acomodación de un stent dentro de la arteria renal, en el caso de endoprótesis ramificadas. Para detectar defectos es necesario realizar múltiples proyecciones. La CBCT es la misma tomografía que se realiza para calibrar la fusión, pero se realiza al finalizar la cirugía. Sin contraste, con muy baja dosis de radiación, se utiliza especialmente para detectar desacoples entre stents o con la inyección de contraste para la detección de endoleaks o la incorrecta alineación del stent con la arteria en la cual se encuentra colocado. La detección intraoperatoria de estas complicaciones logra evitar reintervenciones. 14 Del mismo modo, la CBCT y su uso conjunto con la fusión pueden facilitar la embolización exitosa en endoleaks tipo II con circulación compleja. 15
CONCLUSIÓN
Disponemos hoy de varias soluciones avanzadas en términos de imágenes para ayudar a tratar los aneurismas aórticos complejos. Basándonos en nuestra experiencia, con el uso rutinario de estas aplicaciones en una sala híbrida, recomendamos adoptar este tipo de tecnologías con un claro beneficio clínico para el paciente.
Por otro lado, los moldes personalizados 3D nos brindan una información rápida y precisa, necesaria para fabricar endoprótesis customizadas, sin la necesidad de realizar mediciones manuales, sobre la base de un injerto endovascular estándar. Esta técnica tiene la potencialidad de hacer que la reparación endovascular del aneurisma de aorta esté disponible para más pacientes con anatomía desafiante.















