Introducción
El lupus eritematoso sistémico (LES) es una enfermedad autoinmune y sistémica que involucra diferentes órganos durante su evolución. Aproximadamente el 80% de los pacientes presenta alteraciones hematológicas al momento del diagnóstico y hasta el 70% las desarrolla durante el seguimiento1,2. Las anomalías en el recuento de glóbulos blancos (GB) son parte de los criterios clasificatorios del American College of Rheumatology (ACR) y del Systemic Lupus International Collaborating Clinics (SLICC), y también son consideradas como una manifestación importante cuando se evalúa la actividad de la enfermedad3-5.
Entre las alteraciones hematológicas, la linfopenia y la leucopenia son los hallazgos más frecuentes.
La relación entre leucopenia, linfopenia y neutropenia, y la presencia de infecciones en pacientes con LES, no está bien definida. Tampoco lo está la asociación entre las alteraciones del recuento de GB y la positividad de autoanticuerpos.
Por otro lado, no está claro si presentar leucopenia o linfopenia persistente o intermitente/ fluctuante tiene un impacto distinto en las manifestaciones clínicas del LES. Solo un estudio previo, que analizó esta asociación, encontró linfopenia persistente en el 41,57% de los pacientes evaluados. La persistencia se definió como tener una alteración en el recuento de GB durante más del 75% del seguimiento. No se hallaron diferencias entre las infecciones en pacientes con leucopenia, neutropenia o linfopenia (persistente y no persistente)6.
El objetivo de nuestro estudio fue analizar el comportamiento de los leucocitos y linfocitos en pacientes con LES (niveles normales y debajo del valor normal, de forma persistente o intermitente) y su relación con las manifestaciones clínicas, autoanticuerpos y riesgo de infección.
Materiales y métodos
Estudio de cohorte retrospectivo. Se incluyeron pacientes consecutivos que cumplían los criterios de clasificación para LES ACR 19973, mayores de 18 años de edad, atendidos en nuestro Centro. Los pacientes debían tener más de tres visitas de seguimiento.
Se registraron los recuentos de GB, linfocitos y neutrófilos desde la primera hasta la última visita de seguimiento.
La leucopenia y linfopenia se definieron como el recuento de leucocitos por debajo de 4000 células/mm3 y el recuento de linfocitos por debajo de 1500 células/mm33, respectivamente. En primer lugar, se agruparon los pacientes según si manifestaran leucopenia o linfopenia en cualquier momento de la evolución. Luego, se los agrupó en tres categorías: recuentos normales de leucocitos o linfocitos, pacientes con leucopenia y linfopenia persistente cuando se encontraron anormalidades en más del 50% de las determinaciones, y leucopenia y linfopenia intermitente cuando se detectaron en el 50% o menos de las determinaciones. Se definió el punto de corte de 50% de forma arbitraria porque interpretamos que los pacientes que tenían más de la mitad de los recuentos alterados estaban la mayoría del tiempo con leucopenia y/o linfopenia y por ello consideramos que presentaban la alteración de manera persistente.
Se recolectaron datos demográficos, incluyendo edad y sexo. Las manifestaciones clínicas de la enfermedad se consideraron según lo definido por los criterios de clasificación ACR 1997. Se tuvieron en cuenta las manifestaciones clínicas de forma acumulada desde el diagnóstico hasta la última visita registrada en la historia clínica. Las manifestaciones clínicas acumuladas, la mortalidad, la presencia de infecciones y los valores de autoanticuerpos se recolectaron de las historias clínicas y del sistema de laboratorio. También se registraron los fármacos recibidos durante el seguimiento: glucocorticoides, hidroxicloroquina, inmunosupresores (azatioprina, metotrexato, ciclofosfamida, micofenolato mofetilo -MMF-) y fármacos biológicos.
El daño se midió por damage index (SDI) del Systemic Lupus International Collaborating Clínics (SLICC-SDI) en la primera visita y al final del seguimiento7. En primera instancia, se comparó la asociación entre las variables clínicas, los anticuerpos y los fármacos acumulados entre los grupos que presentaban recuentos de GB normales y leucopenia en cualquier momento de la evolución, y entre los grupos que tenían linfocitos normales y linfopenia en cualquier momento de la evolución.
En segundo lugar, se compararon las asociaciones entre las variables mencionadas anteriormente y los pacientes con recuentos de leucocitos normales, leucopenia persistente e intermitente, y entre los pacientes con linfocitos normales y linfopenia persistente e intermitente.
Análisis estadístico
Las variables se expresaron como mediana y rango intercuartílico (RIC) o media y desvío estándar (DE) según su distribución.
La asociación entre las variables clínicas, los anticuerpos y los fármacos acumulados y la aparición de leucopenia y linfopenia (en cualquier momento de la evolución), y leucopenia y linfopenia persistente e intermitente se examinó mediante análisis univariado. Se evaluaron variables categóricas y continuas mediante el test de chi2 y el test de Student respectivamente. Los test de Mann-Whitney y Fisher se usaron cuando fuera pertinente. Se aplicaron modelos multivariados de regresión logística para identificar factores independientes asociados con las variables dependientes (leucopenia y linfopenia en cualquier momento de la evolución, y leucopenia o linfopenia persistente e intermitente). Todas las variables independientes asociadas con un valor de p<0,10 en el análisis univariado se incluyeron en los modelos de regresión. El análisis estadístico se realizó con el programa Stata 14.0 MP, StataCorp, Texas, EE.UU.
Resultados
En el análisis se incluyeron 89 pacientes. La mayoría (87,6%) de sexo femenino, con una mediana de edad al momento del diagnóstico de 27,5 años (RIC 21-37). La duración de la enfermedad fue de una mediana de 10 años (RIC 5-22) y la mediana de seguimiento de 3,6 años (RIC 1.6-5).
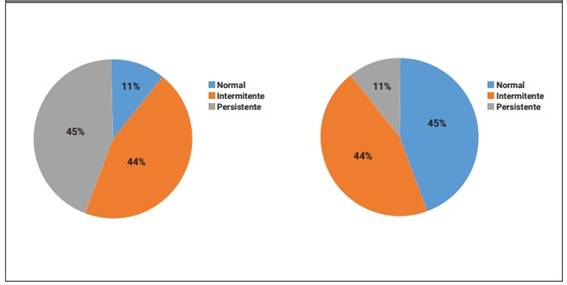
La prevalencia acumulada de linfopenia fue del 89% y la de leucopenia del 55%. Solo el 9% de los pacientes presentó neutropenia durante el seguimiento. Los datos se clasificaron en categorías: recuento de leucocitos normales, leucopenia intermitente o persistente y linfopenia (Gráfico 1).
En la Tabla 1 se muestran las manifestaciones clínicas, los autoanticuerpos y los fármacos acumulados en pacientes con leucopenia en cualquier momento de la evolución, en comparación con aquellos con recuentos normales de GB. El rash discoide fue la única característica clínica asociada a la leucopenia (20,4 vs. 5,1; p=0,059). Diecinueve (48,7%) pacientes en el grupo de leucocitos normales recibieron MMF durante el seguimiento vs. 13 pacientes (27,1%) en el grupo de leucopenia (p=0,046). La subdivisión de pacientes con leucopenia en los que presentaron leucopenia intermitente o persistente reveló resultados similares (datos no mostrados).
Tabla 1: Manifestaciones clínicas, anticuerpos y fármacos prescriptos en pacientes con leucopenia en comparación con aquellos con recuentos normales de glóbulos blancos.
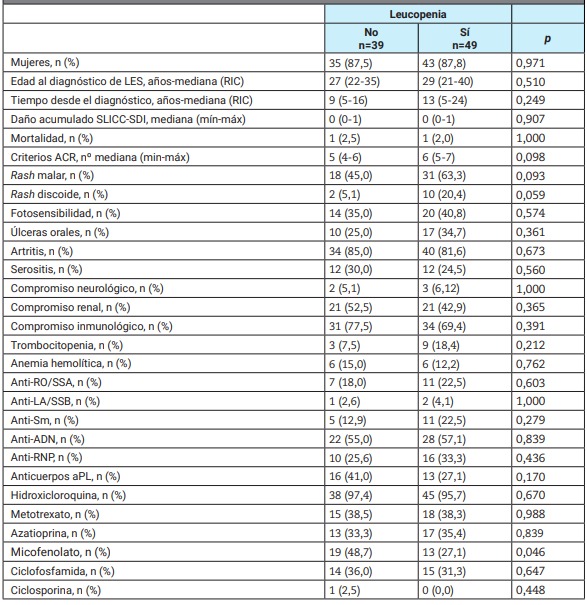
LES: lupus eritematoso sistémico; RIC: rango intercuartílico; SLICC-SDI: Systemic Lupus International Collaborating Clinics damage index; ACR: American College of Rheumatology; anti-RO/SSA: anti-Sjögren’s syndrome related antigen A; anti-LA/SSB: anti-Sjögren’s syndrome related antigen B; anti-Sm: anti-Smith; anti-ADN: anticuerpos ADN; anti-RPN: anti ribonucleoproteína nuclear; aPL: anticuerpos antifosfolipídicos.
Los pacientes con linfopenia en cualquier momento de la evolución mostraron tendencia a tener compromiso neurológico con menor frecuencia que aquellos pacientes con recuentos de linfocitos normales (Tabla 2). Cuando la linfopenia se dividió en persistente e intermitente, los pacientes con compromiso neurológico tenían más probabilidades de presentar un recuento normal de linfocitos que linfopenia intermitente o persistente (22,2% vs. 0% y 7,5%; p=0,027).
Tabla 2: Manifestaciones clínicas, anticuerpos y fármacos prescriptos en pacientes con linfopenia en comparación con aquellos con recuentos normales de glóbulos blancos.
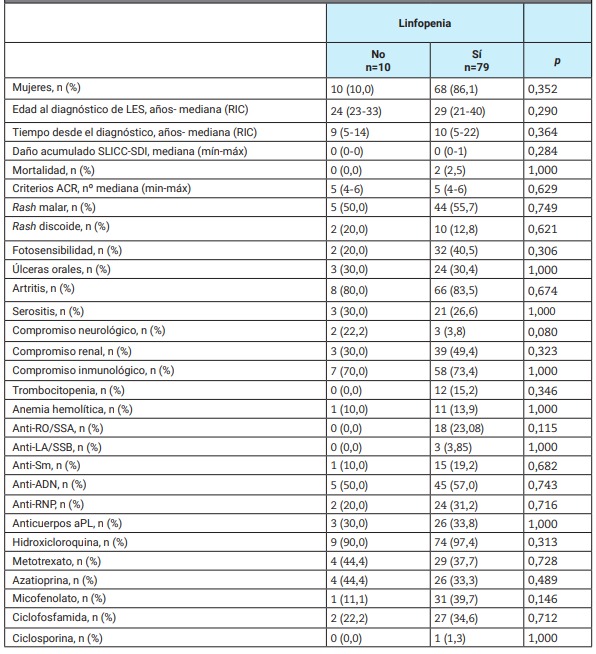
LES: lupus eritematoso sistémico; RIC: rango intercuartílico; SLICC-SDI: Systemic Lupus International Collaborating Clinics damage index; ACR: American College of Rheumatology; anti-RO/SSA: anti-Sjögren’s syndrome related antigen A; anti-LA/SSB: anti-Sjögren’s syndrome related antigen B; anti-Sm: anti-Smith; anti-ADN: anticuerpos ADN; anti-RPN: anti ribonucleoproteína nuclear; aPL: anticuerpos antifosfolipídicos.
Los anticuerpos anti-RNP (anti ribonucleoproteína nuclear) fueron positivos en el 47% de los pacientes en el grupo de linfopenia persistente en comparación con el 15,4% en el grupo linfopenia intermitente, y el 20% en el grupo de recuento de linfocitos normales (p=0,007). No se encontraron diferencias en otras manifestaciones de LES o medicación acumulada (datos no mostrados).
En el análisis multivariado, la leucopenia (en cualquier momento de la evolución) ajustada por la duración de la enfermedad, rash discoide, uso de corticosteroides e inmunosupresores (con excepción de MMF) se asoció negativamente al uso de MMF (OR 0.33; IC 95%: 0,1-0,9; p=0,042). Además, la linfopenia (en cualquier momento de la evolución) ajustada por la presencia de anti-Sm y anti-RNP, el uso de esteroides e inmunosupresores se asoció negativamente a la manifestación de trastornos neurológicos (OR 0.08 IC 95% 0-0,7; p=0,02).
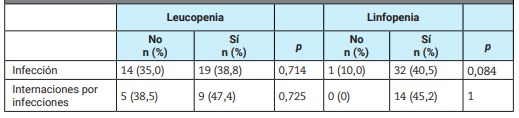
La Tabla 3 detalla la frecuencia de infecciones e internaciones por infecciones en pacientes con linfopenia, leucopenia (en cualquier momento de la evolución) y recuentos de GB normales. Cuantitativamente los pacientes con linfopenia presentaron más infecciones que los pacientes con recuentos de linfocitos normales (40% vs. 10%, respectivamente; p=0,084), pero este hallazgo no fue estadísticamente significativo. No se encontraron diferencias en la prevalencia de infecciones entre las otras categorías.
Discusión
Las anomalías hematológicas son comunes en los pacientes con LES; se encuentran en hasta un 82,7% al momento del diagnóstico2.
En nuestro estudio la alteración encontrada con mayor frecuencia fue la linfopenia (89%), seguida de leucopenia (55%). Solo el 9% de los pacientes incluidos tuvo neutropenia.
El uso de MMF se asoció negativamente a la presencia de leucopenia. En cuanto a la relación con las manifestaciones clínicas, la leucopenia mostró una tendencia a relacionarse con el rash discoide, mientras que los pacientes con linfopenia tenían menos probabilidades de tener compromiso neurológico. En cuanto a la linfopenia, solo se encontró asociación con la presencia de anticuerpos anti-RNP en el grupo de pacientes con linfopenia persistente en el análisis univariado.
No hallamos relación entre las infecciones y la leucopenia o linfopenia. Sin embargo, los sujetos que alguna vez manifestaron linfopenia presentaron más infecciones que los que siempre tuvieron recuentos linfocitarios normales, aunque este hallazgo no fue estadísticamente significativo (p=0,084).
La prevalencia de leucopenia puede variar de 12,9% a 41,8%, según lo reportado por Carli et al. en una revisión sistemática de la literatura8.
Como las anomalías hematológicas son diferentes entre los distintos grupos étnicos, su incidencia varía según las poblaciones estudiadas. Las cohortes del Grupo Latino Americano de Estudio de Lupus (GLADEL) y del LUpus in MInorities: NAture versus nurture (LUMINA), que incluyen pacientes de América Latina, reportaron una incidencia de linfopenia de hasta el 81,9% en LUMINA y del 56,4% en GLADEL. En la cohorte de GLADEL se encontró leucopenia en el 42,2% de los pacientes. Estos datos son similares a los hallados en nuestro estudio2,9.
Respecto del efecto protector del MMF, un estudio previo de Subedi et al. mostró que los pacientes con LES con leucopenia basal (GB <3000 células/mm3) tenían un aumento estadísticamente significativo en el recuento de leucocitos cuando recibían MMF (de 2,55 a 4,38 x 1000 células/mm3; <0,0001). Los pacientes sin leucopenia tuvieron un aumento leve pero no estadísticamente significativo en los recuentos de GB después del tratamiento con MMF10.
Un estudio observacional que evaluó el uso de MMF en manifestaciones no renales de LES reveló una mejoría significativa en los parámetros hematológicos en 8 de 13 pacientes (61,5%) luego de 12 meses de tratamiento. Los GB aumentaron de 2533±572 células/μl en la visita de base a 4167±1063 células/μl después de 6 meses de tratamiento, y hasta 4650±1412 células/μl después 12 meses11.
Este efecto del MMF sobre los GB es importante en la práctica clínica porque varias veces los pacientes necesitan drogas inmunosupresoras para controlar la actividad de la enfermedad y en este escenario a menudo presentan leucopenia.
En la literatura se reportó una prevalencia de linfopenia entre el 15 y 82% de los casos8,12,13. Dias et al. detectaron linfopenia persistente en el 41% de los pacientes14. Estos datos son similares a nuestros resultados.
Varios trabajos de investigación buscaron asociaciones entre linfopenia y las manifestaciones del LES2,9,12. En nuestro trabajo encontramos que el compromiso neurológico se asoció negativamente con linfopenia, hallazgo que no se describió previamente. Al contrario, otros estudios encontraron una asociación positiva entre la linfopenia y el compromiso neurológico como, por ejemplo, con el síndrome de encefalopatía reversible posterior y la meningitis15,16.
En la cohorte LUMINA se informó una asociación entre linfopenia y afectación renal, y una asociación negativa entre linfopenia y fotosensibilidad. Durante el período de seguimiento, se detectó una asociación positiva con serositis y uso de MMF, y asociación negativa con rash malar9.
Una publicación reciente de la cohorte GLADEL no encontró ninguna manifestación particular del LES asociada a linfopenia, pero hallaron que la hidroxicloroquina y la azatioprina serían factores protectores para su desarrollo2. Otros autores descubrieron una relación entre los recuentos de linfocitos y la actividad de la enfermedad13 con el desarrollo de manifestaciones sistémicas en pacientes con lupus cutáneo17.
La asociación de linfopenia con autoanticuerpos se reportó previamente. Wenzel et al. encontraron asociación a anti-Ro/SSA, anti-La/SSB y anti-RNP18. En nuestro caso, hallamos una asociación entre la presencia de anti-RNP en pacientes con linfopenia persistente en comparación con aquellos con linfopenia intermitente y linfocitos normales. Esta asociación no persistió cuando la linfopenia fue dicotomizada. Un estudio anterior detectó asociación entre el anti-RNP y leucopenia, sin embargo no encontró esta asociación con linfopenia19. En la cohorte de LUMINA, la linfopenia se asoció con anti-Ro/SSA y anti-dsDNA9.
En cuanto a las infecciones, la evidencia es controvertida. Un estudio prospectivo en 89 pacientes con LES no encontró diferencia entre la tasa de sobrevida libre de infección grave y la presencia de leucopenia6. Ruiz Irastorza et al. encontraron que la leucopenia, en el momento de la infección, era más frecuente solo en el análisis univariado20. Esta asociación no se mantuvo cuando se ajustó por otras variables.
Merayo-Chalico et al. describieron que la linfopenia aumentó el riesgo de infecciones graves cinco veces21. En nuestro estudio solo se encontró una tendencia a mayor presencia de infecciones en los pacientes con linfopenia.
Este trabajo tiene varias limitaciones. En primer lugar, el estudio es retrospectivo y no todos los pacientes tuvieron el mismo número de determinaciones de leucocitos durante el seguimiento. Es posible que aquellos con enfermedad más grave hayan tenido más determinaciones de leucocitos durante el seguimiento que quienes tuvieron manifestaciones más leves de la enfermedad. Por otra parte, nuestra muestra pudo no ser lo suficientemente grande como para demostrar la diferencia entre grupos, sobre todo cuando se los dividió en normal, persistente e intermitente. Por último, en el contexto de las limitaciones de la revisión retrospectiva de historias clínicas, no fue posible asociar temporalmente las manifestaciones clínicas con las mediciones de GB.
Conclusiones
En nuestra población el uso de MMF se asoció con un recuento de leucocitos normal, y el compromiso neurológico se relacionó con un recuento de linfocitos normal cuando se ajustó con otras variables significativas.
También detectamos que la presencia de rash discoide se asoció a leucopenia (en cualquier momento de la evolución), y que el anti-RNP se asoció a linfopenia persistente, pero solo en el análisis univariado. Las infecciones no se relacionaron de manera significativa con ninguna de las categorías estudiadas.