Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680versión On-line ISSN 1669-9106
Medicina (B. Aires) v.69 n.6 Ciudad Autónoma de Buenos Aires nov./dic. 2009
ARTÍCULO ORIGINAL
Angioedema hereditario. Historia familiar y manifestaciones clínicas en 58 pacientes
Diego S. Fernández Romero, Pamela Di Marco, Alejandro Malbrán
Servicio de Alergia e Inmunología Clínica, Hospital Británico de Buenos Aires
Dirección Postal: Dr. Diego S. Fernández Romero, Peña 2562, 1425 Buenos Aires, Argentina Fax: (54 -11) 4382-8302 e-mail: dfromero@live.com.ar
Resumen
El angioedema hereditario (AEH) es una enfermedad rara, autosómica dominante, caracterizada por episodios de angioedema que comprometen la piel, el tracto gastrointestinal y la laringe. Analizamos las características epidemiológicas y clínicas en una serie de 58 pacientes, 53 (91%) con diagnóstico de AEH tipo I y 5 (9%) con tipo II. La edad media al inicio fue de 10.8 ± 9.5 años (0.1 a 59) y de 25.8 ± 16.2 años (2 a 77) en el momento del diagnóstico, con un retraso diagnóstico de 15.3 ± 14.3 años. El promedio de ataques en los 6 meses previos a la consulta fue de 7.4 ± 7.6 (0 a 40). Cincuenta y cuatro (93%) presentaron ataques cutáneos, 50 (86%) abdominales, 24 (41%) laríngeos y 24 (41%) cutáneos y abdominales combinados. Veintisiete (46.5%) nunca utilizaron medicación preventiva para la enfermedad y 17 (29%) recibieron danazol en diferentes dosis por diferentes periodos de tiempo. Durante los ataques, 15 (26%) pacientes recibieron C1 inhibidor endovenoso alguna vez, 7 (12%) recibieron plasma fresco y 40 (69%) tratamiento sintomático. Ansiedad o situaciones de estrés y traumatismos fueron los desencadenantes más frecuentes. Identificamos a 6 (10%) pacientes como primera mutación y a 52 (90%) con historia familiar previa. Analizamos 20 troncos familiares identificando 205 individuos en riesgo de heredar la enfermedad, 109 (53%) de ellos con síntomas o diagnóstico AEH. El total de individuos con síntomas de AEH fue de 145, de los cuales 19 (13%) murieron por asfixia. Disminuir el retraso diagnóstico y ofrecer una terapéutica adecuada son desafíos a afrontar en el AEH.
Palabras clave: Angioedema hereditario; C1 inhibidor; Ataques de angioedema
Abstract
Hereditary angioedema. Family history and clinical manifestations in 58 patients. Hereditary angioedema (HAE) is a rare autosomal dominant disease, characterized by episodes of edema typically involving the skin, gastrointestinal tract and larynx. We here describe the epidemiologic and clinical characteristic of a series of 58 patients with diagnosis of HAE, 53 (91%) type I and 5 (9%) type II. The mean age at first symptom was 10.8 ± 9.5 years and the mean age at diagnosis was 25.8 ± 16.2 years old, with a diagnosis delay of 15.3 ± 14.3 years. The mean number of attacks in the previous 6 months was 7.4 ± 7.6 range 0 to 40. Fifty four (93%) had cutaneous attacks, 50 (86%) abdominal attacks, 24 (41%) laryngeal attacks and 24 (41%) combined cutaneous and abdominal attacks. Twenty seven (46.5%) patients never received preventive treatments and 17 (29%) received danazol in different doses for different periods of time. During the attacks, 15 (26%) patients were treated with C1 inhibitor at least once, 7 (12%) with fresh frozen plasma and 40 (69%) received only supportive treatment. Stress and trauma were identified as attacks triggers. Six (10%) patients were first mutation and 52 (90%) had HAE ancestors. We reconstructed 20 kindred, identifying 205 individuals at risk of inheriting the disease, 109 (53 %) of them had signs or laboratory diagnosis of HAE. The total number of identified HAE individuals was 145, 19 (13%) died with asphyxia. So, shortening of diagnosis delay and appropriate treatment of HAE are a challenge to be fulfilled.
Key words: Hereditary angioedema; C1 inhibitor; Angioedema attacks
El angioedema hereditario (AEH) es una enfermedad rara, de transmisión autosómica dominante, caracterizada por episodios recurrentes y autolimitados de angioedema que comprometen principalmente la piel, el tracto gastrointestinal y la laringe. Se estima una incidencia de 1:10 000 a 1:50 000 habitantes y ha sido descripta en todas las etnias afectando a ambos sexos por igual1-4. El AEH es causado por la deficiencia funcional de la proteína plasmática C1 inhibidor (C1-INH)5 y clásicamente se han descripto dos variantes con manifestaciones clínicas idénticas. La variante tipo I con niveles antigénicos y funcionales bajos de C1-INH plasmático en el 85% de los casos y la tipo II con nivel antigénico normal o alto de C1-INH pero funcionalmente deficiente en el 15% restante4, 6. Se han notificado más de 150 mutaciones en el gen del C1-INH responsables de estas alteraciones7, 8. El C1-INH es un inhibidor de esterasas serínicas que inactiva a diferentes proteasas del sistema complemento, a la kalicreína del sistema de contacto, a la plasmina del sistema fibrinolítico, al factor Hageman y sus fragmentos y al factor IX de la coagulación. Datos recientes sugieren que la bradiquinina, producida como consecuencia de la acción descontrolada de la kalicreína, vía su interacción con el receptor de bradiquinina tipo 2 (BR-2) es el mediador químico más importante en los ataques de angioedema8-12.
El compromiso cutáneo produce un edema circunscrito y deformante, no pruriginoso, que compromete con mayor frecuencia extremidades, cara y genitales (Fig. 1). Las zonas afectadas están habitualmente doloridas y tensas con afectación considerable del movimiento1-3. El compromiso de la mucosa gastrointestinal produce un abdomen agudo médico con dolor intenso, nauseas, vómitos, diarrea, peritonismo y síntomas de hipovolemia1-3, 13. Finalmente, el compromiso faríngeo y/o laríngeo causa disfonía, alteraciones en la deglución, y obstrucción de la vía aérea superior (Fig. 2) que puede poner en peligro la vida causando la muerte por asfixia1-3, 14, 15. El tratamiento preventivo de los ataques de AEH se realiza con andrógenos como el danazol y el estanozolol y con agentes anti-fibrinolíticos como el ácido épsilon aminocaproico (EACA) y el ácido tranexámico; ambos tipos de fármacos disminuyen el número y la gravedad de los ataques4, 8, 16, 17. Los ataques pueden ser tratados con concentrado de C1 inhibidor humano o plasma fresco como fuente de C1 INH4, 8, 16, 17. Existen nuevos agentes que se encuentran en investigación clínica, como el C1 inhibidor recombinante, el inhibidor de la kalicreína DX-88 y un antagonista de la bradiquinina en su unión con el receptor tipo 2 (BR-2) icatibant, que pueden ofrecer mayor seguridad y más fácil administración para el control de los ataques4, 8, 16-18.
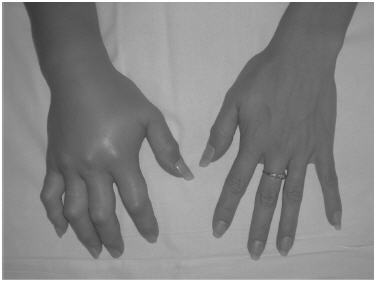
Fig. 1.- Angioedema de mano derecha en un ataque cutáneo de AEH. El AEH suele afectar extremidades a diferencia de otros tipos de angioedema que comprometen fundamentalmente la cara.
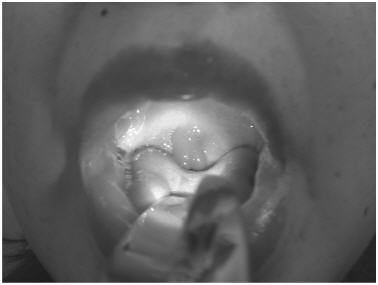
Fig. 2.- Angioedema faríngeo en un ataque de AEH. Se observa edema masivo de ambos pilares faríngeos y úvula, esta última desplazada anteriormente. El paciente se presentó con grave disfagia y dificultad respiratoria moderada.
El objetivo de este estudio fue describir las características clínicas y epidemiológicas de nuestra población de pacientes con diagnóstico de AEH, en tiempos en que la fisiopatología de la enfermedad parece dilucidarse y nuevos tratamientos prometen un mejor pronóstico19.
Materiales y métodos
El estudio incluyó a todos los pacientes con diagnóstico de AEH que fueron asistidos en nuestros centros desde junio del 2005 hasta octubre del 2008. El diagnóstico se realizó en base a la historia personal y familiar de angioedema recurrente y a la determinación de la deficiencia cuantitativa o funcional de C1-INH en plasma. A todos los pacientes se les determinó la concentración plasmática del componente C4 del sistema complemento y en todos los pacientes se descartaron otras causas de angioedema crónico8, haciendo especial hincapié en el diagnóstico diferencial con angioedema alérgico, crónico idiopático, relacionado con la ingesta de anti-inflamatorios no esteroideos y con la ingesta de inhibidores de la enzima convertidota de angiotensina. Los pacientes con niveles disminuidos de C1-INH plasmático se clasificaron como tipo I y aquellos con niveles normales o aumentados pero con función disminuida se clasificaron como tipo II.
Los niveles antigénicos plasmáticos de C1-INH y de C4 fueron determinados por inmunodifusión radial, y la actividad funcional de C1-INH se determinó por fotocolorimetría usando el substrato cromogénico C2H5CO-Lys (e-Cbo)-Gly-Arg-pNA (Immunochrom C1-INH; Technoclone, Viena, Austria). Ambas técnicas se realizaron en laboratorios comerciales de referencia.
Cada paciente fue tomado como un caso índice, y a partir de cada uno de ellos se reconstruyeron las familias y sus respectivos troncos familiares. Tratándose de una enfermedad de transmisión dominante, varios miembros de cada tronco consultaron en nuestros centros y la reconstrucción de la historia familiar se facilitó por el interrogatorio de varios miembros de cada tronco, ocasionalmente de varias generaciones.
A cada caso índice se le documentó la edad de inicio de los síntomas, la edad en el momento del diagnóstico, el número de ataques en los últimos 6 meses, sus características clínicas, los posibles factores desencadenantes, la historia de compromiso laríngeo, la medicación preventiva utilizada y el tratamiento durante los ataques. Como características clínicas de los ataques clasificamos su localización en cutáneos, abdominales, laríngeos, o combinados; y su duración desde el inicio hasta el comienzo de la mejoría clínica y hasta la desaparición de los síntomas. Los ataques laríngeos combinados con angioedema facial, oral o faríngeo se consideraron sólo como laríngeos por su mayor gravedad.
Para analizar la forma de transmisión genética, construimos los árboles genealógicos de los pacientes y determinamos la población en riesgo de heredar la enfermedad, incluyendo sólo aquellas familias con datos completos de todos los descendientes. Definimos como personas en riesgo a todos aquellas cuya madre o padre presentaban síntomas de la enfermedad.
Para documentar la mortalidad por AEH, registramos todos los casos de angioedema reconocidos y a todos aquellos familiares con síntomas de angioedema, y documentamos los casos de muerte por asfixia en esta población de acuerdo al relato de los pacientes.
Los pacientes sin historia familiar positiva pero con síntomas típicos de angioedema y con deficiencia cuantitativa o funcional de C1-INH se consideraron primera mutación del gen de C1-INH.
Resultados
El estudio incluyó a 58 pacientes con diagnóstico de AEH, 53 (91%) de tipo I y 5 (9%) tipo II; 42 eran mujeres (72%) y 16 varones (28%). La edad promedio en el momento de la primera consulta fue de 35 ± 15 años, rango 10 a 79.
Todos los pacientes presentaron niveles plasmáticos bajos del componente C4 del complemento en el momento del diagnóstico.
La edad media de comienzo de los síntomas fue de 10.8 ± 9.5 años, rango 0.1 a 59. Un paciente presentó el primer ataque en su segundo día de vida. La edad promedio en el momento del diagnóstico fue de 25.8 ± 16.2 años, rango 2 a 77. El retraso al diagnóstico de la totalidad de los pacientes fue de 15.3 ± 14.3 años. Sin embargo, tomando en consideración que de los 58 pacientes, a 3 (5%) se les realizó el diagnóstico antes del comienzo de los síntomas y a otros 4 (7%), luego de realizarles el diagnóstico a un familiar y después del primer episodio, el retraso diagnóstico en los 51(88%) pacientes restantes fue de 17.7 ± 14 años, rango 1 a 70 años.
El promedio de ataques de los 58 pacientes en los 6 meses previos a la consulta fue de 7.4 ± 7.6, rango 0 a 40; sólo 4 (7%) pacientes no presentaron ataques. Cincuenta y cuatro (93%) presentaron ataques cutáneos, 50 (86%) abdominales, 24 (41%) laríngeos y 24 (41%) cutáneos y abdominales combinados. Observamos que algunos pacientes presentaron un único tipo de ataque desde el inicio de los síntomas de su enfermedad, mientras que otros presentaron diferentes combinaciones, a pesar de pertenecer al mismo tronco familiar y por ende tener la misma mutación del gen. El tiempo desde el comienzo de los síntomas hasta el inicio de la mejoría y hasta la resolución completa del ataque según las diferentes localizaciones se muestra en la Tabla 1.
TABLA 1.- Tiempos de mejoría y resolución en horas promedio de los distintos tipos de ataques de AEH

DS: Desvío estándar
De los 58 pacientes, 27 (46.5%) nunca habían recibido medicación preventiva para la enfermedad, 17 (29%) recibieron danazol en diferentes dosis por diferentes períodos de tiempo, 2 (3%) EACA, 9 (16%) danazol y EACA en distintos momentos, 1 paciente recibió ácido tranexámico y otro EACA y ácido tranexámico en distintos momentos. En el momento de la primera consulta 36 (62%) pacientes no recibían medicación profiláctica, 18 (31%) estaban tratados con danazol, 2 (3%) con EACA y 2 (3%) con ácido tranexámico. Los efectos adversos más frecuentes referidos para justificar la suspensión de los andrógenos o su uso en forma irregular fueron la masculinización en mujeres, cefalea e intolerancia digestiva. En la Tabla 2 se relaciona el tratamiento de los pacientes en el momento de la consulta con la frecuencia de ataques en los 6 meses previos.
TABLA 2. - Promedio de ataques de AEH en pacientes sin tratamiento y con tratamiento en los 6 meses previos a la consulta

* p<0.02 comparado con pacientes sin tratamiento o tratados con agentes anti-fibrinolíticos. **Acido tranexámico.
Durante los episodios agudos, 15 (26%) pacientes recibieron C1 inhibidor endovenoso alguna vez, 7 (12%) recibieron plasma fresco y 40 (69%) ninguno de los dos y fueron tratados sintomáticamente con anti-inflamatorios no esteroideos, anti-histamínicos, corticoides, anti-espasmódicos y/o morfina. De los 15 pacientes que recibieron C1 inhibidor endovenoso, 5 lo recibieron en sólo un ataque, 8 ocasionalmente y sólo 2 lo usan regularmente.
A 50 pacientes se les preguntó sobre las causas que desencadenaban sus ataques, 9 (18%) no los pudieron relacionan claramente con ningún desencadenante, 34 (68%) identificaron como desencadenantes ansiedad o situaciones de stress y 22 (44%) traumatismos. De las 31 mujeres a las que se les preguntó sobre desencadenantes de sus ataques, 7 (22.5%) reconocieron el período menstrual como desencadenante. Dos pacientes identificaron como desencadenantes de angioedema facial o laríngeo a cuadros infecciosos de vías superiores.
Identificamos a 6 (10%) pacientes como primera mutación y a 52 (90%) con historia familiar previa. De los pacientes que son primera mutación, uno tiene descendencia y constituye el inicio de un nuevo tronco familiar y 5 no tienen descendencia y, por lo tanto, no se consideran aún como troncos familiares. De los 58 pacientes reconstruimos 20 troncos familiares que incluyen a 205 individuos en riesgo de heredar la enfermedad, 109 (53%) de ellos con síntomas o diagnóstico de AEH.
El número total de personas con síntomas de AEH identificado fue de 145 incluyendo los 109 en los troncos familiares y 36 con síntomas de HAE pero sin datos acerca de la enfermedad en los padres, por lo que no cumplen la definición de sujeto en riesgo. Del total de 145 pacientes, 19 (13%) murieron por asfixia, de acuerdo al relato de familiares. En muchos casos la muerte de un familiar por asfixia llevó al diagnóstico en el resto de los miembros de esa familia, no habiendo ningún caso de muerte post-diagnóstico.
Discusión
Describimos las características de un grupo de 58 pacientes con AEH, y de 20 troncos familiares. El 91% de los pacientes fue diagnosticado como HAE de tipo I y el 9% como tipo II. En otras series, la incidencia de angioedema tipo II es un poco mayor, de alrededor del 15%1-3; esta diferencia probablemente se deba a que la detección de un C1 INH antigénico normal o alto induzca a descartar erróneamente el diagnóstico de AEH en algunos pacientes. Nuestra población de pacientes incluye pocos casos de primeras mutaciones, sólo el 10%, comparado con otras series donde aproximadamente un 25% de los casos son por nuevas mutaciones3, 20; aquí la falsa creencia de que una historia familiar es imprescindible para el diagnóstico puede contribuir a la no detección de nuevos casos.
Los ataques pueden comenzar en cualquier momento de la vida, aunque la edad media de comienzo de los síntomas es de 10.8 años. En promedio, los pacientes tienen 14.8 ataques por año que varían en frecuencia, duración y gravedad. La frecuencia y gravedad de los ataques producen un gran impacto en la calidad de vida de los pacientes, que ven afectados por la enfermedad su vida de relación, sus estudios y su trabajo. La edad de inicio, la frecuencia y el amplio rango de la edad de comienzo de los síntomas, son similares a los descriptos por otros autores1-3, y obliga a considerar este diagnóstico en cualquier momento de la vida. Un paciente de nuestro grupo presentó su primer ataque a los 2 días de vida y otro a los 59 años.
El retraso diagnóstico de 15.3 años en nuestra serie es llamativamente prolongado y significativamente mayor que el de 8 años descriptos por otros autores21. Este retraso cobra especial relevancia porque en la actualidad la morbilidad y la mortalidad por la enfermedad disminuyen dramáticamente una vez realizado el diagnóstico8. Durante los ataques, los enfermos suelen buscar asistencia en guardias donde generalmente el compromiso cutáneo y laríngeo suele interpretarse como de origen "alérgico" y el compromiso abdominal como un posible abdomen agudo quirúrgico.
Durante los ataques los síntomas suelen comenzar en forma gradual, progresando durante las primeras 24 horas, para luego comenzar a disminuir lentamente hasta desaparecer por completo en 48 a 168 horas1-3, 8, 22. Los desencadenantes más frecuentemente referidos por nuestros pacientes fueron la ansiedad y las situaciones de stress, los traumatismos y el período menstrual, al igual que en otras series1-3, 8, 22.
Llamativamente casi la mitad de nuestros pacientes, con indicación de tratamiento preventivo por la frecuencia y gravedad de sus ataques nunca lo recibieron. En el momento de la primera consulta, el 62% de los pacientes no utilizaban medicación preventiva, presentando en promedio un número significativamente mayor de ataques que los pacientes tratados con danazol (Tabla 2). La inaccesibilidad a la medicación profiláctica debido a su alto costo y a la falta de cobertura médica adecuada es un problema recurrente en estos pacientes y creemos que explica en parte el bajo uso de medicación preventiva. Los efectos adversos de los andrógenos como la cefalea, la intolerancia digestiva y la masculinización en mujeres son otra causa de abandono del tratamiento o de la utilización de dosis insuficientes. Los pacientes tratados con EACA y con ácido tranexámico sufrieron igual cantidad de ataques que los que no se encontraban en tratamiento preventivo, probablemente porque la dosis era insuficiente (Tabla 2).
El hecho de que la medicación preventiva no es totalmente efectiva y ocasionalmente produce eventos adversos intolerables, hace que sea necesario contar con un tratamiento eficaz para los ataques moderados a severos4, 8, 16. La mayoría de los pacientes reciben tratamiento sintomático con anti-inflamatorios no esteroideos, anti-histamínicos, corticoides, anti-espasmódicos y/o morfina pero ninguno de estos agentes constituye un tratamiento adecuado4. A pesar de existir en el mercado argentino el concentrado de C1-INH y de haberse sugerido su efectividad en varios estudios24-27, no fue utilizado por la mayoría de los pacientes. Es probable que su alto costo y la forma de administración endovenosa sean barreras de acceso al uso generalizado de esta medicación. También constituye una logística difícil de lograr que el medicamento sea administrado en las salas de emergencia, cuyos médicos generalmente presumen que el paciente tiene alergia y se limitan frente a un producto y una enfermedad que no conocen. La utilización del plasma fresco es controvertida porque puede empeorar los síntomas mediante el aporte del precursor de la bradiquinina, el kininógeno de alto peso molecular4. Además, por ser productos humanos, pueden transmitir enfermedades infecciosas8.
La mortalidad histórica por asfixia atribuible a edema laríngeo fue de 13% y todos los casos de muerte fueron antes del diagnóstico de la enfermedad en la familia. Otras series describen un 30 a 50% de mortalidad histórica.1-3, 14, 15, 28, porcentajes que disminuyen significativamente en pacientes con diagnóstico y disponibilidad a los tratamientos preventivos y a las drogas adecuadas durante los ataques24.
Nuestros resultados sugieren una dificultad en la identificación de pacientes con primeras mutaciones y con AEH tipo II, un gran retraso al diagnóstico, tratamiento preventivo insuficiente e inaccesibilidad al tratamiento de los ataques. Estos problemas en su conjunto disminuyen considerablemente la calidad de vida de los pacientes por la frecuencia y morbilidad de los ataques y hacen que el riesgo de mortalidad por edema laríngeo continúe siendo una amenaza. Creemos que difundiendo información sobre la enfermedad a la comunidad médica, a los financiadores del sistema de salud, a los pacientes con AEH y a la población en riesgo de heredar la enfermedad, disminuirá el retraso diagnóstico y el tratamiento será más adecuado, produciendo una consecuente disminución de la morbilidad y mortalidad por la enfermedad.
Conflictos de interés: Los autores declaran no tener conflictos de interés.
1. Frank MM, Gelfand JA, Atkinson JP. Hereditary angioedema: the clinical syndrome and its management. Ann Intern Med 1976; 84: 589-93. [ Links ]
2. Cicardi M, Bergamaschini L, Marasini B, Boccassini G, Tucci A, Agostoni A. Hereditary angioedema: an appraisal of 104 cases. Am J Med Sci 1982; 284: 2-9. [ Links ]
3. Agostoni A, Cicardi M. Hereditary and acquired C-1 inhibitor deficiency: biological and clinical characteristics in 235 patients. Medicine (Baltimore) 1992; 71: 206-15. [ Links ]
4. Bowen T, Cicardi M, Fakas H, et al. Canadian 2003 International Consensus Algorithm for the diagnosis, therapy and management of hereditary angioedema. J Allergy Clin Immunol 2004; 114: 629-37. [ Links ]
5. Donaldson VH, Evans RR. A biochemical abnormality in hereditary angioneurotic edema: absence of serum inhibitor of C'1-esterase. Am J Med 1963; 31: 37-44. [ Links ]
6. Rosen FS, Pensky J, Donaldson V, Charache P. Hereditary angioneurotic edema: two genetic variants. Science 1965; 148: 957-8. [ Links ]
7. Davis AE III. C1 inhibitor and hereditary angioneurotic edema. Annu Rev Immunol 1988; 6: 595-628. [ Links ]
8. Zuraw BL. Hereditary angioedema. N Engl J Med 2008; 359: 1027-36. [ Links ]
9. Nussberger J, Cugno M, Amstutz C, Cicardi M, Pellacani A, Agostoni A. Plasma bradykinin in angioedema. Lancet 1998; 351: 1693-7. [ Links ]
10. Nussberger J, Cugno M, Cicardi M, Agostoni A. Local bradykinin generation in hereditary angioedema. J Allergy Clin Immunol 1999; 104: 1321-2. [ Links ]
11. Nussberger J, Cugno M, Cicardi M. Bradykinin-mediated angioedema. N Engl J Med 2002; 347: 621-2. [ Links ]
12. Han ED, MacFarlane RC, Mulligan AN, Scafidi J, Davis AE III. Increased vascular permeability in C1 inhibitor-deficient mice mediated by the bradykinin type 2 receptor. J Clin Invest 2002; 109: 1057-63. [ Links ]
13. Bork K, Staubach P, Eckardt AJ, Hardt J. Symptoms, course, and complications of abdominal attacks in hereditary angioedema due to C1 inhibitor deficiency. Am J Gastroenterol 2006; 101: 1-9. [ Links ]
14. Bork K, Siedlecki K, Bosch S, Schopf RE, Kreuz W. Asphyxiation by laryngeal edema in patients with hereditary angioedema. Mayo Clin Proc 2000; 75: 349-54. [ Links ]
15. Bork K, Hardt J, Schicketanz K, Ressel N. Clinical studies of sudden upper airway obstruction in patients with hereditary angioedema due to C1 esterase inhibitor deficiency. Arch Intern Med 2003; 163: 1229-35. [ Links ]
16. Frank MM. Hereditary angioedema: the clinical syndrome and its management in the United States. Immunol Allergy Clin North Am 2006; 26: 653-68. [ Links ]
17. Zuraw BL, MD. Novel Therapies for Hereditary Angioedema. Immunol Allergy Clin N Am 2006; 26: 691-708. [ Links ]
18. Bork K, Frank J, Grundt B, Schlattmann P, Nussberger J, Kreuz W. Treatment of acute edema attacks in hereditary angioedema with a bradykinin receptor-2 antagonist (Icatibant) J Allergi Clin Immunol 2007; 119: 1497-503. [ Links ]
19. Frank MM. Hereditary angioedema. Curr opin pediatr 2005; 17: 686-9. [ Links ]
20. Pappalardo E, Cicardi M, Duponchel C, Carugati A Choquet S, Agostoni A, et al. Frequent de novo mutation and exon deletion in the C1 inhibitor gene of patients with angioedema. J Allergy Clin Immunol 2000; 106: 1147-54. [ Links ]
21. Huang SW. Result of an on line survey of patients with hereditary Angiedema. Allergy Asthma Proc 2004; 114: 626-8. [ Links ]
22. Nielsen EW, Gran JT, Straume B, Mellbye OJ, Johansens HT, Mollnes TE. Hereditary angioedema: new clinical observations and autoimmune screening, complement and kallikrein-kinin analyses. J Int Med 1996; 239: 119-30. [ Links ]
23. Kunschak M, Engl W, Maritsch F, et al. A randomized, controlled trial to study the efficacy and safety of C1 inhibitor concentrate in treating hereditary angioedema. Transfusion 1998; 38: 540-9. [ Links ]
24. Bork K, Barnstedt SE. Treatment of 193 episodes of laryngeal edema with C1 inhibitor concentrate in patients with hereditary angioedema. Arch Intern Med 2001; 161: 714-8. [ Links ]
25. Cicardi M, Zingale L. How do we treat patients with hereditary angioedema. Transfus Apher Sci 2003; 29: 221-7. [ Links ]
26. Farkas H, Jakab L, Temesszentandrási G, et al. Hereditary angioedema: a decade of human C1-inhibitor concentrate therapy. J Allergy Clin Immunol 2007; 120: 941-7. [ Links ]
27. Bork K, Meng G, Staubach P, Hardt J. Treatment with C1 inhibitor concentrate in abdominal pain attacks of patients with hereditary angioedema. Transfusion 2005; 45:1774-84. [ Links ]
28. Bork K, Ressel N. Sudden upper airway obstruction in patients with hereditary angioedema. Tranfus Apheresis Sci 2003; 29: 235-8. [ Links ]
Recibido: 29-12-2008
Aceptado: 20-7-2009














