Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Darwiniana, nueva serie
versión impresa ISSN 0011-6793versión On-line ISSN 1850-1699
Darwiniana v.45 n.1 San Isidro ene./jul. 2007
Formación de pelos en el alga agarófita gracilaria chilensis (Gracilariales, Rhodophyta)
Maximiliano D. Garcia1, Alicia B. Miravalles1 & Patricia I. Leonardi1,2
1Laboratorio de Ficología y Micología, Departamento de Biología, Bioquímica y Farmacia, Universidad Nacional del Sur, 8000 Bahía Blanca, Buenos Aires, Argentina; leonardi@uns.edu.ar (autor corresponsal).
2Centro de Recursos Naturales Renovables de la Zona Semiárida, Consejo Nacional de Investigaciones Científicas y Técnicas. Camino La Carrindanga Km 7, 8000 Bahía Blanca, Buenos Aires, Argentina.
Resumen. Garcia, M. D.; A. B. Miravalles & P. I. Leonardi. 2007. Formación de pelos en el alga agarófita Gracilaria chilensis (Gracilariales, Rhodophyta).
Gracilaria chilensis es un alga roja agarófita perteneciente a la clase Florideophyceae. En este estudio se describe la formación de pelos en talos mantenidos en cultivo en agua de mar enriquecida, bajo condiciones controladas de luz y temperatura. La inducción de los pelos fue realizada colocando porciones de talos en un medio de cultivo carente de compuestos nitrogenados. Se emplearon técnicas de microscopía óptica y electrónica de transmisión y barrido. Los pelos se desarrollan a partir de células corticales ovoides grandes. Estas células formadoras de pelos (CFPs) son multinucleadas, poseen pequeños plástidos y una abundante red de retículo endoplasmático de disposición apical. La formación de los pelos comienza con el desarrollo de una protuberancia, inicialmente cubierta por una pared multilaminar, la cual se rompe junto con la pared del talo, con la consecuente elongación de la protuberancia. El pelo queda establecido cuando se produce una citocinesis en la base de la protuberancia, formándose una conexión citoplasmática obliterada o "pit plug" asimétrica entre la base del pelo y la CFP. Los pelos son unicelulares, poseen una vacuola y numerosos núcleos. Tienen un crecimiento activo dejando, al caerse, una cicatriz de forma concéntrica en la pared. Se compara este proceso con el descrito en otras especies de la clase. En medios de cultivo carentes de nitrógeno, el crecimiento del talo de G. chilensis fue menor, aumentando el número de pelos.
Palabras clave. Florideophyceae; Gracilaria; Pelos; Rhodophyta; Ultraestructura.
Abstract. Garcia, M. D.; A. B. Miravalles & P. I. Leonardi. 2007. Hair formation in the agarophyte alga Gracilaria chilensis (Gracilariales, Rhodophyta).
Gracilaria chilensis (Gracilariales) is an agarophyte red alga belonging to class Florideophyceae. The purpose of this study was to describe the hair formation mechanism. Thalli were maintained in culture with enriched seawater under controlled conditions of light and temperature. Hair formation was induced on portions of thalli growing in a nitrogen-free culture medium. Light (bright field) microscopy, transmission and scanning electron microscopy techniques were used. Hairs develop from large ovoid hair-producing cortical cells (HPCs). These cells are multinucleate, contain small plastids, and abundant endoplasmic reticulum apically positioned. Each hair begins as a protuberance initially covered by a multilaminar wall, this is, in turn, ruptured along with the thallus wall as the protuberance elongates. Hairs are formed when cytokinesis occurs at the base of the protuberance. An asymmetric pit plug is formed between the hair's base and the HPC. Hairs are unicellular, with a vacuole and numerous nuclei. They have an active growth, and leave a concentric scar on the wall after detachment. Hair formation mechanism in G. chilensis is also compared with that observed in other species of the same class. In nitrogen-free culture media, the thallus of G. chilensis grows less, but the number of hairs increases.
Keywords. Florideophyceae; Gracilaria; Hair; Rhodophyta; Ultrastructure.
Original recibido el 14 de noviembre de 2006;
aceptado el 17 de abril de 2007
INTRODUCCIÓN
Las primeras observaciones del desarrollo de los pelos unicelulares de las especies de la Clase Florideophyceae fueron realizadas por Rosenvinge (1911). Aunque aproximadamente 4000 especies de esta clase producen pelos (Kraft & Woelkerling, 1990), los estudios de estas células son escasos. Se ha indicado que los pelos de las algas rojas son unicelulares, uninucleados, vacuolados, carecen de plástidos y son de corta vida (Dixon, 1973). Se originan de células formadoras de pelos (CFPs) que, dependiendo de la morfología del talo, pueden ser células apicales de filamentos axiales o células apicales diferenciadas de filamentos corticales (Oates & Cole, 1994). La presencia de pelos en distintas especies del género Gracilaria ha sido indicada en diferentes estudios taxonómicos (Boraso, 1983; Taylor, 1960; Bird et al., 1986; Nelson, 1987). Las observaciones ultraestructurales realizadas en pelos de Florideophyceae incluyen: formación de pelos de corta vida en Nemalion helminthoides (Velley) Batters (Duckett et al., 1974); citología de los pelos de Ceramium rubrum (Hudson) C. Agardh y Audouinella hermannii (Roth) Duby (Chamberlain, 1974; Hymes & Cole, 1983); estructura y desarrollo de pelos en Gelidium caulacantheum J. Agardh, Gelidium vagum Okamura y Gracilaria pacifica Abbott. (Dromgoole & Booth, 1985; Oates & Cole, 1994).
Además se han investigado los factores que influyen en la formación de pelos, tales como el fotoperíodo (West, 1971), la concentración de nutrientes (Schonbeck & Norton, 1979; DeBoer & Whoriskey, 1983; Rueness et al., 1987), la intensidad de la luz (O'Conner & West, 1991; Kratz & Manoli, 1999), la salinidad (Mahasneh et al., 1990) y la temperatura (Mansfield, 1975). La formación de pelos en laboratorio en Gracilaria pacifica y Gelidium vagum fue inducida en medios de cultivo carentes de nitrógeno (Oates & Cole, 1994).
En este trabajo se describe el proceso de formación de pelos con microscopía óptica y electrónica en talos de Gracilaria chilensis Bird, McLachlan & Oliveira mantenidos en cultivo. La estructura fina de sus células vegetativas ha sido estudiada en un trabajo previo (Leonardi et al., 2006).
MATERIALES Y MÉTODOS
El estudio se realizó en talos de Gracilaria chilensis provenientes de cultivos en Caldera (27° 04' S, 70° 50' O), norte de Chile. Se cortaron 30 porciones de talos de 1 cm de longitud a partir del ápice y se colocaron en un medio de cultivo SFC (Correa, 1990), el cual contenía 21,2 g/l de Na NO3. A los 20 días de encontrarse los talos en este medio, se trasladó la mitad de ellos a Erlenmeyers con medio de cultivo carente de nitrógeno. Los restantes talos permanecieron en el medio con nitrógeno.
El material en estudio se mantuvo en una cámara de cultivo bajo condiciones controladas de luz (fotoperíodo de 12:12 horas de luz/oscuridad) y temperatura (12º C).
Se realizaron observaciones periódicas (2 ó 3 veces por semana) durante 35 días con un microscopio Leitz SM Lux. Se midió el ancho del talo (µm), la distancia desde el ápice al primer pelo (µm), el número de pelos y el largo y ancho de los pelos (µm, promedio de 10 pelos tomados al azar). Estas medidas se tomaron a los 20 y 35 días de iniciada la experiencia en los talos mantenidos en medio de cultivo con nitrógeno y a los 35 días en los talos creciendo sin nitrógeno. También se calculó en ambos casos la densidad de pelos como el número de pelos por mm² de talo. Se calcularon los errores estándar de cada variable y se compararon los tratamientos con y sin nitrógeno con un test t para varianzas heterogéneas.
Para la tinción de los núcleos de los pelos, se fijaron porciones de talos de G. chilensis en etanolácido acético glacial (3/1) durante 2 h y se tiñeron con orceína acética (La Cour, 1941).
El procesamiento de muestras para microscopía óptica y electrónica se realizó con porciones de talos de 2-3 mm de longitud que se fijaron en 3% de glutaraldehído en buffer Na-cacodilato 0.1M (pH 7.4), con 0.25M de sacarosa. Los fragmentos se seccionaron luego en porciones menores y se transfirieron a una nueva solución de fijador a la cual se le agregó 1.5% de paraformaldehído. Las muestras se post-fijaron durante 2 h en 2% de OsO4 buffer Na-cacodilato 0.1M, se deshidrataron en series de acetona y se infiltraron en resina Spurr (Spurr, 1969). El material se incluyó mediante el método de inclusión plana (Reymond & Pickett- Heaps, 1983).
Para microscopía óptica se tiñeron secciones semifinas (de 0,5-1 µm de espesor) con azul de toluidina 0,25%.
Para microscopía electrónica de transmisión, se contrastaron secciones de 70-90 nm de espesor con acetato de uranilo acuoso y citrato de plomo y se observaron en un microscopio electrónico de transmisión JEOL 100CX-II en el Centro de Investigaciones Básicas y Aplicadas de Bahía Blanca (CRIBABB).
Para microscopía electrónica de barrido se utilizaron porciones de talos de Gracilaria chilensis de 0,5 -1 cm de longitud que contenían pelos. Se fijaron en glutaraldehído 3% buffer Na-cacodilato 0,1M (pH 7,4), con 0,25M de sacarosa. Las muestras se deshidrataron en series de acetona y posteriormente se sometieron a punto crítico y metalizado con oro. Las observaciones se realizaron con un microscopio electrónico de barrido EVO 40 XVP Leo en el CRIBABB.
RESULTADOS
Formación de pelos
Gracilaria chilensis posee un talo que alcanza hasta 2 m de largo, formado por uno o varios ejes filamentosos largos, ramificados en forma alterna, opuesta o irregular. Los ejes son cilíndricos, de 1- 2 mm de diámetro. Los pelos de G. chilensis se desarrollan a partir de células corticales diferenciadas, denominadas células formadoras de pelos (CFPs) (Fig. 1A-B, flecha). Estas células poseen mayor tamaño (18 - 29 µm), que las células corticales normales (10 - 13 µm); son multinucleadas, tienen pequeños plástidos, sacos de mucílago y una red de retículo endoplasmático dispuesta en su extremo apical (Fig. 1C-D). Inicialmente la porción apical de la CFP se encuentra cubierta por una pared multilaminar y abundante mucílago (Fig. 1E). El proceso de formación de los pelos comienza con el desarrollo de una protuberancia en la parte apical de la CFP (Fig. 1D). A medida que la protuberancia crece, se forma una constricción entre su base y el extremo apical de la CFP (Fig. 1F, flecha). Con la consecuente elongación de la protuberancia se rompe la pared multilaminar junto con la pared del talo (Fig. 1G). El pelo queda establecido cuando se produce una citocinesis en la base de la protuberancia, formándose una conexión citoplasmática obliterada o "pit plug" asimétrica entre la base del pelo y la CFP (Fig. 1H, flecha).
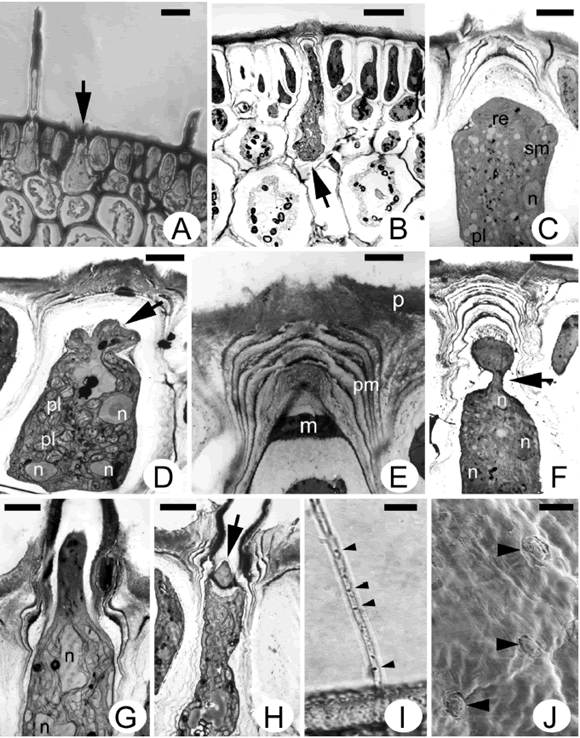
Fig. 1. Formación de pelos en Gracilaria chilensis. A-H, corte transversal de una porción del talo. A, fotomicrografía en la que se observa una célula formadora de pelos (CFP, flecha) y dos pelos en distinto grado de desarrollo. B-H, micrografías electrónicas de transmisión. B, vista general de una CFP (flecha). C, detalle de una CFP. Nótese el retículo endoplasmático de disposición apical. D, formación de una protuberancia (flecha) en la porción apical de una CFP. E, detalle de la pared multilaminar de la CFP. F, constricción entre la base de la protuberancia y el extremo distal de la CFP (flecha). G, ruptura de las paredes multilaminar y del talo por elongación de la protuberancia. H, "pit plug" asimétrica (flecha) entre la CFP y el pelo. I, fotomicrografía de un pelo maduro plurinucleado (puntas de flecha). J, micrografía electrónica de barrido de la superficie del talo. Cicatrices dejadas por los pelos al caerse (puntas de flecha). Escalas: A = 20 µm; B = 10 µm; C, D, F, H = 4 µm; E, G = 2 µm; I = 50 µm; J = 35 µm. Abreviaturas: m, mucílago; n, núcleo; p, pared celular; pl, plástido; pm, pared multilaminar; re, retículo endoplasmático; sm, sacos de mucílago.
Los pelos son unicelulares, poseen una vacuola (Fig. 1A) y numerosos núcleos (Fig. 1I, puntas de flecha). Tienen un crecimiento activo y son de vida corta, dejando, al caerse, una cicatriz de forma concéntrica en la superficie del talo (Fig. 1J, puntas de flecha).
Inducción de la formación de pelos
La densidad de pelos fue significativamente mayor (t = - 4,542, p = 0,0001) en talos cultivados en medio carente de nitrógeno (21,8 ±1,26 pelos/ mm², media ±ES) que en talos mantenidos en cultivo en medio con nitrógeno (12,3 ±1,66 pelos/mm2). También incrementó significativamente el largo y ancho de los pelos (t = - 3,484, p = 0,002 y t = -5,641, p = 0,0001, respectivamente) en medio sin nitrógeno (616 ±15,33 µm, y 12,19 ±0,36 µm, respectivamente), comparado con su desarrollo en medio con nitrógeno (534,25 ±17,76 µm y 9±0,44 µm respectivamente). Por el contrario, se registró una significativa disminución en el ancho de los talos (t = 4,312, p = 0,001) en medio carente de nitrógeno (601,3 ±8,63µm), con respecto a los que desarrollaron con nitrógeno (809,4 ±47,48 µm,).
DISCUSIÓN
Las características de las células formadoras de pelos (CFPs) de Gracilaria chilensis indican que estas células corticales son especializadas y muy activas metabólicamente. La condición multinucleada de estas células constituye una característica de las especies del género, ya que también son multinucleadas las CFPs de G. pacifica (Oates & Cole, 1994), G. compressa (C. Agardh) Greville y G. confervoides (L.) Greville (Kylin, 1930). La presencia de pequeños plástidos en la porción media inferior de las CFPs de G. chilensis coincide con lo indicado para otras células especializadas multinucleadas de algas rojas, como por ejemplo las células gonimoblásticas de Gigartina teedi (Roth) Lamouroux (Tsekos, 1982) y las células de fusión de Gracilaria verrucosa (Delivopoulos & Tsekos, 1985). La abundante red de retículo endoplasmático en la porción apical de las CFPs indicaría su participación en la síntesis del mucílago que acompaña a la pared multilaminar durante los primeros estados de la formación del pelo. En las CFPs de G. pacifica (Oates & Cole, 1994) y en las células de fusión de G.. verrucosa (Delivopoulos & Tsekos, 1985) el retículo endoplasmático se dispone de forma similar. A diferencia de lo observado en las especies de Gracilaria, las CFPs de Gelidium vagum (Oates & Cole, 1994) y de Gelidium caulacantheum (Dromgoole & Booth, 1985) son uninucleadas, poseen plástidos más desarrollados y retículo endoplasmático inconspicuo.
El desarrollo de los pelos de Gracilaria chilensis es comparable con lo descrito para otras Florideophyceae (Dixon, 1973). Durante los estados tempranos en la formación del pelo, en las CFPs de G. chilensis, al igual que en las CFPs corticales de Gracilaria pacifica y Gelidium vagum (Oates & Cole, 1994) y en las CFPs axiales apicales de Nemalion helminthoides (Duckett et al., 1974) y Audouinella hermannii (Hymes & Cole, 1983), se forma una protuberancia apoplástica. Esta forma de exclusión de plástidos de células especializadas durante la citocinesis fue descrita por Duckett et al. (1974) y es considerado un evento inusual en el reino vegetal. Un proceso similar ocurre durante el desarrollo de pelos celulares apoplásticos en el alga verde Bulbochaete hiloensis (Nordst.) Tiffany (Fraser & Gunning, 1973). Como en muchas algas rojas (Duckett et al., 1974; Dromgoole & Booth, 1985; Oates & Cole, 1994) los pelos de G. chilensis son unicelulares, incoloros, carecen de plástidos y poseen una vacuola central rodeada por una delgada capa de citoplasma. Si bien Dixon (1973) ha indicado que los pelos de las algas rojas son uninucleados, en el caso de G. chilensis, al igual que en G. pacifica (Oates & Cole, 1994) los pelos presentaron numerosos núcleos.
Las conexiones citoplasmáticas obliteradas o "pit plugs" de G. chilensis entre la base del pelo y la CFP son asimétricas, con el tapón proteico más grande del lado de la CFP; "pit plugs" similares fueron descriptas en Gracilaria pacifica y Gelidium vagum (Oates & Cole, 1994). En Audouinella hermannii se registraron "pit plugs" típicamente simétricas entre los pelos y las CFPs (Hymes & Cole, 1983).
La localización de los pelos en Gracilaria chilensis es subapical al igual que en Gelidium vagum (Oates & Cole, 1994) y G. caulacantheum (Dromgoole & Booth, 1985). Sin embargo, en G. verrucosa (Rueness et al., 1987), G. pacifica (Oates & Cole 1994), G. foliifera (Edelstein et al., 1978), G. confervoides y G. compressa (Kylin, 1930), los pelos se distribuyen por todo el talo, excepto en la porción inmediatamente apical. En las Florideophyceae Nemalion helminthoides (Duckett et al., 1974) y Audouinella hermannii (Hymes & Cole, 1983) los pelos, producidos repetidamente por células apicales, que actúan como las CFPs en filamentos axiales, se localizan apicalmente.
En este trabajo se observó en G. chilensis un incremento en la formación de los pelos, así como en su largo y ancho en talos cultivados en medio carente de nitrógeno. Estos resultados coinciden con estudios realizados en Gracilaria verrucosa (Rueness et al., 1987), Gracilaria pacifica y Gelidium vagum (Oates & Cole, 1994), Ceramium rubrum (DeBoer & Whoriskey, 1983) y Spyridia filamentosa (Wulfen) Harvey (O`Conner & West, 1991), cultivadas en similares condiciones de cultivo.
Cuando los nutrientes son escasos, el crecimiento del talo de G. chilensis es menor, aumenta el número de pelos, incrementando así el área disponible para el intercambio de nutrientes.
AGRADECIMIENTOS
Este trabajo ha sido realizado con un subsidio otorgado por la Unión Europea, INCO-DEV ICA4-CT2001-10021. Agradecemos a Pablo Martín su colaboración en el análisis estadístico de los datos.
BIBLIOGRAFÍA
1. Bird, C. J., J. McLachlan & E. C. Oliveira. 1986. Gracilaria chilensis sp. nov. (Rhodophyta, Gigartinales), from Pacific South America. Canad. J. Bot. 64: 2928-2934. [ Links ]
2. Boraso, A. L. 1983. Ecología de Gracilaria verrucosa (Hudson) Papenfuss en Poblaciones de la Provincia del Chubut (Argentina). Tesis doctoral, Universidad de Buenos Aires. [ Links ]
3. Chamberlain, A. H. L. 1974. Preliminary observations on the unicellular hairs of Ceramium rubrum (Huds.) C. Ag. Brit. Phycol. J. 9: 216. [ Links ]
4. Correa, J. A. 1990. Pigmented algal endophytes of Chondrus crispus Stackhouse: host specificity, fine structure, and effects on host performance in infections by Acrochaete operculata Correa & Nielsen and A. heteroclada Correa & Nielsen. Ph. D. thesis, Dalhousie University. [ Links ]
5. DeBoer, J. A. & F. G. Whoriskey. 1983. Production and role of hyaline hairs in Ceramium rubrum. Mar. Biol. 77: 229-234. [ Links ]
6. Delivopoulos, S. G. & I. Tsekos. 1985. Ultrastructure of the fusion cell in Gracilaria verrucosa (Huds.) Papenfuss (Rhodophyta, Gigartinales). New Phytol. 101: 605-612. [ Links ]
7. Dixon, P. S. 1973. Biology of the Rhodophyta. Koenigstein: Otto Koeltz Science Publishers. [ Links ]
8. Dromgoole, F. I. & W. E. Booth. 1985. The structure and development of hairs on the thallus of Gelidium caulacantheum J. Ag. New Zealand J. Mar. Freshwater Res. 19: 43-48. [ Links ]
9. Duckett, J. G., J. S. Buchanan, M. C. Peel & M. T. Martin. 1974. An ultrastructural study of pit connections and percurrent proliferations in the red alga Nemalion helminthoides (Vell. in With.) Batt. New Phytol. 73: 497-507. [ Links ]
10. Edelstein, T., L. Chen & J. McLachlan. 1978. Studies on Gracilaria (Gigartinales, Rhodophyta): reproductive structures. J. Phycol. 14: 92-100. [ Links ]
11. Fraser, T. W. & B. E. S. Gunning. 1973. Ultrastructure of the hairs of the filamentous green alga Bulbochaete hiloensis (Nordst.) Tiffany: an apoplastidic plant cell with a well developed Golgi apparatus. Planta 113: 1-19. [ Links ]
12. Hymes, B. J. & K. M. Cole. 1983. The cytology of Audouinella hermannii (Rhodophyta, Florideophyceae). I. Vegetative and hairs cells. Canad. J. Bot. 61: 3366-3376. [ Links ]
13. Kraft, G. T. & W. J. Woelkerling. 1990. Rhodophyta - Systematics and Biology, en M. N. Clayton & R. J. King (eds.), Biology of Marine Plants, pp 41-85, Melbourne: Longman Cheshire. [ Links ]
14. Kratz, R. F. & D. F. Manoli. 1999. The roles of light and the nucleus in the regulation of reproductive onset in Acetabularia acetabulum. Planta 209: 503-512. [ Links ]
15. Kylin, H. 1930. Über die Entwicklungsgeschichte der Florideen. Acta Univ. Lund. 26(6): 1-104. [ Links ]
16. La Cour, L. I. 1941. Acetic Orcein: a new stain fixative for chromosomes. Stain Technol. 16: 169-174. [ Links ]
17. Leonardi, P. I., A. B. Miravalles, S. Faugeron, V. Flores, J. Beltrán & J. A. Correa. 2006. Diversity, phenomenology and epidemiology of epiphytism in farmed Gracilaria chilensis (Rhodophyta) in northern Chile. Eur. J. Phycol. 41: 247-257. [ Links ]
18. Mahasneh, L. A., S. L. J. Grainger, & B. A. Whitton. 1990. Influence of salinity on hair formation and phosphatase activities of the blue-green alga (cyanobacterium) Calothrix viguieri. Brit. Phycol. J. 25: 25-32. [ Links ]
19. Mansfield, M. 1975. The effect of environmental factors in hyaline hair production by Ceramium spp. (Rhodophyceae). Master thesis, Portsmouth Polytechnic, Portsmouth, UK. [ Links ]
20. Nelson, W. A. 1987. The New Zealand species of Gracilaria Greville (Rhodophyta, Gigartinales). New Zealand J. Bot. 25: 87-98. [ Links ]
21. Oates B. R. & K. M. Cole. 1994. Comparative studies on hair cells of two agarophyte red algae, Gelidium vagum (Gelidiales, Rhodophyta) and Gracilaria pacifica (Gracilariales, Rhodophyta). Phycologia 33: 420-433. [ Links ]
22. O'Conner, K. A. & J. A. West. 1991. The effect of light and nutrient conditions on hair cell formation in Spyridia filamentosa (Wulfen) Harvey (Rhodophyta). Bot. Mar. 34: 359-364. [ Links ]
23. Reymond, O. L. & J. D. Pickett-Heaps. 1983. A routine flat embedding method for electron microscopy of microorganisms allowing selection and precisely orientated sectioning of single cells by light microscopy. J. Microscopy 130: 79-84. [ Links ]
24. Rosenvinge, L. K. 1911. Remarks on the hyaline unicellular hairs of the Florideae, en H. Hagerups Forlag (ed.), Biologiske Arbejder Tilegnede Eug. Warming, pp 203-215. Copenhagen: Bianco Lunos Boggrykkei Press. [ Links ]
25. Rueness, J., H. A. Mathiesen & T. Tananger. 1987. Culture and field observations on Gracilaria verrucosa (Huds.) Papenf. (Rhodophyta) from Norway. Bot. Mar. 30: 267-276. [ Links ]
26. Schonbeck, M. W. & T. A. Norton. 1979. The effects of diatoms on the growth of Fucus spiralis germlings in culture. Bot. Mar. 23: 233-236. [ Links ]
27. Spurr, A. R. 1969. A low-viscosity epoxy resin embedding medium for electron microscopy. J. Ultrastruct. Res. 26: 31-43. [ Links ]
28. Taylor, W. R. 1960. Marine algae of the Eastern Tropical and Subtropical coasts of the Americas. Michigan: The University of Michigan Press. [ Links ]
29. Tsekos, I. 1982. Plastid development and floridean starch grain formation during carposporogenesis in the red alga Gigartina teedii. Cryptog. Algol. 3: 91-103. [ Links ]
30. West, J. A. 1971. Environmental control of hair and sporangial formation in the marine red alga Acrochaetium proskaueri sp. nov. Proc. Int. Seaweed Symp. 7: 377-384. [ Links ]














