Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Darwiniana, nueva serie
versión impresa ISSN 0011-6793versión On-line ISSN 1850-1699
Darwiniana vol.48 no.1 San Isidro ene./jun. 2010
ESTRUCTURA Y DESARROLLO
Análisis morfológico y morfométrico del polen de Corchorus, Heliocarpus, Luehea, Mollia y Triumfetta (Malvaceae, Grewioideae) en la región austral de América del Sur
Mónica V. Mambrín1, María M. Avanza2 &María S. Ferrucci1
1Cátedra de Morfología de Plantas Vasculares. Instituto de Botánica del Nordeste (IBONE), Facultad de Ciencias Agrarias (FCA), Universidad Nacional del Nordeste (UNNE). Sargento Cabral 2131, 3400 Corrientes, Argentina; valeman12@hotmail.com (autor corresponsal).
2Cátedra de Cálculo Estadístico y Biometría, FCA, UNNE, Argentina.
Resumen
Aunque Grewioideae es conocida como la única subfamilia estenopalínica de Malvaceae, los análisis de polen publicados sugieren una variación morfológica. Para comprobar si la variación estructural podría tener valor taxonómico, la morfología del polen de 16 especies de los géneros Corchorus, Heliocarpus, Luehea, Mollia y Triumfetta (Malvaceae, Grewioideae) distribuidas en la región austral de América del Sur fue analizada con microscopía óptica y electrónica de barrido. Los granos de polen son 3-zonocolporados, isopolares, radiosimétricos, subesferoidales a prolatos y de tamaño mediano a grande. La escultura de la exina varía desde un birretículo con perforaciones en el lumen a un tectum densamente rugulado o microrreticulado. Los caracteres morfológicos de polen obtenidos con microscopio óptico fueron utilizados en un análisis multivariado para evaluar la variabilidad dentro y entre los géneros. El análisis de componentes principales (PCA) permitió diferenciar cinco grupos sobre la base de forma y tamaño del grano, largo del colpo, ancho y alto de la endoabertura y espesor de la exina. Las especies estudiadas comparten el polen tipo Grewia característico de la mayoría de las especies de Grewioideae y Byttnerioideae, pero los caracteres polínicos analizados son de reducido valor diagnóstico a nivel genérico y/o específico.
Palabras clave. Grewioideae; Malvaceae; Morfometría; Polen.
Abstract
Morphological and morphometrical pollen analysis of Corchorus, Heliocarpus, Luehea, Mollia and Triumfetta (Malvaceae, Grewioideae) in southern South America
Although Grewioideae is known as the only stenopalynous subfamily of Malvaceae, previous published pollen analyses suggest morphological variation. To test if that structural variation could have taxonomic value, pollen morphology of 16 species of the genera Corchorus, Heliocarpus, Luehea, Mollia and Triumfetta (Malvaceae, Grewioideae) distributed in southern South America was analysed by light and scanning electron microscopy. Pollen grains are 3-zonocolporate, isopolar, radially symmetrical, subspheroidal to prolate, and medium to large in size. Exine sculpture varies from a bireticulate reticulum with perforated lumina to densely tectate-rugulate or tectate-microreticulate. Pollen morphological characteristics from light microscopy were used in a multivariate analysis to assess variation within and among the genera. Principal components analyses (PCA) clearly separate five groups based on pollen shape and size, colpus length, endoaperture height and width, and exine thickness. The species here studied share the Grewia pollen type, like most species of Grewioideae and Byttnerioideae, but the palynological characters analyzed have little taxonomic value at genus or species level.
Keywords. Grewioideae; Malvaceae; Morphometry; Pollen.
Introducción
La familia Malvaceae, está representada por árboles, arbustos, subarbustos y plantas herbáceas. Cuenta con 243 géneros y alrededor de 4300 especies de distribución cosmopolita aunque con una mayor representación en las zonas intertropicales (Bayer & Kubitzki, 2003). Estudios recientes, basados en datos morfológicos, moleculares y biogeográficos, recuperan el concepto amplio de Malvaceae propuesto por Adanson (1763) que incluye a miembros de otras familias, entre ellas Sterculiaceae y Bombacaceae. Se delimitaron en Malvaceae nueve subfamilias (Bayer et al., 1999; Judd et al., 1999 y Bayer & Kubitzki, 2003), entre ellas, las Grewioideae y Byttnerioideae constituyen un clado monofilético, correspondiéndole a Grewioideae una posición basal en la familia (Stevens, 2008). Las especies estudiadas en este trabajo, antes incluidas en la familia Tiliaceae Cronquist, 1981), pertenecen actualmente a la subfamilia Grewioideae, palinológicamente caracterizada por granos de polen más o menos prolatos, 3-colporados, usualmente microperforados y frecuentemente con retículo supratectal (Bayer et al., 1999).
Entre los trabajos pioneros sobre la morfología del polen en la familia Tiliaceae, basados en el análisis con microscopio óptico, debemos citar el de Erdtman (1966), quien reconoció tres tipos de granos de polen: Grewia, Tilia y otros, en este último tipo incluye la descripción del polen de especies de diferentes géneros con características disímiles. El tipo Grewia, actualmente representativo de las especies de la subfamilia Grewioideae, se caracteriza por presentar los granos tricolporados, colpos largos y sexina reticulada. Entre las floras polínicas regionales que incluyen la morfología de las Grewioideae se encuentran los trabajos de Sharma (1969), Barth & Barbosa (1973), Markgraf & D'Antoni (1978), Martínez-Hernández et al. (1978), Moncada & Salas (1983), Roubik & Moreno (1991), Corrêa-da-Silva et al. (1992), Quiroz-García et al. (1994), Jacobs (1998), Mambrín & Ferrucci (2006), El-Husseini (2006) y Perveen & Qaiser (2007). Sin embargo, el aporte más significativo a nivel mundial acerca de las antiguas Tiliaceae es el de Perveen et al. (2004), quienes analizaron la morfología del polen de 85 especies correspondientes a 32 géneros de las subfamilias Brownlowioideae, Grewioideae y Tilioideae. Estos autores, sobre la base del tipo de abertura, patrón de exina y forma del grano, reconocen tres tipos de polen: Mortoniodendron, Berrya y Corchorus; este último relacionado con la subfamilia Grewioideae.
Grewioideae es una subfamilia con la mayoría de los géneros estenopalínicos, pero a pesar de esta uniformidad morfológica los estudios sobre morfología polínica de sus especies sugieren que existe variación en la forma y en el patrón de exina. Razón por la cual nos preguntamos si esta variación morfológica será suficiente como para delimitar subgrupos polínicos dentro de las Grewioideae, y si esos grupos son concordantes con la delimitación de los géneros de esta subfamilia. Para analizar este problema este trabajo se propone caracterizar la variabilidad de la morfología polínica de todas las especies de Malvaceae - Grewioideae, representadas en la región austral de América del Sur.
Materiales y métodos
Se analizaron los granos de polen de 16 especies de la familia Malvaceae, Grewioideae, correspondientes a los géneros Corchorus L., Heliocarpus L., Luehea Willd., Mollia Mart. y Triumfetta L.
Los granos de polen fueron tratados utilizando la técnica de acetólisis (Erdtman, 1966), se montaron en gelatina glicerinada y luego se sellaron con parafina. Las preparaciones se encuentran depositadas en la Palinoteca (PAL-CTES) de la Universidad Nacional del Nordeste (UNNE).
En la Tabla 1 se presentan las nueve variables cuantitativas continuas analizadas para cada especie utilizando en cada caso de dos a cinco ejemplares. Se midieron entre 40 a 100 granos de polen por especie para las variables P (eje polar), E (eje ecuatorial) y P/E (eje polar /eje ecuatorial x 100) y entre 20 a 50 granos para las variables IAP (índice de área polar), LC (largo de colpo), AC (ancho de colpo), AP (alto de poro), ANP (ancho de poro) y exina (espesor de exina). Las mediciones de las variables se realizaron con un microscopio óptico (MO) OLYMPUS BX50. Las fotomicrografías se obtuvieron con un microscopio óptico OLYMPUS BX40 con cámara SC 35 OLYMPUS, y para el análisis de la estructura de la pared se utilizaron fotomicrografías tomadas con un microscopio electrónico de barrido (MEB) JSM-5800LV del servicio de microscopía de la UNNE.
Tabla 1. Caracteres palinológicos evaluados en cada especie.

La terminología utilizada en las descripciones de la morfología del polen es la propuesta por Barth & Melhem (1988) y Punt et al. (2007). Con el fin de describir la morfología del polen de cada especie se calcularon los promedios y desvíos estándar de las variables analizadas. Para explorar la variabilidad entre las especies y realizar un agrupamiento según su semejanza, se realizó un análisis de componentes principales (ACP) utilizando como medida de asociación la distancia Euclídea promedio, mediante el software estadístico InfoStat (2008).
Material examinado
Corchorus argutus Kunth (CA). ARGENTINA. Corrientes. Depto. Santo Tomé, 13-II-1991, Tressens et al. 3851 (CTES) PAL 2419. Formosa. Depto. Pilcomayo, 01-XI-1991, Fortunato et al. 2192 (CTES) PAL 2459. Misiones. Depto. Capital, 28-I-1993, Seijo 304 (CTES) PAL 2406. BRASIL. Mato Grosso do Sul. Passo do Lontra, 18-V-2002, Hatschbach et al. 73120 (CTES) PAL 2464. PARAGUAY. Amambay. 14-XII-1997, Schinini & Dematteis 33824 (CTES) PAL 2450.
Corchorus hirtus L. (CH). ARGENTINA. Formosa. Depto. Pilcomayo, 28-II-1996, Schinini & Cuadrado 30503 (CTES) PAL 2407. Salta. Depto. Gral. San Martín, 09-IV-1996, Krapovickas & Cristóbal 46727 (CTES) PAL 2417. BRASIL. Mato Grosso do Sul. Fazenda Santa Cruz, 06-VI-1994, Hatschbach et al. 60746 (CTES) PAL 2465. PARAGUAY. Amambay. Parque Nacional Cerro Corá, 12-XII-1989, Vanni et al. 1361 (CTES) PAL 2344. Cordillera. Piribebuy, 10-I-1987, Mereles 792 (CTES) PAL 2451.
Heliocarpus popayanensis Kunth (HP). ARGENTINA. Misiones. Depto. Guaraní, 17-VI-1994, Rodríguez 944 (CTES) PAL 2414; Depto. San Pedro, 22-IX-1993, Dematteis et al. 123 (CTES) PAL 2403. PARAGUAY. Guairá. Cordillera de Ybytyruzú, 14-VII-1989, Zardini 13431 (CTES) PAL 2348. Paraguarí. VII-1992, Soria 5241 (CTES) PAL 2452.
Luehea candicans Mart. (LC). ARGENTINA. Misiones. Depto. Iguazú, 01-IX-2001, Herrera 259 (CTES) PAL 2420. PARAGUAY. Canindeyú. 24-II-1984, Hahn 2078 (CTES) PAL 2427. Central. Tembetari, 10-I-1955, Schulz 8870 (CTES) PAL 2398.
Luehea conwentzii K. Schum. (LCO). BRASIL. Paraná. 03-I-1967, Hatschbach et al. 15619 (CTES) PAL 2443; Salto Murato, 15-XI-1993, Hatschbach & Silva 59782 (CTES) PAL 2444.
Luehea divaricata Mart. (LD). ARGENTINA. Corrientes. Depto. Monte Caseros, 22-II-1979, Schinini et al. 17565 (CTES) PAL 2421. Misiones. Depto. Iguazú, 19-XII-1991, Vanni et al. 3012 (CTES) PAL 2402. PARAGUAY. Alto Paraná. 15-III-1996, Ferrucci et al. 934 (CTES) PAL 2441.
Luehea fiebrigii Burret (LF). ARGENTINA. Salta. Depto. Santa Victoria, 25-V-1971, Cuezo 8412 (LIL) PAL 2423. BOLIVIA. Tarija. 05-II-1970, Meyer et al. 22980 (CTES) PAL 2400.
Luehea grandiflora Mart. (LG). PARAGUAY. Amambay. 14-IX-1988, Ferrucci et al. 673 (CTES) PAL 2447; 20-VIII-1980, Schinini & Borda 20513 (CTES) PAL 2426.
Luehea microcarpa R. E. Fr. (LM). ARGENTINA. Misiones. Depto. Iguazú: I-1900, s/c (BAF) PAL 2422. BRASIL. Mato Grosso do Sul. 20-V-2002, Hatschbach et al. 73208 (CTES) PAL 2446. PARAGUAY. Amambay. Hassler 12072 (G) PAL 2409.
Luehea paniculata Mart. (LP). BOLIVIA. La Paz. 29-IX-1985, Solomon 14309 (CTES) PAL 2399. BRASIL. Minas Gerais. 29-VIII-1990, Mendonça et al. 1623 (CTES) PAL 2416. PARAGUAY. Paraguarí. Hassler 829 (G) PAL 2458.
Mollia lepidota Spruce ex Benth. (ML). BOLIVIA. Santa Cruz. 31-X-1999, Nee 50369 (CTES) PAL 2460. BRASIL. Amazonas. 08-VII-1986, Thomas et al. 5316 (CTES) PAL 2470. Mato Grosso do Sul. 12-XII-1973, Hatschbach 33092 (CTES) PAL 2457.
Triumfetta bogotensis DC. (TB). ARGENTINA. Corrientes. Depto. Concepción, 30-III-1974, Krapovickas et al. 24651 (CTES) PAL 2440. ECUADOR. Pichincha. 24-XII-1986, Zak 1493 (CTES) PAL 2448. PARAGUAY. Central. XII-1968, Schinini 1346 (CTES) PAL 2449.
Triumfetta guaranitica Villa (TG). ARGENTINA. Misiones. Depto. Iguazú, 1902, Llama s/n (BAF) PAL 2425; 9-III-2002, Múlgura de Romero et al. 3165 (CTES) PAL 2462; Depto. Guaraní, 26-III-1998, Zuloaga et al. 680 (CTES) PAL 2415. BRASIL. Paraná. 20-III-2001, Cordeiro & Barbosa 1903 (CTES) PAL 2445.
Triumfetta obscura A. St.-Hil., A. Juss. & Cambess. (TO). ARGENTINA. Misiones. Depto. El Dorado, 10-III-2001, Keller 653 (CTES) PAL 2454. BRASIL. Santa Catarina. 08-II-1994, Krapovickas & Cristóbal 44830 (CTES) PAL 2453.
Triumfetta rhomboidea Jacq. (TR). BOLIVIA. Beni. 22-V-1987, Solomon 16707 (CTES) PAL 2469. BRASIL. Minas Gerais. 21-V-1990, Arbo et al. 4526 (CTES) PAL 2408. Santa Catarina. 19-I-1991, Krapovickas & Cristóbal 43758 (CTES) PAL 2428.
Triumfetta semitriloba Jacq. (TS). ARGENTINA. Corrientes. Depto. Ituzaingó, 29-III-2000, Tressens et al. 6629 (CTES) PAL 2461; Depto. Saladas, 20-IV-1973, Schinini et al. 6327 (CTES), PAL 2337. Misiones. Depto. Apóstoles, 11-III-1969, Krapovickas et al. 15098 (CTES) PAL 2418; Depto. San Ignacio, Quiroga 7674 (BAF) PAL 2433; 23-III-1996, Tressens et al. 5551 (CTES) PAL 2410. PARAGUAY. Caazapá. 12-II-2001, Herrera 352 (CTES) PAL 2442.
Resultados
Morfología del polen
Caracteres generales de los granos de polen. Los granos de polen son 3-zonocolporados, isopolares, radiosimétricos, subesferoidales a prolatos (Figs. 1A, C, E, G, I, K, M, O, Q-S) y de tamaño mediano a grande (Tabla 2). Contorno en vista polar subcircular (Figs. 1B, D, H, J, P, T), circular (Figs. 1F, L) a semiangular (Fig. 1N), parasincolporados o raro sincolporados. Colpos largos y generalmente angostos (Figs. 1A, C, E, I, M, O, Q-S), menos frecuente no tan angostos (Figs. 1G, 3C, I); endoabertura lalongada, de contorno elíptico (Figs. 1A, S), en algunos casos rectangular (Figs. 1G, O) o subcircular (Fig. 1C), generalmente con los extremos poco discernibles, y a veces fusionadas lateralmente (Figs. 1I, R). La exina de espesor variable, sexina similar o ligeramente más gruesa que la nexina, esta última generalmente engrosada a la altura de las endoaberturas formando costillas (Figs. 1A, C, E, I, Q, R). Sexina tectado-perforada, birreticulada (Figs. 2D-F; 3F-G y 4D-F) o raramente tectado-rugulada o tectado-microrreticulada (Figs. 3J, K); retículo heterobrocado, lúmenes subcirculares con muros curvos (Figs. 3F-G) a poligonales con muros rectos (Figs. 2D-F y 4D-F), el tamaño de éstos se reduce hacia los polos y en el borde de las aberturas formando un margo (Figs. 2B-C y 4A, C, F).

Fig. 1. A-B, Corchorus argutus. A, vista ecuatorial. B, vista polar. C-D, C. hirtus. C, vista ecuatorial. D, vista polar. E-F, Heliocarpus popayanensis. E, vista ecuatorial. F, vista polar. G-H, Luehea candicans. G, vista ecuatorial con detalle del contorno rectangular de la endoabertura. H, vista polar. I-J, L. divaricata. I, vista ecuatorial, zonorado. J, vista polar. K-L, L. microcarpa. K, vista ecuatorial. L, vista polar. M-N, L. grandiflora. M, vista ecuatorial. N, vista polar. O-P, Mollia lepidota. O, vista ecuatorial, con detalle del contorno rectangular de la endoabertura. P, vista polar. Q, Triumfetta semitriloba, vista ecuatorial. R, T. guaranitica, vista ecuatorial, zonorado. S-T, T. obscura. S, vista ecuatorial, endoabertura de contorno elíptico. T, vista polar. Escala: 10 µm. La flecha señala la costilla. A-B de Tressens et al. 3851, C de Schinini 30503, D de Krapovickas & Cristóbal 4677, E de Rodríguez 944, F de Dematteis et al. 123, G de Hahn 2078, H de Schulz 8870, I de Schinini et al. 17565, J de Vanni et al 3012, K-L de Hassler 12072, M-N de Schinini & Borda 20513, O-P de Nee 50369, Q de Krapovickas et al. 15098, R de Llamas s.n., S-T de Keller 653.
Tabla 2. Matriz de promedios, desvíos estándar y valores mínimos y máximos obtenidos para nueve variables (columnas) en las 16 especies (filas).


Fig. 2. A, D, Corchorus argutus. A, vista ecuatorial. D, detalle de escultura, mesocolporo. B, E, C. hirtus. B, vista ecuatorial. E, detalle de escultura, mesocolporo. C, F, Heliocarpus popayanensis. C, vista ecuatorial, se aprecia el margo. F, detalle de colporo. A, D de Hatschbach & Ribas 73120, B, E de Vanni et al. 1361, C, F de Zardini 13431.

Fig. 3. A, Luehea candicans, vista ecuatorial. B, F, L. conwentzii. B, vista ecuatorial. F, detalle de escultura, mesocolporo. C-D, G, L. microcarpa. C, vista ecuatorial. D, vista polar. G, detalle de escultura, mesocolporo. E, L. grandiflora, vista ecuatorial. H-K, Mollia lepidota, H-I, vista ecuatorial. J, detalle de escultura, exina rugulada. K, detalle de escultura, exina microrreticulada. A, de Hahn 2078, B, F de Hatschbach & Silva 59782, C, D, de Hatschbach et al. 73208, E, de Schinini & Borda 20513, H, J de Thomas et al. 5316, I, K de Nee 50369.
Descripciones palinológicas por género. En la Tabla 2 se consignan los promedios, desvíos estándar y valores mínimos y máximos para las variables P, E, P/E, IAP, LC, AC, AP, ANP y espesor de exina correspondientes a las 16 especies analizadas.
Corchorus L.
MO (Figs. 1A-D). Granos subesferoidal-subprolatos a prolatos, de tamaño mediano a grande en C. argutus, en C. hirtus siempre prolatos y medianos. Contorno en vista polar subcircular, área polar pequeña. Colpos largos con costillas, de mayor longitud en C. argutus; endoabertura lalongada de contorno elíptico, o subcircular, raro zonorado en C. argutus. Exina de 2,5 µm de espesor promedio, sexina de igual espesor que la nexina. Lúmenes de 1,44-5,76 µm de diámetro y muros de 0,29-0,96 µm de ancho, simplicolumelados.
MEB (Figs. 2A-B, D-E). Lúmenes irregulares amplios y poco profundos, éstos disminuyen de tamaño próximos a las aberturas; presentan perforaciones distribuidas en todo el lumen de 0,10-0,31 µm de diámetro; muros bajos, rectos y angostos. Colpos con margo.
Heliocarpus L.
MO (Figs. 1E-F). Granos prolatos, de tamaño mediano. Contorno en vista polar circular, área polar pequeña. Colpos largos, con costillas; endoabertura lalongada de contorno elíptico. Exina de 2,8 µm de espesor promedio, la sexina de similar espesor que la nexina. Lúmenes de 1,92-4,8 µm de diámetro y muros de 0,38-0,96 µm de ancho, simplicolumelados.
MEB (Figs. 2C, F). Lúmenes irregulares, amplios, más profundos que en Corchorus, con perforaciones distribuidas en la base de los muros, estos últimos rectos y angostos. Colpos con margo.
Luehea Willd.
MO (Figs.1G-N). La forma en este género es muy variable, las especies L. candicans, L. conwentzii, L. fiebrigii y L. microcarpa presentan granos subesferoidal-subprolatos, en L. divaricata son subesferoidal-subprolatos a prolatos, en L. paniculata subesferoidal-prolato esferoidales a subprolatos, medianos a veces grandes a excepción de L. grandiflora que presenta granos subesferoidal-prolato esferoidales de tamaño grande destacándola de las otras. Contorno en vista polar subcircular, circular a semiangular, área polar en general pequeña, a excepción de L. candicans con área polar grande. Colpos largos pero de menor longitud que en el resto de las especies descriptas, con costillas, endoabertura lalongada de contorno generalmente elíptico, rectangular en L. candicans y L. conwentzii, o a veces zonorados como sucede en L. divaricata. Exina de espesor variable, sexina de similar espesor que la nexina. Lúmenes de 1,44-5,76 µm de diámetro y muros de 0,48-1,67 µm de ancho, generalmente simplicolumelados a excepción de L. candicans, L. divaricata, L. fiebrigii y L. microcarpa que pueden presentar de simpli- a tricolumelados.
MEB (Figs. 3A-G). Lúmenes subcirculares, perforados y pequeños, en algunos casos éstos disminuyen próximos a las aberturas y hacia los polos, con perforaciones de 0,08-0,74 µm de diámetro distribuidas en la base de los muros, los cuales son bajos y curvos; en L. conwentzii las perforaciones también se pueden observar en los muros (Fig. 3F).
Mollia Mart.
MO (Figs. 1O-P). Granos prolatos, de tamaño mediano a grandes. Contorno en vista polar subcircular, área polar pequeña. Colpos largos, con costillas; endoabertura lalongada de contorno elíptico o rectangular. Exina de espesor variable, la sexina es más gruesa que la nexina, densamente rugulada o microrreticulada (aparentemente psilada), lúmenes de 1,44-1,92 µm de diámetro y muros de 0,67 a 0,96 µm de ancho, simplicolumelados.
MEB (Figs. 3H-K). La exina puede presentarse rugulada o microrreticulada, variabilidad observada en dos ejemplares de diferente procedencia.
Triumfetta L.
MO (Figs. 1Q-T). Granos prolatos, de tamaño mediano a grande en T. bogotensis, T. guaranitica, T. rhomboidea y T. semitriloba y grandes en T. obscura. Contorno en vista polar circular a subcircular, área polar pequeña. Colpos largos, con costillas; endoabertura lalongada de contorno elíptico, a veces circular en T. semitriloba o zonorados en T. guaranitica. El espesor de la exina es variable, la sexina es más gruesa que la nexina en T. bogotensis, T. obscura, T. rhomboidea y de similar espesor en T. guaranitica y T. semitriloba. Lúmenes de 1,92-6,72 µm de diámetro y muros de 0,48-0,96 µm de ancho; simplicolumelados.
MEB (Figs. 4A-F). Lúmenes poligonales, con perforaciones distribuidas en todo el lumen de 0,10-0,59 µm de diámetro; muros bajos, rectos y angostos.
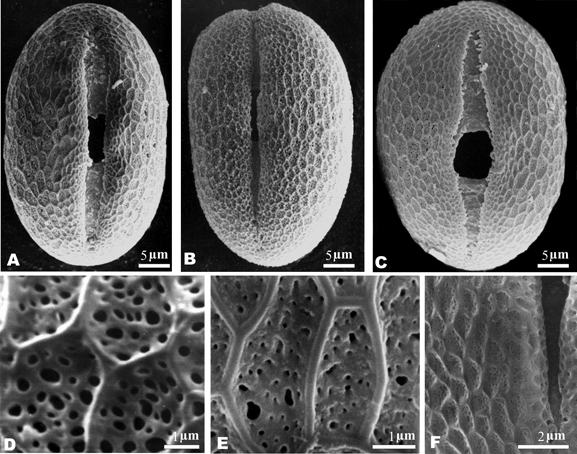
Fig. 4. A, Triumfetta bogotensis, vista ecuatorial. B, T. rhomboidea, vista ecuatorial. C, F, T. semitriloba. C, vista ecuatorial. F, detalle parcial del colpo, mostrando el margo. D, T. guaranitica, detalle de escultura. E, T. obscura, detalle de escultura, mesocolporo. A, de Zak 1493, B de Solomon 16707, C de Tressens et al. 5551, D de Cordeiro & Barbosa 1903, E de Keller 653, F de Schinini et al. 6227.
Análisis de componentes principales (ACP)
En el gráfico en dos dimensiones resultante del ACP (Fig. 5), se muestra que la primera componente (CP1) explicó el 47% de la variación y la segunda componente (CP2) el 31,8%, y entre ambas explican el 79% de la variabilidad total. En la construcción de CP1 las variables eje polar (P), largo de colpo (LC) y alto de poro (AP) reciben los autovectores (e1) positivos más altos, separando las especies por el tamaño de los granos y las aberturas. En la construcción de CP2 las variables (P/E) y espesor de exina (exina) presentan los autovectores (e2) positivos más altos, y las variables eje ecuatorial (E) y ancho de poro (ANP) presentan autovectores negativos (Tabla 3). Esto implica que la CP2 provee información diferente sobre la variabilidad de las especies, agrupándolas de acuerdo a la forma de granos, espesor de exina, E y ANP. Además, en la Tabla 3, se puede observar que las variables P, LC y AP presentan mayor correlación (positiva) con CP1, y por otro lado las variables P/E y espesor de exina presentan alta correlación positiva con CP2, mientras que las variables E y ANP presentan alta correlación negativa con CP2. De acuerdo a estos resultados, se agruparon las variables de igual comportamiento respecto a CP1 y CP2, y se representaron en la Fig. 5 mediante flechas que indican el sentido en que aumenta cada grupo de variables.

Fig. 5. Gráfico bidimensional de las dos primeras componentes del ACP de las 16 especies y sus características palinológicas (Tabla 2).
Tabla 3. Autovectores (e1 y e2) y correlaciones de las componentes principales (CP1 y CP2) con las variables originales, obtenidos en el ACP.

En la Fig. 5 se observan los siguientes agrupamientos, por un lado las especies de Triumfetta: T. rhomboidea, T. bogotensis, T. semitriloba, T. guaranitica y T. obscura, con granos prolatos de tamaño en general grande, colpos largos, poros altos y exina de espesor variable. Corchorus argutus y Mollia lepidota forman un grupo que presenta granos medianos, a veces grandes, subesferoidal-subprolatos a prolatos, colpos de longitud media y exina de similar espesor que las anteriores. Corchorus hirtus y Heliocarpus popayanensis se agrupan, ambas exhiben granos medianos, prolatos, colpos de longitud media y exina de similar espesor que las anteriores. Las especies de Luehea: L. candicans, L. conwentzii, L. divaricata, L. fiebrigii, L. microcarpa y L. paniculata forman un grupo que presenta granos medianos, de forma variable desde subesferoidales a prolatos, colpos largos y espesor de exina media a excepción de L. conwentzii que presenta exina delgada. La especie Luehea grandiflora no se asocia con ninguna de las anteriores debido a que los granos de polen son grandes y subesferoidal-prolato esferoidales, con colpos de mayor longitud.
Discusión
Todas las especies estudiadas en este trabajo corresponden al tipo Grewia, uno de los tres tipos de polen que describió Erdtman (1966) para Tiliaceae, familia incluida actualmente en Malvaceae, y que se caracteriza por granos 3-zonocolporados, con colpos largos y sexina reticulada, y en algunos casos con exina microperforada y con retículo supratectal; este tipo de polen es característico de la mayoría de las especies de las subfamilias Byttnerioideae y Grewioideae (Bayer et al., 1999). Además, el análisis de la morfología polínica indicó que las especies coinciden con el tipo Corchorus, según Perveen et al. (2004), que se caracteriza por los granos prolatos o subprolatos, raro prolato esferoidales y con el subtipo A, que presenta tectum reticulado y lúmenes con perforaciones, a excepción de Mollia lepidota que correspondería al subtipo B, que se caracteriza por un tectum densamente rugulado o microrreticulado. La ornamentación de la exina de las especies analizadas de Corchorus, Heliocarpus, Luehea y Triumfetta concuerda con el tipo Corchorus depresus, mientras que Mollia lepidota coincide con los tipos C. tridens y C. aestuans; tipos polínicos que fueron propuestos por Perveen & Qaiser (2007).
Los resultados de este trabajo coinciden con el rango de variación de las variables analizadas por Mambrín & Ferrucci (2006), quienes en un estudio previo de especies del nordeste de Argentina, analizaron 11 especies de cuatro géneros de Tiliaceae, las que se incluyeron en el tipo llamado Luehea divaricata caracterizado por la forma, el tamaño y el tipo de abertura de los granos de polen, con tres subtipos rediferenciados según la escultura de la exina.
Los granos de polen de Corchorus argutus y C. hirtus principalmente se diferencian por su forma. Por un lado, se destaca el agrupamiento de C. argutus con Mollia lepidota, especies que presentaron similitud en la mayoría de los caracteres palinológicos, principalmente en la forma (subesferoidal-subprolatos a prolatos) y el largo de colpos. Por otra parte, Corchorus hirtus y Heliocarpus popayanensis, con granos prolatos, presentan una similitud ya observada por Perveen et al. (2004) para H. popayanensis y otras especies de Corchorus. Los rangos de valores correspondientes a las variables analizadas en Corchorus argutus y C. hirtus concuerdan con los de cinco especies asiáticas del género (Sharma, 1969) y con los de C. siliquosus L. (Moncada & Salas, 1983). Sin embargo, las dimensiones correspondientes a P y E citadas por Roubik & Moreno (1991) para C. siliquosus sobre la base de material de Panamá, son mayores a las encontradas en C. argutus y C. hirtus. En el análisis del polen de 11 especies del este de África, Jacobs (1998) citó dimensiones similares a las nuestras para P, mientras que son menores para el espesor de la exina. El-Husseini (2006) describió el polen de tres especies representadas en Egipto, donde las dimensiones de los granos son notablemente menores a las observadas en el presente trabajo, sin embargo la razón P/E es similar.
El polen de Heliocarpus popayanensis se caracteriza por presentar un retículo con lúmenes pequeños y muros relativamente anchos. Roubik y Moreno (1991) señalaron para H. popayanensis dimensiones superiores para P, E y ANP. Quiroz-García et al. (1994) en el análisis de H. pallidus Rose, especie mexicana, registraron dimensiones mayores en P y en el IAP, en cambio, los valores de las otras variables concuerdan con los observados aquí. Perveen et al. (2004) observaron en H. americanus L., H. americanus var. popayanensis y H. terebinthinaceus (DC.) Hochr., la presencia de perforaciones distribuidas en el lumen; éste es el único carácter que no concuerda con las observaciones realizadas en H. popayanensis.
En Luehea, el análisis conjunto de las variables estudiadas permitió reconocer dos tipos de granos de polen sobre la base del tamaño y la forma en las especies del género, uno formado por L. candicans, L. conwentzii, L. divaricata, L. fiebrigii, L. microcarpa y L. paniculata, el cual se caracteriza por presentar granos medianos y en algunos casos grandes, de forma subesferoidal-subprolatos a prolatos; y otro tipo sólo presente en L. grandiflora, con granos grandes y subesferoidal-prolato esferoidales. Los valores de las variables palinológicas obtenidas en L. divaricata y L. paniculata coinciden con lo descrito por Barth & Barbosa (1973). Las dimensiones de P y E en L. divaricata son inferiores a los valores encontrados por Markgraf & D'Antoni (1978) sobre la base de material de Entre Ríos (Argentina) y superiores respecto al espesor de la exina. De acuerdo a los resultados presentados por Perveen et al. (2004) para L. conwentzii, los promedios de P y E son inferiores, aunque la relación P/E coincide; para L. divaricata y L. paniculata los promedios de E son inferiores a los nuestros, como así también la relación P/E. Luehea microcarpa, L. divaricata y L. candicans comparten caracteres de escultura como muros angostos, diámetro de lúmenes y sus perforaciones, mientras que L. paniculata posee muros anchos en relación a los lúmenes, los que disminuyen hacia los polos en donde forman un microrretículo; en algunos casos se aprecian granos sincolporados, observaciones que concuerdan con Perveen et al. (2004). Para L. candida (DC.) Mart Quiroz-García et al. (1994) registraron valores semejantes en P/E y espesor de exina, mientras que las variables P, E, LC y AC son mayores a las observadas en esta contribución.
En el género Mollia, los dos especimenes analizados de M. lepidota presentaron variación en la escultura, variando desde densamente rugulada a microrreticulada; mientras Perveen et al. (2004) observaron que en M. grandiflora Mart. la exina es densamente rugulada y en M. speciosa Mart. varía desde densamente rugulada a reticulada, en ambas especies las dimensiones son menores respecto a M. lepidota.
Por último, las especies del género Triumfetta mostraron mayor homogeneidad en la mayoría de las variables analizadas; T. obscura exhibe los valores más altos en tamaño de grano, longitud de colpo y alto de poro. En general, este grupo de especies se caracteriza por presentar granos prolatos y grandes, resultados que concuerdan con Sharma (1969), Barth & Barbosa (1973) y Perveen et al. (2004) para otras especies del género y Corrêa-da-Silva et al. (1992) para T. semitriloba. Las dimensiones de los granos de T. semitriloba son superiores a lo citado por Perveen et al. (2004). Las especies de Triumfetta mostraron resultados similares respecto a la forma de los lúmenes, los cuales son poligonales con perforaciones distribuidas en todo el lumen. Quiroz-García et al. (1994) citan para T. acracantha Hochr. valores similares a T. rhomboidea, información que concuerda con lo señalado por El-Husseini (2006) para T. flavescens A. Rich.
Bayer & Kubitzki (2003), en relación a la morfología polínica, reconocieron para Malvaceae s. l. cinco tipos de polen, se destaca que ninguno de ellos es exclusivo de una subfamilia. La subfamilia Grewioideae es un taxón estenopalínico, pues la mayoría de sus especies comparte el polen tipo Grewia (también presente en las Byttnerioideae). Los caracteres polínicos aquí analizados presentan variaciones de reducido valor diagnóstico a nivel genérico y/o específico, pues si bien permiten distinguir grupos de especies según su morfología polínica, estos grupos no son siempre coherentes con las delimitaciones de los géneros.
Agradecimientos
Agradecemos a I. Wichmann la digitalización de las imágenes, como así también a los revisores anónimos cuyas sugerencias enriquecieron el trabajo. Este trabajo ha sido subsidiado por la Agencia Nacional de Promoción Científica y Tecnológica (ANPCyT-UNNE, PICTO 00096) y por el Consejo Nacional de Investigaciones Científicas y Técnicas (PIP Nº 112-200801-02248).
Bibliografía
1. Adanson, M. 1763. Familles des plantes, vol. 2, pág. 390. Paris: Vincent. [ Links ]
2. Barth, O. M. & A. F. Barbosa. 1973. Catálogo Sistemático dos Pólens das Plantas Arbóreas do Brasil Meridional. XVII-Eleocarpaceae e Tiliaceae. Memórias do Instituto Oswaldo Cruz 71: 203-213. [ Links ]
3. Barth, O. M. & T. S. Melhem. 1988. Glossário ilustrado de Palinologia. Campinas: Editora da UNICAMP. [ Links ]
4. Bayer, C.; M. F. Fay; A. Y. de Bruijn; V. Savolaimen; C. M. Morton; K. Kubitzki; W. S. Alverson & M. WChase. 1999. Support for an expanded family concept of Malvaceae within a recircunscribed order Malvales: a combined analysis of plastid atpB and rbcL DNA sequences. Botanical Journal of the Linnean Society 129: 267-303. [ Links ]
5. Bayer, C., & K. Kubitzki. 2003. Malvaceae, in Kubitzki, K. (ed.), The Families and Genera of Vascular Plants, vol. 5, pp. 225-311. Berlin: Springer. [ Links ]
6. Corrêa-da-Silva, A. M.; H. M.Watanabe & T. S. Melhem. 1992. Flora Poliníca da Reserva do Parque Estadual das Fontes do Ipiranga (São Paulo, Brasil). Hoehnea 19: 117-124. [ Links ]
7. Cronquist, A. 1981. An integrated system of classification of flowering plants. New York: Columbia University Press. [ Links ]
8. El-Husseini, N. 2006. Pollen morphology of Tiliaceae Juss. and Sterculiaceaae Vent. and their relations to Malvaceae Juss. in Egypt. International Journal of Agriculture and Biology 8: 844-847. [ Links ]
9. Erdtman, G. 1966. Pollen morphology and plant taxonomy. Angiosperms. New York: Hafner Publishing. [ Links ]
10. InfoStat. 2008. Grupo InfoStat, FCA, Universidad Nacional de Córdoba, Argentina. [ Links ]
11. Jacobs, T. V. 1998. Advancement index of East African species of Corchorus (Tiliaceae). Phyton 62: 151-154. [ Links ]
12. Judd, W. S.; C. S. Campbell; E. E. Kellog & P. F. Stevens. 1999. Plant Systematics a phylogenetic approach. Sunderland, Massachusetts: Sinauer Associates. [ Links ]
13. Mambrín, M. V. & M. S. Ferrucci. 2006. Tiliaceae, en S. M. Pire; L. M. Anzótegui & G. A. Cuadrado (eds.), Flora Polínica del Nordeste Argentino III: 137-141. [ Links ]
14. Markgraf, V. & H. L. D'Antoni. 1978. Pollen Flora of Argentina. Tucson: The University of Arizona Press. [ Links ]
15. Martínez-Hernández, E.; P Fernández & S. Lozano. 1978. Pollen of tropical trees. I. Tiliaceae. Journal of the Arnold Arboretum 59: 299-309. [ Links ]
16. Moncada, M. & E. Salas. 1983. Polen de las melíferas en Cuba. Centro de Información y Divulgación Agropecuario. La Habana: Centro de información y divulgación agropecuario. [ Links ]
17. Peña, D. 2002. Análisis de datos multivariantes. Madrid: Mc Graw Hill. [ Links ]
18. Perveen, A.; E. Grafström & G. El-Ghazaly. 2004. World Pollen and Spore Flora 23. Malvaceae Adams. p.p., Subfamilies: Grewioideae, Tilidoideae, Brownlowioideae. Grana 43: 129-155. [ Links ]
19. Perveen, A. & M. Qaiser. 2007. Pollen Flora of Pakistan-Malvaceae-Grewioideae-LII. Pakistan Journal of Botany 39: 1-7. [ Links ]
20. Punt, W.; P. P. Hoen; S. Blackmore; S. Nilsson & A. Le Thomas. 2007. Glossary of pollen and spore terminology. Review of Paleobotany and Palynology 143: 1-81. [ Links ]
21. Quiroz-García, D. L.; R. Palacios-Chávez & M. L. Arreguín-Sánchez. 1994. Flora Polínica de Chamela, Jalisco. (Familias Amaranthaceae, Combretaceae, Loasaceae, Martyniaceae, Papaveraceae, Tiliaceae y Viloaceae). Acta Botánica Mexicana 29: 61-81. [ Links ]
22. Roubik, D. W. & J. E Moreno. 1991. Pollen and spores of Barro Colorado Island. Monographs in Systematic Botany from the Missouri Botanical Garden 36: 1-270. [ Links ]
23. Sharma, B. D. 1969. Pollen morphology of Tiliaceae in relation to plant taxonomy. Journal of Palynology: 7-29. [ Links ]
24. Stevens, P. F. 2008. Angiosperm Phylogeny Website. Version 9. http://www.mobot.org/MOBOT/research/APweb/. Accesed: Feb. 2009. [ Links ]














