Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680versión On-line ISSN 1669-9106
Medicina (B. Aires) v.63 n.2 Buenos Aires mar./abr. 2003
Intercambio gaseoso en el síndrome de dificultad respiratoria aguda
G. A. Raimondi
Instituto Raúl Carrea, FLENI, Buenos Aires
Dirección postal: Dr. Guillermo A. Raimondi, Instituto Raúl Carrea FLENI. Montañeses 2325, C1428AQK Buenos Aires, Argentina
Fax: (54-11) 5777-3209. E-mail: raimondi@fleni.org.ar
Resumen
El síndrome de dificultad respiratoria aguda (ARDS) se caracteriza por presentar alteraciones severas del intercambio gaseoso (IG) causadas por «shunt» e importante irregularidad de la ventilación perfusión (VA/Q). Esto es consecuencia del edema intersticial y el colapso y ocupación alveolar. Además de la fracción inspirada de oxígeno y la evolución de la patología pulmonar, hay distintas variables que son capaces de alterar la presión parcial de oxígeno arterial (PaO2). Es así que los cambios del volumen minuto circulatorio, la concentración de hemoglobina, el consumo de oxígeno o la alcalosis pueden modificar la PaO2 a través de su influencia en la PO2 de sangre venosa mixta. A pesar de la influencia de estas diferentes variables, la anormalidad del IG se ha podido analizar adecuadamente por medio de la técnica de eliminación de múltiples gases inertes (MIGET). Asimismo, se han descripto diversas estrategias ventilatorias (presión positiva de fin de espiración, relaciones inspiratorias-espiratorias invertidas, volúmenes corrientes elevados, etc.) que producen mejoría del IG principalmente a través del aumento de la presión media en la vía aérea al reclutar áreas pulmonares previamente colapsadas. También el cambio de decúbito a posición ventral, por modificaciones en la distribución de presión pleural regional, disminuye el colapso alveolar con mejoría de la PaO2. Asimismo hay distintas intervenciones farmacológicas capaces de mejorar el IG tales como la administración de óxido nítrico (ON) o de prostaglandinas (PGI2 o PGE1) por vía inhalatoria. Estas producen vasodilatación de las áreas bien ventiladas aumentando el flujo cardíaco a ese nivel y disminuyendo relativamente el flujo por las áreas de «shunt». La almitrina endovenosa, droga vasoconstrictora pulmonar, mejora el IG al aumentar la vasoconstricción hipóxica. Se ha demostrado efecto aditivo de la almitrina con la inhalación de ON. A pesar del efecto beneficioso de todas estas técnicas en la mejoría del IG en el ARDS, no se ha demostrado efecto beneficioso en la sobrevida.
Palabras clave: Síndrome de dificultad respiratoria aguda; Intercambio gaseoso; Asistencia respiratoria mecánica.
Abstract
Gas exchange in acute respiratory distress syndrome. The hypoxemia of acute respiratory distress syndrome (ARDS) depends chiefly upon shunt and ventilation-perfusion (VA/Q) inequality produced by fluid located in the interstitial space, alveolar collapse and flooding. Variables other than inspired oxygen fraction and the underlying physiological abnormality can influence arterial oxygen partial pressure (PaO2). Changes in cardiac output, hemoglobin concentration, oxygen consumption and alcalosis can cause changes in PaO2 through their influence on mixed venous PO2. Gas exchange (GE) in ARDS may be studied using the inert gas elimination technique (MIGET) which enables to define the distribution of ventilation and perfusion without necessarily altering the FIO2 differentiating shunt from lung units with low VA/Q ratios and dead space from lung units with high VA/Q ratios. Different ventilatory strategies that increase mean airway pressure (positive end-expiratory pressure, high tidal volumes, inverse inspiratory-expiratory ratio, etc) improve PaO2 through increasing lung volume by recruiting new open alveoli and spreading the intra-alveolar fluid over a large surface area. Also prone-position ventilation would result in a marked improvement in GE enhancing dorsal lung ventilation by the effects on the gravitional distribution of pleural pressure and the reduction in the positive pleural pressure that develops in dorsal regions in ARDS. Inhaled nitric oxide (NO) has been shown to increase PaO2 in ARDS patients by inducing vasodilation predominantly in ventilated areas redistributing pulmonary blood flow away from nonventilated toward ventilated areas of the lung thus resulting in a shunt reduction. On the same way inhaled prostaglandins (PGI2 or PGE1) causes selective pulmonary vasodilation improving pulmonary GE. Intravenous almitrine, a selective pulmonary vasoconstrictor, has been shown to increase PaO2 by increasing hypoxic pulmonary vasoconstriction. A synergistic effect was found between inhaled NO and almitrine. In spite of the improval of GE shown by these different techniques on ARDS, no effect was demonstrated on mortality or duration of mechanical ventilation.
Key words: Acute respiratory distress syndrome (ARDS); Gas exchange; Mechanical ventilation.
El síndrome de dificultad respiratoria aguda (ARDS) se caracteriza por anormalidad de la función y estructura respiratoria con disminución de volúmenes pulmonares y compliance y aparición de hipoxemia. El daño que producen las distintas causas desencadenantes, tanto en el endotelio como en el epitelio alveolar, producen aumento de la permeabilidad incrementando el agua pulmonar extravascular en el espacio intersticial y alveolar.
La acumulación de líquidos comienza por el tejido conectivo laxo peribronquial y perivascular1. Si eventualmente este exceso no puede ser evacuado por el drenaje linfático, el intersticio de las paredes alveolares se inunda y cuando la capacidad de esta pared es excedida, el líquido ocupa los alvéolos. Esta ocupación comienza por las esquinas produciendo inestabilidad alveolar por alteración de la tensión superficial y como consecuencia de ello, al ocuparse totalmente el alveolo, se produce el colapso. Por mecanismos de presión hidrostática estos cambios ocurren preferentemente en las zonas pulmonares inferiores («dependent zones»). Este mayor compromiso en las zonas pulmonares inferiores y asimetría a lo largo del eje vertical ha sido descripto muy claramente por el grupo de Gattinoni2, con una zona pulmonar superior continuamente abierta a la ventilación, una inferior con colapso y consolidación y otra intermedia que puede ser reclutada o desreclutada de acuerdo a la estrategia ventilatoria utilizada.
Intercambio gaseoso
La anormalidad del intercambio gaseoso (IG) depende de esta secuencia de acumulación de líquido. Se ha demostrado que el edema intersticial puede producir cierre de la vía aérea pequeña en zonas pulmonares inferiores con disminución del flujo aéreo sin alterar significativamente el intercambio gaseoso3. Este se modifica notablemente cuando ocurre ocupación alveolar4.
De esta manera la hipoxemia en el ARDS se debe a esta última etapa de la secuencia de producción de edema con ocupación alveolar. Los primeros trabajos de ARDS describían hipoxemia sin respuesta a la inhalación de oxígeno por presencia de «shunt» intrapulmonar de zonas alveolares completamente ocupadas y perfundidas5.
Algunos autores sugirieron la existencia de trastornos de difusión. Esto se supuso, entre otras razones, en función del cálculo teórico de engrosamiento de la membrana alveolo-capilar o por la existencia de diferencia alveolo arterial de nitrógeno1,6. Por otro lado King y col.7 observaron aumentos de la presión parcial de oxígeno arterial (PaO2) al aumentar la fracción inspirada de oxígeno (FIO2) que no se podía explicar si el «shunt» fuera la única causa de la hipoxemia. Lamy y col. describieron resultados similares en pacientes en cuya biopsia de pulmón encontraban predominantemente fibrosis, explicando esto por trastorno de difusión y desigualdad de ventilación perfusión extrema8. Asimismo, Bachofen y col.9 sugirieron que las lesiones fibróticas, que son características de las lesiones avanzadas de ARDS, producían alteraciones de difusión a través de disminución del área de intercambio gaseoso pulmonar o el engrosamiento de la barrera aire-sangre. Esta aparente relación del tipo de lesión y el mecanismo fisiológico de la hipoxemia en estos dos últimos trabajos resalta el problema de la inhomogeneidad de los pacientes con ARDS, sobretodo por la evolución temporal de las lesiones. Teniendo en cuenta esto nos referimos en este trabajo a las anormalidades del IG producidas por las lesiones exudativas de los primeros estadios del ARDS.
La interpretación de estos estudios es difícil si tenemos en cuenta que hay otras variables capaces de alterar la PaO2 aparte de la FIO2 y las anormalidades fisiológicas pulmonares. Las modificaciones del volumen minuto circulatorio (Q), la concentración de hemoglobina, el consumo de oxígeno y la alcalosis pueden producir cambios de la PaO2 a través de su influencia en la presión parcial de oxígeno de la sangre venosa mixta (PvO2).
Una manera de obviar esta influencia en la evaluación del mecanismo de la hipoxemia es a través de la técnica de eliminación de múltiples gases inertes (MIGET)10. Este método puede definir la distribución de ventilación-perfusión sin necesariamente alterar la FIO2. Puede diferenciar el «shunt» de las unidades pulmonares con relación baja de ventilación perfusión (VA/Q) y también el espacio muerto de las unidades pulmonares con VA/Q elevados. Asimismo permite inferir a través de distintos cálculos la presencia de anormalidades significativas de difusión11,12.
Con esta técnica se puede demostrar que en pacientes con ARDS el flujo sanguíneo está dividido en dos tipos de unidades pulmonares, unas bien ventiladas y perfundidas, cuyas relaciones VA/Q se encuentran en rango normal y otras sin ventilación o «shunt»13,14. A pesar que estos pacientes están habitualmente en asistencia respiratoria mecánica (ARM) no se observan unidades pulmonares groseramente hiperventiladas y el espacio muerto, en volumen absoluto, es normal. Aparte, algunos pacientes muestran unidades perfundidas con muy baja relación VA/Q13,14. Estas unidades no parecen ser unidades estables y continuamente ventiladas o que estén marcadamente hipoventiladas o sobreperfundidas. Se podría suponer que a este nivel extremo de VA/Q podrían convertirse en zonas atelectásicas debido a la rápida absorción de oxígeno, sobre todo a las FIO2 elevadas a las que habitualmente están ventilados estos pacientes15,16. Sin embargo es posible que estas unidades con VA/Q muy bajos sean alvéolos ocupados con líquido cuyo volumen aumente suficientemente durante parte del ciclo respiratorio para permitir un mínimo IG. A pesar de tener un muy bajo VA/Q, estas unidades pueden intervenir en el IG y explicar el aumento de la PaO2 al aumentar la FIO210.
El hecho que la relación de equilibrio de la difusión de gases inertes sea tan rápida sin la existencia de gradiente alveolar fin de capilar, permite asumir que no existe anormalidad de difusión para el oxígeno17.
Influencia de la PvO2 y el volumen minuto en el intercambio gaseoso
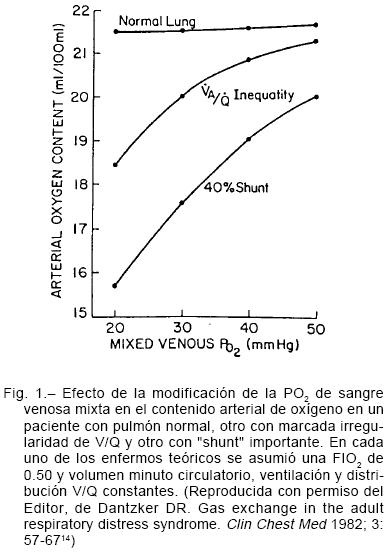
Hay que tener en cuenta el efecto que puede tener el cambio de la PvO2 en la PaO2. La PvO2 influencia notablemente la PO2 de fin de capilar, sobre todo cuanto más bajo sea el VA/Q18. Hay distintas situaciones que se asocian con disminución de la PvO2, tales como la caída del Q, el aumento del consumo de oxígeno, la anemia o la alcalosis severa. En estas circunstancias la disminución de la PvO2 producirá caída de la PaO2. Esta disminución de la PaO2 será más notable cuanto más alto sea el «shunt» o la irregularidad de VA/Q pero casi nada en un pulmón normal13,14 (Fig 1). Debe tenerse en cuenta que distintas variables no pulmonares pueden tener influencia en la PaO2 y que las variaciones de ésta no necesariamente significan cambios de las condiciones respiratorias del ARDS.
Así como indirectamente la PvO2 puede influenciar en la PaO2, el incremento de la FIO2 produce aumento de la PaO2. Este aumento es muy importante en los pacientes con bajo «shunt» mientras que son insignificantes si el «shunt» es alto (Ej.: 50%)(Fig 2). Sin embargo, teniendo en cuenta las características de la curva de disociación de la oxihemoglobina, aun estos pequeños cambios de la PaO2 producen aumentos de contenido arterial de oxígeno con notable mejoría de la entrega de oxígeno tanto en pacientes con bajo o alto «shunt» 13,14 (Fig 2).

Estrategias ventilatorias
Hay distintos enfoques terapéuticos capaces de mejorar el intercambio gasesoso en el ARDS. La ARM es la medida de sostén más importante en estos pacientes. Está demostrado que el agregado de presión positiva espiratoria (PEEP), la ventilación con volúmenes corrientes elevados o la utilización de ARM con relación inspiratoria-espiratoria invertida (entre otras razones por el auto PEEP que genera) producen aumento de la PaO2. Este grado de mejoría de la PaO2 está relacionada con el aumento de la presión media de la vía aérea19,20. En un trabajo clásico de Staub se resume el mecanismo básico de mejoría del intercambio gaseoso con la ARM, haciendo notar que el aumento de volúmenes pulmonares incrementa el tamaño alveolar y escurre líquido en el alveolo sobre una superficie mayor21. Esto permite que el gas entre al alveolo y que la PEEP lo mantenga abierto a lo largo de todo el ciclo respiratorio. Esta mejoría de la PaO2 con la PEEP se la ha relacionado, en trabajos clínicos clásicos, con los aumentos de volúmenes pulmonares medidos con gases inertes5. También se ha supuesto que la PEEP es capaz de modificar el balance neto de agua pulmonar extravascular. Posiblemente no produzca cambios netos en la misma, sino que la redistribuya desde el intersticio alveolar hacia las bandas peribronquiales o perivasculares permitiendo mejorar el IG22.
Se ha demostrado por medio del MIGET, tanto en animales como en humanos, que la PEEP mejora la PaO2 principalmente aumentando los volúmenes alveolares y disminuyendo el volumen minuto distribuido al compartimiento de «shunt». En algunos pacientes la PEEP genera unidades con relaciones de VA/Q altas por hiperventilación y por derivación del flujo sanguíneo de unidades pulmonares relativamente normales10,13,14. Asimismo, aumenta el espacio muerto debido a aumento de volumen pulmonar o al producir condiciones de zona I de West11. La explicación de estos dos últimos hechos ha sido demostrada anatómicamente por Hedenstierna23 que encontraba que la PEEP producía reducción grosera (pero no eliminación total) del flujo sanguíneo a las áreas pulmonares superiores. Estos cambios posiblemente dependan no solamente del valor de la PEEP sino también del estado hemodinámico del paciente.
Si bien la PEEP mejora la PaO2 disminuyendo el «shunt» al reclutar áreas alveolares, hay otros mecanismos que también pueden producir esta disminución. La PEEP, así como toda forma ventilatoria que aumenta la presión media de la vía aérea, disminuye el Q. Esto lo hace principalmente a través de disminución del retorno venoso y de la precarga ventricular izquierda24. Se ha demostrado que este decremento del Q, tanto en animales como en humanos, produce caída del «shunt» intrapulmonar, sean estas modificaciones del Q realizadas con cambios de los volúmenes intravasculares25, cambiando el retorno venoso mecánicamente o mediante drogas vasoactivas26-29. Si bien se han sugerido distintas explicaciones para este hecho, lo más lógico es suponer que la caída del Q produzca disminución de la PvO2 y aumento de la vasoconstricción hipóxica con disminución del «shunt» y mejoría subsecuente del intercambio gaseoso30,31. Hay que tener en cuenta entonces que el aumento de la presión en la vía aérea disminuye el «shunt» al aumentar los volúmenes pulmonares pero también puede disminuir el «shunt» a través de la caída del Q. En el caso que este último efecto predomine, podría disminuir el transporte de oxígeno a los tejidos a pesar de una posible mejoría de la PaO2. Cabe recalcar que las alteraciones del intercambio gaseoso en el ARDS pueden estar influenciadas no solamente por las variaciones de la patología de base, la FIO2 o la forma ventilatoria, sino también por los cambios hemodinámicos.
Otra técnica que ha resultado útil en la mejoría del intercambio gaseoso del ARDS es la ARM en decúbito prono («prone position ventilation») (DP). En pacientes en decúbito dorsal, la presión transpulmonar en las áreas dorsales es menor que la presión de apertura de la vía aérea y eventualmente en presencia de injuria pulmonar se producen atelectasias. El DP mejora el intercambio gaseoso al mejorar la distribución por gravedad hidrostática de la presión pleural, con disminución de la presión positiva pleural en las regiones dorsales aumentando la ventilación pulmonar32. De hecho, tanto la ventilación como las relaciones de VA/Q mejoran en estas áreas cuando se adopta el DP. El DP genera una presión transpulmonar capaz de superar la presión de apertura de la vía aérea en las regiones dorsales donde las atelectasias, «shunt» y heterogenicidad de las relaciones VA/Q son más severas, sin afectar negativamente las regiones pulmonares ventrales. Está probado experimentalmente que en zonas pulmonares inferiores («dependent zones»), al fin de espiración, la presión pleural es más negativa en los animales ventilados en DP33. Asimismo se ha demostrado que el DP disminuye la compresión del pulmón por el corazón34. Esta mejoría del IG se ha estudiado claramente mediante la técnica de MIGET en animales35,36. Esto también se ha demostrado en pacientes con ARDS con mejoría estable de la relación PaO2/FIO2 ya a la hora de adoptar este decúbito y manteniendo este efecto, aunque en forma parcial, una hora después de haber vuelto a decúbito dorsal37. También se ha descripto, al menos hasta 120 minutos después de volver al decúbito dorsal, aumento de la compliance estática pulmonar38. Se ha observado que algunos pacientes responden y otros no a la ventilación en DP37. En aquellos en los que se encuentra respuesta, ésta se mantiene al menos parcialmente 1 hora después de retornar a la posición supina37. Esta mejor respuesta al decúbito prono se observa en aquellos pacientes que tienen mayor compliance estática de la pared torácica (Cst,w) describiéndose una correlación significativa entre la PaO2 y la Cst,w38. También se ha descripto una correlación significativa entre los cambios de la Cst,w al cambiar a decúbito prono vs. el aumento de la PaO238. Así como otras técnicas que mejoran el intercambio gaseoso en el ARDS han mostrado efectos aditivos (ON, almitrina, prostaciclina inhalada) lo mismo ocurre cuando la ventilación en DP se combina con inhalación de ON39 o con almitrina más ON40.
Efecto de la administración de oxígeno puro en el intercambio gaseoso
Se ha descripto en pacientes con insuficiencia respiratoria aguda que la ventilación con oxígeno puro (FIO2 1.0) produce atelectasias por reabsorción como resultado de la «denitrogenación» de unidades alveolares con bajas relaciones de VA/Q15,16,41. Por otro lado, en trabajos clínicos el Qva/Qt, medido por medio de la fórmula de Qs/Qt de oxígeno, aumentaba significativamente42,43. Asimismo, también se ha descripto al respirar oxígeno puro que el «shunt» medido por medio del MIGET o bien no aumentaba44,45 o bien aumentaba46. Por otro lado, en estudios clásicos en los que se estudia la respuesta a la FIO2 1.0 en pacientes con insuficiencia respiratoria grave (Ej.: Qs/Qt>0.50) se ha demostrado disminución de la admisión venosa medida con la técnica de inhalación de oxígeno7,8,47,48. Una de las diferencias de estos estudios era el valor previo del Qva/Qt. En el caso de los estudios antes citados en los que el Qva/Qt aumentaba, la admisión venosa de los pacientes era baja (@0.20)43, en los que no cambiaba el Qva/Qt era intermedio (@0.30)44,45, mientras en los que mejoraba el Qva/Qt era alto (>0.50)7,8,47,48. Es probable que la respuesta al oxígeno pueda depender de la admisión venosa previa de los pacientes. De hecho se ha descripto una relación significativa entre admisión venosa con FIO2 de mantenimiento (Qva/Qtm) vs los cambios de Qva/Qt con FIO2 1.0, es decir DQs/Qt (Qs/t - Qva/Qtm), disminuyendo éste claramente cuando la admisión venosa es alta49,50 (Fig 3).

El hecho que ambas variables presentan datos en común (datos compartidos) (Qva/Qtm) podría hacer suponer que la significación de la correlación hallada se deba a acoplamiento matemático de datos («coupling of data»). Efectivamente, referente a esto, Archie JP51 afirma que este es un error común que puede llevar a la conclusión de que existe una relación cuando de hecho ésta no existe. Si bien el probable acoplamiento matemático de datos puede ser evitado con un adecuado diseño del trabajo evitando datos calculados por técnicas en común, este no era nuestro caso ya que las variables medidas no se podían estimar fácilmente por distintas técnicas. Hay autores que han descripto métodos de corrección de estos posibles errores provenientes de cálculos de regresiones con datos compartidos52,53. El análisis realizado de esta forma en distintos ejemplos de la literatura permite concluir que el error adjudicable al uso de datos compartidos es despreciable siempre y cuando el rango de la variable independiente sea suficientemente grande y los errores y dispersión de las medidas sean de tamaño razonable52,53. Si bien nosotros no hemos realizado el cálculo de corrección, el hecho que la dispersión y error del método para la medición del Qva/Qt o Qs/Qt sea pequeño y el rango de la variable independiente grande, permite suponer la validez de los resultados hallados.
Es entonces evidente que el cambio del Qva/Qt al respirar oxígeno puro depende de múltiples factores. Por un lado, aumento de la admisión venosa por atelectasias por reabsorción y/o inhibición de la vasoconstricción pulmonar hipóxica, y por otro la eventual disminución de la misma con mejoría del intercambio gaseoso en áreas pulmonares con desigualdad extrema de VA/Q y/o eventual trastorno de difusión. Parecería ser que en los pacientes con severas anormalidades del intercambio gaseoso este último efecto juega un papel importante y que el Qs/Qt con FIO2 1.0 tiende a disminuir. Sería importante probar si esto ocurre en enfermos muy comprometidos por medio del MIGET54. Es de hacer notar la diferencia de los pacientes estudiados en los distintos trabajos. En algunos de ellos no está claramente definido el criterio de ARDS45 y en otros son pacientes con neumonía más que pacientes con injuria pulmonar aguda o ARDS44,48,50,55. Por otro lado, hay que tener en cuenta que se han descripto diferencias en la mecánica pulmonar de pacientes con ARDS pulmonar vs. ARDS extra-pulmonar56. No sería de extrañar que así como el comportamiento de la mecánica pulmonar es diferente en distintos tipos de ARDS también fuera diferente el mecanismo de alteración del intercambio gaseoso con distinta respuesta a la inhalación de oxígeno. Tal vez los diferentes modelos de alteración del intercambio gaseoso descriptos en ARDS mediante la técnica de MIGET se deban a estos diferentes tipos de ARDS10,13,14. Sería interesante poder estudiar en el futuro el comportamiento de ambos tipos de ARDS mediante la técnica de MIGET.
Otras técnicas capaces de modificar el intercambio gaseoso en el ARDS
El ON es un potente vasodilatador que puede ser administrado por vía inhalatoria produciendo vasodilatación de la vasculatura pulmonar sin producir efecto sistémico. Se ha demostrado en pacientes con ARDS severo que el ON induce vasodilatación principalmente en áreas ventiladas. De esta manera produce mejoría del intercambio gaseoso con redistribución de flujo de áreas de «shunt» no ventiladas a áreas ventiladas pero poco perfundidas57. La respuesta al ON es diferente en distintos pacientes y debe ser titulada. Hay pacientes que requieren 0.5 ppm o hasta 40 ppm en la mezcla inspirada58. La mejoría de la PaO2 no depende de la PaO2 previa sino que correlaciona con el índice de resistencia vascular pulmonar (IRVP) basal. Es decir, que cuanto más alto el IRVP previo más mejora la PaO259. Asimismo el aumento de la PaO2 no depende de la respuesta a la PEEP ya que tanto los pacientes que mejoran o no con ella aumentan en igual medida la PaO2 al administrar ON59.
Cuando se compara el efecto del ON vs. la terapéutica convencional, la respuesta de la mejoría del intercambio gaseoso es mayor en las primeras 24 hs en el grupo que recibe ON58,60. Después de las 24 hs no hay respuesta a la inhalación de ON, mostrando tanto los pacientes con tratamiento convencional o con ON igual PaO2/FIO258,60. Asimismo, como se ha descripto con otras técnicas capaces de mejorar el intercambio gaseoso en el ARDS, no se ha podido demostrar que la administración de ON mejore la sobrevida de estos pacientes58,61. Esto es lo que ha llevado a un editorialista a cuestionarse si el tratamiento inhalatorio con ON no es solo una terapéutica «cosmética»62.
Otra droga que es capaz de mejorar el intercambio gaseoso en el ARDS es la almitrina. Esta actúa aumentando la vasoconstricción hipóxica63 con aumento de la PaO2 y leve incremento de la presión en la arteria pulmonar64. La administración de almitrina EV junto con la inhalación de ON han mostrado efectos aditivos en la mejoría del IG mayores que cualquiera de estas dos por separado65-68.
Así como la inhalación de ON es capaz de inducir vasodilatación arterial pulmonar, hay otras drogas que también son capaces de producir vasodilatación en el ARDS. Tal es el caso de las prostaglandinas administradas por vía endovenosa, sea la PGI2 o la PGE169,70. De esta manera producen disminución de la vasoconstricción hipóxica regional con aumento de flujo sanguíneo a las unidades de «shunt» y disminución de la PaO2. Por otro lado, si la prostaglandina se administra por vía inhalatoria es capaz de producir vasodilatación selectiva en las unidades pulmonares ventiladas, mejorando el IG al aumentar el flujo por estas áreas respecto a las áreas no ventiladas de «shunt». Hay trabajos realizados tanto con prostaciclina (PGI2) o prostaglandina E1 (PGE1) inhaladas que demuestran que el efecto de éstas es similar a la inhalación de ON en la mejoría del IG71-73.
1. Staub NC, Nagano H, Pearce ML. Pulmonary edema in dogs, especially the sequence of fluid accumulation in lungs. J Appl Physiol 1967; 22: 227-40. [ Links ]
2. Gattinoni L, DAndrea L, Pelosi P, Vitale G, Pesenti A, Fumagalli R. Regional effects and mechanism of positive end-expiratory pressure in early adult respiratory distress syndrome. JAMA 1993; 269: 2122-7. [ Links ]
3. Iliff LD, Greene RE, Hughes IMB. Effects of intersticial edema on distribution of ventilation and perfusion in isolated lung. J Appl Physiol 1972; 33: 462-7. [ Links ]
4. Muir AL, Hall DL, Despas P, Hogg JC. Distribution of blood flow in the lungs in acute pulmonary edema in dogs. J Appl Physiol 1972; 33: 763-9. [ Links ]
5. Pontoppidan H, Geffin, Lowenstein E. Acute respiratory failure in the adult. N Engl J Med 1972; 287: 690-8. [ Links ]
6. Markello R, Winter PM, Olszowska A. Assessment of ventilation inequalities by arterial-alveolar nitrogen differences in intensive care patients. Anesthesiology 1972; 37: 4-15. [ Links ]
7. King TKC, Weber B, Okinaka A, Friedman SA, Smith JP, Briscoe WA. Oxygen transfer in catastrophic respiratory failure. Chest 1974; 65: 40S-44S. [ Links ]
8. Lamy M, Fallat RJ, Koeniger E, et al. Pathologic features and mechanisms of hypoxemia in adult respiratory distress syndrome. Am Rev Respir Dis 1976; 114: 267-84. [ Links ]
9. Bachofen A, Weibel ER. Alterations of gas exchange apparatus in adult respiratory insufficiency associated with septicemia. Am Rev Respir Dis 1977; 116: 589-615. [ Links ]
10. Dantzker DR, Brook CH, DeHart P, Lynch JP, Weg JG. Gas exchange in adult respiratory distress syndrome and the effects of positive end-expiratory pressure. Am Rev Respir Dis 1979; 120: 1039-52. [ Links ]
11. Dueck R, Wagner PD, West JB. Effects of positive end-expiratory pressure on gas exchange in dogs with normal and edematous lungs. Anesthesiology 1977; 47: 359-66. [ Links ]
12. Wagner PD, Saltzman HA, West JB. Measurements of continuous distributions of ventilation-perfusion ratios: theory. J Appl Physiol 1974; 36: 588-99. [ Links ]
13. Dantzker DR. Gas exchange in acute lung injury. Crit Care Clin 1986; 2: 527-36. [ Links ]
14 . Danzker DR. Gas exchange in the adult respiratory distress syndrome. Clin Chest Med 1982; 3: 57-67. [ Links ]
15. Dantzker DR, Wagner PD, West JB. Instability of lung units with low VA/Q ratios during O2 breathing. J Appl Physiol 1975; 38: 886-95. [ Links ]
16. Wagner PD, Laravuso RB, Uhl RB, et al. Continuous distri-butions of ventilation-perfusion ratios in normal subjects breathing air and 100 percent O2. J Clin Invest 1974; 54: 54-68. [ Links ]
17. Forster RE. Diffusion of gases. Handbook Physiol.,1(Sect 3):839,1964. [ Links ]
18. West JB. Ventilation-perfusion relationships. Am Rev Respir Dis 1977; 116: 919-43. [ Links ]
19. Cheney FW, Martin WE. Effect of continuous positive-pressure ventilation on gas exchange in acute pulmonary edema. J Appl Physiol 1971; 30: 378-81. [ Links ]
20. Cheney FW, Burnham SC. Effect of ventilatory pattern on oxygenation in pulmonary edema. J Appl Physiol 1971; 31: 909-12. [ Links ]
21. Staub NC. Pulmonary edema. Physiol Rev 1974; 54: 678-811. [ Links ]
22. Malo J, Ali J, Wood LDH. How does end-expiratory pressure reduce intrapulmonary shunt in canine pulmonary edema. J Appl Physiol 1984; 57: 1002-10. [ Links ]
23. Hedenstierna G, White FC, Mazzone R, et al. Redistribution of pulmonary blood flow in the dog with PEEP ventilation. J Appl Physiol 1979; 46: 278-87. [ Links ]
24. Miro AM, Pinsky MR. Heart-lung interactions. In: Martin J. Tobin (ed). Principle and practice of Mechanical Ventilation. McGraw-Hill, Inc. 1994, p 647-71 [ Links ]
25. Smith G, Cheney FW, Winter PM. The effect of change in cardiac output on intrapulmonary shunting, Br J Anesthes 1974; 46: 37-42. [ Links ]
26. Lemaire F, Gastine H, Regnier B, Teisseire B, Rapin M. Changes in intrapulmonary shunting with alterations in pulmonary vascular resistance. Anesthesiology 1977; 47: 315-6. [ Links ]
27. Lynch JP, Mhyre JG, Dantzker DR. Influence of cardiac output on intrapulmonary shunt. J Appl Physiol 1979; 46: 315-21. [ Links ]
28. Raimondi GA. Monitoreo hemodinámico en el trastorno respiratorio agudo del adulto. Medicina (Buenos Aires) 1987; 47: 416-30. [ Links ]
29. Lemaire F, Jardin F, Harari A et al. Assessment of gas exchange during venoarterial bypass using the membrane lung. In: Zapol WM and Quist J (eds). Artificial Lungs for Acute Respiratory Failure. New York: Academic Press, 1976 p 126-32 [ Links ]
30. Sandoval J, Long GR, Skoog C, Wood LD, Oppenheimer L. Indepent influence of blood flow rate and mixed venous PO2 on shunt fraction. J Appl Physiol 1983; 55: 1128-33. [ Links ]
31. Melot C. ventilation-perfusion relationships in acute respiratory failure. Thorax 1994; 49: 1251-8. [ Links ]
32. Lamm WJ, Graham MM, Albert RK. Mechanism by which the prone position improves oxygenation in acute lung injury. Am Rev Respir Crit Care Med 1994; 150: 184-93. [ Links ]
33. Mutoh T, Guest RJ, Lamm WJ, Albert RK. Prone position alters the effect of volume overload on regional pleural pressures and improves hypoxemia in pigs in vivo. Am Rev Respir Dis 1992; 146: 300-6. [ Links ]
34. Albert RK, Hubmayr RD. The prone position eliminates compression of the lungs by the heart. Am J Respir Crit Care Med 2000; 161:1 660-5. [ Links ]
35. Beck KC, Vettermann J, Rehder K. Gas exchange in dogs in the prone and supine positions. J Appl Physiol 1992; 72: 2292-7. [ Links ]
36. Mure M, Glenny RW, Domino KB, Hlastala MP. Pulmonary gas exchange improves in the prone position with abdominal distention. Am J Respir Crit Care Med 1998; 157: 1785-90. [ Links ]
37. Chatte G, Sab JM, Dubois JM, Sirodot M, Gaussorgues P, Robert D. Prone position in mechanically ventilated patients with severe acute respiratory failure. Am J Respir Crit Care Med 1997; 155: 473-8. [ Links ]
38. Pelosi P, Tubiolo D, Mascheroni D et al. Effects of prone position on respiratory mechanics and gas exchange during acute lung injury. Am J Respir Crit Care Med 1998; 157: 387-93. [ Links ]
39. Papazian L, Bregeon F, Gaillat F et al. Respective and combined effects of prone position and inhaled nitric oxide in patients with acute respiratory distress syndrome. Am J Respir Crit Care Med 1998; 157: 580-5. [ Links ]
40. Jolliet P, Bulpa P, Ritz M, Ricou B, Lopez J, Chevrolet JC. Additive beneficial effects of the prone position, nitric oxide, and almitrine bismesylate on gas exchange and oxygen transport in acute respiratory distress syndrome. Crit Care Med 1997; 25: 786-94. [ Links ]
41. Suter PM, Fairley HB, Schlobohm RM. Shunt, lung volume and perfusion during short periods of ventilation with oxygen. Anesthesiology 1975; 43: 617-27. [ Links ]
42. Rothen HV, Sporre B, Engberg B, Wegenius G, Reber A, Hendestierna G. Prevention of atelectasis during general anesthesia. Lancet 1995; 345: 1387-91. [ Links ]
43. Shapiro BA, Cane RD, Harrison RA, Steiner MC. Changes in intrapulmonary shunting with administration of 100 percent oxygen. Chest 1980; 77: 138-41. [ Links ]
44. Lampron N, Lemaire F, Teisseire B, et al. Mechanical ventilation with 100% oxygen does not increase intra-pulmonary shunt in patients with severe bacterial pneu-monia. Am Rev Respir Dis 1985; 131: 409-13. [ Links ]
45. Lemaire F, Matamis D, Lampron N, Teisseire B, Harf A. Intrapulmonary shunt is not increased by 100% oxygen ventilation in acute respiratory failure. Bull Eur Physio-pathol Respir 1985; 21: 251-6. [ Links ]
46. Santos C, Ferrer M, Roca J, Torres A, Hernández C, Rodriguez-Roisin R. Pulmonary gas exchange response to oxygen breathing in acute lung injury. Am J Respir Crit Care Med 2000; 161: 26-31. [ Links ]
47. Briscoe WA, Bergofsky E, King TKC. Catastrophic pulmonary failure. Am J Med 1976; 60: 248-58. [ Links ]
48. Raimondi GA, Raimondi AC. Changes in intrapulmonary shunting (communication to the Editor) Chest 1981; 80: 253-4. [ Links ]
49. Quan SF, Kronberg GM, Schlobohm RM, Feeley TW, Don HF, Lister G. Changes in venous admixture with alterations of inspired oxygen concentration. Anesthesiology 1980; 52: 477-82. [ Links ]
50. Raimondi GA, Raimondi AC. Mechanical ventilation and intrapulmonary shunt in pneumonia patients (Correspon-dence). Am Rev Respir Dis 1986; 134: 843-4. [ Links ]
51. Archie JP. Mathematic coupling of data. Ann Surg 1981; 193: 296-303. [ Links ]
52. Moreno LF, Stratton HH, Newell JC, Feustel PJ. Mathe-matical coupling of data: correction of a common error for linear calculations. J Appl Physiol 1986; 60: 335-43. [ Links ]
53. Stratton HH, Feustel PJ, Newell JC. Regression of calculated variables in the presence of shared measu-rement error. J Appl Physiol 1987; 62: 2083-93. [ Links ]
54 . Raimondi GA, Raimondi AC. Response to oxygen breathing in ALI/ARDS patients (Correspondence). Am J Respir Crit Care Med 2001; 163: 793-4. [ Links ]
55. Gea J, Roca J, Torres A, Agusti AGN, Wagner PD, Rodriguez-Roisin R. Mechanisms of gas exchange in patients with pneumonia. Anesthesiology 1991; 75: 782-9. [ Links ]
56. Gattinoni L, Pelosi L, Suter PM, Pedoto A, Vercesi P, Lissoni A. Acute respiratory distress syndrome caused by pulmonary and extrapulmonary disease. Different syn-dromes? Am J Respir Crit Care Med 1998; 158: 3-11. [ Links ]
57. Rossaint R, Falke KJ, López F, Slama K, Pison U, Zapol WM. Inhaled nitric oxide (NO) in ARDS patients. N Engl J Med 1993; 328: 399-405. [ Links ]
58. Troncy E, Collet JP, Shapiro S, et al. Inhaled nitric oxide in acute respiratory distress syndrome. A pilot randomized controlled study. Am J Respir Crit Care Med 1998; 157: 1483-8. [ Links ]
59. Puybasset L, Rouby JJ, Mourgeon E, et al. Factors influencing cardiopulmonary effects of inhaled nitric oxide in acute respiratory failure. Am J Respir Crit Care Med 1995; 152: 318-28. [ Links ]
60. Michael JR, Barton RG, Saffle JR, et al. Inhaled nitric oxide versus conventional therapy: effect on oxygenation in ARDS. Am J Respir Crit Care Med 1998; 157: 1372-80. [ Links ]
61. Rossaint R, Gerlach H, Schmidt-Ruhnke H, et al. Efficacy of inhaled nitric oxide in patients with severe ARDS. Chest 1995; 107: 1107-15. [ Links ]
62. Payen DM. Is nitric oxide inhalation a «cosmetic» therapy in acute respiratory distress syndrome? Am J Respir Crit Care 1998; 157: 1361-2. [ Links ]
63. Gottschall EB, Fernyak S, Wuertemberg G, Voelkel NF. Almitrine mimics hypoxic vasoconstriction in isolated rat lungs. Am J Physiol 1992; 263: 383-91.
64. Prost JF, Desché P, Jardin F, Margairaz A. Comparison of the effects of intravenous almitrine and positive end-expiratory pressure on gas exchange in adult respiratory distress syndrome. Eur Respir J 1991; 4: 683-7. [ Links ]
65. Gallart L, Lu Q, Puybasset L, Umamaheswara Rao GS, Coriat P, Rouby JJ. Intravenous almirtine combined with inhaled nitric oxide for acute respiratory distress syndrome. The NO Almitrine Study Group. Am J Respir Crit Care Med 1998; 158: 1770-7. [ Links ]
66. Papazian L, Roch A, Bregeon F, et al. Inhaled nitric oxide and vasoconstrictors in acute respiratory distress syndrome. Am J Respir Crit Care Med 1999; 160: 473-9. [ Links ]
67. Benzing A, Mols G, Brieschal T, Geiger K. Hypoxic pulmonary vasoconstriction in nonventilated lung areas contributes to differences in hemodynamic and gas exchange response to inhalation of nitric oxide. Anesthe-siology 1997; 86: 1254-61. [ Links ]
68. Wysocki M, Delclaux C, Roupie E, et al. Additive effect on gas exchange of inhaled nitric oxide and intravenous almitrine bismesylate in the adult respiratory distress syndrome. Intensive Care Med 1994; 20: 254-9. [ Links ]
69. Radermacher P, Santak B, Wust HJ, Tarnow J, Falke KJ. Prostacyclin for the treatment of pulmonary hypertension in the adult respiratory distress syndrome: effects on pulmonary capillary pressure and ventilation-perfusion distributions. Anesthesiology 1990; 72: 238-44. [ Links ]
70. Mélot C, Lejeune P, Leeman M, Moraine JJ, Naeje R. Prostaglandin E1 in the adult respiratory distress syndrome. Am Rev Respir Dis 1989; 139: 106-10. [ Links ]
71. Zwissler B, Kemming G, Habler O, et al. Inhaled pros-tacyclin PGI2 versus inhaled nitric oxide in adult respi-ratory distress syndrome. Am J Respir Crit Care Med 1996; 154: 1671-7. [ Links ]
72. Putensen C, Horman C, Kleinsasser A, Putensen-Himmer G. Cardiopulmonary effects of aerosolized prostaglandin E1 and nitric oxide inhalation in patients with acute respi-ratory distress syndrome. Am J Respir Crit Care Med 1998; 157: 1743-7. [ Links ]
73. Walmarth D, Schneider T, Schermuly R, Olschewski H, Grimminger F, Seeger W. Direct comparison of inhaled nitric oxide and aerosolized prostacyclin in acute respiratory distress syndrome. Am J Respir Crit Care Med 1996; 153: 991-6. [ Links ]
Recibido: 11 de enero de 2002
Aceptado: 1 de noviembre de 2002














