Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680versión On-line ISSN 1669-9106
Medicina (B. Aires) v.66 n.1 Buenos Aires ene./feb. 2006
Tratamiento con eritropoyetina humana recombinante
Hugo Donato1, Hugo Ferro2
1Departamento de Neonatología, Sanatorio de la Trinidad; 2Clínica y Maternidad Suizo Argentina, Buenos Aires
Dirección postal: Dr Hugo Donato. Ocampo 3308, 1754 San Justo, Buenos Aires, Argentina. Fax: (54-11) 4924 3601. E-mail: hugodonato@aol.com
Resumen
La eritropoyetina recombinante (rHuEPO) se ha transformado en la citoquina más utilizada terapéuticamente en el mundo. Luego del éxito obtenido en pacientes con insuficiencia renal terminal, se pudo establecer la utilidad de la terapia con rHuEPO para mejorar otras anemias, incluso en pacientes pediátricos y neonatos. El tratamiento o la prevención de la anemia del prematuro mediante el uso de rHuEPO llevó a una significativa reducción en cantidad de transfusiones y en exposición a dadores. Aún debe establecerse una clara definición sobre cuáles niños prematuros deben recibir tratamiento rutinariamente. Otras indicaciones en período neonatal incluyen anemias hiporregenerativas y hemolíticas. La eficacia de la rHuEPO en niños mayores, con excepción de la insuficiencia renal crónica, no ha sido tan exhaustivamente evaluada como en adultos. Mientras que durante los últimos años se han realizado gran cantidad de estudios en adultos con anemia asociada al cáncer o a infección por HIV, permitiendo establecer conclusiones claras sobre su eficacia, sólo escasa cantidad de estudios con pequeño número de pacientes han sido realizados en niños. Hasta la fecha, los resultados sugieren que la terapia con rHuEPO en niños es tan útil como en adultos, pero la realización de estudios aleatorizados prospectivos incluyendo gran número de pacientes es esencial para alcanzar conclusiones definitivas. Los resultados de estudios dirigidos a evaluar la eficacia de la rHuEpo para mantener una dosis adecuada de ribavirina en pacientes en tratamiento por hepatitis C son alentadores. La utilización potencial de los efectos no hemopoyéticos de la rHuEPO en neonatos es un terreno novedoso y apasionante. El rol de la Epo como citoprotector para sistema nervioso central y mucosa intestinal está bajo investigación exhaustiva.
Palabras clave: eritropoyetina, anemia del prematuro, neuroprotección, cáncer, infección por HIV, insuficiencia renal, síndrome urémico hemolítico
Abstract
Human recombinant erythropoietin therapy. Recombinant human erythropoietin (rHuEpo) has become the most widely used cytokine in the world. Following the success of its use in patients with end-stage renal disease, the usefulness of rHuEpo to ameliorate other anemias was assessed, including pediatric patients and newborn infants. The treatment or prevention of anemia of prematurity with rHuEpo resulted in a significant reduction in the number of transfusions and donor exposure. A clear definition of which premature babies must receive therapy needs yet to be established. Other indications in neonatal period include hyporegenerative and hemolytic anemias. With the exception of chronic renal failure, in older children the efficacy of rHuEpo has not been evaluated as in adults. While an impressive amount of studies were carried out during the last years in adult patients with cancer-related or HIV-infection-related anemias, allowing to establish clear conclusions on its efficacy, only a few trials with small number of patients have been reported in children. Up to date, results in pediatric patients suggest that rHuEpo therapy is as useful as in adult patients, but prospective, randomized trials including large number of patients are essential to achieve definitive conclusions. Results of studies designed to evaluate the efficacy of rHuEpo for sustaining an adequate dose of ribavirin in patients receiving treatment for hepatitis C are encouraging. The potential for use of the non-hematopoietic effects of rHuEpo in newborn infants is a novel and exciting issue. The role of rHuEpo as a tissue protective factor for central nervous system and intestinal mucosa is under exhaustive investigation.
Key words: erythropoietin, anemia of prematurity, neuroprotection, cancer, HIV infection, renal failure, hemolytic uremic syndrome
La eritropoyetina (Epo), glicoproteína de 30,4 kd compuesta por 165 aminoácidos, es el regulador primario de la eritropoyesis. Actúa inhibiendo la apoptosis de los progenitores eritroides e induciendo su proliferación clonal a normoblastos1, 2. Es responsable de la producción eritrocitaria en el feto, el recién nacido (RN), el niño y el adulto, pero no en el embrión (los eritroblastos primitivos no son Epo-dependientes)3.
Su ritmo de síntesis está regulado por la hipoxia a través de un mecanismo de retroalimentación. Al ocurrir hipoxia tisular, las células intersticiales peritubulares del riñón reciben la información y aumentan la producción de Epo1. Entre varios reguladores positivos y negativos, este mecanismo es mediado por el factor inducible por hipoxia 1a (HIF-1a), una proteína regulada por el gen von Hippel-Lindau (un gen supresor tumoral), que se une a la región facilitadora inducible por hipoxia del gen de Epo1, 2, 4. En ausencia de O2, el HIF-1a activa la trascripción de varios genes, entre ellos el de la Epo5.
En el adulto se sintetiza primariamente en el riñón, que produce 90-95% de la Epo total circulante, mientras que la restante es sintetizada por hígado. Durante la gestación la relación entre las fuentes renal y hepática de Epo está invertida6. La eritropoyesis fetal es independiente de la materna6, 7. Considerando que la molécula de Epo no atraviesa la placenta7, sus niveles sanguíneos en el feto reflejan exclusivamente la producción de Epo endógena. El sitio donde más precozmente se detecta la presencia de Epo es en líquido amniótico durante la embriogénesis8. Posteriormente, durante el desarrollo fetal, el hígado es el sitio principal de producción9. Hasta la semana 30 de gestación el riñón produce menos del 9% del total. El cambio del sitio de producción primaria de hepática a renal comienza en el tercer trimestre. Al comienzo del 7° mes, aproximadamente 27% de la Epo es de origen renal10. Varias semanas después del nacimiento, en un momento aún no exactamente determinado, el cambio está completado11. El mecanismo regulador del mismo no está totalmente aclarado, pero parece estar ontogénicamente determinado. En consecuencia, la edad a la cual se completa la transferencia del hígado fetal al riñón es independiente de la edad gestacional al nacimiento.
En 1977 Miyake y col. purificaron la molécula de Epo12, haciendo posible la clonación del gen y el posterior desarrollo de la Epo recombinante13. Luego Eschbach y col. publicaron el primer ensayo clínico, demostrando corrección de la anemia de la insuficiencia renal terminal (IRT) mediante la utilización de Epo humana recombinante (rHuEPO)14. Desde entonces, su uso se ha transformado en una importante ayuda terapéutica para muchos otros tipos de anemia. El desarrollo durante la última década de agentes estimulantes de la eritropoyesis con mayor grado de glicosilación y vida media prolongada ha facilitado su aplicación con menor frecuencia de dosis. Además, la potencial utilización terapéutica de sus efectos no hematopoyéticos se encuentra actualmente bajo investigación exhaustiva.
Esta revisión se focaliza sobre avances, controversias y perspectivas existentes con relación a los usos terapéuticos de la rHuEPO en pacientes pediátricos y adultos.
Indicaciones terapéuticas
Anemia secundaria a enfermedades renales
En pacientes bajo diálisis continua, tanto adultos como pediátricos, el tratamiento con rHuEPO logró eliminar casi totalmente la dependencia transfusional, permitiendo alcanzar una mejoría significativa en la calidad de vida15-17. El rango de hemoglobina que se recomienda alcanzar es 11-12 g/dl. Para ello, generalmente es suficiente con administrar dosis iniciales de 50-150 unidades/kg, y posteriormente de mantenimiento con alrededor de 40 unidades/kg18-20. Los niños habitualmente requieren dosis más elevadas que los adultos para alcanzar una respuesta hemoglobínica similar16, 17, 20. Las dosis requeridas disminuyen a medida que la edad y el peso corporal aumentan; los niños más pequeños necesitan dosis por kg de peso corporal más elevadas que los niños mayores o adolescentes16, 17, 20. No existe todavía explicación para esta observación. Considerando que los receptores de Epo (Epo-R) se expresan en una amplia variedad de células, se ha especulado que el ritmo de depuración podría estar aumentado en los niños más pequeños debido a la existencia de sitios de unión y eliminación de la Epo que se inactivarían en etapas posteriores de la vida21. En adultos existe la posibilidad de utilizar dosis reducidas de rHuEPO asociada a andrógenos, que potencian el efecto de la misma22.
Aún existe debate sobre el momento óptimo para iniciar la terapia con rHuEpo y el nivel de hemoglobina que debe alcanzarse. Existen evidencias de que una corrección precoz de la anemia en etapa predialítica podría prolongar el tiempo requerido para llegar al fallo renal terminal23, pero esta observación debe aún ser corroborada mediante estudios controlados24. Existen diversas opiniones relativas al nivel de hemoglobina deseable y su efecto sobre el pronóstico cardiovascular. En el estudio cooperativo en EE.UU. se observó mayor mortalidad en los pacientes que habían sido llevados a corrección total de la hemoglobina25 en el estudio canadiense se beneficiaron sólo los pacientes que no tenían dilatación del ventrículo izquierdo26, y en el australiano se observó mejoría de la performance cardiovascular en aquellos pacientes aleatorizados para alcanzar niveles de hemoglobina normales27. En este estudio se debió incrementar la dosis en 80% para alcanzar niveles de hemoglobina dentro de valores fisiológicos.
En los últimos años se ha planteado la administración de rHuEPO en dosis única semanal, en forma similar a la utilizada con los nuevos estimulantes de la eritropoyesis de vida media prolongada28. Este esquema ha sido utilizado en pacientes en hemodiálisis cronica29, en diálisis peritoneal30 y en etapa predialítica31. Las respuestas fueron similares a las obtenidas con la administración convencional, siendo alcanzadas con ligeros incrementos en la dosis total semanal de rHuEPO29. Sin embargo, otros autores comunicaron que al convertir a los pacientes del esquema habitual a la administración semanal se observaba una caída en los niveles de hemoglobina32. Por ahora, sólo podría recomendarse esta forma de administración en pacientes que responden bien a dosis no elevadas de rHuEPO y que están clínicamente estables28.
Algunos pacientes no responden al tratamiento o desarrollan resistencia al mismo luego de una buena respuesta inicial. Esta refractariedad a la rHuEPO, clásicamente definida por la necesidad de emplear más de 20.000 unidades semanales para mantener una hemoglobina estable, puede ser causada por diferentes mecanismos (Fig. 1), siendo los más comunes la deficiencia de hierro y el hiperparatiroidismo grave (HPS)17. El HPS afecta a la eritropoyesis produciendo inhibición directa de los progenitores eritroides y fibrosis de médula ósea. La deficiencia de hierro, observable en 43-90% de pacientes en hemodiálisis, puede ser resultado de extracciones excesivas, pérdida de sangre por el acceso, hemorragia digestiva o administración inadecuada del tratamiento. Considerando que el mal cumplimiento de la terapia con hierro oral era una de las causas más frecuentes de esta deficiencia, en los últimos años se ha generalizado en adultos el uso de hierro endovenoso, siendo actualmente una interesante alternativa para considerar en pacientes pediátricos33. Un reciente meta-análisis llegó a la conclusión que todavía no se puede establecer con certeza el mejor régimen de administracion34.
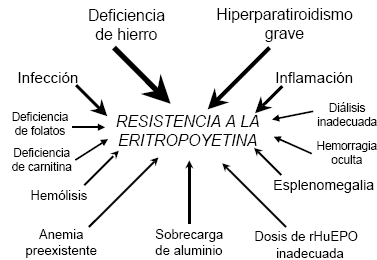
Fig. 1.- Mecanismos de resistencia al tratamiento con rHuEPO.
Los pacientes en diálisis peritoneal continua también se benefician del tratamiento con rHuEPO. En ellos la vía subcutánea demostró ser la más efectiva, pues requieren menos Epo que los pacientes en hemodiálisis para alcanzar la misma respuesta35-36. La administración intraperitoneal parece ser tan efectiva como la subcutánea35.
La anemia tardía post-transplante (ATPT) renal es frecuente, ocurriendo en 12-23% de pacientes adultos y con mayor frecuencia en niños37, 38. En el mayor estudio publicado, Yorgin y col. comunicaron que prácticamente todos presentaron anemia dentro del primer año post-transplante; entre los 6 y 60 meses después del transplante, 60-80% de los niños permanecían aún anémicos38. Los factores involucrados en su patogénesis son múltiples: producción disminuida de Epo, deficiencia de hierro, función renal alterada, acción de drogas inmunosupresoras, edad al transplante, niveles de calcio sérico38, 39. La secreción inadecuada de Epo, secundaria a anemia de las enfermedades crónicas y/o al efecto de drogas inmunosupresoras, juega un importante rol patogénico38,39. Considerando que se han detectado niveles disminuidos de Epo en suero en 81.6% de niños con ATPT38, el tratamiento con rHuEPO parece estar indicado. Los resultados comunicados por algunos autores, demostrando corrección de la anemia mediante el uso de la rHuEPO, han llevado a que esté siendo utilizada cada vez con mayor frecuencia38,39.
La insuficiencia renal aguda (IRA) es una causa potencial de anemia. Se han comunicado, en adultos con IRA, niveles inadecuadamente bajos de Epo, similares a los observados en la IRT40, 41. El síndrome urémico hemolítico (SUH) es en nuestro país la causa más común de IRA en niños. Hemos comunicado niveles inadecuadamente bajos de Epo en niños con SUH e IRA42. Al comienzo, esta deficiencia osciló entre leve a grave; después de la primera transfusión, y con persistencia de insuficiencia renal, los niveles de Epo invariablemente alcanzaron niveles muy bajos; durante la fase de recuperación los niveles aumentaron lentamente. Si bien en estos pacientes el descenso inicial de hemoglobina está indudablemente relacionado a la intensidad de la hemólisis, hemos sugerido que la ausencia de una respuesta eritropoyética adecuada podría contribuir a que se alcancen niveles más bajos que los esperables de acuerdo al grado de hemólisis. La secreción inadecuada de Epo, secundaria tanto al fallo renal como al efecto inhibitorio de las transfusiones sobre la eritropoyesis, probablemente contribuya a la persistencia de niveles bajos de hemoglobina. Las comunicaciones sobre mejoría de la anemia con el uso de rHuEPO en adultos con SUH inducido por quimioterapia43-45 dan apoyo adicional a esta hipótesis. En consecuencia, el uso terapéutico de la rHuEPO con el objetivo de disminuir el requerimiento transfusional en niños con SUH deberá ser cuidadosamente evaluado.
La anemia es frecuente en pacientes con síndrome nefrótico (SN) y función renal normal46, desarrollándose habitualmente en pacientes con SN resistente a la terapia inmunosupresora que aún mantienen filtración glomerular normal47. Considerando que estos pacientes presentan pérdidas urinarias aumentadas y niveles séricos disminuidos de albúmina y otras proteínas48-50, se ha postulado que la eliminación excesiva de transferrina y Epo por orina podría ser un factor causante de anemia. Se ha comunicado excreción urinaria significativa de Epo en adultos50 y respuesta inadecuada de Epo en niños con SN47. Estudios en animales demostraron la existencia de pérdidas urinarias masivas, baja concentración sérica, volumen de distribución aumentado, ritmo de depuración plasmática aumentado, sobrevida acortada y producción disminuida de Epo51. La alteración en su síntesis podría ser causada por daño de las células intersticiales peritubulares51. La buena respuesta obtenida en algunos pacientes adultos y pediátricos tratados con rHuEPO47, 52-54 sugiere que la deficiencia de Epo (secundaria a pérdida urinaria, producción disminuida, o ambas) podría ser importante tanto para el desarrollo inicial de la anemia como para su persistencia en caso que ésta hubiera sido desencadenada por otro factor47. Estos resultados justifican algunos trabajos en marcha dirigidos a evaluar la eficacia de la terapia con rHuEPO en niños con SN.
Anemia del prematuro
Aunque el uso de la rHuEPO en RN con anemia del prematuro (AP) ha sido motivo de estudios y opiniones exhaustivos durante los últimos 15 años, aún persisten controversias sobre algunos aspectos6.
La AP es causada por múltiples mecanismos (Fig. 2), siendo los principales una inadecuada respuesta de Epo y la excesiva cantidad de sangre extraída para estudios55. Otros factores involucrados, en mucho menor grado, son la sobrevida eritrocitaria acortada en el prematuro de muy bajo peso de nacimiento (MBPN) comparado con el RN de término (RNT), y la hemólisis secundaria a las enfermedades graves que usualmente presentan estos pacientes (sepsis, hipoxia, acidosis).

Fig. 2.- Mecanismos causantes de la anemia del prematuro. La inhibición de la síntesis de Epo lleva a disminución de la eritropoyesis y, por lo tanto, a una disminución en la concentración de hemoglobina. Además, la combinación de esta producción disminuida de glóbulos rojos con una elevada velocidad de crecimiento corporal da como resultado una dilución de la masa eritrocitaria que contribuye a la anemia. Las extracciones de sangre frecuentes son la otra causa principal que produce anemia del prematuro. A su vez, el efecto inhibitorio de las transfusiones sobre la síntesis de Epo empeora aún más la supresión de la eritropoyesis. Otro de los factores involucrados es la destrucción eritrocitaria secundaria a envejecimiento o a hemólisis.
En el momento del nacimiento, el niño presenta una elevada concentración de hemoglobina, como resultado de la hipoxia relativa a que está sometido en vida intrauterina. Al nacer, la tensión de O2 respirada aumenta bruscamente y, como consecuencia, el estímulo para la producción de Epo se inhibe en forma casi completa; al 2° día de vida extrauterina la síntesis de hemoglobina disminuye a la mitad, y al 10° día a menos del 10%, de la producción intrauterina56. Esta supresión casi completa de la eritropoyesis se mantiene durante varias semanas, mientras los hematíes fetales envejecen y van siendo destruidos. Esta combinación de inhibición de eritropoyesis más destrucción eritrocitaria lleva a una disminución gradual y sostenida de la concentración de hemoglobina, que alcanza valores considerablemente inferiores a los que son normales para niños mayores. En el pretérmino esta caída es más severa y ocurre más precozmente que en el RNT57. En el niño de término, cuando la baja concentración de hemoglobina lleva a hipoxia tisular, se estimula la producción de Epo y se reinicia la eritropoyesis. En los prematuros MBPN, por el contrario, se desarrollan síntomas de hipoxia tisular sin que se reinicie una producción adecuada de Epo58. Los RNT y los pretérmino nacen con niveles similares de Epo circulante59. Durante las primeras semanas post-nacimiento los niveles en los pretérminos MBPN permanecen estables mientras los niveles de hemoglobina van disminuyendo, alcanzando así valores 10-100 veces menores que los esperados para el grado de anemia58,60. En nuestro grupo de prematuros MBPN el hematocrito descendió casi 20 puntos desde el nacimiento hasta la 4a semana de vida, mientras los niveles de Epo sérica permanecían estables durante el mismo período (Tabla 1) (Vivas N, González E, Marangunich L y col. IV Congreso Argentino de Perinatologia, 1992). Esta falta de correlación entre niveles de Epo y de hemoglobina es más marcada cuanto más inmaduro es el pretérmino60. Se ha demostrado en animales que un estímulo hipóxico de similar intensidad lleva a la producción en hígado de una cantidad de Epo que es sólo 10% de la producida por el riñón. Además, el período requerido para estimular su síntesis es significativamente más prolongado para la producción hepática61. Considerando que las proporciones relativas de producción hepática y renal dependen fundamentalmente de la edad gestacional, siendo considerablemente mayor la proporción de Epo hepática en prematuros que en niños de término, esta diferente respuesta a la hipoxia entre los sensores hepático y renal probablemente sea responsable de la respuesta alterada de Epo en los prematuros comparada con los RNT con similar grado de anemia. Además, las transfusiones recibidas llevan a una inhibición aún mayor de la eritropoyesis, a través de un mecanismo todavía no aclarado62.
TABLA 1.- Valores de hematocrito y niveles de eritropoyetina sérica durante el primer mes de vida en pretérminos MBPN

Esta respuesta inadecuada de Epo se vuelve el principal mecanismo involucrado en la AP a partir de la tercera semana de vida; previamente, la causa principal es la cantidad de sangre extraída. Hace unos años, era habitual extraer 20-30 ml/kg durante las primeras semanas; en muchos pacientes el volumen total extraído durante la primera semana igualaba o superaba a su volemia63. En los últimos años se han reevaluado las prácticas de extracción, llevando a una reducción sustancial de los volúmenes extraidos64-66, aunque continúan siendo elevados. Lin y col. demostraron que en los neonatos se extrae casi un 20% más de sangre que la necesaria para los estudios solicitados67, infiriendo que este exceso sería responsable de 5-15% de las transfusiones recibidas por los niños MBPN. Como consecuencia de estos elevados volúmenes de extracción, los prematuros MBPN tienen altos requerimientos transfusionales; casi todos ellos necesitan al menos una transfusión durante las primeras dos semanas de vida, y más del 80% requieren transfusiones posteriormente68.
A fines de los 80 se demostró que los progenitores eritroides de los prematuros MBPN respondían adecuadamente a la estimulación con rHuEPO69. En 1990 Halperin y col. comunicaron un estudio piloto mostrando que la administración de rHuEPO a pretérminos MBPN estimulaba la eritropoyesis70. Posteriormente se conocieron varios estudios en los que se administraba rHuEPO a dosis similares a las utilizadas en pacientes con IRT, observándose una franca respuesta reticulocitaria pero sin poder demostrar una reducción del requerimiento transfusional71-73. Frente a evidencia experimental demostrando que la Epo en neonatos tiene mayor velocidad de depuración plasmática, sobrevida acortada, mayor ritmo de producción y mayor volumen de distribución que en el adulto74, 75, se sugirió que podría ser necesaria la utilización de dosis mayores de rHuEPO en neonatos para alcanzar una respuesta eritropoyética adecuada. Los resultados de algunos ensayos clínicos dieron apoyo a esta hipótesis76, 77. En nuestro estudio, con dosis de 150 y de 300 unidades/kg/semana no pudimos alcanzar una respuesta reticulocitaria diferente al grupo tratado con placebo, pero con 750 unidades/kg/semana obtuvimos un rápido y significativo ascenso del recuento reticulocitario, alcanzando valores tres veces mayores que los iniciales al 7o día de tratamiento, y permaneciendo elevados durante todo el tratamiento77 (Fig. 3).

Fig. 3.- Respuesta reticulocitaria a la administración de placebo y de tres diferentes dosis de rHuEPO. La dosis de 750 unidades/kg/semana indujo un rápido aumento del recuento reticulocitario, el cual alcanzó valores tres veces superiores al inicial al 7° día de tratamiento, y permaneció elevado durante las 8 semanas de terapia (p < 0.001 en comparación con los grupos que recibían rHuEPO a 300 unidades/kg/semana, rHuEPO a 150 unidades/kg/semana y placebo). IPR: índice de producción reticulocitaria.
Se publican entonces otros estudios, administrando rHuEPO a 500-900 unidades/kg/semana y hierro >3 mg/kg/día (Tabla 2), comenzando el tratamiento entre 2a-4a semanas de vida en la mayoria76-81. La conclusión fue que este régimen inducía una estimulación significativa de la eritropoyesis y disminuía significativamente el requerimiento transfusional. Administrar la rHuEPO a partir de la 2a-3a semana de vida, durante 6 a 8 semanas, parecía ser el esquema terapéutico más efectivo. Un metaanálisis sobre ensayos clínicos controlados publicados desde 1990 a 1999 concluyó que la administración de rHuEPO tenía un efecto modesto aunque estadísticamente significativo (p<0.001) sobre los volúmenes transfundidos82.
TABLA 2.- Estudios clínicos de administración de eritropoyetina recombinante (rHuEPO) en los cuales el tratamiento comenzaba después de la primera semana de vida
Posteriormente fue evaluada la eficacia de la administración precoz de rHuEPO (desde las primeras 48 horas de vida). En dos pequeños estudios, Ohls y col. relataron que la administración desde el día 1 al 14 en pretérminos con PN <1500 g disminuía el requerimiento transfusional83, 84. El grupo cooperativo argentino comparó la utilidad del uso precoz de rHuEPO (desde las 48-72 horas de vida) contra placebo en 114 prematuros con PN <1250 g, no observando diferencia entre ambos grupos ni en número de transfusiones/paciente ni en volumen transfundido; sin embargo, en los niños más pequeños y más gravemente enfermos, el uso precoz fue eficaz para disminuir significativamente el requerimiento transfusional64. Yeo y col. comunicaron resultados similares sobre 100 prematuros65. El estudio multicéntrico norteamericano sobre 290 neonatos MBPN aleatorizados para recibir rHuEPO o placebo desde el 4o día no mostró diferencia entre grupos85. El estudio cooperativo europeo sobre 219 pretérminos de PN <1000 g demostró que el uso precoz (entre 3- 5 días de vida) fue efectivo para disminuir el requerimiento transfusional66. En conclusión, la mayoría de los estudios (Tabla 3) confirmaron que el uso precoz de rHuEPO en los prematuros más pequeños y más gravemente enfermos es útil para disminuir el requerimiento transfusional. Un metaanálisis reciente sobre 12 ensayos clínicos concluyó que la administración precoz redujo moderadamente el número de transfusiones, especialmente las recibidas tardíamente86.
TABLA 3.- Estudios clínicos de administración de rHuEPO en los cuales el tratamiento comenzaba después de la primera semana de vida
Simultáneamente con el uso de la rHuEPO se establecieron criterios transfusionales más estrictos80, se limitó la cantidad de sangre extraída para estudios64, 66, 80, 87 y se implementaron nuevas estrategias transfusionales (donante dirigido, autotransfusión con sangre placentaria)72, 88-91, permitiendo disminuir en pocos años de aproximadamente 10 a 2-5 transfusiones/paciente92. Quedan aún por definir factores de riesgo transfusional que permitan definir cuáles niños deben recibir tratamiento con rHuEPO6.
El tratamiento con rHuEPO en pretérminos MBPN debe suplementarse con hierro (e>6 mg/kg/día)70, 71, 79 y ácido fólico (1-2 mg/día)78, 93 para poder sostener una respuesta eritropoyética marcadamente incrementada. No hay evidencia que justifique la administración de vitamina E, que además puede producir efectos adversos graves94, 95.
Anemias hiporregenerativas del recién nacido (RN)
El uso de las transfusiones intrauterinas (TIUs) ha mejorado pronóstico y tratamiento de la enfermedad hemolítica del RN por incompatibilidad Rh (EHRh). Actúan aumentando los niveles de hemoglobina fetal circulante, para evitar el desarrollo de hipoxia e hydrops, e inhibiendo la eritropoyesis y consecuentemente el grado de hemólisis. Como consecuencia de las TIUs, entre 2a y 6a semanas de vida se desarrolla una "anemia hiporregenerativa tardía", caracterizada por reticulocitopenia y niveles inadecuadamente bajos de Epo96, 97. Como en estos casos la reactivación espontánea de la eritropoyesis ocurre recién entre los 2-4 meses de edad96, se suelen necesitar transfusiones durante este período. Algunos estudios no controlados con escaso número de pacientes comunicaron que la rHuEPO inducía aumento significativo del recuento reticulocitario en todos, permitiendo alcanzar un aumento gradual y sostenido de los niveles de hemoglobina circulante98-100 (Fig. 4) (Donato H, Vain N, Rendo P y col. XII Congreso Argentino de Hematología, 1995). Ninguno de los niños estudiados fue transfundido luego de comenzado el tratamiento con rHuEPO. En el único estudio controlado, sobre 20 neonatos distribuidos aleatoriamente para recibir rHuEPO o placebo, el grupo tratado con rHuEPO recibió significativamente menos transfusiones que el tratado con placebo (1.8 vs. 4.2 transfusiones/paciente, respectivamente)101. Estos investigadores continuaron con el mismo esquema terapéutico en los 103 casos subsiguientes, logrando que la mayoría (55%) no recibiera ninguna transfusión102. También se ha comunicado el tratamiento exitoso con rHuEPO en niños que habían recibido exsanguíneo transfusiones intrauterinas103.

Figura 4. Cambios ocurridos en hematocrito y recuento reticulocitario luego de la administración de rHuEPO en cuatro neonatos con enfermedad hemolítica por Rh que habían recibido previamente transfusiones intrauterinas. Los cuatro niños comenzaron tratamiento con rHuEPO cuando su hematocrito era indicativo de transfusión, alcanzando un rápido y sostenido aumento del mismo.
Los anticuerpos anti-Kell pueden inhibir el crecimiento de los progenitores eritroides, llevando a supresión de la eritropoyesis104. En un niño con anemia grave secundaria a alloinmunización anti-Kell, con niveles inadecuadamente bajos de reticulocitos y Epo sérica, se pudo evitar la transfusión mediante el tratamiento con rHuEPO105.
Muchos niños con EHRh que no han recibido TIUs, o con enfermedad hemolítica grave por incompatibilidad ABO, pueden presentar niveles muy bajos de hemoglobina sin desarrollar una respuesta eritropoyética adecuada (reticulocitopenia y bajos niveles séricos de Epo). Con el objetivo de evitar transfundir a estos pacientes, habitualmente administramos tratamiento con rHuEPO. Hasta la fecha, solo 1 de 20 niños tratados tuvo necesidad de ser transfundido luego de comenzado el tratamiento (datos no publicados).
El tratamiento con rHuEPO ha demostrado ser útil para mejorar la anemia en pacientes infectados por el virus de inmunodeficiencia humana (HIV)106,107. Por otra parte, está claramente establecida la eficacia del tratamiento con zidovudine (AZT) al RN para prevenir la transmisión del HIV desde la madre al niño. Esta terapia lleva a una reducción significativa de la concentración de hemoglobina en los neonatos durante el tratamiento108. Teniendo en cuenta los resultados alcanzados en niños mayores106, decidimos administrar rHuEPO a algunos neonatos que estaban recibiendo tratamiento profiláctico con AZT, comenzando el mismo cuando los valores de hematocrito eran indicativos de transfusión, logrando evitar la transfusión en todos los casos (datos no publicados). La realización de estudios controlados prospectivos en neonatos tratados con AZT y/o otros antirretrovirales establecerán la real utilidad de esta terapia.
La dosis óptima a administrar a neonatos con anemias hiporregenerativas es de 200-250 unidades/kg/dosis, tres veces por semana98-103,105.
Anemias hemolíticas
Todos los neonatos presentan algún grado de respuesta eritropoyética alterada a la hipoxia. Los niveles de Epo sérica en neonatos y lactantes menores de 6 meses están disminuidos en comparación con niños mayores o adultos, a cualquier valor de hemoglobina60. Esta respuesta inadecuada ha sido descripta en pacientes con anemias hemolíticas congénitas, como la esferocitosis hereditaria (ESH)109, y podría explicar el hecho de que muchos niños con ESH requieran múltiples transfusiones durante las primeras semanas de vida, pero posteriormente disminuyan marcadamente sus requerimientos transfusionales110. Tchernia y col. investigaron la eficacia de la rHuEPO para compensar el ritmo de hemólisis, en 16 niños menores de 4 meses con ESH de elevado requerimiento transfusional111. Luego de comenzado el tratamiento, 10 pacientes no recibieron más transfusiones, otros 3 fueron transfundidos sólo una vez, y los 3 restantes fueron no respondedores. El tratamiento con rHuEPO en neonatos parece ser efectivo, pero su utilidad debe ser confirmada por estudios futuros. También se ha comunicado el caso de un neonato con EHRh diagnosticada al nacimiento, con marcada hiperbilirrubinemia y anemia hemolítica grave; debido a la negativa paterna al uso de transfusiones (testigos de Jehová), fue tratado con rHuEPO a partir del 4º día, alcanzando un aumento gradual y sostenido de la hemoglobina y un lento descenso de los valores de bilirrubinemia112.
Estos resultados parecen justificar la realización de futuras investigaciones sobre su uso potencial para el tratamiento de otras anemias hemolíticas graves en período neonatal.
Anemia asociada al cáncer
La anemia asociada al cáncer (AAC) es un hallazgo frecuente, que ocurre en 30-90% de pacientes adultos113 y en más del 80% de pediátricos114. Sobre 15.367 pacientes de 24 países europeos, se encontró anemia en 72% con neoplasias hematológicas y en 66% con tumores sólidos114b. Su etiología es compleja e involucra mielosupresión secundaria al tratamiento, hemorragias, invasión tumoral de médula ósea, hemólisis, deficiencias de hierro o folato, anemia de las enfermedades crónicas y niveles inadecuadamente bajos de Epo115.
La anemia tiene impacto negativo en la calidad de vida y es un factor pronóstico negativo para progresión y sobrevida116, 117. La introducción del tratamiento con rHuEPO ha representado un avance importante en el manejo de estos pacientes. Numerosos estudios con más de 10.000 pacientes incluidos han confirmado su eficacia115, 118-122. También se ha evaluado la posibilidad de extender su uso a pacientes anémicos tratados con quimiorradioterapia, a pacientes anémicos que no estén recibiendo quimioterapia y a pacientes no anémicos (para prevenir la aparición de anemia)124-126.
Los lineamientos generales de la terapia con rHuEPO han sido exhaustivamente analizados127-129. Sus objetivos principales son aumentar el nivel de hemoglobina, disminuir el requerimiento transfusional y mejorar la calidad de vida. En la Tabla 4 se muestran los resultados en los principales estudios realizados. El aumento promedio de hemoglobina fue 1.7-2.2 g/dl al final del tiempo de evaluación. Ultimamente se presta atención al concepto de cambio cumulativo de hemoglobina. Considerando que los índices de calidad de vida mejoran en forma paralela al incremento de hemoglobina, es lógico asumir que cuanto más rápida sea la mejoría de la hemoglobina, más rápida será la mejoría de estos índices. Así, el tiempo para alcanzar un incremento en la concentración de hemoglobina de 1-2 g/dl será mejor índice que la simple medición del nivel de hemoglobina alcanzado al final del estudio129b. Los novedosos esquemas "front loading" se basan en estos conceptos. Con respecto al requerimiento transfusional, se observó disminución del mismo hasta en 47%119-122,130. La calidad de vida es considerada actualmente uno de los principales objetivos a mejorar cuando se evalúan los resultados de la terapéutica antineoplásica. Se la ha correlacionado con la gravedad de la anemia, habiéndose observado relación entre el aumento de hemoglobina alcanzado con rHuEPO y mejores scores de calidad de vida131.
La concentración óptima de hemoglobina con la cual conviene comenzar tratamiento con rHuEPO es 10-11 g/dl128, 129. La dosis recomendada es de 150 unidades/kg, tres veces por semana. Generalmente, el cumplimiento adecuado del tratamiento es pobre. Con el objetivo de mejorar su aceptación, durante los últimos años se investigó la eficacia de la administración de una dosis única elevada (30.000 a 60.000 unidades) semanal121,132. Los resultados fueron equivalentes a los del régimen de administración trisemanal, por lo que es actualmente recomendado por la mayoría de los autores118.
TABLA 4.- Utilización de rHuEPO en pacientes con anemia relacionada al cáncer y en tratamiento quimioterápico
El conocimiento de factores predictivos de respuesta tiene implicancias pronósticas y económicas. En neoplasias hematológicas se ha demostrado que la disminución del nivel de Epo sérica es el principal determinante de respuesta132,133. En tumores sólidos los datos son más conflictivos. Algunos autores han comunicado la importancia de distintos factores para predecir la respuesta al tratamiento: pico reticulocitario a la segunda semana, infiltración de médula ósea, Epo sérica <100 mU/ml, o incrementos en el receptor soluble de transferrina a los 15 dias134,135. Aunque otros trabajos no pudieron confirmar su importancia y cuestionan su utilidad136, la combinación de déficit de Epo más respuesta precoz al tratamiento parece ser actualmente el mejor indicador de respuesta.
Es mucho menos lo que se sabe sobre el impacto del tratamiento con rHuEPO en niños con cáncer. La información disponible es limitada, debido a importantes diferencias metodológicas en los pocos estudios publicados y al bajo número de pacientes incluido en cada uno137, 138. La mayoría de los estudios concluyen que el tratamiento es útil para elevar los niveles de hemoglobina y disminuir el requerimiento transfusional139-142, pero otros no han confirmado estos resultados143. Un importante ensayo utilizando una dosis semanal única de rHuEPO en 203 niños con AAC demostró mejoría significativa de la calidad de vida en los pacientes143b. Una revisión sobre 15 estudios concluyó que parece existir un efecto beneficioso de la rHuEPO, pero es imprescindible la realización de futuros estudios multicéntricos para confirmarlo137.
Algunos autores han sugerido que la rHuEPO podría mejorar la sobrevida de los pacientes con cáncer122. Una revisión Cochrane incluyendo ensayos publicados hasta 2001 sugirió una tendencia a sobrevida más prolongada en los pacientes tratados con rHuEPO144. Estudios más recientes han descartado este beneficio potencial145,146. Como últimamente se han detectado receptores de Epo funcionantes en varias líneas celulares tumorales humanas, actualmente se está investigando el potencial efecto favorecedor de progresión tumoral de la rHuEPO147-150. Considerando la discordancia actualmente existente, tanto en los resultados de los ensayos clínicos como en los trabajos experimentales, se requiere de estudios adicionales en los cuáles se deberá realizar un muy estricto control de la evolución del tumor para poder alcanzar conclusiones definitivas.
Anemia asociada a infección por HIV
La anemia era un hallazgo común en la infección por HIV, con una prevalencia de 50-75% en adultos y hasta 90% en niños151, 152, siendo además un reconocido factor pronóstico de progresión de enfermedad y de mortalidad153. El uso de altas dosis de AZT era uno de los factores causales para su desarrollo. A partir de la introducción de la terapia retroviral altamente activa (HAART) y el consecuente uso de dosis menores de AZT, la prevalencia de anemia ha declinado, aunque continúa siendo un problema importante153, 154. En uno de los estudios prospectivos más grandes, con más de 7.000 pacientes tratados con HAART, su incidencia fue de 46%154. Bajo terapia HAART la anemia se asocia también a peor evolución, calidad de vida inferior y mayor riesgo de demencia155. Por tanto, un objetivo importante del tratamiento es mantener una hemoglobina cercana a lo normal.
El tratamiento con rHuEPO ha demostrado ser inocuo y efectivo. Su impacto ha sido confirmado por numerosos estudios prospectivos aleatorizados, que además han establecido que el aumento de hemoglobina, la mejoría en calidad de vida y la disminución del requerimiento transfusional se asocian a niveles de Epo endógena <500 mU/ml156.
La efectividad del régimen de administración semanal parece ser igual al de tres veces por semana, pero con la ventaja de ser más práctico y mejor aceptado157. El esquema habitual consiste en dosis semanales de 40.000 UI, que se incrementan a 60.000 UI si a las 2 semanas no hay respuesta. En un estudio controlado sobre 285 pacientes se comparó este esquema con el tradicional, observándose que a la 8a semana se obtenía el máximo de respuesta en grado similar para ambos grupos158. Otro estudio sobre 650 pacientes, no controlado, también demostró su utilidad159. La mejoría en calidad de vida fue similar a la alcanzada con el tratamiento trisemanal158, 160.
El tratamiento con rHuEPO ha sido tan útil en pacientes tratados con dosis convencionales de AZT como en aquellos tratados con regímenes conteniendo dosis bajas de AZT o sin ella106, 107, 155, 161, 162.
El uso de rHuEPO en pacientes pediátricos no ha sido exhaustivamente investigado. Algunos autores han comunicado que el tratamiento aumentó los niveles de hemoglobina y disminuyó el requerimiento transfusional. En nuestro estudio sobre 22 niños, el grupo tratado con rHuEPO alcanzó concentraciones de hemoglobina significativamente mayores que el grupo control, pero no hubo diferencia en el requerimiento transfusional106. El tratamiento con rHuEPO parece estar recomendado, pero es imprescindible la realización de estudios prospectivos sobre un número elevado de pacientes para establecer conclusiones definitivas.
Anemia asociada a hepatitis C
Para la hepatitis crónica por virus C (HCV) se utiliza tratamiento combinado con ribavirina e interferón. La anemia es uno de los principales efectos colaterales de esta terapia. El interferón produce una anemia hiporregenerativa, mientras que la ribavirina produce una de tipo hemolítica163. La ribavirina es captada por los eritrocitos y convertida en ribavirina-trifosfato; la incapacidad para metabolizar este complejo lleva a un incremento intracelular del mismo, lo cual produce depleción de los niveles de ATP intraeritrocitarios, y como consecuencia inmediata daño de la membrana por estrés oxidativo y subsiguiente destrucción del eritrocito164. También existe una disrregulación de los Epo-R.
La recomendación actual consiste en reducir la dosis de ribavirina, llegando incluso a suspensión de su administración si la hemoglobina disminuye por debajo de 8.5 g/dl. Como estos ajustes de dosis influyen notablemente en la eficacia terapéutica de la droga, se ha planteado que el tratamiento con rHuEPO podría atenuar los efectos de esta complicación. Un estudio controlado demostró que la rHuEPO (40.000 unidades/semana) fue efectiva para mantener la dosis adecuada de ribavirina, mejorar la calidad de vida y aumentar los niveles de hemoglobina165; la dosis pudo ser mantenida en 88% de los que recibían tratamiento con rHuEPO y solo en 60% de los que no lo recibían.
La infección por HCV en niños no es rara y se trata con el mismo régimen terapéutico, por lo que el uso de rHuEPO en esta población debe ser evaluado.
Anemia en pacientes críticamente enfermos
Alrededor del 50% de pacientes en terapia intensiva requieren al menos una transfusión durante su internación166. En un estudio controlado sobre 1302 pacientes aleatorizados para recibir rHuEPO (40.000 UI, dosis única semanal) o placebo, se observó que fueron transfundidos el 50% de los pacientes tratados con rHuEPO y el 60.4% de los que recibieron placebo167. Actualmente se debate intensamente acerca del costo/beneficio de esta modalidad terapéutica.
Uso terapéutico potencial de los efectos no hemopoyéticos de la rHuEPO
Una enorme cantidad de estudios han confirmado la presencia de Epo-R en tejidos no hemopoyéticos: sistema nervioso central (SNC) (neuronas y células de la glía), endotelio vascular, miocardio, endotelio intestinal, músculo liso, tejidos placentarios, testículo (células de Leydig) y placenta168. El principal mecanismo por el cual la Epo ejerce su efecto citoprotector es promover la sobrevida celular a través de inhibición de apoptosis169. La presencia de Epo y Epo-R en el cerebro en desarrollo sugiere que la Epo juega un rol de máxima importancia en el desarrollo del SNC, y se ha propuesto que es un importante inductor de neurogénesis durante las etapas tempranas del desarrollo embrionario168, 170, 171.
Primeramente se exploraron las potenciales aplicaciones terapéuticas de la rHuEPO como neuroprotector168, 170-173. Este efecto fue originalmente demostrado en animales. La inyección intraventricular directa a ratas con isquemia cerebral dio como resultado una marcada reducción del área de necrosis en los animales pretratados con rHuEPO174. Posteriormente se observó que, administrada por vía sistémica, la rHuEPO solo alcanzaba SNC si había disrupción de la barrera hematoencefálica175, o si era administrada en dosis mucho mayores que las habituales176, 177.
El primer ensayo de investigación clínica (fase I/II) evaluó el efecto de la administración intravenosa precoz de altas dosis de rHuEPO a 53 adultos con accidente cardiovascular isquémico, mostrando que el tratamiento estuvo asociado a reducción significativa del tamaño del infarto cerebral y a mejor evolución clínica al mes de evolución178. No se observó ningún efecto adverso importante. En pacientes con mielopatías y daño isquémico secundario a lesión o compresión espinal, el tratamiento con rHuEPO mostró efecto beneficioso sobre la mejoría de la función motora (Voulgaris S, Kaliora C, Zago-rianakou R y col. 9th Congress of the European Hematology Association, 2004).
El daño neurológico secundario a hipoxia es frecuente en niños RN, siendo sus causas más frecuentes la asfixia perinatal y la hemorragia intraventricular. Estudios en roedores neonatos demostraron que la administración de rHuEPO tenía el mismo efecto neuroprotector que en animales adultos168, 179. En un estudio fase I, Levitt y col. investigaron farmacodinamia, efectos biológicos e inocuidad de la administración de dosis muy altas de rHuEPO (5.000 unidades/kg, única dosis) a 15 pretérminos MBPN en riesgo de hemorragia intraventricular (Levitt SM, Calhoun DA, Martin B, Fox SE, Christensen RD. PAS Annual Meeting, 2003). La rHuEPO fue bien tolerada y no se observó ningún efecto adverso. Se esperan los resultados de estudios de investigación clínica diseñados para evaluar eficacia y seguridad de esta terapia para tratamiento o profilaxis del daño secundario a hipoxia cerebral en neonatos180.
También está siendo evaluado el efecto de la rHuEPO sobre las células del endotelio intestinal181, ya que presentan amplia expresión de Epo-R funcionales tanto en el feto como en el niño RN182. La Epo desempeñaría un rol importante en mantenimiento y reparación de la mucosa. Estudios in vitro demostraron que protege a las células intestinales contra la injuria química, y experiencias en ratas RN mostraron que su administración produjo aumento del largo de las vellosidades, del área vellosa, de la profundidad de las criptas y de la proliferación de las células epiteliales de las criptas182. Se observó incidencia de enterocolitis necrotizante significativamente menor en prematuros MBPN que recibían rHuEPO para tratamiento de AP que en aquellos que no la recibían183. El efecto de su administración enteral está actualmente siendo investigado. Aún no está aclarado si la rHuEPO es absorbida cuando se administra oralmente, pues mientras dos ensayos con 6 neonatos cada uno concluyeron que la misma era absorbida184, 185, un estudio prospectivo sobre 32 MBPN no encontró evidencia de que fuera absorbida181. Recientemente se han comunicado los primeros estudios utilizando un líquido amniótico artificial que contiene además rHuEPO, Filgrastim y otras citoquinas, en niños RN pretérmino, concluyendo que el mismo es inocuo y bien tolerado181, 186. Están en marcha estudios prospectivos aleatorizados para evaluar su eficacia en neonatos que no reciben alimentación oral.
Están en estudio múltiples posibles aplicaciones para citoprotección en neuropatía periférica, retinopatías, isquemia miocárdica, protección gonadal y otras187.
Efectos adversos
Las complicaciones habitualmente encontradas en adultos y niños con IRT incluyen: síndrome gripal, hipertensión arterial, encefalopatía hipertensiva, convulsiones, trombosis del acceso vascular y desarrollo de anticuerpos anti-Epo15. El más frecuente es la hipertensión, con una incidencia global de 33% en niños y adultos. El síndrome gripal tiene una incidencia similar15,17.
El desarrollo de anticuerpos anti-Epo es una complicación muy rara, y una de las causas de resistencia al tratamiento con rHuEPO. Desde 1998 se ha observado un aumento significativo en el número de pacientes que desarrollaron aplasia pura de células rojas (APCR) secundaria a la aparición de anticuerpos neutralizantes anti-Epo. Su incidencia ha variado de 0.2 a 26.7 casos/100.000 pacientes/año188, debido fundamentalmente al aumento de casos en Europa después de la introducción de rHuEPO libre de albúmina y el uso de polisorbato 80 en su reemplazo. La APCR se caracteriza por anemia grave, altísimo requerimiento transfusional y falta total de respuesta a dosis crecientes de rHuEPO. La mayoría de los más de 250 casos comunicados hasta la fecha son varones con fallo renal crónico que recibían Epo por vía subcutánea189. No se han descripto casos de APCR en pacientes con anemia inducida por quimioterapia; tampoco en niños o neonatos. Para su diagnóstico se han propuesto los criterios enumerados en la Tabla 5190. La determinación de anticuerpos se puede realizar por varios métodos191: a) ELISA: Sensible, poco específico; está en desarrollo uno con mayor especificidad192; b) Radioinmunoprecipitación: Específico, buena sensibilidad; es el más utilizado193; c) Biacore: Específico, muy sensible, permite conocer la afinidad del anticuerpo a la Epo; es el utilizado por la compañías farmacéuticas en estudios de farmacovigilancia194. Los factores reconocidos como favorecedores de APCR son administración subcutánea, reemplazo de la albúmina por polisorbato 80 y formación de micelas con potencialidad antigénica195.
TABLA 5.- Criterios diagnósticos de aplasia pura de células rojas secundaria a anticuerpos anti-Epo

La conducta frente a un posible caso consiste en suspender la rHuEPO, realizar punción de médula ósea, y pesquisar anticuerpos anti-Epo en suero. La terapia de elección es el tratamiento inmunosupresor190, comenzando con corticoides; si no hay respuesta pasar a ciclosporina A, asociándola o no a los corticoides196. No se han comunicado casos de desaparición espontánea de los anticuerpos197. Los tratamientos con ciclofosfamida, inmunoglobulina G intravenosa o rituximab (anticuerpo monoclonal anti-CD20) no han sido suficientemente evaluados. Pacientes sometidos a transplante renal exitoso negativizaron los anticuerpos y corrigieron la anemia198.
Una vez superada la etapa aguda en enfermos que quedan gravemente anémicos, se puede recomenzar el tratamiento pero utilizando darbapoetina u otros análogos; siempre debe considerarse la posibilidad latente de reacciones cruzadas entre las diversas formas de Epo recombinante199.
Aún no se ha establecido si los anticuerpos anti-Epo juegan algún papel en la resistencia a la rHuEPO; no se encontró asociación entre títulos bajos de anticuerpos y respuesta disminuida al tratamiento (Valtuille R, Ferro H, González E y col. ERA EDTA XLI Congress, 2004). Casadevall y col. sugieren seguimiento estricto de los pacientes asintomáticos que presentan anticuerpos, pues han detectado casos de APCR durante la evolución de los mismos (Casadevall N, Rossert J, Swanson S y col. American Society of Nephrology Renal Week, 2004)
Estos efectos adversos precedentemente enumerados pueden potencialmente desarrollarse en lactantes y niños en tratamiento con rHuEPO por otras patologías que no sean IRT, por lo que deben ser considerados al evaluar la conveniencia de indicar un tratamiento.
En neonatos, ninguno de los efectos adversos descriptos en adultos y niños mayores ha sido comunicado. Solamente hemos detectado trombocitosis mayor de 500 x 109//l en 30% de los niños MBPN durante el tratamiento con rHuEPO, pero sin que produjera ninguna manifestación clínica y de resolución espontánea64.
Discusión
El uso de la rHuEPO en adultos o niños con IRT no presenta demasiados aspectos conflictivos. La deficiencia de hierro es responsable de la mayoría de los casos de resistencia a la rHuEPO. La administración de hierro endovenoso, de uso rutinario en adultos, podría ayudar a eliminar esta causa de fallo terapéutico en niños. El rol de la rHuEPO en SUH y SN abre nuevas áreas de investigación casi inexploradas.
El manejo de la AP mediante la combinación de terapia con rHuEPO, guías de transfusión más estrictas, cambios en las conductas de extracción e implementación de nuevas técnicas transfusionales llevó a un marcado descenso del requerimiento transfusional y la exposición a donantes. El papel relativo de cada uno de estos factores debe aún ser establecido. En opinión de los autores, y hasta que los resultados de los estudios en marcha establezcan criterios definitivos, el tratamiento con rHuEPO debe administrarse a niños con peso de nacimiento <1000 g desde la primera semana de vida. La relación costo-beneficio de esta política debe ser evaluada en cada país, considerando los costos locales.
La evidencia para el uso de rHuEPO en anemias hiporregenerativas en período neonatal es altamente convincente, por lo que debería estimularse su indicación. Su utilidad para tratar anemias hemolíticas con respuesta de Epo inadecuada no está establecida y requiere futuras investigaciones.
El impacto del tratamiento con rHuEPO sobre calidad de vida en adultos con AAC y anemia asociada a infección por HIV ha sido notable, siendo actualmente considerado de elección por la mayoría de los autores. Este aspecto ha sido poco investigado en niños, no existiendo aún certeza sobre su indicación sistemática. La administración de una única dosis intravenosa semanal podría estimular su uso, permitiendo alcanzar una respuesta definitiva.
La utilización potencial de los efectos no hematopoyéticos de la Epo es uno de los aspectos más promisorios para ser evaluados. Su acción antiapoptótica, neuroprotectora y citoprotectora de células endoteliales abre un panorama alentador para el tratamiento de diversas enfermedades, especialmente para mejorar el pronóstico de trastornos isquémicos cerebrales en neonatos, pero primero debe establecerse la inocuidad del tratamiento. El uso de altas dosis debe ser cuidadosamente monitoreado, siendo imperativa la evaluación de la evolución a largo plazo. Considerando que no existe terapia efectiva para la injuria cerebral, se deben realizar esfuerzos para llevar adelante estos estudios lo más pronto posible.
Conflicto de interés: Los Dres. Hugo Donato y Hugo Ferro son asesores del Area de Investigación Clínica de Bio Sidus S.A.
Bibliografía
1. Krantz SB. Erythropoietin. Blood 1991; 77: 419-25. [ Links ]
2. Fisher JW. Erythropoietin: Physiology and pharmacology update. Exp Biol Med 2003; 228: 1-14. [ Links ]
3. Dame C, Juul SE. The switch from fetal to adult erythropoiesis. Clin Perinatol 2000; 27: 507-26. [ Links ]
4. Semenza GL, Rue EA, Iyer NV, Pang MG, Kearns WG. Assignment of the hypoxia-inducible factor 1alfa gene to a region of conserved synteny on mouse chromosome 12 and human chromosome 14q. Genomics 1996; 34: 437-9. [ Links ]
5. Kaelin WG Jr. The von Hippel-Lindau gene, kidney cancer, and oxygen sensing. J Am Soc Nephrol 2003; 14: 2703-11. [ Links ]
6. Ohls RK. The use of erythropoietin in neonates. Clin Perinatol 2000; 27: 681-96. [ Links ]
7. Zanjani ED, Pixley JS, Slotnick N, et al. Erythropoietin does not cross the placenta into the fetus. Pathobiology 1993; 61: 211-5. [ Links ]
8. Campbell J, Wathen N, Lewis M, et al. Erythropoietin levels in amniotic fluid and extraembryonic coelomic fluid in the first trimester of pregnancy. Br J Obstet Gynaecol 1992; 99: 974-6. [ Links ]
9. Koury ST, Koury MJ. Erythropoietin production by the kidney. Semin Nephrol 1993; 13: 78-86. [ Links ]
10. Dame C, Fahnenstich H, Freitag P, et al. Erythropoietin mRNA expression in human fetal and neonatal tissue. Blood 1998; 92: 3218-25. [ Links ]
11. Muta K, Krantz SB, Bondurant MC, et al. Distinct roles of erythropoietin, insulin-like growth factor I, and stem cell factor in the development of erythroid progenitor cells. J Clin Invest 1994; 94: 34-43.
12. Miyake T, Kung CKH, Goldwasser E. Purification of human erythropoietin. J Biol Chem 1977; 252: 5558-64.
13. Lin FK, Suggs S, Lin CH, et al. Cloning and expression of the human erythropoietin gene. Proc Natl Acad Sci U S A 1985; 92: 7850-84.
14. Esbach JW, Egrie JC, Downing MT, et al. Correction of the anemia of end-stage renal disease with recombinant human erythropoietin. Results of a combined phase I and II clinical trial. N Engl J Med 1987; 316: 73-8.
15. Gimenez LF, Scheel PJ. Clinical application of recombinant erythropoietin in renal dialysis patients. Hematol Oncol Cl NA 1994; 8: 913-26.
16. Scigalla P. Effect of recombinant human erythropoiein treatment on renal anemia and body growth of children with end-stage renal disease. En: Baldamus CA, Scigalla P, Wieczorek L, et al (eds). Erythropoietin in renal and non-renal anemias. Basel: Kargel, 1991.
17. Rendo P, Biscigniano L, Turconi A, Sánchez Avalos JC, Greco J. Tratamiento de la anemia en niños sometidos a hemodiálisis crónica con eritropoyetina humana recombinante. Medicina (Buenos Aires) 1994; 54: 392-98.
18. Locatelli F, Aljama P, Barany P, et al. Revised European best practice guidelines for the management of anaemia in patients with chronic renal failure. Nephrol Dial Transplant 2004; 19 Suppl 2 : ii1-50.
19. National Kidney Foundation. K/DOQI Clinical practice guidelines for anemia of chronic kidney disease, 2000. Am J Kidney Dis 2001; 37: S182-238.
20. Jabs K, Alexander S, McCabe D. Primary results from the U.S. multicenter pediatric recombinant eryhropoiein (epo) study. J Am Soc Nephrol 1994; 5: 456.
21. Port RE, Kiepe D, Van Guilder M, Jellife RW, Mehls O. Recombinant human erythropoietin for the treatment of renal anaemia in children. Clin Pharmacokinet 2004; 43: 57-70.
22. Cusumano A, Rendo P, Macheroni C, Sánchez Avalos JC. Tratamiento de los pacientes en hemodiálisis crónica (HDC) con dosis bajas de eritropoyetina recombinante (r.Hu EPO) asociada o no a andrógenos. Nefrología 1996; 16: 374-8.
23. Kuriyama S, Tomonari H, Yoshida H, Hashimoto T, Kawaguchi Y, Sakai O: Reversal of anemia by erythropoietin therapy retards the progression of chronic renal failure, especially in nondiabetic patients. Nephron 1997; 77: 176–85.
24. Macdougall IC, Steering Committee of the CREATE trial, CREATE Study Group. CREATE: new strategies for early anaemia management in renal insufficiency. Nephrol Dial Transplant 2003; 18 (Suppl 2):ii13-16.
25. Besarab A, Bolton WK, Browne JK, et al. The effects of normal as compared with low hematocrit values in patients with cardiac disease who are receiving hemodialysis and epoetin. N Engl J Med 1998; 339: 584-90.
26. Foley RN, Parfrey PS, Morgan J, et al. Effect of hemoglobin levels in hemodialysis patients with asymptomatic cardiomyopathy. Kidney Int 2000; 58:1325-35.
27. McMahon LP, Mason K, Skinner SL, Burge CM, Grigg LE, Becker GJ. Effects of haemoglobin normalization on quality of life and cardiovascular parameters in end-stage renal failure. Nephrol Dial Transplant 2000; 15:1425-30.
28. Macdougall IC. Optimizing the use of erythropoietic agents-pharmacokinetic and pharmacodynamic considerations. Nephrol Dial Transplant 2002; 17 (Suppl 5): 66-70.
29. Barre P, Reichel H, Suranyi MG, Barth C. Efficacy of once-weekly epoetin alfa. Clin Nephrol 2004; 62: 440-8.
30. Frifelt JJ, Tvedegaard E, Bruun K et al. Efficacy of recombinant human erythropoietin administered subcutaneously to CAPD patients once weekly. Perit Dial Int 1996; 16: 594-8.
31. Provenzano R, Garcia-Mayol L, Suchinda P, et al. Once-weekly epoetin alfa for treating the anemia of chronic kidney disease. Clin Nephrol 2004; 61:392-405.
32. Jones CH, Ridley L, Richardson D. Which EPO dose per week? Nephrol Dial Transplant 2002; 17: 1855.
33. Fishbane S, Maesaka JK. Iron management in end-stage renal disease. Am J Kidney Dis 1997; 29: 319-33.
34. Gillespie RS, Wolf FM. Intravenous iron therapy in pediatric hemodialysis patients : a meta-analysis. Pediatr Nephrol 2004; 19: 662-6.
35. Schroder CH, The European Pediatric Peritoneal Dialysis Working Group. The management of anemia in pediatric peritoneal dialysis patients. Guidelines by an ad hoc European committee. Pediatr Nephrol 2003; 18: 805-9.
36. Piraino B, Johnston JR. The use of subcutaneous erythropoietin in CAPD patients. Clin Nephrol 1990; 33: 200-11.
37. Saito S, Fujiwara T, Sakagami K, Matsuno T, Tanaka N. Anemia following renal transplantation. Transplant Proc 1998; 30: 3025-6.
38. Yorgin PD, Belson A, Sanchez J, et al. Unexpectedly high prevalence of posttransplant anemia in pediatric and young adult renal transplant recipients. Am J Kidney Dis 2002; 40: 1306-18.
39. Al-Uzri A, Yorgin PD, Kling PJ. Anemia in children after transplantation: etiology and the effect of immuno-suppressive therapy on erythropoiesis. Pediatr Transplant 2003; 7: 253-64.
40. Nielsen OJ, Thaysen JH. Erythropoietin deficiency in acute renal failure. Lancet 1989; 1: 624-5.
41. Fernández V, Campbell M, Itscoff P,et al. Deficit relativo de EPO endógena en anemia por IRA. Nefrología 1992; 12 (Suppl 2): 64.
42. Exeni R, Donato H, Rendo P, et al. Low levels of serum erythropoietin in children with endemic hemolytic uremic syndrome. Pediatr Nephrol 1998; 12: 226-30.
43. OBrien MER, Casey S, Treleaven J, Powles TJ. Use of erythropoietin in the management of the haemolytic uraemic syndrome induced by mitomycin C/tamoxifen. Eur J Cancer 1994; 30: 894-5.
44. Catalano C, Gianesini C, Fabbian F. Erythropoietin is beneficial in mitomycin-induced hemolytic-uremic syndrome. Nephron 2002; 91: 324-6.
45. Citarrella P, Gebbia V, Teresi M, et al. Hemolytic uremic syndrome after chemotherapy with gemcitabine and taxotere : a case report. Anticancer Res 2002; 22: 1183-5.
46. Ellis D. Anemia in the course of the nephrotic syndrome secondary to transferrin depletion. J Pediatr 1977; 90: 953-5.
47. Feinstein S, Becker-Cohen R, Algur N, et al. Erythropoietin deficiency causes anemia in nephrotic childen with normal kidney function. Am J Kidney Dis 2001; 37: 736-42.
48. Rifkin D, Kravetz HM, Knight V, Schade AL. Urinary excretion of iron-binding protein in the nephrotic syndrome. N Engl J Med 1961; 265: 115-8.
49. Hancock DE, John W, Onstad JW, Wolf PL. Transferrin loss into the urine with hypochromic, microcytic anemia. Am J Clin Pathol 1976; 65: 73-8.
50. Vaziri ND, Kaupke CJ, Barton CH. Gonzales E. Plasma concentration and urinary excretion of erythropoietin in adult nephrotic syndrome. Am J Med 1992; 92: 35-40.
51. Zhou KJ, Vaziri ND. Erythropoietin metabolism and pharmacokinetics in experimental nephrosis. Am J Physiol Renal Physiol 1992; 263: F812-5.
52. Gansevoort RT, Vaziri ND, De Jong PE. Treatment of anemia of nephrotic syndrome with recombinant erythropoietin. Am J Kidney Dis 1996; 28: 274-7.
53. Ishimitsu T, Ono H, Sugiyama M, et al. Sucessful erythropoietin treatment for severe anemia in nephrotic syndrome without renal dysfunction. Nephron 1996; 74: 607-10.
54. Bayés B, Serra A, Juncá J, Lauzurica R. Successful treatment of anaemia of nephrotic syndrome with recombinant human erythropietin. Nephrol Dial Transplant 1998; 13: 1894-5.
55. Donato H, Vain N, Rendo P. Tratamiento con eritropoyetina humana recombinante en período neonatal: indicaciones y controversias. Arch Arg Pediatr 1996; 94: 28-45.
56. Garby L, Sjolin S, et al. Studies on erythrokinetics in infancy. III. Plasma dissapearance and red cell uptake of intravenously injected radioiron. Acta Paediatr 1963; 52: 537-40.
57. Dallman PR, Siimes MA. Percentile curves for hemoglobin and red cell volume in infancy and childhood. J Pediatr 1979; 94: 28-33.
58. Stockmann JA III, Graeber JE, Clark DA, et al. Anemia of prematurity: Determinants of erythropoietin response. J Pediatr 1984 105: 786-92.
59. Forestier F, Daffos F, Catherine N, Renard M, Andreux JP. Developmental hematopiesis in normal human fetal blood. Blood 1991; 11: 2360-3.
60. Yamashita H, Kukita J, Ohga S, et al. Serum erythropoietin levels in term and preterm infants during the first year of life. Am J Pediatr Hematol Oncol 1994; 16: 213-8.
61. Tan CC, Eckardt KU, Firth JD, et al. Feedback modulation of renal and hepatic erythropoietin mRNA in response to graded anemia and hypoxia. Am J Physiol 1992; 263: F474-81.
62. Frey B. Transfusion in premature infants impairs production and/or release of red blood cels, white blood cells and platelets. J Paediatr Child Health 2002; 38: 265-7.
63. Strauss RG. Transfusion therapy in neonates. Am J Dis Child 1991; 145: 904-11.
64. Donato H, Vain N, Rendo P, et al. Effect of early versus late administration of human recombinant erythropoietin on transfusion requirements in premature infants: Results of a randomized, placebo-controlled, multicenter trial. Pediatrics 2000; 105: 1066-72.
65. Yeo CL, Choo S, Ho L. Effect of recombinant human erythropoietin on transfusion needs in preterm infants. J Paediatr Child Health 2001; 37: 352-8.
66. Maier RE, Obladen M, Muller-Hansen I, et al. Early treatment with erythropoietin b ameliorates anemia and reduces transfusion requirements in infants with birth weight below 1000 g. J Pediatr 2002; 141: 8-15.
67. Lin JC, Strauss RG, Kulhavy JC, et al. Phlebotomy overdraw in the neonatal intensive care unit. Pediatrics 2000 106: e19-25.
68. Bifano EM, Curran TR. Minimizing donor blood exposure in the neonatal intensive care unit. Clin Perinatol 1995 22: 657-69.
69. Rhondeau SM, Christensen RD, Ross MP, et al. Responsiveness to recombinant human erythropoietin of marrow erythroid progenitors from infants with the "anemia of prematurity". J Pediatr 1988; 112: 935-40.
70. Halperin DS, Wacker P, Lacourt G, et al. Effects of recombinant human erythropoietin in infants with the anemia of prematurity: A pilot study. J Pediatr 1990 116: 779-86.
71. Shannon KM, Mentzer WC, Abels RI, et al. Recombinant human erythropoietin in the anemia of prematurity: Results of a placebo-controlled pilot study. J Pediatr 1991 118: 949-55.
72. Ohls R, Christensen RD. Recombinant erythropoietin compared with erythrocyte transfusion on the treatment of anemia of prematurity. J Pediatr 1991; 119: 781-8.
73. Beck D, Masserey E, Meyer M, et al. Weekly intravenous administration of recombinant human erythropoietin in infants with the anemia of prematurity. Eur J Pediatr 1991; 150: 767-72.
74. George JW, Bracco C, Shannon K, et al. Response of Rhesus monkeys to recombinant human erythropoietin: Comparison of adults and infants. Pediatr Res 1989; 25: 269A.
75. Widness JA, Veng-Pedersen P, Modi NB, et al. Developmental differences in erythropoietin pharmacokinetics: Increased clearance and distribution in fetal and neonatal sheep. J Pharmacol Exp Therap 1992; 261: 977-84.
76. Messer J, Haddad J, Donato L, et al. Early treatment of premature infants with recombinant human erythropoietin. Pediatrics 1993; 92: 519-23.
77. Donato H, Rendo P, Vivas N, Schvartzman G, Digregorio J, Vain N. Recombinant human erythropoietin in the treatment of anemia of prematurity: A randomized, double-blind, placebo-controlled trial comparing three different doses. Int J Pediatr Hematol Oncol 1996; 3: 279-85.
78. Emmerson AJB, Coles HJ, Stern CMM, et al. Double blind trial of recombinant human erythropoietin in preterm infants. Arch Dis Child 1993; 68: 291-6.
79. Meyer MP, Meyer JH, Commerford A, et al. Recombinant human erythropoietin in the treatment of the anemia of prematurity: Results of a double-blind, placebo-controlled study. Pediatrics 1994; 93: 918-23.
80. Shannon KM, Keith JF, Mentzer WC, et al. Recombinant human erythropoietin stimulates erythropoiesis and reduces erythrocyte transfusions in very low birth weight preterm infants. Pediatrics 1995; 95: 1-8.
81. Soubasi V, Kremonopoulos G, Diamandi E, et al. In which neonates does early recombinant human erythropoietin treatment prevent anemia of prematurity? Results of a randomized, controlled study. Pediatr Res 1993 34: 675-9.
82. Vamvakas EC, Strauss RG. Meta-analysis of controlled clinical trials studying the efficacy of rHuEPO in reducing blood transfusions in the anemia of prematuriry. Transfusion 2001; 41: 406-15.
83. Ohls RK, Osborne KA, Christensen RD. Efficacy and cost analysis of treating very low birth weight infants with erythropoietin during their first two weeks of life: A randomized, placebo-controlled trial. J Pediatr 1995; 126: 421-6.
84. Ohls RK, Harcum J, Schibler KR, Christensen RD. The effect of erythropoietin on the transfusion requirements of preterm infans weighing 750 grams or less: a randomized, double-blind, placebo-controlled study. J Pediatr 1997; 131: 661-5.
85. Ohls RK, Ehrenkranz RA, Wright LL, et al. Effects of early erythropoietin therapy on the transfusion requirements of preterm infants below 1250 grams birth weight: A multicenter, randomized, controlled trial. Pediatrics 2001; 108: 934-42.
86. Kotto-Kome AC, García MG, Calhoun DA, Christenser RD. Effect of beginning recombinant erythropoietin treatment within the first week of life, among very-low-birth-weight neonates, on "early" and "late" erythrocyte transfusions : A meta-analysis. J Perinatol 2004; 24:Basel 24-9.
87. Ohls RK. Erythropoietin treatment in extremely low birth weight infants : Blood in versus blood out. J Pediatr 2002; 141: 3-6.
88. Ibojie J, Greiss M, Lloyd DJ, Urbaniak SJ. Donor exposure rate to transfusion ratio: a better discriminator of improvement in neonatal transfusion practice. Transf Med 2003; 13: 287-91.
89. Hilsenrath P, Nemechek J, Widness JA, Cordle DG, Strauss RG. Cost-effectiveness of a limited donor blood program for neonatal red cell transfusions. Transfusion 1999; 39: 938-43.
90. Brune T, Garritsen H, Hentschel R, Louwen F, Harms E, Jorch G. Efficacy, recovery, and safety of RBCs from autologous placental blood: clinical experience in 52 newborns. Transfusion 2003; 43: 1210-5.
91. Bifano EM, Dracker RA, Lorah K, Palit A. Collection and 28-days storage of human placental blood. Pediatr Res 1994; 36: 90-4.
92. Maier RF, Sonntag J, Walka MM, Liu G, Metze BC, Obladen M. Changing practices of red blood cell transfusions in infants with birth weights less than 1000 g. J Pediatr 2000; 136: 220-4.
93. Donato H, Vain N, Rendo P. Folate and vitamin B12 supplementation in very low birth weight infants treated with erythropoietin: A cautionary note. Pediatrics 2002; 108: 218.
94. Pathak A, Roth P, Piscitelli J, Johnson L. Effects of vitamin E supplementation during erythropoietin treatment of the anaemia of prematurity. Arch Dis Child Fetal Neonatal Ed 2003; 88: F324-8
95. Zipursky A. Vitamin E deficiency anemia in newborn infants. Clin Perinatol 1984; 11: 393-402.
96. Millard DD, Gidding SS, Socol ML, et al. Effects of intravascular, intrauterine transfusion on prenatal and postnatal hemolysis and erythropoiesis in severe fetal isoimmunization. J Pediatr 1990; 117: 447-54.
97. Koenig JM, Ashton DR, De Vore GR, et al. Late hyporegenerative anemia in Rh hemolytic disease. J Pediatr 1989; 115: 315-8.
98. Ohls RK, Wirkus PE, Christensen RD. Recombinant erythropoietin as treatment for the late hyporegenerative anemia of Rh hemolytic disease. Pediatrics 1992; 90: 678-80.
99. Scaradavou A, Inglis S, Peterson P, et al. Suppression of erythropoiesis by intrauterine transfusions in hemolytic disease of the newborn : Use of erythropoietin to treat the late anemia. J Pediatr 1993; 123: 279-84.
100. Nenadov Beck M, Dessing C, Vial Y, Hohlfeld P. Efficacy of recombinant human erythropoietin (rHuEPO) in anemic neonates after intrauterine transfusions. J Pediatr Hematol Oncol 1999; 21: 333.
101. Ovali F, Samanci N, Dagoglu T. Management of late anemia in rhesus hemolytic disease: Use of recombinant human erythropoietin (A pilot study). Pediatr Res 1996; 39: 831-4.
102. Ovali F. Late anaemia in Rh haemolytic disease. Arch Dis Child Fetal Neonatal Ed 2003; 88: F444-6.
103. Nicaise C, Gire C, Casha P, dErcole C, Chau C, Palix C. Erythropoietin as treatment for late hyporegenerative anemia in neonates with Rh hemolytic disease after in utero exchange transfusion. Fetal Diagn Ther 2002; 17: 22-4.
104. Vaughan JL, Manning M, Warwick RM, Letsky EA, Murray NA, Roberts IA. Inhibition of erythroid progenitor cells by anti-Kell antibodies in fetal alloimmune anemia. N Engl J Med 1998; 338: 798-803.
105. Dhodapkar KM, Blei F. Treatment of hemolytic disease of the newborn caused by anti-Kell antibody with recombinant erythropoietin. J Pediatr Hematol Oncol 2001; 23: 69-70.
106. Rendo P, Freigeiro D, Barboni G, Donato H, Drelichman G, Gonzalez A. A multicenter, randomized, double-blind trial with recombinant human erythropoietin (rHuEPO) in anemic HIV-infected children treated with antiretrovirals. Intern J Pediatr Hematol Oncol 2001; 7: 235-9.
107. Caselli D, Maccabruni A, Zucoti GV, et al. Recombinant erythropoietin for treatment of anaemia in HIV-infected children. AIDS 1996; 10: 929-31.
108. Le Chenadec J, Mayaux MJ, Guihenneuc-Jouyaux C, Blanche S for the Enquete Perinatale Francaise Study Group. Perinatal antiretroviral treatment and hematopoiesis in HIV-uninfected infants. AIDS 2003; 17: 2053-61.
109. Lux SE, Palek J. Disorders of the red cell membrane. En: Handin RI, Stosel TP, Lux SE (eds). Blood: Principles and Practice of Hematology. Philadelphia: J. B. Lippincot, 1995, p 1701-95.
110. Delhommeau F, Cynober T, Schischmanoff P, Rohrlich P, Delaunay J, Tchernia G. Hereditary spherocytosis during the first year of life: natural history and transfusion need. Blood 2000; 95: 393-9.
111. Tchernia G, Delhommeau F, Perrotta S, et al. Recombinant erythropoietin therapy as an alternative to blood transfusions in infants with hereditary spherocytosis. Hematol J 2001; 1: 146-52.
112. Kayemba-Kayss S, Christin P, Yahouanc-Lapalle H, Oriot D. Anémie néonatale par incompatibilité rhésus traitée par érythropoiétine. Arch Pediatr 2004; 11: 868-9.
113. Knight K, Wade S, Balducci L. Prevalence and outcomes of anemia in cancer: A systematic review of the literature. Am J Med 2004; 116: 11S-26S.
114. Michon J. Incidence of anemia in pediatric cancer patients in Europe: results of a large, international survey. Med Pediatr Oncol 2002; 39: 448-50.
114b. Ludwig H, Barrett-Lee PJ, Gascon P, Scneider M, Van Belle S. European Cancer Anemia Survey (ECAS) defines factors surrounding anemia in thousands cancer patients. Proc Am Soc Clin Oncol 2002; 21: 387(a)
115. Ferrario E, Ferrari L, Bidoli P, et al. Treatment of cancer-related anemia with epoetin alfa: a review. Cancer Treat Rev 2004; 30: 563-75.
116. Bokemeyer C, Oechsle K, Hartmann JT. Treatment-induced anaemia and its potential clinical impact in patients receiving sequential high dose chemotherapy for metastatic testicular cancer. Br J Cancer 2002; 87: 1066-71.
117. Caro JJ, Salas M, Ward A. Anemia as an independent prognostic factor for survival in patients with cancer: A systematic, quantitative review. Cancer 2001; 91: 2214-21.
118. Aapro M, San Miguel J. Evolving treatment strategies for anaemia in cancer: experience with epoetin beta. Oncology 2004; 67 (Suppl 1): 17-22.
119. Witzig TE, Silberstein PT, Loprinzi CL, et al. Phase III, randomized, double-blind study of epoetin alfa versus placebo in anemic patients with cancer undergoing chemotherapy. J Clin Oncol 2004; Sept 27: (Epub).
120. Demetri GD, Kris M, Wade J, Degos L, Cella D, for the Procrit Study Group. Quality-of-life benefit in chemotherapy patients treated with epoetin alfa is independent of disease response or tumor type: results from a prospective community oncology study. J Clin Oncol 1998; 16: 3412-25.
121. Gabrilove JL, Cleeland CS, Livingston RB, Sarokhan B, Winer E, Einhorn LH. Clinical evaluation of once-weekly dosing of epoetin alfa in chemotherapy patients: improvements in hemoglobin and quality of life are similar to three-times-weekly dosing. J Clin Oncol 2001; 19: 2875-82.
122. Littlewood TJ, Bajetta E, Nortier JW, Vercammen E, Rapoport B, for the Epoetin Alfa Study Group. Effects of epoetin alfa on hematologic parameters and quality of life in cancer patients receiving nonplatinum chemotherapy: results of a randomized, double-blind, placebo-controlled trial. J Clin Oncol 2001; 19: 2865-74.
123. Glaspy J, Bukowski R, Steinberg D, et al. Impact of therapy with epoetin alfa on clinical outcomes in patients with non-myeloid malignancies during cancer chemotherapy in community oncology practice. J Clin Oncol 1997; 15: 1218-34.
124. Shasha D, George MJ, Harrison LB. Once-weekly dosing of epoetin-alpha increases hemoglobin and improves quality of life in anemic cancer patients receiving radiation therapy either concomitantly or sequentially with chemotherapy. Cancer 2003; 98: 1072-9.
125. Quirt I, Robeson C, Lau CY. Epoetin alfa in patients not on chemotherapy - Canadian data. Semin Oncol 2002 29: 75-80.
126. Quirt I, Robeson C, Lau CY. Epoetin alfa therapy increases hemoglobin levels and improves quality of life in patients with cancer-related anemia who are not receiving chemotherapy and patients with anemia who are receiving chemotherapy J Clin Oncol 2001;19: 4126-34.
127. National Comprehensive Cancer Network: Clinical Practice Guidelines in Oncology, v.2.2004. Cancer and treatment-related anemia. Disponible en: http://www.enccn.com/professionals/physician_gls/PDF/anemia.pdf
128. Rizzo JD, Lichtin AE, Woolf SH, et al. Use of epoetin in patients with cancer: evidence-based clinical practice guidelines of the American Society of Clinical Oncology and the American Society of Hematology. J Clin Oncol 2002; 20: 4083-107.
129. Bokemeyer C, Aapro MS, Courdi A, et al. EORTC guidelines for the use of erythropoietic proteins in anaemic patients with cancer. Eur J Cancer 2004; 40: 2201-16.
129b. Rosberg J, Lefebvre P, Fastenau J. Clinical significance of a >1 gram/deciliter (g/dL) rise in hemoglobin (Hb) at week 4 (early response) or at week 8 during epoetin alfa (EPO) treatment. Blood 2003; 102 (abstract 2777).
130. Henry DH, Abels RI. Recombinant human erythropoietin in the treatment of cancer and chemotherapy-induced anemia: Results of double-blind and open-label follow-up studies. Semin Oncol 1994; 21: 21-8.
131. Cella D, Zagari MJ, Vandoros C et al. Epoetin alfa treatment results in clinically significant improvements in quality of life in anemic cancer patients when referenced to the general population. J Clin Oncol 2003; 21: 366-73.
132. Cazzola M, Messinger D, Battistel V, et al. Recombinant human erythropoietin in the anemia associated with multiple myeloma or non-Hodgkins Lymphoma: dose finding and identification of predictors of response. Blood 1995; 86: 4446-53.
133. Cazzola M, Beguin Y, Kloczko J, Spicka I, Coiffier B. Once-weekly epoetin beta is highly effective in treating anaemic patients with lymphoproliferative malignancy and defective endogenous erythropoietin production. Br J Haematol 2003; 122: 386-93.
134. Lastiri J M, Specterman S, Rendo P, Pallotta MG, Varela M, Goldztein S. Variables predictivas de respuesta a la eritropoyetina recombinante humana en pacientes con anemia y cáncer. Medicina (Buenos Aires) 2002; 62: 41-7.
135. Beguin Y. Prediction of response and other improvements on the limitations of recombinant human erythropoietin therapy in anemic cáncer patients. Haematologica 2002; 87: 1209-21.
136. Littlewood TJ, Zagari M, Pallister C, Perkins A. Baseline and early treatment factors are not clinically useful for predicting individual response to erythropoietin in anemic cancer patients. Oncologist 2003; 8: 99-107.
137. Feusner J, Hastings C. Recombinant human erythropoietin in pediatric oncology: a review. Med Pediatr Oncol 2002; 39: 463-8.
138. Parsons SK. Oncology practice patterns in the use of hematopoietic growth factors. Curr Opin Pediatr 2000; 12: 10-7.
139. Yilmaz D, Cetimgul N, Kantar M, Oniz H, Kansoy S, Kavakli K. A single institutional experience: is epoetin alpha effective in anemic children with cancer? Pediatr Hematol Oncol 2004; 21: 1-8.
140. Zoubek A, Kronberger M. Early epoetin alfa treatment in children with solid tumours. Med Pediatr Oncol 2002; 39: 459-62.
141. Buyukpamukcu M, Varan A, Kutluk T, Akyuz C. Is epoetin alfa a treatment option for chemotherapy-related anemia in children? Med Pediatr Oncol 2002; 39: 455-8.
142. Kronberger M, Fischmeister G, Poertschger U, Gadner H, Zoubek A. Reduction in transfusion requirements with early epoetin alfa treatment in pediatric patients with solid tumors: a case-control study. Pediatr Hematol Oncol 2002; 19: 95-105.
143. Wagner LM, Billups CA, Furman WL, Rao NB, Santana VM. Combined use of erythropoietin and granulocyte colony-stimulating factor does not decrease blood transfusion requirements during induction therapy for high-risk neuroblastoma: a randomized controlled trial. J Clin Oncol 2004; 22: 1886-93.
143b.Razzouk BI, Hockenberry M, Hinds PS, Feusner J, Rackoff W, Hord JD. Influence of hemoglobin response to epoetin alfa on quality of life in anemic children with cancer receiving myelosuppressive chemotherapy. Blood 2004; 104: 609 (abstract 2218)
144. Bohlius J, Langensiepen S, Schwrzer G, et al. Erythropoietin for patients with malignant disease (Cochrane Review). En: The Cochrane Library, Issue 3. Chichester: John Wiley & Sons, 2004.
145. Henke M, Laszig R, Rube C, et al. Erythropoietin to treat head and neck cancer patients with anaemia undergoing radiotherapy: randomised, double-blind, placebo-controlled trial. Lancet 2003; 362: 1255-60.
146. Leyland-Jones B, BEST Investigators and Study Group. Breast cancer trial with erythropoietin terminated unexpectedly. Lancet Oncol 2003; 4: 459-60.
147. Ribatti D, Marzullo A, Nico B, Crivellato E, Ria R, Vacca A. Erythropoietin as an angiogenic factor in gastric carcinoma. Histopathology. 2003; 42: 246-50.
148. Arcasoy MO, Amin K, Karayal AF, et al. Functional significance of erythropoietin receptor expression in breast cancer. Lab Invest 2002; 82: 911-8.
149. Batra S, Perelman N, Luck LR, Shimada H, Malik P. Pediatric tumor cells express erythropoietin and a functional erythropoietin receptor that promotes angiogenesis and tumor cell survival. Lab Invest 2003; 83: 1477-87.
150. Yasuda Y, Fujita Y, Matsuo T, et al. Erythropoietin regulates tumour growth of human malignancies. Carcinogenesis 2003; 24: 1021-29.
151. Sullivan PS, Hanson DL, Chu SY, et al. Epidemiology of anemia in human immunodeficiency virus (HIV)-infected persons: results from the multistate adult and adolescent spectrum of HIV disease surveillance project. Blood 1998; 91: 301-8.
152. Belperio PS, Pharm D, Rhew DC. Prevalence and outcomes of anemia in individuals with human immunodeficiency virus: A systematic review of the literature. Am J Med 2004; 116: 27S-43S.
153. Mocroft A, Kirk O, Barton SE, et al. Anaemia is an independent predictive marker for clinical prognosis in HIV-infected patients across Europe. AIDS 1999; 13: 943-50.
154. Buskin SE, Sullivan PS. Anemia and its treatment and outcomes in persons infected with human immunodeficiency virus. Transfusion 2004; 44: 826-32.
155. Lundgren JD, Mocroft A, Gatelli JM, et al. A clinically prognostic scoring system for patients receiving highly active antiretroviral therapy: results from the EuroSIDA Study. J Infect Dis. 2002; 185: 178–87.
156. Henry DH, Beall GN, Benson CA, et al. Recombinant human erythropoietin in the treatment of anemia associated with human immunodeficiency virus (HIV) infection and zidovudine therapy: overview of four clinical trials. Ann Intern Med 1992; 117: 739-48.
157. Levine AM. Anemia in the setting of cancer and human immunodeficiency virus. Clin Infect Dis 2003; 37: S304-14.
158. Grossman HA, Goon B, Bowers P, Leitz G. 010 Study Group. Once-weekly epoetin alfa dosing is as effective as three times-weekly dosing in increasing hemoglobin levels and is associated with improved quality of life in anemic HIV-infected patients. J Acquir Immune Defic Syndr 2003; 34: 368-78.
159. Saag MS, Bowers P, Leitz GJ, Levine AM; Community HIV Anemia Management Protocol Sites (CHAMPS) Study Group. Once-weekly epoetin alfa improves quality of life and increases hemoglobin in anemic HIV+ patients. AIDS Res Hum Retroviruses 2004; 20: 1037-45.
160. Abrams DI, Steinhart C, Frascino R. Epoetin alfa therapy for anaemia in HIV-infected patients: impact on quality of life. Int J STD AIDS. 2000; 11: 659–65.
161. Phair JP, Abels RI, McNeill MV, Sullivan DJ. Recombinant human erythropoietin treatment: investigational new drug protocol for the anemia of the acquired immunodeficiency syndrome. Ach Intern Med 1993; 153: 2669-75.
162. Balfour HH. Recombinant human erythropoietin for treatment of anemia in persons with AIDS not receiving zidovudine. Int J Antimicrob Agents 1997; 8: 189-92.
163. McHutchison JG, Gordon SC, Schiff ER, et al. Interferon alfa-2b alone or in combination with ribavirin as initial treatment for chronic hepatitis C. Hepatitis Interventional Therapy Group. N Engl J Med. 1998 ; 339: 1485-92.
164. De Franceschi L, Fattovich G, Turrini F, et al. Hemolytic anemia induced by ribavirin therapy in patients with chronic hepatitis C virus infection: role of membrane oxidative damage. Hepatology 2000; 31: 997-1004.
165. Afdhal NH, Dieterich DT, Pockros PJ, et al. Epoetin alfa mantains ribavirin dose in HCV-infected patients: A prospective, double-blind, randomized controlled study. Gastroenterology 2004; 126: 1302-11.
166. Corwin HL, Surgenor SD, Gettinger A. Transfusion practice in the critically ill. Crit Care Med 2003 (Suppl): S668-71.
167. Corwin HL, Gettinger A, Pearl RG, et al. Efficacy of recombinant human erythropoietin in critically ill patients: a randomized controlled trial. JAMA 2002; 288: 2827-35.
168. Juul SE. Recombinant erythropoietin as a neuroprotective treatment: in vitro and in vivo models. Clin Perinatol 2004; 31: 129-42.
169. Ghezzi P, Brines M. Erythropoietin as an antiapoptotic tissue-protective cytokine. Cell Death Differ 2004; 11: S37-44.
170. Dame C, Juul SE, Christensen RD. The biology of erythropoietin in the central nervous system and its neurotrophic and neuroprotective potential. Biol Neonate 2001; 79: 228-35.
171. Genc S, Koroglu TF, Genc K. Erythropoietin and the nervous system. Brain Res 2004; 1000: 19-31.
172. Cerami A. Beyond erythropoiesis: Novel applications for recombinant human erythropoietin. Semin Hematol 2001; 38: S33-9.
173. Marti HH. Erythropoietin and the hypoxic brain. J Exp Biol 2004; 207: 3233-42.
174. Bernaudin M, Marti HH, Roussel S, et al. A potential role for erythropoietin in focal permanent cerebral ischemia in mice. J Cereb Blood Flow Metab 1999; 19: 643-51.
175. Buemi M, Allegra A, Corica F, et al. Intravenous recombinant erythropoietin does not lead to an increase in cerebrospinal fluid erythropoietin concentration. Nephrol Dial Transplant 2000; 15: 422-3.
176. Brines ML, Ghezzi P, Keenan S, et al. Erythropoietin crosses the blood-brain barrier to protect against experimenal brain injury. PNAS 2000; 97: 10526-31.
177. Juul SE, McPherson RJ, Farrell FX, Jollife L, Ness DJ, Gleason CA. Erythropoietin concentrations in cerebrospinal fluid of nonhuman primates and fetal sheep following high-dose recombinant erythropoietin. Biol Neonate 2004; 85: 138-44.
178. Ehrenreich H, Hasselblatt M, Dembowski C, et al. Erythropoietin therapy for acute stroke is both safe and beneficial. Mol Med 2002; 8: 495-505.
179. Kumral A, Ozer E, Yilmaz O, et al. Neuroprotective effect of erythropoietin on hypoxic-ischemic brain injury in neonatal rats. Biol Neonate 2003; 83: 224-8.
180. Sola A, Wen TC, Hamrick SEG, Ferriero DM: Potential for protection and repair following injury to the developing brain: a role for erythyropoietin? Pediatr Res 2005; 57: 110R-17R.
181. Calhoun DA, Christensen RD. Hematopoietic growth factors in neonatal medicine: the use of enterally administered hematopoietic growth factors in the neonatal intensive care unit. Clin Perinatol 2004; 31: 169-82.
182. Juul SE, Joyce AE, Zhao Y, et al. Why is erythropoietin present in human milk? Studies of erythropoietin receptors on enterocytes of human and rat neonates. Pediatr Res 1999; 46: 263-8.
183. Ledbetter DJ, Juul SE. Erythropoietin and necrotizing enterocolitis in the very low birth weight infant. Pediatr Surg 2000; 35: 178-82.
184. Britton J, Chistensen R. Enteral administration of recombinant erythropoietin to preterm infants. J Perinatol 1995; 15: 281-3.
185. Ballin A, Bilker-Reich A, Arbel E, Davidovitz Y, Kohelet D. Erythropoietin, given enterally, stimulates erythropoiesis in premature infants. Lancet 1999; 353: 1849.
186. Lima-Rogel V, Calhoun DA, Maheshwari A, et al. Tolerance of a sterile isotonic electrolyte solution containing select recombinant growth factors in neonates recovering from necrotizing enterocolitis. J Perinatol 2003; 23: 200-4.
187. Lewis LD. Preclinical and clinical studies: a preview of potential future applications of erythropoietic agents. Semin Hematol 2004; 41(suppl 7): 17-25.
188. Cournoyer D, Toffelmire EB, Wells GA, et al. Canadian PRCA Focus Group.: Anti-erythropoietin antibody-mediated pure red cell aplasia after treatment with recombinant erythropoietin products: recommendations for minimization of risk. J Am Soc Nephrol 2004; 15: 2728-34.
189. Bennett CL, Luminari S, Nissenson AR, et al. Pure red-cell aplasia and epoetin therapy. N Engl J Med 2004; 351: 1403-08.
190. Rossert J, Casadevall N, Eckardt KU: Anti-erythropoietin antibodies and pure red cell aplasia. J Am Soc Nephrol 2004; 15: 398-406.
191. Swanson SJ, Ferbas J, Mayeux P, Casadevall N: Evaluation of methods to detect and characterize antibodies against recombinant human erythropoietin. Nephron Clin Pract 2004; 96: c88-95.
192. Hoesel W, Gross J, Moller R, et al. Development and evaluation of a new ELISA for the detection and quantification of antierythropoietin antibodies in human sera. J Immunol Methods 2004; 294: 101-10.
193. Tacey R, Greway A, Smiell J, et al. The detection of anti-erythropoietin antibodies in human serum and plasma. Part I. Validation of the protocol for a radioimmunoprecipitation assay. J Immunol Methods 2003; 283: 317-29.
194. Mason S, La S, Mytych D, Swanson SJ, Ferbas J. Validation of the BIACORE 3000 platform for detection of antibodies against erythropoietic agents in human serum samples. Curr Med Res Opin. 2003; 19: 651-9.
195. Locatelli F, Aljama P, Barany P, et al. Erythropoiesis-stimulating agents and antibody-mediated pure red-cell aplasia: here are we now and where do we go from here? Nephrol Dial Transplant 2004; 19: 288-93.
196. Verhelst D, Rossert J, Casadevall N, Kruger A, Eckardt KU, Macdougall IC. Treatment of erythropoietin-induced pure red cell aplasia: a retrospective study. Lancet 2004; 363: 1768-71.
197. Duffield JS, Mann S, Horn L, Winney RJ. Low-dose cyclosporin therapy for recombinant erythropoietin-induced pure red-cell aplasia. Nephrol Dial Transplant 2004; 19: 479-81.
198. Snanoudj R, Beaudreuil S, Arzouk N, et al. Recovery from pure red cell aplasia caused by anti-erythropoietin antibodies after kidney transplantation. Am J Transplant 2004; 4: 274-7.
199. Macdougall IC, Roche A, Rossert J, Casadevall N, Francois P, Kemeny DM. Re-challenging patients who developed pure red cell aplasia with epoetin: can it be done? Nephrol Dial Transplant 2004; 19: 2901-5.
Recibido: 8-07-2005
Aceptado: 5-10-2005














