Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680versión On-line ISSN 1669-9106
Medicina (B. Aires) v.66 n.6 Buenos Aires nov./dic. 2006
Tratamiento del cáncer por captura neutrónica de boro. Su aplicación al carcinoma indiferenciado de tiroides
Mario A. Pisarev1,2, MarIa A. Dagrosa1, Lisa Thomasz1, Guillermo Juvenal1
1 División Bioquímica Nuclear, Centro Atómico Constituyentes, Comisión Nacional de Energía Atómica;
2 Departamento de Bioquímica Humana, Facultad de Medicina, Universidad de Buenos Aires
Dirección postal: Dr. Mario Pisarev, Departamento de Radiobiología, Centro Atómico Constituyentes, Av. General Paz 1499,1650 San Martín, Buenos Aires, Argentina. Fax: (54-11) 6772-7148
E-mail: pisarev@cnea.gov.ar
Resumen
El cáncer indiferenciado de tiroides es un tumor muy agresivo, de muy mal pronóstico y sin tratamiento efectivo. La terapia por captura neutrónica de boro (BNCT) podría ser una alternativa para el tratamiento de esta enfermedad. Se basa en la captación selectiva de boro por el tumor y su activación por un haz de neutrones. El boro activado libera un núcleo de litio-7 y una partícula alfa, las cuales tienen una alta transmisión linear de energía (linear energy transfer, LET) y un alcance de 5-9 µm, destruyendo el tumor. En estudios previos hemos mostrado que la línea celular humana de cáncer indiferenciado de tiroides (ARO) tiene una captación selectiva de borofenilalanina (10BPA) tanto in vitro como después de ser implantada en ratones NIH nude. También demostramos en estos animales inyectados con BPA e irradiados con un haz de neutrones térmicos, un 100% de control sobre el crecimiento tumoral y un 50% de cura histológica. En trabajos posteriores mostramos que la porfirina 10BOPP tetrakis-carborane carboxylate ester de 2,4-bis-(a,b-dihydroxyethyl)-deutero-porphyrin IX) cuando es inyectada 5-7 días antes que el BPA se obtiene una concentración tumoral de boro de aproximadamente el doble que el BPA solo (45-38 ppm vs. 20 ppm). La posterior irradiación con neutrones mostró un 100% de remisión completa en animales con tumores cuyo volumen pre-tratamiento era de 50 mm3 o menor. Los perros padecen CIT espontáneo, con un comportamiento biológico similar al humano, y una captación selectiva de BPA, abriendo la posibilidad de su tratamiento por BNCT.
Palabras clave: Tiroides; Boro; Neutrones; Cáncer
Abstract
Boron neutron capture therapy applied to undifferentiated thyroid carcinoma. Undifferentiated thyroid carcinoma (UTC) is an aggressive tumor with a poor prognosis due to the lack of an effective treatment. Boron neutron capture therapy (BNCT) is based on the selective uptake of boron by the tumor and its activation by a neutron beam, releasing lithium-7 and an alpha particle that will kill the tumor cells by their high linear energy transfer (LET). In previous studies we have shown a selective uptake of borophenylalanine (10BPA) in a human UTC cell line (ARO) and in NIH nude mice implanted with this cell line. When these animals were injected with BPA and irradiated with an appropriated neutron beam, we observed a 100% of tumor growth control and a 50 % of histological cure when the initial tumor volume was 50 mm3 or less. Further studies with BOPP (tetrakis-carborane carboxylate ester of 2,4-bis-(a, b-dihydroxyethyl)-deutero-porphyrin IX) showed that when this porphyrin was injected 5-7 days before BPA, and the animals were sacrificed 60 min after the i.p. injection of BPA, a significant increase in boron uptake by the tumor was found (45-38 ppm with both compounds vs. 20 ppm with BPA alone). The application of BNCT using the combination of boron compounds showed a 100% of complete remission in tumors with initial volumes under 50 mm3. Dogs suffer spontaneous UTC, with a similar biological behavior to the human tumor, and a selective uptake of BPA. These results open the possibility of applying BNCT to UTC.
Key words: Thyroid; Boron; Neutrons; Cancer
¿Qué es la terapia por captura neutrónica de boro?
La terapia por captura neutrónica de boro (Boron Neutron Capture Therapy, BNCT) es una modalidad de tratamiento binario que brinda una manera de destruir selectivamente células tumorales sin dañar al tejido normal circundante. La misma se basa en las reacciones de captura nuclear y posterior fisión que ocurren cuando, luego de la administración de compuestos borados, el boro-10 (10B), isótopo natural no radiactivo del elemento boro, es irradiado con neutrones térmicos de baja energía (< 0.4 eV) para producir su activación a 11B, que decae liberando una partícula a (4He) y un núcleo de litio-7 en retroceso (7Li). Debido a que estas partículas de alto LET (Linear Energy Transfer) tienen un alcance limitado en el tejido (5-9 µm), sus efectos destructivos son limitados a las células que contienen boro1.
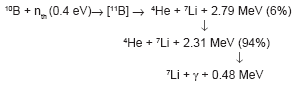
Para que este tratamiento resulte efectivo, se deben cumplir una serie de pautas:
1) la concentración de boro en el tumor en el momento de la irradiación tiene que estar en el rango entre 15 y 25 mg 10B/g de tejido (ppm).
2) la captación del compuesto de boro utilizado debería ser al menos tres veces mayor en el tumor que en la sangre y que en los tejidos normales circundantes.
3) la farmacocinética del compuesto, en cuanto a la persistencia de boro en el tumor, debe ser compatible con el tiempo necesario para completar la irradiación.
4) el compuesto borado usado no debe ser tóxico.
Aunque numerosos compuestos de boro han sido sintetizados, hasta el momento sólo dos de ellos han sido utilizados en ensayos clínicos, el di-sodio-undecahidro-mercapto-closo-dodecarborato (BSH) y la p-hidroxiboro-fenilalanina (BPA)2.
Por otro lado, en cuanto a los neutrones, el haz utilizado debe ser el apropiado. Debido a que la energía de los neutrones es atenuada en los tejidos, la energía inicial de los mismos debe ser suficiente para alcanzar el sitio del tumor con una energía menor a 0.4 eV. En este sentido, para tumores superficiales un haz de neutrones térmicos es suficiente, pero para tumores localizados profundamente en el cuerpo, se requiere un haz de neutrones epitérmicos con energías entre 0.4 eV y 10 KeV1, 2.
Otro aspecto importante a tener en cuenta es que el campo de radiación producido durante BNCT es muy complejo, una mezcla de componentes de alto y bajo LET. Además de la reacción de captura neutrónica en boro 10B (n, a) 7Li, otros elementos presentes en el tejido, en proporciones importantes, capturan neutrones. Estos elementos son el hidrogeno y el nitrógeno [1H (n, g) 2H y 14 N(n, p) 14C]. Además, en el haz hay también presentes radiación gamma y neutrones rápidos. Estos últimos colisionan con núcleos de hidrógeno y producen protones con una energía similar a la producida por la captura en nitrógeno. Por lo tanto la dosis física total absorbida será la suma de la dosis específica debida al boro y todas las demás contribuciones. Debida a que el haz de neutrones no puede ser colimado por sufrir dispersión en los tejidos, la dosis de neutrones a entregar al volumen del blanco, estará limitada por la tolerancia de los tejidos normales a la dosis inespecífica1, 2.
Esta terapia ha sido utilizada en ensayos clínicos realizados en diferentes centros nucleares de Japón, Europa, EE.UU. y Argentina para el tratamiento de gliomas de alto grado y melanomas cutáneos primario o metástasis de los mismos en cerebro3-7. Recientemente esta modalidad de tratamiento ha sido extendida al tratamiento de cáncer metastásico de hígado y a tumores de cabeza y cuello. Solamente los tumores que no tiene un tratamiento efectivo son incluidos en los protocolos.
Cáncer indiferenciado o anaplásico de tiroides
El cáncer anaplásico o indiferenciado de tiroides (CIT) es un tumor sólido muy agresivo con una mayor incidencia en mujeres. La edad habitual de los pacientes al momento del diagnóstico es de 57 a 67 años, con un rango de 15-90 años. En muchos casos el tumor se desarrolla a partir de un bocio establecido o en el contexto de un cáncer de tiroides diferenciado preexistente. El tumor primario puede producir metástasis en pulmón, hueso y cerebro, y en muchos pacientes causa disfagia y disnea o ambas, también puede causar adenopatías locales. La tiroidectomía total no es fácil de lograr y el mal pronóstico que tiene este carcinoma reside en que no capta iodo radiactivo y en que usualmente tiene una respuesta inadecuada a la quimioterapia o a la radioterapia. El tiempo de sobrevida media de los pacientes es menor a un año y la muerte puede ser causada por obstrucción de las vías respiratorias o por los efectos de las metástasis. Aunque los tratamientos convencionales a veces alivian los síntomas y prolongan la sobrevida, los efectos secundarios de estos tratamientos son importantes8, 9.
Otros tratamientos alternativos y novedosos están siendo ensayados. La rediferenciación con ácido retinoico ha sido propuesta como una alternativa10. Otra forma posible de tratamiento se basa en la terapia génica en las células tumorales transfectando el simporter iodo/sodio, logrando la recuperación de la capacidad de captar el radioiodo11. Al menos seis diferentes ensayos clínicos para CIT están siendo llevados a cabo en la actualidad12, 13. Además, se están realizando estudios para explorar la posibilidad de aplicar BNCT al tratamiento del CIT.
Biodistribución de compuestos de boro en el carcinoma indiferenciado de tiroides
Los primeros estudios fueron realizados en la línea humana de CIT (ARO). Los cultivos de células ARO con concentraciones crecientes de BPA mostraron que la captación de boro sigue una relación lineal dosis-respuesta y que las células ARO concentran cuatro y cinco veces más boro que las células bovinas normales y que las células de adenoma folicular tiroideo humano, respectivamente. La captación máxima de boro fue observada después de doce horas de incubación, y no se observó diferencia en la misma cuando las células estaban proliferando o en quiescencia14. Distintas explicaciones se han dado al porqué de la captación selectiva de BPA por parte de células tumorales. En un sentido amplio, esta incorporación elevada puede reflejar simplemente un metabolismo más activo de las células tumorales, como fue demostrado ampliamente en oncología para muchos tumores con el uso de 18F-deoxiglucosa. Mishima y col.15 demostraron que el BPA marcado con fluor-18 (18F-BPA) tiene una tasa de incorporación neta cuatro veces mayor en gliomas y melanomas que en los tejidos normales circundantes. El mecanismo de transporte de BPA fue analizado en una línea celular de gliosarcoma (GS-9L) y en la línea de fibroblastos (V79) por Wittig y col.16 y sus resultados apoyan la hipótesis de que el BPA es transportado por el sistema L de aminoácidos, un antiporter independiente de sodio cuya fuerza de movimiento es un gradiente químico de aminoácidos pre-acumulados en el interior de la célula.
La captación similar de BPA observada entre células quiescentes y células proliferando está de acuerdo con estudios realizados por Slatkin y col.17. quienes compararon la incorporación de BPA entre un hígado normal de rata y otro en regeneración con un índice de actividad mitótica similar al de un glioma. Los autores observaron que en ambos hígados la acumulación de boro era similar, siendo de tres a cuatro veces más baja que en el glioma.
Se desarrolló un modelo in vivo de CIT mediante la implantación subcutánea de células de la línea humana ARO en ratones nude del US National Institute of Health (NIH). El crecimiento del tumor fue muy rápido y en algunos animales se detectaron metástasis en pulmón, indicando que el modelo reproduce características del comportamiento biológico de tumores espontáneos en humanos18. Con este modelo animal se realizaron estudios de biodistribución del aminoácido borado BPA con dos distintas dosis: 350 y 600 mg/kg de peso corporal. Se observó una captación selectiva de BPA por el tumor con relaciones tumor/sangre, tumor/tiroides normal entre 3 y 5. Los estudios de farmacocinética realizados mostraron un pico de boro en el tumor a los 60 minutos con la dosis de 350 mg/kg y a los 90 minutos con la dosis de 600 mg/kg. Las concentraciones absolutas de boro fueron de 17-24 ppm dependiendo de la dosis de BPA administrada. Un dato importante de estos estudios de biodistribución y farmacocinética fue la elevada captación de boro por la piel circundante al tumor comparada a la piel distal al mismo. Los estudios histológicos realizados mostraron que la piel que rodea al tumor se halla infiltrada con células tumorales14. Estos datos son interesantes porque sugieren que BNCT puede ser usado para el tratamiento de toda la masa de CIT o como una terapia complementaria de la cirugía, con el objetivo final de destruir las células residuales infiltrantes.
Estudios posteriores fueron realizados con una porfirina borada, el 2,4-bis-(a, b-dihidroxyethyl)-deutero-porphyrin IX o BOPP. Este compuesto19 tiene 40 átomos de 10B/molécula comparado con el BPA, que sólo tiene un átomo de boro. El BOPP demostró una captación selectiva y una larga persistencia en gliomas en distintos modelos experimentales. El mecanismo de captación celular parece estar relacionado al receptor de la lipo-proteína de baja densidad LDL. Por otro lado, estudios de distribución subcelular mostraron que el BOPP se halla localizado en la fracción enriquecida en mitocondrias20-22.
Los primeros estudios de la porfirina borada en el modelo animal de CIT fueron muy desalentadores, ya que no mostraron una captación selectiva por el tumor a ninguna de las dos dosis estudiadas (10 y 100 mg/kg de peso corporal) por ninguna de las dos rutas de administración probadas (intraperitoneal y endovenosa), cuando los animales fueron sacrificados 24 horas más tarde. Sin embargo, cuando el BOPP fue inyectado en una dosis intermedia de 60 mg/kg de peso corporal y los animales sacrificados a tiempos variables (1-7 días) y 1 hora luego de la administración de BPA (350 mg/kg), se observó una concentración significativa de boro en el tumor. Cuando el BOPP fue administrado 5 días antes del BPA, la concentración de boro en el tumor alcanzó un valor de 45 ppm23, lo que duplica la concentración intra-tumoral de boro cuando se utiliza BPA solo.
Los perros padecen cáncer indiferenciado de tiroides en forma espontánea y su comportamiento biológico es similar al del CIT en humanos. Se realizaron estudios de biodistribución en animales de distintas razas en los cuales se practicó una tiroidectomía como tratamiento primario de la enfermedad. Estos estudios fueron realizados usando BPA como molécula transportadora de boro, el cual fue infundido (iv) durante 60 minutos previos a la cirugía. Se obtuvieron muestras de sangre durante todo el procedimiento y muestras de distintas áreas del tumor durante la operación. Las muestras tumorales fueron divididas en partes simétricas, utilizándose una de ellas para la medición del boro y la otra para evaluación histopatológica. La concentración de boro de todas las áreas tumorales fue variable entre los distintos individuos, con relaciones tumor/sangre que estuvieron entre 2 y 6 y con variaciones intra-individuales entre 0.33 y 10.48. Tanto las variaciones entre individuos como aquellas observadas en un mismo perro pudieron ser explicadas por los estudios histológicos que mostraron dos patrones bien distintos de tumor: por un lado un tumor con homogeneidad celular y activo crecimiento y por el otro un tumor heterogéneo con regiones tumorales separadas por columnas de tejido conectivo. En este último tipo de tumor se observaron áreas de necrosis, hemorragia y de tejido adiposo. El número de células tumorales viables en cada muestra del tumor fue variable y mostró una correlación positiva con su concentración de boro24.
Tratamiento del cáncer indiferenciado de tiroides por la terapia por captura neutrónica de boro
Grupos de ratones nude transplantados con células de CIT humano (ARO) fueron tratados por la técnica completa de BNCT en el reactor nuclear RA-6 (Centro Atómico Bariloche). Los animales fueron inyectados con BPA y luego irradiados con un haz de neutrones epitérmicos termalizado. En el 100% de los animales se observó un completo control del crecimiento del tumor durante el primer mes post-tratamiento. Cuando sólo se tuvo en cuenta el subgrupo de animales con tumores de un tamaño inicial igual o menor a 50 mm3 se observó la regresión completa del tumor (cura histológica) en el 50% de los ratones irradiados, luego de la administración de cualquiera de las dos dosis de BPA (350 y 600 mg/kg)25. Los cálculos dosimétricos realizados mostraron que los tumores más pequeños recibieron, con el mismo flujo de neutrones e irradiados durante el mismo tiempo, una fluencia de neutrones mayor y una componente de radiación gamma menor. En estos estudios, el daño al ADN tumoral fue analizado por la técnica del cometa inmediatamente después de la irradiación y mostró una correlación positiva entre éste y la dosis física total absorbida25. Es sabido que el daño al ADN inducido por la radiación y la capacidad de la célula de repararlo depende de la calidad de la radiación. En este sentido, la radiación de alto LET (partículas alfa y núcleos de litio) es más efectiva biológicamente que la radiación de bajo LET (radiación gamma o rayos X) por causar lesiones en el ADN más complejas y difíciles de reparar por los sistemas de reparación de las células26.
En estudios adicionales, la irradiación fue realizada en ratones inyectados con BOPP más BPA. Dentro del marco de un estudio de escalada de la dosis física total, en una primera irradiación los resultados obtenidos no fueron mejores que aquellos logrados con la administración del BPA solo como transportador de boro27. En una segunda irradiación, en la cual la dosis física total fue aumentada en un 50% respecto a las dosis previas, se consiguió un 100% de cura histológica en ratones con tumores con un volumen inicial igual o menor a 50 mm3. Mientras se observó un 100% de control sobre el crecimiento del tumor durante el primer mes de seguimiento (Dagrosa y col., en preparación).
Perspectivas futuras
Estos resultados son alentadores y abren la posibilidad de aplicar el BNCT al tratamiento del CIT en humanos. Antes de que este objetivo sea intentado varias preguntas deberían ser contestadas.
1) ¿La captación selectiva de los compuestos de boro en los modelos animales de CIT se confirma para el tumor en humanos? Para responder esta pregunta estamos iniciando estudios de biodistribución en pacientes, con autorización de la ANMAT. Otro estudio similar está siendo realizado en Alemania (A. Wittig, comunicación personal).
2) ¿Es posible irradiar el cuello de un paciente sin dañar significativamente a las estructuras normales circundantes, como la tráquea, el esófago y los vasos sanguíneos? Para responder esta pregunta, planeamos irradiar perros con CIT espontáneo y de esta manera evaluar el efecto de BNCT en estas estructuras del cuello. Para reducir el daño de BNCT a estas estructuras vitales, son posibles dos alternativas: 1) realizar primero una tiroidectomía total y luego BNCT del tejido residual, irradiando con bajas dosis; 2) aplicar BNCT a la masa del tumor directamente.
3) ¿Pueden ser tratadas las metástasis de CIT en pulmón? Si bien no todos los tumores anaplásicos producen metástasis, para responder esta pregunta es necesaria información respecto a la tolerancia del pulmón normal al haz de neutrones28. Con respecto a las metástasis en cerebro, la amplia experiencia previa en estudios realizados en glioblastoma han mostrado que es posible irradiar el cerebro sin daños graves en los tejidos normales.
Recientemente se ha realizado una primera aplicación de BNCT al cáncer de tiroides en Japón. El paciente fue un hombre mayor de 71 años de edad con un adenocarcinoma papilar no operable. El 17 de septiembre de 2004, el hombre recibió una infusión de BPA y fue irradiado con un haz de neutrones. Cuatro meses más tarde, la tomografía computada mostró una importante disminución del tamaño y la histología reveló grandes áreas de necrosis. No se observaron efectos adversos en la piel, cavidad oral o pulmón. Una tomografía realizada en mayo del 2005 mostró una disminución en la captación de 18F-2-deoxi-glucosa por el tumor comparada con aquella previa a la irradiación. Hasta la fecha el paciente se mantiene estable, sin signos de progresión (Comunicación personal de J. Hiratsuka).
Agradecimientos: Los autores agradecen a la CNEA, ANPCYT y al CONICET por la ayuda económica y al Departamento de Energía de los EE.UU. por el apoyo a las visitas de expertos a nuestro laboratorio durante las primeras etapas del proyecto. Asimismo se agradece a los profesionales que participaron en las diferentes etapas de los estudios propios, Dres. M. Viaggi, R. Garavaglia, R. Jiménez Rabagliati, D. Batistoni, J. Longhino, H. Blaumann, O. Calzetta, R.L. Cabrini, S. Castiglia, V. Castillo, S. Kahl.
Bibliografía
1. Coderre JA, Morris G. The radiation biology of boron neutron capture. Radiat Res 1999; 151: 1-18.
2. Barth RF, Soloway AH, Pisarev MA. Terapia por captura neutrónica en boro (BNCT) en tumores de cerebro: estado actual y potencial futuro. Oncología 1998; 21: 387-99.
3. Hideghethy K, Sauerwein W, Wittig A, et al. Tissue uptake of BSH in patients with glioblastoma in the EORTC 11961 phase I BNCT trial. J Neuro-Oncology 2003; 62: 135-44.
4. Busse PM, Harling OK, Palmer WS, et al. A clinical examination of the results of the Harvard MIT NCT program phase I clinical trial of neutron capture therapy for intracranial disease. J Neuro-Oncology 2003; 62: 101-9.
5. Capala, J, Stenstam BH, Skold PM, et al.Boron neutron capture therapy for glioblastoma multiforme: clinical studies in Sweden. J of Neuro-Oncology 2003; 62: 135-45.
6. González SJ, Bonomi MR, Santa Cruz GA, et al. First BNCT treatment of a skin melanoma in Argentina: Dosimetric analysis and clinical outcome. Applied Radiation and Isotopes 2004; 61: 1101-5.
7. Barth R, Coderre J, Vicente G, Blue T. Boron neutron capture therapy of cancer: current status and future prospects. Clin Cancer Res 2005; 11:3987-4002.
8. Ain KB. Anaplastic thyroid carcinoma: behavior, biology, and therapeutic approaches. Thyroid 1998; 8: 715-26.
9. Pasieka JL. Anaplastic thyroid cancer. Current opinion in Oncology 2003; 15: 78-83.
10. Schmutzler C, Koehrle J. Retinoic acid redifferentiation therapy for thyroid cancer. Thyroid 2002; 10: 393-406.
11. Schmutzler C, Koehrle J. Innovative strategies for the treatment of thyroid cancer. Eur J of Endocrinol 2000; 143: 15-24.
12. Friedman T. Overcoming the obstacles to gene therapy. Scientifics American 1997; 276: 96-101.
13. Baléese RM. Gene therapy for cancer. Scientific American 1997; 276: 111-5.
14. Dagrosa MA, Viaggi ME, Kreimann E, et al. Selective uptake of p-borophenylalanine by undifferentiated thyroid carcinoma for boron neutron capture therapy. Thyroid 2002; 12: 7-12.
15. Mishima Y, Imahori Y, Honda C, Hiratsuka J, Ueda S, Ido T. In vivo diagnosis of human melanoma with positron emission tomography using specific melanoma-seeking 18F-DOPA analogue. J Neurooncology 1997; 33: 163-9.
16. Wittig A, Sauerwein WA, Coderre JA. Mechanisms of transport of p-borono-phenylalanine trough the cell membrane in vitro. Radiation Research 2000; 153: 173-80.
17. Slatkin DN, Nawrocky MM, Coderre JA, et al. Boron concentration in rat tissues after partial hepatectomy and a single injection of L-BPA/fructose complex. En: Advances in Neutron Capture Therapy. Larsson B., Crawford J., Weinreich R (eds). Amsterdan: Elsevier, pp. 223-229, 1997.
18. Viaggi M, Dagrosa MA, Gangitano D, et al. A new animal model human for undifferentiated thyroid carcinoma in a nude mice. Thyroid 2003; 13: 529-36.
19. Kahl SB, Koo MS. Synthesis and properties of tetrakiscarborane-carboxylate esters of 2, 4-bis (-dihy-droxyethyl ) deuteroporphyrin IX. En: Progress in Neu-tron Capture Therapy for Cancer. Allen BJ, Moore DE, Harrington BV (eds). New York: Plenum Press, pp. 223-226, 1992.
20. Hill JS, Kahl SB, Kaye A, et al. Selective tumor uptake of a boronated porphyrin in an animal model of cerebral gliomas. Proc Natl Acad Sci USA 1992; 89: 1785-9.
21. Ceberg CP, Brun A, Kahl SB, et al. A comparative study on the pharmacokinetics and biodistribution of boronated porphyrin (BOPP) and sulfhydril boron hydride (BSH) in the RG2 rat gliomas model. J Neurosurg 1995; 83: 86-92.
22. Callahan DE, Forte T, Afzal J, et al. Boronated protoporphyrin (BOPP): localization in lysosomes of the human glioma cell line SF-767 with uptake modulated by lipoprotein levels. Int J Radiat Oncol Biol Phys 1999; 45: 761-71.
23. Dagrosa MA, Viaggi M, Jiménez Rebagliati R, et al. Biodistribution of boron compounds in a animal model of undifferentiated thyroid cancer for boron neutron capture therapy. Molecular Pharmaceutic 2005; 2: 152-6.
24. Dagrosa MA, Viaggi M, Jiménez Rebagliati R, et al. Biodistribution of p-borophenylalanine (BPA) in dogs with spontaneous undifferentiated thyroid carcinoma (UTC). Appl Radiat and Isot 2004; 61: 911-5.
25. Dagrosa MA, Viaggi ME, Longhino J, et al. Experimental application of boron neutron capture therapy (BNCT) to undifferentiated thyroid carcinoma (UTC). Int J Radiat Oncol Biol Phys. 2003; 57: 1084-92.
26. Rydberg B. Clusters of DNA damage induced by ionizing radiation: formation of short DNA fragments. II. Experimental detection. Radiat Res 1996;145: 200-9.
27. Viaggi M, Dagrosa MA, Longhino J, et al. Boron neutron capture therapy for undifferentiated thyroid carcinoma: preliminary results with the combined use of BPA and BOPP. Appl Radiat and Isot 2004; 61: 905-9.
28. Kiger JL, Kiger WS, Patel H, et al. Effects of boron neutron capture irradiation on the normal lungs of rats. Appl Radiat Isot 2004; 61: 969-73. [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ]
Recibido: 9-01-2006
Aceptado: 24-04-2006














