Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680versión On-line ISSN 1669-9106
Medicina (B. Aires) v.67 n.1 Buenos Aires ene./feb. 2007
Una variedad genética de la UDP-glucuronosil transferasa asociada a toxicidad gastrointestinal por irinotecan
Matías Valsecchi1, 2, Juan Garberi1, Silvia Ferrandini3, Roxana Berenguer3, Ernesto Trini1, Pedro Politi4, 5
1Laboratorio de Biología y Patología Molecular;
2Hospital Fernández;
3Hospital de Clínicas José de San Martín;
4Cancerteam Equipo Interdisciplinario de Oncología;
5Segunda Cátedra de Farmacología, Universidad de Buenos Aires
Dirección Postal: Dr. Matías Valsecchi, Marcelo T. de Alvear 2010, 1122 Buenos Aires, Argentina. Fax: (54-11) 4961-5868
e-mail: meval78@yahoo.com
Resumen
Los avances en genética y biología molecular han impulsado la aparición de nuevas áreas de estudio en la medicina, como la farmacogenómica, la cual intenta predecir la respuesta y toxicidad a drogas en función de la variabilidad genética de cada individuo, constituyendo los llamados síndromes fármacogenómicos. La oncología podría beneficiarse debido a la gran toxicidad de sus fármacos. Hay varios loci genéticos que se están analizando por su potencial valor predictivo y hasta ahora sólo tres de ellos demostraron cierto grado de utilidad clínica. En especial, el estudio del número de repeticiones del dinucleótido timina-adenina (TA) en el promotor de la enzima UDP-glucuronosil-transferasa (UGT) mostró ser capaz de predecir neutropenia severa en pacientes expuestos a dosis intermedias y altas de irinotecan. Comunicamos el caso de una paciente con cáncer de pulmón de células pequeñas que padeció toxicidad hematológica y gastrointestinal grave tras haber sido tratada con dosis relativamente bajas (65 mg/m2) de irinotecan, y en quien un análisis del ADN leucocitario mostró la presencia de homocigosis para siete repeticiones de TA. Este caso es un ejemplo de aplicabilidad clínica del test, se discute su utilidad como predictor de toxicidad y la conducta a tomar frente a pacientes con estas características.
Palabras clave: Irinotecan; Farmacogenómica; UGT 1A1; TA indel
Abstract
A prevalent genetic variety of UDP-glycuronosyl transferase predicts high risk of irinotecan toxicity. The advances in genetics and molecular biology have raised new areas in medicine, such as pharmacogenomics, which tries to predict drug responses and toxicities based on the individual genetic variability, describing the so called: pharmacogenomic syndromes. Oncology would find this development extremely useful because of the severe toxicity of chemotherapy. There are a lot of genetic loci under investigation for their potential in predicting drug toxicity, but only three of them have showed clinical usefulness up to now. In particular, quantification of the number of thymine-adenine (TA) dinucleotics in the promoter region of the UDP-glucuronosyl-transferase 1A1 enzime (TA indel) proved to be capable of predicting severe neutropenia in patients exposed to intermediate or high doses of irinotecan. Herein we report a case of a patient with small cell lung cancer who suffered severe hematological and gastrointestinal toxicity after being treated with relatively low doses (65 mg/m2) of irinotecan and whose leucocyte DNA analysis showed the presence of seven TA repetitions in both alleles. This case is an example of the clinical applicability and the utility of the test as a toxicity predictor. We also discuss the clinical decisions that may be taken with these patients.
Key words: Irinotecan; Pharmacogenomics; UGT 1A1; TA indel
Irinotecan es hoy parte del tratamiento estándar del cáncer de colon o recto avanzados1, y ha probado ser eficaz y seguro en combinación con cisplatino en cáncer de pulmón de células pequeñas2. Desafortunadamente, entre el 20 y el 30% de los pacientes tratados con la droga experimentan toxicidad grave gastrointestinal o hematológica. Hasta hace poco tiempo era imposible detectar estos pacientes antes de la administración de la droga. Sin embargo, esta situación ha cambiado desde que se conocieron los resultados del primer estudio prospectivo que mostró una asociación estadísticamente significativa entre un tipo de variante genética de la enzima hepática UGT 1A1 y la presencia de neutropenia grave en pacientes que recibieron esta droga3.
Caso clínico
Paciente de sexo femenino de 50 años de edad, tabaquista importante, quien en el año 2005 fue diagnosticada con cáncer de pulmón de células pequeñas, estadio avanzado, con adenopatías mediastinales positivas confirmadas por mediastinoscopia, no plausible de recibir tratamiento quirúrgico, por lo cual comenzó quimioterapia con etopósido y cisplatino más radioterapia torácica concurrente. La paciente presentó reacción tipo anafiláctica durante la administración del etopósido en el primer ciclo, hecho que se repitió durante el segundo ciclo. Por el riesgo de muerte asociado a este tipo de reacción se decidió rotar el esquema de quimioterapia por cisplatino (100 mg/m2) más irinotecan (65 mg/m2) de acuerdo con lo publicado por Noda y col.4 para enfermedad avanzada. Horas después de la administración de estas drogas la paciente desarrolló toxicidad gastrointestinal grave, caracterizada por episodios de más de 15 deposiciones diarias y cólicos intestinales, por lo cual debió ser internada y recibir hidratación endovenosa, atropina, loperamida, bismuto y otros cuidados estándares. Simultáneamente la paciente presentó neutropenia (polimorfonucleares < 100 cel/ml), trombocitopenia (< 20.000 cel/ml) y anemia, requiriendo tratamiento con factores estimulantes de colonias y transfusiones. Teniendo en cuenta que la paciente fue expuesta a dosis relativamente bajas de irinotecan, así como su necesidad de continuar recibiendo quimioterapia, se decidió estudiar su ADN con el objeto de determinar si la misma era portadora de homocigosis para la variante genética de la enzima hepática UGT 1A1 que posee siete repeticiones del dinucleótido timinaadenina en su región promotora conocida como "TATAA Box". Para ello se le extrajo sangre periférica, se aisló el ADN leucocitario y se amplificó una pequeña porción del mismo a través de la reacción en cadena de la polimerasa (PCR) utilizando cebadores localizados a los extremos de la región donde se encuentran los dímeros de TA de esta enzima. Los fragmentos, productos de la PCR, fueron analizados en un equipo llamado GenScan Abi 310 Genetic Analizer. El mismo, básicamente, realiza una electroforesis capilar y analiza el tiempo que tarda el fragmento amplificado, -el cual posee una marca fluorescente-, en ser detectado por un sensor; y se compara ese tiempo, llamado tiempo de retención, con el tiempo de un fragmento patrón, que posee otra marca fluorescente y cuyo número exacto de bases es conocido. Para el análisis de estos datos se utilizó el software Genescan (Applied Biosystems, EE.UU.) que determina el tamaño del producto y que permitió conocer el número de repeticiones TA que posee la muestra de la paciente. Este mismo procedimiento es el que se utiliza, por ejemplo, para detectar el número de tripletes que posee el gen que origina la enfermedad de Huntington. En nuestro caso en particular, se utilizaron además dos muestras, provenientes de otros dos individuos sin ninguna relación con la paciente, que fueron usadas como muestras testigos. El objetivo de esto es demostrar que si al menos un individuo posee un alelo diferente, la variación se debe a dos pares de bases (o un múltiplo de dos), ya que los alelos se diferencian en el número de repeticiones de dímeros de TA.
Nuestro análisis demostró homocigosis de siete repeticiones en la paciente y en uno de los controles, mientras que el segundo control resultó ser homocigoto para 6 repeticiones del dinucleótido (Fig.1). La frecuencia alélica de nuestra población es hasta el momento desconocida, pero con los datos hasta ahora publicados de otras poblaciones, se podría estimar una frecuencia alélica de homocigosis para 7 repeticiones de entre 10 y 20%.
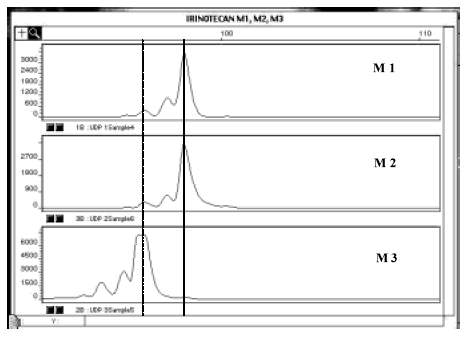
Fig. 1.- Análisis de fragmentos correspondientes a la región promotora de la enzima urididin-glucuronosin-transferasa de la paciente estudiada (M1) y de dos muestras testigos (M2, M3). En el eje de las abscisas se grafican fluorescencia en función el numero de pares de bases. M1 y M2 corresponden a homocigosis para el alelo TA7 (7 repeticiones TA) y M3 a homocigosis para el alelo TA6 (6 repeticiones).
Posteriormente, con esta información, se decidió reiniciar el segundo ciclo de cisplatino e irinotecan (cuarto ciclo total) reduciendo la dosis del irinotecan en un 20% y utilizando atropina, loperamida y carbón activado desde el primer día del ciclo. La paciente evolucionó con sólo 2 deposiciones diarias por tres días y mielotoxicidad menor. Posteriormente completó su esquema terapéutico con radioterapia holocraneana profiláctica. Presentó respuesta completa y se encuentra al momento de esta comunicación viva y libre de enfermedad.
Discusión
En el año 1995 se pudo explicar la fisiopatogenia del síndrome de Gilbert5, una enfermedad hereditaria de curso totalmente benigno y cuya prevalencia en la población caucásica es aproximadamente del 8%. El síndrome se debe, mayoritariamente, a que los afectados poseen dos copias, una en cada alelo, de una variante genética de la enzima UGT 1A1 que posee siete repeticiones del dímero TA en su región promotora, a diferencia de las 6 repeticiones normales. Los portadores de este haplotipo denominado 7/7, poseen una deficiencia relativa en la expresión y actividad de la UDP-glucuro-nosil-transferasa, hecho que se pone de manifiesto en un aumento de la bilirrubina indirecta frente a determinadas situaciones, siendo el ayuno la más conocida.
A partir del año 2000 diferentes investigadores comenzaron a comunicar, a través de reportes de casos y estudios retrospectivos, la asociación entre el haplotipo 7/7 y la toxicidad grave al irinotecan6. La utilidad clínica de detectar a los portadores homocigotos de esta variante genética, antes de recibir irinotecan, quedó demostrada en el trabajo de Innocenti y col.3, quienes tras analizar cinco variantes genéticas de la UGT 1A1, consideradas a priori como factores de riesgo, mostraron que sólo dos de ellas, el haplotipo 7/7 y el -3156 AA, se relacionaban en forma estadísticamente significativa con la toxicidad hematológica severa. Asimismo se evidenció que ninguno de los portadores del haplotipo 6/6 desarrollaron toxicidad. Con estos datos, Innocenti y col. concluyeron que el TA indel (cuantificación de la cantidad de repeticiones de TA) posee un valor predictivo positivo de 0.5 para toxicidad hematológica grave en aquellos portadores del haplotipo 7/7, y que la presencia de dos alelos normales (6/6) posee un valor predictivo negativo de 1.0 para toxicidad hematológica grave. Si bien la muestra fue pequeña y los resultados fueron criticados por algunos autores, la FDA aprobó el test a fines del 2005.
En ninguno de los estudios hasta aquí mencionados pudo demostrarse una asociación significativa entre el TA indel y la toxicidad gastrointestinal grave por irinotecan, probablemente por la baja incidencia descripta en ellos. Sin embargo, basándonos en la información publicada sobre la farmacocinética del irinotecan, nosotros creemos que la toxicidad gastrointestinal grave bien puede estar relacionada con la detoxificación anormal de la droga, por lo cual algunos pacientes que fuesen a sufrir diarrea grave también podrían ser detectados con el mismo análisis de TA indel.
El irinotecan es una prodroga que requiere ser metabolizada por reacciones hepáticas complejas que incluyen su oxidación por citocromo P450 3A4 y luego su activación por la carboxilesterasa 2 para la producción de la droga activa, el compuesto denominado SN-38. Este metabolito conserva las propiedades lipofílicas del irinotecan, y al igual que otros compuestos de esta naturaleza, para su eliminación requiere ser glucuroni-zado y luego excretado por la bilis. Existen pocas dudas de que el SN-38 es la molécula responsable tanto de los efectos deseados como nocivos del irinotecan. En el caso particular del tracto gastrointestinal, este compuesto podría producir sus efectos a través de dos rutas, sea por vía hematógena (sistémica) o por la vía directa (local) al ser secretado por la bilis. En concordancia con el efecto tóxico directo, podemos mencionar que el rol de la neomicina en la profilaxis secundaria de la toxicidad mediada por irinotecan se debe a su habilidad de inhibir la b-glucuronidasa bacteriana7, por lo cual parece lógico asumir que la incapacidad de glucuronizar al SN-38, como ocurre en las personas con fenotipo 7/7, resulte en una excesiva exposición de los enterocitos a la acción tóxica del SN-38.
Nuestro caso permite preguntarnos si el haplotipo 7/7 para el dinucleótido timina-adenina podría estar asociado a toxicidad grave, no sólo hematológica sino también gastrointestinal, aunque es claro que un solo caso no permite realizar ningún análisis minucioso o generalizar nuestro hallazgo. Al mismo tiempo, es razonable imaginar que otras diferencias genotípicas puedan determinar el metabolismo del irinotecan, aunque es escasa la información que se conoce hasta el momento. Futuros estudios, tal vez, aporten mayor claridad en este campo.
Por último, consideramos importante discutir cómo manejarse con pacientes cuyo análisis de ADN es desfavorable. Una decisión empírica, y a priori razonable, sería la suspensión definitiva de la exposición de estos pacientes al irinotecan. Sin embargo, nosotros consideramos que la detoxificación inadecuada podría ser en cierta manera compensada por una reducción de la dosis, y en el caso de la toxicidad gastrointestinal el carbón activado podría adsorber al SN-38 reduciendo su contacto con la mucosa intestinal. No existe evidencia acerca de reducción de dosis en pacientes con un perfil genético de TA indel desfavorable y, a pesar de las bien conocidas recomendaciones para el manejo de la diarrea en pacientes expuestos a este tipo de drogas8, se carece de información referente al manejo clínico en función del perfil genómico, probablemente por lo reciente de la aparición de estos métodos diagnósticos.
Nuestro caso sugiere la posibilidad de que una modesta reducción de la dosis de irinotecan, junto con el tratamiento de soporte estándar, podría permitir la continuación del uso de la droga. Por otro lado, teniendo en cuenta que la prevalencia de la enfermedad de Gilbert en la población caucásica se estima en el 8-9%, creemos que el juicioso uso de este método de diagnóstico podría predecir la toxicidad grave del irinotecan aunque debido a que la utilidad de un estudio de laboratorio depende en parte de la prevalencia de lo buscado, consideramos relevante establecer la frecuencia del TA indel en una muestra de pacientes y voluntarios en nuestro medio.
Bibliografía
1. Douillard JY, Cunningham D, Roth AD, et al. Irinotecan combined with fluorouracil compared with fluorouracil alone as first-line treatment for metastatic colorectal cancer: a multicentre randomised trial. Lancet 2000; 355: 1041-7.
2. Saltz LB, Cox JV, Blanke C, et al. Irinotecan and fluorouracil and leucovorin for metastatic colorectal cancer. N Engl J Med 2000; 343: 905-14.
3. Innocenti F, Undevia SD, Iyer L, et al. Genetic variants in the UDP-glucuronosyltransferase 1A1 gene predict the risk of severe neutropenia of irinotecan. J Clin Oncol 2004; 22: 1382-8.
4. Noda K, Nishiwaki Y, Kawahara M, et al. Irinotecan plus cisplatin compared with etoposide plus cisplatin for extensive small-cell lung cancer. N Engl J Med 2002; 346: 85-91.
5. Bosma P, Chowdhury J, Bakker C, et al. The genetic basis of the reduced expression of bilirrubin UDP-glucuronosyltransferase 1 in Gilbert´s syndrome. N Engl J Med 1995; 333: 1171-5.
6. Rouits E, Boisdron-Celle M, Dumont A, Guerin O, Morel A, Gamelin E. Relevance of different UGT1A1 polymorphisms in irinotecan-induced toxicity: a molecular and clinical study of 75 patients. Clin Cancer Res 2004; 10: 5151-9.
7. Schmittel A, Jahnke K, Thiel E, Keilholz V. Neomycin as secondary prophylaxis for irinotecan-induced diarrhea. Ann Oncol 2004; 15: 1296 (Letter).
8. Benson AB, Ajani JA, Catalano RB, et al. Recommended guidelines for the treatment of cancer treatment-induced diarrhea. J Clin Oncol 2004; 22: 2918-26. [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ]
Recibido: 5-04-2006
Aceptado: 18-09-2006














