Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680versión On-line ISSN 1669-9106
Medicina (B. Aires) v.67 n.1 Buenos Aires ene./feb. 2007
Papel de las células dendríticas en la infección por HIV y HCV
Liliana Belmonte, Cecilia Parodi, Patricia Baré, Mariela Bastón, María Marta E. Bracco, Beatriz Ruibal-Ares
Instituto de Investigaciones Hematológicas, Academia Nacional de Medicina, Buenos Aires
Correspondencia a: Dra Beatriz Ruibal-Ares, Academia Nacional de Medicina, Pacheco de Melo 3081, 1425 Buenos Aires, Argentina.
e-mail: ruibalbea@hematologia.anm.edu.ar
Resumen
Las células dendríticas son las principales células presentadoras de antígenos para el montaje de la respuesta inmune. Por lo tanto es importante estudiar de qué manera intervienen en el equilibrio que el sistema inmune desarrolla frente a infecciones virales persistentes como la infección por el HIV o el HCV. En esta revisión se presentan en primer término generalidades sobre las diferentes clases de células dendríticas, las características fenotípicas y funcionales que las definen y los receptores que pueden estar involucrados en la infección viral. Luego se analiza su participación en los mecanismos de defensa o facilitadores de la infección por estos virus. Es importante tener en cuenta estos conocimientos para poder diseñar adecuadas estrategias de vacunación o protección y para intentar la reconstrucción funcional del sistema inmune impidiendo la subversión de los mecanismos inmunes de defensa causada por la infección con el HIV y el HCV.
Palabras clave: HIV; HCV; Células dendríticas
Abstract
The role of dendritic cells in the infection by HIV and HCV. Dendritic cells are most important as antigen presenting cells during the induction of an effective immune response. Therefore, it is important to study their role during the generation of persistent or chronic viral infections, such as HIV or HCV infection. In this review we shall describe the phenotypic and functional characteristics of the different classes of dendritic cells and of their membrane receptors. Their participation in defence or facilitation mechanisms involved in the immune response against these viruses will be discussed. It is important to take this knowledge into account when trying to design therapeutic strategies for protection or reconstruction of the immune system that may be altered as a consequence of infection with HIV or HCV.
Key words: HIV; HCV; Dentritic cells
Las células dendríticas (CD) son los centinelas naturales del sistema inmune, siendo las encargadas de iniciar la respuesta inmune frente a la presencia de células alteradas del huésped y/o a la invasión de patógenos. Al ser las principales células presentadoras de antígenos (APC) son importantes tanto en la estimulación, activación como en la regulación de la respuesta de los linfocitos T1.
Se postula que en ausencia de estímulos externos, las CD permanecen en estado de reposo, en el cual su capacidad de señalización hacia los linfocitos T naïve se encuentra limitada. La infección de las CD provoca varios cambios fenotípicos y funcionales los cuales, en forma coordinada, mejoran su capacidad para interactuar con los linfocitos T, promover su expansión clonal y diferenciación. Sin embargo, los virus patógenos pueden utilizar a las células dendríticas para subvertir la respuesta inmune, logrando establecer la infección en el huésped2.
Las CD penetran en la corriente sanguínea de dos formas: como CD inmaduras (CDi) o bien como CD maduras (CDm) (Fig. 1). Las CDi incluyen a las células de Langerhans, a las CD de la zona marginal esplénica y a las CD intersticiales que se encuentran dentro de los tejidos linfoides3. Estas células están principalmente involucradas en la captura de antígenos tanto exógenos como endógenos, contienen baja a moderada expresión de moléculas del complejo mayor de histocompatibilidad de clase II (MCH II) y de moléculas coestimuladoras (CD40, CD80 y CD86) y son capaces de inducir y mantener la tolerancia, ya que continuamente presentan antígenos propios a los linfocitos T.
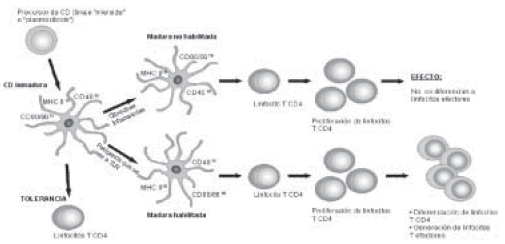
Fig. 1.- Maduración de las células dendríticas y su relación con los linfocitos T. Consecuencias en el desarrollo de la respuesta inmune.
Existen dos clases de estímulos para que estas células se transformen en formas inmunológicamente maduras (CDm). Uno de ellos involucra el reconocimiento de los patógenos por parte de sus receptores (como el toll like receptor, TLR). El otro mecanismo es indirecto, dependiendo de la exposición de las CDi a señales endógenas peligrosas, como los mediadores inflamatorios o el material liberado por células dañadas4. Distintos TLR presentes en las CDi son utilizados para reconocer diferentes clases de señales (derivados de virus, bacterias, células dañadas, etc). Esto es fundamental tanto para su función como centinelas de la inmunidad innata como para ejercer su rol de nexo entre la inmunidad innata y la inmunidad adaptativa5. El paradigma de que las CD se diferencian en dos etapas, las CDi (involucradas en tolerancia) y las CDm (que colaboran en el desarrollo de respuestas inmunes efectoras) ha sido útil para explicar el rol de las células dendríticas en la generación de la respuesta inmune6. Sin embargo, se ha demostrado que según la naturaleza del estímulo, las CDm pueden resultar heterogéneas en cuanto a su calidad funcional y por otro lado, ser capaces de modificar sus funciones efectoras7. Cuando las CDm han madurado a consecuencia del contacto con patógenos, resultan habilitadas (licensed ) para la presentación antigénica y la estimulación de los linfocitos T naïve, lo que da lugar a su diferenciación en células efectoras. En cambio, cuando la maduración se ha producido sólo por la presencia de citoquinas inflamatorias en un medio libre de gérmenes, las CDm no habilitadas (unlicensed) podrían colaborar en la inducción de la proliferación de los linfocitos T CD4+ naïve incapaces de diferenciarse a células efectoras. Tanto las CDm habilitadas como las no habilitadas regulan la expresión de moléculas coestimuladoras y de MHC II8. En algunos casos, la interacción de los patógenos con los TLR (toll like receptor) no da lugar a la generación de células dendríticas maduras funcionales clásicas.
Se ha propuesto que la interacción de las CDi con el HIV, puede llevar a un estado semimadurativo, en el cual las CDi migran a los ganglios linfáticos pero no alcanzan la maduración completa a CDm. En esta situación las células dendríticas semimaduras inducen un estado de tolerancia sin lograr la inmunidad a los antígenos, probablemente por medio de la generación de células T reguladoras (T reg)9.
De acuerdo a sus características fenotípicas y funcionales se reconocen dos tipos de CD precursoras: CD de origen mieloide (pre-MCD) y CD plasmocitoides (pre-PCD) (Fig. 2). Las pre-CD migran de la médula ósea a los tejidos periféricos por la corriente sanguínea estimuladas por los gradientes de quimoquinas, y su posterior diferenciación en CD residentes es gobernada por el balance de citoquinas. Las pre-CD difieren de las CDi y CDm, ya que pueden asumir rápidamente el fenotipo de éstas bajo condiciones apropiadas, tanto in vitro como in vivo. Las pre-CD han sido identificadas en sangre y en tejidos linfoides como células de linaje negativo definidas por la ausencia de los marcadores de superficie CD3, CD4, CD11b, CD56 y CD 19, acompañada de la expresión moderada a alta de HLA-DR y de CD11c.

Fig. 2.- Diferenciación y maduración de las células dendríticas precursoras
Las células dendríticas constituyen cerca del 1% de las células mononucleares de la sangre y pueden ser divididas en dos subpoblaciones principales que difieren en el fenotipo y función: CD mieloides (MCD) y CD plasmocitoides (PCD).
Las CD mieloides (MCD) son las células más importantes en la presentación antigénica (CPA). Están involucradas en la respuesta innata y adaptativa del huésped a la infección viral. Se han efectuado numerosos trabajos utilizando MCD obtenidas estimulando in vitro los monocitos de sangre periférica con factores de crecimiento. Para ello, los monocitos CD14+ son colocados in vitro en presencia de IL-4 y del factor estimulante de colonias de granulocitos y macrófagos (GM-CSF), logrando así su transformación en potentes CPA, CD14-5, 6, 7, 8 denominadas células dendríticas derivadas de los monocitos (MCDD). Las células troncales CD34+ pueden servir también como células precursoras de las MCDD. In vitro, las MCDD inmaduras (MCDDi) tienen menor expresión de CD4 que los monocitos. Sin embargo, aumenta la expresión de moléculas involucradas en la presentación de antígenos, incluyendo a las moléculas de HLA clase II en los linfocitos T CD4+ y a los co-receptores de los linfocitos T (CD80, CD86, el receptor CD40) en los linfocitos B y T CD4+. También se eleva en MCDD la expresión de CD209 (DC-SIGN), el cual interactúa con ICAM-2 y ICAM-3 presente en el endotelio y en los linfocitos T. Las MCDD también expresan un conjunto de receptores de quimoquinas necesarias para el tráfico de las CD. Cuando las MCDDi son estimuladas por el CD40L o por citoquinas proinflamatorias (TNF-a, IL-1ß, IL-6, INF-a) maduran convirtiéndose en MCDDm, que expresan en la superficie celular cantidades de CD80 y CD86 mayores que las MCDDi. Además, las MCDDm adquieren el CD83+, el cual favorece su capacidad para estimular a los linfocitos T. Otra característica de las MCDDm es su capacidad de liberar IL-12 en gran cantidad, lo cual resulta necesario para prolongar las respuestas T helper y estimular a los linfocitos T citotóxicos (CTL) efectores. Por otra parte, estas células (MCDDm) tienen niveles bajos de DC-SIGN, de CD4 y de receptores para quimoquinas.
La segunda subpoblación de CD que circula en la sangre se denomina CD plasmocitoide (PCD). Se distinguen de las MCD por no expresar CD11c. No obstante, expresan altos niveles de CD123 (receptor de la IL-3) y producen grandes cantidades de la proteína antiviral INF-a (10) en respuesta a infecciones virales11-13 cumpliendo de esta forma, un importante rol en la respuesta inmune innata.
Se demostró que el INF-a producido por las PCD maduras en los ganglios linfáticos, aumenta la función de las MCD10, 11. Otra función de las PCD es el procesamiento de antígenos y su presentación a los linfocitos T; sin embargo, son menos eficientes que las MCD. Por otro lado, como las PCD sanguíneas expresan CD4, CCR5 y CXCR4, son susceptibles a la infección por el HIV12, en particular cuando son estimuladas por el CD40L14. Estas células también expresan DC-SIGN y pueden "trans" infectar con HIV a los linfocitos T CD4 en reposo15. Un resumen del fenotipo de las PCD y de las MCD se muestra en la Tabla 1. Al contrario de las MCD, las cuales migran a los tejidos e interceptan los patógenos invasores antes de su migración a los ganglios linfáticos, las PCD migran directamente de la sangre a los tejidos linfáticos secundarios, donde se diferencian en las células que originalmente se denominaban células T plasmocitoides por la extensión de su retículo endoplásmico13. La diferenciación de los monocitos sanguíneos en presencia de INF-a y GM-CSF da lugar a células con expresión de TLR-7, que muestran varias características funcionales parecidas a las PCD16. Esto indica que las pre-CD precursoras pueden expandirse y diferenciarse en células de fenotipo diverso y distintas funciones, influenciadas por la composición del medio circundante y la naturaleza de los estímulos.
TABLA 1.- Fenotipo de las células dendríticas mieloides (MCD) y plasmacitoides (PCD)

El análisis fenotípico por citometría de flujo facilita la identificación de MCD y PCD: el CD4 se detecta en ambas poblaciones pero se expresan más intensamente en las PCD después de 48 h de cultivo su expresión desciende en las MCD pero no varía en las PCD14. Se observaron niveles bajos de CCR5 en las MCD y relativamente más elevados en las PCD. El CCR5 se hace indetectable en la superficie de ambos tipos de CD después de 48 h de cultivo, mientras que la expresión de CXCR4 fue levemente modificada. También se observó descenso de CD4 en las MCD14.
Células dendríticas y HIV
La capacidad migratoria de las CD posiblemente sea la responsable del transporte del HIV a los sitios de drenaje de los ganglios linfáticos ilíacos y colónicos. La infección de un linfocito T CD4 activado es más eficiente cuando el virus es transferido durante la interacción CD-linfocito T CD4+. Durante la fase temprana de replicación del HIV in vivo, este sinergismo posiblemente tenga un rol importante en la replicación viral. Aunque con menor frecuencia que los macrófagos y los linfocitos T CD4+ activados, las CD pueden ser infectadas por el HIV-1 in vitro e in vivo y transmitir a estos linfocitos los viriones resultantes de la replicación en su interior (infección "cis"). Por otro lado, las CD pueden actuar como donantes en la infección "trans" (sin padecer ellas mismas una infección productiva), cediendo a los linfocitos T CD4+ el virus unido a receptores de membrana2.
Mediante experimentos de infección in vitro se ha confirmado que ambos tipos de CD (MCD y PCD) pueden ser infectados por el HIV-117, 18. Sin embargo, la replicación viral fue más eficiente en las PCD. Esto puede deberse a la menor expresión de CD4 en las MCD que en las PCD. El aislamiento de MCD y PCD altamente purificadas, obtenidas de pacientes infectados, logró demostrar que ambas subpoblaciones pueden ser infectadas con el HIV y que algunas MCD contienen provirus integrado19. Además, estas poblaciones son marcadamente deficientes en su capacidad para estimular la proliferación de los linfocitos T, por lo tanto se supone que la pérdida (numérica y funcional) de las MCD y PCD a causa de la infección por el HIV, puede ser un factor importante en la declinación de la respuesta inmune innata y adquirida en estos pacientes HIV+. Más aún, como las MCD y PCD presentes en el timo son susceptibles a la infección por el HIV, muriendo posteriormente por apoptosis, se ha sugerido que la infección viral podría afectar la timopoiesis18.
Recientemente se ha demostrado que las MCD y las PCD tienen distinta capacidad para transferir el HIV a células CD4+ permisivas; linfocitos T CD4 preferentemente activados y macrófagos tisulares. Para ello, se utilizaron poblaciones de CD4 humanas purificadas y se estudió su efecto estimulador o inhibitorio de la transmisión del HIV in vitro a linfocitos T CD4+. Mientras que las MDC aumentaron la replicación del HIV, el efecto opuesto se logró con PDC20.
El HIV adherido a las CD, independientemente del CD4 y de los correceptores de quimoquinas, puede ser internalizado y/o transferido al linfocitoT permisivo16, 19 (Fig. 3). Tanto los receptores celulares convencionales de la membrana, CD4 y CCR5, como receptores del tipo de lectinas Ca-dependientes (CLR) son responsables de iniciar la adherencia viral. Los mecanismos de adherencia del HIV son a menudo específicos del tipo celular, siendo la expresión de CLR diversa y abundante en las CD epiteliales y en las MCD.

Fig. 3.- Papel de las células dendríticas en la infección por el HIV
Inicialmente, se sugirió que el receptor DC-SIGN de las CD desempeñaba un papel crucial en la diseminación "trans" del HIV 21, 22. La internalización del DC-SIGN con el HIV adherido protegería al HIV de la inactivación, dejándolo en condiciones de ser transferido a las células que admiten la infección21. En trabajos recientes se sugirió que la internalización del DC-SIGN no es indispensable para la transferencia del HIV a las células T permisivas, haciendo hincapié en el papel de la propia infección de las CD en la transmisión a las células T CD4+17. Otras subpoblaciones de CD, identificadas in vivo, que poseen otros CLR como langerina en las células de Langerhans (CL) o los receptores de manosa (MR) en las CD dérmicas22 tienen relevancia en la transmisión viral. Por lo tanto, aunque importante, el DC-SIGN puede representar solamente uno de varios CLR presentes en las CD capaces de interactuar con el HIV in vivo23, 24. Las CL que expresan langerina y no DC-SIGN o MR, pueden ser tan importantes como las de la lámina propia o las CD dérmicas para la transmisión del HIV a través del epitelio estratificado escamoso genital. En particular, las CL pueden ser fundamentales en las infecciones virales de los epitelios no traumatizados. Tienen una marcada capacidad para unirse a la gp120 de la envoltura del HIV, vía langerina y quizás otros receptores CLR25, 26. En las CD provenientes del epitelio escamoso de la piel, la unión con la gp120 se realiza a través de CLR. La expresión de estos receptores CLR varían en distintos grupos de CD. Los receptores de lectina de tipo C: DC-SIGN, MR y posiblemente langerina pueden proporcionar una ruta natural para el HIV por las vías endolisosomales de las CD22, 26. La captura del HIV por CLR, DC-SIGN y MR puede facilitar la entrada del HIV mediante la fusión neutral en la membrana del citoplasma, por medio de los convencionales CD4/CCR5 (infección "cis"). Por lo tanto, los CLR favorecerían la entrada del HIV por dos vías posibles: endocitosis o fusión neutral/infección. En los linfocitos T CD4+ predomina la fusión neutral del HIV en la membrana celular y en las CD, la endocitosis.
Para el estudio de la interacción CD/HIV se ha recurrido a modelos in vitro basados en la estimulación de los precursores de monocitos con IL-4/GM-CSF por una semana (MCDD, monocyte derived dendritic cells). Sin embargo, aún no se ha determinado a cuáles CD in vivo se asemejan las MCDD. Tampoco se han definido sistemas in vitro válidos para la generación de PDC semejantes a las que naturalmente se encuentran en circulación en el hombre27.
El procedimiento de la transferencia viral de las poblaciones de CD, a los linfocitos T CD4+ naïve o activados, puede variar dependiendo de varios factores claves. Estos incluyen: el fenotipo (inmaduro versus maduro) y la clase de CD (MCD versus PCD), el tipo de contacto con el estímulo, la cantidad del virus unido a las CD y el tiempo transcurrido entre la unión del HIV a las CD.
La expresión de los receptores de quimoquinas también varía. Así, el CCR5 predomina claramente sobre el CXCR4 en los tejidos inmaduros28. Una expresión elevada de CLR en las CD, puede favorecer el proceso de toma y transferencia del HIV presente en las CD a los linfocitos T CD4+, pero los CLR parecen no ser esenciales. Sin embargo, los CLR pueden ser importantes en la captura y transferencia del HIV cuando éste se encuentra en baja concentración. Luego de la transferencia del HIV desde las CD a los linfocitos T CD4+ en el epitelio, se forman agregados de CD y linfocitos T que participan en la transferencia local; ocurriendo algo similar en los ganglios linfáticos. Es improbable que la transferencia directa del HIV por la vía endosomal desde las CD a los linfocitos T CD4+ sea selectiva (tropismo diferencial CXCR4 o CCR5), mientras que la infección de las CD de novo sea probablemente selectiva para el virus con tropismo para el CCR5. Los experimentos que examinan la interacción de las CD con los linfocitos T CD4+ han llegado a la conclusión que, tanto los agregamientos entre CD y linfocitos T CD4+ como la proliferación inducida por las CD que presentan HIV en los linfocitos en reposo son mediadas por la interacción DC-SIGN -ICAM 3, la cual produce un entorno transitoriamente estable para la señalización eficiente del TCR.
A pesar del menor nivel de DNA proviral encontrado en las MCD respecto a los linfocitos T CD4+, se han detectado virus integrados en 4 de 14 muestras de MCD, mientras que en los linfocitos T CD4+ de los mismos individuos, sólo se detectó en 1 de las 14 muestras estudiadas. Estos hallazgos indican que las MCD podrían potencialmente convertirse en sitios de producción viral y de transmisión del virus a los linfocitos. A consecuencia de los efectos citopáticos de la infección, podría también explicarse la pérdida de las CD observada luego de la infección por el HIV29, 30.
La pérdida de ambas clases de CD, produciría la declinación de la respuesta inmune debido a la presentación antigénica deteriorada, pero la pérdida específica de las CD involucradas en la liberación de IFN-a (PCD), podría afectar aún más la capacidad del huésped infectado por el HIV para controlar las infecciones oportunistas y mantener un sistema de defensa inmune intacto31. El número absoluto de las PCD circulantes (> 2 cel/µl) puede ser utilizado para monitorear el sistema inmune de los pacientes infectados por el HIV. El número de PCD en la sangre, principales células productoras de IFN-a, está reducido de manera llamativa en los pacientes con sida, pero aumenta en los pacientes HIV+ asintomáticos con largo tiempo de sobrevida13. Aun cuando el nivel de linfocitos T CD4+ continúe disminuyendo, el número de PCD puede descender a bajos niveles y permanecer allí de manera relativamente constante32. El concepto que las PCD y los linfocitos T CD4+ pueden ser alterados independientemente después de la infección por el HIV, fue comprobado en un estudio que comparó la producción del IFN-a con el recuento de linfocitos T CD4+ en un grupo numeroso de pacientes infectados por el HIV33. Sólo cuando el nivel de IFN-a y el de linfocitos T CD4+ descendió conjuntamente por debajo de un valor crítico, las infecciones oportunistas marcaron el comienzo del sida33. Una posible explicación para la pérdida de las PCD en los pacientes infectados por el HIV, podría ser que estas células emigrarían de la sangre periférica a los órganos linfoides secundarios o a los tejidos. Sin embargo, los niveles de producción del IFN-a estuvieron significativamente correlacionados con la carga viral plasmática del HIV más que con el nivel absoluto de PCD. Esto sugiere que una viremia elevada, sea directa o indirectamente, podría influenciar de manera negativa la función de las PCD. Mientras que en sangre periférica, tanto las MCD como las PCD de pacientes con infección por el HIV se redujeron en número. En las PCD existe además una deficiencia funcional en su capacidad de producir IFN-a, especialmente en estadios avanzados de la infección por el HIV. La Tabla 2 resume las consecuencias de la infección por el HIV, sobre el balance y función de las CD.
TABLA 2.- Cambios en la actividad de las células dendríticas (CD) causados por la infección con el HIV

Células dendríticas y HCV
La característica más llamativa de la infección por el HCV es la habilidad de este virus para persistir en la mayoría de los individuos infectados34. La terapia anti-HCV se basa en la utilización de IFN-a recombinante conjuntamente con el nucleósido análogo ribavirina. Sin embargo, no es totalmente adecuada y en la mayoría de los casos es efectiva sólo temporalmente35, 36.
El HCV pertenece a la familia Flaviviridae. Es un virus pequeño y envuelto. Su genoma está constituido por una única cadena de ARN de 9.600 nucleótidos de largo, codificando una única poliproteína que es clivada en proteínas estructurales localizadas en la región N-terminal (core, E1, E2 y p7) y 6 proteínas no estructurales37, 38, 39. No se conoce el receptor del HCV. Se ha demostrado que el receptor de la lipoproteína de baja densidad (LDLR) interviene en la internalización de las partículas del HCV, asociado a la lipoproteína de baja densidad (LDL)40. La tetraspanina CD81 ha sido identificada como un receptor de unión de alta afinidad para recombinar E2 proveniente del genotipo 1a del HCV41. Sin embargo, teniendo en cuenta que el LDLR y CD81 son expresados en la mayoría de los diferentes tipos celulares, el tropismo hepático de este virus no puede atribuirse a la presencia de esas moléculas en la membrana42. La infección viral es caracterizada por un alto porcentaje de cronicidad, que en el 20% de los casos lleva a la cirrosis hepática, con un eventual desarrollo de carcinoma hepatocelular43. El HCV es sumamente variable y diferentes "quasiespecies" consistentes en un conjunto de distintas variantes relacionadas, pero genéticamente distintas coexisten en las personas infectadas44.
La replicación del genoma del HCV ha sido demostrada principalmente en los hepatocitos y hepatocitos de líneas celulares45, como también en células hematopoyéticas46, 47, 48.
A partir de la secuenciación genómica del HCV, se ha progresado en la comprensión de la función de las proteínas codificadas del HCV. Aunque la ausencia de un sistema de replicación in vitro eficiente o un modelo de infección experimental en animales pequeños ha dificultado el estudio de la naturaleza de la interacción HCV/huésped. Los estudios del ARN-HCV en células mononucleares sanguíneas periféricas, sugieren la coexistencia de reservorios del HCV independientes, y es posible que el virus utilice receptores distintos para infectar células diferentes49.
Recientemente, se ha hecho mayor hincapié en la posibilidad de que los receptores tipo CLR sean utilizados por el HCV50. Por lo tanto, el DC-SIGN y otra molécula relacionada (L-SIGN) que está presente en el endotelio interno de los sinusoides hepáticos, podrían unirse al HCV a través de la glicoproteína E2 de la envoltura rica en glicanos con elevada manosa. Es posible especular, consecuentemente a la unión con el L-SIGN endotelial51, que el HCV podría ser trasmitido a los hepatocitos del entorno en una interacción "trans", como se ha propuesto para el HIV unido al DC-SIGN. Además, la unión eficiente de E2 soluble al DC-SIGN y DC-SIGNR, ha sido también demostrada en líneas celulares y en células endoteliales primarias humanas52. Ambas MCDDm y MCDDi podrían unirse a E2 soluble, pero mientras que DC-SIGN fue necesario para la captura de E2 por las MCDDi, la unión de E2 a las MCDDm fue parcialmente independiente de la expresión de DC-SIGN, sugiriendo que otras moléculas de superficie pueden mediar interacciones del HCV en estas células52. Hay evidencias que además de unirse a los receptores de las CD, el HCV puede replicarse en estas células, obtenidas de pacientes crónicamente infectados con el HCV53, sugiriendo que las MCD pueden constituir un reservorio, en el cual la replicación del HCV se produce durante la infección natural del virus. Por lo tanto, como se ha demostrado para la infección por el HIV, ambas subpo-blaciones de MCD y de PCD disminuyen en número y su función se deteriora54, lo cual puede explicar su pobre respuesta inmune antiviral de adaptación en aquellos pacientes que cursan con HCV de forma crónica. La secreción del IFN-a estaba descendida en los pacientes que recibían terapia (IFN-a recombinante y ribavirina). Este hallazgo se relacionó con el número de las PCD determinado en la sangre, sugiriendo que el descenso de estas células y la disminución de la secreción del IFN-a eran la consecuencia del tratamiento, y no el resultado de la infección viral per se53. En otros estudios, se comprobó que otras funciones de las CD (capacidad alloestimulatoria, producción de IL-10, expresión del TLR2) podían estar alteradas en los pacientes con infección persistente por el HCV55, 56, 57, 58. En todo caso, los defectos funcionales de las CD de sangre periférica (principalmente aquellos que corresponden a la subpoblación PCD) podrían empeorar dramáticamente la respuesta innata y adaptativa anti-HCV, induciendo a la persistencia viral59.
En conclusión, tanto para poder comprender la naturaleza compleja de las relaciones entre estos virus y su huésped (las cuales llevan al establecimiento de la infección crónica con sus importantes consecuencias patológicas), como para poder encarar tratamientos más eficaces o diseños terapéuticos preventivos, es importante profundizar el estudio de la interacción de las CD con ambos virus, ya que estas células proporcionan la clave para el balance de la respuesta inmune defensiva.
Bibliografía
1. Banchereau J, Steinman RM. Dendritic cells and the control of immunity. Nature 1998; 392: 245-52.
2. Wilflingsleder D, Banki Z, Dierich MP, Stoiber H. Mechanisms promoting dendritic cell-mediated transmision of HIV. Mol Immunol 2005; 42: 229-37.
3. Liu Y-J, Kanzler H, Soumelis V, Gilliet M. Dendritic cell lineage, plasticity and cross-regulation. Nat Immunol 2001; 2: 585-9.
4. Reid SD, Penna G, Adorini L. The control of T cell responses by dendritic cell subsets. Curr Opin Immunol 2000; 12: 114-21.
5. Reis e Sousa C. Activation of dendritic cells: translating innate into adaptive immunity. Curr Opin Immunol 2004; 16: 21-5.
6. Steinman RM, Nussenzweig MC. Avoiding horror autotoxicus: the importance of dendritic cells in peripheral T cell tolerante. Proc Natl Acad Sci USA 2002; 99: 351-8.
7. Sporri R, Reis e Sousa C. Inflammatory mediators are insufficient for full dendritic cell activation and promote expansion of CD4+ T cell populations lacking helper function. Nat Immunol 2005; 6: 163-70.
8. Heath WR, Villadangos JA. No driving without a license. Nat Immunol 2005; 6: 125-6.
9. Krathwohl MD, Schacker TW, Anderson JL. Abnormal presence of semimature dendritic cells that induce regulatory T cells in HIV-infected subjects. J Infect Dis 2006; 193: 494-504.
10. Ito T, Amakawa R, Inaba M, et al. Plasmacytoid dendritic cells regulate Th cell responses through OX40 ligand and type I IFNs. J Immunol 2004; 172: 4253-9.
11. Blom B, Ho S, Antonenko S, Liu YJ. Generation of interferon alpha-producing predendritic cell (Pre-DC)2 from human CD34(+) hematopoietic stem cells. J Exp Med 2000; 192: 1785-96.
12. Donaghy H, Gazzard B, Gotch F, Patterson S. Dysfunction and infection of freshly isolated blood myeloid and plasmacytoid dendritic cells in patients infected with HIV-1. Blood 2003; 101: 4505-11.
13. Patterson S, Rae A, Hockey N, Gilmour J, Gotch F. Plasmacytoid dendritic cells are highly susceptible to human immunodeficiency virus type 1 infection and release infectious virus. J Virol 2001; 75: 6710-3.
14. Cella M, Facchetti F, Lanzavecchia A, Colonna M. Plasmacytoid dendritic cells activated by influenza virus and CD40L drive a potent TH1 polarization. Nat Immunol 2000; 1: 305-10.
15. Kwon DS, Gregorio G, Bitton N, Hendrickson WA, Littman DR. DC-SIGN-mediated internalization of HIV is required for trans-enhancement of T cell infection. Immunity 2002; 16: 135-44.
16. Mohty M, Vialle-Castellano A, Nunes JA, Isnardon D, Olive D, Gaugler B. IFN-alpha skews monocyte differentiation into Toll-like receptor 7-expressing dendritic cells with potent functional activities. J Immunol 2003; 171: 3385-93.
17. Burleigh L, Lozach PY, Schiffer C et al. Infection of dendritic cells (DCs), not DC-SIGN-mediated internalization of human immunodeficiency virus, is required for long-term transfer of virus to T cells. J Virol 2006; 80: 2949-57.
18. Schmitt N, Nugeyre MT, Scott-Algara D et al. Differential susceptibility of human thymic dendritic cell subsets to X4 and R5 HIV-1 infection. AIDS 2006; 20: 533-42.
19. Masso M. DC-SIGN points the way to a novel mechanism for HIV-1 transmission. Med Gen Med 2003; 5: 2.
20. Groot F, van Capel TMM, Kapsenburg ML, Berkhout B, de Jong E. Opposing roles of blood myeloid and plasmacytoid dendritic cells in HIV-1 infection of T cells: transmisión facilitation versus replication inhibition. Blood 2006; 108: 1957-64.
21. Geijtenbeek TB, Kwon DS, Torensma R, et al. DC-SIGN, a dendritic cell-specific HIV-1-binding protein that enhances trans-infection of T cells. Cell 2000; 100: 587-97.
22. Turville S, Wilkinson J, Cameron P, Dable J, Cunningham AL. The role of dendritic cell C-type lectin receptors in HIV pathogenesis. J Leukoc Biol 2003; 74: 710-8.
23. Rinaldo CR Jr, Piazza P. Virus infection of dendritic cells: portal for host invasion and host defense. Trends Microbiol 2004; 12: 337-45.
24. McDonald D, Wu L, Bohks SM, KewalRamani VN, Unutmaz D, Hope TJ. Recruitment of HIV and its receptors to dendritic cell-T cell junctions. Science 2003; 300 (5623): 1295-7.
25. Engering A, Geijtenbeek TB, van Vliet SJ, et al. The dendritic cell-specific adhesion receptor DC-SIGN internalizes antigen for presentation to T cells. J Immunol 2002; 168: 2118-26.
26. Engering A, Van Vliet SJ, Geijtenbeek TB, Van Kooyk Y. Subset of DC-SIGN(+) dendritic cells in human blood transmits HIV-1 to T lymphocytes. Blood 2002; 100: 1780-6.
27. Mennechet FJD, Uzé G. Interferon-l-treated dendritic cells specifically induce proliferation of FOXP3-expressing supresor T cells. Blood 2006; 107: 4417-23.
28. Kawamura T, Cohen SS, Borris DL, et al. Candidate microbicides block HIV-1 infection of human immature Langerhans cells within epithelial tissue explants. J Exp Med 2000; 192: 1491-500.
29. Donaghy H, Pozniak A, Gazzard B, et al. Loss of blood CD11c(+) myeloid and CD11c(-) plasmacytoid dendritic cells in patients with HIV-1 infection correlates with HIV-1 RNA virus load. Blood 2001; 98: 2574-6.
30. Pacanowski J, Kahi S, Baillet M, et al. Reduced blood CD123+ (lymphoid) and CD11c+ (myeloid) dendritic cell numbers in primary HIV-1 infection. Blood 2001; 98: 3016-21.
31. Feldman S, Stein D, Amrute S, et al. Decreased interferon-alpha production in HIV-infected patients correlates with numerical and functional deficiencies in circulating type 2 dendritic cell precursors. Clin Immunol 2001; 101: 201-10.
32. Soumelis V, Scott I, Gheyas F, et al. Depletion of circulating natural type 1 interferon-producing cells in HIV-infected AIDS patients. Blood 2001; 98: 906-12.
33. Siegal FP, López C, Fitzgerald PA, et al. Opportunistic infections in acquired immune deficiency syndrome result from synergistic defects of both the natural and adaptive components of cellular immunity. J Clin Invest 1986; 78: 115-23.
34. Eisen-Vandervelde AL, Yao ZQ, Hahn YS. The molecular basis of HCV-mediated immune dysregulation. Clin Immunol 2004; 111: 16-21.
35. Gerotto M, Sullivan DG, Polyak SJ, et al. Effect of retreatment with interferon alone or interferon plus ribavirin on hepatitis C virus quasispecies diversification in nonresponder patients with chronic hepatitis C. J Virol 1999; 73: 7241-7.
36. Hino K, Yamaguchi Y, Fujiwara D, et al. Hepatitis C virus quasispecies and response to interferon therapy in patients with chronic hepatitis C: a prospective study. J Viral Hepat 2000; 7: 36-42.
37. Bartenschlager R, Lohmann V. Replication of hepatitis C virus. J Gen Virol 2000; 81: 1631-48.
38. Grakoui A, McCourt DW, Wychowski C, Feinstone SM, Rice CM. A second hepatitis C virus-encoded proteinase. Proc Natl Acad Sci USA 1993; 90: 10583-17.
39. Hijikata M, Mizushima H, Akagi T, et al. Two distinct proteinase activities required for the processing of a putative nonstructural precursor protein of hepatitis C virus. J Virol 1993; 67: 4665-75.
40. Flint M, Quinn ER, Levy S. In search of hepatitis C virus receptor(s). Clin Liver Dis 2001; 5: 873-93.
41. Wunschmann S, Medh JD, Klinzmann D, Schmidt WN, Stapleton JT . Characterization of hepatitis C virus (HCV) and HCV E2 interactions with CD81 and the low-density lipoprotein receptor. J Virol 2000; 74: 10055-62.
42. Zhang J, Randall G, Higginbottom A, Monk P, Rice CM, McKeating JA. CD81 is required for hepatitis C virus glycoprotein-mediated viral infection. J Virol 2004; 78: 1448-55.
43. Seeff LB. Natural history of hepatitis C. Am J Med 1999; 107 (Suppl 6B): 10S-15S.
44. Simmonds P. Viral heterogeneity of the hepatitis C virus. J Hepatol 1999; 31 (Suppl 1): 54-60.
45. Ikeda M, Sugiyama K, Mizutani T, et al. Human hepatocyte clonal cell lines that support persistent replication of hepatitis C virus. Virus Res 1998; 56: 157-67.
46. Bare P, Massud I, Belmonte L, et al. HCV recovery from peripheral blood mononuclear cell culture supernatants derived from HCV-HIV co-infected haemophilic patients with undetectable HCV viraemia. Haemophilia 2003; 9: 598-604.
47. Bare P, Massud I, Parodi C, et al. Continuous release of hepatitis C virus (HCV) by peripheral blood mononuclear cells and B-lymphoblastoid cell-line cultures derived from HCV-infected patients. J Gen Virol 2005; 86: 1717-27.
48. Bartenschlager R, Lohmann V. Replication of hepatitis C virus. J Gen Virol 2000; 81: 1631-48.
49. Laskus T, Radkowski M, Piasek A, et al. Hepatitis C virus in lymphoid cells of patients coinfected with human immunodeficiency virus type 1: evidence of active replication in monocytes/macrophages and lymphocytes. J Infect Dis 2000; 181: 442-8.
50. Lozach PY, Lortat-Jacob H, de Lacroix de Lavalette A, et al. DC-SIGN and L-SIGN are high affinity binding receptors for hepatitis C virus glycoprotein E2. J Biol Chem 2003; 278: 20358-66.
51. Gardner JP, Durso RJ, Arrigale RR, et al. L-SIGN (CD 209L) is a liver-specific capture receptor for hepatitis C virus. Proc Natl Acad Sci USA 2003; 100: 4498-503.
52. Pohlmann S, Zhang J, Baribaud F, et al. Hepatitis C virus glycoproteins interact with DC-SIGN and DC-SIGNR. J Virol 2003; 77: 4070-80.
53. Goutagny N, Fatmi A, De Ledinghen V, et al. Evidence of viral replication in circulating dendritic cells during hepatitis C virus infection. J Infect Dis 2003; 187: 1951-8.
54. Kanto T, Inoue M, Miyatake H, et al. Reduced numbers and impaired ability of myeloid and plasmacytoid dendritic cells to polarize T helper cells in chronic hepatitis C virus infection. J Infect Dis 2004; 190: 1919-26.
55. Bain C, Fatmi A, Zoulim F, Zarski JP, Trepo C, Inchauspe G. Impaired allostimulatory function of dendritic cells in chronic hepatitis C infection. Gastroenterology 2001; 120: 512-24.
56. Kanto T, Hayashi N, Takehara T, et al. Impaired allostimulatory capacity of peripheral blood dendritic cells recovered from hepatitis C virus-infected individuals. J Immunol 1999; 162: 5584-91.
57. Kanto T, Inoue M, Miyatake H, et al. Reduced numbers and impaired ability of myeloid and plasmacytoid dendritic cells to polarize T helper cells in chronic hepatitis C virus infection. J Infect Dis 2004; 190: 1919-26.
58. Kanto T, Inoue M, Miyazaki M, et al. Impaired function of dendritic cells circulating in patients infected with hepatitis C virus who have persistently normal alanine aminotransferase levels. Intervirology 2006; 49: 58-63.
59. Gerlach JT, Diepolder HM, Jung MC, et al. Recurrence of hepatitis C virus after loss of virus-specific CD4(+) T-cell response in acute hepatitis C. Gastroenterology 1999; 117: 933-41.
Recibido: 6-09-2006
Aceptado: 4-10-2006














