Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680versión On-line ISSN 1669-9106
Medicina (B. Aires) v.67 n.6-2 Ciudad Autónoma de Buenos Aires nov./dic. 2007
Biopsia en enfermedad intersticial pulmonar
Silvia Quadrelli, Gustavo Lyons, Lorena Ciallella, Alejandro Iotti, Julio Chertcoff
Unidad de Medicina Respiratoria y Servicio de Cirugía Torácica del Hospital Británico de Buenos Aires
Dirección postal: Dra. Silvia Quadrelli, Hospital Británico, Perdriel 74, 1280, Buenos Aires, Argentina Fax: (54-11) 4304 3393 e-mail: silvia_quadrelli@hotmail.com
Resumen
El objetivo del presente estudio fue determinar el rédito diagnóstico y los factores asociados a mayor morbimortalidad en la biopsia quirúrgica de pulmón en pacientes con enfermedad intersticial difusa. Se analizaron en forma retrospectiva los registros clínicos de 71 pacientes. Se registraron complicaciones en 16 pacientes (22.5%). La mortalidad operatoria fue 11.2%. Los pacientes en quienes la biopsia se realizó por videotoracoscopia (n = 52) y por toracotomía (n = 17) tuvieron la misma duración de estadía en terapia intensiva y de estadía hospitalaria. La tasa de complicaciones (22.2% vs. 21.0%, p = 1.0000) y la mortalidad (9.2 vs. 15.7%, p = 0.2738) no fueron diferentes. Ocho pacientes murieron dentro de los 30 días. La prevalencia de inmunosupresión (4/8 vs. 9/63, p = 0.0325) fue significativamente superior en el grupo de pacientes fallecidos. Estos pacientes tuvieron valores preoperatorios más elevados de urea (50 ± 20.1 mg/dl vs. 31.2 ± 10.3 mg/ dl, p = 0.0013) y menores valores de saturación de O2: 82.7 ± 14.8% vs. 92.8 ± 3.4%, p = 0.0009. En los 11 pacientes con iniciación aguda la mortalidad fue significativamente más elevada (36.3% vs. 7.1%, p = 0.0223). La biopsia aportó un diagnóstico específico en 100% de los pacientes y cambió la estrategia terapéutica en 66.7%. En conclusión, la biopsia de pulmón por vía toracoscópica es un procedimiento útil y seguro en los pacientes con enfermedad intersticial difusa del pulmón. Sin embargo, en el grupo de pacientes inmunocomprometidos, con cuadros de presentación aguda y con insuficiencia respiratoria preoperatoria, la mortalidad es elevada y deben balancearse muy críticamente los riesgos contra los beneficios en ese grupo de enfermos.
Palabras clave: Biopsia de pulmón; Biopsia toracoscópica; Enfermedad intersticial pulmonar; Neumonía intersticial usual
Abstract
Lung biopsy for the diagnosis of interstitial lung disease. The objective of this study was to determine the morbidity, mortality and diagnostic yield of video assisted thoracoscopy (VATS) and thoracotomy lung biopsy in interstitial lung disease (ILD). Clinical records of 71 patients were retrospectively analyzed. There was no difference in mean hospital stay, intensive care unit stay and duration of chest tube drainage in patients with VATS (n = 52) compared with those undergoing open thoracotomy (n = 17). Complications rate (22.2% vs. 21.0%, p = 1.0000) and operating mortality (9.2 vs. 15.7%, p = 0.2738) were also similar. Overall, complications occurred in 16 patients (22.5%). Thirty-day mortality rate was 11.2% (n = 8). Prevalence of immunosupression (4/8 vs. 9/63, p = 0.0325) was significantly higher in the group of patients who died. No surviving patients had higher values of plasmatic urea (50 ± 20.1 mg/dl vs. 31.2 ± 10.3 mg/dl, p = 0.0013) or lower values of preoperative oxygen saturation (SaO2): 82.7 ± 14.8% vs. 92.8 ± 3.4%, (p = 0.0009). Eleven patients had an acute illness. Those patients did not show a higher complication rate (4/11 vs. 10/45, p = 0.4390) but mortality was significantly higher (4/11, 36.3% vs. 3/45, 7.1%, p = 0.0223). Biopsy allowed a specific histologic diagnosis in 100% of patients and changed therapy in 66.7%. We conclude that surgical lung biopsy is a safe and useful procedure in patients with ILD. However the higher mortality rate in patients with acute symptoms, immunocompromise, or in respiratory failure must be balanced against potential benefits of altering treatment decisions.
Key words: Lung biopsy; VATS; Interstitial lung disease; UIP
El diagnóstico de las enfermedades difusas del pulmón se obtiene generalmente por la combinación de datos clínicos, radiológicos y de estudios complementarios no invasivos o mini-invasivos. Sin embargo, dependiendo del contexto clínico, en un número variable de casos no puede obtenerse un diagnóstico de certeza sin la confirmación histopatológica1, 2. Los distintos consensos sobre enfermedad intersticial acuerdan que en estos casos debe realizarse una biopsia quirúrgica para definir la naturaleza exacta de la enfermedad3, 4. Sin embargo, la práctica clínica muestra que la biopsia quirúrgica se utiliza con poca frecuencia y que hay una marcada tendencia al tratamiento empírico. Probablemente esto esté relacionado con las controversias existentes en la literatura alrededor del verdadero impacto del uso de la biopsia de pulmón en las neumopatías intersticiales idiopáticas5 y a la consecuente prudencia que inclina a valorar muy críticamente los potenciales riesgos de la biopsia quirúrgica. El objetivo del presente estudio fue determinar el rédito diagnóstico de la biopsia quirúrgica en pacientes con enfermedad intersticial difusa del pulmón de etiología indeterminada así como la morbimortalidad asociada al procedimiento a fin de poder determinar el balance costobeneficio del uso de la biopsia quirúrgica en nuestro medio.
Materiales y métodos
Se revisaron en forma retrospectiva los registros clínicos de todos los pacientes a quienes se realizó una biopsia quirúrgica de pulmón para diagnóstico de una enfermedad intersticial difusa del pulmón en el Hospital Británico de Buenos Aires entre julio de 1985 y julio de 2006. Se consignaron los datos demográficos, la enfermedad de base, los síntomas de presentación, las características de la radiografía de tórax y la tomografía, los antecedentes clínicos, la realización de broncoscopia y los estudios de laboratorio preoperatorios. Los pacientes fueron considerados inmunosuprimidos: a) si tenían una enfermedad maligna por la cual recibieron recientemente radioterapia, quimioterapia o tenían alteraciones hematológicas, b) si recibían corticoides en dosis superiores a 20 mg/d o cualquier otra droga inmunosupresora, c) si tenían insuficiencia renal crónica, d) si tenían diagnóstico de síndrome de inmunodeficiencia adquirida del adulto. Se consignó la presencia de oxigenoterapia domiciliaria o asistencia respiratoria mecánica (ARM) previa y la PaO2 y PaCO2 previa al procedimiento. Se registraron las complicaciones, la estadía hospitalaria y la mortalidad operatoria (definida como el deceso hasta los 30 días desde la fecha de la cirugía).
El método de elección utilizado para realizar la biopsia quirúrgica fue la videotoracoscopia (VT). En aquellos pacientes que no toleraban la intubación selectiva con ventilación de un solo pulmón, a causa de su grado de insuficiencia respiratoria o inestabilidad hemodinámica, el abordaje utilizado fue una toracotomía axilar limitada (TAL). La VT se realizó bajo anestesia general e intubación selectiva con tubo de doble luz. Se colocó al paciente en decúbito lateral a 90º y se utilizaron 3 trócares de 12 mm en región axilar. Se tomaron habitualmente dos muestras de biopsia de lóbulos distintos. La elección del sitio de biopsia fue determinada por el área de mayor afectación pero sin signos de panalización franca en la tomografía computada o la radiografía de tórax. Los especímenes de biopsia fueron frecuentemente de 3-4 cm en su diámetro máximo y se envió un fragmento de 1 cm en forma rutinaria a estudio microbiológico. En todos los casos se realizó estudio anatomopatológico por congelación de las muestras para determinar su representatividad. Se usó sutura mecánica utilizando uno o dos disparos de Endo GIA® Universal 12 mm con cartuchos de 45 mm. y agrafes de 4.8 mm. (United States Surgical, a division of Tyco Healthcare Group. Mansfield, MA). La TAL se realizó bajo anestesia general e intubación con tubo de luz única. Se colocó al paciente en decúbito lateral de 45°, realizando la incisión de 7 cm en región axilar a nivel del quinto espacio intercostal. La sutura pulmonar se realizó con un disparo de GIA 80™ de 80 mm y agrafes de 4.8 mm (United States Surgical, a division of Tyco Healthcare Group. Mansfield, MA). Al finalizar la resección de la muestra se comprobó la aerostasia, hemostasia y correcta reexpansión pulmonar, colocando drenaje pleural de 24 F exteriorizado a través de la incisión inferior y conectado a sifón. El drenaje fue retirado al comprobar ausencia de aerorragia, expansión pulmonar completa y débito menor de 200 cm3 en 24 horas.
Las muestras se enviaron al laboratorio de bacteriología para estudio de bacterias, micobacterias y hongos. Las muestras de histopatología fueron procesadas de la manera habitual y se realizó rutinariamente análisis con hematoxilinaeosina, tinción de Gram y técnicas para ácido-alcohol-resistentes y metenamina plata. Se utilizaron coloraciones especiales cuando fueron consideradas necesarias.
Análisis estadístico: Las variables continuas fueron comparadas mediante test t de Student y las comparaciones de proporciones mediante chi cuadrado y test exacto de Fisher. Se utilizó regresión logística para determinar factores pronósticos de mortalidad operatoria. Todas las operaciones fueron realizadas con el programa estadístico SPSS (versión 13.0).
Resultados
En el período 1985-2006 se realizaron 85 biopsias de pulmón para diagnóstico de enfermedad intersticial. Se incluyeron los 71 pacientes en quienes había datos histopatológicos completos. La edad media fue 55.5 ± 14.2 años (rango 19 a 80) y 46.5% de los pacientes eran de sexo femenino (n = 33). Nueve pacientes se estudiaron en un período previo a la disponibilidad de la videotoracoscopía (VT). De los 60 pacientes en que se pudo optar, en 52 pacientes (86.6%) el procedimiento fue por VT. En ningún paciente debió convertirse la VT a toracotomía. La estadía media en terapia intensiva (UTI) fue de 1.2 ± 4.4 días. En 7.0% de los pacientes (n = 5) se requirió internación por más de 48 h en Unidad de Terapia Intensiva (UTI) y 80.2% (n = 57) no fueron derivados en ningún momento a terapia intensiva. El promedio de días de estadía hospitalaria fue 8.9 ± 19.7 días (rango 0 a 148) y 65.7% de los pacientes estuvieron internados 5 días o menos. El promedio de días del drenaje fue 2.6 ± 3.8 días (rango 0-21 días) y en 69.9% el drenaje no estuvo más de 48hs.
En 41.6% (n = 25/60) de los pacientes se había realizado una fibrobroncoscopia que no fue diagnóstica, en los restantes, por contraindicaciones al procedimiento o por la sospecha clínica de neumopatía intersticial idiopática y expectativa de bajo o nulo rendimiento diagnóstico, no se realizó broncoscopia previa. Un 12.8% de los pacientes (n = 9/70) sufrían enfermedad pulmonar obstructiva crónica, 12.7% recibían corticoides (9/71) y 12.8% (9/70) tenían el antecedente de una enfermedad maligna previa o actual. Un 19% de los pacientes (n = 11/56) tuvo como forma de presentación un cuadro de inicio agudo con o sin fiebre en el que no se descartaba la sospecha de infección Las características de los pacientes se detallan en la Tabla 1.
TABLA 1.- Características clínicas de los pacientes
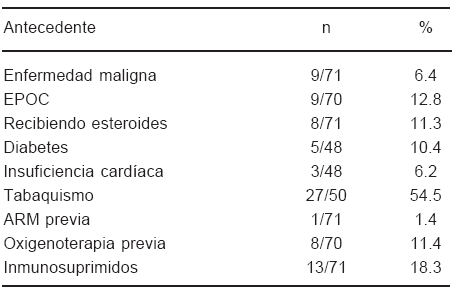
TABLA 2.- Mortalidad operatoria: comparación de los pacientes fallecidos y sobrevivientes.

Se registraron complicaciones en 16 pacientes (22.5%). Las más comunes fueron neumotórax residual en 5 pacientes y aerorragia por más de 48 h en 3 pacientes. Solamente un paciente requirió ARM por más de 48 h (trastorno respiratorio agudo del adulto). Las restantes complicaciones fueron insuficiencia renal aguda (2) insuficiencia cardíaca (1), shock séptico (1) empiema (1) y falla multiorgánica (3). La mortalidad operatoria fue 11.2% (n = 8).
Los pacientes en quienes la biopsia se realiz ó por VT (n = 52) y por toracotomía (n = 17) tuvieron la misma duración de estadía en UTI (1.19 ± 4.40 vs. 1.47 ± 4.83 días, p = 0.8258), de estadía hospitalaria (8.8 ± 20.6 vs. 9.3 ±17.8 días, p = 0.9335) y permanencia de drenaje pleural (2.9 ± 4.1 vs. 1.8 ± 2.4 días, p = 0.1917). La tasa de complicaciones (22.2% vs. 21.0%, p = 1.0000) y la mortalidad (9.2 vs. 15.7%, p = 0.2738) no fueron diferentes.
Los pacientes que presentaron complicaciones (n = 16) tuvieron una estad ía en UTI (4.5 ± 8.6 vs. 0.3 ± 0.8 días, p = 0.0002), en el hospital (24.2 ± 37.2 vs 4.4 ± 5.1 días, p = 0.0001) y un tiempo de permanencia de drenaje pleural (6.4 ± 6.3 vs 1.5 ± 1.5 días, p = 0.0001) significativamente más prolongada. El VEF1 preoperatorio no fue diferente (69.4 ± 14.0 vs 71.7 ± 17.5%, p = 0.4501) y tampoco fue diferente la prevalencia de pacientes recibiendo esteroides (2/16 vs 7/55, p = 1.0000), con EPOC (3/16 vs 8/55, p = 0.6992) o bajo inmunosupresión (6/16 vs 7/55, p = 0.0595. En cambio, la saturación de oxígeno (SaO2) preoperatoria fue significativamente menor en los pacientes que presentaron complicaciones (85.83 ± 12.90 vs 92.08± 3.77%, p = 0.0010).
Ocho pacientes (11.2%) murieron dentro de los 30 d ías de realizada la biopsia. Tres de los 8 pacientes (37.5%) tenían una leucemia aguda y en 4 de los 8 (50%) la sospecha pre-biopsia no podía excluir un cuadro infeccioso. Los pacientes que murieron no fueron diferentes en edad (55.1 ± 14.4 vs 57.4 ±12.6 años, p = 0.6309). La prevalencia de inmunosupresión (4 vs. 9/63, p = 0.0325) fue significativamente superior en el grupo de pacientes fallecidos. Los pacientes fallecidos tuvieron valores preoperatorios más elevados de urea (50 ± 20.1 mg/dl vs 31.2 ± 10.3 mg/dl, p = 0.0013) y menores valores de saturación de O2 (SaO2): 82.7 ± 14.8% vs 92.8 ± 3.4%, p = 0.0009). Entre los 50 pacientes en quienes se tenía dato confiable de SaO2 pre-operatoria, en los que tenían SaO2 ≥ 90% la mortalidad fue 5.5% (2/34) mientras que en los pacientes con SaO2 < 90% hubo una mortalidad significativamente mayor (6/8, 75%, p = 0.0038). En un modelo de regresión logistica, la inmunosupresión (OR 4.0073, IC 0.6184 - 25.9692), la presencia de una enfermedad aguda (OR: 6.7621, IC 1.1302 - 40.4584) y el valor de SaO2 (OR 0.8016, IC 0.6624 - 0.9701) fueron variables independientes predictoras de mortalidad.
En el grupo de los fallecidos los diagn ósticos preoperatorios fueron: neumopatía infecciosa (2), fibrosis pulmonar de origen indeterminado (3), infiltración leucémica vs. infección (1) neumonía intersticial aguda (1) y enfermedad intersticial asociada a artritis reumatoidea (1). Los diagnósticos anatomopatológicos fueron neumonía por CMV (1), daño alveolar difuso (1), neumonía intersticial usual (3), amiloidosis (1), infiltración leucémica (1) neumonía criptogénica en organización (1).
Se analizaron las caracter ísticas de los pacientes operados antes del año 2000 (1985-1999) y después de la publicación de las recomendaciones de la ATS/ERS6. Si bien el número de pacientes operados en ambos períodos fue similar (3.27 ± 2.76 vs. 2.86 ± 3.44 pacientes/ año, p = 0.7672), la proporción de pacientes con UIP fue significativamente mayor en el segundo período (7/35, 20% vs. 11/20, 55%, p = 0.0155) y la tasa de complicaciones significativamente menor (15/49, 30.6% vs. 4.7%, p = 0.0152). No hubo ninguna muerte operatoria en el segundo período.
Quince de 56 pacientes con datos cl ínicos completos tenían fiebre como parte de su cuadro clínico de inicio. Si bien la tasa de complicaciones no fue superior en este grupo (6/15 vs. 9/41, p = 0.1926), la mortalidad fue significativamente más elevada en el grupo de pacientes con fiebre (5/15 vs. 2/39, p = 0.0115). En los 11 pacientes que mostraron un cuadro de iniciación agudo, las complicaciones no fueron más frecuentes (4/11 vs. 10/45, p = 0.4390) pero la mortalidad fue significativamente más elevada (4/11, 36.3% vs. 3/45, 7.1%, p = 0.0223). La tasa de mortalidad de los pacientes no inmunosuprimidos (4/ 60, 6.8%) o con cuadros de evolución crónica (7.1%) estuvo por debajo de la media global (11.6%). La mortalidad operatoria de los pacientes con diagnóstico final de NIU no fue diferente de la de los otros pacientes (3/22 vs. 5/33, p = 1.0000).
El esp écimen de biopsia permitió un diagnóstico histológico definitivo en el 100% de los pacientes, aunque el mismo fue considerado inespecífico en 3.33%. En 66.7% (n = 48) el resultado histopatológico significó un cambio en la conducta terapéutica. Sesenta muestras estuvieron disponibles para revisión en el momento del análisis retrospectivo. Aplicando los criterios actuales de clasificación histopatológica de las neumonías intersticiales, el diagnóstico más común fue el de neumonía intersticial usual (n = 22, 36.6%) (Tabla 3).
TABLA 3.- Diagnóstico histológico de las biopsias obtenidas

Discusión
Los resultados del presente estudio muestran que la biopsia toracoscópica tiene un alto rédito diagnóstico e impacto en la toma de decisiones sobre el tratamiento, pero que en el grupo de pacientes inmunosuprimidos o en insuficiencia respiratoria tiene una mortalidad considerable que exige seleccionar cuidadosamente su utilización.
La biopsia diagnóstica de pulmón puede realizarse a través de una toracotomía limitada o de una toracoscopia7. Varios estudios no aleatorizados han comparado estas técnicas, algunos de ellos sugirieron cierta ventaja comparativa de la VT8-11 fundamentalmente en términos de magnitud de dolor y tiempo de estadía operatoria. Dada la naturaleza retrospectiva de nuestro estudio, no fue posible evaluar la magnitud de dolor ni el impacto sobre la función pulmonar post-operatoria, pero los pacientes sometidos a VT tuvieron el mismo tiempo de estadía en UTI, de estadía hospitalaria y de colocación de tubos de drenaje, tal como fue previamente comunicado por Miller y col. en un estudio alea-torizado en 42 pacientes12. Tampoco difirieron la tasa de complicaciones ni la mortalidad, y la rentabilidad diagnóstica fue comparable demostrando que la VT es una opción segura y confiable. Los tiempos de estadía hospitalaria de nuestros pacientes fueron comparables a los comunicados en la literatura internacional10-13.
Dado que se ha sugerido que el uso de la VT incrementa los costos10 podría alegarse que no hay razones para preferir el uso de la VT en lugar de una cirugía convencional. Sin embargo, cabe señalar como ventajas de la VT que ofrece una mejor accesibilidad intratorácica y más amplia exposición de la superficie pulmonar comparada a la minitoracotomía13, que ha sido demostrada una recuperación post-operatoria más rápida de la fuerza de los músculos respiratorios14, que es potencialmente realizable en forma ambulatoria con alta hospitalaria antes de las 8 horas en más del 70% de los pacientes15 y que es sin duda más fácilmente aceptada por los pacientes, sobre todo para un procedimiento diagnóstico. Pese a estas ventajas, nuestros resultados, como los de Miller, apoyan la hipótesis de que la toracotomía es un procedimiento absolutamente aceptable para la realización de una biopsia y que la limitación tecnológica o financiera no debería modificar la política de las instituciones en cuanto a las indicaciones de la realización de la biopsia.
La tasa global de complicaciones en nuestros pacientes fue elevada: 22.5%. Las complicaciones estrictamente quirúrgicas (aerorragia por más de 48 h en 3 pacientes y neumotórax residual en 5 pacientes) se presentaron en 11.6% de la población. La mayor parte de las complicaciones estuvieron relacionadas con la gravedad de la enfermedad de base y asociadas a menor SaO2 como expresión de gravedad del compromiso pul-monar preoperatorio. La tasa de complicaciones estrictamente quirúrgicas tuvo una prevalencia y distribución similar a la comunicada por otros grupos quirúrgicos16-17.
La mortalidad operatoria en nuestra serie fue del 11.2%. Han sido comunicadas en la literatura, cifras muy variables de mortalidad, algunas muy por debajo de nuestros hallazgos, como por ejemplo las publicadas por el grupo del Papworth Hospital (1.5%)18 o el Royal Bromptom Hospital (3%)19. Sin embargo, las tasas de mortalidad son difíciles de comparar entre las distintas series, debido a la diferente composición de las poblaciones y a la definición de mortalidad operatoria. Por ejemplo, en la serie de Hiatt y col., si bien se consideró que solamente un paciente de un grupo de 68 era una "muerte operatoria", 56% de los pacientes nunca dejaron el hospital20. De manera similar, las series que incluyen solamente pacientes con sospecha de enfermedad inflamatoria intersticial excluyendo pacientes inmunosuprimidos o sospechas de infección tienen, naturalmente, una mortalidad mucho más baja10-21. Cuando las indicaciones de la biopsia incluyen pacientes inmunosuprimidos o en insuficiencia respiratoria, las tasas de mortalidad son aún más elevadas que la que hemos encontrado en nuestro grupo de pacientes. En la serie de Lee y col., en un grupo de 196 pacientes de los cuales 96 tenían enfermedades asociadas a inmunosupresión, la mortalidad a 30 días fue del 24% pese a que los autores consideran que no hubo "mortalidad asociada al procedimiento"22. Nuestra definición de mortalidad operatoria incluyó a todos los pacientes fallecidos dentro de los 30 días de la cirugía. Sin embargo, en la mayor parte de ellos, la causa de la muerte no estuvo directamente relacionada con el procedimiento sino con el empeoramiento progresivo de la enfermedad de base. Esto quedó demostrado por la mayor prevalencia de inmunosupresión (50 vs. 14%) en el grupo de pacientes que fallecieron, así como la presencia de deterioro de la función renal expresada en mayores valores de urea plasmática preoperatoria (50 ± 20.1 mg/dl vs. 31.2 ± 10.3 mg/dl, p = 0.0013) y de insuficiencia respiratoria puesta en evidencia por valores significativamente más bajos de SaO2 preoperatoria (82.7 ± 14.8% vs. 92.8 ± 3.4%, p = 0.0009).
El riesgo conferido por la inmunosupresión ya había sido previamente sugerido por los hallazgos de Lettieri y col.23 y reproduce los datos previos comunicados con la biopsia por toracotomía convencional que revelaron escaso beneficio terapéutico (18%) y cifras elevadas de mortalidad (39%) en los pacientes inmunocom-prometidos24. En estos pacientes los beneficios potenciales deberían ser cuidadosamente balanceados con los riesgos del procedimiento. Al igual que lo comunicado en otras series, otras condiciones de comorbilidad (enfermedad pulmonar obstructiva crónica, diabetes, insuficiencia cardíaca) no estuvieron relacionadas con la tasa de mortalidad de nuestros pacientes.
La influencia de la función pulmonar preoperatoria fue manifiesta en nuestros pacientes. La misma no se pudo poner en evidencia por los valores de la espirometría, lo cual puede deberse a que el número de pacientes con una espirometría cercana a la cirugía era muy pequeño en nuestra serie, pero también a la escasa sensibilidad de la espirometría convencional para detectar riesgo de complicaciones y mortalidad post-operatoria que se ha descripto en otros tipos de cirugía torácica o abdominal25- 26. La presencia de compromiso pulmonar suficientemente severo como para causar alteraciones del intercambio gaseoso, fue un importante predictor de mortalidad operatoria. Los pacientes con SaO2 menor de 90% tuvieron una mortalidad de 75% (comparada al 5.5% de mortalidad de los pacientes con SaO2 igual o superior a 90%, p = 0.0038). Esta alarmante cifra de mortalidad había sido previamente descripta en la biopsia por toracotomía convencional27 habiéndose comunicado diferencias tan marcadas como 50 vs. 2.6% por la sola presencia de insuficiencia respiratoria. El grupo de Carrillo y col. en una serie de 722 pacientes demostró que la PaO2 <48 mm Hg era uno de los predictores más fuertes de mortalidad28. Si bien ha sido comunicado que la mortalidad operatoria asociada a las biopsias de pacientes, con neumonía intersticial usual es mayor29 en nuestro grupo de pacientes, esto no pudo ser demostrado, hallazgo coincidente con las publicaciones más recientes21. Parece evidente que más que el diagnóstico anatomopatológico final, el contexto clínico y la gravedad de la enfermedad son los factores determinantes de la mortalidad. En nuestra serie los pacientes con enfermedades agudas (con cuadros caracterizados por síntomas de menos de un mes de evolución y rápida progresión) tuvieron una mortalidad significativamente más elevada (33.3 vs. 5.1%, p = 0.0115). Puede afirmarse que si se restringe el uso del procedimiento a los pacientes no inmunocomprometidos y con cuadros sugestivos de neumopatía intersticial idiopática, la biopsia toracoscópica es un procedimiento seguro. La selección más rigurosa de los pacientes a ser evaluados mediante biopsia quirúrgica (a punto de partida de nuestra experiencia institucional y en función de los datos que comenzaban a ser publicados en la década del 90) significó una marcada reducción de la mortalidad sin repercusión en la rentabilidad diagnóstica. Nuestros pacientes operados después del año 2000 presentaron una menor tasa de complicaciones (4.7% vs. 30.6% p = 0.0152) y no hubo ninguna muerte operatoria. Esto refleja la distinta conformación de los pacientes seleccionados. Mientras durante los primeros años, los pacientes con cuadros agudos (varios de ellos con sospecha de infección) representaron el 28.5%, en el período post-año 2000 fueron solamente el 4.6% de las indicaciones. Este cambio de perfil de pacientes seleccionados (a pesar de que el porcentaje de pacientes inmunosu-primidos no fue significativamente diferente) redundó en una mayor proporción de diagnósticos de neumopatías intersticiales idiopaticas (55 vs. 20% fueron NIU, p = 0.0155) y en la drástica disminución de la mortalidad.
La biopsia permitió un diagnóstico definido en el 100% de los pacientes. Al menos en 66.7% (n = 48) esto significó un cambio de la estrategia terapéutica. Aunque el diseño de nuestro estudio no permite determinar el impacto de este cambio sobre la mortalidad, de acuerdo al conocimiento actual de las limitaciones del tratamiento en pacientes con NIU30, muy probablemente el evitar tratamientos inútiles y con elevada tasa de efectos adversos31 o el abrir a la posibilidad de nuevas opciones terapéuticas32, puedan significar una marcada reducción en la morbilidad de pacientes con NIU y, eventualmente, un aumento en la sobrevida. La elevada rentabilidad de la biopsia por toracotomía había sido previamente comunicada19- 33 y confirmada luego para la videotoracoscopia34 con porcentajes de diagnósticos definidos de 56 a 94%. La comparación de la exactitud diagnóstica en la literatura es difícil, ya que la definición de diagnóstico "específico" es altamente variable y la composición de la muestra en cuanto a diagnósticos pre-operatorios modifica substancialmente la expectativa del rendimiento histopatológico. En la serie del Brompton Hospital, la biopsia aportó diagnóstico en 94% de los 410 pacientes pero sólo en 83.3% de los inmunocomprometidos19, mientras que el grupo de Qureshi y col. refirió que en sus pacientes en que se obtuvo material adecuado, el 42% había tenido un diagnóstico específico y el 58% un diagnóstico "inespecífico"33. En nuestros pacientes, al igual que en la mayor parte de las series, el diagnóstico más frecuente fue el de neumonía intersticial usual. El enorme valor pronóstico de este diagnóstico, así como las eventuales connotaciones terapéuticas a la luz de los hallazgos actuales, jerarquizan el valor de su utilización.
En conclusión, la biopsia de pulmón por vía toracoscópica es un procedimiento útil y seguro en los pacientes con enfermedad intersticial difusa del pulmón. Sin embargo, en el grupo de pacientes inmunocomprometidos, con cuadros de presentación aguda y con insuficiencia respiratoria preoperatoria, la mortalidad es elevada y deben evaluarse muy críticamente los riesgos contra los beneficios en ese grupo de enfermos.
1. Lee KS, Chung MP. Diagnostic accuracy of thin-section CT in idiopathic interstitial pneumonia. Radiology 2000 215: 918-9.
2. Raghu G, Mageto YN, Lockhart D, Schmidt RA, Wood DE, Godwin JD. The accuracy of the clinical diagnosis of new-onset idiopathic pulmonary fibrosis and other interstitial lung disease: A prospective study. Chest 1999; 116: 1168-74.
3. American Thoracic Society and European Respiratory Society. International multidisciplinary consensus classification of the idiopathic interstitial pneumonias. Am J Respir Crit Care Med 2002; 165: 277-304.
4. Costabel U, King TE. International consensus statement on idiopathic pulmonary fibrosis. Eur Respir J 2001; 17: 163-7.
5. Fishbein MC. Diagnosis: To biopsy or not to biopsy: assessing the role of surgical lung biopsy in the diagnosis of idiopathic pulmonary fibrosis. Chest 2005; 128: 520-5.
6. American Thoracic Society. Idiopathic pulmonary fibrosis: diagnosis and treatment. International consensus statement. American Thoracic Society (ATS), and the European Respiratory Society (ERS). Am J Respir Crit Care Med 2000; 161: 646-64.
7. Ferson PF, Landreneau RJ. Thoracoscopic lung biopsy or open lung biopsy for interstitial lung disease. Chest Surg Clin North Am 1998; 8: 749-62.
8. Bensard DD, McIntyre RC Jr, Waring BJ, Simon JS. Comparison of video thoracoscopic lung biopsy to open lung biopsy in the diagnosis of interstitial lung disease. Chest 1993; 103: 765-70.
9. Ferson PF, Landreneau RJ, Dowling RD, et al. Comparison of open versus thoracoscopic lung biopsy for diffuse infiltrative pulmonary disease. J Thorac Cardiovasc Surg 1993; 106: 194-9.
10. Molin LJ, Steinberg JB, Lanza LA. VATS increases costs in patients undergoing lung biopsy for interstitial lung disease. Ann Thorac Surg 1994; 58: 1595-8.
11. Ravini M, Ferraro G, Barbieri B, Colombo P, Rizzato G. Changing strategies of lung biopsies in diffuse lung diseases: the impact of video-assisted thoracoscopy. Eur Respir J 1998; 11: 99-103.
12. Miller JD, Urschel JD, Cox G, et al. RNA Randomized, controlled trial comparing thoracoscopy and limited thoracotomy for lung biopsy in interstitial lung disease. Ann Thorac Surg 2000; 70: 1647-50.
13. Rena O, Casadio C, Leo F, et al. Videothoracoscopic lung biopsy in the diagnosis of interstitial lung disease. Eur J Cardiothorac Surg 1999; 16: 624-7.
14. Bernard A, Brondel L, Arnal E, Favre JP. Evaluation of respiratory muscle strength by randomized controlled trial comparing thoracoscopy, transaxillary thoracotomy, and posterolateral thoracotomy for lung biopsy. Eur J Cardiothorac Surg 2006; 29: 596-600.
15. Chang AC, Yee J, Orringer MB, Iannettoni MD. Diagnostic thoracoscopic lung biopsy: an outpatient experience. Ann Thorac Surg 2002; 74: 1942-6.
16. Zegdi R, Azorin J, Tremblay B, Destable MD, Lajos PS, Valeyre D. Videothoracoscopic lung biopsy in diffuse infiltrative lung diseases: a 5-year surgical experience. Ann Thorac Surg 1998; 66: 1170-3.
17. Ayed AK, Raghunathan R. Thoracoscopy versus open lung biopsy in the diagnosis of interstitial lung disease: a randomised controlled trial. J R Coll Surg Edinb 2000; 45: 159-63.
18. Ooi A, Iyenger S, Ferguson J, Ritchie AJ. VATS lung biopsy in suspected, diffuse interstitial lung disease provides diagnosis, and alters management strategies. Heart Lung Circ 2005; 14: 90-2.
19. Shah SS, Tsang V, Goldstraw P. Open lung biopsy: a safe, reliable and accurate method for diagnosis in diffuse lung disease. Respiration 1992; 59: 243-6.
20. Hiatt JR, Gong H, Mulder DG, Ramming KP. The value of open lung biopsy in the immunosuppressed patient. Surgery 1982; 92: 285-91.
21. Tiitto L, Heiskanen U, Bloigu R, Paakko P, Kinnula V, Kaarteenaho-Wiik R. Thoracoscopic lung biopsy is a safe procedure in diagnosing usual interstitial pneumonia. Chest 2005; 128: 2375-80.
22. Lee YC, Wu CT, Hsu HH, Huang PM, Chang YL. Surgical lung biopsy for diffuse pulmonary disease: experience of 196 patients. J Thorac Cardiovasc Surg 2005; 129: 984-90.
23. Lettieri CJ, Veerappan GR, Helman DL, Mulligan CR, Shorr AF. Outcomes and safety of surgical lung biopsy for interstitial lung disease. Chest 2005; 127: 1600-5.
24. Kramer MR, Berkman N, Mintz B, Godfrey S, Saute M, Amir G. The role of open lung biopsy in the management and outcome of patients with diffuse lung disease. Ann Thorac Surg 1998; 65: 198-202.
25. Doyle RL. Assessing and modifying the risk of postoperative pulmonary complications. Chest 1999; 115: 77-81.
26. Lawrence VA, Dhanda R, Hilsenbeck SG, Page CP. Risk of pulmonary complications after elective abdominal surgery. Chest 1996; 110: 744-50.
27. Wagner JD, Stahler C, Knox S, Brinton M, Knecht B. Clinical utility of open lung biopsy for undiagnosed pulmonary infiltrates. Am J Surg 1992; 164: 104-7.
28. Carrillo G, Estrada A, Pedroza J, et al. Preoperative risk factors associated with mortality in lung biopsy patients with interstitial lung disease. J Invest Surg 2005; 18: 39-45.
29. Utz JP, Ryu JH, Douglas WW, et al. High short-term mortality following lung biopsy for usual interstitial pneumonia. Eur Respir J 2001; 17: 175-9.
30. Shah NR, Noble P, Jackson RM, et al. A critical assessment of treatment options for idiopathic pulmonary fibrosis. Sarcoidosis Vasc Diffuse Lung Dis 2005; 22: 167-74.
31. Flaherty KR, Toews GB, Lynch JP 3rd, et al. Steroids in idiopathic pulmonary fibrosis: a prospective assessment of adverse reactions, response to therapy, and survival. Am J Med 2001; 110: 278-82.
32. Demedts M, Behr J, Buhl R, et al. High-dose acetylcysteine in idiopathic pulmonary fibrosis. N Engl J Med 2005; 353: 2229-42.
33. Qureshi RA, Ahmed TA, Grayson AD, Soorae AS, Drakeley MJ, Page RD. Does lung biopsy help patients with interstitial lung disease? Eur J Cardiothorac Surg 2002; 21: 621-6.
34. Vansteenkiste J, Verbeken E, Thomeer M, Van Haecke P, Eeckhout AV, Demedts M. Medical thoracoscopic lung biopsy in interstitial lung disease: a prospective study of biopsy quality. Eur Respir J 1999; 14: 585-90.
Recibido: 5-03-2007
Aceptado: 27-06-2007














