Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680versión On-line ISSN 1669-9106
Medicina (B. Aires) v.69 n.4 Ciudad Autónoma de Buenos Aires sep./oct. 2009
ARTÍCULO ORIGINAL
Epidemia de influenza A(H1N1) en la Argentina. Experiencia del Hospital Nacional Profesor Alejandro Posadas
Comisión para la Contingencia de Influenza A (H1N1), Hospital Nacional Profesor Alejandro Posadas
Dirección postal: Dra. Lucrecia Raffo, Hospital Nacional Profesor A. Posadas, Pte Illia s/n, El Palomar 1684 Buenos Aires, Argentina. Fax: (54-11) 4654-7982 e-mail: lucreciaraffo@hospitalposadas.gov.ar
Resumen
Se describe la preparación y la atención médica durante la epidemia de influenza A(H1N1) (junio 2009) en un hospital general de agudos, público, de alta complejidad; con diagnóstico de laboratorio, internación general y cuidados intensivos (UCI). Se elaboró un plan para aumentar la capacidad asistencial, reasignar recursos y garantizar la bioseguridad. La consulta fue 7.1 ± 3.8 veces mayor que en 2006-2008. La detección de casos de A(H1N1) fue confirmada por PCR-RT en 186/486 (38.3%) pacientes internados y en 56/176 (31.8%) ambulatorios. Internados: mediana de edad 20 años; 75% menores de 45 y 32.3% menores de 15. Mortalidad global: 6.8%; 9.1% en los positivos. Adultos: recepción en un área de atención ambulatoria, internación (aislamiento) y ventilación mecánica. Sala general: ingresaron 110 pacientes (5 veces más que 1999-2006) con saturación de oxígeno <96% y/o factores de riesgo (65.5% presentaron asma, enfermedad pulmonar obstructiva crónica, obesidad, embarazo, otros). Radiografía con infiltrados y/o consolidación pulmonar: 97.3%. Hipoxemia significativa: 43.5%. En 21/49 se confirmó A(H1N1), sin diferencias clínico-radiológicas significativas con PCR-negativa/pendiente. Tratamiento: oseltamivir, ampicilina-sulbactam y claritromicina. UCI: fueron ingresados 28 pacientes con neumonía grave (21 con condiciones asociadas). Veinticuatro recibieron ventilación mecánica por síndrome de distress respiratorio agudo, 21 presentaron shock y 8/9 requirieron hemodiálisis por fallo renal agudo. Mortalidad: 14/28; con infección A(H1N1) confirmada 7/14. Niños: 70 con A(H1N1) confirmada fueron internados (27 requirieron UCI, 6 fallecieron). La mediana de edad fue 11 meses; 61.8% con comorbilidades (prematurez, asma, displasia broncopulmonar, cardiopatía congénita). Recibieron oseltamivir y antibióticos. Mortalidad en niños: 8.6%.
Palabras clave: Epidemia influenza A(H1N1); Neumonía; Síndrome de distrés respiratorio agudo; Fallo renal; Ventilación mecánica; Bioética
Abstract
Influenza A(H1N1) epidemic in Argentina. Experience in a National General Hospital (Hospital Nacional Profesor Alejandro Posadas). The preparation and medical care during the influenza A(H1N1) outbreak (June 2009) in a high complexity level, public, general hospital with laboratory diagnosis, general and intensive care (ICU) hospitalization is described. A plan was designed to increase the hospital's surge capacity, reallocate resources and guarantee bio-safety. The number of consultations was 7.1 ± 3.8 times higher than during June 2006-2008. Detection of A(H1N1) cases were confirmed by PCR-RT in 186/486 (38.3%) in-patients and 56/176 (31.8%) out-patients. Median age among in-patients was 20 years; 75% <45 and 32.3% <15. Global mortality: 6.8%; 9.1% among confirmed cases. Adults were directed to a reception area of out-patient care, hospitalization (isolation) and mechanical ventilation. General ward: 110 patients with oxygen saturation <96% and/or risk factors (65.5% had asthma, chronic obstructive pulmonary disease, obesity, pregnancy or other) were admitted (5 times more than in 1999-2006). Chest X-ray showed lung infiltrates and/or lung consolidation in 97.3%. Severe hypoxemia: 43.5%. There were no significant clinical or X-ray differences between 21/49 confirmed and non confirmed A(H1N1) cases. Treatment: oseltamivir, ampicillin-sulbactam, and clarithromycin. ICU: 28 severe pneumonia patients were admitted (21 with associated conditions); 24 with acute respiratory distress syndrome received mechanical ventilation, 21 of them had shock; 8/9 acute renal failure cases required hemodialysis. Mortality: 14/28; 7/14 with confirmed A(H1N1) infection. Seventy A(H1N1) infected children were hospitalized (27 required ICU, 6 of them died). The children's median age was 11 months; 61.8% presented comorbidities (prematurity, asthma, broncho-pulmonary dysplasia and congenital heart disease). Oseltamivir and antibiotics were administered. Children's mortality: 8.6%.
Key words: Influenza A(H1N1) epidemic; Pneumonia; Acute respiratory distress syndrome; Renal failure; Mechanical ventilation; Bioethics
Ha habido en el mundo tantas pestes como guerras y, sin embargo,
pestes y guerras toman a la gente siempre desprevenida
Albert Camus, La peste
La preparación del Hospital
Desde mediados de abril de 2009 el Hospital Nacional Profesor Alejandro Posadas (HNPAP) se involucró en la preparación y después en la asistencia de la epidemia de influenza A (H1N1), lo que generó un cambio de conductas y un aprendizaje. Se relata aquí la preparación del hospital y el fenómeno epidemiológico. Desde el punto de vista clínico se analizan los casos desde el 12 al 27 de junio de 2009, se hizo un corte en esa fecha para poder analizar también la evolución de los pacientes. Hasta esa fecha se internaron más de 300 pacientes con diagnóstico de neumonía de la comunidad.
Se consideraron conjuntamente todos los casos de influenza, ya sean confirmados para el nuevo virus influenza A (H1N1) por PCR-RT (reacción en cadena de la polimerasa en tiempo real), como los negativos y aquellos de los que aún se esperan los resultados, porque no hay diferencias significativas entre estos grupos ni desde el punto de vista de su presentación clínica ni de la demanda asistencial.
Esta experiencia significó un gran esfuerzo de todo el personal; por ello, la autoría corresponde al conjunto del HNPAP.
El HNPAP, situado al oeste del conurbano de la ciudad de Buenos Aires, atiende la consulta espontánea y derivación de un área de 4 000 000 de habitantes, principalmente del oeste y noroeste del conurbano. Es un hospital general de agudos, público, gratuito, y de alta complejidad. Cuenta con 478 camas. En 2008 se registraron 19 738 egresos y 695 000 consultas ambulatorias programadas y de emergencia. Capacita a 280 residentes, a alumnos de medicina y de enfermería de la Universidad de Buenos Aires; además, a técnicos en salud.
Desde septiembre de 2008 se adoptó la modalidad de internación por cuidados progresivos e internación indiferenciada. La internación quedó dividida en cuatro sectores: cuidados críticos, intermedios, especiales y generales, coordinada por una Unidad de Gestión de Internación (UGI).
Desde que la OMS lanzó el alerta sobre la pandemia de influenza por un nuevo virus, por los casos identificados en EE.UU. y México el 24 de abril de 2009, la conducción del hospital inició los planes para adoptar las soluciones oportunas y apropiadas a los mayores y complejos requerimientos de la población. Se consideraron las tres variables que incidirían en las características y gravedad de una pandemia de influenza: 1) la virulencia del virus, no conocida con certeza; 2) la cantidad de personas susceptibles; 3) la capacidad del sistema de salud para dar respuesta asistencial1-8.
Etapa inicial de preparación
El 26 de abril las autoridades del Hospital participaron de la primera reunión realizada en el Ministerio de Salud de la Nación (MSN), y asignaron médicos clínicos para el control sanitario en el aeropuerto internacional de Ezeiza durante tres semanas.
La preparación del Hospital como respuesta a la pandemia implicó las siguientes acciones:
Conformación de un Comité de Preparación para la Pandemia4, 9. Lo integraron el Consejo de Administración, la Dirección, los jefes de Clínica, Pediatría, Terapias Intensivas, Emergencias, Infectología, Neumonología, Epidemiología, Consultorios Externos, Cirugía, Unidad de Comunicación, Unidad de Gestión de Internación, Enfermería, Departamento de Diagnóstico y Tratamiento, Laboratorio, Esterilización, Farmacia, Trabajo Social, Vigilancia, Limpieza, Reconocimientos Médicos y Personal. Participaron, además, los jefes de Diagnóstico por Imágenes, Suministros, Comité de Ética, Mantenimiento, Docencia e Investigación. El objetivo fue organizar de forma efectiva y eficiente los servicios ambulatorios y de internación para reducir el daño, en especial la mortalidad; garantizar la bioseguridad, los insumos y el equipamiento; capacitar, comunicar, contener e investigar.
Elaboración de un Plan Hospitalario y de Guías Clínicas para la asistencia y bioseguridad. Incluido en la página Web del hospital, facilitó el acceso a esta propuesta a otras instituciones de salud6, 9.
Organización de la asistencia. A partir del Plan Nacional de Influenza, se discutió una modalidad para el nuevo sector de aislamiento respiratorio, para cada una de las posibles situaciones que podían presentar los pacientes5:
a) Cuadros leves de gripe con atención ambulatoria convencional; b) Cuadros de gravedad intermedia pasibles de internación abreviada (24 a 48 h) para intervenciones de recuperación y seguimiento ambulatorio o telefónico; c) Cuadros graves que requirieran internación, donde fuera necesario contar con diagnóstico confirmado para agrupar en habitaciones de aislamiento respiratorio; d) Cuadros graves que requirieran asistencia respiratoria mecánica invasiva cuando la capacidad de la terapia intensiva estuviera completa.
El ámbito físico se organizó destinando espacios para consultorios convencionales, habitaciones individuales de internación abreviada y camas de terapia intensiva.
Preparación de la planta física. Se definieron sectores y se realizaron obras de acondicionamiento para permitir el acceso diferenciado desde el exterior, uno para adultos y otro para niños, con áreas de espera, selección de pacientes, consultorios y puestos de observación e internación por cuidados (generales, intermedios y críticos), con capacidad para asistencia respiratoria mecánica invasiva. Se realizaron reformas para ampliar el Laboratorio de Virología e incorporar un lector de PCR en tiempo real (PCR-RT) para diagnóstico.
Preparación de equipamiento e insumos. Se analizó la cantidad y calidad del equipamiento disponible para la atención de pacientes graves y se estimó un techo de 75 puestos de asistencia respiratoria mecánica (niños y adultos). Con estos cálculos se adquirieron 40 respiradores, 25 monitores multi-paramétricos, 30 oxímetros de pulso y cuatro carros de reanimación. Para los insumos considerados críticos se organizó un registro semanal del stock de los sectores Esterilización, Farmacia y Laboratorio. Se reforzaron compras de materiales de bioseguridad, descartables, medicamentos, reactivos de laboratorio y limpieza. Los antivirales fueron provistos por el MSN y resguardados en un depósito en la Dirección. Se designaron responsables de la distribución y almacenamiento de insumos y se calculó el consumo diario necesario para los equipos de de protección individual, según la cantidad de personal de cada sector por turno y se acordaron vías precisas de distribución. El control de los insumos se asignó a los jefes de servicio.
Gestión de recursos humanos. Se formaron equipos de trabajo de médicos, enfermeros, personal administrativo, de vigilancia y limpieza en los nuevos sectores. Se realizaron tres tipos de acciones: se redistribuyó a médicos de Clínica y Pediatría, reduciendo el número de consultorios programados y trasladando médicos de Emergencias a los nuevos sectores de aislamiento. Luego se reasignaron tareas a neumonólogos y gastroenterólogos de guardia en esos sectores. Los turnos nocturnos y de fin de semana se reforzaron con guardias médicas extra. Se incorporaron temporalmente enfermeros y personal de limpieza y vigilancia, y se agregaron jornadas extra remuneradas al personal habitual.
Seguimiento telefónico. Sus objetivos fueron orientar consultas a centros de atención primaria y controlar la evolución de casos de gripe no complicados y evitar controles médicos innecesarios. Posteriormente se agregó un sistema de seguimiento diario de enfermos con neumonía que, por su moderada gravedad, fueron controlados en un plan de asistencia domiciliaria.
Capacitación en asistencia y bioseguridad, comunicación social. Se realizó una reunión inicial informativa con el personal sobre el estado de situación, las medidas de bio-seguridad y la definición de sectores de aislamiento. Se organizaron 12 charlas en distintos servicios no profesionales y con los médicos y enfermeros del servicio de clínica médica y pediatras destinados al sector de triage; se emitieron tres comunicados y dos memoranda con actualización de las normas ministeriales. Se diseñaron dos folletos de prevención y orientación dirigidos a los pacientes y al personal. Se señalizaron los nuevos sectores desde el ingreso al predio del hospital.
Contención. Se organizó un grupo formado por trabajadores sociales, psicólogos y psiquiatras, con el apoyo de la Dirección Nacional de Emergencia Sanitaria y de la OPS/OMS, para intervenir donde se identificaran conflictos, dirigido a los pacientes y al personal3. Las áreas de internación y las unidades de cuidados intensivos de adultos y niños consideraron como muy beneficiosas estas intervenciones.
Sistema de Información. Se organizó un sistema entre el Departamento de Personal y Reconocimientos Médicos para identificar a los trabajadores del hospital con síntomas sospechosos de influenza, para ofrecerles asistencia, tratamiento y contar con información diaria de ausentismo6 (Tabla 1).
TABLA 1.- Preparación del Hospital Nacional Posadas para la pandemia de influenza. Disponibilidad de recursos previos y posteriores a la preparación, 2009

Dificultades de la etapa inicial
En el inicio, surgieron dudas y controversias en el Comité de Preparación para la Pandemia. Por ejemplo: ¿Se debería considerar caso sospechoso a todo paciente con síntomas respiratorios y fiebre, una vez comprobada la transmisión local? Considerando que comenzaba el invierno, ¿eso significaba que los habituales pacientes con EPOC re-agudizado por infecciones, o las personas con neumonías de la comunidad deberían incluirse inicialmente entre los casos sospechosos?, ¿estos pacientes deberían asistirse en los lugares de aislamiento respiratorio junto con aquellos con verdadera influenza?, ¿esto no aumentaría su riesgo? ¿Cómo agruparlos por el diagnóstico clínico? ¿Cómo asignar personal a nuevos sectores sin desatender el resto? ¿Cuándo comenzar la atención diferenciada?
Planificar con incertidumbre es difícil. Las reuniones fueron útiles, contribuyeron a que los responsables de servicios comprendieran el problema y pasaran de la duda, o el descreimiento, al aporte constructivo.
Segunda etapa. Aparición de casos.
Primera ola epidémica
El 28 de abril ingresó el primer caso sospechoso proveniente del aeropuerto de Ezeiza. Fue necesario insistir en las medidas de bioseguridad. El 26 de mayo se atendió el primer caso confirmado, ambulatorio, procedente del extranjero, y el 3 de junio se internó el primer caso confirmado con transmisión local.
A partir de mediados de abril (semana epidemiológica 15) se observó un aumento de consultas por enfermedad tipo influenza (ETI) con predominio de niños, coincidente con el inicio del brote estacional de infecciones respiratorias agudas bajas (IRAB). En la tercera semana de junio (semana 24) se observó un incremento de la demanda de adultos con enfermedad tipo influenza y neumonía, con formas bilaterales, y de niños con neumonía, aunque de menor gravedad clínica. El gráfico con datos del último trienio producido por el Sector de Epidemiología del hospital mostró un pico de consultas por enfermedad tipo influenza (ETI) mayor que el de los años anteriores (Fig. 1). Este aumento de demanda llevó a disponer de nuevas habitaciones para aislamiento respiratorio, con oxígeno, aspiración central y monitores. De esta manera, 89 de 200 camas de cuidados intermedios de adultos, fueron ocupadas por enfermos con neumonía.

Fig. 1.- Media (+2 desvíos estándar) y (-1 desvío estándar) de los consultas por enfermedad tipo influenza 2006-2008 y consultas de 2009. Hospital Nacional Profesor A. Posadas.
Las 17 plazas del nuevo sector se ocuparon con pacientes de cuidados intermedios y críticos (relación 12/5). La asignación de camas para estos pacientes, a cargo de la UGI, fue realizada en principio creando cohortes de pacientes por cuadro clínico y radiología (neumonías bilaterales y neumonía unilateral). La posibilidad posterior de realización de PCR-RT en el hospital permitió cotejar esta agrupación con la etiología viral confirmada.
De igual modo se procedió para la internación indiferenciada en Pediatría. Se destinaron primariamente 12 camas para el aislamiento. Con la creciente demanda, se destinó la mayor proporción de las camas restantes a pacientes con síntomas respiratorios, llegando a representar un 83% de la internación total. Se agrupó por habitación a los pacientes con influenza A, separados de los infectados por virus sincicial respiratorio, adenovirus, metaneumovirus, para-influenza, influenza B y otros, según el resultado del test de inmunofluorescencia directa (IFD), cuyos resultados están disponibles en el día en la Sección Virología del Hospital.
El 18 de junio el Consejo de Administración declaró la Emergencia Institucional y formó un Comité de Crisis con el objetivo de asesorar en la toma de decisiones. Se limitaron las licencias a todo el personal. Se realizaron reuniones semanales de información a todos los jefes de Departamento; luego se agregaron representantes gremiales. La relación con otros efectores de salud se articuló con las Secretarías de Salud y Direcciones de Atención Primaria de los Municipios con mayor afluencia de pacientes al hospital, para descentralizar el control de embarazadas a centros de Asistencia Primaria de Salud. Se participó el 30 de junio de una reunión con efectores de salud provinciales y municipales de las regiones sanitarias vecinas para compartir información y estrategias. Desde el inicio, el Hospital se integró a la Mesa de Trabajo y al grupo de expertos en el MSN. Los sectores de Epidemiología y Laboratorio de Virología informaron diariamente al equipo de dirección, los municipios, regiones sanitarias, provincias y al MSN sobre los nuevos casos de influenza A (H1N1) detectados, ambulatorios o internados (Fig. 2).

Fig. 2.- Resumen secuencial de decisiones y acciones en el Hospital Nacional Posadas y las producidas por organismos nacionales e internacionales (24 de abril al 8 de julio, 2009).
Monitoreo diario de la demanda de atención
Se diseñaron modelos de registro con datos epidemiológicos, clínicos, de mortalidad, de laboratorio, de disponibilidad de camas críticas y generales, de insumos críticos, de personal ausente y de personal con gripe. Además de la ficha de vigilancia epidemiológica nacional, se diseñó una ficha clínica como instrumento de recolección de datos. Esta permitió los primeros análisis acerca de las características de la población afectada, riesgos y aspectos clínicos no conocidos de esta enfermedad1,2. A partir de los primeros 40 casos de neumonía en adultos, se elaboró un algoritmo diagnóstico que fue de suma utilidad para la decisión médica. Este fue incorporado por el Comité de Expertos del Ministerio de Salud como herramienta a difundir en el resto del país. Los indicadores y señales de alarma utilizados respondieron al modelo de registros implementados y a las capacidades informáticas disponibles en el hospital. Permitieron disponer de información básica para identificar los picos de demanda y sus características, el porcentaje ocupacional de camas, la distribución por complejidad y el número de personas en asistencia respiratoria, y por lo tanto la capacidad potencial disponible antes de llegar al techo prefijado, así como el momento de descenso de la primera ola pandémica. Estos datos fueron proporcionados por la UGI, por los informes diarios de Enfermería y por Estadística.
El Sector de Epidemiología dispuso a diario de información sobre el número de casos confirmados y sospechosos de influenza A (H1N1) ubicándolos en un gráfico con los datos de vigilancia de ETI. También agrupó a los fallecidos, que fueron analizados por el Comité de Mortalidad.
Con estos datos, el equipo de dirección conformó un tablero de mando con diferentes indicadores que permitió monitorear las variaciones diarias, facilitando la toma de decisiones y la difusión de la información a los servicios.
A partir del 25 de junio, el Laboratorio de Virología fue otra fuente de información de casos confirmados, así como de identificación de otros virus respiratorios. Esta información mostró que una proporción de pacientes con cuadros clínicos idénticos a los confirmados presentaron PCR-RT negativa para influenza A (H1N1). Se enviaron estas muestras al Instituto Nacional de Enfermedades Infecciosas Dr. C. Malbrán (INEI Malbrán), Administración Nacional de Laboratorios e Institutos de la Salud, (Centro Nacional de Referencia de Laboratorio), y se congelaron otras para su posterior evaluación.
La tarea diaria de la UGI durante la ola pandémica de gripe abarcó: el relevamiento de camas libres en todos los sectores; los requerimientos de internación desde las guardias y sectores de aislamiento de pediatría y adultos, y pases de unidades críticas a pisos de internación indiferenciada; la asignación de camas según la complejidad; el registro de altas de cada sector y la reasignación de camas a nuevos pacientes; la utilización de resultados virológicos para organizar cohortes de pacientes; la evaluación de necesidades de recursos de cada sector; la aceptación o rechazo de derivaciones según disponibilidad de camas; la evaluación de las solicitudes de cirugías programadas. En la gran mayoría de los casos no fue necesario suspender cirugías de pacientes que no requirieran alta complejidad post-quirúrgica en unidades críticas.
La información obtenida, se presenta en las Figs. 3, 4 y 5 que muestran: a) la evolución de las internaciones por causas respiratorias de adultos y niños en el año 2009, donde se observa una curva con ascenso, meseta y descenso similares en ambos grupos; b) la ocupación de camas críticas con asistencia respiratoria mecánica en adultos y niños, en el mismo período; c) la evolución secuencial de la atención ambulatoria, general y de camas críticas. Se observa un incremento de las consultas ambulatorias (casos leves) hasta la semana epidemiológica 25, y un descenso posterior, mientras que las internaciones ascienden en la semana epidemiológica 24 y se mantienen con leve descenso hasta la semana 28. Esto coincide con una demanda sostenida de camas críticas, observándose un pico en la semana 24 con más de 60 ventilados. Es decir, cambia el perfil de los consultantes de síntomas de ETI a neumonías.

Fig. 3.- Evolución de la internación por causa respiratoria de adultos y niños. Hospital Nacional Posadas, 16 de junio a 15 de julio, 2009.
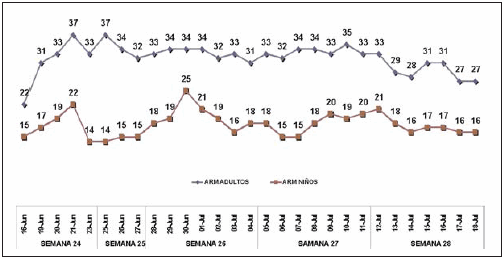
Fig. 4.- Ocupación de camas de cuidados intensivos con asistencia respiratoria mecánica de adultos y niños. Hospital Nacional Posadas, 16 de junio a 15 de julio, 2009.

Fig. 5.- Progresión de la demanda de atención ambulatoria, internación general y de cuidados intensivos entre las semanas epidemiológicas 23 y 28. Hospital Nacional Posadas, 2009.
Del análisis de la evolución de la internación de bajo y mediano cuidado de adultos, surge que al comienzo de la demanda el 21% de las camas estaban ocupadas por pacientes respiratorios. Para la semana 25, éstos representaban el 50% de los internados.
De las internaciones generales en Pediatría, en la semana 24 ya el 50% de las camas estaban ocupadas por pacientes con enfermedad respiratoria, que a la semana 26 superaban el 80% del total. El requerimiento de asistencia respiratoria mecánica (ARM) en adultos y niños aumentó un 75% en 5 días en la semana epidemiológica 24.
Se registraron dos picos en la demanda de ARM en niños: uno en la semana 24 y otro en la 26, permaneciendo hasta el cierre de este informe (semana 28) con un 30% más de casos respiratorios que al comienzo.
En forma preliminar se pueden extraer las siguientes conclusiones:
La preparación del hospital 5 semanas antes de que fuera evidente la circulación local del virus permitió organizar insumos, equipamiento, sectores de aislamiento y asignación de personal para hacer frente al pico de demanda.
La flexibilización del trabajo asistencial en los nuevos sectores de aislamiento (de ambulatorio a cuidado crítico), mantuvo el acceso a la asistencia por cuidados progresivos en las semanas pico. No fue necesario solicitar derivaciones a otros centros y pudieron aceptarse pacientes de otros hospitales.
El registro y análisis de información desde los diferentes servicios ordenó la conducción, aportó al conocimiento de los criterios de severidad iniciales (algoritmo de decisión médica) y sugirió recomendaciones respecto a la ventilación mecánica (VM) de estos pacientes. Su difusión, a través del MSN (Grupo de Expertos) y de sociedades científicas, fue útil para centros con menor experiencia clínica.
La organización de cohortes de pacientes con EPOC re-agudizado y de aquellos con neumonía por influenza fue difícil al comienzo, por desconocimiento de las nuevas formas clínicas graves en personas jóvenes y previamente sanas.
Fue insuficiente la coordinación con otros centros de salud municipales y provinciales. Debiera fortalecerse una red permanente. La disminución significativa de consultas por otros problemas de salud, supone que se recibirán personas con enfermedades más avanzadas en el futuro cercano y una nueva sobre-demanda por otras causas en el período posterior al pico pandémico.
La vigilancia epidemiológica de influenza
En la primavera del hemisferio norte, última semana de marzo, semana epidemiológica (SE) 13 en México10, y mediados de abril (SE 15) en EE.UU.11, se detectaron enfermos por un nuevo virus de influenza que se diseminó rápidamente a todos los continentes. Llamado en un primer momento gripe porcina por estar relacionado con el virus que habitualmente infecta a los cerdos, actualmente se prefiere llamarlo nuevo H1N1, ya que las epidemias de 1918, 1957 y 1968 fueron provocadas por un virus H1N1, que estuvo circulando durante los últimos 90 años12-14.
El 24 y 25 de abril el MSN comunica alertas sobre infecciones respiratorias agudas como todos los años al comenzar la vigilancia estacional. Al mismo tiempo, se alerta sobre la existencia de casos de "gripe porcina" y se difunde por la página web del Hospital para todos los profesionales15. El 30 de abril, SE 17, se redacta en el país el primer instructivo para la detección de enfermos definiéndose caso sospechoso a "toda persona que presente enfermedad respiratoria aguda febril (> 38 °C) en un espectro que va de enfermedad tipo influenza a neumonía y que presente síntomas dentro de los 7 días posteriores a la fecha de su salida de zonas afectadas con transmisión humano-humano sostenida (México, EE,UU. y Canadá.)" o " ...haber tenido contacto con un caso confirmado de influenza A." Se toma material para estudio a todos los sospechosos16. El 11 de junio la OMS declaró la pandemia por el nuevo virus de influenza A(H1N1)17.
El 16 de junio el MSN, mediante el Alerta N° 8 (Alerta DIREPI \ ALERTA \ J10-J18 \ 8.2009), modifica la definición de caso sospechoso para la Ciudad de Buenos Aires y el Conurbano Bonaerense, incluida la ciudad de La Plata, por considerarlas áreas de transmisión extensa, a todos los que tengan los síntomas enunciados, continuando con la definición anterior para el resto del país. Se les tomaba muestra para estudio a los pacientes internados, a los ambulatorios con factores de riesgo y a personal del hospital.
En ese momento la OPS/OMS, consideraba como países de América con transmisión comunitaria sostenida a México, EE.UU., Canadá y Chile. Al 06/07/09 (SE 29) el número de casos atribuidos a este virus en el mundo, registrados en la OMS, era de 94 512 con 429 muertes18.
El 29 de junio se decide realizar toma de muestra sólo a los pacientes internados y a los ambulatorios con neumonía.
El 16 de julio, al difundir la nota informativa N° 3 sobre la gripe pandémica (H1N1) 2009, la OMS comenta que en las pandemias de influenza del siglo XX la difusión de la enfermedad tardó aproximadamente 6 meses, en tanto que el nuevo virus se difundió en 6 semanas19.
Una notificación oportuna necesita: 1) una definición de caso clara y que no cambie durante la vigilancia de un evento creando confusión en el equipo de salud; 2) conocimiento de los síntomas y acceso a la consulta por la población; 3) detección temprana por el equipo de salud, 4) disposición de sus integrantes para notificar y 5) un método de confirmación de laboratorio que haya probado ser sensible, específico y operativo para que sea útil a toda la red sanitaria. Si alguno no se cumple existirá un subregistro que se alternará con un "sobre-registro" de casos, durante los picos epidémicos20. Durante una pandemia se debe realizar además la evaluación integral de los primeros casos de la enfermedad en cada jurisdicción, documentar la propagación geográfica, la evolución epidemiológica, analizar y difundir los cambios en las características genéticas y antigénicas, patogénicas, clínicas, en la sensibilidad a los antivirales (en este caso), adecuar las definiciones de casos, y colaborar en el desarrollo y la adaptación de los algoritmos clínicos y de laboratorio. Ante la presencia de un nuevo microorganismo toda la población es susceptible, por lo que es importante calcular la tasa de ataque y los casos secundarios (contagiados) de los enfermos confirmados21.
El objetivo de este análisis es mostrar la magnitud del aumento del número de consultas por ETI, comparado con los 3 años anteriores, la evolución según SE, las características de los pacientes internados y ambulatorios registrados, hasta la SE 26 inclusive (28/06-04/07) con relación a la confirmación diagnóstica, grupo etario, sexo y lugar de residencia, registrados al 10 de julio de 2009.
Se diseñó una planilla individual de registro de enfermedad tipo influenza, basada en la establecida por el MSN, con datos de nombre, edad, sexo, factores de riesgo, contacto, fecha de comienzo de síntomas y evolución previa a la consulta, confirmación por el laboratorio, tratamiento y evolución.
Se compararon las consultas por enfermedad tipo influenza por SE del año 2009 con las correspondientes a los 3 años anteriores y se calculó el índice epidémico por SE. Se analizaron los casos de internados según resultados de laboratorio, SE, sexo, grupo etario y se calculó la letalidad relacionada con la confirmación.
Para analizar las semanas de las consultas donde el índice epidémico resultó sostenidamente mayor se utilizaron, 1) el diagrama de cajas (box plot) que grafica diferencias en medianas, cuartiles y rangos y 2) se realizó el análisis de varianzas (ANOVA) con la prueba no paramétrica de Kruskal-Wallis para inferir la significación de la diferencia de los datos. Para comparar datos de letalidad en los distintos grupos de internados, se utilizó el método de proporciones. Para realizar los cálculos se utilizaron los programas Microsoft Office Excel 2007® y Statistix 7.
Los datos anuales de la consulta, hasta la SE 26, mostraron que en la SE 4 (25-31/01) hay un aumento por encima de la media de los 3 años anteriores (1.4 veces), y en la SE 15 (12-18/04) esta diferencia es 2.5 veces mayor. A partir de la SE 17 (26/04-02/05) se nota un incremento semanal sostenido, en promedio de 7.1 ± 3.8 (1.7-12.7) veces la suma de los tres años precedentes. El pico máximo se produjo en las semanas 23 y 24. La Fig. 6 muestra el número de consultas por SE en escala semilogarítmica. El índice epidémico fue mayor de 1.24 en la SE 15 (2.14) y en las SE 17-26 con valores que oscilaron entre tres en la semana 20 y 22.62 en la 23.

Fig. 6.- Consultas por enfermedad tipo influenza según semana epidemiológica (SE). Años 2006-2008*. Año 2009 *hasta semana epidemiológica 26. Escala semilogarítmica.
En la Tabla 2 los datos estadísticos de las SE 17 - 26 de los años 2006 a 2009 muestran las diferencias de los valores de este último con los años anteriores y la Fig. 7, el diagrama (box plot), de las semanas 17 a 26 grafica la mediana y los cuartiles 1° y 3° y el rango de los valores. Las diferencias en el número de consultas de estas semanas del año 2009 con respecto a los años anteriores fue altamente significativa (p = 0.0001).
TABLA 2.- Características estadísticas del número de consultas por enfermedad tipo influenza (ETI), SE 17-26. Años 2006-2009

SE: semana epidemiológica.

Fig. 7.- Consultas por enfermedad tipo influenza. Diagrama de cajas. SE 17-26. Años 2006-2009.
En las semanas 15 a 26, de los 486 pacientes internados a los que se les extrajo muestra para estudio virológico, 186 fueron positivos para FLU A(H1N1), 90 (48.4%) varones, 164 tuvieron resultado negativo (45.7% varones), en 11 (5 varones) se detectó FLU A estacional, y en 75 los datos están pendientes. La Fig. 8 muestra la distribución por SE del total de casos internados y los positivos para FLU A(H1N1), se aprecia el mayor pico de positivos en la SE 25 (21-27/06).

Fig. 8.- Total de casos internados por enfermedad tipo influenza y positivos para influenza A (H1N1) según SE. Año 2009 (SE 15-26).
La mediana de edad de los casos positivos internados fue de 20 años, el 75% de los casos era menor de 45 y el 32.3% menores de 15; en los negativos la mediana fue de 41 años, el 75% menor de 57 y el 13.4% pertenecía al grupo etario menor de 15 años. Durante las mismas semanas epidemiológicas los adultos tuvieron menor proporción de resultados positivos que los niños. La Fig. 9 muestra la distribución por grupo etario de los casos positivos y negativos. Cuando se analizó el porcentaje de fallecidos en ambos grupos con el método de proporciones, no se observaron diferencias (p= 0.3877). La Fig.10 muestra los casos internados positivos, negativos y pendientes según SE, año 2009 (SE 15-26).

Fig. 9.- Total de casos internados positivos y negativos según grupo etario. Año 2009, hasta SE 26

Fig. 10.- Casos internados positivos, negativos y pendientes de resultado, según SE. Año 2009 (SE 15-26). Datos sobre 457 pacientes.
Fallecieron 33 pacientes (6.8%), 17 en el grupo de positivos (9.1%), 10 de ellos varones, 10 en el de negativos, 6 de ellos varones (6.1%), y 6 con datos de laboratorio pendientes (8.6%), 3 varones. La media del total de fallecidos fue de 35 ± 23 años (2 días-81 años), la mediana fue de 38 años y el 75% era menor de 53 años, 6 (18.2%) eran menores de 15 años.
De los 176 pacientes ambulatorios a los que se tomaron muestras para estudio virológico, 7 resultaron FLU A estacional, 56 positivos para FLU A(H1N1), 25 (44.6%) varones, la mediana de edad fue de 32 años, el 75% tenía menos de 45 años y 6 (10.7%) eran menores de 15 años, 70 negativos y 43 con datos de laboratorio pendientes.
La Fig. 11 muestra la distribución por procedencia, partido del área metropolitana o ciudad de Buenos Aires, de los 550 casos de pacientes asistidos en que constaba el dato. El 91.3% de los casos procedieron de la zona oeste y noroeste del Gran Buenos Aires y de la Ciudad de Buenos Aires (Fig. 12).

Fig. 11.- Casos estudiados por enfermedad tipo influenza según área (partido) de residencia.

Fig. 12.- Localización de partidos de residencia de casos de ETI atendidos hasta la SE 26. Mapa
La progresión de los casos confirmados, desde el comienzo del brote hasta la cima de la curva, fue en México de cuatro semanas, en EE.UU. de una y en nuestra población de tres, todas enmarcadas en la definición de epidemia explosiva relacionada con la susceptibilidad de toda la población10, 11.
En nuestro hospital la curva de consulta espontánea por ETI mostró un primer pico en la SE 15, que desconocemos si ha tenido relación con el nuevo virus, y luego, desde la semana 17 a la 26 un aumento continuo, con índice epidémico varias veces superior al máximo, y mediana, cuartiles y varianza significativamente mayores a los años anteriores. En la ciudad de Buenos Aires, con datos, del Departamento de Epidemiología del Ministerio de Salud del Gobierno Autónomo de Buenos Aires, actualizados al 22/07/09 (Fuente: Dr. Raúl Forlenza), se observa que el primer aumento de casos se registró en los residentes de la ciudad en la SE 11 (15-21/03), con un incremento continuo a partir de la SE 15, mostrando un mayor porcentaje de residentes con respecto a los no residentes. Se observó el brote en menores de 5 años 2 semanas antes que en nuestro hospital y el aumento de neumonía a partir de la SE 18, en tanto en niños de 5 a 14 años en la SE 20 y de neumonía SE 22, posteriores al comienzo del brote detectado en nuestras consultas. En mayores de 15 años ambas enfermedades tienen un incremento sostenido a partir de la SE 18, tanto en la Ciudad de Buenos Aires como en nuestro hospital. Es de hacer notar que el 6% de los pacientes atendidos en el hospital tenían residencia en la Ciudad de Buenos Aires, frecuencia superior a la habitual en nuestras consultas.
Es posible además, que haya existido un aumento de las consultas por cuadros leves, en una población alarmada, que no hubieran motivado la consulta en años anteriores.
La diferencia de la mediana y los cuartiles de los grupos etarios en los internados positivos y negativos se debió a un alto porcentaje de muestras negativas en los adultos con respecto a los niños, que pudo ser debida a factores técnicos de la toma de muestra o a que los niños son llevados a la consulta rápidamente, facilitando la obtención de muestras positivas. La proporción de muertes en ambos grupos permitió inferir que no existía diferencia significativa entre las dos poblaciones.
No existió diferencia significativa de sexo en el número de internados positivos, negativos o con resultados pendientes, en tanto que el 57.6 % de los fallecidos fueron varones.
El diagnóstico etiológico de influenza.
Rol del Laboratorio
Las muestras remitidas de niños fueron aspirados nasofaríngeos (ANF) obtenidos en solución fisiológica y las de niños mayores y adultos, hisopados nasales y faríngeos (HNF) obtenidos en tubos con medio de transporte viral (Virocult) o en solución de buffer fosfato (PBS). En el caso de pacientes intubados se recibieron aspirados traqueales. Las muestras se conservaron en heladera hasta su envío y se transportaron refrigeradas en triple envase de seguridad hasta el laboratorio. Una vez recibidas con la correspondiente ficha epidemiológica fueron procesadas inmediatamente.
En la primera etapa (hasta el 25/06/09) las muestras de ANF fueron alicuotadas en dos fracciones una para IFD y la otra para el Centro de Referencia. Durante este período el laboratorio de Virología procesó las muestras de ANF y de HNF por IFD. Todas las muestras de adultos y las positivas para influenza A de niños fueron enviadas para realizar la detección de H1N1 al centro de referencia ANLIS-Malbrán.
En la segunda etapa, todas las muestras fueron divididas en tres alícuotas, una para procesar, otra para guardar a -70 °C y la restante para remitir al Centro de Referencia (INEI). Las muestras fueron procesadas por IFD y por PCR en tiempo real (PCR-RT) en el laboratorio de Virología del Hospital
Para IFD las muestras fueron lavadas con PBS, fijadas con acetona fría y coloreadas con anticuerpos monoclonales específicos marcados con fluoresceína (Panel Respiratorio de Chemicon) para detectar influenza A (FLU-A), virus sincicial respiratorio (VSR), adenovirus (ADV), influenza B (FLU-B) y parainfluenza 1,2 y 3 (PINF). La observación se efectuó en microscopio de Axiostar Plus (Carl Zeiss).
Para PCR-RT se utilizó el protocolo del CDC para Influenza A swine H1N1 que incluye un panel de cuatro juegos de primers y sondas de hidrólisis doblemente marcadas (Taqman) que permite la detección y caracterización del virus de influenza porcina en muestras respiratorias. El set de primers y sondas de influenza A está diseñado para la detección de virus de influenza A universal. El de swine-influenza A está diseñado para detectar específicamente los virus de influenza A porcina. El de swine H1 está diseñado para detectar H1 porcina. El set de primers y sondas de RNAsa P amplifica el gen que codifica para esta enzima que actúa como control interno, cuya positividad asegura la correcta extracción y la ausencia de inhibidores en la muestra. La extracción de ARN de todas las muestras se realizó con columnas Qiamp viral RNA (Qiagen) y la amplificación en un equipo IQ5 (BIO RAD).
Se realizó IFD en todas las muestras de ANF y en una pequeña cantidad de muestras de HNF de adultos y PCR-RT en todas las de ANF positivas para FLU-A por IFD y en las negativas con alta sospecha clínica o pertenecientes a pacientes inmunocomprometidos. Los HNF fueron todos procesados por PCR-RT, independientemente del resultado de la IFD 22-25.
Test rápido (TR). Se ensayó el método inmunocromatográfico QuickVue Influenza A+B (TR) (Quidel) para detección del virus de Influenza A y B, empleando para ello 50 reacciones donadas por el fabricante. El procesamiento se realizó siguiendo las recomendaciones del fabricante en muestras seleccionadas positivas para FLU-A y/o FLU-B por IFD o positivas para H1N1 por PCR-RT, y también en muestras negativas por ambos métodos. Se procesaron 6 controles y 44 muestras, de las cuales 27 eran ANF del área de pediatría y 17 HNF del área de adultos.
De las 491 muestras de ANF procesadas para virus respiratorios por IFD en las semanas epidemiológicas 23 a 27 del 2009 resultaron positivas 331. La distribución de los positivos según la edad se detalla en la Tabla 3. Durante el mismo período se recibieron 74 HNF y resultaron positivos por IFD 14. La distribución por edades se observa en la Tabla 4.
TABLA 3.- Número de muestras de aspirado nasal faríngeo (ANF) procesadas y positivas por inmunofluorescencia directa (IFD) para los virus respiratorios en los distintos grupos etarios, en las semanas epidemiológicas 23 a 27 del 2009

pos: positivos, ADV: adenovirus; FLU-A: influenza A; FLU-B: influenza B; PINF: para-influenza 1, 2 ,3; VSR: virus sincicial respiratorio.
TABLA 4.- Número de muestras de hisopado nasal faríngeo (HNF) procesadas y positivas por IFD para los virus respiratorios en los distintos grupos etarios, en las semanas epidemiológicas 23 a 27 del 2009

pos: positivos, ADV: adenovirus; FLU-A: influenza A; FLU-B: influenza B; PINF: para-influenza 1, 2 ,3; VSR: virus sincicial respiratorio.
Durante la segunda etapa, desde 25/06/09 al 11/07//09, se realizó PCR-RT a 364 muestras de HNF de pacientes adultos y a 163 ANF de pacientes pediátricos, 65 con FLU-A positivo por IFD y 98 con IFD negativa, pero con cuadros clínicos graves, antecedentes de contacto o inmunosuprimidos. El número de positivos para influenza A(H1N1) swine y para-influenza A estacional en cada grupo se muestra en la Tabla 5.
TABLA 5.- Muestras procesadas por PCR-RT desde el 25/06/09 al 11/07/09 y positivos obtenidos

La Tabla 6 muestra los resultados obtenidos del procesamiento en paralelo de muestras por el TR, IFD y PCR-RT.
TABLA 6.- Resultados obtenidos por el TR comparados con IFD y con PCR-RT

PCR-RT.: PCR en tiempo real; IFD: Inmunofluorescencia directa, TR: Test rápido; NRZ: no realizado;+ positivo; - negativo, FLU-A: influenza A; FLU-B: influenza-B.
En la Fig. 13 se muestra la distribución etiológica de todos los virus respiratorios por SE del año 2009, y en la Fig. 14 lo mismo para el 2008. En las Figs. 15 y 16 se compara la distribución de FLU-A y RSV en los diferentes grupos etarios de niños en los años 2009 y 2008 respectivamente.

Fig. 13.- Distribución etiológica de todos los virus respiratorios por semana epidemiológica del año 2009 expresado en porcentaje del total de muestras recibidas para cada semana. ADV: adenovirus; FLU A: influenza A; FLU B: influenza B; PINF: para influenza, RSV: Virus sincicial respiratorio.

Fig. 14.- Distribución etiológica de todos los virus respiratorios por semana epidemiológica del año 2008 expresado en porcentaje del total de muestras recibidas para cada semana.

Fig. 15.- Comparación de FLU-A y RSV en el 2009 en los diferentes grupos etarios de pacientes pediátricos. FLU A: influenza A. RSV: virus sincicial respiratorio.

Fig. 16.- Comparación de FLU-A y RSV en el 2008 en los diferentes grupos etarios de pacientes pediátricos. FLU A: influenza A; RSV: virus sincicial respiratorio.
Se observan diferencias en el número de resultados positivos obtenidos tanto por IFD como por PCR-RT entre muestras de adultos y de niños. En el caso de los adultos, el 33% de las muestras procesadas por PCR-RT resultó positiva, mientras que en los niños resultaron positivas el 59% de las muestras. Esto se lo podríamos atribuir al tipo y calidad de la muestra, al momento de la toma y al nivel de excreción viral. No se conoce y se está investigando el número de días en que la PCR continúa positiva a partir del inicio de los síntomas. Posiblemente la consulta -y la toma de las muestras- sea más tardía en pacientes adultos que en niños. Recordemos que las muestras de adultos corresponden a neumonías graves internadas, y por lo tanto con tomas de muestra alejadas del inicio de los síntomas respiratorios. Además, el ANF, usado en niños, tiene mejor rendimiento que el HNF, empleado en adultos. Esto se ve claramente cuando se analizan muestras por IFD; así, entre las 74 muestras de HNF en las que se realizó IFD sólo resultaron positivas 14 (18%); mientras que de las 491 muestras de ANF procesadas por IFD (SE 23 y 27) fueron positivas 331 (67%).
Si analizamos lo ocurrido con los ANF de pediatría se ve que, si bien todas las muestras con IFD positivas (65) resultaron positivas por PCR-RT, esta última técnica permitió detectar 32 muestras de las 97 que tenían IFD negativa, sugiriendo que estos pacientes tendrían un nivel menor de excreción viral que no permitiría detectar el virus por una técnica menos sensible, como IFD, pero sí por PCR-RT. De manera que el uso aislado de IFD produciría resultados falsos negativos en algunas muestras.
Por otra parte, muchas de las muestras de adultos que se consideraron negativas por PCR-RT presentaron curvas de crecimiento exponenciales importantes pero que no llegaban a tres logaritmos en los target de M swine y H1 swine generando dudas en la interpretación. Estas muestras podrían contener variantes del virus y son motivo de actuales estudios. Por lo tanto, los resultados deben ser interpretados con precaución, teniendo en cuenta la presentación clínica, ya que la sensibilidad de la PCR no es total. Por ello se debe contar con métodos adicionales de diagnóstico, como cultivo y secuenciación.
Se determinó durante este período una alta prevalencia de A (H1N1) comparada con influenza A estacional: como podemos observar, de los pacientes adultos con FLU-A, más del 90% correspondió al virus A (H1N1), y en pediatría el 98% correspondió a dicho virus.
Se apreciaron diferencias en la distribución etiológica de los virus respiratorios durante las semanas 23 a 27 con respecto al año anterior. Comparando los gráficos de barras de las Figs. 13 y 14, datos de los años 2009 y 2008 respectivamente, se observa un incremento en 2009 de la frecuencia de detección de FLU-A en todas las SE, con un pico en la semana 25. Asimismo, se observa una menor frecuencia de detección para RSV y una disminución en la detección del resto de los virus respiratorios.
Se evidenciaron también diferencias en la detección de FLU-A y RSV en niños pertenecientes a distintos grupos etarios durante las semanas 23 a 27 en 2009 comparado con temporadas anteriores. Aquí se muestra la comparación con 2008. Como se observa en las Figs. 15 y 16, en el año 2009 hay una mayor frecuencia de detección de FLU-A en todas las edades, principalmente en los niños mayores (entre 5 y 14 años) en los que los porcentajes de detección superan los de RSV, contrariamente a lo ocurrido en el 2008.
En la prueba del TR, de las 19 muestras de ANF positivas por IFD y PCR-RT para FLU-A, sólo 14 (74%) resultaron positivas por el TR. De los 5 ANF positivos para FLU-B por IFD ninguno resultó positivo por TR. En cambio, de los 15 HNF procesadas que fueron positivas para influenza A.(H1N1) o influenza A estacional por PCR-RT, solo 3 (20%) arrojaron resultados positivos por el TR. Todas las muestras negativas tanto por IFD como por PCR-RT resultaron negativas por TR.
En resumen, de las muestras positivas por otros métodos (34) el TR sólo detectó el 50% (17) para FLU-A y de las positivas para FLU-B no detectó ninguna. De acuerdo a estos resultados creemos entonces que el TR no resultaría un método apropiado para el tamizaje del virus influenza A y B, por lo menos durante la pandemia, ya que se observó un gran número de falsos negativos tanto para FLU-A como FLU-B. Esto coincide con lo observado por otros autores26, 27.
La epidemia de influenza A (H1N1) y la internación en sala general del Hospital
El esquema de contingencia elaborado por la Dirección del Hospital comprendía la atención ambulatoria, de emergencia y de internación (tanto en sala general como en cuidados intensivos). Gracias a esas previsiones el sistema no se vio desbordado cuando se produjo la afluencia masiva de afectados. Todos los pacientes fueron atendidos en lapsos razonables y no hubo déficit de camas generales para su ingreso. Sí hubo reducciones en operaciones programadas, y en la atención de otras enfermedades no urgentes. Esto último se dio en gran medida en forma espontánea, porque la población enterada de la situación evitó concurrir al hospital salvo que le fuera imprescindible.
Luego de la aparición del primer caso positivo en el hospital (a principios de junio) y el incremento notable de consultas por afecciones respiratorias, se tomó la decisión de efectuar estudios virológicos a todo paciente con estas características que presentara signos de gravedad. Hasta ese momento sólo se estudiaba a aquéllos con posibles contactos, según las directivas de las autoridades nacionales. En los 16 días que comprende el período entre el 12 y el 27 de junio de 2009 inclusive, se internaron en las salas generales de adultos del Hospital 110 pacientes con cuadros respiratorios agudos graves. En el área ambulatoria eran evaluados según el algoritmo de contingencia.
Se internaron aquéllos con saturación de oxígeno menor a 96% y los que presentaban factores de riesgo aunque tuvieran una cifra mayor. Los que tenían insuficiencia respiratoria grave al ingreso permanecieron en el área de aislamiento de emergencia o pasaron a la unidad de cuidados intensivos y no fueron incluidos en este análisis. A todos se los trató al ingreso con oseltamivir 75 mg/12h, ampicilina-sulbactam 1.5g/6h y claritromicina 500 mg/12h (azitromicina 500 mg/d en las embarazadas), independientemente de las diferencias en el cuadro clínico o radiológico que presentaran. Se elaboró una base de datos donde se registró la edad, el sexo, los días de síntomas previos a la consulta que motivó la internación, las enfermedades previas u otros factores de riesgo (obesidad, embarazo), la pO2 registrada en el primer estudio, la relación entre esa pO2 y la fracción inspirada de oxígeno (PAFI), los resultados de la búsqueda viral y bacteriana (hemo-cultivos y esputo) y la evolución.
De los internados, 54 eran hombres (49%). La edad promedio fue de 45 años en ambos sexos, con extremos de 15 y 90 años. Treinta y ocho pacientes (34.5%) no presentaban enfermedades asociadas ni otros factores condicionantes de la evolución conocidos. En el resto, los factores de riesgo más importantes en orden decreciente fueron: asma en 18, enfermedad pulmonar obstructiva crónica en 10, obesidad en 8, embarazo en 6, HIV en 5, diabetes en 5 y cardiopatía en 5.
La radiografía de tórax presentó infiltrados intersticioalveolares bilaterales en 51 (46.3%) y consolidación bilateral en 16 (14.5)%, y el resto otro tipo de infiltrado. En tres casos la radiografía de tórax fue considerada normal (2.7%). Tres de los cuatro con virus estacional tenían infiltrados bilaterales. La relación entre pO2 y fracción inspirada (PAFI) fue menor a 300 en 38 (34.5%) e inferior a 200 en 10 (9%). La cifra de pO2 no se analizó pues gran parte de los pacientes ya estaban tratados con oxígeno cuando se determinó.
En 49 pacientes se obtuvo el resultado de los hisopado de fauces y nasal siendo positivos para virus A (H1N1) 21 casos (42%) y negativo el resto. En 4 se observaron virus estacionales y por diversas causas no tenemos resultados de 57. Sólo en dos hubo hemocultivos positivo, de ambos se aisló neumococo.
De acuerdo al resultado de la PCR-RT se distinguieron tres grupos para analizarlos comparativamente: con PCR positiva, negativa y sin resultado. Como se puede observar en la Tabla 7, no se observaron diferencias significativas entre los grupos. Para este análisis se descartaron las 4 personas de las que se aislaron virus estacionales.
TABLA 7.- Comparación entre poblaciones de pacientes según resultado de PCR-RT para virus influenza A (H1N1) positivo, negativo o no obtenido

*: Distribución de edades, de 15 a 24 años:15 pacientes; de 35 a 34: 18; de 33 a 44: 19; de 45 a 54: 23; de 55 a 64: 16; =65 años: 19.
PAFI: índice que relaciona la presión arterial de oxigeno y la fracción inspirada de oxigeno.
Falleció un paciente con retraso madurativo grave y múltiples internaciones previas por problemas respiratorios, del que se carece de resultado del análisis de hisopado. Cuatro pacientes fueron derivados a terapia intensiva (con recuperación posterior) y el resto fue dado de alta con 5 días de promedio de estadía (esta última cifra es estimativa ya que algunos pacientes seguían internados, aunque por causas no relacionadas con su situación respiratoria). De los que pasaron a cuidados intensivos uno era positivo, uno negativo y dos sin resultado. Todos tenían factores de riesgo: 3 obesidad y 1 embarazo, 3 de ellos presentaban una relación entre presión arterial de oxigeno y fracción inspirada de oxigeno (PAFI) inferior a 300 e infiltrados intersticio-alveolares bilaterales y un paciente condensación unilateral. La derivación se concretó a los 2 días como promedio.
Hasta el final de este período los estudios para virus eran enviados al Instituto Malbrán. Recién a partir de esa fecha se contó con PCR-RT en el hospital. Está establecido que la búsqueda de virus de influenza por PCR es el estudio adecuado por su alta sensibilidad28. Pero eso es válido para los virus conocidos y puede no serlo para el actual. Por otro lado, no existen actualmente pruebas serológicas válidas. Lo que resulta evidente es que no hay diferencias entre las tres poblaciones en los parámetros analizados. Las manifestaciones clínicas no alcanzan especificidad suficiente para separar poblaciones29. Por otro lado, la comparación del número de internaciones con los datos históricos y los patrones radiológicos que se encontraron hacen suponer que gran parte de la población atendida se encontraba afectada por el virus A (H1N1), independientemente del resultado del estudio virológico.
Para tener datos comparativos sobre la cantidad de pacientes se analizaron las internaciones acaecidas en el mes de junio entre los años 1999 y 2006 que fueron dadas de alta con diagnóstico de neumonía aguda de la comunidad, enfermedad obstructiva crónica re-agudizada y asma. Se tomó esa población para cubrir el mayor espectro de internaciones por cuadros respiratorios agudos. La cifra histórica de internaciones con esas enfermedades en ese mes es extremadamente variable oscilando entre 18 y 65 casos (promedio 39 pacientes). La cifra actual, 110 en 16 días, implica 5 veces más pacientes que los esperados.
Cerca de la mitad de los casos (46.3%) presentaban infiltrados intersticio-alveolares bilaterales, algo excepcional en las neumonías habituales, por lo que se puede suponer que la casi totalidad de estos se debían al nuevo virus. Además, en los pacientes positivos se encontraron también infiltrados de otro tipo en la misma proporción que en los negativos.
Se pueden hacer distintas valoraciones, pero es difícil definir el número de casos de influenza A (H1N1) reales que se atendieron. Parece retrospectivamente que ante la ausencia de elementos diagnósticos que permitan una distinción, la decisión de tratar a todos con antivirales fue correcta.
La distribución por edades muestra como en México13 un neto predominio de menores de 65 años (91 sobre 110) y una gran diferencia con la situación habitual de epidemias de influenza estacional en que es esperable que el 50% corresponda a mayores de esa edad30, 31.
Otro de los datos a remarcar es la buena evolución de la mayoría de los pacientes apenas iniciado el tratamiento. Esa buena evolución clínica se daba aun con la persistencia de los infiltrados radiológicos sin aparente modificación. Sólo pasaron a cuidados intensivos cuatro pacientes dentro de las 72 horas de ingresados y uno de ellos a las pocas horas del ingreso. La mayoría de los pacientes que fueron a ese servicio lo hicieron directamente desde la guardia. Parecería que los casos graves ya lo eran a su arribo al hospital y que una medicación rápida podría ser esencial. Tal vez una consulta temprana (el promedio fue 5.5 días) hubiera evitado internaciones.
A continuación se presenta el esquema de atención seguido en la emergencia:
A su llegada al Hospital los pacientes eran recibidos en una zona especial con varios consultorios y estaciones de aislamiento. En el predio externo, así como en cada entrada, se colocaron carteles indicativos. Se aleccionó al servicio de vigilancia para una información adecuada. El lugar de atención, ubicado en un extremo de la planta baja, está en conexión directa con el resto del Hospital aunque adecuadamente aislado y con una zona de ingreso única para este tipo de enfermedad. Las habitaciones individuales cuentan con oxígeno y aspiración central, monitores y respiradores.
La observación de los primeros 46 casos de neumonía permitió identificar los signos clínicos de gravedad y elaborar un algoritmo de conducta (ver www.hospitalposadas.gov.ar) El mismo se basa esencialmente en la saturometría de pulso y la auscultación pulmonar. Todo paciente con una saturación inferior a 96, o que presentara estertores a la auscultación era estudiado con una radiografía de tórax (que se realizaba en la misma zona de atención), un hisopado de fauces y nasal, y un examen de laboratorio de rutina, aunque no impresionara como gravemente comprometido. Al resto de los pacientes con
síntomas gripales se les indicaba oseltamivir y se los enviaba a su domicilio con pautas de alarma y contacto telefónico.
Los pacientes estudiados eran luego derivados según su situación y siguiendo las recomendaciones internacionales, a una sala general o a terapia intensiva. Aquéllos que pudieran ser controlados ambulatoriamente eran seguidos mediante contacto telefónico a las 24 y 48 horas y con una nueva consulta a las 72 horas. Algunos pacientes fueron ventilados en esas estaciones de aislamiento ya que las camas de cuidados intensivos fueron insuficientes, pero siempre hubo profesionales capacitados en cuidados intensivos, con la infraestructura necesaria.
Infecciones graves por el virus de influenza A (H1N1) en cuidados intensivos
El día 11 de junio, coincidiendo con la declaración de Fase 6 de pandemia por parte de la OMS, se envían al Instituto Dr. Carlos G. Malbrán (ANLIS) las primeras muestras que mostraron resultados positivos para el virus en pacientes adultos del HNPAP. Una de las muestras correspondía a la primer paciente internada en la Unidad de Terapia Intensiva de Adultos con diagnóstico de influenza A (H1N1); la enferma había ingresado el 7 de junio y, luego de recibir ventilación mecánica (VM) durante una semana y oseltamivir, evolucionó favorablemente y fue dada de alta del hospital en buenas condiciones.
Acerca de la internación de pacientes gravemente enfermos en la pandemia de influenza actual13, Pérez Padilla y col., del Instituto Nacional de Enfermedades Respiratorias de la Ciudad de México publicaron un informe10 sobre los primeros pacientes internados en la Unidad de Cuidados Intensivos de esa institución. En un período de 30 días se internaron 18 pacientes con neumonía bilateral e insuficiencia respiratoria, 12 de los cuales requirieron VM. El 90% de los pacientes tenían menos de 52 años. El síndrome de distrés respiratorio agudo (ARDS) que presentaban era muy grave y se requirieron niveles elevados de presión positiva al fin de espiración (PEEP) para ventilarlos adecuadamente. La mitad de los pacientes requirieron drogas vasoactivas por shock. Fallecieron 7 de los pacientes que requirieron VM (58.1%).
Estos resultados son similares a los publicados sobre los pacientes graves tratados durante la pandemia de gripe aviar A (H5N1)32, que cursaron con ARDS y alta frecuencia de disfunción multiorgánica. La mortalidad de los que requirieron internación en Cuidados Intensivos fue superior al 50%33.
Se describen aquí las características demográficas y clínicas de los primeros pacientes ingresados en la Unidad de Cuidados Intensivos de Adultos (UCIA) del Hospital con insuficiencia respiratoria aguda y disfunción multiorgánica atribuida a influenza A (H1N1), y su evolución y resultados. Se describen también las modificaciones estructurales y funcionales que se generaron en el Hospital para responder a esta demanda.
Se realizó el análisis retrospectivo de los pacientes ingresados en las UCIA del Hospital entre los días 3 y 27 de junio de 2009, que presentaron un cuadro clínico de enfermedad tipo influenza con neumonía grave e insuficiencia respiratoria aguda, en el contexto del comienzo de la epidemia de influenza A (H1N1) en Argentina. El Hospital cuenta en la UCIA con 26 camas polivalentesno coronarias (10 camas de Terapia Intensiva y 16 camas de Terapia Intermedia).
Durante el período del estudio fue admitida en el hospital una importante cantidad de pacientes con neumonía adquirida en la comunidad (NAC) que reunían criterios de gravedad. Los enfermos más comprometidos fueron ingresados en la UCIA, mientras que otros no analizados en este estudio recibieron cuidados intensivos en otros sectores del hospital. En ese período, 28 pacientes que reunían los criterios de inclusión fueron referidos a la UCIA por hipoxemia grave, ARDS establecido o por la incapacidad de lograr parámetros gasométricos adecuados con las modalidades convencionales de VM36, 37 iniciada en otras áreas del hospital. Se registraron los datos disponibles de estos pacientes hasta el día 13 de julio de 2009. Se efectuaron los estudios clínicos, de imágenes y bioquímicos habituales en los enfermos con fallos orgánicos.
Se tomaron muestras de hisopado nasofaríngeo para investigación de virus de influenza por IFD. En aquellas muestras que fueron positivas para influenza A y en las que resultaron negativas para virus respiratorios se solicitó la determinación de influenza A (H1N1) por PCR-RT. En dos de los pacientes cuya muestra de hisopado fue negativa para influenza A (H1N1) se reiteró el resultado negativo cuando se repitió la PCR-RT en muestras obtenidas por aspirado traqueal.
En la UCIA todos los pacientes fueron tratados con oseltamivir, en dosis adecuada a la función renal. Inicialmente se lo utilizó a 150 mg/día (12 enfermos), mientras que a posteriori se les administró una dosis de 150 mg de oseltamivir cada 12 horas (14 pacientes), siguiendo las recomendaciones publicadas en 2006 por la OMS para casos de neumonía asociada a virus de influenza A (H5N1)33, 35. Dos pacientes recibieron 150 mg/día al comienzo de su tratamiento, y el doble de esa dosis posteriormente. Además, el tratamiento empírico inicial incluyó ampicilina sulbactam y claritromicina para extender la cobertura a otros posibles agentes etiológicos de la NAC grave. Dos de los pacientes recibieron metilprednisolona en altas dosis precozmente.
Ante la llegada masiva de pacientes relacionados con esta pandemia y dada la sobrecarga asistencial que se produjo, se adoptaron pautas para facilitar el manejo del ARDS y de la VM36, 37. Las principales fueron las siguientes: restringir el uso de ventilación no invasiva a los improbables casos que presentaran buena respuesta inicial; secuencia de intubación rápida para minimizar el riesgo de dispersión de inóculos virales durante la maniobra; circuito del respirador con sistemas cerrados de aspiración para minimizar el desreclutamiento por caída de la PEEP; prescindir de una restricción de aporte de volumen de líquidos indebida y de inducir un balance negativo con diuréticos para minimizar los riegos de instalación de fallo hemodinámico y de fallo renal agudo; ventilación protectiva con PEEP fijada por criterios mecánicos para mantener el pulmón abierto o -en su defecto- por la fracción inspirada de oxígeno requerida36, 38 comenzar la VM con la modalidad de control de presión para facilitar el mantenimiento de presiones de ventilación moderadas (presión de fin de inspiración menor de 30 cm H2O), y volúmenes pequeños (volumen corriente de alrededor de 6 ml/kg de peso teórico); en presencia de acidemia adoptar como valores objetivo para la oxigenación los de la PaO2 (55-80 torr) en lugar de los de la SaO2, dados los cambios de la curva de disociación de la hemoglobina secundarios a la acidosis respiratoria; restar jerarquía al objetivo de reducción de la fracción inspirada de oxígeno; frecuencias respiratorias altas (hasta 35 ciclos/min) para controlar la hipercapnia; utilizar maniobras de reclutamiento, ventilación en posición prona o insuflación de gas traqueal, de acuerdo a la necesidad39; permisividad para la utilización de bloqueantes neuromusculares, dada la dificultad para el manejo de la VM.
Incremento de la capacidad de atención de pacientes agudos graves
Considerando los antecedentes mencionados, la primera previsión que se tomó para enfrentar la pandemia de influenza por virus de influenza A (H1N1) fue mejorar la capacidad de respuesta a la demanda de pacientes agudos graves: incremento del número de camas de Cuidados Intensivos y provisión de nuevo equipamiento necesario para atender estos pacientes. Hasta el 27 de junio se incorporaron 19 respiradores microprocesados, 13 monitores multiparamétricos y oxímetros de pulso. Además, se tramitó la incorporación de personal, principalmente enfermería capacitada, y los insumos necesarios para atender estos pacientes.
Además de las 26 camas con que contaban la UCIA, se habilitaron 8 nuevas camas de Terapia Intensiva en un sector quirúrgico del hospital que contaba con instalación de oxígeno, aire comprimido y aspiración central en cada cama. El Hospital acondicionó un sector para la internación inicial de pacientes con patología respiratoria aguda, con aislamiento, provisión de gases centrales y respiradores microprocesados, localizado en la cercanía del área de Emergencias.
Para las áreas nuevas destinadas a la atención de pacientes con compromiso de las funciones vitales se dispuso la cobertura con médicos intensivistas de planta y de guardia, capacitados para atender pacientes con disfunción multiorgánica y requerimiento de VM.
Para el control de la infección viral intrahospitalaria y la protección del personal se adoptaron las medidas de bioseguridad adecuadas a las posibilidades del área física: 1) se controló la disponibilidad permanente de equipos de protección personal (gorro, barbijo, camisolín, antiparras, guantes) y se promovió su uso sistemático; 2) se indicó la utilización de barbijos N95 por parte del personal, dada la frecuente realización de maniobras generadoras de aerosoles en la UCIA (intubación endotraqueal. aspiración de secreciones, toma de muestras respiratorias, fibrobroncoscopia); 3) se utilizaron sistemas de aspiración cerrados para evitar abrir el circuito del respirador, y se colocaron filtros en línea de alta eficiencia -inspiratorios y espiratorios- para impedir la exhalación de partículas virales, y 4) se establecieron normas destinadas a restringir la circulación de personal y las visitas a los pacientes.
Métodos estadísticos. Los datos referentes a la descripción de la población se expresan como rango, media y desviación estándar, o mediana y percentilos 25-75, según corresponda. Se compararon las características clínicas al ingreso entre los pacientes con PCR-RT positiva y negativa y entre los que murieron y quienes sobrevivieron. Se realizó el test exacto de Fisher a dos colas para comparar las variables categóricas dicotómicas.
Entre los días 7 y 27 de junio fueron ingresados en la UCIA 28 pacientes que cumplían los criterios de inclusión, 8 de los cuales permanecían hospitalizados mejorando su situación clínica al 13 de julio de 2009; catorce de ellos eran mujeres (50.0%). El rango de edad fue 19 a 72 años, con una mediana de 39; fueron menores de 48 años el 75% de los pacientes. El rango de los días transcurridos entre el comienzo de los síntomas de influenza y la internación en el hospital fue de 4 a 11 días, mediana (IQR) de 6 (5,8).
Las condiciones asociadas a la enfermedad aguda que motivó la internación se describen en la Tabla 8. Es de destacar el elevado porcentaje de embarazadas o puérperas: 5/28 pacientes. Los 2 pacientes portadores de HIV tenían un recuento menor a 100 de linfocitos CD4 y no recibían tratamiento antirretroviral.
TABLA 8.- Condiciones asociadas a influenza A (H1N1)

Del total de los 28 pacientes analizados, se recibió la confirmación de infección por virus de influenza A (H1N1) por PCR-RT en 14 pacientes (50.0%). En 6 pacientes el resultado del estudio para virus fue informado como negativo, uno por IFD y 5 por PCR-RT, mientras que en los 8 restantes no se disponía del resultado al 13 de julio de 2009.
La radiografía de tórax efectuada al ingreso fue anormal en todos los pacientes: infiltrados pulmonares bilaterales con patrón alveolar, compatibles con neumonía multilobar o ARDS.
La mayoría de los pacientes presentaban cifras normales de leucocitos, elevación moderada de enzimas hepáticas y LDH. En los pacientes en quienes se realizó determinación de CPK al ingreso, el rango fue de 255 a 27 082.
De los 28 pacientes con cuadro compatible con neumonía grave por influenza internados en la UCIA, 25 (89.3%) fueron intubados y tratados con VM. Desarrollaron shock y recibieron drogas vasoactivas (norepinefrina o dobutamina) 21 enfermos (75.0%). Nueve pacientes (32.1%) desarrollaron insuficiencia renal aguda (IRA) y 8 de ellos requirieron hemodiálisis. Todos los pacientes que presentaron shock recibían VM, y todos los que se complicaron con insuficiencia renal tuvieron shock y fueron tratados con agentes vasoactivos.
La mortalidad de los pacientes de esta serie es de 14/28 (50.0%). Si se toma en cuenta sólo a los pacientes con resultado para A (H1N1) positivo, fallecieron 7/14 pacientes.
Entre los pacientes muertos con confirmación de influenza A (H1N1), 6/7 requirieron VM, 6/7 presentaron shock y 3/7 pacientes cursaron con insuficiencia renal aguda. De los 7 fallecidos con sospecha de influenza A (H1N1), todos recibieron VM y presentaron shock con requerimiento de norepinefrina; 4/7 pacientes desarrollaron fallo renal.
La mortalidad se relacionó con la presencia e intensidad de la disfunción de órganos. Con la presencia de sólo un fallo la mortalidad fue de 28.5%, con dos fallos 44.5%, con tres fallos 77.7% y con cuatro fallos, un solo paciente que falleció.
Recibieron VM por presencia de ARDS 24 pacientes, de los cuales murieron 13 (54.2%); la mayoría de estos enfermos fallecieron en fallo respiratorio, con imposibilidad de alcanzar los objetivos de la VM. Un elemento que marca la gravedad del ARDS es la necesidad de ventilación en posición prona utilizada como maniobra de rescate34. De los 11 pacientes que fueron ventilados en decúbito prono, 9 fallecieron. El único paciente fallecido no ventilado fue un enfermo portador de cardiopatía isquémica que, luego de recibir tratamiento por neumonía e infección por virus de influenza A (H1N1) confirmada y de superar el cuadro de insuficiencia respiratoria con manejo conservador, habiendo egresado de la Unidad Coronaria, presentó un episodio de edema agudo de pulmón rápidamente seguido de muerte.
El ARDS en este grupo de pacientes se caracterizó por: 1) presentación con marcada hipoxemia previa a la VM; 2) compromiso radiológico en los 4 cuadrantes en la mayor parte de los casos, con predominio del patrón alveolar, 3) presencia característica de secreciones mucohemáticas, poco abundantes; 4) profunda alteración del intercambio gaseoso una vez comenzada la VM, con gran hipoxemia y frecuentemente también hipercapnia de 60- 80 torr. Dada la habitual coexistencia de acidosis metabólica, valores de pH de alrededor de 7.00 no fueron infrecuentes; 5) distensibilidad tóraco-pulmonar disminuida con registros menores a 20 ml/cm H2O en algunos casos; 6) inestabilidad en los valores de PaO2 y de SaO2, que requirieron reiteradas maniobras de reclutamiento; 7) necesidad de utilizar elevados valores de PEEP y fracción inspirada de oxígeno de 1 durante varios días; 8) respuesta inconstante a las maniobras de reclutamiento y al decúbito prono, 8) sólo un paciente de esta serie presentó neumotórax durante la VM; 9) el destete del respirador una vez mejorado el intercambio gaseoso resultó difícil en varios pacientes: desarrollo de hipoxemia, mal patrón ventilatorio con utilización de músculos accesorios, intolerancia cardiovascular, excitación y/o delirio.
En dos pacientes se realizó el estudio histológico de muestras de tejido pulmonar post mortem. En uno de los casos los hallazgos fueron: septos alveolares congestivos con neumonocitos hipertróficos, algunos con núcleo hipercromático y presencia de formación de membrana hialina. En el otro se encontró epitelio pavimentoso con alteraciones citopáticas virales: núcleos vacíos, inclusiones virales, multinucleadas y células gigantes.
Fallecieron 13 de los 21 pacientes que desarrollaron shock (mortalidad 61.9%). En 2 enfermos se realizó evaluación hemodinámica con catéter en arteria pulmonar al comienzo del cuadro de shock, comprobándose la presencia de un patrón distributivo con volumen minuto no elevado y resistencias periféricas en valores intermedios. En otros 3 pacientes se comprobó por ecocardiografía la presencia de dilatación de cavidades cardíacas y deterioro de la función ventricular izquierda
Los 9 pacientes que desarrollaron fallo renal estaban sometidos a VM y habían presentado shock; siete de ellos murieron. No se pudo establecer una relación entre rabdomiolisis al ingreso y desarrollo de fallo renal.
Respecto de las 5 pacientes obstétricas de esta serie, 3 cursaban el tercer trimestre de embarazo, una el segundo trimestre y una ingresó en el día 40 de puerperio. Se decidió la interrupción del embarazo por cesárea debido al riesgo para el feto por hipoxemia materna en 3 casos. Dos de los recién nacidos -PCR-RT negativos- evolucionaron favorablemente en el Servicio de Neonatología, mientras que el tercero, cuya madre había sufrido un paro cardiorrespiratorio antes de su ingreso a la UCIA, nació muerto. Requirieron VM 3/5 pacientes, 2 de ellas desarrollaron shock y fallecieron, en ambos casos días después de realizada la cesárea.
En 5 pacientes se realizó determinación de antígeno urinario para neumococo al ingreso, siendo negativo en todos los casos. Seis pacientes presentaron serología positiva IgM para Mycoplasma pneumoniae. En 4 de estos casos coexistió con PCR-RT positiva para influenza A (H1N1).
Durante la evolución, en el 42.8% de los pacientes ventilados se observó desarrollo de bacterias en los cultivos de aspirado traqueal. Los microorganismos hallados fueron los habituales en las infecciones nosocomiales en nuestra Unidad, con predominio de Pseudomonas aeruginosa y Acinetobacter baumannii.
No se demostró significación estadística para las comparaciones entre PCR-RT positiva y negativa y las características clínicas de los pacientes, a su ingreso ni en cuanto a su evolución. Tampoco se observaron diferencias estadísticamente significativas en mortalidad ni en fallos de órganos para los grupos que recibieron oseltamivir en dosis de 150 mg/día y de 300 mg/día.
Durante el período en estudio, ningún miembro del equipo de salud que trabajó en la UCIA desarrolló infección confirmada por el virus de la influenza A (H1N1). Sólo uno de los médicos de guardia presentó un cuadro febril pero el resultado del hisopado fue negativo
Impacto de la epidemia sobre el sector de Cuidados Intensivos. Uno de los aspectos a considerar para evaluar la actividad es analizar la cantidad de pacientes bajo VM asistidos, dado la carga de trabajo que representa sobre el personal médico, de enfermería y kinesiólogos. El número de pacientes ventilados/día ascendió de 18- 22 en la primera quincena de junio a 31-37 pacientes ventilados/día en la semana del 21 al 27 del mismo mes. Además, se modificó marcadamente la modalidad y el clima de trabajo debido a la llegada repentina de la población de pacientes aquí descripta.
Es de destacar que, dado el inusitado y brusco aumento de la demanda de camas de cuidados intensivos generada por la pandemia, el proceso empírico de establecimiento de prioridades para la asistencia dirigió a los pacientes más graves a las UCIAs, mientras que otros pacientes con importante compromiso funcional -incluso pacientes que debieron recibir VM y soporte hemodinámico- fueron tratados en otros sectores del hospital.
La sensibilidad y especificidad de la IFD en la detección de este nuevo virus es desconocida y depende de la calidad de la toma de la muestra, por lo que un resultado negativo no debe ser asumido como diagnóstico final. En los pacientes que tienen una vía aérea artificial la obtención de las muestras por aspirado traqueal podría mejorar el rendimiento. Además, el resultado positivo para virus de influenza A no permite efectuar la diferenciación con el virus estacional. También las determinaciones por PCR-RT pueden ser afectadas por los problemas técnicos.
Las características clínicas de los enfermos que murieron con confirmación de infección por influenza A (H1N1) y los fallecidos en el grupo de pacientes con sospecha pero sin confirmación por PCR-RT, no presentaron diferencias notorias en el cuadro clínico inicial ni en la presencia y características de la disfunción multiorgánica. De tal modo, hemos incluido los 28 pacientes en el análisis ya que el cuadro clínico era similar y el contexto epidemiológico orientaba fuertemente al diagnóstico.
Desde hace muchos años se conoce que las mujeres embarazadas son un grupo de riesgo en relación con morbilidad y mortalidad en infecciones por virus de influenza. Esto ya se observó en la pandemia de influenza del año 191840. El incremento del riesgo de complicaciones se relacionaría con los diversos cambios fisiológicos que ocurren durante el embarazo, incluyendo alteraciones en los aparatos cardiovascular, respiratorio y en el sistema inmune41, 42.
La elevada prevalecencia de obesidad llama la atención. No se conoce por qué la obesidad aparece como un factor de riesgo para la aparición de complicaciones graves por la infección por el virus A (H1N1). Esta comorbilidad no había sido identificada previamente como un factor de riesgo para influenza estacional. Sin embargo, se ha observado en modelos experimentales en ratones, que una dieta que genera obesidad induce mayor mortalidad cuando los animales son infectados con virus de la influenza estacional43.
El cuadro de ARDS de estos pacientes fue muy grave, con difícil manejo. A diferencia del ARDS de otras etiologías, la muerte en la mayoría de los casos de esta serie se produjo por insuficiencia respiratoria.
En la mayor parte de los enfermos, la VM fue dificultosa por el importante trastorno del intercambio gaseoso y la rigidez pulmonar resultante de la reducción de la distensibilidad pulmonar. Resultó difícil alcanzar objetivos de oxigenación aceptables, aun con altos niveles de PEEP aplicados, y fue necesario recurrir al uso de relajantes musculares para asegurar la adaptación del paciente al respirador. Fue frecuente el hallazgo de hipercapnia y acidemia grave, por la hipoventilación controlada a la que fueron sometidos o por la sobredistensión pulmonar secundaria a la presión positiva aplicada.
El estudio histológico efectuado (Fig. 17) muestra fundamentalmente evidencias de inflamación importante con infiltración celular, edema, áreas de necrosis y membrana hialina. El compromiso pulmonar descrito sugiere que el daño pulmonar grave ocurre como resultado de la neumonía viral primaria. Este daño podría ser atribuido a la respuesta inmune secundaria del huésped, por ejemplo una desregulación de la liberación de citocinas proinflamatorias inducida por la elevada replicación viral. Sin embargo, la coinfección bacteriana inicial del pulmón no puede ser excluida.

Fig. 17.- Infección grave por el virus de Influenza A (H1N1) swl (corte histológico)
La frecuencia con la que se presentó el fallo hemodinámico fue elevada. Las evaluaciones efectuadas mediante cateterismo de la arteria pulmonar en cierto número de casos de shock pusieron en evidencia un volumen minuto cardíaco inadecuado para la situación de hiperdinamia esperada, y la ecocardiografía evidenció la presencia de dilatación de cavidades cardíacas y de déficit de la contractilidad del ventrículo izquierdo. En ausencia de infección bacteriana, estos hallazgos podrían poner en evidencia la afectación miocárdica por el proceso viral.
Otro dato de interés es el desarrollo de insuficiencia renal aguda como parte de la disfunción multiorgánica. Aunque a menudo estos pacientes presentaron valores elevados de CPK, y es posible especular que el mecanismo de rabdomiolisis contribuya al desarrollo de fallo renal, no ha sido posible establecer una relación causal clara en este grupo de pacientes. La insuficiencia renal no estuvo presente al ingreso, sino que se desarrolló durante la evolución y se comportó como oligoanúrica en todos los casos. Al comienzo de la epidemia, en varios pacientes se utilizó un abordaje inicial que incluía restricción hídrica para el manejo del ARDS, y tratamiento del shock con altas dosis de noradrenalina sin valoración hemodinámica objetiva con catéter en la arteria pulmonar o métodos alternativos; no se puede descartar que este enfoque pudiera haber contribuido a la instalación del fallo renal en algunos de los pacientes. Considerando que todos los casos de fallo renal habían sido precedidos de shock, resulta razonable establecer una relación causa-efecto entre ambos fenómenos. Casi todos los pacientes con fallo renal debieron ser tratados con hemodiálisis, requiriéndose la realización de sesiones diarias en razón de su hipercatabolismo y tendencia a la acidosis.
La elevada frecuencia de fallos de órganos y la gravedad del ARDS observadas en este grupo de pacientes podría estar relacionada con su llegada tardía al hospital y con la demora en iniciar el tratamiento antiviral desde el comienzo de la sintomatología. El hecho de que algunos pacientes hayan ingresado después de una semana de iniciado los síntomas y haber realizado un tratamiento muy tardío puede explicar en parte la mortalidad elevada encontrada en esta serie.
La duración del tratamiento antiviral en estos casos no está claramente establecida, pero se aconseja mantenerlo durante 10 días, y este fue el criterio que se adoptó. El tratamiento antiviral temprano (antes de 48 horas del comienzo de los síntomas) es óptimo para el tratamiento de esta enfermedad en pacientes con influenza estacional. A pesar de ello, ha sido comunicada una reducción de la mortalidad en pacientes hospitalizados con esa enfermedad o con influenza aviar A (H5N1), aun cuando el tratamiento con oseltamivir hubiera sido iniciado más tarde33. Con este fundamento nuestros pacientes recibieron tratamiento antiviral independientemente del tiempo de evolución de la enfermedad.
El diagnóstico de neumonía asociada a la VM es difícil de establecer en pacientes portadores de ARDS, máxime cuando ya están cursando una enfermedad infecciosa. Dada la gravedad del fallo respiratorio, no se realizaron técnicas broncoscópicas en estos casos y los elementos diagnósticos utilizados fueron los de orden clínico.
Acerca de los pacientes que presentaron serología positiva IgM para Mycoplasma pneumoniae, no queda claro el significado de esta asociación y se deberá continuar la investigación de este hallazgo.
La epidemia afectó notablemente el funcionamiento de la UCIA, así como ocurrió con otras áreas del hospital. En primer término, se incrementó notablemente el volumen de trabajo y se modificaron las modalidades de funcionamiento de las unidades y el ambiente laboral.
Resultó conmocionante para el equipo de salud la llegada brusca y masiva de pacientes muy graves, con varias fallas orgánicas, a menudo jóvenes previamente sanos y en varios casos embarazadas, muy difíciles de tratar, que en los primeros días presentaron alta mortalidad.
Varios factores contribuyeron a generar un clima de inquietud en los integrantes del equipo: la incertidumbre generada por tratarse de una enfermedad nueva, el natural temor debido a los riesgos personales y familiares que asumían, la necesidad de modificar el estándar de funcionamiento para adecuarse a las medidas de bioseguridad, la sobrecarga de trabajo que fue necesario sobrellevar, etc. A pesar de ello, se consiguió mantener una actitud positiva de compromiso con el trabajo y de solidaridad entre los integrantes del equipo.
Este estudio corrobora la gravedad de los pacientes ingresados en las unidades de Terapia Intensiva, por un cuadro compatible con ARDS y disfunción multiorgánica secundaria a influenza A (H1N1) confirmando resultados similares de estudios efectuados en México y EE.UU. Se pone de manifiesto la elevada frecuencia de shock y los indicios que indicarían la presencia de compromiso miocárdico secundario a la enfermedad viral. Asimismo, se ratifica que esta enfermedad es capaz de afectar gravemente en una proporción significativa a las embarazadas y a los adultos menores de 50 años aunque no sean portadores de comorbilidades. Las pautas para el manejo de estos pacientes aquí comunicadas deberán ser actualizadas con base en las observaciones clínicas y el análisis epidemiológico a medida que el número de casos permita adquirir más conocimientos y experiencia en el manejo de esta enfermedad.
Se destaca también que una epidemia como la que se presenta produce una importante influencia en el funcionamiento de las unidades de Terapia Intensiva y un impacto emocional significativo en el equipo de salud.
El virus influenza A(H1N1) y la internación en Pediatría
La infección respiratoria aguda baja (IRAB) de etiología viral es una de las infecciones más frecuentes en la infancia. En la Argentina, las IRAB son la tercera causa de muerte (neumonía-bronquiolitis-neumonitis) en menores de un año y la segunda causa de muerte en menores de 5 años43-49.
El espectro clínico de la enfermedad descripto va desde la afección leve hasta neumonía grave o mortal51.
Se revisaron las historias clínicas (HC) de los niños internados por influenza A (H1N1), en el Servicio de Pediatría del Hospital Posadas, desde 1/6/09 al 27/6/09. Para ello se confeccionó un protocolo donde consta: edad, sexo, tiempo de evolución previa a la internación, diagnóstico de ingreso y egreso, factores de riesgo para influenza estacional, radiografía de tórax (Rx), exámenes de laboratorio de ingreso y evolución.
Se definió: a) Neumonía: infección aguda del parénquima pulmonar con signos clínicos de ocupación alveolar y signos radiológicos de opacidad, sin pérdida de volumen, de localización única. b) Neumonía multifocal: cuadro con múltiples imágenes de opacidad radiológica, generalmente mal definidas, sin límites segmentarios. c) Neumonía intersticial: infiltrados radiológicos reticulonodulillares. d) Atelectasia: imagen radio-opaca con límites precisos, con pérdida de volumen. Finalmente, se definió como coinfección viral a la presencia de dos o más virus en secreciones nasofaríngeas al ingreso.
Como factores de riesgo para influenza estacional se consideraron: la enfermedad pulmonar crónica, el asma grave corticoide dependiente, la fibrosis quística, desórdenes metabólicos (diabetes), obesidad, enfermedad renal crónica, hepatopatías, enfermedades neurológicas-neuromusculares, hemato-oncológicas, trasplantados de órganos sólidos y líquidos, inmunocomprometidos por medicación, por virus de inmunodeficiencia humana (HIV), síndrome de Down, cardiopatías. También se consideró factor de riesgo en niños menores de 2 años, el antecedente de prematurez o el peso al nacer menor de 2 500 g.
Desde 1/6/09 al 27/6/09 (corresponde a las SE 22 a 25) se internaron 49 niños con infección confirmada por virus influenza A (H1N1), 23 fueron varones. La mediana de edad fue 10 meses, con rango entre 1 y 180 meses. La distribución por grupo etario, los síntomas y signos, el diagnóstico y las imágenes radiográficas al ingreso, se presentan en la Tabla 9. El tiempo de evolución previa a la internación, de acuerdo a la definición de caso, tuvo una mediana de 3.5 días (1 a 7 días).
TABLA 9.- Edad, signos y síntomas, Rx y diagnóstico al ingreso de 49 niños internados con influenza A (H1N1)

BQL/SBO: Bronquiolitis / Síndrome bronquial obstructivo.
CRIA: Claudicación respiratoria inminente aguda.
*: Gastroenteritis (2), Enfermedad oncológica: Tumor de Wilms,
Leucemia Mieloide Crónica, (2), politrauma (1), crisis adrenal (1), sepsis (1).
Los pacientes internados con factores de riesgo fueron 34, lo que correspondió al 69% (Tabla 10). Hubieron coinfecciones virales en 10 pacientes, 7 con virus sincicial respiratorio (VSR) y dos con influenza B.
TABLA 10.- Factores de riesgo al ingreso en Pediatría en 34/39 casos de influenza A (H1N1)

*Obstrucción bronquial recurrente, neumonías.
**Los 2 niños con Síndrome de Down son los que presentaban cardiopatías congénitas.
El recuento de glóbulos blancos tuvo una mediana de 12 000/mm3. Osciló entre 2 200 y 25 300/mm3. Se excluyó un paciente oncológico con recuento de glóbulos blancos de 800/mm3. La mediana de los valores de proteína C-reactiva fue 1.56 mg/dl (0.1 a 20.5 mg/dl). Los cultivos de sangre periférica tomados al ingreso fueron negativos en todos los casos para infecciones bacterianas concomitantes. La IF directa resultó positiva para influenza A en 47 de los 49 pacientes. El diagnóstico específico se realizó en todos los casos por PCR-RT.
Además del oseltamivir, los pacientes recibieron antibióticos según su enfermedad asociada. De esta población, 6 pacientes requirieron derivación a cuidados intensivos pediátricos. El restante había ingresado por politraumatismo, con antecedente de asma.
En conclusión, en el período analizado los niños que requirieron internación en nuestro servicio, fueron en su mayoría menores de 5 años. Presentaron factores de riesgo el 69% de los casos. La fiebre y la dificultad ventilatoria constituyeron los signos más frecuentes al ingreso. Los diagnósticos de ingreso predominantes fueron: neumonía más síndrome bronco-obstructivo/bronquiolitis. En ningún caso se documentó infección bacteriana concomitante. En la gran mayoría de los casos la IFD permitió el diagnóstico de influenza A en nuestra población, y la confirmación de influenza A (H1N1) se realizó por PCR-RT en todos los casos. El 20% de los niños presentó además coinfección viral, predominantemente con VSR.
El virus influenza A (H1N1) en cuidados intensivos pediátricos
La epidemia de infección respiratoria aguda baja (IRAB) ocurre anualmente en nuestro país en la temporada invernal, entre los meses de junio y agosto y afecta a los niños, en especial a los menores de 12 meses. Un grupo importante de ellos evoluciona al fallo respiratorio agudo y requiere internación en Unidades de Cuidados Intensivos Pediátricos (UCIP) y ventilación mecánica (VM). El agente etiológico más frecuente es el virus sincicial respiratorio (VSR).
Este año, el comienzo de la epidemia de IRAB en niños coincidió con la difusión de informes de casos de una enfermedad respiratoria producida por un virus de influenza A (H1N1) distinto de los conocidos previamente, con casos en EE.UU. y México.
En nuestra Unidad Pediátrica de Cuidados Intensivos, el primer caso confirmado fue el de un paciente ingresado al Hospital el 3 de junio con IFD positiva para influenza A, confirmándose A (H1N1) en el Instituto Malbrán el 14/06/2009.
Se describen aquí las características clínicas y epidemiológicas de la población de niños internados en la UCIP del Hospital Posadas (unidad polivalente de 20 camas) con infección confirmada o sospechosa por virus influenza A (H1 N1) en el período comprendido entre el 1 de junio y el 10 de julio de 2009, hasta el alta de la unidad o fallecimiento.
Los datos fueron obtenidos de las historias clínicas, de las fichas epidemiológicas y de la base de datos del Servicio (Sati-Q, base de datos de la SATI, Sociedad Argentina de Terapia Intensiva )52. Se recabaron datos de edad en meses, sexo, lugar de origen, días de comienzo de los síntomas, supervivencia, score de mortalidad al ingreso (PIM 2 y SMR). El PIM2 es un score pediátrico de cálculo de riesgo de mortalidad. El SMR (standardized mortality ratio) es un índice que compara la mortalidad real con la esperada. Si la relación es ideal, es decir todo lo que fue predicho se cumplió, su valor es 1, pero si los muertos superan lo esperado, es mayor a 1. Si el número de muertos es inferior al de los esperados la relación es menor de 1. Esta tasa es la forma más difundida de evaluar los resultados53, 54. El Ministerio de Salud de la Nación la usa como única medida de calidad de las terapias intensivas. Se recabaron datos clínicos, motivo de ingreso, coinfecciones, comorbilidades, fallo de órganos, evolución, días de internación, requerimientos de enfermería (TISS 28, sistema de puntaje que mide la carga de trabajo de enfermería y establece la relación paciente-número de enfermeras de acuerdo con la complejidad que presentan los pacientes)55.
Se incluyeron resultados de laboratorio general: hemograma, hepatograma, coagulograma, urea, creatinina, CPK; radiología, bacteriología (hemocultivo, urocultivo, mini-BALl o aspirado traqueal, cultivo de LCR), serología y PCR para micoplasma; virología (hisopado IFD, PCR-RT). Ventilación mecánica según indicación, ventilación invasiva (VI) o no invasiva (VNI), días de VM, parámetros de respirador, cociente PaO2 /FiO2 (PaFi), requerimiento de maniobras de rescate de hipoxemia, complicaciones relacionadas y resultados de la discontinuación de VM.
En el periodo considerado se internaron en la Unidad 65 pacientes, 44/65 (67%) con IRAB, 27/44 pacientes (61%) con virus influenza A (H1N1) (Tabla 11).
TABLA 11.- Motivo de ingreso a la Unidad de Cuidados Intensivos Pediátrica (UCIP), entre 1/6/2009 y 10 /7 /2009.

Del grupo de pacientes con influenza A (H1N1) el 44% eran de sexo femenino (12/27).
La edad promedio fue de 47.5 meses y la mediana 13 meses, rango 1-168 meses. El 56 % (15/27) de los pacientes provenía de nuestra institución (Guardia y Clínica Pediátrica) y el 44 % restante fue derivado de otros hospitales.
El motivo de ingreso fue IRAB: 77.7% (21/27); shock séptico: 14.8% (4/27); alteración de la conciencia: 1/27 (traumatismo de cráneo con síndrome febril) y 1/27 síndrome febril más taquiarritmia.
De los 21 pacientes que ingresaron con IRAB influenza A (H1N1), 4 fueron intrahospitalarios (IH): 2 de nuestro hospital y 2 de otras instituciones. El tiempo transcurrido entre el comienzo de los síntomas y la internación en la UCIP varió entre 1 y 12 días, con un promedio de 5 y una mediana de 5 días. En los pacientes fallecidos, el promedio fue de 6 días de evolución previa (rango de 5 a 7 días). De estos pacientes, 7 habían ingresado por síndrome bronquiolítico + neumonía, 5 por neumonía, 6 por síndrome bronquiolítico, 3 con neumonía con síndrome de escape de aire. De los 27 pacientes con influenza A(H1N1), el 92.5% (25/27) presentaron fallo respiratorio agudo y requirieron VM. El 48% de ellos (13/27) eran previamente sanos. Los 14 restantes (52%) presentaban comorbilidades, alguno más de una, descriptas en la Tabla 12.
TABLA 12.- Comorbilidades asociadas en los pacientes con infección por influenza A(H1 N1) en UCIP

La comorbilidad más frecuente fue la prematurez, seguida de la enfermedad pulmonar respiratoria crónica (displasia broncopulmonar y asma) y las cardiopatías congénitas. De estos 27 pacientes, 7 presentaban coinfección por VSR, 4 por micoplasma (2 confirmados con PCR, 2 con serología +) y uno con Staphylococcus aureus.
La estadía promedio de los pacientes en UCIP fue de10.7 días y la mediana de 9 días.
El TISS 28 promedio al ingreso fue de 32, el máximo durante la internación 35 y el promedio al alta de 22. La mortalidad fue del 22% (6/27) Las causas de muerte fueron: 66% hipoxemia refractaria (4/6), shock cardiogénico (1/6) y shock séptico (1/6)
Recibieron tratamiento con oseltamivir 23 de 27 pacientes (85%) de acuerdo a la normativa vigente en el momento. Las dosis fueron calculadas según la edad y el peso de los pacientes, en ningún paciente se duplicó la dosis. De los cuatro que no recibieron tratamiento dos fallecieron dentro de las primeras 12 horas del ingreso y dos por falta de confirmación etiológica (en etapa inicial de la epidemia). El tratamiento se extendió por 10 días en 20/23 pacientes y por 5 días en 3 pacientes, según las normativas vigentes en el momento de la internación. Se observaron 2 pacientes con diarrea y vómitos atribuibles al tratamiento con oseltamivir. Todos recibieron tratamiento antibiótico al ingreso. Se ventilaron 25 de los 27. Los días de ventilación promedio fueron 12 con una mediana de 10 días y un rango de 2 a 30 días. Tuvieron VM prolongada por más de 21 días 3 de 24 pacientes. Dos continúan ventilados (uno en unidad de recuperación cardiovascular y otro, con traqueostomía, en la unidad). Se utilizó ventilación invasiva en todos los casos. Los modos ventilatorios utilizados fueron volumen control exclusivo en 11 de 24, presión control exclusivo en 6 y cambio entre modos durante la evolución en 7/24.
La PEEP promedio al ingreso fue de 9 cm de H2O con una mediana de 8 (rango de 5 a 16). La relación entre presión arterial de oxígeno y la fracción inspirada de oxígeno (PaFi) promedio al ingreso fue de 146 con una mediana de 130 (rango de 46 a 312). La PIM promedio al ingreso fue de 28 al igual que la mediana, con un rango entre 23 y 34 cm de H2O.
El 66.6 % (16/24) ingresó por distrés respiratorio, de los cuales 25% (4/16) presentaron hipoxemia refractaria.
De los 16 pacientes con distrés se utilizaron como rescate hipoxemia: posición prona (8/16), otras maniobras de reclutamiento (3/16), hipercapnia permisiva en (2/16), inversión de la relación I:E (4/16) y administración de surfactante como coadyuvante (1/16).
Se observó síndrome de escape de aire en 32% (8/25), de los cuales 3 ingresaron con el cuadro y 5 lo desarrollaron durante la VM. La discontinuación de la VM se realizó exitosamente en 72.2% de los pacientes (13/18) con una única prueba de tubo en T. Se reintubaron 28% de los pacientes (5/18) en quienes la discontinuación fue dificultosa.
Se registraron 6 episodios de extubación no planeada en el 16% de los pacientes (4/24). Todas fueron accidentales y requirieron reintubación inmediata por insuficiencia respiratoria. El balance acumulado de fluidos en los 24 pacientes ventilados fue en promedio 109 ml/kg con una mediana de 93 ml/kg y un rango entre -245 y 475.
Las complicaciones que se presentaron en estos pacientes fueron: fallo de órganos, dos no presentaron fallo; 8/27 pacientes tuvieron sólo un fallo de órganos. En estos dos grupos de pacientes todos sobrevivieron. El 40.7% (11/27) de los pacientes presentó dos fallos (respiratorio y hemodinámico). Fallecieron 2 pacientes. Con tres fallos, 4 pacientes (respiratorio, hemodinámico y hepático). Fallecieron 2 pacientes. Con cuatro fallos (respiratorio, hemodinámico, hepático y hematológico): 2 pacientes. Ambos fallecieron.
Con respecto a las infecciones intrahospitalarias, se registraron 4 neumonías asociadas a la VM en 25 pacientes ventilados (16%). En los 27 pacientes internados se constataron 2 bacteriemias primarias.
Veinticuatro pacientes egresaron de la UCIP y 3 permanecen internados. El 59% de los pacientes (16 /27) pasó a la Sala de internación clínica, en nuestro Hospital o en su hospital de origen. Un paciente pasó a cirugía para corrección de su cardiopatía y de allí a la de Recuperación Cardiovascular, y un paciente se fue de alta domiciliaria. El 22% de los pacientes (6/27) fallecieron. La mortalidad calculada de los pacientes a su ingreso según el score de PIM2 fue de 16%. El SMR fue de 1.37.
Estos datos muestran una variación del mapa virológico en pacientes con IRAG (Infección Respiratoria Aguda Grave) con predominio del virus influenza A(H1N1) versus el VSR habitual en esta época del año. Se vieron afectados pacientes de mayor edad con respecto a la media histórica de pacientes con IRAG. Mediana 13 meses vs. 3 meses.
El 51.8% de los pacientes presentó comorbilidades, siendo la más frecuente prematurez, seguida por enfermedad respiratoria (asma y DBP) y cardiopatía congénita. No se evidenciaron diferencias con el comportamiento de otras infecciones respiratorias virales.
La efectividad del tratamiento antiviral específico está demostrada para influenza A estacional y aviar cuando se administra dentro de las primeras 48 horas de inicio de los síntomas. Pese a que en nuestros pacientes el promedio de tiempo transcurrido entre el inicio de los síntomas y el ingreso a la unidad fue de 5 días, todos recibieron tratamiento excepto cuatro. La razón fue falta de confirmación en 2 (primera semana de junio) y 2 por fallecimiento antes de las 12 horas de internación.
El tratamiento antiviral se hizo según normas oficiales que variaron en el tiempo. En etapa inicial se indicó sólo con diagnóstico confirmado, posteriormente se amplió a pacientes sospechosos clínicos con virológico negativo o detección de influenza A por IFD (sin tipificar). La duración del tratamiento fue de 10 días en 20 pacientes y 5 días en 3 (según la norma inicial).
Todos los pacientes recibieron ceftriaxone y claritromicina, como tratamiento inicial de la neumonía grave de la comunidad, hasta obtener resultados de los cultivos y estudios virológicos. En el 44.4% de ellos se observó coinfección viral o bacteriana.
El 92.5% de los pacientes requirió VM invasiva al ingreso. El 66.6% ingresó con diagnóstico de distrés respiratorio agudo definido como PaFi < 200, infiltrados bilaterales radiológicos y requerimiento de PEEP.
Se observó escape de aire al ingreso en 3 pacientes (2 neumotórax y 1 neumomediastino) y otros 5 lo desarrollaron durante la internación. De los 16 pacientes que presentaron distrés 4 (25%) presentaron hipoxemia refractaria (requerimiento de FiO2 de 80% o más para lograr el objetivo de oxigenación de PaO2 de 60 mm Hg). Estos pacientes son los que requirieron mayores intervenciones de rescate de hipoxemia y en los que se observó presencia de escape de aire durante la ventilación. Los pacientes que no lograron mejorar su PaFi por encima de 100 al cuarto día, fallecieron.
Si bien el distrés respiratorio no difirió del observado por otras etiologías tanto en la estrategia ventilatoria protectiva utilizada como en su resultado, lo particular fue la simultaneidad de pacientes con este diagnóstico. Este aumento de la carga de trabajo quedó demostrado por los altos promedios de TISS 28, superiores a la media histórica en la unidad y requirió de un equipo suficiente en número y entrenado.
El manejo de los líquidos (aporte hídrico y nutricional) en estos pacientes fue conservador, siendo su resultado un balance acumulado, en promedio, positivo (109 ml/kg).
La duración de la VM fue en promedio de 12 días, superior al estándar observado en IRAG en años anteriores, cuyo promedio fue de 5 a 6 días.
Fue particularmente dificultosa la retirada del ventilador, ya que un 28% de los pacientes que cumplían con criterios de destete (mejoría clínica, PaFi > 200, PEEP de 5 mm Hg, sin inotrópicos) y realizaron una prueba exitosa de ventilación espontánea con tubo en T de 30 minutos, requirieron: reintubación por falla respiratoria hipoxémica con reducción gradual del soporte, o ventilación no invasiva para prevenir reintubación por un aumento exagerado de la demanda ventilatoria, imposible de predecir mientras el paciente se hallaba con presión positiva
La asociación de falla de órganos más frecuente fue la respiratoria con la hemodinámica (40.7%). La mayor mortalidad se observó en los pacientes con falla de tres o más órganos. La mortalidad esperada, 16%, para este grupo de pacientes (calculada por el PIM2) es superior a la histórica en nuestra unidad. Se trata, pues, de pacientes más graves al ingreso.
La mortalidad observada, 22%, supera también la media habitual de nuestros pacientes.
El valor de SMR (> de 1) demuestra que la mortalidad observada fue mayor que la esperada, por lo que la elevada mortalidad de estos pacientes no puede atribuirse exclusivamente a la gravedad de la enfermedad de ingreso, como la evalua el PIM2, sino al agravamiento y persistencia de su enfermedad respiratoria hipoxémica, entre otras. No obstante estos resultados nos obligan a mantener nuestra estrategia de mejoramiento continuo de la calidad.
En conclusión, el aumento de la demanda de pacientes con insuficiencia respiratoria aguda grave motivó la necesidad de aumentar el número de camas de terapia intensiva.
La población con infección por influenza A (H1N1) se diferenció con la histórica en que presentó mayor edad, mayor gravedad y mayor mortalidad. Se observó el desplazamiento del VSR por el virus de influenza A(H1N1) como agente etiológico de la enfermedad respiratoria. Se destaca la presencia de coinfección viral y bacteriana al ingreso, así como la de comorbilidades. La presencia de hipoxemia refractaria fue el principal marcador de gravedad en esta población.
La revisión continua de los procesos nos permitirá planear y ejecutar las intervenciones adecuadas para afrontar futuros sucesos optimizando los resultados.
Prioridades para la atención de pacientes en condiciones de demanda asistencial masiva por la pandemia de influenza A (H1N1)
El sistema de salud fue abruptamente sobre-exigido por el aumento de demanda de atención debido a la pandemia de influenza A (H1N1). En nuestro hospital, ello se tradujo en sobrecarga en los sectores de Emergencias e internación, con déficit de camas -en especial en las unidades de Cuidados Intensivos- retrasos y suspensiones de intervenciones quirúrgicas programadas. En estas circunstancias se plantean cuestiones éticas sobre la justicia en la asignación de los recursos, que si bien también se presentan en condiciones de funcionamiento habitual, son características de las situaciones de desastres o epidemias.
Sería adecuado que las discusiones sobre ética y valores se llevaran a cabo antes de que sobrevenga una situación crítica. Los sistemas de cuidados de la salud deben estar mejor preparados para abordar las difíciles decisiones éticas que aparecen rápidamente durante una crisis, dado que la información científica sola no es suficiente para las medidas requeridas.
Las ediciones más recientes de las guías sobre planes preparatorios para hacer frente a una pandemia de influenza de la OMS56-58, la Organización Panamericana de la Salud59,60 y otros documentos nacionales o regionales61,62, han acentuado la consideración de los problemas éticos. Entre ellos, han sido discutidos e incorporados fundamentos63-69 y procedimientos59-62,71-77 para establecer estrategias en la toma de decisiones sobre prioridades en la atención de pacientes, que requiere prestar atención a los principios éticos como herramientas para evaluar y arbitrar entre intereses y valores que compiten entre sí, considerando las conveniencias individuales (principio de autonomía, principalmente) y las de la comunidad (principio de justicia), las cuales pueden entrar en conflicto.
Desde un enfoque ético se deben considerar principios tales como la equidad, la utilidad y la eficiencia, la libertad, la reciprocidad y la solidaridad, en el contexto de la situación y los valores culturales locales, que ofrecen un marco de evaluación y ponderación de los intereses afectados.
A partir de la experiencia del SARS en Canadá, el Grupo de Trabajo del Centro Conjunto de Bioética (JCBWG) de la Universidad de Toronto ha identificado, explicado y presentado recomendaciones para varios problemas éticos clave64, 65, entre ellos el establecimiento de prioridades en la asistencia a los pacientes para la asignación de recursos cuando la disponibilidad de los mismos no alcanza para todos (por ej., vacunas, medicamentos antivirales, cama hospitalaria, atención en cuidados intensivos, recurso humano). Para la planificación y la toma de decisiones durante una pandemia de influenza, el informe propone una guía que contiene una serie de valores éticos que deben ser considerados en la emergencia.
Entre ellos: a) libertad individual (autonomía), que puede sufrir limitaciones -las que sean necesarias, relevantes, aplicadas de modo proporcional y equitativo, sin discriminación- para evitar perjuicios el conjunto de la población; b) protección de la población del daño (asignación de prioridades), un principio fundacional de la ética de la salud pública, que puede imponer restricciones (por ej. las de bioseguridad o la suspensión de ciertas prestaciones de salud) para resguardar la seguridad general; c) equidad, en la medida de lo posible, dadas las restricciones a que puede obligar la situación sanitaria para la prestación de atención requerida por los pacientes afectados por la influenza y por otros que requieran tratamiento con urgencia; d) responsabilidad administrativa para el manejo de la escasez de recursos (vacunas, medicamentos, respiradores, camas de internación, personal) con sentido del deber, comportamiento ético y capacidad para la toma de decisiones para proteger y desarrollar recursos, asignarlos con eficiencia maximizando los beneficios y reduciendo los daños colaterales, distribuir cargas y beneficios de modo justo.
A menudo, las medidas a adoptar implican restricciones obligadas porque los recursos no son suficientes para ser ofrecidos a todos los pacientes: uso de medicamentos y vacunas, criterios de internación y de atención, por ejemplo.
Los establecimientos sanitarios involucrados deben reorganizar su actividad de acuerdo a las nuevas prioridades: maximizar las medidas para la vigilancia epidemiológica y el aislamiento de pacientes, hacer más eficiente la utilización de los recursos, incrementar la oferta de atención médica y de sectores de internación, definir los instrumentos para la priorización de la atención.
Las situaciones de crisis sanitaria exponen al sistema de salud a perder la capacidad de respuesta previa ante un importante y brusco aumento de las necesidades. Para el caso de la gripe pandémica, la disponibilidad limitada de vacunas y de drogas antivirales requiere de la toma de decisiones de acuerdo a los criterios enunciados previamente para su asignación.
Una cuestión especialmente difícil es la referida a la necesidad de optar por asignar recursos críticos escasos (internación en Terapia Intensiva, respirador para proveer ventilación mecánica, etc.) cuando la demanda de tales recursos se encuentra sobrepasada. En estas situaciones, la detenida consideración de los distintos factores que entran en juego durante la discusión mediante los procedimientos habituales para la toma de decisión de limitación del esfuerzo terapéutico suelen perder vigencia ante la urgencia con que se presenta la demanda.
Las concepciones que entran en juego a la hora de definir las prioridades son el utilitarismo y la equidad, que pueden contraponerse entre sí. La posición utilitaria prioriza el beneficio que obtendría el individuo y/o la sociedad en caso de recibir un tratamiento. En tanto que el enfoque en pro de la equidad implica privilegiar al más gravemente enfermo o al más vulnerable. Si la edad debe entrar en consideración en la toma de decisión es una cuestión debatida: una posición le otorga prevalecencia a los más jóvenes en razón de considerar que resulta más justo porque tienen "más vida por delante".
Los criterios para el establecimiento de prioridades no deberán discriminar a los individuos en base a género, raza / etnia, religión, afiliación política, nacionalidad, situación social o económica, etc.
Para facilitar el establecimiento de prioridades para decidir en la utilización de recursos de soporte vital en la atención de pacientes críticos, se han propuesto diversas herramientas con fundamento ético59-62, 71-77. Su utilización puede contribuir a estandarizar el proceso de toma de decisiones y a minimizar los riesgos de decisión en la urgencia, con escasas posibilidades de consulta y discusión.
Como lineamiento general, los recursos escasos deben ser reservados a los pacientes con riesgo de vida. Cuando no todos estos pacientes puedan ser tratados, se les deben asignar prioridad a aquellos con mejores chances de sobrevivir como resultado del tratamiento. A a los individuos con peor pronóstico se les proveerá tratamiento paliativo.
La incorporación de un instrumento que defina las prioridades para distribuir los recursos de soporte vital, cuando no son suficientes, requiere una discusión amplia fuera del período de pandemia. Por ello, para la contingencia actual se ha propuesto adoptar una herramienta propuesta por organismos de planificación62, 76 y por OPS (por ej.: Organización de la respuesta de los establecimientos de salud ante una emergencia por casos masivos de infección respiratoria aguda grave (IRAG) y enfermedad tipo influenza (ETI)59. Su introducción se transcribe a continuación:
"Protocolo para el triage de cuidado crítico: Otro de los puntos críticos es la insuficiente disponibilidad de ventiladores y unidades de cuidado intensivo que se requerirán para la atención de los casos graves de ETI o IRAG. El proceso de toma decisiones podrá ser complejo cuando se junten demasiados casos con similares necesidades pero con insuficientes capacidades para asistirlas. Es aquí en donde tendrán que aparecer mecanismos de priorización con mayor objetividad que le permitan al clínico tomar una decisión en medio de situaciones críticas pero con respaldo científico"… "El protocolo que se presenta es sólo una forma de abordar la problemática, pero deberá ser un consenso de clínicos y directivos del establecimiento de salud quienes definan en últimas cuales serán las directrices en esta materia."
Este protocolo se basa en una adaptación del SOFA (Sequential Organ-Failure Assessment score)78, adoptado para la asignación de prioridades en el protocolo de triage en pacientes que necesitan cuidado intensivo en una pandemia de influenza. Con este sistema se establece un puntaje de acuerdo a la evaluación de la presencia de fallos en los sistemas respiratorio, cardiovascular, nervioso, renal y de la coagulación. Con el puntaje obtenido se establece la prioridad para el ingreso a Cuidados Intensivos, de acuerdo a 4 rangos identificados con los colores verde, amarillo, rojo y azul, cuyos criterios se modifican evolutivamente.
Se valoran ciertos criterios de inclusión y de exclusión, y se califica al paciente de acuerdo a los fallos que presenta para obtener el score correspondiente y contribuir así a la toma de decisiones al inicio (Tabla 13), a las 48 horas y a las 120 horas. Los criterios de inclusión establecen una serie de condiciones de alteraciones fisiológicas, y los de exclusión definen enfermedades preexistentes o actuales de mal pronóstico. La presencia de factores de exclusión o los puntajes muy altos dirigen al paciente a recibir cuidados paliativos, pero no cuidados intensivos (disposición de no ingresar o de salir de la unidad de Cuidados Intensivos).
TABLA 13.- Evaluación inicial de pacientes que necesitan cuidado intensivo en una epidemia de influenza

SOFA: Sequential Organ-Failure Assessment score78
Este instrumento o el que definitivamente se establezca habrá de ser herramienta que -utilizada juiciosamente, compartiendo las valoraciones, integrando a los profesionales con experiencia- facilite el proceso de toma de decisiones en el establecimiento de prioridades para el acceso a los recursos, cuando éstos no estén disponibles para todos.
Agradecimientos: La Comisión para la Contingencia de Influenza agradece a todo el personal del Hospital Nacional Profesor Alejandro Posadas, por el trabajo responsable y su compromiso durante esta pandemia.
Conflictos de interés: Los autores declaran no tener conflictos de interés respecto de esta publicación.
1. Marracino C, Abadie JP, Vera Figueroa M. Indicadores para monitoreo de programas de coberturas. (Resumen de la presentación al 1° Seminario Nacional sobre Indicadores), julio 2001. [ Links ]
2. Plan Nacional de Preparación para una Pandemia de Influenza: Ministerio de Salud Santiago 2007; 2a Edición Autorizada. En: www.pandemia.cl; consultado julio 2009. [ Links ]
3. Guía de Procedimientos Clínicos y Hospitalarios para la atención de Influenza Pandémica. Comité de Influenza Pandémica. Secretaría de Salud, Dr. José Ángel Córdoba Villalobos. www.scribd.com/doc/14668625/Acciones-basicas-ante-una-pandemia-de-influenza; consultado 25/4/2009 [ Links ]
4. Plan Nacional de Preparación y Respuesta ante una Pandemia de Influenza: Secretaría de Salud. México. ISBN. Secretaría de Salud. En: http://www.salud.gob.mx; consultado junio 2009. [ Links ]
5. Plan Nacional para la Pandemia. Argentina En: www.msal.gov.ar; consultado 4/6/2007 [ Links ]
6. Actualización Regional Pandemia H1N1 2009. En: http://new.paho.org/hq/index.php?option=comfrontpageItemid; consultado 2/7/2009 [ Links ]
7. Consideraciones para evaluar la gravedad de una pandemia de gripe. En: http://www.who.int; consultado junio 2009. [ Links ]
8. Guía instructiva para la aplicación de la lista de verificación del estado de preparación de los establecimientos de salud ante una pandemia de influenza. En: http://new.paho.org/hq/index.php, consultado junio 2009 [ Links ]
9. Plan de acción para la respuesta a la pandemia de influenza A (H1N1) Hospital Nacional Profesor Alejandro Posadas. Abril 2009 En: http://www.hospitalposadas.gov.ar/gripea/index.htm; consultado abril 2009. [ Links ]
10. Pérez Padilla R, de la Rosa-Zamboni D, Ponce de León S, et al. Pneumonia and respiratory failure from swine-origin Influenza A (H1N1) in Mexico. N Engl J Med 2009; 360: 1-10 [ Links ]
11. Virus Investigation Team. Novel Swine-Origin Influenza A (H1N1). Emergence of a novel swine origin Influenza A (H1N1) virus in Humans. N Engl J Med 2009; 2009: 2605-15 [ Links ]
12. Wein H, New Insights Into Novel H1N1. En: www.nih.gov/news/research_matters/july2009/07132009flu.htm, consultado 13/07/09 [ Links ]
13. Chowell G, Bertozzi SM, Colchero A, et al. Severe respiratory disease concurrent with the circulation of H1N1 Influenza. En:http://content.nejm.org/cgi/reprint/NEJMoa0904023.pdf , consultado 03/07/09 [ Links ]
14. Stein RA. Lessons from outbreaks of H1N1 Influenza. Ann Intern Med 2009; 151:59-62. [ Links ]
15. OMS. Declaracion de pandemia de la Directora General de la OMS. En: http://www.who.int/mediacentre/news/statements/2009/h1n1_pandemic_phase6_20090611/es, consultado julio 2009 [ Links ]
16. OMS. Gripe pandemica (H1N1) 2009 (Nota informativa N°3). En: http://www.who.int/csr/disease/swineflu/notes/h1n1_surveillance_20090710/es, consultado 17/07/09 [ Links ]
17. Riva Posse CA, Miceli INP. Evolución de la coqueluche en Argentina a finales del siglo XX. Medicina (Buenos Aires) 2005; 65:7-16 [ Links ]
18. WHO Current WHO phase of pandemic alert En: http://www.who.int/csr/disease/avian_influenza/phase/en/index.html, consultado 29/06/09 [ Links ]
19. Organización Panamericana de la Salud. Notificación de Enfermedades trasmisibles y Respuesta ante un brote epidémico. En: Manual para el control de las enfermedades transmisibles. Informe oficial de la Asociación Estadounidense de Salud Pública. (Publicación científica 613). 18° ed. Washington DC: David L Heynann Editor, 2005, p xxxii-xxxviii [ Links ]
20. Ministerio de Salud de la Nación. Dirección de Epidemiología. Manual de normas y procedimientos de Vigilancia y Control de Enfermedades de Notificación Obligatoria. Revisión nacional 2007. En: http://www.msal.gov.ar/htm/site/pdf/manual-normas-obligatorias.pdf, consultado 09/05/09. [ Links ]
21. Organización Panamericana de la Salud. Influenza. En: Manual para el control de las enfermedades transmisibles. Informe oficial de la Asociación Estadounidense de Salud Pública. (Publicación científica 613). 18° ed. Washington DC: David L Heynann Editor, 2005, p 379-86. [ Links ]
22. Shinde V, Bridges CB, Uyeki T, et al . Triple Reassortant Swine Influenza A (H1N1) in Humans in the United States, 2005-2009. N Engl J Med 2009; 360: 2616-25. [ Links ]
23. CDC protocol of real time RT-PCR for Influenza A (H1N1). World Health Organization, April 2009. En: Http://www.who.int/crs/resources/publications/swineflu/CDCRealtimeRTPCRSwineH1Assay2009-20090430.pdf, consultado el 01/06/09. [ Links ]
24. CDC. Use of Rapid Influenza Diagnostic Tests for Patients with Influenza-like Illness during the Novel H1N1 Virus (Swine Flu) Outbreak. En: http://www.cdc.gov/h1n1/guidance/rapidtesting.htm; consultado el 11/06/09. [ Links ]
25. Zimmer SM, Burke DS. Historical Perspective. Emergence of Influenza A (H1N1) viruses. N Engl J Med 2009; 361: 279-85. [ Links ]
26. Uyeki T.M., Prasad R, Vukotich C, et al. Low sensitivity of rapid diagnostic test for Influenza. Clin Infect Dis 2009; 48:89-92. [ Links ]
27. Faix DJ. Rapid Test Sensitivity for Novel Swine-Origin Influenza A (H1N1) Virus in Humans. En: http://www.nejm.org; consultado el 11/06/09. [ Links ]
28. Ellis JS, Zambon MC. Molecular diagnosis of influenza. Rev Med Virol 2002; 12: 375-89. [ Links ]
29. Call SA, Villenweider MA, Hornung CA, et al. Does this patient have influenza? JAMA 2005; 293: 987-97. [ Links ]
30. Fry AM, Shay DK, Holman RC, Curns AT, Anderson LJ. Trends in hospitalizations for pneumonia among persons aged 65 years or older in the United States, 1988-2002. JAMA 2005; 294: 2712-19. [ Links ]
31. Treanor J. Virus de la gripe. En: Gerald L. Mandell, John E. Bennett, Raphael Dolin Enfermedades infecciosas. Principios y práctica, sexta edición. Barcelona: Elsevier España. Año 2006. [ Links ]
32. Sessler C, Gray N. Intensive care management of life threatening avian influenza A (H5N1). Respirology 2008;13 (suppl 1): S27 - S32. [ Links ]
33. Abdel-Ghafar AN, Chorpitayasunohdh T, Gao Z, et al. Update on avian influenza A (H5N1) virus infection in humans. N Eng J Med 2008; 358: 261-73. [ Links ]
34. Gattinoni L, Tognoni G, Pesenti A, et al. Effect of prone positioning on the survival of patients with acute respiratory failure. N Engl J Med 2001; 345: 568- 73. [ Links ]
35. MMWR. Intensive-Care Patients with Severe Novel Influenza A (H1N1)Virus infection-Michigan, June 2009. MMWR Dispatch 2009; 58, July 10, 2009 [ Links ]
36. The ARDS Network. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the ARDS. N Engl J Med 2000; 342: 1301-8. [ Links ]
37. Lapinsky SE, Hawryluck L. ICU management of severe acute respiratory syndrome. Intensive Care Med 2003; 29: 870-5. [ Links ]
38. Mercat A, Richard J-CM, Vielle B, et al. Expiratory Pressure (Express) Study Group. Positive end-expiratory pressure setting in adults with acute lung injury and acute respiratory distress syndrome: a randomized controlled trial. JAMA 2008; 299: 646-5. [ Links ]
39. Meade MO, Cook DJ, Guyatt GH, et al. Lung Open Ventilation Study Investigators. Ventilation strategy using low tidal volumes, recruitment maneuvers, and high positive end-expiratory pressure for acute lung injury and acute respiratory distress syndrome: a randomized controlled trial. JAMA 2008; 299: 637-45. [ Links ]
40. Harris JW. Influenza occurring in pregnant women. JAMA 1919;72: 978-80. [ Links ]
41. Jamieson DJ, Theiler RN, Rasmussen SA, et al. Emerging infections and pregnancy. Emerg Infect Dis 2006;12: 1638-43. [ Links ]
42. Gonzales J, Ofori E, Burf I, et al. Maternal mortality from systemic illness: unravelling the contribution of the immune response. Am J Obstet Gynecol 2009; 200: 430.e1-8. [ Links ]
43. Smith AG, Sheridan PA, Harp JB, et al. Diet-induced obese mice have increased mortality and altered immune response when infected with influenza virus. J Nutr 2007; 137: 1236-43. [ Links ]
44. Centres for Disease Control and Prevention. Prevention and control of influenza: recommendations of Advisory Committee on Immunization Practices. MMWR 2003; 52: 1-34. [ Links ]
45. Recomendaciones para el diagnóstico y tratamiento de las infecciones respiratorias agudas bajas en menores de 2 años. Arch Argent Pediatr 2006;104: 159-76. [ Links ]
46. Influenza. En: Libro Azul de Infectología Pediátrica, 3ª ed. Buenos Aires: Sociedad Argentina de Pediatría, 2007, p 481-7. [ Links ]
47. Bossio J, Arias S. Mortalidad infantil en Argentina. Resumen de situación, 1999. Arch Argent Pediatr 2001; 99: 547-54. [ Links ]
48. Bakir J, Umido V, Romanin V, et al. Impacto del virus influenza en los niños: la realidad de un Hospital Pediátrico. Rev Hosp Niños B Aires 2005; 47: 270-5. [ Links ]
49. Ministerio de Salud de la Nación. Programa Nacional de Infecciones Respiratorias Bajas. Dirección de Estadísticas e Información de Salud. Dirección Nacional de Salud Materno Infantil. Enfermedades prevalentes de la infancia. Salud Integral del niño. Marzo 2004, N° 1. [ Links ]
50. Sociedad Argentina de Pediatría, Comité Nacional de Infectología/Sociedad Argentina de Infectología. Guías y consensos: Influenza A (H1/N1). Buenos Aires: SAP/SADI, junio 2009. En: www.sap.org.ar/influenza; consultado julio 2009. [ Links ]
51. CDC. Swine influenza A (H1N1) infection in two children- Southern California, March-April 2009. MMWR 2009;58: 400-2. [ Links ]
52. Sati-Q, base de datos orientada al mejoramiento continuo de la calidad de la Sati (Sociedad Argentina de Terapia Intensiva). En: www.sati.org.ar, consultado junio 2009. [ Links ]
53. Slater A, Shann F, Pearson G. PIM2: A revised version of the Paediatric Index of Mortality. Intensive Care Med 2003; 29: 278-85. [ Links ]
54. Cueto G, Torres Boden M. Scores utilizados en Terapia Intensiva. En: Ceraso Daniel H. y col.: Terapia Intensiva. Buenos Aires: Ed. Médica Panamericana, 4ta Edición, 2007. p 1095-209. [ Links ]
55. Reis Miranda D, De Rijk A, Schaufeli W. Simplified Therapeutic Intervention Scoring System: the TISS-28 items - results from a multicenter study. Crit Care Med 1996; 24: 64-73. [ Links ]
56. World Health Organization. Ethical considerations in developing a public health response to pandemic influenza, 2007. En: www.who.int/csr/resources/publications, consultado junio 2009. [ Links ]
57. World Health Organization. Addressing ethical issues in pandemic influenza planning. Discussion papers, 2008. En: www.who.int, cons. junio 2009. [ Links ]
58. Organización Mundial de la Salud. Documento de Orientación de la OMS. Programa Mundial de Influenza. Preparación y respuesta ante una pandemia de influenza, 2009. En: www.who.int, cons. junio 2009. [ Links ]
59. Organización Panamericana de la Salud. Servicios de Salud. Organización de la respuesta de los establecimientos de salud ante una emergencia por casos masivos de infección respiratoria aguda grave (IRAG) y enfermedad tipo influenza (ETI), abril 2008. En: www.mex.ops-oms.org/influenzah1n1/documentos/Modulo%20Servicios%20de%20Salud%20030408.pdf, cons.junio 2009. [ Links ]
60. Organización Panamericana de la Salud. Preparación de los establecimientos de salud ante caso inusitado o imprevisto o conglomerado de infección respiratoria aguda grave - IRAG, 2009. En: http://www.crid.or.cr/digitalizacion/pdf/spa/doc17360/doc17360.pdf, cons. junio 2009. [ Links ]
61. Ministry of Health. New Zealand Influenza Pandemic Action Plan, 2006. En: http://www.moh.govt.nz/moh.nsf/indexmh/nz-influenza-pandemic-action-plan-2006?Open, cons.junio 2009. [ Links ]
62. Ontario Health Plan for an Influenza Pandemic, 2008. En: http://www.health.gov.on.ca/english/providers/program/emu/pan_flu/ohpip2/plan_full.pdf , cons. junio 2009. [ Links ]
63. Gómez Rubí JA. Etica en Medicina Crítica. Madrid: Ed. Triacastela, 2002. [ Links ]
64. Singer PA, Benatar SR, Bernstein M, et al. Ethics and SARS: lessons from Toronto. BMJ, 2003; 6: 1342-4 [ Links ]
65. University of Toronto Joint Centre for Bioethics, Pandemic Influenza Working Group. Stand on guard for thee. Ethical considerations in preparedness planning for pandemic influenza, 2005. En: http://www.jointcentreforbioethics.ca/people/documents/upshur_stand_guard.pdf, cons: junio 2009. [ Links ]
66. Asociación Médica Mundial. Declaración de la Asociación Médica Mundial sobre la Etica Médica en Casos de Catástrofes, 2006. En: http://www.wma.net/s/policy/d7.htm; cons.junio 2009. [ Links ]
67. Veatch RM. Disaster Preparedness and Triage: Justice and the Common Good. The Mount Sinai Journal of Medicine, 2005; 72: 236. [ Links ]
68. National Ethics Advisory Committee. Getting Through Together. Ethical Values for a Pandemic, 2007. En: http://www.neac.health.govt.nz/moh.nsf/indexcm/neac-resourcespublications-gettingthroughtogether; cons. junio 2009. [ Links ]
69. Kraus CK, Levy F, Kelen GD. Lifeboat ethics: considerations in the discharge of inpatients for the creation of hospital surge capacity. Disaster Med Public Health Prep 2007; 1: 51-6. [ Links ]
70. Persad G, Wertheimer A, Emanuel EJ. Principles for allocation of scarce medical interventions. Lancet 2009; 373: 423- 31. [ Links ]
71. Christian MD, Hawryluck L, Wax RS, et al. Development of a triage protocol for critical care during an influenza pandemic. CMAJ 2006; 175: 1377-81. [ Links ]
72. Ardagh M. Criteria for prioritising access to healthcare resources in New Zealand during an influenza pandemic or at other times of overwhelming demand. Journal of the New Zealand Medical Association 2009; 119 (1243). En: http://www.nzma.org.nz/journal/119-1243/2256/, cons. junio 2009. [ Links ]
73. Hick JL, O'Laughlin DT. Concept of operations for triage of mechanical ventilation in an epidemic. Acad Emerg Med 2006; 13: 223-9. [ Links ]
74. Hick JL, Rubinson L, O'Laughlin DT, Farmer JC . Allocating ventilators during large-scale disasters - problems, planning, and process. Critical Care 2007; 11: 217. [ Links ]
75. Devereaux AV, Dichter JR, Christian MD, et al.; Task Force for Mass Critical Care. Definitive care for the critically ill during a disaster: a framework for allocation of scarce resources in mass critical care. Chest 2008;133:51S-66S. [ Links ]
76. Powell T, Christ KC, Birkhead GS. Allocation of ventilators in a public health disaster. Disaster Med Public Health Prep 2008; 2: 20-6. [ Links ]
77. White DB, Katz MH, Luce JM, Lo B. Who should receive life support during a Public Health Emergency? Using ethical principles to improve allocation decisions. Ann Intern Med 2009; 150: 132-8. [ Links ]
78. Ferrerira FL, Bota DP, Bross A., et al. Serial evaluation of the SOFA score to predict outcome in critically ill patients. JAMA 2001; 286: 1754-8. [ Links ]
Recibido: 22-8-2009
Aceptado: 30-7-2009














