Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Medicina (Buenos Aires)
versão impressa ISSN 0025-7680
Medicina (B. Aires) vol.70 no.5 Ciudad Autónoma de Buenos Aires set./out. 2010
ARTÍCULO ORIGINAL
Hiperparatiroidismo primario: Evolución postoperatoria a largo plazo
Francisco R. Spivacow, Carolina Martínez, Ana Polonsky
Instituto de Investigaciones Metabólicas, Universidad del Salvador (USAL)
Dirección postal: Dr. Francisco R Spivacow. Instituto de Investigaciones Metabólicas. Libertad 836, 1012 Buenos Aires, Argentina Fax: (54-11) 5031-9703 e-mail: spiva@idim.com.ar
Resumen
Presentamos la evolución postoperatoria a largo plazo de 87 pacientes con hiperparatiroidismo primario. Del total, 78 mujeres y 9 varones, relación: 8.7:1. Edad media 55.3 ± 10.2 años. Antes de la cirugía el 44% presentó litiasis renal, el 70% osteopenia u osteoporosis y un 71.2% tuvo hipercalciuria. Se encontró disminución del filtrado glomerular en el 12.6%. Del total, 72 pacientes presentaron un adenoma único, dos un doble adenoma, dos hiperplasia, cuatro histología normal y en siete no se pudo disponer del resultado. El calcio sérico, el calcio iónico, el fósforo y la parathormona intacta se normalizaron en todos los pacientes postcirugía. La densitometría ósea aumentó un 6.9% en columna lumbar y un 3% en cuello de fémur. Los marcadores del remodelado óseo se normalizaron y persistieron normales a los 23 meses del seguimiento, coincidiendo con la parathormona intacta. Lo mismo sucedió con los valores de 25 OH D. Cuando se compararon pacientes con hipercalciuria inicial vs. aquellos con normocalciuria, no se encontraron diferencias en los valores basales y postcirugía en ambos grupos. En 11 pacientes con filtrado glomerular previo < 60 ml/min, encontramos una parathormona intacta más elevada que el resto y menor densidad mineral ósea. El filtrado glomerular no cambió en forma significativa luego de la cirugía. En conclusión, el hiperparatiroidismo primario operado por cirujanos especializados tiene una excelente evolución a largo plazo, con normalización de todos los parámetros del metabolismo fosfocálcico y del remodelado óseo y mejoría significativa en la densidad mineral ósea. Los efectos adversos son escasos y de resolución espontánea.
Palabras clave: Hiperparatiroidismo primario; Evaluación postoperatoria alejada
Abstract
Primary hyperparathyrodism: Postoperative long-term evolution. The long-term postoperative outcome of 87 patients with primary hyperparathyrodism is here presented. Of the total 78 were females and 9 males, ratio: 8.7:1. Mean age 55.3 ± 10.2 years. Before surgery, 44% had kidney stones, 70% had osteopenia or osteoporosis and 71.2% had hypercalciuria. Decrease renal glomerular filtration was found in 12.6%. Of the total, 72 patients had a single adenoma, two double adenoma, two hyperplasia, four had normal histology and seven could not dispose of the result. Serum calcium, ionized calcium, phosphorus and intact parathyroid hormone were normalized in all post surgery patients. Bone mineral density increased by 6.9% in lumbar spine and 3% in femoral neck. Markers of bone remodeling were normalized and persisted normal 23 months of follow-up, coinciding with the normal intact parathyroid hormone. Same thing happened with the values of 25 OH D. When patients whith initial hypercalciuria were compared with those with normocalciuria, no differences were found in the basal values and postsurgery in both groups. In 11 patients with previous renal glomerular filtration < 60 ml / min, we found a higher intact parathyroid hormone and lower bone mineral density than the rest. The glomerular filtration rate did not change significantly after surgery. In conclusion, the surgical primary hyperparathyroidism, operated by specialized surgeons has an excellent long-term outcome, with normalization of all parameters of phosphocalcic metabolism and bone remodeling and significant improvement in bone mineral density. Adverse effects were scarce and had spontaneous resolution.
Key words: Primary hyperparathyroidism; Long term postoperative evaluation
El hiperparatiroidismo primario (HPP) es una enfermedad caracterizada por persistente hipercalcemia en presencia de un inapropiado (normal o elevado) nivel de hormona paratiroidea (PTH)1. Si bien no hay estudios de prevalencia en nuestro medio, un estudio realizado en el Instituto de Investigaciones Médicas entre 1958 y 19692 describe una frecuencia de un caso cada 2520 pacientes estudiados. En países desarrollados como EE.UU., el hiperparatiroidismo primario varía entre el 0.1% y 1%3.
Es 2-5 veces más frecuente en mujeres que en varones. La base anatomopatológica más común es el adenoma de una de las glándulas paratiroideas, aunque otras causas son la hiperplasia multiglandular, el doble adenoma y el carcinoma4. Se coincide en que la solución definitiva de esta enfermedad es la cirugía5. Los requisitos que se siguen en la actualidad. para decidir la misma, se basan en los criterios del Consenso realizado por The National Institute of Diabetes and Digestive and Kidney Diseases, junto con The Office of Medical Applications of Research of the National Institutes of Health (NHI). en 19906, reformulados en 20027 y posteriormente en 20098. Según estas Guías, con sólo uno de los siguientes requisitos se justificaría la cirugía: calcemia superior a 1 mg/dl sobre el nivel normal, presencia de litiasis renal, osteoporosis, filtrado glomerular menor a 60 ml/min o una edad menor a 50 años. Sin embargo, en una reunión de Consenso de la Federación Argentina de Sociedades de Endocrinología (FASEN),sobre hiperparatiroidismo primario, realizada en la provincia de Córdoba en 2005, a los criterios quirúrgicos referidos se adicionó la presencia de una calciuria > 400 mg/24 h9.
El compromiso óseo de esta enfermedad ha variado marcadamente desde la osteítis fibrosa quística, hoy casi una rareza, a la disminución de la masa ósea fácilmente medida por técnicas de absorciometría dual por rayos X (DXA)5, que permiten evaluar con alta sensibilidad la disminución de la densidad mineral ósea. La DXA ha ayudado a evaluar el mayor o menor compromiso del hueso cortical o trabecular en esta enfermedad10-13. Varios estudios14 15 han focalizado el compromiso en el hueso apendicular de predominio cortical, con conservación del hueso esponjoso de tipo trabecular. Incluso se ha demostrado16 un aumento en el número de fracturas de radio, vertebra y de miembros inferiores antes de la cirugía. Algunos autores17-19 han encontrado beneficios en la densitometría ósea (DMO) en pacientes operados vs. no operados. Por otro lado, la mayor facilidad en la determinación de marcadores bioquímicos, ha permitido conocer con mayor precisión y rapidez los cambios en el metabolismo mineral como en el remodelado óseo de estos pacientes. Ambrogini y col.20 muestran beneficios en los marcadores del remodelado óseo a los dos meses de la paratiroidectomía, que se mantienen en el tiempo.
El objetivo del presente trabajo fue evaluar, en nuestros pacientes con HPP, la respuesta ósea, los marcadores del metabolismo fosfocálcico y del remodelado óseo antes y después de una cirugía paratiroidea exitosa a largo plazo.
Materiales y métodos
Se seleccionaron, en forma retrospectiva, las historias clínicas de 87 pacientes con HPP confirmados por hipercalcemia, calcio iónico elevado, hipofosfatemia y aumento de la parathormona intacta (PTHi) en por lo menos dos oportunidades. Del total, 78 fueron mujeres (90%) y 9 varones (10%) relación M/V: 8.7: 1. La edad media fue 55.3 ± 10.2 años. Del total 19 (10%) fueron menores de 50 años y entre las mujeres 13 (16.7%) fueron premenopáusicas. Presentaron litiasis renal 38 pacientes (44%), osteopenia 24 (26%) y osteoporosis 45 (52%), el resto presentó densitometría ósea normal. En 5 pacientes se encontraron fracturas relacionadas con la baja masa ósea. En 62 pacientes (71.2%) se observó, en el preoperatorio, hipercalciuria (HI) y en 16 (18.8%) normocalciuria (NHI). Presentaron hipercalcemia marcada (> 1 mg/dl sobre el valor normal) 24 pacientes (28%). Disminución del filtrado glomerular (< 60 ml/min) 11 (12.6%). Todos los pacientes fueron sometidos a paratiroidectomía (Ptx) debido a que reunían criterios absolutos para cirugía del HPP. Esta se realizó, en todos los casos, con cirujanos especializados en cabeza y cuello. Se consideró exitosa la cirugía cuando se normalizaron la calcemia, el calcio iónico, el fósforo y la PTHi en el postoperatorio. Dos pacientes presentaron disfonía post-quirúrgica que se corrigió espontáneamente con la evolución. No hubo otras complicaciones de interés, excepto en 7 casos leve hipocalcemia en el postoperatorio inmediato que revirtió con el agregado de calcio y/o calcitriol. Los datos histológicos mostraron: adenoma único en 72 pacientes, adenoma doble en 2, hiperplasia en 2, histología normal en 4 y en 7 no se pudo disponer del resultado.
La densidad mineral ósea fue medida en todos los pacientes en columna lumbar y cuello de fémur izquierdo (no se tuvieron en cuenta, para el análisis las pocas mediciones realizadas en radio distal). Los equipos utilizados fueron Lunar DPX IQ y Lunar Prodigy (Lunar Corp.of Madison. WI) y Hologic Delphy A (Hologic Inc.of Waltham, MA). sometidos a calibración y control de calidad diarios10. Los criterios diagnósticos de masa ósea se basaron en la clasificación densitométrica establecida en 1994 por la Organización Mundial de la Salud (OMS), referida al número de desvíos estándar en que se aleja la DMO de la media de una población joven normal (T-score) tomada como referencia. En el caso de mujeres premenopáusicas y varones menores de 50 años se utilizó el Z-score considerando baja masa ósea a valores menores a 2. La interpretación en los varones > 50 años se asimiló a los de las mujeres postmenopáusicas. La presencia de litiasis renal se estableció por la eliminación de un cálculo, la extracción de los mismos por parte de un cirujano o la presencia en estudios por imágenes (Rx, ultrasonografía y/o tomografía computada). A pesar que el diagnóstico de HPP es bioquímico, en todos los casos se trató de localizar el probable adenoma mediante la realización de ecografías del cuello y centellogramas paratiroideos con Sesta-mibi.
Se obtuvieron dos muestras de orina de 24 h seguidas de una muestra en ayunas de 2 h recogida en forma espontánea a la mañana del día siguiente en que se realizó una extracción de sangre. En ésta se midió: calcemia, calcio iónico, fósforo, PTHi, creatinina, 25 OH D, fosfatasa alcalina (FAL), FAL isoenzima ósea (FAIO), osteocalcina (BGP) y β crosslaps (CTX). En orina se midieron: calcio, creatinina, sodio y deoxipiridinolina. Los métodos y valores normales de laboratorio fueron: creatinina: método cinético de Jaffe, VN: 0.60-1.20 mg/dl en sangre, calcio (Ca): método ISE, VN: 8.8-10.5 mg/dl en plasma y menor en orina a 220 y 300 mg/24 h en mujeres y hombres respectivamente, fósforo (P): método cinético, VN: 2.7-4.5 mg/dl sérico, parathormona intacta: PTHi electroquimioluminiscencia, VN: 10-65 pg/ml. 25 (OH) D3: radioinmunoanálisis, VN: 20-40 ng/dl, fosfatasa alcalina total (FAL): método cinético, VN: 90-280 UI/l,,fosfatasa alcalina ósea (FAIO): método cinético. VN: 20-48% y β crosslaps sérico (CTX): electroquimioluminiscencia,VN: 556 ± 226 pg/ml, deoxipiridinolina/creatinina: ELISA, Metra Biosystems VN: 3-8 nM DPir/mM Creat.
Se calcularon en orina: la relación deoxipiridinolina/creatinina de 2 h (DPD/Cr 2 h), el calcio/kg/peso y el clearence de creatinina. Este último fue corregido por superficie corporal.
En el primer mes de la cirugía se realizaron las siguientes mediciones en sangre: calcio, calcio iónico, fósforo y PTHi. Luego, y como parte del presente estudio, se consideraron las mediciones en sangre y orina realizadas a los 23 ± 12 meses de la cirugía, con una mediana de 20.
No se evaluó en el postoperatorio la recurrencia de la litiasis renal en este estudio.
Los marcadores del remodelado óseo se compararon cuando existieron, en un mismo paciente, marcadores pre y postcirugía de los mismos. Por tal motivo, en algunos se consideró el índice DPD/Cr 2h y en otros el β crosslaps.
Los resultados se expresaron como media ± DS. El test de Student apareado se utilizó para comparar los valores pre y postcirugía. En las variables que no presentaban distribución normal, el tratamiento estadístico se realizó luego de transformación logarítmica. Una p ≤ 0.05 se consideró un valor significativo.
Resultados
En la Tabla 1 se muestran los valores séricos de los 87 pacientes en el preoperatorio dentro del primer mes de la cirugía, y en promedio a los 23 meses de seguimiento. Los rangos basales fueron: calcemia: 9.6 a 13.4 mg%, calcio iónico: 4.1 a 7.4 mg%, fósforo: 2 a 4.2 mg% y PTHi: 56.6 a 362 pg/ml. Los rangos a los 23 ± 12 meses fueron: calcemia: 8.8 a 10.4, calcio iónico: 3.05 a 5.2 mg%, fósforo: 2.7 a 4.8 mg% y PTHi: 13.6 a 94.8 pg/ml. Es de destacar que el paciente con PTHi elevada presentó una calcemia de 9.6 mg%, un calcio iónico de 4.7 mg% y un fósforo de 3.6 por lo que el diagnóstico de HPP persistente o recurrente no pudo ser establecido a los 33 meses de seguimiento. Este mismo paciente presentó al mes de la cirugía una calcemia de 9.8 mg% y un calcio iónico de 4.7 mg%. Los datos presentados en esta Tabla muestran normalización de todos los parámetros séricos en los 87 pacientes estudiados, luego de la cirugía paratiroidea. El clearence de creatinina (Cl Cr) basal fue de 83.4 ± 27 ml/min y a los 23 meses de 76.6 ± 17.6 ml/min, siendo la diferencia no estadísticamente significativa. La calciuria de 24 h varió de 359.1 ± 148 mg/24 h en el período basal a 206.3 ± 105.4 mg/24 h a la finalización del estudio (p < 0.001). El sodio urinario varió de 151.9 ± 56.3 mEq/d basal a 141.8 ± 58.6 mEq/d a los 23 meses, diferencia no significativa. Del total de pacientes que persistieron con hipercalciuria postoperatoria, al año se agregó hidroclorotiazida a 9 de ellos y a los demás se los colocó en una dieta con 800 mg de calcio/día, dependiendo si la hipercalciuria fue dieta dependiente o no.
TABLA 1.- Comparación de parámetros bioquímicos en sangre, basales, al mes y a los 23 meses postcirugía (Ptx)
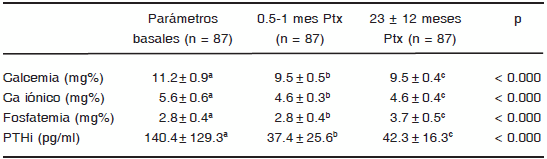
Significancia entre a y b-c. No hubieron diferencias entre b y c
Los valores densitométricos en columna lumbar (DMO CL) y cuello de fémur izquierdo (DMO CF) se muestran en la Tabla 2. Comparando los valores basales con los medidos a los 23 ± 12 meses, hubo un aumento del 6.9% (0.880 ± 0.018 a 0.939 ± 0.02 en columna lumbar, p < 0.001) y del 3% (0.762 ± 0.015 a 0.783 ± 0.013 en cuello de fémur, p < 0.01) a los 23 meses de la cirugía paratiroidea. Es de destacar que los controles de los pacientes siempre fueron realizados con el mismo equipo densitométrico que el inicial. De los 87 pacientes analizados (174 regiones medidas) al cabo de los 23 meses del seguimiento 26 (15%) presentaron un aumento de la DMO mayor al 10% en columna lumbar y 16 (9%) en cuello de fémur. De los pacientes que no mejoraron la DMO al año, en 19 se agregó un bisfosfonato como parte del tratamiento.
TABLA 2.- Diferencias densitómetricas en columna lumbar (DMO CL) y cuello de fémur izquierdo (DMO CF), basal y a los 23 ± 12 meses

En la Tabla 3 se muestran los datos del remodelado óseo y la vitamina D al inicio y final del estudio.
TABLA 3.- Valores del remodelado óseo y vitamina D pre y postcirugía (23 meses)

FAL: fosfatasa alcalina; FAIO: FAL isoenzima ósea, BGP: osteocalcina; CTX: β crosslaps, DPD/Cr: deoxipiridinolina/creatinina, Ptx: post-cirugía
Los valores del remodelado óseo fueron medidos en todos los pacientes con referencia a la FAL, FAIO y vitamina D. En cuanto a los marcadores de resorción, en algunos pacientes se utilizó el índice DPD/Cr 2 h y en otros el CTX. Es decir, se repitió el mismo marcador que el inicial en todos los pacientes en que se pudo medir. En la Tabla 3 se muestran los resultados con su n correspondiente. Todos los pacientes que presentaron déficit de vitamina D fueron suplementados con la misma, dato reflejado en el control a los 23 meses.
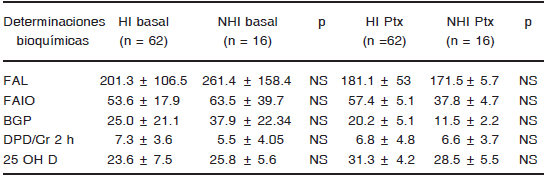
En las Tablas 4, 5 y 6 se comparan los valores del metabolismo fosfocálcico, densitométricos y del remodelado óseo pre y poscirugía en 62 pacientes con hipercalciuria y 16 normocalciúricos. Es de destacar que el promedio de seguimiento en los pacientes con HI fue de 20.7 ± 16.2 meses mientras que en los NHI fue de 27.5 ± 22.1 meses. Como se observa, no existen diferencias significativas en aquellos con hipercalciuria o normocalciuria en referencia a los parámetros del metabolismo fosfocálcico, del remodelado óseo ni de los valores densitométricos al inicio y en la respuesta lograda luego de la cirugía paratiroidea. En cuanto a la presencia de litiasis renal, ésta fue observada en 31 pacientes con HI (50%) y en 5 con NHI (31%). De los 62 pacientes con hipercalciuria preoperatoria, persistieron con la misma 18 (29%).
TABLA 4.- Comparación de parámetros bioquímicos en sangre, basales y postcirugía entre HI y NHI

HI: pacientes hipercalciúricos. NHI: no hipercalciúricos; PTHi: parathormona intacta
TABLA 5.- Diferencias densitométricas basales y postcirugía entre HI y NHI

TABLA 6.- Valores del remodelado óseo y vitamina D pre y postcirugía alejada entre pacientes con HI y NHI
Finalmente seleccionamos 11 pacientes previo a la cirugía, con filtrado glomerular (FG) < 60 ml/min (criterio quirúrgico, según las normas del Consenso) y no encontramos cambios significativos en la calcemia, calcio iónico y fósforo basales. Hubo un leve aumento en el nivel de PTHi, 160.3 ± 129 vs. 137.5 ± 129 con respecto al resto de los 67 pacientes con FG > 60 ml/min, que fue estadísticamente significativo (p < 0.001). La DMO basal de columna lumbar fue de 0.815 ± 0.115 g/cm2 (- 7.4% comparada con el grupo total, p < 0.001) y en cuello de fémur de 0.669 ± 0.119 g/cm2 (- 12%, p < 0.001). El filtrado glomerular varió de 48.7 ± 7.2 a 53 ± 12.4 ml/min, sin significado estadístico.
Discusión
En el presente estudio se muestran los resultados previos y posteriores (largo plazo) de pacientes con HPP y cirugía paratiroidea. Se evalúan los cambios en la densitometría ósea, tanto en hueso trabecular como cortical, las variaciones en los parámetros del metabolismo fosfocálcico y del remodelado óseo. Además se compara la evolución de aquellos pacientes hipercalciúricos o normocalciúricos antes y después de la cirugía.
En general se acepta que la paratiroidectomía tiene un alto porcentaje de éxito3, 7, 21 que oscila entre 90-95% en manos especializadas. En nuestro grupo de pacientes hemos observado un 100% de éxitos postquirúrgicos. Creemos que esto puede estar vinculado al estricto rigor que se puso para establecer el diagnóstico y fundamentalmente al trabajo del equipo quirúrgico, reduciendo al mínimo la posibilidad de error. Uno de nuestros pacientes presentó a los 23 meses una PTHi elevada con calcemia, calcio iónico y fósforo dentro de valores normales. Además, este mismo paciente, en el control al mes, presentó todos estos parámetros normales, por lo que descartamos un HPP recurrente o persistente. De todos modos, el seguimiento periódico aclarará esta duda. Todos los pacientes normalizaron la calcemia, el calcio iónico, el fósforo y la PTHi en el control al mes de la cirugía y se mantuvieron de esta forma durante todo el seguimiento. Encontramos hipercalciuria en el 71.2% de nuestros pacientes, similar al 63.6% de Corbetta y col24 en 55 pacientes con HPP, y superior al 39% encontrado por Silverberg y col25 en 24 pacientes en quienes relacionó el aumento de la calciuria al de 1.25 (OH)2 D, dato no corroborado por Pak y col26 y tampoco por nuestro estudio en los pocos pacientes en que pudimos medir calcitriol (dato no mostrado). La calciuria de 24 h se redujo en promedio, desde el valor basal hasta el control final, un 42% siendo estadísticamente significativa. Este dato coincide con el 44% observado en 61 pacientes en el primer año y a los 10 años de la paratiroidectomía por Silverberg y col23 y con el 55 % encontrado en 59 pacientes por Parks y col27. Es de destacar que la natriuria pre y postoperatoria en nuestros pacientes no se modificó en forma significativa (dato no mostrado).
La densitometría ósea aumentó significativamente tanto en columna lumbar como en cuello de fémur luego de la cirugía. Mayor diferencia se produjo en columna lumbar (hueso a predominio esponjoso) que en el cuello de fémur (a predominio cortical). El aumento observado por nosotros (6.9%) en columna lumbar coincide con el 8.2% encontrado por Silverberg y col5 en 34 pacientes con HPP durante los 2 primeros años post-cirugía, aumentado a un 12.8% al cabo de 4 años. En cambio, estos autores encuentran un aumento mayor en cuello de fémur, 5.9%, que es levemente superior al 3% hallado por nosotros. Ambrogini y col20 encuentran un aumento del 4.16% en columna lumbar y del 2.61% en cadera total, datos también similares a los nuestros. No encuentran cambios en la densidad del radio distal en forma similar a otros autores28. En el presente estudio hemos observado un total de 24% de pacientes con más de un 10% de aumento en la DMO de columna lumbar o cuello de fémur. Sin embargo, debido al alto porcentaje de pacientes con osteoporosis u osteopenia, la cirugía no logró normalizar la densidad mineral ósea en todos, a pesar de corregir el remodelado óseo, aunque sí hubo un aumento marcado en la mayoría. Clásicamente, el exceso sostenido de PTH como se observa en el HPP, se asocia a un mayor compromiso del hueso cortical como el cuello de fémur y principalmente del radio distal, que sobre el hueso trabecular29. Paradójicamente, si bien hay un aumento de la DMO en el hueso cortical y el trabecular luego de la cirugía paratiroidea, el mayor incremento se describe en el hueso esponjoso5 tal cual lo observado en nuestros pacientes. Una hipótesis podría ser la sugerida por Reeve y col30 y por Slovik y col31 quienes sostienen que la cirugía restaura la pulsatibilidad normal de la secreción de hormona paratiroidea, que estimula fundamentalmente el hueso esponjoso. Sin embargo esto contrasta con lo descripto por otros autores utilizando estudios histomorfométricos en donde encuentran un aumento del hueso esponjoso en el HPP previo a la cirugía del 26 y 32%13, 32 y una reducción en el hueso de tipo cortical, poniendo en duda la correlación de los hallazgos en estudios histológicos y los realizados comúnmente por densitometrías por Rx.
Entre los parámetros del remodelado óseo hemos observado una caída significativa en 2 marcadores de formación como la FAL y FAIO y 2 de resorción como el β crosslaps y la DPD/Cr 2h. No encontramos cambios pre y poscirugía en la osteocalcina. También hemos observado leve aumento de la 25 OH D aunque sin alcanzar cambios significativos. Quizás el pequeño número de nuestras muestras no permitieron encontrar una significancia mayor. De todos modos, está claro que la normalización de la PTHi poscirugía normaliza el turnover óseo. Datos similares fueron encontrados por Ambrogini y col20, quienes encontraron disminución de los marcadores a los 2 meses de la cirugía que se mantuvieron durante todo el período de seguimiento. Por otro lado, Janson y col33 encuentran una disminución del la FAIO a los 12 y 24 meses de la cirugía, sin cambios significativos en los valores de osteocalcina, similar a nuestros hallazgos. El aumento de la 25 HO D que se observa en algunos estudios postcirugía podría ser atribuido a una reversión de la acción de la 25 hidroxilasa hepática, disminuida en parte por los bajos niveles de 25 OH D observados en el HPP34.
Cuando comparamos los valores bioquímicos, densitométricos y del remodelado óseo entre los pacientes que presentaban hipercalciuria o normocalciuria en el preoperatorio, no encontramos diferencias significativas. La normalización de los parámetros del metabolismo fosfocálcico, del remodelado óseo y de la densitometría ósea fue similar entre sí y al total de los pacientes analizados. De esto se desprende que no influye en la respuesta quirúrgica del HPP la presencia o no de hipercalciuria inicial. Sin embargo, aquellos que persistían con hipercalciuria luego de la cirugía fueron corregidos, o bien con dieta o con el agregado de diuréticos tiazídicos.
Finalmente y considerando que un filtrado glomerular < 60 ml/min, (insuficiencia renal estadio 3 según las guías de la National Kidney Foundation Disease Outcomes Quality Initiative-K/DOQI), está considerado como una indicación de tratamiento quirúrgico7 dado que se acompañaría de mayor nivel de PTHi y mayor deterioro de la función renal, encontramos en 11 pacientes que reunían dichos criterios que la calcemia, el calcio iónico y el fósforo sérico fueron similares en la medición basal al resto de los pacientes, aunque sí hubo un aumento significativo de la PTHi con respecto a los pacientes con HPP y FG > 60 ml/min y no observamos modificaciones en el filtrado glomerular antes o después de la cirugía, a diferencia de lo referido por Tassone y col35. En cambio sí observamos en estos pacientes una menor DMO tanto en columna lumbar y principalmente en cuello de fémur con respecto al grupo total, alcanzando significado estadístico.
En conclusión: la paratiroidectomía en la población con HPP analizada tuvo resultados exitosos en la totalidad de los pacientes. La DMO se recuperó, en forma significativa, tanto en hueso trabecular como cortical, aunque no se observó normalización de la misma. Los parámetros del remodelado óseo se corrigieron al normalizarse la PTHi.
Los pacientes con FG < 60 ml/min tuvieron mayor valor de PTHi y menor DMO basal y constituyen una indicación de cirugía paratiroidea, como se establece en las guías de tratamiento universales. El HPP, con hipercalciuria o normocalciuria basal, tiene un mismo patrón inicial y un comportamiento similar luego de la cirugía. Las complicaciones postoperatorias fueron leves, transitorias y se resolvieron en forma espontánea.
En definitiva, la suma de un correcto diagnóstico bioquímico y un cirujano experimentado en cabeza y cuello son garantía suficiente para alcanzar la "curación de esta enfermedad.
Conflictos de interés: no hay conflicto de intereses entre los autores del presente trabajo.
1. Bilezikian JP, Silverberg HJ. Asymptomatic primary hyperparathyroidism. N Engl J Med 2004; 350: 1746-51. [ Links ]
2. Mautalen CA, Gallo Morando C, Torres Agüero M, Barcat JA, Arata RO. Molins M. Tratamiento quirúrgico del hiperparatiroidismo. Medicina (Buenos Aires) 1972; 32: 150-8. [ Links ]
3. Boonstra C. Jackson C. Serum calcium survey for hyperparathyroidism: Results in 50.000 clinic patients. Am J Clin Pathol 1971; 55: 523-8. [ Links ]
4. AACE/AAES Task Force on Primary Hyperparathyroidism. The American Association of Clinical Endocrinologists and the American Association of Endocrine Surgeons position statement on the diagnosis and management of primary hyperparathyroidism. Endocr Pract 2005; 11: 49-54. [ Links ]
5. Silverberg SJ, Gartenberg F, Jacobs TP, et al. Increased bone mineral density after parathyroidectomy in primary Hyperparathyroidism. J Clin Endocrinol Metab 1995; 80: 729-34. [ Links ]
6. Consensus Development Conference Statement on Diagnosis and Management of Asyntomatic Primary Hyperparathyrodism. J Bone Miner Res 1991; 6: S9-S13. [ Links ]
7. Bilezikian JP, Potts JT, Jr Fuleihan GE, et al. Summary statement from a workshop on asymptomatic primary hyperparathyroidism: a perspective for the 21st century. J Clin Endocrinol Metab 2002; 87: 5353-61. [ Links ]
8. Bilezikian JP, Khan AA, Potts JT Jr. Guidelines for the management of asymptomatic primary hyperparathyroidism: Summary Statement from the Third International Workshop. J Clin Endocrinol Metab 2009; 94: 335-39. [ Links ]
9. Sánchez A, Ercolano M, Frigeri A, et al. Consenso de la Federación Argentina de Sociedades de Endocrinología (FASEN) sobre Hiperparatiroidismo Primario. Revista Argentina de Endocrinología y Metabolismo 2006; 43: 160-73. [ Links ]
10. Orwoll ES, Oviatt SK, Biddle JA. Precision of Dual-Energy X-Ray 12. Absorptiometry: Development of quality control rules and their application in longitudinal studies. J Bone Miner Res 1993; 8: 693-9. [ Links ]
11. Martin P, Bergmann P, Gillet C. Partially reversible osteopenia after surgery for primary hyperparathyroidism. Arch Intern Med 1986; 146: 689-91. [ Links ]
12. Richardson ML, Pozzi-Mucelli RS, Kanter AS, Kolb FO, Ettinger B, Genant HK. Bone mineral changes in primary hyperparathyroidism. Skel Radiol 1986; 15: 85-95. [ Links ]
13. Parisien M, Dempster DW, Shane E, Bilezikian J. Histomorphometric analysis of bone in primary hyperparathyroidism. In The Parathyroids. (Edited by JP Bilezikian. MA Levine and R Marcus) New York: Raven Press Ltd, 1994, pp 493-503. [ Links ]
14. Wishart J, Horowitz M, Need A, Nordin BE. Relationship between forearm and vertebral mineral density in postmenopausal women with primary hyperparathyroidism Arch Intern Med 1990; 150: 1329-31. [ Links ]
15. Wilson RJ, Rao S, Ellis B, Kleerekoper M, Parfitt AM. Mild asymptomatic primary hyperparathyroidism is not a risk factor for vertebral fractures.Ann Intern Med 1988; 109: 95962. [ Links ]
16. Vestergaard P, Mollerup CL, Frakjaer VG, Christiansen P, Blichert-Toft M, Mosekilde L. Cohort study of risk of fracture before and after surgery for primary hyperparathyroidism. BMJ 2000; 321: 598-602 [ Links ]
17. Rao DS,Phillips ER, Divine GW, Talpos GB. Randomized controlled clinical trial of surgery versus no surgery in patients with mild asymptomatic prymary hyperparathyroidism. J Clin Endocrinol Metab 2004; 80: 5415-22. [ Links ]
18. Bollerslev J, Jansson S, Mollerup CL, et al. Medical observation compared to Parathyroidectomy for asymptomatic primary hyperparathyroidism: a prospective. Randomized trial. J Clin Endocrinol Metab 2007; 92: 1687-92. [ Links ]
19. Christiansen P, Steiniche T, Brixen K, et al. Primary hyperparathyroidism: effect of parathyroidectomy on regional bone mineral density in Danish patients. A three year followup study. Bone 1999; 25: 589-95. [ Links ]
20. Ambrogini E, Cetani F, Cianferotti L, et al. Surgery or Surveillance for Mild Asynptomatic Primary Hyperparathyroidism: A Prospective. Randomized Clinical Trial. J Clin Endocrinol Metab 2007; 92: 3114-21. [ Links ]
21. Alledorf J, Kim I, Chabot J, DiGiorgi M, Spanknebel K, LoGerfo P. The impact of Sestamibi scanning on the outcome of parathyroid surgery. J Clin Endocrinol Metab 2003; 88: 3015-8. [ Links ]
22. Walgenbach S, Hommel G, Junginger T. Outcome after surgery for primary hyperparathyroidism: ten year prospective follow-up study. World J Surg 2004; 24: 564-9. [ Links ]
23. Silverberg SJ, Shane E, Jacob TP, Siris E, Bilezikian JP. A 10 - year prospective study of primary hyperparathyroidism with or without parathyroid surgery. N Engl J Med 1999; 341: 1249-55. [ Links ]
24. Corbetta S, Baccarelli A, Aroldi A, et al. Risk factors associated to kidney stones in primary hyperparathyroidism. J Endocrinol Invest 2005; 28: 122-8. [ Links ]
25. Silverberg SJ, Shane E, Jacobs TP, et al. Neprholithiasis and bone involvement in primary hyperparathyroidism. Am J Med 1990; 89: 327-34. [ Links ]
26. Pak CY, Nicar MJ, Peterson R, et al. A lack of unique pathophysiologic background for neprhrolithiasis of primary hyperparathyroidism. J Clin Endocrinol Metab 1981; 53: 536-42. [ Links ]
27. Parks JH, Coe FL, Evan AP, Worcester Evan, Elaine M. Clinical and laboratory characteristics of calcium stone-formers with and without primary hyperparathyroidism. BJU Int 2009; 103: 670-8. [ Links ]
28. Parfitt AM. Accelerated cortical bone loss; primary and secondary hyperparathyroidism. In: Uhthoff HK. Stahl E. eds. Current concepts of bone fragility. Berlin: Springer-Verlag,1986: 279-85. [ Links ]
29. Silverberg SJ, Shane E, de la Cruz L, et al. Skeletal disease in primary hyperparathyroidism. J Bone Miner Res 1989; 4: 283-91. [ Links ]
30. Reeve J, Meunier PJ, Parsons JA, et al. Anabolic effect of human parathyroid hormone fragment on trabecular bone in involutional osteoporosis: a multicentre trial. BMJ 1980; 280: 1340-4. [ Links ]
31. Slovik DM, Rosenthal DI, Doppelt SH, et al. Restoration of spinal bone in osteoporosis men by treatment with human parathyroid hormone (1-34) and 1.25-dihydroxyvitamin D. J Bone Miner Res 1986; 1: 377-81. [ Links ]
32. Delling G. Bone morphology in primary hyperparathyrodism. A qualitative and quantitative study of 391 cases. Appl pathol 1987; 55: 147-59. [ Links ]
33. Jansson S, Morgan E. Biochemical effects from treatment with bisphosphonate and surgery in patients with primary hyperparathyroidism. World J Surg 2004; 28: 1293-7. [ Links ]
34. Clemens MR, Davies M, Fraser DR, Lumb GA, Mawer EB, Adams PH. Metabolic inactivation of vitamin D is enhanced in primary hyperparathyroidism. Clin Sci 1987; 73: 659-64. [ Links ]
35. Tassone F, Gianotti L, Emmolo I, Ghio M, Borretta G. Glomerular filtration rate and parathyroid- hormone secretion in primary hyperparathyroidism. J Clin Endocrinol Metab 2000; 94: 4458-61. [ Links ]
Recibido: 7-1-2010
Aceptado: 18-6-2010














