Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680
Medicina (B. Aires) vol.71 no.2 Ciudad Autónoma de Buenos Aires mar./abr. 2011
CASUÍSTICA
Mielitis transversa relacionada con vacunación anti-influenza A(H1N1)
María Florencia Arcondo1, Adolfo Wachs1, Marcelo Zylberman1
1División Clínica Médica, Hospital General de Agudos Dr. Cosme Argerich, Buenos Aires
Dirección postal: Dra. María Florencia Arcondo, Sarmiento 815, 1832 Lomas de Zamora, Buenos Aires, Argentina Fax: 4362-6490 e-mail: farcondo@gmail.com
Resumen
La mielitis transversa es una enfermedad inflamatoria que se caracteriza por disfunción de la médula espinal. Las causas reconocidas de mielitis transversa son autoinmunes, enfermedades desmielinizantes, post infecciosas y post vacunales, aunque hasta el 50% de los casos son idiopáticas. Las vacunas contra la rubéola, paperas, rabia y gripe estacional han sido asociadas a diversos trastornos neurológicos, como el Síndrome de Guillain Barré, la encefalomielitis diseminada aguda (ADEM) y la mielitis transversa. Como mecanismo preventivo luego de la pandemia de 2009, en febrero del año 2010 se inició en nuestro país la campaña de vacunación contra la Influenza A (H1N1). Se presenta el caso de una paciente con hipoestesias que aparecieron cuatro días después de haber recibido la vacuna monovalente anti-influenza A (H1N1) y progresaron con evidente nivel sensitivo. La paciente cumplía criterios diagnósticos de mielitis transversa, según el Transverse Myelitis Consortium Working Group. Tuvo remisión de las imágenes de la resonancia magnética y estabilidad clínica sin tratamiento con corticoides. Se discuten aspectos diagnósticos, pronósticos y terapéuticos de esta entidad clínica.
Palabras clave: Mielitis; Vacunación; Influenza A (H1N1)
Abstract
Transverse myelitis associated with anti-influenza A (H1N1) vaccination. Transverse myelitis is an inflammatory disorder characterized by spinal cord dysfunction. Infectious, autoimmune, postinfectious and postvaccination diseases are the most common recognized causes of transverse myelitis, but near 50% of the cases are finally assumed as idiopathic. Rubeolla, mumps, rabies and influenza vaccines were associated with many neurologic complications, such as Guillain Barré Syndrome, acute disseminated encephalomyelitis (ADEM) and transverse myelitis. As a prevention measure after the 2009 pandemia, in February 2010 a National Campaigne of Vaccination against the Influenza A (H1N1) was started in our country. We report a case of a woman who received a monovalent Influenza A (H1N1) vaccine and four days after, began with sensory symptoms that progressed to a clear defined sensory level. She reached the clinical criteria of transverse myelitis, according to the Transverse Myelitis Consortium Working Group. One month later, the patient remained clinically stable and the MRI showed an improvement of the image without corticosteroids treatment. We discuss diagnostic, prognostic and therapeutic aspects of this clinical entity.
Key words: Mielytis; Vaccination; Influenza A (H1N1)
En junio del 2009 la OMS declaró la primera pandemia de este siglo sobre la base de las características epidemiológicas del virus de influenza tipo A (H1N1). La Argentina fue uno de los 10 países más afectados, habiéndose registrado cerca de 12 000 casos confirmados, 14 160 hospitalizados por infección respiratoria y más de 600 defunciones1, 2. En febrero de 2010 comenzó la campaña nacional de vacunación contra la gripe A, con vacuna monovalente a virus inactivado de la cepa viral pandémica A/California/7/2009 con adyuvante MF 9.
La mielitis transversa es un proceso inflamatorio medular cuya etiología se presume autoinmune2. Su asociación con vacunas contra la rubéola, paperas, rabia y gripe estacional se halla ampliamente descripta en la literatura4, 5.
Presentamos un caso de mielitis transversa con compromiso sensitivo de comienzo agudo luego de la aplicación de la vacuna monovalente contra la Gripe A.
Caso clínico
Mujer de 37 años que consulta por parestesias en ambos miembros inferiores, de 5 días de evolución, que progresan hasta la región submamaria al momento del ingreso.
Al examen se halla lúcida, sin evidencia de compromiso motor y con reflejos osteotendinosos conservados. Presenta alteración de la sensibilidad termoalgésica con nivel T3-T4 con sensibilidad profunda conservada. El resto del examen clínico es normal.
Como antecedente relevante, recibió vacuna monovalente para gripe A (H1N1) 4 días antes del comienzo de los síntomas. Al ingreso, Hto: 36%, GB: 5 000/mm3, glucemia: 100mg/dl, urea: 31 mg/dl, creatinina: 0.61 mg/dl, TGO: 12 UI/dl, TGP: 15 UI/dl, FAL: 200 UI/dl, albúmina: 4.2 g/dl, Ca: 9.3 mg/dl, P: 2.9 mg/dl, Mg: 2 mg/dl, colesterol: 195 mg/dl, eritrosedimentación: 36 mm/1° hora, proteína C reactiva: 0.3 mg/dl, Na: 137 mEq/l, K: 3.6 mEq/l, Cl: 99 mEq/l, TSH: 0.47 UI/ml, T4: 8.76 ng/dl, FAN negativo, FR negativo, HIV negativo. Punción lumbar: líquido cefalorraquídeo (LCR) incoloro, 1 célula/mm3, glucorraquia: 0.93 g/dl, proteínas totales: 0.4 g/dl, proteína básica de mielina y bandas oligoclonales negativas. PCR para herpes simple 1 y 2, Zoster y CMV negativas.
Resonancia Magnética Nuclear (RMN) de encéfalo: normal. La de columna (Fig. 1) mostró a nivel C6-C7 imagen hiperintensa en las secuencias T2 y STIR, e iso-hipointensa en T1 de localización central y posterior, de 10 mm de diámetro craneocaudal, de 6 mm de diámetro transverso y 4 mm de diámetro anteroposterior, con tenue realce periférico con gadolinio. Difusión negativa.
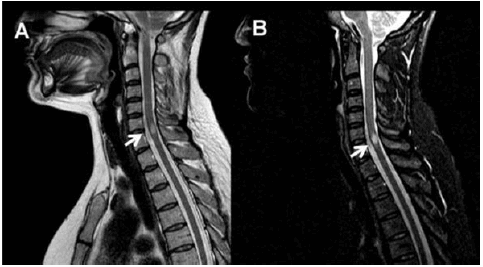
Fig. 1.- Resonancia de columna cervical con gadolinio. Se identifica una imagen ovoidea medular a nivel C6-C7 hiperintensa en T2 (A) y STIR (B) e isointensa en T1.
Los potenciales evocados visuales y auditivos fueron normales. Fue dada de alta luego de 15 días de internación sin cambios en el examen neurológico.
Al mes del comienzo de los síntomas, la paciente refiere mejoría de las parestesias, sin cambios objetivos al examen. Al mes del primer estudio se repite RMN que demuestra imagen levemente hiperintensa en T2 y STIR sin realce luego de la administración de contraste. (Fig. 2).

Fig. 2.- Resonancia de columna cervical con gadolinio, control al mes. Se identifica una atenuación de la intensidad de señal de la imagen medular en T2 (A) y STIR (B).
Se notifica a la Administración Nacional de Medicamentos Alimentos y Tecnología Médica el día 20 de noviembre de 2009 (N° de denuncia: 2449).
Discusión
Diversas complicaciones neurológicas, como neuritis óptica, síndrome de Guillain Barré, parálisis facial periférica, plexitis braquial y lumbar, ataxia cerebelosa, mielitis transversa y encefalomielitis aguda diseminada (ADEM)6, han sido vinculadas con diferentes vacunas.
La mielitis transversa es una injuria segmentaria de la médula espinal causada por un proceso inflamatorio agudo. Reconoce múltiples etiologías: infecciosa, vacunal, asociada a enfermedades autoinmunes como lupus eritematoso sistémico, enfermedad de Sjögren, enfermedad mixta del tejido conectivo, síndrome antifosfolípido y enfermedades desmielinizantes como la esclerosis múltiple (EM) o la enfermedad de Devic. Hasta un 50% son finalmente asumidas como idiopáticas. Su incidencia estimada ronda entre los 1.3 y 4.6 casos por millón por año con picos bimodales de edad: 10-19 años y 30-39 años7. No existe predisposición familiar, étnica, sexual ni variación geográfica descripta3.
Para su diagnóstico, el Transverse Myelitis Consortium Working Group propuso en el año 2002 los siguientes criterios: disfunción motora, sensitiva o autonómica atribuible a la médula espinal con claro nivel definido, cuya mayor intensidad se alcanza entre las 4 horas y los 21 días de comienzo de los síntomas, con evidencia de inflamación ya sea por pleocitosis en LCR, aumento de síntesis intratecal de IgG o hallazgos en la RMN con gadolinio8. En el análisis publicado por Agmon-Levin9 se recolectaron 37 casos de mielitis transversa relacionada con vacunación desde 1970 a 2009. En el 73% de los casos, los síntomas comenzaron en el primer mes posterior a la vacunación. La mayoría de los casos fueron consecutivos a la vacuna anti-hepatitis B (HBV) seguido por la triple viral (SRP), la triple bacteriana (DPT), la antirrábica y antipolio oral; dos casos ocurrieron luego de la vacuna anti-influenza estacional.
Dentro de los mecanismos que se postulan las vacunas pueden inducir mielitis transversa se encuentran: el mimetismo molecular10 entre los antígenos infecciosos y los propios, propagación de epitopes, mediante el cual los antígenos invasores aceleran un proceso autoinmune en curso por la activación local de células presentadoras de antígenos y la activación policlonal de linfocitos B (LB) que aumenta la producción de citoquinas y además induce la expansión de linfocitos T (LT) autorreactivos11. Cabe destacar que no pueden descartarse dentro de los mecanismos desencadenantes a los adyuvantes o conservantes.
La vacuna antigripal se encuentra formulada con virus muerto o inactivado y a diferencia de otras vacunas, su perfil antigénico cambia año tras año. La vacuna administrada a nuestra paciente es una vacuna con virus inactivo de la cepa pandémica A/California/7/2009 con adyuvante MF 9. Según los registros del VAERS (Vaccine Adverse Event Reporting System) al 24 de noviembre de 2009 en EE.UU. se denunciaron 82 reacciones adversas por millón de vacunas anti-H1N1 distribuidas, de las cuales sólo el 4.4 por millón fueron graves (204 casos). De ellos, 12 fueron Guillain-Barré, 19 casos por anafilaxia, los 173 restantes están aún en evaluación. Cabe destacar que estos casos incluyen también la vacuna a virus atenuado intranasal de uso en EE.UU.11.
El Brighton Collaboration Encephalomyelits/ADEM Working Group identificó las principales características clínicas y epidemiológicas necesarias para la definición de casos de encefalitis, mielitis y ADEM y debidas a reacción adversa post inmunización13. Se estipulan 3 niveles de evidencia que otorgan seguridad al diagnóstico. La confirmación histopatológica define al nivel 1. La evidencia de mielopatía por compromiso sensitivo, motor o autonómico define los niveles 2 y 3. El nivel 2 requiere además la presencia de dos de los siguientes hallazgos sugestivos de inflamación/desmielinización: fiebre, pleocitosis en LCR (> 5 leucocitos/mm3 en niños ≥2 meses o> 15 leucocitos/mm3 en niños menores de 2 meses) o neuroimágenes que demuestren inflamación o desmielinización. La presencia de uno solo de los criterios anteriores en un paciente con mielopatía define al nivel 3.
Nuestra paciente tiene un diagnóstico de mielitis post vacunal con un nivel 3 de confianza, ya que presenta mielopatía por compromiso sensitivo con nivel definido e imágenes de RMN compatibles con inflamación/desmielinización.
El tiempo entre la vacunación y el comienzo de los síntomas no se considera para este grupo como criterio diagnóstico; aquel puede oscilar entre 2 días y 6 meses.
La principal diferencia entre un inicio de esclerosis múltiple (EM) y un evento desmielinizante post vacunal es la naturaleza monofásica de este último. Por lo tanto, el seguimiento a largo plazo es el que dará la certeza diagnóstica.
En un estudio de 22 casos de mielitis se compararon los hallazgos de RMN entre los pacientes con diagnóstico de EM (previo o en el seguimiento) y aquellos que no lo tenían. Se encontró que las lesiones asociadas a EM abarcan menos segmentos, no refuerzan con contraste y en su mayoría se acompañan de lesiones encefálicas14.
A pesar que la imagen de nuestro caso sólo abarca 2 segmentos, la ausencia de lesiones cerebrales, la ausencia de alteraciones en los potenciales evocados, de PBM y de bandas oligoclonales en LCR alejan la posibilidad de una esclerosis múltiple15.
Con respecto al pronóstico, clásicamente se conoce que un tercio de las mielitis transversas tiene recuperación completa, un tercio queda con algún grado de secuela y el tercio restante permanecerá con deterioro neurológico grave3.
Como en otras tantas enfermedades de baja prevalencia, no existen conductas terapéuticas avaladas por trabajos aleatorios. En la mayoría de los casos se utilizan corticoides, aun siendo controvertida su capacidad de modificar la evolución16. La evidencia disponible sugiere que los esteroides endovenosos serían efectivos cuando son administrados en la fase aguda de la mielitis transversa17. Nuestra paciente llevaba 15 días de evolución y su enfermedad se hallaba estable al diagnóstico. Frente a la fuerte sospecha de asociación con la vacunación, se decidió no instaurar tratamiento y evaluarla periódicamente. Al mes se realizó nueva RMN que demostró regresión de las imágenes.
En conclusión, se presenta un caso de mielitis transversa relacionada con vacunación contra gripe A (H1N1) con compromiso sensitivo y mejoría radiológica al mes del diagnóstico.
Agradecimientos: A los Dres. Jorge Docampo, Carolina Mariluis y Carlos Morales por el apoyo técnico y la colaboración en la presentación de este trabajo.
Conflictos de interés: Los autores declaran no tener conflicto de intereses.
1. Campaña de Invierno 2010. Estado de situación. Ministerio de Salud de la Nación, en http://www.msal.gov.ar/gripe/2_situacion/situacion.asp; consultado el 30 de julio de 2010. [ Links ]
2. Comisión Influenza A (H1N1), Hospital Nacional A. Posadas. Epidemia de influenza A (H1N1) en la Argentina. Experiencia del Hospital Nacional Profesor Alejandro Posadas. Medicina (Buenos Aires) 2009; 69 393-423. [ Links ]
3. Anupama B, Stanley N, Gurtej Ch. The epidemiology of transverse myelitis. Autoimmun Rev 2010; 9: A395-A399. [ Links ]
4. Jeffery DR, Mandler RN, Davis LE. Transverse myelitis. Retrospective analysis of 33 cases, with differentiation of cases associated with multiple sclerosis and parainfectious events. Arch Neurol 1993; 50: 532-5. [ Links ]
5. Nakamura N, Nokura K. Neurologic complications associated with influenza vaccination: two adults cases. Intern Med 2003; 42: 191-4. [ Links ]
6. Schattner A. Consequence or coincidence? The occurrence, pathogenesis and significance of autoimmune manifestations after viral vaccines. Vaccine 2005; 23: 3876-86. [ Links ]
7. Berman M, Feldman S. Acute transverse myelitis: incidence and etiologic considerations. Neurology 1981; 31: 966-71. [ Links ]
8. Transverse Myelitis Consortium Working Group. Proposed diagnostic criteria and nosology of acute transverse myelitis. Neurology 2002; 59: 499-505. [ Links ]
9. Agmon-Levin N, Kivity S. Transverse myelitis and vaccines: a multi-analysis. Lupus 2009; 18: 1198-204. [ Links ]
10. Blank M, Barzilai O. Molecular mimicry and autoinmunity. Clin Rev Allergy Immunol 2007; 32: 111-8 [ Links ]
11. Pittock SJ, Lucchinetti CF. Inflammatory transverse myelitis: evolving concepts. Curr Opin Neurol 2006; 19: 362-8. [ Links ]
12. Safety of Influenza A (H1N1) 2009 Monovalent Vaccines- United States, October 1 November 24, 2009. Morbidity and Mortality Weekly Report (MMWR) 58(48); 1351-6. En: www.cdc.gov/mmwr/preview/mmwrhtml/mm5848a4.htm [ Links ]
13. Sejvar JJ, Kohl KS, Bilynsky R. Encephalitis, myelitis and acute disseminated encephalomyelitis (ADEM): Case definitions and guidelines for collection, analysis and presentation of immunization safety data. Vaccine 2007; 25: 5771-92. [ Links ]
14. Bakshi R, Kinkel PR. Magnetic resonance imaging findings in 22 cases of myelitis: comparison between patients with and without multiple sclerosis. Eur J Neurol 1998; 5: 35-48. [ Links ]
15. McDonald WI, Compston A, Edan G, et al. Recommended diagnostic criteria for multiple sclerosis: guidelines from the International Panel on the diagnosis of multiple sclerosis. Ann Neurol 2001; 50: 121-7. [ Links ]
16. Kalita J, Misra UK. Is methyl prednisolone useful in acute transverse myelitis? Spinal Cord 2001; 39: 471-6. [ Links ]
17. Adam I, Kaplin MD, Chitra Krishnan MHS, et al. Diagnosis and management of acute myelopathies. Neurologist 2005; 11: 1-18. [ Links ]
Recibido: 8-9-2010
Aceptado: 17-11-2010














