Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680
Medicina (B. Aires) vol.71 no.4 Ciudad Autónoma de Buenos Aires jul./ago. 2011
ARTÍCULO ORIGINAL
Comparación entre las ecuaciones CKD-EPI y MDRD para la estimación del filtrado glomerular en pacientes con enfermedad renal crónica
Guillermo J. Rosa-Diez, Federico Varela, Soledad Crucelegui, Salomón L. Algranati, Gustavo Greloni
Servicio de Nefrología Adultos, Hospital Italiano de Buenos Aires
Dirección postal: Dr. Federico Varela, Servicio de Nefrologia de Adultos, Hospital Italiano, Gascón 450, 1181 Buenos Aires, Argentina
Fax (54-11) 4959-0200 e-mail: federico.varela@hospitalitaliano.org.ar
Resumen
La ecuación MDRD para la estimación del índice de filtrado glomerular (IFG), es la estrategia más utilizada para evaluar pacientes con enfermedad renal crónica (ERC). Sin embargo, puede subestimar el IFG con el riesgo de asignar al paciente a estadios más avanzados de ERC. La nueva ecuación CKD-EPI, mejoraría la exactitud y precisión de las estimaciones. Sus autores sugieren que reemplace a la anterior. No habiendo comparaciones de estas ecuaciones aplicadas en un gran número de pacientes en nuestro país, nuestro objetivo fue realizarla en una amplia cohorte de pacientes. Se evaluó la concordancia de asignación en estadios de ERC entre ambas ecuaciones, tomando como referencia los datos surgidos de MDRD. Se calculó la media de las diferencias de los IFG obtenidos empleando ambas ecuaciones y se aplicó el análisis estadístico de Bland-Altman. Se estudió una cohorte de 9 319 pacientes con una media de creatinina sérica de 1.60 ± 1.03 mg/dl, 67% de sexo femenino y edad media 58 ± 20 años. En el grupo total, CKD-EPI presentó una media de IFG 0.61 ml/min/1.73 m2 mayor que MDRD (p: NS). En los estadios 2 y 3A las medias del IFG fueron respectivamente 6.95 ± 4.76 y 3.21 ± 3.31, y la concordancia de 81 y 74%. El porcentaje de pacientes con un IFG menor de 60 ml/min/1.73 m2, se redujo de 76.3% (MDRD) a 70.1% (CKD-EPI). Por lo tanto, la nueva ecuación CKD-EPI disminuye el número de pacientes con IFG debajo de 60 ml/min/1.73 m2 y asigna estadios de IFG más elevado a un número mayor de pacientes.
Palabras clave: Índice de filtrado glomerular; Clearance de creatinina; MDRD; CKD-EPI; Enfermedad renal crónica; Insuficiencia renal crónica
Abstract
Comparison between CKD-EPI and MDRD-equations to estimate glomerular filtration rate in chronic kidney disease patients. The MDRD equation to estimate glomerular filtration rate (GFR) is the most widely used strategy to assess chronic kidney disease. Nonetheless, for the individual patient the true GFR can be underestimated with the risk of diagnosing a more elevated CKD stage. This novel CKD-EPI equation would improve accuracy and precision of estimations, and several authors recommend this new equation replace the former. In our country there is only a limited registration of these comparisons performed on a large number of patients. Therefore, our aim was to develop a comparison in a wide cohort of patients. The concordance between both equations to assign the GFR stages was determined by using the MDRD formula as a reference. The mean difference of GFR obtained with both equations as well as the Bland-Altman analysis were calculated. A cohort of 9 319 individuals, of whom 67% were females, aged 58 ± 20 years, with serum creatinine values of 1.6 ± 1.03 mg/dl, was studied. In the whole group, CKD-EPI displayed an average GFR 0.61 ml/min/1.73 m2 larger than MDRD (p: NS). For CKD stages 2 and 3A the mean estimated GFR difference was 6.95 ± 4.76 and 3.21 ± 3.31, while the concordance was 81 and 74% respectively. The percentage of patients with GFR < 60 ml/min/1.73 m2, decreased from 76.3% with the former equation to 70.1% with the latter. The novel equation CKD-EPI reduces the number of patients with GFR values lower than 60 ml/min/1.73 m2 and consequently assigns a higher GFR stage to a considerable quantity of individuals.
Key words: Glomerular fíltrate rate; Creatinine clearance; MDRD; CKD-EPI; Chronic kidney disease; Chronic renal failure
En la Argentina la prevalencia de insuficiencia renal crónica permanente alcanza los 638 pacientes por millón de habitantes, mostrando ascenso en los últimos años1. Se estima que la Enfermedad Renal Crónica (ERC) afecta en el mundo al 9-15% de la población de la cual existen datos2-5, y se reconoce en la actualidad su asociación desde estadios iniciales, con un incremento en el riesgo cardiovascular y mortalidad prematura6, 7. Por ello, en el desarrollo de programas de prevención, detección precoz y tratamiento de enfermedades renales, es esencial el uso de herramientas simples y seguras para la evaluación de la función renal (FR).
Aunque su medición directa en la práctica clínica resulte cara y dificultosa, el índice de filtrado glomerular (IFG) es el mejor marcador de FR8. Las ecuaciones para su estimación a partir de marcadores endógenos de filtrado glomerular como la creatinina sérica, han extendido su uso clínico para el diagnóstico y estadificación de la ERC9 y han sido sugeridas por distintas sociedades científicas con el fin de mejorar la relación existente entre creatinina sérica y FR, y alertar a los médicos ante situaciones de afectación renal incipiente10-14. La Sociedad Argentina de Nefrología se ha expresado también en este sentido15.
La ecuación (MDRDe) surgida del estudio Modification of Diet in Renal Disease (MDRD)16, 17 que incorpora datos sobre edad, sexo, etnia y creatinina sérica, ha sido la más utilizada tanto en la práctica clínica como en estudios epidemiológicos2, 5, 10. Su desarrollo original se realizó con datos provenientes de pacientes con ERC y con determinaciones de creatinina realizadas con el método de Jaffé cinético sin estandarización, convirtiendo en problema las características de la población utilizada y la amplia variabilidad entre laboratorios al realizar esta estimación, y por lo tanto en el IFG estimado (IFGe)18-20. Así, la ecuación se modificó, adaptándose a estimaciones de creatinina estandarizada a un método de referencia internacional, como lo es el de Dilución Isotópica y Espectrometría de Masa (DI-EM)21, 22.
No obstante una generalización en el uso, existen dudas respecto de su validez, cuando es utilizada en poblaciones distintas a la que le dio origen, observándose una sistemática infraestimación del IFG, fundamentalmente para valores normales y altos de FR18, 19.
El grupo de trabajo Chronic Kidney Disease Epidemiology Collaboration (CKD-EPI) desarrolló recientemente una nueva ecuación para estimar el IFG23 con el fin de minimizar los errores de la anterior. Fue confeccionada a partir de una población de 8254 individuos, provenientes de diez estudios diferentes incluido el MDRD, de quienes se contaba con una medición directa del filtrado glomerular mediante aclaramiento de iotalamato. Esta nueva ecuación (CKD-EPIe) logró mejorar la precisión y exactitud frente a la medida directa de IFG, respecto de lo observado con MDRDe, en especial para valores de IFG superiores a 60 ml/min/1.73 m2. Por este motivo, sus autores sugieren que MDRDe, podría ser sustituida por CKD-EPIe en la práctica clínica.
Ambas ecuaciones han sido desarrolladas y evaluadas fuera de nuestro país. No existiendo evaluación de CKD-EPIe en nuestro medio, el objetivo de este estudio es comparar en una amplia cohorte propia de pacientes los valores de IFG e obtenidos mediante ambas ecuaciones, y analizar la distribución de los pacientes que cada una de éstas produce, en la clasificación por estadios de ERC.
Materiales y métodos
El Comité de Etica en Protocolos de Investigación de la institución dio su aprobación a este estudio.
A partir de junio de 2 008, el laboratorio central del Hospital Italiano de Buenos Aires cuenta con estimación de creatinina sérica con estandarización al método DI-EM. Todas las estimaciones de creatinina utilizadas para este estudio se realizaron mediante este método.
Se realizó una búsqueda de pacientes en el sistema informático del laboratorio central del hospital con los siguientes criterios de elegibilidad: edad mayor o igual a 18 años, de ambos sexos, en régimen ambulatorio, a quienes se solicitó una medida de creatinina sérica y una determinación de proteínas en orina. Sólo se incluyeron pacientes con ambas muestras remitidas al laboratorio el mismo día. La determinación de proteínas en orina se consideró positiva mediante cualquiera de los tres siguientes métodos: proteinuria de 24 horas mayor o igual a 150 mg en 24 horas (Rojo de pirogalol, reactivo Beckman, Instrumento LX20 Beckman), microalbuminuria de 24 horas mayor o igual a 30 mg en 24 horas (Nefelometría, Instrumento Beckman) u orina completa con 2 o más cruces en la tira reactiva (Tiras reactivas automatizadas Clinitek Atlas). El período de selección fue del 1 de julio de 2 008 hasta el 26 de abril de 2 010. De cada paciente se obtuvo un único par de determinaciones (último) y se realizó una estimación del IFG con cada una de las ecuaciones en estudio. Las mismas se exponen a continuación.
MDRDe
IFG = 175 × (creatinina)-1.154 × (edad)-0.203 × (0.742 para sexo femenino) × (1.212 para "etnia negra")
CKD-EPIe
Fórmula para "etnia negra"
Sexo femenino y creatininemia ≤ 0.7 mg/ml; IFG = 166 × (creatinina/ 0.7)-0.329 × (0.993)edad y creatininemia > 0.7 mg/ml; IFG = 166 × (creatinina/ 0.7)-1.209 × (0.993)edad
Masculino y creatininemia ≤ 0.9 mg/ml; IFG = 163 × (creatinina/0.9)-0.411 × (0.993)edad y creatininemia > 0.9 mg/ml; IFG = 163 × (creatinina/ 0.9)-1.209 × (0.993)edad
Fórmula para "etnia blanca"
Sexo femenino y creatininemia ≤ 0.7 IFG = 144 × (creatinina/0.7)-0.329 × (0.993)edad y creatininemia > 0.7 IFG = 144× (creatinina/ 0.7)-1.209 × (0.993)edad
Masculino y creatininemia ≤ 0.9 IFG = 141 × (creatinina/ 0.9)-0.411 × (0.993)edad y creatininemia > 0.9 IFG = 141 × (creatinina/0.9)-1.209 × (0.993)edad
Para el análisis definitivo sólo se utilizaron los datos de aquellos pacientes que cumplían con criterios de ERC sugeridos por la National Kidney Foundation (NKF) en sus guías de manejo clínico Kidney Disease Outcomes Quality Initiative (KDOQI)10.
Los resultados fueron expresados como media ± desvío estándar (DE), o frecuencia y porcentaje, según correspondiera. Las diferencias entre medias se analizaron mediante el test-t, considerándose significativos los valores de p < 0.05. Las comparaciones para asociaciones entre variables fueron realizadas según coeficiente de Spearman.
Se dividió a la población en estudio en los estadios de ERC sugeridos por la NKF mediante el IFGe con MDRDe, de acuerdo al sexo y al grupo etario (menores: menor o igual a 65 años y mayores: mayor a 65 años). Se evaluó la concordancia de asignación a estadios de ERC (individuos que eran asignados al mismo estadio de ERC con ambas ecuaciones, tomando como referencia el estadio asignado por MDRDe). Sobre la totalidad de la población y en cada uno de los grupos mencionados se calculó la media de las diferencias de los IFGe obtenidos por ambas ecuaciones y el análisis estadístico de Bland-Altman expresado como la relación porcentual de dicha diferencia con respecto al IFGe obtenido por MDRDe.
Para el análisis estadístico se utilizó el programa STATA (versión 8.0).
Resultados
Se obtuvo una cohorte de 14 603 pacientes. De éstos, 9 319 cumplían criterios de ERC (7 110 con IFGe menor a 60 ml/min/1.73 m2, 2 209 con IFGe mayor o igual a 60 ml/min/1.73 m2 más proteinuria), considerando este como número total de pacientes del estudio.
La Tabla 1 reúne las características basales de la población estudiada. En el grupo total la media del IFGe fue mayor por CKD-EPIe que por MDRDe, con una diferencia de 0.61 ml/min/1.73 m2 (Fig. 1). Esta diferencia no fue estadísticamente significativa. En la Fig. 2 se representa la diferencia entre cada pareja de valores de IFGe obtenidos por MDRD y CKD-EPI frente a la media de los mismos. Puede verse que por encima de valores de 100 ml/min de IFGe, la diferencia de los resultados obtenidos por ambas ecuaciones queda por fuera de los límites de concordancia (límites de confianza del 95%).
TABLA 1.- Características demográficas, creatininemia e IFG (Indice de filtrado glomerular) obtenido por ambas fórmulas (MDRD y CDK-EPI) en la población en estudio

(*) Número y proporción de dicha población en los distintos estadios de ERC (Enfermedad Renal Crónica) según el IFG determinado por la fórmula MDRD.
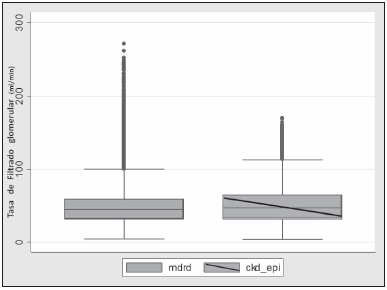
Fig. 1.- Media y desvío standard del IFGe obtenido por MDRD y CKD-EPI de la población en estudio.
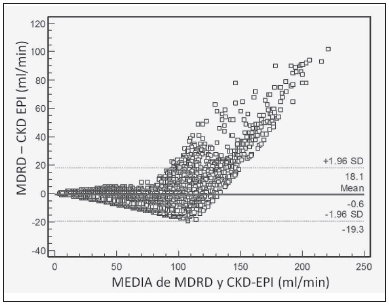
Fig. 2.- Gráfico de Bland-Altman para MDRD y CKD-EPI. Gráfico de Bland-Altman donde se representa la diferencia entre cada pareja de valores de IFGe obtenidos por MDRD y CKD-EPI frente a la media de los mismos. Puede verse que a partir de valores por encima de 100 ml/min de IFGe, la diferencia de los resutados obtenidos por ambas ecuaciones quedan por fuera de los límites de concordancia (límites de confianza del 95%).
Al dividir la población según estadios de ERC, los estadios 1 y 5 mostraron valores más elevados mediante MDRDe, encontrándose en el primero la diferencia más abultada. En los estadios restantes, CKD-EPIe mostró valores más elevados, con un pronunciamiento mayor en el estadio 2 (Tabla 2). El análisis de concordancia del grupo total mostró una concordancia global (media de las concordancias de los estadios de ERC) del 86%. El estadio 3A mostró el valor más reducido que accedió a 74%, moviendo hacia estadios de mayor IFGe a la mayoría de sus pacientes desplazados. La CKD-EPIe mostró también un porcentaje menor de pacientes con un IFGe menor a 60 ml/min/1.73 m2 respecto de lo observado con MDRDe (70.1% versus 76.3% respectivamente).
TABLA 2.- Valores de creatinina sérica, IFG, concordancia y análisis de Bland- Altman para las ecuaciones MDRD y CKD-EPI en la población general, con respecto al estadio de ERC
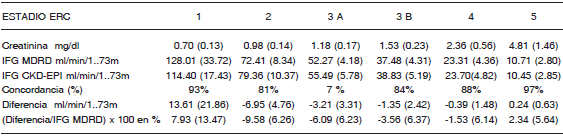
ERC: Enfermedad Renal Crónica. IFG: Indice de filtrado glomerular. Todos los valores se expresan en media y desvío estándar (entre paréntesis).
Siendo Diferencia = valor absoluto de IFG CKDE-EPI menos IFG CKD-EPI.
Al incluir la variable sexo, encontramos diferencias significativas respecto de la media del IFGe, en la comparación entre ambas ecuaciones tanto en el grupo mujeres como en el grupo hombres. En las primeras CKD-EPIe fue superior con una diferencia de 2.68 ml/min/1.73 m2 (p < 0.05). En los segundos, MDRDe mostró valores más elevados con una diferencia de 3.56 ml/min/1.73 m2 (p < 0.05). La concordancia fue menor en el grupo mujeres oscilando entre el 71% para el estadio 3A y el 100% para el estadio 1, mientras que en los hombres fue de 80% en el estadio 2 y de 99% en el 5 (Tabla 3).
TABLA 3.- Promedio de la diferencia y porcentaje de concordancia entre ambas fórmulas para los distintos subgrupos

Promedio de la diferencia (MDRD - CKD/EPI) en ml/min (entre par éntesis desvío estándar) y porcentaje de concordancia entre ambas fórmulas
para los subgrupos mujeres, hombres, ancianos y jóvenes a nivel general y por estadio.
Observamos similares hallazgos significativos en la media del IFGe con la variable edad. En el grupo mayores, MDRDe mostró valores más elevados con una diferencia de 1.28 ml/min/1.73 m2 (p < 0.05) y la concordancia fue superior, observándose un valor de 100% en el estadio 5 y del 65% en el estadio 1. En el grupo menores, fue superior el valor obtenido mediante CKD-EPIe (p < 0.05) con una concordancia inferior que alcanzó un 100% en el estadio 1 y un 61% en el estadio 3A (Tabla 3). Se destaca en nuestra observación que en el grupo menores, al ser evaluado mediante CKD-EPIe, ningún paciente fue reasignado a un estadio de mayor gravedad de ERC, realizándose todos los desplazamientos hacia estadios de IFGe más elevados exclusivamente, jerarquizando así la variable edad en la nueva ecuación.
Dado que en los grupos antes mencionados las diferencias en la media del IFGe entre ambas ecuaciones fueron significativas y no lo fue en el grupo total, decidimos ampliar la evaluación generando subgrupos que incluyan ambas variables (sexo y edad) a la vez. La Tabla 4 muestra el número total de pacientes en los distintos estadios de ERC, en cada uno de los 4 subgrupos, la concordancia obtenida al ser evaluados mediante CKD-EPIe y el número neto y el sentido de los pacientes que sufrieron desplazamientos en la clasificación de ERC. Destacamos que la mayor discrepancia entre ambas ecuaciones se observó en el estadio 3A, alcanzando el 41% en las mujeres menores. De modo inverso, las concordancias más elevadas se ubicaron en los estadios 1 y 5. En los hombres mayores, si bien un número importante de pacientes presentó un desplazamiento desde el estadio 1 al 2, pocos fueron los que se ubicaron con filtrados menores a 60 ml/min/1.73 m2.
TABLA 4.- Análisis de concordancia de las ecuaciones MDRD y CKD-EPI para hombres y mujeres en dos grupos etarios
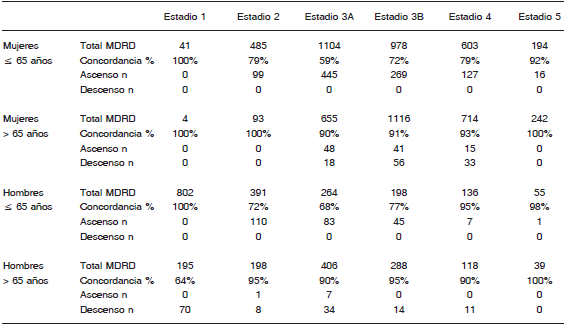
Todos los datos se expresan en números absolutos y en porcentaje.
En la Tabla 5 realizamos un análisis de las diferencias en el IFGe entre ambas ecuaciones para cada uno de los subgrupos, expresadas como valores absolutos (ml/min/1.73 m2) y en el análisis de Bland-Altman como porcentaje. Observamos así que el estadio 1 experimentó las diferencias más pronunciadas tanto para una u otra ecuación, dependiendo del subgrupo evaluado, y que las mujeres menores fue el subgrupo de mayor afectación en su IFGe con la nueva ecuación.
TABLA 5.- Valores de diferencia (valor absoluto de IFG MDRD menos IFG CKD-EPI) y análisis de Bland- Altman para las ecuaciones MDRD y CKD-EPI en los distintos grupos con respecto a cada estadio de ERC
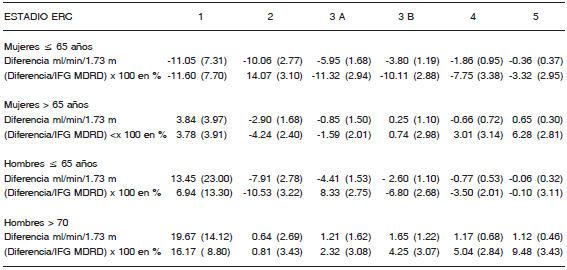
Todos los valores se expresan en media y desvío estándar (entre paréntesis).
Discusión
La actual clasificación y definición de ERC, publicada en el año 2 002 por la NKF10, generó un marco conceptual de criterios unificados que facilitó la evaluación de pacientes individuales y permitió comparar ensayos clínicos y estudios poblacionales. En su texto, aunque obvia la necesidad de fijar la etiología de la ERC, determina un espacio de tiempo mínimo para su diagnóstico, propone evaluar la presencia de proteinuria como marcador de daño orgánico y sugiere cuantificar la FR con la estimación del IFG mediante el uso de ecuaciones a partir del nivel de la creatinina sérica. En relación a ello, distingue distintos grados de severidad en torno a un esquema de daño renal progresivo.
La amplia aceptación de este esquema sucedió entre confirmaciones y críticas. Tres conferencias (Controversies Conference) auspiciadas por Kidney Disease Improving Global Outcomes (KDIGO) y sus respectivos documentos24-26 discutieron, enriquecieron y sostuvieron la clasificación, sin modificarla hasta la actualidad, refiriendo como principal fortaleza la aplicabilidad que su simplicidad ofrece. Un cuarto documento27 aprobado por ambas entidades, KDOQI y KDIGO, sugiere que el debate no debería focalizarse exclusivamente en la FR y en el daño estructural, sino también en el pronóstico renal y cardiovascular que la ERC asigna.
Quienes observan limitaciones en este esquema centraron sus comentarios en la posibilidad de sobreestimar la prevalencia de ERC utilizando la metodología propuesta y el hecho de utilizar ecuaciones de estimación en ancianos y en poblaciones de distintas etnias27.
Respecto de este último punto, las guías actuales sugieren dos metodologías para la evaluación: MDRDe y clearance de creatinina estimado por la ecuación de Cockcroft y Gault10. La primera ha sido la más utilizada. Las ya referidas críticas realizadas a esta ecuación derivan de la población utilizada en su desarrollo: individuos mayoritariamente portadores de ERC (filtrado glomerular medio de 40 ml/min/1.73 m2) y escasa participación de pacientes diabéticos (6%). Se menciona también su imprecisión e infraestimación sistemática19, sobre todo para valores normales o altos de FR. Por último, la prácticamente nula participación de individuos de distintas etnias obligó a realizar correcciones sobre la ecuación, para su utilización en distintos grupos poblacionales28, 29.
La CKD-EPIe para estimar el IFG incluye el logaritmo de creatinina (con dos versiones diferentes dependiendo del valor de creatinina sérica), el sexo, la etnia y la edad en escala natural. Se generó a partir de una población de 8 254 pacientes, de diez estudios diferentes de los que se contaba con una medición directa del IFG. Se realizó posteriormente una validación externa en 3 896 pacientes, surgidos a partir de 16 estudios diferentes. La población que dio origen a la nueva ecuación presenta una media de IFG de 68 ± 40 ml/min/1.73 m2, media de creatinina sérica de 1.65 mg/dl, edad media de 47 ± 15 años, con una escasa representación de pacientes mayores de 71 años (3%). Presenta también un 29% de pacientes diabéticos y un 13% de donantes de riñón. La nueva ecuación incluye las mismas variables que MDRDe y en su diseño se utilizaron estimaciones de creatinina sérica con estandarización al método DI-EM. De su estructura destacamos tres aspectos: en primer lugar, consta de versiones diferentes según etnia, género y creatinina sérica, con cortes diferentes en el hombre y la mujer (0.9 y 0.7 mg/dl respectivamente), lo que podría distinguir población sana de pacientes con ERC. En segundo lugar, el factor numérico que encabeza la ecuación es más bajo que en la versión anterior, con valores diferentes en el hombre y la mujer (141 y 144 respectivamente). En tercer término, la nueva ecuación utiliza la edad como exponente de una constante (0.993edad), lo que, a edades avanzadas, deriva en valores más bajos de IFGe con esta ecuación23.
Al comparar ambas ecuaciones con el método de referencia, CKD-EPIe resultó similar a MDRDe para filtrados menores a 60 ml/min/1.73 m2 en cuanto a su exactitud, y aún más en el subgrupo con filtrado mayor a 60 ml/min/1.73 m2. Presentó también menor desviación o sesgo (mediana de la diferencia entre filtrado medido y estimado de 2.5 frente a 5.5 ml/min/1.73 m2), menor imprecisión (rango intercuartílico de las diferencias 16.6 ante 18.3 ml/min/1.73 m2) y mayor exactitud (porcentaje de estimaciones del filtrado glomerular dentro del 30% del valor medido de 84.1 frente a 80.6%)23.
Nuestro estudio compara ambas ecuaciones en una amplia cohorte de pacientes con ERC y su consecuente reagrupación en la clasificación de ERC.
De lo observado se desprende que la nueva ecuación genera valores de IFGe más elevados que los obtenidos por MDRDe, aunque esta diferencia no fue estadísticamente significativa en el grupo total. Permitió una reclasificación hacia estadios de mayor IFGe en 1 314 pacientes (14.1% de la población estudiada). Los estadios de ERC afectados principalmente fueron el estadio 2 con un 17.9% de pacientes que se reclasificaron a estadio 1, el 3A con un 24% que se reclasificó a 2 y el 3B con un 13.7% que reclasificó en 3A. Similares hallazgos fueron observados en otros estudios comparativos30-33. Decimos también que tales modificaciones lograron disminuir en un 6.2% al grupo de pacientes que se encontraba con un IFGe menor a 60 ml/min/1.73 m2, para ubicarlos en los estadios con mayor IFGe.
En sentido inverso, en el estadio 1, MDRDe mostró valores de filtrado glomerular más elevados que la nueva ecuación. Este hallazgo podría vincularse con el hecho que MDRDe resulte en valores desproporcionadamente altos de IFGe en pacientes de edad avanzada, con creatininas bajas y pérdida de masa muscular, y no vincularse a un filtrado glomerular verdaderamente elevado. Esto se refleja en una baja concordancia (65%) para este estadio en el grupo mayores, dado que la nueva ecuación reagrupó en el estadio 2 un significativo número de pacientes.
El hecho de que el estadio 3A, tanto en el grupo total como en la mayoría de los grupos y subgrupos analizados, presente menor concordancia que el resto de los estadios, a expensas de reagrupar pacientes en el estadio 2, refleja la intención de esta nueva ecuación de no rotular como portadores de ERC a pacientes sin una verdadera afectación renal.
Encontramos importantes diferencias entre ambas ecuaciones según género y edad. En las mujeres y en los menores, CKD-EPIe mostró valores más elevados de IFGe que resultaron ser estadísticamente significativos. En sentido inverso, en los hombres y en los mayores, MDRDe mostró valores más elevados, igualmente significativos. De los 5 251 pacientes analizados en el grupo menores, ninguno se desplazó hacia estadios de menor IFGe, con una concordancia promedio de todos los estadios del grupo de 81% y una concordancia del estadio 3A de sólo 61%.
Nuestro estudio coincide con la publicación original en la reasignación de pacientes a estadios de mayor IFGe, fundamentalmente a partir de pacientes en estadio 3A. Estos 2 429 pacientes representan un 26% del total de la población estudiada y que probablemente no debieran ser considerados, al menos en cuanto a su IFG, como portadores de ERC. Lamentablemente carecemos hasta el momento de un gran estudio epidemiológico de carácter nacional de enfermedad renal que nos permita establecer el porcentaje de esta patología en nuestro medio. Esta justa apreciación tiene a su vez importancia en cuanto a políticas sanitarias, ya que la asignación de recursos en patologías crónicas resulta uno de los mayores desafíos para las entidades responsables en salud, y el empleo de esta nueva fórmula podría disminuir una injustificada carga al sistema de salud de pacientes mal rotulados como "enfermos renales crónicos".
Finalmente, debe señalarse que el "reacomodamiento" de esos pacientes en un estadio de menor compromiso renal no es parte de un desplazamiento automático para aquellos ubicados en los niveles más próximos al límite superior de FG, sino que observamos que se desarrolla en forma distinta según las diferentes edades y según se trate de hombres y mujeres.
Destacamos que este estudio constituye una de las primeras comparaciones entre ambas ecuaciones, con un gran número de pacientes en nuestro medio. Dentro de las limitaciones del mismo, el análisis se realizó exclusivamente en una población con ERC y en un único centro de nuestro país, lo que impide evaluar la utilidad de la ecuación en pacientes sanos (si bien no estaba incluido en los objetivos del estudio) y su representatividad a nivel nacional. Con la intención de obtener una muestra aleatoria de la Argentina, y considerando que la nueva ecuación se comporta de modo dispar con respecto a MDRDe de acuerdo a grupo etario y género, sugerimos que la metodología usada en este trabajo sea replicada por otros grupos, incluyendo la comparación de la población en estudio con la que se usó en estudios previos, lo que permitirá confirmar el valor y el lugar adecuado para esta nueva ecuación en nuestro país.
Conflictos de interés: Los autores no presentan ningún tipo de conflictos de interés.
1. Instituto Nacional Centro Único Coordinador de Ablación e Implante (INCUCAI). Sistema Nacional de Información SINTRA. https://irct.incucai.gov.ar/public/Modulo1.do; consultado el 10/4/2010. [ Links ]
2. Coresh J, Selvin E, Stevens LA, et al. Prevalence of chronic kidney disease in the United States. JAMA 2007; 298: 2038-47. [ Links ]
3. Hallan SI, Coresh J, Astor BC, et al. International comparison of the relationship of chronic kidney disease prevalence and ESRD risk. J Am Soc Nephrol 2006; 17: 2275-84. [ Links ]
4. Chadban SJ, Briganti EM, Kerr PG, et al. Prevalence of kidney damage in Australian adults: the AusDiab Kidney Study. J Am Soc Nephrol 2003; 14: S131-138. [ Links ]
5. Otero A, de Francisco A, Gayoso P, García F. EPIRCE Study Group. Prevalence of chronic renal disease in Spain: results of the EPIRCE study. Nefrología 2010; 30: 78-86. [ Links ]
6. Go AS, Chertow GM, Fan D, McCulloch CE, Hsu CY. Chronic kidney disease and the risks of death, cardiovascular events, and hospitalization. N Engl J Med 2004; 351: 1296-1305. [ Links ]
7. Keith DS, Nichols GA, Gullion CM, Brown JB, Smith DH. Longitudinal follow-up and outcomes among a population with chronic kidney disease in a large managed care organization. Arch Inter Med 2004; 164: 659-63. [ Links ]
8. Vassalotti JA, Stevens LA, Levey AS. Testing for chronic kidney disease: a position statement from the National Kidney Foundation. Am J Kidney Dis 2007; 50: 169-80. [ Links ]
9. Stevens LA, Coresh J, Schmid CH, et al. Estimating GFR using serum cystatin C alone and in combination with serum creatinine: a pooled analysis of 3,418 individuals with CKD. Am J Kidney Dis 2008; 51: 395-406. [ Links ]
10. National Kidney Fundation. K/DOQI Clinical Practice Guidelines for Chronic Kidney Disease: evaluation, classification, and stratification. Am J Kidney Dis 2002; 39: S1-S266. [ Links ]
11. Levey AS, Eckardt KU, Tsukamoto Y, et al. Definition and classification of chronic kidney disease: a position statement from kidney disease: Improving Global Outcomes (K-DIGO). Kidney Int 2005; 67: 2089-100. [ Links ]
12. Mathew TH, Australasian Creatinine Consensus Working Group. Chronic kidney disease and automatic reporting of estimated glomerular filtration rate: a position statement. Med J Aust 2005; 183: 138-41. [ Links ]
13. Crowe E, Halpin D, Stevens P, Guideline Development Group. Early indentification and management of chronic kidney disease: summary of NICE guidance. BMJ 2008; 337: a1530. [ Links ]
14. García S, Montañes R, Bover J, et al. Documento de consenso: Recomendaciones sobre la utilización de ecuaciones para la estimación del filtrado glomerular en adultos. Nefrología 2006; 26: 658-65. [ Links ]
15. Alles A, Fraga A, García R, et al. Detección de Enfermedad Renal Crónica. Documento Multidisciplinario. Revista de Nefrología, Diálisis y Trasplante 2010; 30: 110-7. [ Links ]
16. Levey AS, Bosch JP, Lewis JB, Greene T, Rogers N, Roth D. A more accurate method to estimate glomerular filtrate rate from serum creatinine: a new prediction equation. Modification of Diet in Renal Disease Study Group. Ann Intern Med 1999; 130: 461-70. [ Links ]
17. Levey AS, Greene T, Kusek JW, Beck GJ. A simplified equation to predict glomerular filtration rate from serum creatinine. J Am Soc Nephrol 2000; 11: 155A. [ Links ]
18. Rule AD, Larson TS, Bergstralh EJ, Slezak JM, Jacobsen SJ, Cosio FG. Using serum creatinine to estimate glomerular filtration rate: accuracy in good health and in chronic kidney disease. Ann Intern Med 2004; 141: 929-37. [ Links ]
19. Stevens LA, Coresh J, Feldman HI, et al. Evaluation of the Modification of Diet in Renal Disease Study equation in a large diverse population. J Am Soc Nephrol 2007; 18: 2749-57. [ Links ]
20. Stevens LA, Manzi J, Levey AS, et al. Impact of creatinine calibration on performance of GFR estimating equations in a pooled individual patient database. Am J Kidney Dis 2007; 50: 21-35. [ Links ]
21. Levey AS, Coresh J, Greene T, et al. Expressing the MDRD Study equation for estimating GFR with IDMS traceable (gold standard) serum creatinine values. J Am Soc Nephrol 2005; 16: 69A. [ Links ]
22. Levey AS, Coresh J, Greene T, et al; Chronic Kidney Disease Epidemiology Collaboration. Expressing the modification of diet in renal disease study equation for estimating glomerular filtration rate with standardized serum creatinine values. Clin Chem 2007; 53: 766-72. [ Links ]
23. Levey AS, Stevens LA, Schmid CH, et al. CKD-EPI (Chronic Kidney Disease Epidemiology Collaboration) A new equation to estimate glomerular filtration rate. Ann Intern Med 2009; 150: 604-12. [ Links ]
24. Levey AS, Eckardt KU, Tsukamoto Y, et al. Definition and classification of chronic kidney disease: A position statement from Kidney Disease: Improving Global Outcomes (KDIGO). Kidney Int 2005; 67: 2089-100. [ Links ]
25. Levey AS, Atkins R, Coresh J, et al. Chronic kidney disease as a global public health problem: Approaches and initiatives - a position statement from Kidney Disease Improving Global Outcomes. Kidney Int 2007; 72: 247-59. [ Links ]
26. KDIGO Controversies Conference: Definition, Classification and Prognosis in CKD, London, October 2009. En: http://www.kdigo.org/meetings_events/CKD_Controversies_Conference.php; consultado el 15/12/2010. [ Links ]
27. Eckardt KU, Berns JS, Rocco MV, Kasiske BL. Definition and classification of CKD: the debate should be about patient prognosis- a position statement from KDOQI and KDIGO. Am J Kidney Dis 2009; 53: 915-20. [ Links ]
28. Ma YC, Zuo L, Chen JH, et al. Modified glomerular filtration rate estimating equations for Chinese patients with chronic kidney disease. J Am Soc Nephrol 2006; 17: 2937-44. [ Links ]
29. Imai E, Horio M, Nitta K, et al. Estimation of glomerular filtration rate by MDRD Study equation modified for Japanese patients with chronic kidney disease. Clin Exp Nephrol 2007; 11: 41-50. [ Links ]
30. Delanaye P, Cavalier E, Mariat C, Maillard N, Krzesinski JM. MDRD or CKD-EPI study equations for estimating prevalence of stage 3 CKD in epidemiological studies: which difference? Is this difference relevant? BMC Nephrol 2010; 1: 11-8. [ Links ]
31. Montañéz Bermúdez R, Bover Sanjuán J, Oliver Samper A, Ballarín Castán JA, Gràcia García S. Assessment of the new CKD-EPI equation to estimate the glomerular filtration rate. Nefrologia 2010; 30: 185-94. [ Links ]
32. Matsushita K, Selvin E, Bash LD, Astor BC, Coresh J. Risk implications of the new CKD Epidemiology Collaboration (CKD-EPI) equation compared with the MDRD Study equation for estimated GFR: The Atherosclerosis Risk in Communities (ARIC) Study. Am J Kidney Dis 2010; 55: 648-59. [ Links ]
33. White SL, Polkinghorne KR, Atkins RC, Chadban SJ. Comparison of the prevalence and mortality risk of CKD in Australia using the CKD Epidemiology Collaboration (CKD-EPI) and Modification of Diet in Renal Disease (MDRD) Study GFR estimating equations: the AusDiab (Australian Diabetes, Obesity and Lifestyle) Study. Am J Kidney Dis 2010; 55: 660-70. [ Links ]
Recibido: 17-12-2010
Aceptado: 20-6-2011














