Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Medicina (Buenos Aires)
versión impresa ISSN 0025-7680
Medicina (B. Aires) vol.72 no.2 Ciudad Autónoma de Buenos Aires mar./abr. 2012
CASUÍSTICA
Neuromielitis óptica con alta expresión de acuaporina-4 y anticuerpos anti-acuaporina-4 positivos en suero
Alejandra Báez1, Mariana Báez1, Valeria Kuchkaryan1, Adrián Schoijedman2, Carlos Lozano3, Ignacio Casas Parera1
1División Neurología, Instituto de Oncología Ángel H. Roffo, Facultad de Medicina, Universidad de Buenos Aires,
2Laboratorios Zavala, Buenos Aires,
3Hospital Público Dr. Guillermo Rawson, San Juan
Dirección postal: Dra. Alejandra Báez, División Neurología, Instituto de Oncología Ángel H. Roffo, Av. San Martín 5481, 1417 Buenos Aires, Argentina
Fax (11-54) 4504-2835 e-mail: neurooncoroffo@yahoo.com
Resumen
La presencia de anticuerpos IgG en suero, con blanco en los canales de acuaporina-4, es específica de la neuromielitis óptica (NMO). El 60% de los pacientes con NMO presentan lesiones cerebrales en la resonancia magnética (RM); en un 8% (mayoría niños) estas lesiones se consideraron "atípicas". Presentamos dos pacientes con NMO y lesiones en el SNC de alta expresión de acuaporina-4. Caso 1: varón de 50 años, que comenzó con pérdida de visión en ojo derecho (OD). Recibió tratamiento empírico con metilprednisolona 1 g/d x 3 días. Al mes presentó dolor generalizado y hemiparesia derecha; nuevamente recibió metilprednisolona 1 g/d x 5 días e IgG IV 400 mg/kg/d × 5 días. Recuperó la deambulación persistiendo el dolor y fenómenos paroxísticos en los 4 miembros. Potenciales evocados visuales: P100, ojo izquierdo (OI) 123 mseg. OD sin respuesta. La RM de cerebro (FLAIR) mostró hiperintensidad en nervio óptico derecho, hipotálamo y comisura blanca anterior. RM cervical: lesión medular extensa (5 cuerpos vertebrales). Caso 2: mujer de 53 años, con disminución de la agudeza visual en ambos ojos y parestesias en miembros inferiores que remitieron espontáneamente. Evolucionó al mes con cuadriparesia e incontinencia esfinteriana. Recibió metilprednisolona 1 g/d x 5 días, sin mejoría. Potenciales evocados visuales: P100 OI 124 mseg. OD 128 mseg. RM cerebro: (FLAIR) hiperintensidad hipotalámica y periacueductal. RM cervical: lesión medular extensa (7 cuerpos vertebrales). Anticuerpos anti-acuaporina-4 positivos en ambos pacientes (inmunofluorescencia indirecta). Las lesiones consideradas "atípicas", como aquí, en sitios con alta densidad de proteínas canales de agua AQP4 deberán considerarse para el diagnóstico diferencial.
Palabras clave: Neuromielitis óptica; Proteínas canales de agua; Anticuerpos anti-acuaporina-4; Síndrome de Devic
Abstract
Neuromyelitis optica with high aquaporin-4 expression and positive serum aquaporin-4 autoantibodies. Disease-specific aquaporin-4 antibodies (NMO-IgG) are the main effector of lesions in neuromyelitis optica (NMO) patients. Brain MRI lesions are detected in 60% of them, with 8% (almost infants) at sites of high aquaporin-4 expression. Patient 1: A fifty-year-old male with loss of vision in the right eye. Empiric treatment with metilprednisolone 1g/d for 3 days was indicated. After 30 days he complained of generalized pain, and a right hemiparesis was evident. The patient received bolus of metilprednisolone 1g/d for 5 days plus IgG 400 mg/kg/d IV for 5 days. He recovered ambulation but persisted with pain and paroxysmal phenomena (Lhermitte). Visual Evoked Potentials (VEP): P100 left eye 123 ms, right eye without response. Brain MRI (FLAIR) showed hyperintensity in the right optic nerve, hypothalamus and anterior white commissure. Cervical MRI showed extensive spinal cord lesion to an extension of 5 vertebral bodies. Patient 2: A fifty-three-year-old female who referred decreased visual acuity in both eyes and paresthesia in lower limbs which subsided spontaneously. One month later the patient evolved with cuadriparesis and sphincter incontinence. No improvement was observed with bolus of metilprednisolone 1g/d for 5 day. VEP: P100 left eye 124 ms, right eye 128 ms. Brain MRI (FLAIR) disclosed hypothalamic and periaqueductal hyperintensity. Cervical MRI showed extensive spinal cord lesion to an extension of 7 vertebral bodies. NMO-IgG antibodies were positive in both patients (indirect immunofluorescence assay). NMO brain lesions at sites of high aquaporin-4 expression, once considered "atypical"for their topography and infrequency in adults, should be borne in mind when considering differential diagnosis.
Key words: Neuromyelitis optica; Water channels proteins; Anti-aquaporin-4 antibody; Devic´s syndrome
La neuromielitis óptica (NMO) es una enfermedad idiopática autoinmune, desmielinizante e inflamatoria del sistema nervioso central (SNC) que afecta el/los nervio/s óptico/s y la médula espinal en forma simultánea o secuencial1. Aproximadamente el 50% de los pacientes con NMO presentan anticuerpos anti-acuaporina-4 (NMO-IgG) y en el 60% se observan lesiones en SNC, 8% (mayoría en niños) en sitios con alta expresión de proteínas canales de agua acuaporina-4 (AQP4)2, 3. Estos anticuerpos de inmunoglobulina-G en suero sirven como marcadores específicos de la enfermedad1-4.
Se presentan dos casos de pacientes con NMO y lesiones en SNC en sitios de alta expresión de proteínas canales de agua AQP4 y anticuerpos NMO-IgG positivos.
Casos clínicos
Paciente 1: varón de 50 años de edad, con antecedentes de hipotiroidismo subclínico, gastritis y dislipidosis, que comenzó en octubre 2007 con dolor y disminución de la visión de instalación brusca en ojo derecho (OD) y que en una semana evolucionó a la amaurosis. Recibió tratamiento empírico con pulsos de metilprednisolona 1 g/día/IV por 3 días consecutivos sin recuperación de la agudeza visual. Al mes vuelve a consultar por presentar pérdida de visión en ojo izquierdo (OI), parestesias dolorosas en hemicuerpo izquierdo y hemiparesia braquiocrural derecha; nuevamente internado, recibió metilprednisolona 1 g/día/IV por 5 días consecutivos, seguido de inmunoglobulina-G 400 mg/kg/IV día por 5 días consecutivos. Al día 14 el paciente había recuperado la deambulación y parcialmente la visión del OI, persistiendo con dolor y fenómenos paroxísticos homologables a "L´hermitte espontáneo"en hemicuerpo izquierdo.
La resonancia magnética (RM) de columna cervical mostró una imagen en la médula, hipointensa en T1 e hiperintensa en T2 con extensión de casi 5 cuerpos vertebrales; tras la administración de gadolinio captó tenuemente el contraste. La RM de cerebro mostró hipointensidad en T1 e hiperintensidad en T2 y FLAIR en nervio óptico derecho, hipotálamo y comisura blanca anterior (Fig.1). Los potenciales evocados visuales (PEV) mostraron una P100 en OI de 123 milisegundos (mseg) y en OD no se obtuvo respuesta (valor normal P100: < 115 mseg).
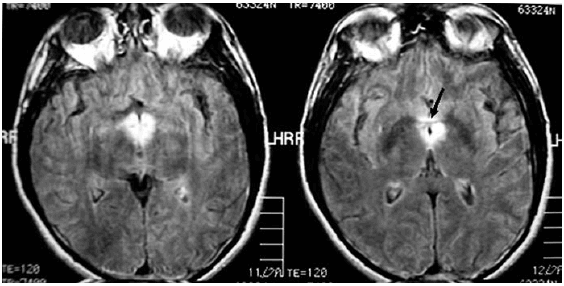
Fig. 1.- RM de cerebro (axial FLAIR). Hiperintensidades en hipotálamo y comisura blanca anterior (flecha).
Se realizó una punción lumbar obteniéndose líquido cefalorraquídeo (LCR) con presión de apertura normal, cristal de roca; el análisis mostró 20 linfocitos (valor normal: hasta 5 células), glucosa 43 mg/dl (glucemia 72 mg/dl), proteínas 0.96 mg/dl (valor normal: hasta 0.40 mg/dl), IgG 24 mg/dl (valor normal: 0.1-5.7 mg/dl) y ausencia de bandas oligoclonales (BOC) con técnica de isoelectroenfoque.
Realizó tratamiento con meprednisona vía oral 40 mg/día durante 4 meses y continuó con azatioprina 150 mg/día y amitriptilina 150 mg/día.
Actualmente el paciente persiste con defecto campimétrico temporal en OI y dolor fulgurante en hemicuerpo izquierdo, de inicio paroxístico y actualmente continuo.
Paciente 2: mujer de 53 años de edad, con antecedentes de hipotiroidismo, que comenzó con disminución súbita de la agudeza visual en ambos ojos y parestesias dolorosas en ambos miembros inferiores, síntomas que remitieron espontáneamente en 4 días. La paciente permaneció asintomática durante 30 días para evolucionar luego con debilidad progresiva de miembros inferiores hasta instalarse una cuadriparesia 2/5 e incontinencia urinaria y fecal. La RM de columna cervical mostró una lesión medular hipointensa en T1 e hiperintensa en T2 y FLAIR con una extensión aproximada de 7 cuerpos vertebrales, que no se modificó luego de la administración del contraste paramagnético. La RM de cerebro en secuencia FLAIR mostró hiperintensidades en regiones hipotalámica, periacueductal y piso del IV ventrículo (Fig. 2 A-B). Los PEV mostraron la P100 en OI de 124 mseg y en OD de 128 mseg.

Fig. 2 A-B.- RM de cerebro (axial FLAIR). A. Hiperintensidades en hipotálamo y periacueductal/ IV ventrículo (B) (flechas).
Recibió tratamiento con pulsos de metilprednisolona 1g/día/IV por 5 días consecutivos. No presentó mejoría neurológica luego del tratamiento y comenzó con fenómenos paroxísticos dolorosos. Continuó tratamiento con meprednisona 60 mg/día y azatioprina 150 mg/día; los espasmos dolorosos mejoraron en cuanto a intensidad y frecuencia, no así el déficit neurológico. La paciente evolucionó con cuadriplejía y espasmos tónicos dolorosos en los cuatro miembros; falleció a los 32 meses del diagnóstico de NMO.
Ambos pacientes presentaron títulos positivos en suero para anticuerpos NMO-IgG (técnica de inmunofluorescencia indirecta en cerebelo de ratón y mono, título de corte 1/500).
Discusión
La primera descripción que asoció la inflamación medular y el compromiso de los nervios ópticos con pérdida de la visión fue realizada por Clifford Allbutt en 18705. Posteriormente, en 1894 Eugène Devic y Fernand Gault describieron 17 casos con pérdida de la visión uni o bilateral y posterior desarrollo de compromiso motor, alteración de la sensibilidad e incontinencia/retención urinaria; desde entonces la afección del nervio óptico y médula espinal se conoce como síndrome de Devic6.
Las características que distinguen a la NMO de la esclerosis múltiple (EM) incluyen neuritis óptica uni o bilateral relativamente más grave, mielitis, pleocitosis en el LCR en su mayoría de polimorfonucleares durante los ataques agudos en aproximadamente el 25% de los casos de NMO, y una baja frecuencia de detección de bandas oligoclonales (20-30%)2.
En los últimos años se han diferenciado estas dos entidades debido a sus características clínica, patológica y radiológica disímiles, y con pronóstico diferente. Un factor determinante fue el descubrimiento del anticuerpo NMO-IgG, biomarcador de esta enfermedad que tiene una sensibilidad del 73% y una especificidad del 91% para distinguir la NMO de la esclerosis múltiple7. El método de inmunofluorescencia indirecta para la determinación de los anticuerpos NMO-IgG es considerado de elección8.
Existen criterios necesarios y de soportes paraclínicos (al menos uno). Los primeros son: neuritis óptica unilateral/bilateral (puede ser o no sincrónica), mielitis aguda habitualmente transversa que se extiende ≥ 3 segmentos vertebrales en la secuencia T2 (hipointensa en T1 durante el ataque), y sin evidencia de otras enfermedades (p. ej., sarcoidosis, vasculitis, síndrome de Sjögren, LES, etc.). Los segundos son: RM de cerebro reciente normal o que no cumpla los criterios para lesiones desmielinizantes (p. ej., lesiones hipotalámicas, periacueductales y en el bulbo dorsal -piso IV ventrículo-) y anticuerpos NMO-IgG positivos en el suero. Estos nuevos criterios propuestos, presentan una sensibilidad y especificidad del 99% y 90% respectivamente para NMO, en pacientes con enfermedad desmielinizante en SNC de presentación óptico-espinal9.
Las lesiones en la NMO se caracterizan por depósitos de IgG e IgM y activación del complemento con un patrón vascular central, sugiriendo un rol patogénico de la inmunidad humoral en el espacio perivascular. El autoanticuerpo IgG-NMO tiene como blanco las proteínas canales de agua AQP4, y éstas son las que más abundan en el SNC1, 3, 4, 10.
La distribución de las proteínas canales de agua AQP4 en la interfase glía-LCR en la médula espinal de ratón coincide con los sitios de unión de IgG-NMO, y es similar al patrón de depósito de inmunoglobulinas y productos de activación del complemento observados en las lesiones desmielinizantes/necrotizantes activas en pacientes con NMO11-12.Los estudios inmunohistoquímicos demostraron una intensa inmunorreactividad en las terminales astrocíticas sobre los capilares y piamadre del cerebro y médula espinal, especialmente en la lámina glial del núcleo supraóptico, hipotálamo, tronco cerebral y de las células ependimarias, especialmente en regiones periventriculares y subependimarias como el área postrema13. Estos sitios son coincidentes con las lesiones encontradas en la RM de cerebro en el 8-10% de pacientes con NMO, especialmente en la secuencia FLAIR3, 14.
La espectroscopia en la RM contribuye al diagnóstico diferencial, dado que la sustancia blanca aparentemente "normal"en pacientes con EM presenta un índice n-acetil-aspartato/creatina (Naa/Cr) disminuido, en contraste con el índice Naa/Cr normal en pacientes con NMO15.
Las lesiones observadas por RM en los casos presentados, consideradas "atípicas"por su ubicación e infrecuencia pero con alta densidad de proteínas canales de agua AQP4, deberán tenerse presentes al momento del diagnóstico diferencial.
Conflictos de interés: Adrián Schoijedman es director técnico de Laboratorios Zavala. El resto de los autores no tiene conflictos de interés para declarar.
1. Wingerchuk DM, Lennon VA, Pittock SJ, Luchinetti CF, Weinshenker BG. Revised diagnostic criteria for neuromyelitis optica. Neurology 2006; 66: 1485-9. [ Links ]
2. Mattiello M, Lennon VA, Jacob A, et al. NMO-IgG predicts the outcome of recurrent optic neuritis. Neurology 2008; 70: 2197-200. [ Links ]
3. Pittock SJ, Lennon VA, Krecke K, Wingerchuk DM, Luchinetti CF, Weinshenker BG. Brain abnormalities in neuromyelitis optica. Arch Neurol 2006; 63: 390-6. [ Links ]
4. Roemer SF, Parisi JE, Lennon VA, et al. Pattern-specific loss of aquaporin-4 immunoreactivity distinguishes neuromyelitis optica from multiple sclerosis. Brain 2007; 130: 1194-205. [ Links ]
5. Clifford Allbutt T. On the ophthalmoscopic signs of spinal disease. Lancet 1870; l: 76-8. [ Links ]
6. Devic M. Myélite subaiguë compliquée de névrite optique. Bull Med 1894; 8: 1033-4. [ Links ]
7. Lennon VA, Wingerchuk DM, Kryzer TJ, et al. A serum autoantibody marker of neuromyelitis optica: Distinction from multiple sclerosis. Lancet 2004; 364: 2106-12. [ Links ]
8. De Vidi I, Boursier G, Delouche N, et al. Strategy for anti-aquaporin-4 auto-antibody identification and quantification using a new cell-based assay. Clin Immunol 2011; 138: 239-46. [ Links ]
9. Miller DH, Weinshenker BG, Filippi MF, et al. Differential diagnosis of suspected multiple sclerosis: a consensus approach. Mult Scler 2008; 14: 1157-74. [ Links ]
10. Lucchinetti CF, Mandler RN, Mc Gavern D, et al. A role for humoral mechanisms in the pathogenesis of Devic's neuromyelitis optica. Brain 2002; 125: 1450-61. [ Links ]
11. Misu T, Fujihara K, Nakamura M, et al. Loss of aquaporin-4 in active perivascular lesions in neuromyelitis optica: A Case Report. Tohoku J Exp Med 2006; 209: 269-75. [ Links ]
12. Marignier R, Nicolle A, Watrin Ch, et al. Oligodendrocytes are damaged by neuromyelitis optica inmunoglobulin G via astrocyte injury. Brain 2010; 133: 2578-91. [ Links ]
13. Pittock SJ, Weinshenker BG, Luchinetti CF, Wingerchuk DM, Corboy JR, Lennon VA. Neuromyelitis optica brain lesions localizated at sites of high aquaporin 4 expression. Arch Neurol 2006; 63: 964-8. [ Links ]
14. Poppe AY, Lapierre Y, Melancol D, et al. Neuromyelitis óptica with hypothalamic involvement. Mult Scler 2005; 11: 617-21. [ Links ]
15. Bichuetti DB, Rivero RL, de Oliveira EM, et al. White matter spectroscopy in neuromyelitis optica: A case control study. J Neurol 2008; 255: 1895-9. [ Links ]
Recibido: 18-10-2011
Aceptado: 27-12-2011














