Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Medicina (Buenos Aires)
Print version ISSN 0025-7680On-line version ISSN 1669-9106
Medicina (B. Aires) vol.77 no.2 Ciudad Autónoma de Buenos Aires Apr. 2017
ARTÍCULO ORIGINAL
Dosis de hemodiálisis sub-óptima. Factores predisponentes, causas y prevención
Pehuén Fernández, Silvana Núñez, Javier De Arteaga, Carlos Chiurchiu, Walter Douthat, Jorge De La Fuente
Servicio de Nefrología, Unidad de Hemodiálisis, Hospital Privado Universitario de Córdoba,
Carrera de Postgrado de Nefrología, Universidad Católica de Córdoba,
Instituto Universitario de Ciencias Biomédicas de Córdoba, Fundación Nefrológica de Córdoba, Argentina
Recibido: 27-V-2016
Aceptado: 26-IX-2016
Resumen
Los pacientes que reciben dosis sub-óptima de hemodiálisis tienen mayor morbimortalidad. El objetivo del trabajo fue identificar los factores predisponentes y las principales causas de diálisis inadecuada y diseñar un algoritmo para aplicar en estos casos. Se realizó un estudio de corte transversal. Se incluyeron 90 pacientes en hemodiálisis crónica, en el Hospital Privado Universitario de Córdoba, en septiembre 2015. Veintidós recibieron una dosis sub-óptima de hemodiálisis. Aquellos con un volumen de distribución de urea (V) mayor a 40 l (72 kg de peso corporal aproximadamente), tienen 11 veces mayores posibilidades (OR = 11.6; IC95% = 3.2-51.7, p < 0.0001) de recibir una dosis inadecuada de hemodiálisis que los que tienen un V menor a esa cifra; y los hombres 3 veces más probabilidad que las mujeres (OR = 3.5; IC95% 1.0-15.8; p = 0.0292). El V mayor a 40 l fue el único factor independiente predictor de sub-diálisis en el análisis multivariado (OR = 10.3; IC95% 2.8-37; p = 0.0004). La principal causa de diálisis sub-óptima fue recibir un flujo sanguíneo (Qb) menor al prescripto (336.4 ± 45.8 vs. 402.3 ± 28.8 ml/min, respectivamente, p < 0.0001) (n = 18). Otras causas fueron: menor duración de la sesión (n = 2), recirculación del acceso vascular (n = 1) y error en las muestras (n = 1). En conclusión, el único factor independiente predisponente de sub-diálisis fue el V mayor a 40 l. La principal causa de diálisis inadecuada fue recibir un Qb menor al prescripto. A partir de estos hallazgos, se desarrolla un algoritmo para aplicar en estos casos.
Palabras clave: Hemodiálisis; Sub-diálisis; Dosis de diálisis; Modelo cinético de la urea.
Abstract
Inadequate doses of hemodialysis. Predisposing factors, causes and prevention
Patients receiving sub-optimal dose of hemodialysis have increased morbidity and mortality. The objectives of this study were to identify predisposing factors and causes of inadequate dialysis, and to design a practical algorithm for the management of these patients. A cross-sectional study was conducted. Ninety patients in chronic hemodialysis at Hospital Privado Universitario de Córdoba were included, during September 2015. Twenty two received sub-optimal dose of hemodialysis. Those with urea distribution volume (V) greater than 40 l (72 kg body weight approximately) are 11 times more likely (OR = 11.6; CI 95% = 3.2 to 51.7, p < 0.0001) to receive an inadequate dose of hemodialysis, than those with a smaller V. This situation is more frequent in men (OR = 3.5; 95% CI 1.01-15.8; p = 0.0292). V greater than 40 l was the only independent predictor of sub-dialysis in the multivariate analysis (OR = 10.3; 95% CI 2.8-37; p < 0.0004). The main cause of suboptimal dialysis was receiving a lower blood flow (Qb) than the prescribed (336.4 ± 45.8 ml/min vs. 402.3 ± 28.8 ml/min respectively, p < 0.0001) (n = 18). Other causes were identified: shorter duration of the session (n = 2), vascular access recirculation (n = 1), and error in the samples (n = 1). In conclusion, the only independent predisposing factor found in this study for sub-optimal dialysis is V greater than 40 l. The main cause was receiving a slower Qb than prescribed. From these findings, an algorithm for the management of these patients was developed.
Key words: Hemodialysis; Sub-dialysis; Dialysis dose; Urea kinetic modeling.
El método tradicional para cuantificar la dosis del tratamiento de hemodiálisis intermitente, en los pacientes con insuficiencia renal crónica terminal, es la medición del kt/V.
El cálculo del Kt/V tiene en cuenta principalmente tres elementos: la depuración de urea en el dializador (K), el tiempo de duración de la sesión (t) y el volumen de distribución de la urea (V), que es equivalente al agua corporal total. Este cálculo se corrige, además, por la pérdida de volumen secundario a la ultrafiltración (UF), y por la ganancia de urea intradiálisis (g). La depuración de urea depende principalmente de la eficacia del dializador (KoA), del flujo sanguíneo (Qb) y del flujo del dializado (Qd)1.
El modelo monocompartimental del Kt/V (spKt/V) asimila que la urea se distribuye homogéneamente en todos los tejidos del organismo, y no tiene en cuenta ni el secuestro de urea durante la diálisis debido a la diferencia del flujo regional, ni el rebote posterior a la misma.
Este método mide el aclaramiento de urea de una única sesión de diálisis, que muchas veces no representa el resto de las sesiones mensuales del mismo paciente. Además, no representa el comportamiento cinético de otras moléculas, también potencialmente tóxicas, y tiende a sobreestimar la dosis de diálisis que reciben los pacientes con bajo peso, o desnutrición2. Si bien este método tiene muchas limitaciones conocidas, continúa siendo el más utilizado en la práctica clínica3.
Las guías NKF-DOQI 2006 (National Kidney Foundation/ Dialysis Outcomes Quality Initiative) recomiendan, en los pacientes en hemodiálisis con función residual renal mínima, una dosis mayor o igual a 1.2 de spKt/V, y una dosis objetivo de 1.4 para cada sesión1. Mensualmente se calcula el spKt/V a todos los pacientes en hemodiálisis crónica, a partir de los valores de urea plasmática previa y posterior a una sesión. Definimos una dosis subóptima o inadecuada, a cualquier valor de spKt/V menor a 1.2. Es bien conocido, desde hace ya muchos años, el impacto negativo en la morbimortalidad de quienes reciben una dosis menor a esta4, 5.
Existen diferentes causas de diálisis inadecuada. La mayoría de las veces, la dosis prescripta no es igual a la dosis efectivamente recibida. Y esto se puede deber a: una reducción en el Qb (mal funcionamiento del acceso vascular por hipoflujo, estenosis, recirculación, inadecuada posición de las agujas, aumento de presiones venosas con alarmas en el equipo, errores del equipo de salud y negativa del paciente), en el Qd (mal funcionamiento del equipo de diálisis y del flujo de agua), en el KoA (menor que el valor in vitro, reducción de las fibras capilares del dializador), en el t efectivo de diálisis (negativa del paciente, complicaciones durante la sesión, retrasos en la conexión, alarmas y parada de bomba en el equipo por aumento de presiones), o que el paciente haya aumentado su peso corporal de manera significativa posterior a la prescripción. Otras causas probables pueden ser: recirculación cardiopulmonar significativa (por insuficiencia cardiaca grave), desequilibrio veno-venoso, con retraso en la transferencia de urea del intra al extracelular, y secuestro en diferentes tejidos por alteración del flujo regional (enfermedad vascular periférica grave), o errores en la técnica de recolección de las muestras o en el análisis del laboratorio6, 7.
Es muy importante identificar en cada paciente las causas de diálisis inadecuada, para poder actuar individualmente a tiempo y evitar complicaciones graves a largo plazo.
El objetivo de este trabajo fue identificar los factores predisponentes y las causas de diálisis inadecuada, en los pacientes con insuficiencia renal crónica terminal en tratamiento de hemodiálisis intermitente en el Hospital Privado Universitario de Córdoba, durante el mes de septiembre del 2015.
El segundo objetivo fue diseñar, a partir de los resultados obtenidos, un algoritmo práctico para aplicar a los pacientes en esta situación.
Materiales y métodos
Se realizó un estudio de corte transversal, observacional, analítico y descriptivo. Se incluyeron en el estudio todos los pacientes prevalentes con insuficiencia renal crónica terminal, sometidos a tratamiento de hemodiálisis crónica intermitente durante el mes de septiembre del 2015, en el Hospital Privado Universitario de Córdoba, a los que se les realizaron los análisis sanguíneos mensuales de rutina.
Fueron estratificados según el valor de spKt/V de la primera sesión de la semana. Se dividió la muestra en dos grupos: Grupo 1, con diálisis inadecuada (spKt/V menor a 1.2), y grupo 2, con diálisis adecuada (spKt/V mayor o igual a 1.2).
Se registró sexo, edad en años, tipo de acceso vascular (fístula, prótesis, catéter), peso corporal total en kg, altura en metros, volumen de distribución de la urea (V) en l, antecedentes personales patológicos de insuficiencia cardiaca congestiva (ICC), y enfermedad vascular periférica grave (EVPG).
Se registraron las especificaciones del tratamiento prescripto y recibido, Qb en ml/min, Qd en ml/min, KoA, t en minutos, volumen de UF en l, superficie de membranas 1.5 m2 o 2.1 m2, tamaño de las agujas 15G o 16G, y el porcentaje de recirculación de urea del acceso vascular.
Se analizaron las diferentes situaciones en las que no se cumplían con las especificaciones prescriptas.
Los equipos de diálisis utilizados son Fresenius 4008, 4008S, y Nipro Diamax TM. Los dializadores son NIPRO Sureflux 210N y 150N, con membrana semipermeable de triacetato, de superficie efectiva 1.5 m2 y 2.1 m2, KoA 736 y 902 ml/min, y esterilizados con rayos gamma. La reutilización de filtros se realiza según la medición del volumen residual (más del 80% del volumen residual inicial), de roturas de fibras, y cantidad de usos (menos de 20 re-usos). Si no cumple cualquiera de los tres criterios el filtro se descarta. Las agujas que se utilizan son Kawasumi 15G y 16G. Se usan Biotec 17G para las primeras canalizaciones en accesos vasculares nuevos. La temperatura del dializado varía entre 35.5 y 36.5 grados según criterio clínico. Las soluciones de diálisis son K-Dial, la solución B en base a bicarbonato y la solución A varía de acuerdo a los requerimientos de cada paciente. La dosis de heparina es de 75 UI/kg de peso corporal como bolo inicial y 500 UI horaria, a excepción de que el paciente tenga una contraindicación activa.
La extracción de las muestras sanguíneas se realiza siguiendo las recomendaciones de las guías K-DOQI 20061.
El esquema habitual del tratamiento de diálisis de la mayoría de los pacientes en nuestro servicio es trisemanal, de 4 h de duración. A modo de excepción, pocos realizan 2 o 4 sesiones a la semana, y de 3.5 a 5 h. Además, muchos conservan parte de su función residual. A pesar de esto, consideramos para todos los mismos valores límites de spKt/V que se utilizan en esquemas trisemanales y sin función residual.
Los valores de urea plasmática se expresan en mg/dl.
Para el cálculo del spKt/V se utilizó la fórmula de Daugirdas:
spKt/V = -In (R - 0.008 x t) + (4 – 3.5 x R) x UF/P
Donde R = SUN postdiálisis/SUN prediálisis; t = duración de la sesión en horas; UF = volumen de líquido eliminado durante la diálisis en litros; P = peso corporal inicial.
Para estimar el volumen de distribución de la urea (V) se utilizó el método de Hume-Weyers, para calcular el agua corporal total8.
Para hombres: V = - 14.012934 + 0.296785 x P + 0.192786 × A
Para mujeres: V = - 35.270121 + 0.183809 x P + 0.344547 × A
Donde P = peso en kg posdiálisis; A = altura en cm.
La técnica de recolección de las muestras para el cálculo de recirculación del acceso vascular se realizó con el método de las dos agujas9, utilizando la siguiente fórmula:
Porcentaje de recirculación = ([Us] – [Ua]) / ([Us] – [Uv])
Donde [Us] = Concentración de urea sistémica; [Ua] = Concentración de urea arterial; [Uv] = Concentración de urea venosa.
Para analizar las variables categóricas se utilizaron las frecuencias absolutas (n) y relativas (%), y para las variables continuas, medias (M) y desvío estándar (DS).
Para la comparación de las variables continuas se utilizó el test t-student o el test Mann Whitney según correspondiera. Para las variables categóricas se utilizó el chi2 y el test exacto de Fisher.
Para evaluar las causas predisponentes de sub-diálisis se usó como medida de asociación el Odds Ratio (OR), con su intervalo de confianza del 95% (IC 95%). Las variables que mostraron significación estadística se analizaron por regresión logística múltiple.
Todos los test fueron a dos colas. Se consideró estadísticamente significativo un valor de p < 0.05.
El análisis estadístico se realizó con el programa Stata 14 (StataCorp. LP., College Station, TX).
Resultados
El total de pacientes analizados fue 90, de los cuales 22 pertenecían al grupo 1 (diálisis inadecuada, con un spKt/V promedio de 1.1 ± 0.1) y 68 (75.6%) al grupo 2 (diálisis adecuada, spKt/V promedio de 1.6 ± 0.3). Se excluyeron 2, que en el momento de la extracción sanguínea mensual estaban internados. No se encontraron diferencias significativas entre ambos grupos en cuanto a las comorbilidades, tipo de acceso vascular, recirculación, y prescripciones de hemodiálisis. En cambio, sí hubo diferencias en relación al porcentaje de varones (81.8% del grupo 1 vs. 55.9% del grupo 2, p = 0.0292), y al volumen de distribución de la urea (V 45.1 ± 7.9 l en el grupo 1 y V 36.5 ± 7.5 l en el grupo 2, p < 0.0001) (Tabla 1).
Tabla 1. Características basales de los pacientes del grupo 1 (spKt/V < 1.2) y grupo 2 (spKt/V > 1.2)
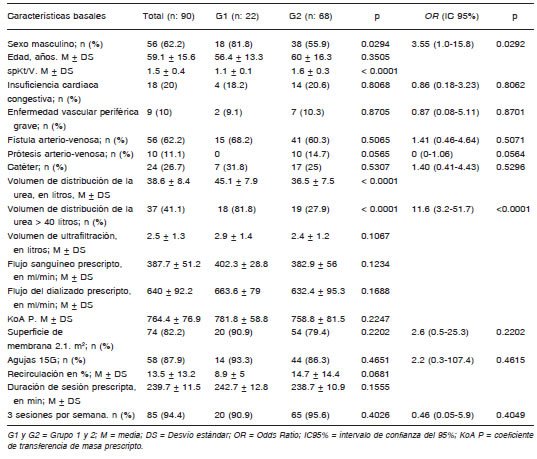
Para los varones el OR de realizar una diálisis inadecuada fue 3.5 (IC95%: 1.01-15.76, p = 0.0292) veces mayor que para las mujeres; y los pacientes con un V mayor a 40 l (aproximadamente 72 kg de peso corporal), tuvieron un OR de presentar sub-diálisis de 11.6 (IC95% 3.2 - 51.7, p < 0.0001) veces mayor, que aquellos con un V menor a esa cifra (Tabla 1). Al hacer un análisis más exhaustivo, observamos que el sexo masculino está fuertemente asociado a tener un V mayor a 40 l (OR = 7.7, IC95% 2.4 - 28.7, p < 0.0001), y que en realidad, los hombres con un V menor a 40 l no tienen una predisposición de tener subdiálisis; al contrario, el V menor a 40 l actúa como un factor protector de diálisis inadecuada (OR = 0.04; IC95% 0.0009 - 0.3; p < 0.0001). Es decir que el sexo masculino por sí solo no sería un factor predisponente para tener una dosis baja de diálisis, pero si el V mayor a 40 l. El análisis de regresión logística multivariada muestra lo mismo, el único factor independiente de subdiálisis es V mayor a 40 l (OR = 10.31; IC95% 2.8 -37.9; p = 0.0004).
El principal motivo de diálisis inadecuada identificada en nuestra población fue recibir un Qb menor al prescripto (Qb recibido: 336.4 ± 45.8 ml/min vs. Qb prescripto: 402.3 ± 28.8 ml/min, p < 0.0001). La duración de diálisis de estos pacientes también fue menor a la prescripta, aunque los resultados no fueron significativos. No se encontraron diferencias respecto al Qd y KoA prescriptos y recibidos (Tabla 2).
Tabla 2. Diferencias entre las especificaciones técnicas del tratamiento de diálisis prescriptas y recibidas, en pacientes con diálisis inadecuada (n: 22), septiembre 2015, Hospital Privado Universitario de Córdoba
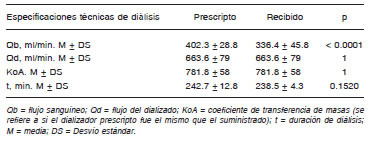
Al analizar individualmente los 22 casos del grupo 1, se adjudicó como causa principal de subdiálisis, el haber recibido un Qb menor al prescripto a 18, y el haber recibido un t menor al prescripto a 2 de ellos. En los que habían cumplido con las especificaciones prescriptas (n = 2), uno presentaba recirculación significativa del acceso vascular, por hipoflujo secundario a estenosis, y en el otro se consideró que pudo haber un error en la recolección o procesamiento de las muestras, ya que posteriormente el Kt/V mejoró sin ninguna modificación.
En la Tabla 3 se describen las diferentes situaciones identificadas en los que recibieron un Qb y t menor al prescripto.
Tabla 3. Descripción de situaciones identificadas en los pacientes con un Qb y t menor al prescripto, septiembre 2015, Hospital Privado Universitario de Córdoba (n: 20)

A partir del análisis de las diferentes causas de diálisis inadecuada, se diseñó un algoritmo práctico para aplicarse a este tipo de pacientes (Fig. 1).
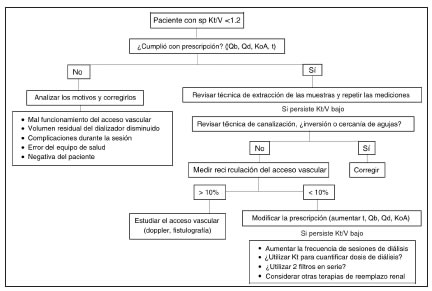
Fig. 1. Algoritmo de tratamiento de pacientes con spKt/V menor que 1.2.
Discusión
Resulta muy importante identificar los casos de mayor riesgo, y las causas de diálisis inadecuada, para poder actuar a tiempo y evitar consecuencias negativas.
Existen pocos trabajos publicados que analicen este problema. Fortounas y col.6 analizaron el motivo de las fluctuaciones del Kt/V en 59 pacientes en hemodiálisis crónica, en un centro de hemodiálisis en Grecia. Las causas identificadas en los pacientes con descenso anormal del Kt/V (n: 24) en este estudio fueron: 37% por diálisis de menor duración, por mala adherencia del paciente, 17% por disminución del flujo sanguíneo, 17% por agujas invertidas, 4% por trombosis de la fistula y 25% por causas desconocidas que luego se revirtieron. Coyne y col.7, estudiaron también los motivos de disminución del Kt/V en 146 pacientes en un centro de diálisis en EE.UU. Las causas halladas fueron: 42% por disminución del flujo sanguíneo o del tiempo efectivo de diálisis, 25% por recirculación significativa, ya sea por disfunción del acceso o por inversión de las agujas, 1% por disfunción del dializador y 32% por causa desconocida, que con el tiempo revirtió.
Algunas de las causas encontradas en estos estudios son semejantes a las identificadas en el nuestro, excepto el porcentaje de cada una de ellas. En nuestro trabajo, además, se describen las diferentes situaciones por las que el Qb fue menor al prescripto, a diferencia de los trabajos citados anteriormente. Una de las situaciones halladas fue la disminución del Qb por síntomas de hipotensión; a esto se lo considera un error, ya que la gran mayoría de las veces este síntoma se debe a un exceso de UF, y no se recomienda tomar esta medida10 salvo en situaciones extremas. La disminución del tiempo de diálisis debido a mala adherencia de los pacientes es un problema descripto hace ya muchos años11, que continúa vigente en la actualidad.
A diferencia de nuestro trabajo, los dos estudios citados previamente no realizan un análisis comparativo entre las características basales de los pacientes con spKt/V disminuido y adecuado. Esto creemos que puede ser de valor para determinar factores predisponentes de diálisis inadecuada. En nuestro caso, no encontramos diferencias significativas relacionadas a los antecedentes personales de enfermedad, el tipo de acceso vascular, y especificaciones de diálisis, pero sí encontramos diferencias relacionadas al V entre los grupos y una fuerte asociación entre V mayor a 40 l y sub-diálisis. Esto adquiere importancia en el manejo de estos casos, particularmente vulnerables. Al no haber diferencias en la prevalencia de ICC y EVPG entre ambos grupos, asumimos que tampoco lo hubo en el grado de recirculación cardiopulmonar y desequilibrio veno-venoso, y que estos parámetros no fueron influyentes en los resultados.
Otra diferencia con los estudios citados es que, además de describir las posibles causas identificadas de diálisis inadecuada, se realizó un análisis comparativo entre las especificaciones prescriptas y las recibidas, encontrando diferencias significativas solo en el Qb. El t de diálisis fue menor al prescripto, aunque sin significancia estadística.
Consideramos relevante la creación de un algoritmo para aplicar a pacientes con sub-diálisis, para facilitar el diagnóstico y la conducta médica, y evitar complicaciones graves a largo plazo en esta población.
La utilización del Kt para medir la dosis de diálisis es un tema discutido en la actualidad. Algunas publicaciones muestran que tanto el Kt, como el V, son variables independientes de mortalidad, y que el incremento de ambas mejoran la supervivencia, por lo que deberían utilizarse por separado12. Además, los pacientes con un V extremadamente bajo suelen tener valores de Kt/V muy elevados, y se los cataloga como diálisis adecuada, aunque en realidad muchos de ellos tienen un Kt bajo y subdiálisis2, 13. Otra de las diferencias con el Kt/V, es que las fórmulas antropométricas utilizadas actualmente sobreestiman el V en un 15% aproximadamente en los sujetos en hemodiálisis14, por lo que se puede inferir que aquellos con V elevado que tienen un Kt/V levemente disminuido, en realidad tienen un Kt adecuado. Por estos y otros motivos, algunos autores sugieren que el Kt provee una mejor medición de la dosis de diálisis que el Kt/V, aunque se necesita aún mayor evidencia para asegurarlo2.
La utilización de dos filtros en serie o en paralelo es considerada como una de las últimas opciones para mejorar el aclaramiento en sujetos de gran tamaño corporal. Existen algunas comunicaciones con buenos resultados, aunque esta práctica no está aún universalmente aceptada15, 16. Cabe señalar también que este algoritmo aún no ha sido validado por otro estudio similar.
La realización del estudio en un único centro de diálisis, en un único mes y en una sesión aislada de hemodiálisis, son las limitaciones principales de este trabajo. La cantidad de sujetos incluidos dificulta la generalización de los resultados.
La escasa cantidad de trabajos de investigación que abordan este tema, con la importancia y el impacto del mismo en la morbimortalidad, y la creación de un algoritmo práctico, representan las principales fortalezas del estudio.
En conclusión, el único factor predisponente independiente de diálisis sub-óptima hallado en este estudio fue el V. Los pacientes con un V mayor a 40 l (equivale a 72 kg de peso corporal aproximadamente) tienen 11 veces más posibilidades de recibir una dosis de diálisis inadecuada que aquellos con un V menor, por lo que requieren de máxima precaución y cuidado. La principal causa de diálisis inadecuada hallada fue el Qb menor al prescripto, ya sea por error del equipo de salud, por mal funcionamiento del acceso vascular, por infiltración, por síntomas, o por negativa del paciente. La segunda causa en frecuencia fue la reducción de la duración de la sesión, ya sea por complicaciones y desconexión anticipada o por mala adherencia del paciente. Otras causas encontradas fueron la recirculación del acceso vascular, y el error en la recolección de las muestras. A partir de estos hallazgos se desarrolla un algoritmo práctico de aplicación en esta situación. Recomendamos su utilización para identificar las causas de sub-diálisis, modificarlas, y así reducir la cantidad de casos con diálisis inadecuada y las graves consecuencias que esto conlleva.
Conflicto de intereses: Ninguno para declarar
1. Hemodialysis Adequacy 2006 Work Group. Clinical practice guidelines for hemodialysis adequacy, update 2006. Am J Kidney Dis 2006; 48 Suppl 1: S2-90. [ Links ]
2. Chertow GM, Owen WF, Lazarus JM, Lew NL, Lowrie EG. Exploring the reverse J-shaped curve between urea reduction ratio and mortality. Kidney Int 1999; 56: 1872-8. [ Links ]
3. Barroso S. ¿Es el Kt/V el mejor indicador de la dosis de diálisis? Nefrología 2007; 27: 667-9. [ Links ]
4. Hakim RM, Breyer J, Ismail N, Schulman G. Effects of dose of dialysis on morbidity and mortality. Am J Kidney Dis 1994; 23: 661-9. [ Links ]
5. Held PJ, Port FK, Wolfe RA, et al. The dose of hemodialysis and patient mortality. Kidney Int 1996; 50: 550-6. [ Links ]
6. Fourtounas C, Kopelias I, Paraskevopoulos A, Dimitriadis G, Agroyannis B. Causes of impaired delivery of hemodialysis prescription. Artificial organs 2006; 30: 878-81. [ Links ]
7. Coyne DW, Delmez J, Spence G, Windus DW. Impaired delivery of hemodialysis prescriptions: an analysis of causes and an approach to evaluation. J Am Soc Nephrol 1997; 8: 1315-8. [ Links ]
8. Hume R, Weyers E. Relationship between total body water and surface area in normal and obese subjects. J Clin Pathol 1971; 24: 234-8. [ Links ]
9. Pederson WC, Dunlay R, Llach F. Two-needle calculation of recirculation compared with the standard three-needle method. Clin Nephrol 1990; 33: 203-6. [ Links ]
10. Schytz PA, Mace ML, Soja AMB, et al. Impact of extracorporeal blood flow rate on blood pressure, pulse rate and cardiac output during haemodialysis. Nephrol Dial Transplant 2015; 30: 2075-9. [ Links ]
11. Rocco MV, Burkart JM. Prevalence of missed treatments and early sign-offs in hemodialysis patients. J Am Soc Nephrol 1993; 4: 1178-83. [ Links ]
12. Lowrie EG, Li Z, Ofsthun N, Lazarus JM. Body size, dialysis dose and death risk relationships among hemodialysis patients. Kidney Int 2002; 62: 1891-97. [ Links ]
13. Lowrie EG, Li Z, Ofsthun N, Lazarus JM. Measurement of dialyzer clearance, dialysis time, and body size: death risk relationships among patients. Kidney Int 2004; 66: 2077-84. [ Links ]
14. Daugirdas JT, Greene T, Depner TA, Chumlea C, Rocco MJ, Chertow GM. Anthropometrically estimated total body water volumes are larger than modeled urea volume in chronic hemodialysis patients: effects of age, race, and gender. Kidney Int 2003; 64: 1108-19. [ Links ]
15. Splendiani G, Zazzaro D, Tullio T, Colombo R, Beciani M, Violante A. Bidialysis: a new technique. Int J Artif Organs 2001; 24:70-8. [ Links ]
16. Fritz BA, Doss S, McCann LM, Wrone EM. A comparison of dual dialyzers in parallel and series to improve urea clearance in large hemodialysis patients. Am J Kidney Dis 2003; 41: 1008-15. [ Links ]














