El síndrome INOCA (Ischemia with Non-Obstructive Coronary Arteries) se define por la presencia de signos o síntomas de isquemia sin enfermedad coronaria epicárdi ca obstructiva y es un hallazgo cada vez más frecuente1-3.
Actualmente, su prevalencia alcanza hasta a un 70% de las mujeres sintomáticas y hasta a un 30% de los hombres sintomáticos, que son remitidos a una angio grafía diagnóstica.
Una de las causas propuestas de este síndrome es la angina microvascular (AMV) provocada por disfunción microvascular (DMV), que puede evaluarse en forma no invasiva, mediante la cuantificación del flujo sanguí neo miocárdico (FSM) y la reserva de flujo miocárdica (RFM)4-6.
Los nuevos equipos CZT-SPECT permiten establecer la presencia de DMV evaluando diferentes mecanis mos fisiopatológicos según el apremio que se utilice: dipiridamol para la valoración del mecanismo endotelio independiente y test de frío (TF), para la valoración en dotelio dependiente7-9.
En condiciones normales, tras la administración de dipiridamol, el FSM debe aumentar al menos dos veces su valor basal, con lo que se obtendrá una RFM mayor o igual a 2, mientras que, con el TF el FSM debe aumentar al menos 50% sobre el valor basal, con lo que se obtendrá una RFM mayor o igual a 1.510-12.
La valoración clínica de los pacientes con INOCA se puede realizar a través del cuestionario de Seattle, una escala que permite conocer de manera sencilla la fre cuencia de los síntomas de isquemia, la clase funcional y la calidad de vida los pacientes durante el último mes. La realización del cuestionario de Seattle a un mismo paciente en diferentes entrevistas durante su seguimiento, permitiría evaluar si existe o no una mejoría clínica13.
Existen múltiples métodos para establecer el diag nóstico de DMV en sujetos con INOCA, pero todavía no contamos con un enfoque de tratamiento específico para este grupo de pacientes. La tendencia actual es tratar de ajustar el tratamiento al mecanismo fisiopatológico involucrado, agregando bloqueantes cálcicos (principal mente diltiazem) en quienes se demuestre disfunción endotelial o beta bloqueantes (principalmente nebivolol) en aquellos con disfunción dependiente del músculo liso, o la combinación de ambos fármacos si se sospechara la coexistencia de ambos mecanismos14.
Caso clínico 1
Mujer de 55 años, que consultó al Servicio de Emergen cias por dolor precordial opresivo en CF II, prolongado, de reciente comienzo sin cambios isquémicos agudos en el ECG al momento del ingreso. Antecedentes de hipertensión (en tratamiento con enalapril), dislipémica y con sobrepeso. Inicialmente se interpretó el cuadro clínico como síndrome coronario agudo, por lo que se le realizó cinecoronariografía (CCG) que no evidenció lesiones angiográficamente signifi cativas, reinterpretándose como INOCA.
Se continuó el estudio etiológico de forma no invasiva, realizándole perfusión miocárdica con dipiridamol y TF con cálculo de RFM.
Ambas perfusiones miocárdicas fueron normales y los resultados obtenidos de RFM fueron 1.5 y 0.67 respectiva mente, ambos valores anormales, arribando al diagnóstico de DMV por ambos mecanismos fisiopatológicos, músculo liso dependiente y endotelio dependiente respectivamente (Fig. 1A).
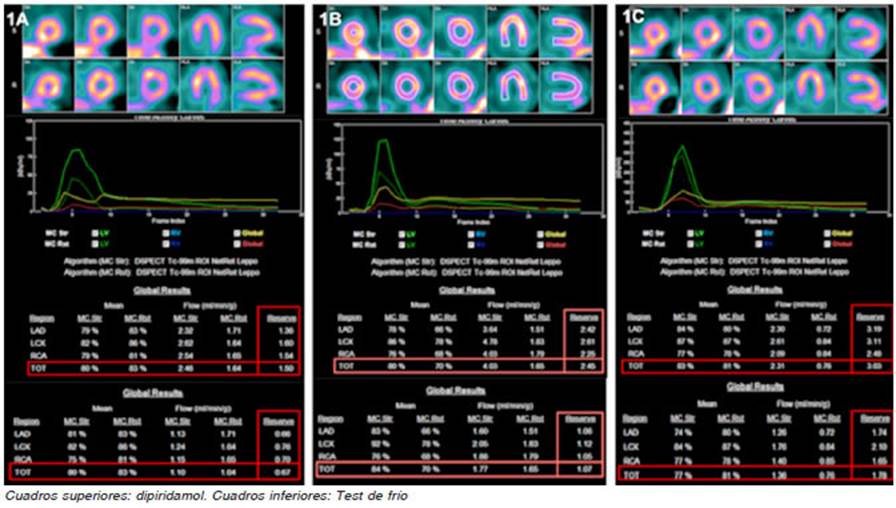
Fig. 1 Valores de flujo sanguíneo miocárdico y reserva de flujo miocárdica obtenidos en los estudios basales.
Con estos resultados, la primera medicación en agregarse al tratamiento habitual fue nebivolol y según tolerancia, se combinó posteriormente con diltiazem a dosis bajas. Tam bién se optimizó el tratamiento de los factores de riesgo con inhibidores de la enzima convertidora de angiotensina (IECA) y estatinas.
El estudio se repitió a los 6 meses del tratamiento, cuando ya se percibía una mejoría clínica valorada por la escala de Seattle, donde se documentó menor frecuencia de los episodios de dolor precordial y menor intensidad de los mismos. Se observó una normalización de la función mi crovascular músculo liso dependiente (RFM con dipiridamol de 2.29), aunque el TF no mostró cambios significativos en ese período (Fig. 2A).
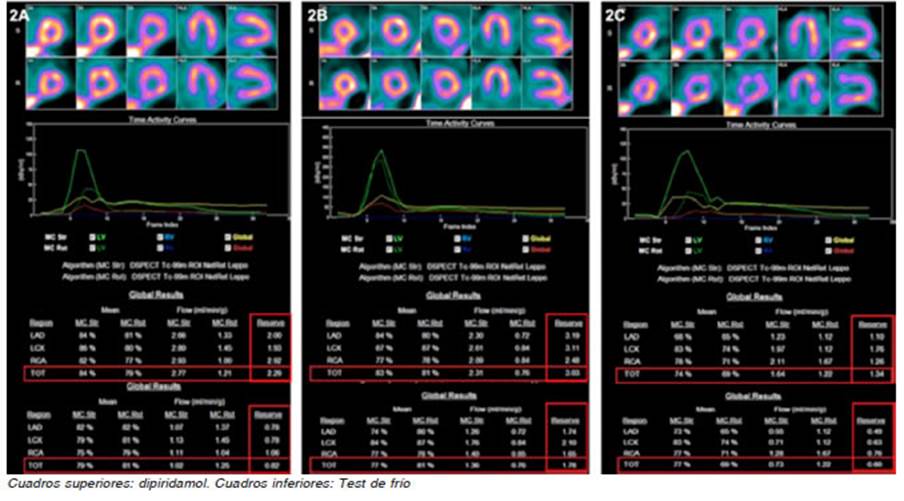
Fig. 2 Valores de flujo sanguíneo miocárdico y reserva de flujo miocárdica obtenidos en los estudios de seguimiento.
Si bien estos datos son experimentales y no se registran hasta el momento publicaciones con seguimiento de RFM post-tratamiento, estos resultados apoyarían la hipótesis de la existencia de dos mecanismos de DMV independientes, con diferente respuesta al tratamiento médico. Podría ser que el componente endotelial, quizás, necesite tratamiento por más tiempo para recuperar su función, o quizás, se trate de una DMV de tipo estructural y no meramente funcional a este nivel, con menor potencial de respuesta al tratamiento.
Caso clínico 2
Mujer de 59 años que consultó por episodio de dolor precor dial típico y disnea de esfuerzo de aproximadamente un mes de evolución. Antecedentes de diabetes tipo II, dislipemia y ex tabaquismo (5 paquetes/año). Inicialmente se interpretó el cuadro clínico como angina de reciente comienzo, por lo que se le realizó CCG que no evidenció lesiones angiográficamente significativas, reinterpretándose el cuadro clínico como INOCA.
Se continuó el estudio etiológico de forma no invasiva, mediante perfusión miocárdica con dipiridamol y TF con cálculo de RFM.
Ambas perfusiones miocárdicas fueron normales y los resultados obtenidos de RFM fueron 2.45 (normal) y 1.07 (anormal) respectivamente, arribando al diagnóstico de DMV por mecanismo endotelio dependiente (Fig. 1B).
Con los resultados obtenidos, se ajustó el tratamiento médico según la fisiopatología, agregando diltiazem a dosis máximas tolerables y optimizando el tratamiento de los fac tores de riesgo con IECA y estatinas.
Presentó una mejoría clínica notoria a partir de los 6 me ses de tratamiento óptimo, también valorada por la escala de Seattle. Se repitió el estudio para cuantificar nuevamente la RFM (Fig. 2B).
En el segundo estudio, observamos un valor de RFM con dipiridamol y TF normal, lo que supuso una recuperación de la función del endotelio microvascular.
Caso clínico 3
Mujer de 65 años, con antecedentes de dislipemia, sedenta rismo y sobrepeso, en seguimiento por dolor precordial típico al inicio del esfuerzo (menos de 100 metros de caminata), con ecostress positivo por cambios en el electrocardiograma durante el máximo esfuerzo a los 7 METS (infradesnivel del segmento ST en DII, DIII y de V4 a V6).
Se le realizó CCG que no evidenció lesiones angiográ ficamente significativas, interpretándose como INOCA. La paciente se medicó empíricamente con nebivolol y diltia zem. Meses más tarde, sin interrumpir la medicación, se le solicitó perfusión miocárdica con dipiridamol y TF con cálculo de RFM.
Ambas perfusiones miocárdicas fueron normales y los resultados obtenidos de RFM fueron 2.29 (normal) y 1.5 (normal) respectivamente (Fig. 1C). Los resultados no fueron compatibles con DMV, pero el tratamiento ya instaurado no se modificó. Sin embargo, la paciente comenzó a manifestar signos leves de intolerancia a los fármacos, por lo que decidió no continuar el tratamiento con los mismos.
Un año más tarde, consultó por empeoramiento de la frecuencia e intensidad de los síntomas. Esta vez, previo al reinicio del tratamiento, se le realizó cálculo de RFM. Los resultados obtenidos fueron RFM con dipiridamol de 1.34 (anormal) y con TF de 0.60 (anormal), compatible con una DMV músculo liso y endotelio dependiente. (Fig. 2C).
En esta paciente se pudo observar la función microvascular de manera inversa: cuando estaba medicada no se evidenció DMV, mientras que, tras meses de abandono de tratamiento y concomitantemente a la reaparición de los síntomas, pudo demostrarse un mecanismo mixto de DMV subyacente.
Discusión
Si bien es sabido que la presencia de DMV empeora el pronóstico con respecto a quienes poseen una función microvascular conservada, y que éste es peor aún cuan do la DMV es sintomática, todavía no contamos con un enfoque de tratamiento específico para este grupo de pacientes. Esto trae aparejado, la existencia de múltiples combinaciones de fármacos, incluso sin una evidencia certera de su beneficio.
Existe acuerdo científico en considerar a los cambios en el estilo de vida, el control de los factores de riesgo coronario y el entrenamiento físico regular, como pilares terapéuticos fundamentales para lograr una mejoría clínica. Sin embargo, con respecto al tratamiento farma cológico, la recomendación no es tan clara ni tan precisa, aunque la tendencia actual es adecuar el uso de drogas al mecanismo fisiopatológico causal de la DMV, basándose principalmente en los hallazgos del CormicA trial15.
Este estudio evaluó la función coronaria de 151 pa cientes sintomáticos durante la angiografía diagnóstica invasiva inicial, aleatorizándolos en dos grupos: manejo terapéutico orientado por los resultados fisiopatológicos invasivos (grupo 1) y un grupo control, y comparó los efectos sobre la calidad de vida y los eventos clínicos a largo plazo entre ambos grupos. Durante el seguimiento logró demostrar que, el grupo 1 presentó una mejoría clínica marcada y sostenida, con una mejor calidad de vida frente al grupo control16.
Nuestro grupo de trabajo, propone realizar un estudio no invasivo diagnóstico de DMV, idealmente sin que el/la paciente esté recibiendo beta-bloqueantes o bloqueantes cálcicos, para luego agregarlos y titularlos conforme a los resultados obtenidos de RFM y el o los mecanismos fisio patológicos involucrados. Esto fue lo que ocurrió con las dos primeras pacientes presentadas, que se encontraban solo medicadas con aspirina, IECA y estatinas, pudiendo cuantificarse posteriormente una mejoría de la función microvascular coincidente con la respuesta clínica.
El beneficio de contar con el estudio cuantitativo de la DMV, radica en que la asociación empírica de ambos fármacos (beta-bloqueantes y bloqueantes cálcicos) puede ocasionar menor adherencia al tratamiento en los pacientes debido a la aparición de efectos adversos indeseables de forma más frecuente, como ocurrió en la tercera paciente. Lo paradójico en este caso fue que, al dejar de tomar la medicación, pudimos evaluar la función microvascular sin la acción crónica de ningún fármaco, llegando a la conclusión de que ambos eran necesarios para su tratamiento, ya que el empeoramiento clínico sin duda guardaba relación con el deterioro de DMV por ambos mecanismos.
La DMV es una enfermedad con prevalencia creciente en los últimos años, que todavía se encuentra sub-diag nosticada y tratada en condiciones sub-óptimas. Conocer la fisiología de la microcirculación, sus mecanismos pa tológicos y los métodos disponibles para diagnosticarla, resulta fundamental para la práctica clínica diaria actual. El interés científico creciente en esta enfermedad, resulta prometedor para lograr nuevos avances en el tratamiento y seguimiento de la DMV.














