Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
El hornero
versión impresa ISSN 0073-3407versión On-line ISSN 1850-4884
Hornero v.18 n.1 Buenos Aires ene./ago. 2003
La reproducción de cinco especies de Emberizidae y Fringillidae en la Reserva de Ñacuñán, Argentina
Eduardo T. Mezquida
Grupo de Investigación en Ecología de Comunidades de Desierto (Ecodes), Unidad de Fisiología y Ecofisiología Vegetal, IADIZA. CC 507, 5500 Mendoza, Argentina. Dirección actual: P. Alameda de Osuna 74 1°C, 28042 Madrid, España. ricardo.mezquida@adi.uam.es.
Resumen
En este estudio se describe la nidificación de cinco especies de Emberizidae y Fringillidae en la Reserva de Ñacuñán, situada en el desierto del Monte central. El periodo de puesta comenzó en octubre o principios de noviembre y continuó hasta diciembre o enero. En Diuca diuca y, de forma menos clara, en Saltatricula multicolor, la fecha promedio de puesta tendió a ser más tardía en la temporada lluviosa de 1997-1998. Todas las especies construyeron nidos abiertos de tipo taza, aunque Diuca diuca utilizó nidos viejos de otras aves (principalmente de especies de Furnariidae) cuando nidificó en ambientes naturales, mientras que los nidos abiertos se observaron únicamente junto a la estación biológica de la reserva. Zonotrichia capensis situó los nidos en el suelo, generalmente al pie de gramíneas. El resto de las especies utilizó arbustos como el atamisque y la zampa (Saltatricula multicolor), árboles de chañar (Diuca diuca en nidos viejos de Asthenes baeri), árboles naturales o exóticos plantados y estructuras de origen humano junto a la estación biológica (Saltator aurantiirostris, Carduelis magellanica). La puesta de los huevos se realizó en días consecutivos y el tamaño de puesta fue de 3–4 huevos en todos los casos. Tres nidos de Diuca diuca (43%) contenían huevos del parásito Molothrus bonariensis. En todos los casos, los nidos parasitados se localizaron junto a construcciones humanas. El tamaño de puesta en Saltatricula multicolor fue mayor en 1997-1998 comparado con 1996-1997 y 1998-99. La productividad promedio en esta especie fue de 0.5 volantones por nido activo y de 2.3 volantones por nido exitoso. Se describe la duración del periodo de incubación y de permanencia de los pollos y las características de los pollos tras el nacimiento.
Palabras clave: Argentina, Carduelis, Emberizidae, nidificación, Ñacuñán.
Abstract
The breeding of five species of Emberizidae and Fringillidae in the Reserve of Ñacuñán, Argentina
The breeding of five species of Emberizidae and Fringillidae in the Reserve of Ñacuñán, located in the central Monte desert, is described. The laying period started in October or early November, and lasted until December or January. The average date of egg laying tended to be later in the wet 1997-1998 breeding season for Diuca diuca and, less clearly, for Saltatricula multicolor. All species built open-cup nests, although Diuca diuca used old nests of other birds (mainly Furnariidae) when nested in natural habitats; the open nests built by this species were found only beside the biological station of the reserve. Zonotrichia capensis placed the nests on the ground, usually covered by a tussock of grass. The remainder species used shrubs such as atamisque and zampa (Saltatricula multicolor), chañar trees (Diuca diuca using old nests of Asthenes baeri), natural or exotic planted trees and artificial structures from humans beside the biological station (Saltator aurantiirostris, Carduelis magellanica). Eggs were laid on consecutive days and clutch size was 3–4 eggs in all studied species. Three nests of Diuca diuca (43%) had eggs of the parasitic Molothrus bonariensis. In all cases, parasitized nests were placed around human settings. Mean clutch size of Saltatricula multicolor was larger in 1997-1998 compared to 1996-1997 and 1998-1999. Mean productivity in this bird species was 0.5 fledgings per active nest and 2.3 fledgings per successful nest. The duration of incubation and nestling periods, and chick characteristics after hatching are described.
Key words: Argentina, Carduelis, Emberizidae, nesting, Ñacuñán.
Recibido 24 diciembre 2002, aceptado 14 julio 2003
Las especies de aves incluidas en las familias Emberizidae y Fringillidae forman un grupo grande y complejo cuyas relaciones filogenéticas todavía no han sido claramente resueltas. En la Reserva de Ñacuñán, provincia de Mendoza (Argentina), se han citado hasta 17 especies de Emberizidae y Fringillidae en las últimas décadas (Contreras 1979, Marone 1992a, Lopez de Casenave 2001), aunque la mayoría de ellas se han observado de forma ocasional y otras han modificado su estatus de residencia durante ese periodo (Lopez de Casenave 2001). Las densidades de estas especies también son muy variables entre años y entre estaciones dentro de un mismo año (Marone 1992b, Lopez de Casenave 2001). Marone et al. (1997) analizaron los patrones de uso de los dos hábitats principales de Ñacuñán por parte de las especies granívoras numéricamente más importantes y encontraron que éstos variaban estacionalmente, de forma tal que durante la estación reproductiva las aves se distribuían de forma consistente con sus requerimientos de hábitat (i.e., alimento y sitios apropiados para la nidificación). El pastoreo por el ganado, una de las principales actividades económicas en el desierto del Monte, parece influir de forma negativa sobre las poblaciones de granívoros (Gonnet 2001). Sin embargo, los principales mecanismos implicados en este proceso no están suficientemente claros, aunque se ha sugerido que los sitios de nidificación utilizados por la mayor parte de estas aves no parecen verse muy afectados por este tipo de perturbación del hábitat (Gonnet 2001). Por lo tanto, a pesar de que el conocimiento de los requerimientos de hábitat para la nidificación y, en general, de la biología reproductiva de estas especies es fundamental para el estudio, manejo y conservación de estas aves, esta información es escasa y puntual en la mayoría de los casos.
El objetivo de este trabajo es describir la reproducción de cuatro especies de Emberizidae (Saltator aurantiirostris, Diuca diuca, Zonotrichia capensis, Saltatricula multicolor) y una de Fringillidae (Carduelis magellanica) en la Reserva de Ñacuñán. Existen algunas referencias antiguas sobre la reproducción de estas especies en Argentina y Chile (e.g., Hartert y Venturi 1909, Dinelli 1918, 1924, Reed 1919, Smyth 1928, Pereyra 1937, Partridge 1953, Goodall et al. 1957) y trabajos más completos y recientes para algunas de ellas en el este de Argentina y Chile (Fraga 1978, 1983, Mason 1985, Lazo y Anabalón 1991, 1992, de la Peña 1996). En este estudio se incluye información acerca del periodo de puesta, características del nido y del sitio de nidificación, tamaño y ritmo de puesta, duración del periodo de incubación y de permanencia de los pollos, características de los huevos y pollos, y productividad.
Métodos
Durante cuatro temporadas reproductivas (1995-1996 a 1998-1999), estudié la biología reproductiva de las cinco especies en la Reserva de la Biosfera de Ñacuñán (34°03'S, 67°54'O), localizada en la provincia de Mendoza, en el centro-oeste de Argentina. La reserva se sitúa en la porción central de la Provincia Fitogeográfica del Monte (Morello 1958, Marone 1992a). El hábitat que ocupa mayor extensión dentro de la reserva es un bosque abierto de algarrobo (Prosopis flexuosa). En el estrato arbóreo también hay algunos chañares (Geoffroea decorticans) y bajo este escaso dosel aparecen diversos arbustos como jarilla (Larrea divaricata), atamisque (Capparis atamisquea), piquillín (Condalia microphylla) y zampa (Atriplex lampa), y varias especies de arbustos bajos (e.g., Lycium spp., Verbena aspera, Acantholippia seriphioides). El estrato herbáceo está compuesto principalmente por gramíneas (e.g., de los géneros Pappophorum, Trichloris, Aristida, Digitaria). El clima de Ñacuñán es árido-semiárido, con una marcada estacionalidad. Las precipitaciones anuales son altamente variables de un año a otro (rango 193–533 mm, n = 27 años), cayendo principalmente (78% de las precipitaciones) durante la primavera y el verano (octubre a marzo).
En cada estación reproductiva realicé búsquedas de nidos (generalmente desde septiembre hasta febrero) observando la vegetación y el comportamiento de los adultos (Martin y Geupel 1993). De cada uno de los nidos encontrados medí su diámetro externo e interno (promedio del diámetro mayor y el perpendicular a éste, en ambos casos), altura externa y profundidad. También caractericé los sitios de nidificación mediante una serie de variables: especie, altura y diámetro de la copa (promedio del diámetro mayor y el perpendicular a éste) de la planta soporte del nido, altura desde el suelo hasta el borde superior del nido, distancia del borde superior del nido al límite superior de la planta directamente por encima del nido y un índice de posición del nido (calculado visualmente como la posición relativa del nido entre el tronco principal y el borde de la planta a la altura del nido; Lazo y Anabalón 1991).
Revisé los nidos cada 1–3 días para controlar su estado de actividad hasta que el nido fracasó o los pollos abandonaron el nido. Calculé la fecha de comienzo de la puesta de los nidos ya iniciados restando la duración del periodo de incubación y el tamaño de la puesta completa (un día por cada huevo, ver Resultados) desde la fecha en que ocurrió la eclosión de los huevos. Marqué los huevos con tinta indeleble y medí su longitud y ancho máximos (precisión 0.1 mm). Además, pesé los huevos y los pollos con una precisión de 0.1 g. La mayoría de los huevos fueron pesados durante la fase de puesta o al inicio de la incubación.
Algunos nidos de Diuca diuca fueron parasitados por Molothrus bonariensis (ver Resultados). Para el cálculo del tamaño de puesta en esta especie no se tuvieron en cuenta los nidos parasitados. Calculé el periodo de incubación como el intervalo entre la puesta del último huevo y la eclosión del mismo (Nice 1954), y el periodo de permanencia de los pollos como el número de días entre la eclosión del primer pollo y el abandono del nido por el último pollo.
Para comparar las fechas de puesta de los huevos entre diferentes temporadas reproductivas, utilicé la Prueba de t o un Análisis de Varianza. Para la comparación del tamaño de puesta entre años, usé la prueba no paramétrica de Mann-Whitney. El tamaño de muestra varía para las distintas mediciones, ya que algunas variables no pudieron medirse en todos los nidos o no se midieron al comienzo de este estudio. A lo largo de todo el trabajo, los datos son expresados como promedio ± error estándar.
Resultados
El total de nidos encontrados de las cinco especies de Emberizidae y Fringillidae fue de 49 en las cuatro temporadas de estudio. En general, el número de nidos observados fue muy bajo y variable entre años, y solo en dos especies (Diuca diuca y Saltatricula multicolor) se encontraron más de 10 nidos. En todos los casos, el inicio de la puesta fue durante octubre o principios de noviembre (Tabla 1). La puesta de los huevos en los nidos más tardíos ocurrió habitualmente en diciembre o comienzos de enero (Tabla 1). En Diuca diuca, el periodo de puesta mostró dos picos de actividad, uno a principios de noviembre (50% de los nidos) y otro durante diciembre (42%), debido principalmente a diferencias interanuales en el patrón de puesta. En 1995-1996 no se observaron nidos de esta especie, y en un nido encontrado en 1998-1999 durante la fase de construcción no se observó la puesta de ningún huevo. La fecha promedio de puesta en 1996-1997 (47.5 ± 8.8, n = 6; contando cada fecha consecutivamente desde el 1 de octubre, considerado como día 1) fue anterior a la de 1997-1998 (68.5 ± 6.4, n = 6; t = -2.3, gl = 10, P = 0.045). De igual manera, en el 50% de los nidos de Saltatricula multicolor la puesta se inició a finales de octubre y comienzos de noviembre, mientras que en el 31% se inicio durante diciembre. Sin embargo, la fecha promedio de puesta no difirió estadísticamente entre las tres temporadas reproductivas en las que se encontraron nidos de esta especie (1996-1997: 65.0 ± 34.5, n = 3; 1997-1998: 64.1 ± 9.3, n = 9; 1998-1999: 42.0 ± 9.1, n = 4; F2,13 = 0.7, P = 0.53). La gran variabilidad registrada en la temporada 1996-1997 se debió a que se observaron dos nidos a fines de octubre y uno a mediados de febrero.
Tabla 1. Periodo de puesta de los huevos de cinco especies de Emberizidae y Fringillidae observado durante cuatro estaciones reproductivas consecutivas (1995-1996 a 1998-1999) en la Reserva de Ñacuñán. Se indica entre paréntesis el número de nidos en los que se pudo calcular la fecha de puesta.

Todas las especies construyeron nidos abiertos de tipo taza (Tabla 2). Los nidos de Saltator aurantiirostris estaban compuestos por ramas delgadas de jarilla y Verbena aspera y por hojas de algarrobo y de Schinus molle (en el nido situado en esta planta), y estaban forrados interiormente con peciolos de hojas de algarrobo. El resto de las especies utilizó como materiales de construcción del nido tallos de gramíneas y herbáceas, y forró el interior con alguna pluma, fibras vegetales y crines. En Ñacuñán, Diuca diuca nidificó frecuentemente (62% de los casos) en nidos viejos de otras especies (en un nido de Pseudoseisura lophotes, en seis de Asthenes baeri y en uno de Myiopsitta monachus). Cuatro de los nidos de Asthenes baeri utilizados estaban semidestruidos, con un amplio hueco lateral, mientras que en los otros dos casos los nidos se encontraban en buen estado. Aunque no se realizó un seguimiento detallado durante la fase de construcción del nido, solo se observó a la hembra aportar material al nido. En todos los casos, el macho permaneció próximo a la hembra y, en ocasiones, cantó en una rama cercana mientras la hembra colocaba el material. Dos nidos (uno abierto y otro en un nido viejo de Asthenes baeri) fueron utilizados en dos ocasiones durante la estación reproductiva. En Saltatricula multicolor, el periodo de construcción del nido fue estimado en 8–9 días. También, una hembra de Carduelis magellanica construyó el nido en 9 días. Una observación casual de esta pareja copulando durante la fase de construcción del nido tuvo lugar 7 días antes de la puesta del primer huevo.
Tabla 2. Tipo y dimensiones del nido (en cm) de cinco especies de Emberizidae y Fringillidae que nidifican en la Reserva de Ñacuñán. Los datos se expresan como promedio ± error estándar, con el tamaño de muestra entre paréntesis. A: abierto, Ab: abandonado.

Saltator aurantiirostris nidificó en grandes plantas de atamisque (Tabla 3) o en chañar cerca de la zona de influencia de la estación biológica de Ñacuñán (i.e., a unos 100–200 m de distancia, pero en un área perturbada por acción humana). También utilizó plantas exóticas (e.g., Schinus molle) junto a construcciones humanas. Todos los nidos construidos por Diuca diuca (i.e., los nidos abiertos de tipo taza) se localizaron junto a la estación biológica, principalmente sobre algarrobos. Los nidos acondicionados de Asthenes baeri estaban situados en chañares de gran tamaño (Tabla 3), que es la disposición habitual de los nidos de esta especie de Furnariidae en Ñacuñán (Mezquida 2001). Zonotrichia capensis situó los nidos en el suelo, al pie de gramíneas en zonas abiertas junto a bordes de caminos, aunque en una ocasión utilizó una planta de chañar (Tabla 3). Los nidos de Carduelis magellanica se localizaron únicamente en los alrededores de la estación biológica sobre plantas exóticas y estructuras de origen humano. Por último, Saltatricula multicolor situó los nidos a baja altura, principalmente en plantas de atamisque y zampa (Tabla 3), aunque también nidificó sobre chañar (dos nidos), jarilla (dos nidos) y piquillín (un nido).
Tabla 3. Características del sitio de nidificación de cinco especies de Emberizidae y Fringillidae que nidifican en la Reserva de Ñacuñán. Se incluyen los nidos construidos sobre las plantas utilizadas con mayor frecuencia. Los datos se expresan como promedio ± error estándar. IP: índice de posición del nido.

La descripción de la coloración de los huevos de estas especies se puede encontrar en trabajos anteriores (e.g., Dinelli 1918, Smyth 1928, Pereyra 1937, Goodall et al. 1957, Mason 1985, de la Peña 1996). El ritmo de puesta de los huevos fue diario y el tamaño de puesta fue de 3–4 huevos (Tabla 4) en todas las especies. De los siete nidos de Diuca diuca en los que se pudo observar el contenido, tres (43%) tenían huevos (uno o dos) de Molothrus bonariensis. En Saltatricula multicolor, todas las puestas de cuatro huevos se realizaron en la temporada reproductiva de 1997-1998, por lo que el tamaño promedio de puesta en ese año (3.7 ± 0.2, n = 7) fue significativamente mayor que el de 1996-1997 y 1998-1999 (promedio para ambos años: 3.0 ± 0.0, n = 5; Mann-Whitney U-test, Z = 2.0, P < 0.05).
Tabla 4. Dimensiones y peso de los huevos, tamaño de puesta y duración de los periodos de incubación y de permanencia de los pollos de cinco especies de Emberizidae y Fringillidae que nidifican en la Reserva de Ñacuñán. Los datos se expresan como promedio ± error estándar, con el tamaño de muestra entre paréntesis.
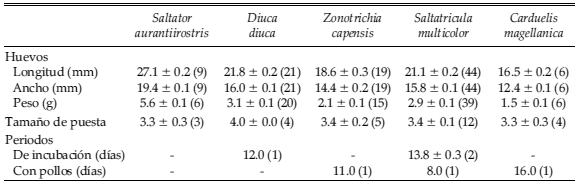
El periodo de incubación de los huevos se pudo calcular sólo para Diuca diuca y Saltatricula multicolor (Tabla 4). En Carduelis magellanica, la incubación y el cuidado inicial de los pollos fueron realizados por la hembra. Una vez que eclosionaron los huevos, ambos adultos de la pareja participaron en la alimentación de los pollos. En tres de las cinco especies se calculó la duración del periodo con pollos (Tabla 4).
En todos los casos, los pollos al eclosionar presentaban el pico naranja, amarillo (Saltator aurantiirostris) o gris (Saltatricula multicolor), con los bordes amarillo pálido y el paladar rojo. La piel era anaranjada o gris rojiza (Saltatricula multicolor), con plumón gris y patas anaranjadas. Durante el desarrollo, los pollos de Saltatricula multicolor incrementaron de peso gradualmente de 3.5 ± 0.2 g (n = 5 pollos de dos nidos) el día 0 (i.e., el día que eclosionó el huevo) a 10.5 ± 0.2 g (n = 5 pollos de dos nidos) el día 3 y 18.8 ± 0.8 g (n = 2 pollos de un nido) el día 7. Diuca diuca fue la única especie, de las cinco incluidas en este trabajo, en la que se observaron pollos con larvas de moscas parásitas (Philornis sp.). En Saltatricula multicolor, el número de volantones por nido activo fue de 0.5 ± 0.3 (n = 17), y por nido exitoso fue de 2.3 ± 0.5 (n = 4). Los nidos exitosos en 1997-1998 fueron algo más productivos (3.0 ± 0.0 volantones, n = 2) que los observados en 1996-1997 y 1998-1999 (1.5 ± 0.5, n = 2; un nido de cada temporada reproductiva).
Discusión
El periodo reproductivo de las especies de aves estudiadas coincide, a grandes rasgos, con el encontrado en otras áreas de Argentina y Chile (e.g., Dinelli 1918, Smyth 1928, Mason 1985, Lazo y Anabalón 1992, de la Peña 1996). De todas formas, hay que tener en cuenta que los datos para algunas especies, ya sea en Ñacuñán o en otras zonas, son muy escasos. También se observaron variaciones interanuales en el periodo de puesta en Diuca diuca. En esta especie, la fecha promedio de puesta fue más tardía en la temporada reproductiva de 1997-1998. En Saltatricula multicolor, las variaciones interanuales en la fecha de puesta no mostraron diferencias estadísticas. El patrón observado en esta especie no fue muy claro debido a la gran variabilidad registrada en 1996-1997 y al bajo tamaño de muestra, principalmente en 1996-1997 y 1998-1999. Saltatricula multicolor mostró un incremento en el tamaño de puesta durante la estación reproductiva de 1997-1998. Estas diferencias podrían estar relacionadas con las condiciones climáticas asociadas al fenómeno de El Niño de 1997-1998 (Jaksic 2001). En un estudio a largo plazo, Grant et al. (2000) observaron que en los años más lluviosos asociados a eventos de El Niño, los pinzones de Darwin (Geospiza spp.) presentaron una temporada de reproducción más prolongada, realizaron un mayor número de puestas y aumentaron el tamaño de puesta y la productividad de juveniles. Este incremento de la productividad se debió fundamentalmente a la mayor disponibilidad de alimento. En Ñacuñán, las fechas extremas de puesta para Diuca diuca y Saltatricula multicolor fueron similares entre años, pero en 1997-1998 la reproducción fue generalmente más intensa y hubo más puestas hacia el final de la estación reproductiva (ver también Mezquida 2002). La mayor cantidad de precipitaciones, asociada a El Niño de 1997-1998, provocó un aumento significativo en la disponibilidad de alimento (i.e., semillas; Marone et al. 2000), de forma tal que Saltatricula multicolor pareció responder con una mayor inversión en el número de huevos por puesta (ver también Murphy 1986, Rotenberry y Wiens 1991). La observación de una mayor productividad por nido exitoso en 1997-1998 comparada con los otros años sugiere que el incremento en el tamaño de puesta se tradujo en una mayor productividad. En cualquier caso, el número de nidos exitosos es anecdótico debido al bajo tamaño de muestra y a la alta tasa de mortalidad de los nidos (Mezquida y Marone 2001). Las variaciones observadas en el comportamiento reproductivo de Diuca diuca y Saltatricula multicolor son sugerentes y están en consonancia con lo encontrado para otras especies, entre ellas dos emberízidos, durante el mismo periodo de estudio en Ñacuñán (Mezquida 2002; Mezquida y Marone, datos no publicados). Sin embargo, el bajo número de nidos encontrados indica que hay que ser cauteloso con esta interpretación de los resultados, por lo que sería necesario realizar un estudio más detallado que incluyera años de condiciones meteorológicas contrastantes para analizar estos patrones de forma más confiable.
Goodall et al. (1957) y Lazo y Anabalón (1991) indicaron que Diuca diuca construye nidos abiertos de tipo taza en Chile. Sin embargo, Pereyra (1937) comentó que, en la provincia de La Pampa (Argentina), esta especie construye nidos de tipo taza o utiliza nidos de otras aves, sobre todo de furnáridos (ver también citas de nidos de Diuca diuca en nidos abandonados, en otras provincias de Argentina, en de la Peña 1983 y Salvador y Salvador 1984). En Ñacuñán, esta especie nidificó principalmente en nidos de furnáridos y los nidos abiertos de tipo taza se observaron únicamente junto a la estación biológica de la reserva. Mezquida y Marone (2001) mostraron, al nivel de ensamble, que los nidos situados junto a construcciones humanas presentaron una mayor tasa de supervivencia que los nidos localizados en los hábitats naturales de esta reserva. Además, Lazo y Anabalón (1991) encontraron que Diuca diuca presentaba un comportamiento reproductivo flexible, nidificando en arbustos no espinosos con gran densidad de follaje o en arbustos espinosos con escasas hojas. En este último caso, los nidos estaban cubiertos externamente con materiales espinosos. Estos autores sugirieron que ese patrón de nidificación estaba relacionado con una disminución del riesgo de depredación del nido. De igual manera, el comportamiento reproductivo de Diuca diuca en Ñacuñán parece estar relacionado con la presión de depredación, de forma tal que estas aves solo construyeron nidos abiertos en zonas con menor riesgo de depredación.
Diuca diuca parece ser comúnmente parasitada por Molothrus bonariensis en Chile y Argentina (Goodall et al. 1957, Salvador y Salvador 1984; R Fraga, com. pers.). Zonotrichia capensis también es habitualmente parasitada (Fraga 1978, 1983, de la Peña 1996). Además, en de la Peña (1996) se cita un nido de Saltator aurantiirostris con dos huevos parásitos de Molothrus bonariensis, y Salvador y Salvador (1984) y de la Peña (1996) mencionan un nido de Saltatricula multicolor con huevos de este parásito de nidos. En este estudio, solo se observaron algunos eventos de parasitismo en nidos abiertos de Diuca diuca situados junto a la estación biológica. Molothrus bonariensis es una especie poco abundante dentro de la Reserva de Ñacuñán, pero de presencia habitual junto a construcciones humanas (Lopez de Casenave 2001; Mezquida, obs. pers.). Por lo tanto, la incidencia de este parásito de nidos en Ñacuñán está prácticamente restringida a los alrededores de construcciones humanas, aunque también se ha observado algún caso de parasitismo en ambientes naturales de la reserva (Mezquida, datos no publicados).
Los sitios usados para nidificar fueron variables entre las especies estudiadas e, incluso, algunas mostraron cierta flexibilidad, por lo que es de esperar que muestren distintas respuestas ante las perturbaciones del hábitat. El pastoreo por ganado, una de las perturbaciones más extendidas en el desierto del Monte, no parece disminuir la cobertura de árboles y arbustos altos, pero sí la de arbustos no espinosos (Gonnet 2001), muy utilizados como lugar de nidificación por varias especies de granívoros en este área (ver también Mezquida 2000). Además, las perturbaciones del hábitat pueden modificar las tasas de mortalidad de los nidos, por ejemplo incrementando el riesgo de depredación o la incidencia de parasitismo por Molothrus bonariensis. La densidad poblacional de este parásito de nidos aumenta en las zonas alteradas (Milesi et al. 2002), por lo que es predecible un mayor impacto de esta especie en la productividad de sus anfitriones. Por lo tanto, las alteraciones del hábitat que afectan los requerimientos para la nidificación y el éxito reproductivo de las aves podrían constituir mecanismos potencialmente importantes, aunque escasamente estudiados, para explicar parte de las modificaciones observadas en las poblaciones de aves después de las perturbaciones (Gonnet 2001, Milesi et al. 2002).
Agradecimientos. Durante el desarrollo del trabajo en Argentina, el autor recibió una beca predoctoral del Instituto de Cooperación Iberoamericana (ICI) de España. Agradezco a L. Marone por su apoyo y dirección, y a I. Lazo, J. Lopez de Casenave, V. R. Cueto y F. Milesi por su ayuda y sugerencias. L. Marone revisó críticamente una versión previa de este manuscrito y dos revisores anónimos contribuyeron a mejorar una versión posterior. Contribución número 27 del Grupo de Investigación en Ecología de Comunidades de Desierto (Ecodes), UF&EV, IADIZA, Argentina.
Bibliografía Citada
Contreras JR (1979) Lista faunística preliminar de los vertebrados de la Reserva Ecológica de Ñacuñán. Cuaderno Técnico de IADIZA 5:39-47 [ Links ]
Dinelli L (1918) Notas biológicas sobre las aves del noroeste de la República Argentina. Hornero 1:57-68 [ Links ]
Dinelli L (1924) Notas biológicas sobre aves del noroeste de la Argentina. Hornero 3:253-258 [ Links ]
Fraga RM (1978) The Rufous-collared Sparrow as a host of the Shiny Cowbird. Wilson Bulletin 90:271-284 [ Links ]
Fraga RM (1983) Parasitismo de cría del Renegrido, Molothrus bonariensis sobre el Chingolo, Zonotrichia capensis: nuevas observaciones y conclusiones. Hornero Número extraordinario:245-255 [ Links ]
Gonnet JM (2001) Influence of cattle grazing on population density and species richness of granivorous birds (Emberizidae) in the arid plain of the Monte, Argentina. Journal of Arid Environments 48:569-579 [ Links ]
Goodall JD, Johnson AW y Philippi RA (1957) Las aves de Chile. Suplemento I. Platt Establecimientos Gráficos, Buenos Aires [ Links ]
Grant PR, Grant BR, Keller LF y Petren K (2000) Effects of El Niño events on Darwin's Finch productivity. Ecology 81:2442-2457 [ Links ]
Hartert E y Venturi S (1909) Notes sur les oiseaux de la République Argentine. Novitates Zoologicae 16:159-267 [ Links ]
Jaksic FM (2001) Ecological effects of El Niño in terrestrial ecosystems of western South America. Ecography 24:241-250 [ Links ]
Lazo I y Anabalón J (1991) Nesting of the Common Diuca finch in the central Chilean scrub. Wilson Bulletin 103:143-146 [ Links ]
Lazo I y Anabalón J (1992) Dinámica reproductiva de un conjunto de aves passeriformes de la sabana de espinos de Chile central. Ornitología Neotropical 3:57-64 [ Links ]
Lopez de Casenave J (2001) Estructura gremial y organización de un ensamble de aves del desierto del Monte. Tesis Doctoral, Universidad de Buenos Aires, Buenos Aires [ Links ]
Marone L (1992a) Estatus de residencia y categorización trófica de las especies de aves en la Reserva de la Biosfera de Ñacuñán, Mendoza. Hornero 13:207-210 [ Links ]
Marone L (1992b) Seasonal and year-to-year fluctuations of bird populations and guilds in the Monte desert, Argentina. Journal of Field Ornithology 63:294-308 [ Links ]
Marone L, Horno ME y González del Solar R (2000) Post-dispersal fate of seeds in the Monte desert of Argentina: patterns of germination in successive wet and dry years. Journal of Ecology 88:940-949 [ Links ]
Marone L, Lopez de Casenave J y Cueto VR (1997) Patterns of habitat selection by wintering and breeding granivorous birds in the central Monte desert, Argentina. Revista Chilena de Historia Natural 70:73-81 [ Links ]
Martin TE y Geupel GR (1993) Nest-monitoring plots: methods for locating nests and monitoring success. Journal of Field Ornithology 64:507-519 [ Links ]
Mason P (1985) The nesting biology of some passerines of Buenos Aires. Ornithological Monographs 36:954-972 [ Links ]
Mezquida ET (2000) Ecología reproductiva de un ensamble de aves del desierto del Monte central, Argentina. Tesis Doctoral, Universidad Autónoma, Madrid [ Links ]
Mezquida ET (2001) La reproducción de algunas especies de Dendrocolaptidae y Furnariidae en el desierto del Monte central, Argentina. Hornero 16:23-30 [ Links ]
Mezquida ET (2002) Nidificación de ocho especies de Tyrannidae en la Reserva de Ñacuñán, Mendoza, Argentina. Hornero 17:31-40 [ Links ]
Mezquida ET y Marone L (2001) Factors affecting nesting success of a bird assembly in the central Monte Desert, Argentina. Journal of Avian Biology 32:287-296 [ Links ]
Milesi FA, Marone L, Lopez de Casenave J, Cueto VR y Mezquida ET (2002) Gremios de manejo como indicadores de las condiciones del ambiente: un estudio de caso con aves y perturbaciones del hábitat en el Monte central, Argentina. Ecología Austral 12:149-161 [ Links ]
Morello J (1958) La Provincia Fitogeográfica del Monte. Opera Lilloana 2:1-155 [ Links ]
Murphy MT (1986) Temporal components of reproductive variability in Eastern Kingbirds (Tyrannus tyrannus). Ecology 67:1483-1492 [ Links ]
Nice MM (1954) Problems of incubation periods in North American birds. Condor 56:173-197 [ Links ]
Partridge WH (1953) Observaciones sobre aves de las provincias de Córdoba y San Luis. Hornero 10:23-73 [ Links ]
de la Peña M (1983) Notas nidobiológicas sobre Mistos y Diuca (Aves, Emberizidae), tercera parte. Historia Natural 3:33-38 [ Links ]
de la Peña M (1996) Ciclo reproductivo de las aves argentinas. Segunda parte. L.O.L.A., Buenos Aires [ Links ]
Pereyra JA (1937) Contribución al estudio y observaciones ornitológicas de la zona norte de la gobernación de La Pampa. Memorias del Jardín Zoológico de La Plata 7:197-326 [ Links ]
Reed CS (1919) Breves notas acerca de nidos y huevos de algunas aves de la cordillera de Mendoza. Hornero 1:267-273 [ Links ]
Rotenberry JT y Wiens JA (1991) Weather and reproductive variation in shrubsteppe sparrows: a hierarchical analysis. Ecology 72:1325-1335 [ Links ]
Salvador SA y Salvador LA (1984) Notas sobre hospedantes del Renegrido (Molothrus bonariensis) (Aves, Icteridae). Historia Natural 4:121-130 [ Links ]
Smyth CH (1928) Descripción de una colección de huevos de aves argentinas, II. Hornero 4:125-152 [ Links ]














