Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
El hornero
versión impresa ISSN 0073-3407versión On-line ISSN 1850-4884
Hornero v.18 n.2 Buenos Aires sept./dic. 2003
Notas sobre la conducta de crianza del Carpintero Bataraz Grande (Picoides lignarius) en el bosque lluvioso templado del sur de Chile
Ricardo A. Figueroa Rojas 1,2 y E. Soraya Corales Stappung 1
1 Estudios para la Conservación y Manejo de la Vida Silvestre Consultores. Blanco Encalada 350, Chillán, Chile.
2 asio@surnet.cl
Resumen
En el verano de 1995, durante tres días estudiamos la conducta de crianza de una pareja de Carpintero Bataraz Grande (Picoides lignarius) en el bosque lluvioso templado del sur de Chile. La pareja observada anidó en el interior de un tocón muerto de arrayán (Luma apiculata), en una franja de bosque ripario. La hembra hizo una mayor contribución a la alimentación de los pichones (78% del total de aportes de presa) en comparación con el macho (22%). Esta tendencia fue constante durante los tres días de observación. La hembra entregó las presas de manera exitosa en todas las ocasiones, mientras el macho fracasó el 57% de los intentos. El intervalo de tiempo promedio entre aportes de presa fue de 798 s. Las presas provistas fueron únicamente insectos, tanto larvas como imagos. Las presas más ofrecidas a los pichones fueron coleópteros, con larvas e imagos en proporción similar.
Palabras clave: alimentación, bosque lluvioso templado austral, Carpintero Bataraz Grande, crianza de pichones, Picoides lignarius.
Abstract
Notes on the chick-rearing behavior of the Striped Woodpecker (Picoides lignarius) in the temperate rainforest of southern Chile
During the summer of 1995, for three days we studied the chick-rearing behaviour of a Striped Woodpecker (Picoides lignarius) pair in the temperate rainforest of southern Chile. The pair nested in a Luma apiculata stump in a riparian forest strip. The female made a higher contribution to the feeding of chicks (78% of all prey deliveries) than the male (22%). This trend was constant during all three days. The female was always successful at feeding nestlings, while the male failed in 57% of their attempts. The mean time interval between prey deliveries was 798 s. The prey delivered were exclusively insects, both larvae and imagoes. The most frequent insect preys given to chicks were beetles, with larvae and imagoes in similar proportion.
Key words: chick rearing, feeding, Picoides lignarius, Southern temperate rainforest, Striped Woodpecker.
Recibido 11 septiembre 2003, aceptado 29 diciembre 2003
El Carpintero Bataraz Grande (Picoides lignarius) se distribuye ampliamente en Argentina y Chile, habitando principalmente en bosques y matorrales andino-patagónicos (Vuilleumier 1985, Fjeldså y Krabbe 1990). La historia natural de esta especie ha sido documentada solo de manera anecdótica y parcial (Housse 1945, Short 1970, 1982). En esta nota describimos las características de un nido y documentamos un breve estudio acerca de su conducta de crianza en un ambiente boscoso del sur de Chile.
El 20 de noviembre de 1995, durante un estudio de aves rapaces a lo largo de una franja de bosque nativo que bordea el estero Sagllúe en la localidad de Chahuilco (40°44'S, 75°09'O), 15 km al sur de Osorno, descubrimos un nido activo de Carpintero Bataraz Grande. Con el propósito de generar información sobre la biología reproductiva de esta especie, iniciamos las observaciones del nido a partir del mismo momento de su descubrimiento. Nuestros objetivos fueron: (1) describir las características del nido y su entorno, (2) evaluar la participación de los padres en la alimentación de los pichones, (3) evaluar la tasa de alimentación de los pichones, y (4) estimar la composición de la dieta de los pichones. Las observaciones se realizaron en tres visitas entre el 20 y el 29 de noviembre, totalizando 7.88 h de observación. Cuando iniciábamos el cuarto día de observación (30 de noviembre) encontramos abundantes plumas y restos de sangre en la base del tocón, y descubrimos que el nido estaba vacío. No fue posible, sin embargo, asociar la desaparición de los pichones a algún evento o factor en particular (e.g., depredación). Tal vez nuestra presencia pudo haber atraído a algún depredador al sitio, aunque también pudo haber sido simplemente un evento azaroso.
Para observar el nido nos ocultamos en un sitio con vegetación densa localizado a aproximadamente 4 m de distancia. Los registros de aporte de presas los hicimos mediante binoculares y las mediciones de tiempo fueron tomadas con un cronómetro estándar. Los sexos de ambos padres fueron distinguibles fácilmente por la diferencia de coloración en el plumaje de la cabeza (Araya y Millie 1986, Narosky e Yzurieta 1987). Para medir el tiempo entre aportes de presa, solo se consideraron los intentos de entrega en la entrada del nido, ya que en general los padres no llegaron directamente a ésta, sino que primero se posaron en los árboles cercanos, moviéndose de uno a otro lado o de rama en rama. La determinación de las presas se hizo visualmente, basándonos en nuestra experiencia y por comparación de nuestros dibujos con textos especializados (e.g., Apablaza 1994). Cuando iniciamos las observaciones, los dos pichones (número calculado sobre la base de sus vocalizaciones) ya recibían alimento en la entrada del nido, por lo que estimamos que su edad alcanzaba al menos dos semanas desde su eclosión (Kilham 1962). Considerando que la duración promedio de la crianza en el género Picoides es de 25 días (Yom-Tov y Ar 1993), nuestras observaciones habrían correspondido a la segunda mitad de este período.
El nido se encontró en el interior de un tocón muerto de arrayán (Luma apiculata) de 2.2 m altura, con un diámetro a la altura del pecho de 14 cm, levemente inclinado (15°). La entrada del nido consistió en un orificio circular de 4.7 cm de diámetro ubicado a 1.85 m del suelo. La profundidad del nido, medida después de la desaparición de los pichones, fue aproximadamente de 18–20 cm. El tocón estaba en un sitio relativamente protegido dentro de la delgada franja de bosque (15–20 m de ancho) en donde existía una vegetación arbustiva dispersa (Chusquea quila, Fuchsia magellanica, Drimys winteri, Myrceugenia exsucca, Blepharocalyx cruckshanksii). El estrato superior del bosque estaba conformado principalmente por roble (Nothofagus obliqua) y laurel (Laurelia sempervirens), los que, en promedio, alcanzaban una altura de 20–25 m.
Se detectó una diferencia notoria en la participación de los padres en la alimentación de los pichones. Del total de aportes de presa observados (n = 27), la hembra participó el 78% de las veces y el macho el 22%. Esta tendencia fue constante para los tres días de observación (Fig. 1). La hembra entregó las presas exitosamente en todos los arribos, y el macho sólo en el 43% de ellos. De las cuatro presas rechazadas al macho por los pichones, tres fueron larvas de lepidópteros. En uno de los arribos el macho fue insistente con una misma presa, intentando tres veces que fuera aceptada por los pichones, pero sin tener éxito. Considerando la participación de ambos padres, el intervalo de tiempo promedio (± EE) entre aportes de presa fue de 798 ± 144 s. La moda estadística fue de 180 s, y el rango mínimo y máximo fue de 40.2 s y 2580 s, respectivamente. Las presas aportadas a los pichones fueron únicamente insectos, tanto larvas como imagos. Los insectos entregados con mayor frecuencia fueron coleópteros, con larvas e imagos en proporción similar (Fig. 2).
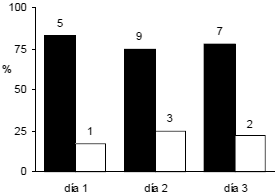
Figura 1. Porcentaje de arribos con presa para los pichones por parte de la hembra (barras negras) y el macho (barras blancas) de Carpintero Bataraz Grande (Picoides lignarius) durante tres días en el sur de Chile. Los números sobre las barras indican el número de observaciones de aporte de presas.
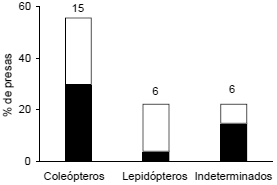
Figura 2. Composición de la dieta ofrecida a los pichones por parte de una pareja de Carpintero Bataraz Grande (Picoides lignarius) durante tres días en el sur de Chile. En negro se muestran los imagos y en blanco las larvas. Los números sobre las barras indican el número de observaciones de aporte de presas.
A excepción de su estado sanitario y su profundidad, las otras características físicas del nido de Chahuilco no fueron coincidentes con las características descriptas previamente por otros autores. Housse (1945) describió nidos con alturas superiores a los 2 m. En un bosque de lenga puro en Argentina, se ha encontrado que la altura promedio del nido y el diámetro promedio del sustrato pueden alcanzar 6.2 m (rango: 2.2–12 m) y 55.3 cm (rango: 31–54 cm), respectivamente (A Trejo, com. pers.). Johnson (1967) mencionó que los nidos del Carpintero Bataraz Grande son usualmente ubicados a alturas inferiores que los de otros carpinteros, pero no especificó las alturas. La profundidad del nido de Chahuilco coincide con aquella indicada por Housse (1945) para un nido encontrado en Chile central.
Debido al escaso conocimiento de la historia natural del Carpintero Bataraz Grande, nosotros no podemos explicar claramente la mayor participación y mayor éxito que tuvo la hembra con relación al macho en la entrega de presas a los pichones. Nuestros resultados pueden ser un artefacto producido por un tamaño de muestra muy pequeño. Sin embargo, si este éxito diferencial en la entrega de presas fuera una tendencia general para la especie, su explicación debería ser buscada en aspectos tales como diferencias en: (1) la selección del sustrato de alimentación (Ligon 1968, Jackson 1970, Kilham 1970, Koch et al. 1970, Short 1970, 1971, Willson 1970, Kisiel 1972, Austin 1976), (2) la técnica de alimentación (ver Selander 1966, Short 1970, Wallace 1974, Austin 1976), (3) la selección de presas, (4) la experiencia de vida o la edad de los individuos, (5) la condición física, o (6) la inversión parental durante las distintas etapas del ciclo reproductivo. Respecto de esto último, en varias ocasiones observamos al macho buscando alimento o moviéndose sobre árboles muy cercanos al nido, lo que sugiere que éste podría haber dado prioridad a la vigilancia del nido. Es posible, sin embargo, que nuestra presencia haya influido en la conducta del macho, obligándolo a permanecer alerta y, a la vez, causado un menor rendimiento en la provisión de presas. Aunque el Carpintero Bataraz Grande es descripta como la especie más generalista del género Picoides respecto de su alimentación (Short 1982), creemos que es necesario enfatizar estudios cuantitativos que aborden todos los aspectos mencionados arriba para conocer qué patrones conductuales dirigen sus decisiones tróficas y cómo éstas afectarían la calidad de la alimentación de los pichones.
Agradecimientos. Este estudio es parte del proyecto "Vida Silvestre en Paisajes Agrícolas", financiado con fondos privados. Agradecemos a Roberto Schlatter por darnos acceso a su literatura privada, a la familia Figueroa Ampuero por facilitarnos estadía y darnos su apoyo incondicional durante nuestro trabajo en el terreno, y a Diane Haughney por mejorar nuestro inglés. Los artículos de la revista Condor citados aquí fueron obtenidos desde el sitio http://www.cooper.org/. Los comentarios de Ana Trejo, Sergio Alvarado, Marcelo Saavedra y de dos revisores anónimos ayudaron a mejorar sustancialmente la versión final de esta nota.
Bibliografía Citada
Apablaza JU (1994) Introducción a la entomología general y agrícola. Manual de laboratorio. Ediciones Universidad Católica de Chile, Santiago [ Links ]
Araya B y Millie G (1986) Guía de campo de las aves de Chile. Editorial Universitaria, Santiago [ Links ]
Austin GT (1976) Sexual and seasonal differences in foraging of Ladder-backed Woodpeckers. Condor 78:317–323 [ Links ]
Fjeldså J y Krabbe N (1990) Birds of the high Andes. Apollo Books y Zoological Museum, Svendborg y Copenhagen [ Links ]
Housse R (1945) Las aves de Chile en su clasificación moderna: su vida y sus costumbres. Ediciones Universidad de Chile, Santiago [ Links ]
Jackson JA (1970) A quantitative study of the foraging ecology of Downy Woodpeckers. Ecology 51:318–323 [ Links ]
Johnson AW (1967) The birds of Chile and adjacent regions of Argentina, Bolivia and Peru. Volume 2. Platt Establecimientos Gráficos, Buenos Aires [ Links ]
Kilham L (1962) Reproductive behavior of Downy Woodpeckers. Condor 64:126–133 [ Links ]
Kilham L (1970) Feeding behavior of Downy Woodpeckers. I. Preferences for paper birches and sexual differences. Auk 87:544–556 [ Links ]
Kisiel DS (1972) Foraging behavior of Dendrocopos villosus and D. pubescens in eastern New York state. Condor 74:393–398 [ Links ]
Koch RF, Courchesne AE y Colling CT (1970) Sexual differences in foraging behavior of White-headed Woodpeckers. Bulletin of the South California Academy of Science 69:60–64 [ Links ]
Ligon JD (1968) Sexual differences in foraging behavior in two species of Dendrocopos woodpeckers. Auk 85:203–215 [ Links ]
Narosky T e Yzurieta D (1987) Guía para la identificación de las aves de Argentina y Uruguay. Asociación Ornitológica del Plata, Buenos Aires [ Links ]
Selander RK (1966) Sexual dimorphism and differential niche utilization in birds. Condor 68:113–151 [ Links ]
Short LL (1970) Notes on the habits of some Argentine and Peruvian Woodpeckers (Aves, Picidae). American Museum Novitates 2413 [ Links ]
Short LL (1971) Systematics and behavior of some North American woodpeckers, genus Picoides (Aves). Bulletin of the American Museum of Natural History 145:1–118 [ Links ]
Short LL (1982) Woodpeckers of the world. Delaware Museum of Natural History, Greenville [ Links ]
Vuilleumier F (1985) Forest birds of Patagonia: ecological geography, speciation, endemism, and faunal history. Ornithological Monographs 36:255–304 [ Links ]
Wallace RA (1974) Ecological and social implications of sexual dimorphism in five melanerpine woodpeckers. Condor 76:238–248 [ Links ]
Willson MF (1970) Foraging behavior of some winter birds of deciduous woods. Condor 72:169–174 [ Links ]
Yom-Tov Y y Ar A (1993) Incubation and fledging durations of woodpeckers. Condor 95:283–287 [ Links ]














