Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Archivos argentinos de pediatría
Print version ISSN 0325-0075
Arch. argent. pediatr. vol.109 no.2 Buenos Aires Mar./Apr. 2011
PRESENTACIÓN DE CASOS CLÍNICOS
Taquicardia auricular focal incesante originada en la orejuela derecha: riesgo de taquicardiomiopatía.
Rol de la ablación por radiofrecuencia
Incessant focal atrial tachycardia arising from the right appendage: risk of tachycardia mediated cardiomyopathy. Role of the radiofrequency ablation
Dr. Francisco Femeníaa, Dr. Mauricio Arcea, Tec. Martín Arrietaa y Dr. Adrián Baranchukb
aUnidad de Arritmias. Departamento de Cardiolog ía. Hospital Español de Mendoza. Argentina.
bArrhythmia Service, Kingston General Hospital, Queen's University, Kingston, Ontario, Canadá.
Correspondencia: Dr. Francisco Femenía femeniafavier@hotmail.com
Conflicto de intereses: Ninguno que declarar.
Recibido: 27-9-10
Aceptado: 17-11-10
RESUMEN
Las taquicardias auriculares focales pueden originarse en distintas regiones de la aurícula derecha, incluidos la crista terminalis, el anillo tricuspídeo, el septum interauricular y la orejuela derecha. Las originadas en esta última región anatómica se caracterizan por presentar un comportamiento incesante y mala respuesta al tratamiento farmacológico antiarrítmico, con desarrollo de taquicardiomiopatía; su tratamiento de elección es la ablación por radiofrecuencia. Presentamos el caso de una infante de 36 meses de edad, con taquicardiomiopatía secundaria a taquicardia auricular incesante de orejuela derecha, a quien se le realizó ablación por radiofrecuencia.
Palabras clave: Taquicardia auricular incesante; Disfunción ventricular izquierda; Taquicardiomiopatía; Ablación por radiofrecuencia.
SUMMARY
Focal atrial tachycardias originate from different anatomic regions of the right atrium including the crista terminalis, the coronary sinus ostium, the tricuspid annulus, the interatrial septum and the right atrial appendage. The latter are characterized by being incessant and presenting poor response to antiarrhythmic treatment. They frequently evolve into tachycardiomyopathy and radiofrequency ablation is the treatment of choice. We present the case of a 36 month old girl with tachycardiomyopathy as a result of an incessant atrial tachycardia originated in the right atrial appendage. Patient underwent radiofrequency ablation.
Key words: Incessant atrial tachycardia; Left ventricular dysfunction; Tachycardiomyopathy; Radiofrequency ablation.
INTRODUCCIÓN
Las taquicardias auriculares focales (TAF) originadas en la orejuela auricular derecha (OAD) suelen desarrollarse espontáneamente en niños y jóvenes, con un comportamiento incesante y mala respuesta al tratamiento farmacológico, con desarrollo de taquicardiomiopatía. El tratamiento de elección es la ablación por radiofrecuencia, pero por las características anatómicas de la OAD, la utilización de catéteres estándar puede no ser suficiente para la eliminación de focos automáticos. 1-4
Presentamos un caso donde discutimos el procedimiento de ablación por radiofrecuencia.
CASO CLÍNICO
Paciente femenino de 36 meses de edad y 12 kg de peso, sin antecedentes patológicos previos, internada por edema agudo de pulmón, luego de 48 h de crisis de palpitaciones de aparición súbita. Ingresa en mal estado general, que requiere asistencia respiratoria mecánica (ARM) y soporte con inotrópicos, diuréticos y vasodilatadores. La radiografía de tórax evidencia cardiomegalia con edema bilateral; serología para echovirus, coxsackie virus y Chagas negativa. Hormonas tiroideas, enzimas cardíacas y troponina normales. El ecocardiograma transtorácico demuestra cardiopatía dilatada con hipoquinesia global difusa, insuficiencia mitral leve-moderada y deterioro grave de la función ventricular izquierda (fracción de eyección: 35%, fracción de acortamiento: 20%). En el ECG se observa una taquicardia regular con QRS angosto, con una frecuencia cardíaca de 215-220 latidos/min, y ondas P auriculares con una frecuencia de aproximadamente 320 ms y polaridad negativa en V1 y V2, lo cual sugiere un origen en OAD (Figura 1). Para intentar definir el mecanismo electrofisiológico se realizó adenosina IV 6 mg en bolo, observándose reversión transitoria de la taquicardia, con fenómeno de calentamiento ("warm-up") y reinicio posterior, lo cual sugiere una taquicardia auricular automática (Figura 2). Dada la ausencia de otros factores reversibles causantes de cardiopatía dilatada, se asumió el cuadro clínico como una taquicardiomiopatía grave y se inició tratamiento farmacológico antiarrítmico con amiodarona (10 mg/kg de carga y 5 mg/kg/día de mantenimiento), digital (10 μg/kg/día) y esmolol (200 μg en dosis de carga y 100 μg/kg/día de mantenimiento). Luego de 24 h de iniciado el tratamiento, al no conseguirse el control de la taquiarritmia se deriva a nuestro servicio para el mapeo electrofisiológico y ablación por radiofrecuencia.

Figura 1. ECG de 12 derivaciones durante la internación de la paciente
Taquicardia regular con QRS angosto, frecuencia cardíaca de 215-220 latidos/min, ondas P auriculares con una frecuencia de aproximadamente 320 ms con polaridad negativa en V1 y V2, sugiriendo origen en orejuela auricular derecha.

Figura 2. Tira de ritmo en derivación II. Prueba de adenosina
Durante la infusión de adenosina 6 mg en bolo endovenoso, a los pocos segundos se observa fenómeno de enfriamiento o cool-down previo al bloqueo a nivel del nodo aurículo ventricular, con la aparición de dos ondas P, con un intervalo de aproximadamente 240 ms y reversión transitoria de la taquicardia. Desaparecido el efecto de la adenosina, se evidencia claramente el fenómeno de calentamiento o warm-up, con reinicio de la taquicardia, lo cual confirma un mecanismo de automaticidad aumentada.
Estudio electrofisiológico y ablación por radiofrecuencia
El procedimiento se realizó bajo sedación profunda en ARM y manejo de la vía aérea asistida por anestesiólogo. Previa antisepsia de la piel, bajo anestesia local (lidocaína al 2%), por técnica de Seldinger, se realizó venopunción femoral derecha y se introdujeron, consecutivamente, dilatadores de 4, 5, 6 y 7 F para evitar el traumatismo venoso. Con un catéter 6 F y punta dirigible de 4 mm (Celsius®, Cordis, Biosense Webster) realizamos el mapeo y posterior ablación. Para la reconstrucción electroanatómica utilizamos el sistema de mapeo en 3D NavX (EnSite, St. Jude Medical) tomando, como referencia fija, un parche ubicado en la región abdominal de la paciente. Las aplicaciones de radiofrecuencia se realizaron con un equipo Stockert 100 EP-Shuttel (Biosense Webster, Johnson & Johnson). El mapeo electroanatómico confirmó el origen de la taquicardia en la OAD, con un área de mayor precocidad en la región basal (Figura 3). En esta área se realizaron aplicaciones de radiofrecuencia, con T° de 55°C y potencia de entre 25 y 50 vatios (W). Luego de varias aplicaciones sin éxito, se rotó a un catéter 7 F, irrigado abierto, con punta de 5 mm (Celsius® Thermo-Cool, Cordis, Biosense Webster), el cual presenta la ventaja de que, al refrigerarse la punta con solución salina, disminuye la resistencia de la interfaz catéter-tejido y produce lesiones amplias y profundas. Sin embargo, dado su especial diseño (extremo distal muy rígido), la manipulación de este catéter, en la OAD, fue extremadamente dificultosa, por lo que se decidió utilizar un catéter 7 F con punta de 8 mm (Celsius® DS, Cordis, Biosense Webster), el cual, al presentar su extremo distal muy maleable, nos permitió posicionarlo fácilmente en el área de mayor precocidad auricular y con una sola aplicación con 60°C y 70 W; a los pocos segundos, se observó la aceleración de la taquicardia y su posterior reversión a ritmo sinusal (Figura 4A), completando 60 segundos de aplicación. Posteriormente, bajo infusión con isoproterenol (1-2 μg/min) no se indujeron extrasístoles auriculares ni taquicardia, y con trenes de estimulación auricular, no se evidenció otro mecanismo electrofisiológico que indujese alguna arritmia. Transcurridos 60 minutos y al mantenerse en ritmo sinusal, se dio por finalizado el procedimiento sin complicaciones. (Figura 4B)

Figura 3. Reconstrucción electroanatómica con sistema no-fluoroscópico en 3D
A: reconstrucción anatómica de la aurícula derecha, venas cavas, anillo tricuspídeo y región del haz de His. B: mapa de activación durante la taquicardia, tomando como referencia para el mapeo de activación la onda p del ECG de superficie (recuadro C) y el registro intracavitario de la actividad auricular. Mediante un sistema arbitrario de colores, se reproduce el circuito de activación desde el blanco (región de mayor precocidad) hasta el violeta y azul (región más tardía) pasando por zonas intermedias teñidas de color rojo y amarillo. Obsérvese que la región de mayor precocidad se obtiene en la región de la base de la orejuela derecha (forma triangular) y desde ahí el circuito de extiende al resto de la aurícula, lo cual coincide con la obtención del electrograma más precoz (recuadro D). Durante la manipulación del catéter mapeador y por contacto mecánico en la región del haz de His, se produce un bloqueo aurículo ventricular transitorio, evidenciándose claramente la actividad auricular (recuadro e - flechas rojas).
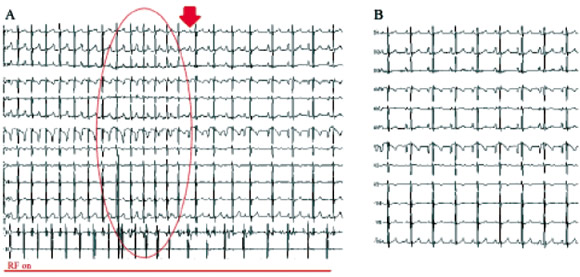
Figura 4. Ablación por radiofrecuencia
A: durante la taquicardia auricular, con el catéter punta de 8 mm, se inicia la aplicación de radiofrecuencia (RF on) en la región de mayor precocidad obtenida luego del mapeo electroanatómico, evidenciándose a los pocos segundos la inestabilidad eléctrica del circuito (círculo rojo), previo a su desaparición con posterior reversión a ritmo sinusal (flecha). B: ECG en ritmo sinusal, luego de la ablación por radiofrecuencia y bajo infusión con isoproterenol.
La paciente mejoró su estado clínico y fue dada de alta al séptimo día, en buen estado general, con ritmo sinusal y función cardíaca normalizada. Al momento del informe no ha presentado recurrencias.
DISCUSIÓN
La OAD ha sido caracterizada como un sitio infrecuente de origen de TAF incesantes, especialmente en la población adulta.1-3 Recientemente, Toyohara y cols.,4 en un análisis retrospectivo de una serie consecutiva de 35 niños con TAF incesante, sin cardiopatía estructural y de aparición espontánea, demostraron que el sitio más frecuente de localización de la taquicardia fue la OAD (9,25%). El 28% de los pacientes, presentó taquicardiomiopatía con grave deterioro de la función ventricular izquierda (intervalo de fracción de eyección: 20-27%). En todos los pacientes de esta serie se demostró un mecanismo de automaticidad aumentada y en ningún caso la taquicardia pudo ser iniciada o suprimida con estimulación auricular programada; el uso de adenosina (ATP) produjo reversión transitoria de la taquicardia con fenómenos de enfriamiento (cooldown) y calentamiento (warm-up) característicos de este tipo de mecanismo, como en nuestro caso. El mecanismo electrofisiológico de la mayoría de las TAF pueden ser actividad gatillada o incremento de la automaticidad y son poco frecuentes las relacionadas con microreentradas o macroreentradas. La utilización de ATP puede ayudar a diferenciar estos mecanismos electrofisiológicos. En las TAF sensibles a la ATP, donde el mecanismo es la actividad gatillada, la ATP suele revertir la taquicardia por acción directa sobre el AMPc y disminución de la concentración del calcio intracelular, a diferencia de cuando existe automaticidad aumentada, donde se produce una reversión transitoria de la taquicardia con reinicio posterior, y cuyo mecanismo se encuentra relacionado con una hiperpolarización del potencial de acción transmembrana.5-7
Con respecto a la OAD, su particular anatomía presenta desafíos específicos durante la ablación con catéteres. La naturaleza pectínea con múltiples trabeculaciones, especialmente en la base (zona de implante) de la orejuela, el escaso grosor del vértice y el flujo sanguíneo disminuido, se han relacionado con fracasos del procedimiento ablativo al dificultarse el correcto contacto electrodotejido. Esto conduce a una inadecuada liberación de energía y potenciales complicaciones graves, como la perforación y el taponamiento cardíaco, relacionadas especialmente con la manipulación del catéter, la potencial carbonización del tejido o la profundidad de la lesión producida por la radiofrecuencia. 1-3,8,9
En el caso descripto, por la gravedad del cuadro clínico, se planificó el procedimiento intentando una aproximación de localización de la TAF, a través de distintos algoritmos que utilizan la polaridad de la onda P del ECG.10-13 Mediante una aproximación simplificada con un solo catéter estándar y con el soporte del sistema de navegación en 3D, se pudo realizar una adecuada reconstrucción anatómica y eléctrica de la OAD.15
En condiciones hemodinámicas favorables, existen maniobras específicas (encarrilamiento de la taquicardia, medición del ciclo de retorno posestimulación) que pueden ayudar a determinar el origen y confirmar el mecanismo de la taquicardia, 16,17 pero, dado el compromiso clínico de la infante y al contar con el mapa de activación del sistema de navegación, se identificó el sitio de activación más precoz para liberar radiofrecuencia con el objetivo de terminar la taquicardia lo más rápido posible. Durante la manipulación del catéter, al colocar la referencia del haz de His por contacto mecánico directo se produjo bloqueo AV transitorio, lo cual permitió confirmar la morfología y polaridad de las ondas P; asimismo, la ausencia de relación AV 1:1 permitió descartar un mecanismo de reentrada, con la participación necesaria para el mantenimiento de la taquicardia, del nodo AV o de una vía accesoria. (Figura 3E)
El mapa de activación obtenido muestra claramente que la zona de mayor precocidad se encontraba en la zona de implante de la OAD. Como está descripto en la bibliografía,1-3,9 no se logró un adecuado contacto con el catéter estándar; esta situación se facilitó con el electrodo de mayor superficie, con obtención de la temperatura y la potencia necesarias para eliminar el foco automático y suprimir la taquicardia.
Van Hare et al.,18 en un estudio prospectivo y multicéntrico, con más de 2500 pacientes pediátricos a quienes se les realizó ablación por radiofrecuencia de taquiarritmias supraventriculares, comunicaron una elevada tasa de éxito (95,7%) con baja incidencia de complicaciones (~4%), ninguna fatal. En el caso específico de pacientes con TAF, el éxito primario fue del 92%, con similar índice de complicaciones que en toda la serie. Estos resultados son comparables con otros registros anteriores.3,19
Como conclusión, la ablación por catéteres en la población pediátrica es una alternativa terapéutica segura, eficaz y curativa en la mayoría de las taquiarritmias supraventriculares, pero es necesario arbitrar todos los medios para disminuir el riesgo de complicaciones graves, en pacientes pequeños y con grave deterioro de la función ventricular izquierda.
1. Roberts-Thomson KC, Kistler PM, Haqqani HM, McGavigan AD et al. Focal atrial tachycardias arising from the right atrial appendage: electrocardiographic and electrophysiologic characteristics and radiofrequency ablation. J Cardiovasc Electrophysiol 2007; 18(4):367-72. [ Links ]
2. Freixa X, Berruezo A, Mont L, Magnani S, et al. Characterization of focal right atrial appendage tachycardia. Europace 2008; 10(1):105-9. [ Links ]
3. Roberts-Thomson K, Kistler PM, Kalman JM. Focal atrial tachycardia II: management. Pacing Clin Electrophysiol 2006; 29(7):769-78. [ Links ]
4. Toyohara K, Fukuhara H, Yoshimoto J, Ozaki N, Nakamura Y. Electrophysiologic studies and radiofrequency catheter ablation of ectopic atrial tachycardia in children. Pediatr Cardiol 2010 (En prensa). [ Links ]
5. Wellens HJ. Twenty-five years of insights into the mechanisms of supraventricular arrhythmias. J Cardiovasc Electrophysiol 2003; 14(9):1020-25. [ Links ]
6. Markowitz SM, Nemirovsky D, Stein KM, Mittal S et al. Adenosine-insensitive focal atrial tachycardia: evidence for de novo micro-re-entry in the human atrium. J Am Coll Cardiol 2007; 49(12):1324-33. [ Links ]
7. Weber R, Letsas K, Arentz T, Kalusche D. Adenosine sensitive focal atrial tachycardia originating from the noncoronary aortic cusp. Europace 2009; 11(6):823-6. [ Links ]
8. Walsh EP, Saul JP, Hulse JE, Rhodes LA, et al. Transcatheter ablation of ectopic atrial tachycardia in young patients using radiofrequency current. Circulation 1992; 86(4):1138-46. [ Links ]
9. Anguera I, Brugada J, Roba M, Mont L, et al. Outcomes after radiofrequency catheter ablation of atrial tachycardia. Am J Cardiol 2001; 87(7):886-90. [ Links ]
10. Zimerman LI, Shenasa H, Sorrentino. Utility of p-wave morphology on predicting site of right atrial tachycardia. Pacing Clin Electrophysiol 1995; 18:861. [ Links ]
11. Tang CW, Scheinman MM, Van Hare GF, Epstein LM, et al. Use of P wave configuration during atrial tachycardia to predict site of origin. J Am Coll Cardiol 1995; 26(5):1315-24. [ Links ]
12. de Voogt WG, van Mechelen R, van den Bos A, Scheffer M, et al. Electrical characteristics of low atrial septum pacing compared with right atrial appendage pacing. Europace 2005; 7(1): 60-6. [ Links ]
13. Kistler PM, Roberts-Thomson KC, Haqqani HM, Fynn SP et al. P-wave morphology in focal atrial tachycardia: development of an algorithm to predict the anatomic site of origin. J Am Coll Cardiol 2006; 48(5):1010-7. [ Links ]
14. Higa S, Tai CT, Lin YJ, Liu TY, et al. Focal atrial tachycardia. New insight from noncontact mapping and catheter ablation. Circulation 2004; 109(1):84-91. [ Links ]
15. Tracy CM, Swartz JF, Fletcher RD, Hoops HG et al. Radiofrequency catheter ablation of ectopic atrial tachycardia using paced activation sequence mapping. J Am Coll Cardiol 1993; 21(4):910-7. [ Links ]
16. Micahud GF, Morady F. An excellent refinement of the postpacing interval-tachycardia cycle length (PPI-TCL) and stimulus atrial-ventriculoatrial (SA-VA) criteria. Heart Rhythm 2006; 3(9):1114-5. [ Links ]
17. González-Torrecilla E, Arenal A, Atienza F, Osca J et al. First postpacing interval after tachycardia entrainment with correction for atrioventricular node delay: a simple maneuver for differential diagnosis of atrioventricular nodal reentrant tachycardias versus orthodromic reciprocating tachycardias. Heart Rhythm 2006; 3(6):674-9. [ Links ]
18. Van Hare GF, Javitz H, Carmelli D, Saul JP, et al. Prospective assessment after pediatric cardiac ablation: demographics, medical profiles, and initial outcomes. J Cardiovasc Electrophysiol 2004; 15(7):759-770. [ Links ]
19. Lee PC, Hwang B, Chen SA, Tai CGT, et al. The results of radiofrequency catheter ablation of supraventricular tachycardia in children. Pacing Clin Electrophysiol 2007; 30(5):655-661. [ Links ]














