Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos argentinos de pediatría
versión impresa ISSN 0325-0075
Arch. argent. pediatr. vol.112 no.5 Buenos Aires oct. 2014
http://dx.doi.org/10.5546/aap.2014.413
ARTÍCULO ORIGINAL
http://dx.doi.org/10.5546/aap.2014.413
Situación epidemiológica de coqueluche y estrategias para su control. Argentina, 2002-2011
Dra. Viviana Romanina, Lic. Vanina Agustinhoa, Dra. Gloria Califanoa, Dra. Sandra Sagradinia, Lic. Analía Aquinoa, Dra. María del Valle Juáreza, Lic. Julián Antmanb, Lic. Carlos Giovacchinib, Dr. Marcelo Galasc, Bioq. Claudia Larac,Dra. Daniela Hozbord, Dra. Ángela Gentilee y Dra. Carla Vizzottia
a. Programa Nacional de Control de Enfermedades Inmunoprevenibles (ProNaCEI), Ministerio de Salud de la Nación, Argentina.
b. Dirección de Epidemiología, Ministerio de Salud de la Nación, Argentina.
c. Laboratorio Nacional de Referencia de Pertussis, INEI-ANLIS "Dr. Carlos G. Malbrán".
d. Laboratorio Nacional de Referencia Coqueluche, VacSal, Instituto de Biotecnología y Biología Molecular. Facultad de Ciencias Exactas. Universidad Nacional de La Plata.
e. Sociedad Argentina de Pediatría.
Correspondencia: Dra. Viviana Romanin: vivianaromanin@gmail.com
Conflicto de intereses: Ninguno que declarar.
Recibido: 25-2-2014
Aceptado: 5-6-2014
RESUMEN
Introducción. Coqueluche constituye un problema de salud pública. Objetivos: Describir la morbimortalidad y coberturas de vacunación entre 2002 y 2011, el perfil de los casos de 2011 y las estrategias de control implementadas por el Ministerio de Salud (MSN).
Métodos. Estudio descriptivo de vigilancia epidemiológica. Los datos de morbilidad se tomaron del Sistema Nacional de Vigilancia, y los de mortalidad, de la Dirección de Estadística e Información en Salud del MSN y de los informes oficiales de las jurisdicciones. Se utilizó la cobertura administrativa de vacunación a partir de datos provistos por las jurisdicciones al MSN. Se analizó con Epiinfo 7.1.2.
Resultados. Entre 2002 y 2011, la notificación de casos de coqueluche y de fallecimientos se incrementó y alcanzó los mayores valores en 2011: tasa de 16 x 100 000 habitantes y 76 fallecidos. Las muertes ocurrieron mayoritariamente en <1 año y las coberturas nacionales de vacunación para 3ra dosis e ingreso escolar fueron >90% y para el primer refuerzo, 80-90%. En 2011, se notificaron 2821 casos confirmados (incidencia 7 x 100 000 hab.): 84% <1 año; 76 fallecidos: 97% <1 año (60,5% <2 meses). Entre las estrategias implementadas, se consolidaron 906 nodos clínicos y 405 de laboratorio; se implementaron la reacción en cadena de la polimerasa como método diagnóstico y la clasificación diferencial de los casos, y se incorporaron dosis adicionales de vacunación.
Conclusiones
• Entre 2002 y 2011, aumentaron los casos de coqueluche; la mayor morbimortalidad fue en <1 año, con coberturas de vacunación de 80 y 90%.
• El mayor número de fallecidos por coqueluche fue en el año 2011.
• El MSN fortaleció la vigilancia epidemiológica y orientó las medidas de control.
Palabras clave: Coqueluche; Vigilancia epidemiológica; Vacunación antipertussis.
INTRODUCCIÓN
Coqueluche es una enfermedad respiratoria aguda altamente contagiosa causada por la bacteria Bordetella pertussis. La inmunización universal con vacuna antipertussis en los niños menores de 7 años es crítica para el control de la enfermedad.1 Sin embargo, aun en países con altas coberturas de vacunación, constituye un problema de salud pública. Se han hecho grandes esfuerzos a nivel mundial para lograr avances en la notificación, el diagnóstico y la prevención. La mayoría de los casos se describen en menores de 6 meses, quienes presentan mayor frecuencia de hospitalización, complicaciones y muerte.1-4 Es una enfermedad endemoepidémica, con brotes cada 3-5 años. Según estimaciones de la Organización Mundial de la Salud, en el año 2008, ocurrieron en el mundo 16 millones de casos (95%, en países en desarrollo) y se registraron 195 000 muertes.5
Este estudio tiene como objetivos describir la evolución de la morbimortalidad por coqueluche y de las coberturas de vacunación antipertussis en el decenio 2002-2011, caracterizar el perfil epidemiológico de los casos del año 2011 y describir las estrategias de control implementadas por el Ministerio de Salud de la Nación (MSN) durante ese período.
MÉTODOS
Estudio descriptivo observacional de vigilancia epidemiológica.
Datos de morbilidad: se tomaron del Sistema Nacional de Vigilancia de la Salud de Argentina (SNVS), que recibe las denuncias de las enfermedades de notificación obligatoria (Ley 15465), entre ellas coqueluche. El SNVS es una red que conecta de manera oportuna a los distintos efectores que se encuentran distribuidos en las 24 jurisdicciones (23 provincias y la Ciudad Autónoma de Buenos Aires), quienes comparten e intercambian información. La red internet es el soporte comunicacional del sistema, con datos alojados en servidores centrales. El software del SNVS es concebido de manera modular; para la notificación de coqueluche, hay dos módulos: clínico (C2) y de laboratorio (SIVILA). Ambos recogen información de distintas fuentes: C2, la procedente de la consulta médica (externa, guardia o internación), y SIVILA, la producida por los laboratorios que obtienen, derivan o estudian muestras. La población fueron los casos notificados al SNVS entre el 1 de enero de 2002 y el 31 de diciembre de 2011. Entre 2002 y 2011, se analizó la morbilidad mediante la notificación de casos en el módulo C2, mientras que, para el análisis de los casos confirmados de 2011, se integraron las bases de C2 y SIVILA mediante el algoritmo recomendado por el MSN.6-8
Datos de mortalidad: se obtuvieron de la Dirección de Estadística e Información en Salud (DEIS) del MSN y, en el año 2011, se utilizaron además informes oficiales de las provincias.9
Las definiciones y clasificaciones de caso fueron las recomendadas por el MSN (véase el Anexo en formato electrónico).6,1012
Para los cálculos de tasas, se emplearon los datos de población de los Censos 2001 y 2010 del Instituto Nacional de Estadística y Censos según correspondiera. Para el cálculo de las coberturas de vacunas, se utilizó la cobertura administrativa (cociente entre el número de dosis aplicadas y el número de población para vacunar por cien), a partir de datos provistos por las jurisdicciones al Programa Nacional de Control de Enfermedades Inmunoprevenibles (ProNaCEI) del MSN.
Para la detección en el laboratorio de las infecciones causadas por Bordetella pertussis, se emplearon técnicas microbiológicas (cultivo) y moleculares basadas en la reacción en cadena de la polimerasa (PCR) en aspirado (muestras de elección) o hisopados nasofaríngeos que se realizan en laboratorios ubicados en diferentes jurisdicciones del país. El algoritmo de trabajo fue el recomendado por los dos Laboratorios Nacionales de Referencia (LNR), Laboratorio
VacSal de la Facultad de Ciencias Exactas de la Universidad Nacional de La Plata y el Instituto Nacional de Enfermedades Infecciosas - ANLIS "Dr. Carlos G. Malbrán", según recomendaciones de la OMS y los Centros para el Control y Prevención de Enfermedades de Estados Unidos (CDC). Los ensayos serológicos se realizan en el Instituto Nacional de Enfermedades Infecciosas - ANLIS "Dr. Carlos G. Malbrán".
Para el cultivo, se emplearon los medios ReganLowe y BordetGengou suplementados con sangre de caballo o de carnero (10-15% v/v) y en placas con y sin el agregado de cefalexina, en concentración de 40 ug/ml. Las placas sembradas con las secreciones de los pacientes se visualizaron hasta transcurridos 10 días de incubación antes de considerarlas como negativas.13 Para el diagnóstico molecular, se emplearon las reacciones de PCR de punto final (PCR convencional) y/o reacciones de PCR en tiempo real. Para detectar la presencia de ADN de B. pertussis por PCR de punto final, se utilizaron como secuencias blanco a la secuencia de inserción IS481 y al promotor del gen de la toxina pertussis (ptx).14,15 En la PCR tiempo real, se realizó un ensayo multiplex y uno singleplex según la plataforma puesta a punto por los CDC.16 En el diagnóstico por serología, se evaluaron los títulos de anticuerpos anti-Bordetella spp mediante ELISA (que emplea dos muestras de suero tomadas con un intervalo de 21 días), y se consideró una diferencia de dos o más títulos entre ambas muestras de suero como resultado positivo.
Los datos fueron analizados mediante Epiinfo 7.1.2.
RESULTADOS
Datos epidemiológicos de 2002-2011
La notificación de casos sospechosos mostró una tendencia ascendente, que alcanzó la mayor tasa en 2011: 16 x 100 000 habitantes (Figura 1). El mayor número de fallecimientos asociados a la enfermedad se registró en 2011 y todas las muertes ocurrieron en el grupo de menores de 1 año, excepto cinco casos, que ocurrieron en el grupo de 1-4 años (3), 25-34 años (1) y mayor de 75 años (1) (Figura 2).

Figura 1. Notificación de coqueluche y coberturas de vacunas seleccionadas. Argentina, 2002-2011
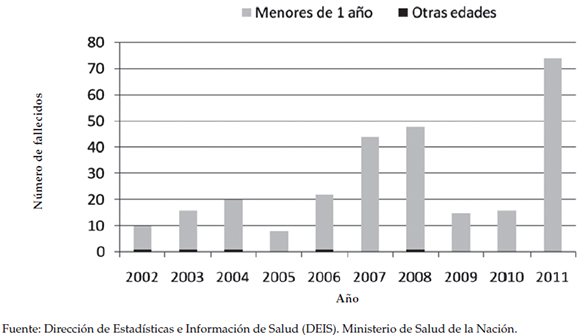
Figura 2. Fallecimientos asociados a coqueluche. Argentina, 2002-2011
Coberturas nacionales de vacunación antipertussis de 2002-2011
La 3ra dosis y la de ingreso escolar estuvieron por encima del 90%, mientras que el refuerzo de los 18 meses presentó coberturas de entre 80 y 90% (Figura 1). El refuerzo de los 11 años, incluido en el Calendario desde 2009, tuvo una cobertura del 54,6% y del 72,8% en los años 2010 y 2011, respectivamente.
Datos epidemiológicos de los casos confirmados de 2011
Se notificaron 10 395 casos sospechosos; se clasificaron como confirmados 2821 (27%); 1928 tuvieron pruebas de laboratorio positivas y 893 se confirmaron por el módulo clínico. Los casos confirmados se registraron en todas las semanas del año, con aumento a partir de la semana epidemiológica (SE) 36. El mínimo de casos (17) se registró en la SE 19 y el máximo (107), en las SE 44 y 45. La mediana de notificación semanal fueron 46 casos. El 99% (2784) tenía registrada la edad: el 84% eran menores de 1 año; el 54%, menores de 4 meses; y el 21%, menores de 2 meses (Figura 3). La tasa de incidencia fue de 7 x 100 000 habitantes, mientras que la correspondiente a los menores de 1 año fue de 344 x 100 000 (Tabla 1). La distribución por sexo fue similar: 51% de mujeres.

Figura 3. Casos y tasas de incidencia de coqueluche por grupo de edad. Argentina, 2011
Tabla 1. Casos, tasas de incidencia de coqueluche (general y <1 año) y coberturas de vacunación por provincia. Argentina, 2011
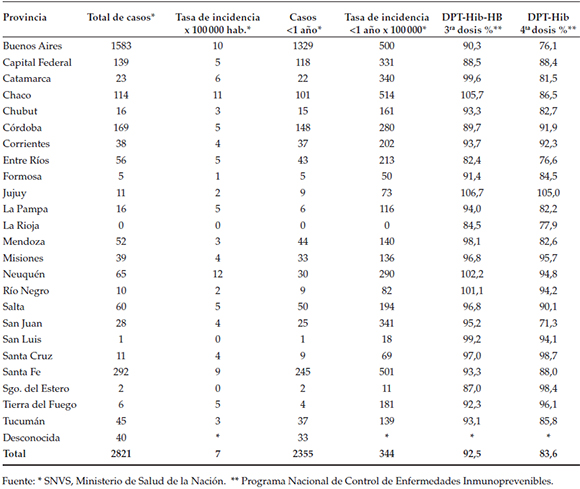
Todas las provincias detectaron casos confirmados con excepción de La Rioja. La distribución por provincia fue asimétrica: las mayores tasas de incidencia se registraron en Neuquén, Chaco, Buenos Aires y Santa Fe; en el grupo de menores de 1 año, la mayor incidencia fue en Chaco, Santa Fe y Buenos Aires (Tabla 1).
Cuatro provincias presentaron tasas de incidencia superiores a la nacional, tres de las cuales (Chaco, Buenos Aires y Neuquén) emitieron alertas por brote o las notificaron a nivel nacional.
Según la información colectada en SIVILA, 1181/1928 tenían dato de vacunación: 426/1181 eran menores de 2 meses y no tenían indicación de vacunación según nuestro Calendario Nacional; 290/1181 tenían la vacunación completa para su edad; y 465/1181, incompleta para la edad.
Según la DEIS, en el 2011, fallecieron 74 casos, todos menores de 1 año. Las jurisdicciones notificaron al ProNaCEI durante ese año 76 casos fallecidos: 74 menores de 1 año y 2 niños de 1 año de edad. La tasa de letalidad fue del 2,69% en el total de casos confirmados y del 3,14% en los menores de 1 año de edad. El 89,5% (68/76) fueron menores de 4 meses y el 60,5% (46/76) tenían menos de 2 meses de edad. El 15,8% (12/76) no registraba datos de vacunación; el 15,8% (12/76) presentó esquema de vacunación incompleto para la edad; y el 7,9% (6/76) tenía esquema completo (5 niños habían recibido 1 dosis y uno, tres).
Estrategias implementadas por el MSN
• 2003: Desarrollo del SNVS como una red que utiliza internet como soporte comunicacional, con el fin de lograr una conexión oportuna con los distintos efectores que trabajan en el área de salud. En los años siguientes, la distribución de los participantes se amplió en forma progresiva a las 24 jurisdicciones, y se alcanzó, en el año 2011, un número de 906 nodos clínicos y 405 de laboratorio, capacitados mediante talleres en las provincias.
• 2005: Se inició la transferencia de las metodologías diagnósticas microbiológicas y moleculares basadas en la PCR desde los LNR a los distintos laboratorios ubicados en diferentes localidades de nuestro país.
• 2006: Se cambió la modalidad y periodicidad de notificación en el C2 a individual e inmediata en vez de agrupada y semanal.
• 2009: Se incorporó al Calendario Nacional de Vacunación una dosis de triple bacteriana acelular de adultos (dTpa) a los 11 años y a los trabajadores de la salud en contacto con menores de un año.
• 2010: Los LNR pusieron en práctica las metodologías diagnósticas basadas en técnicas de PCR en tiempo real transferidas por los Centros para el Control y Prevención de Enfermedades de Estados Unidos (CDC), con el apoyo del Proyecto Latinoamericano de Pertussis.*
• 2011: Se introdujo en C2 la clasificación epidemiológica final de los casos como sospechosos, probables, confirmados y descartados (previamente no existía esta distinción en el C2).
• 2011: Se recomendó la vacunación a los convivientes de recién nacidos con un peso menor de 1500 gramos. A fines de 2011, el ProNaCEI convocó a la Comisión Nacional de Inmunizaciones para consensuar una propuesta ante la situación epidemiológica de la enfermedad en el país: se acordó aplicar una dosis de dTpa a las mujeres embarazadas a partir de la vigésima semana de gestación.
DISCUSIÓN
El aumento en la notificación registrado a partir de 2002 coincide con lo reportado en los últimos quince años en otros países con altos niveles de vacunación antipertussis (Australia, Canadá, Italia, Japón, Países Bajos, Suiza y Estados Unidos).4,17-21 En Estados Unidos, han reportado brotes el Estado de California (2010)20 y el de Washington (2012)21 y, en la región, Chile22 y Uruguay23 también han informado aumento de casos de coqueluche en 2011.
Los fallecimientos del período 2002-2011 ocurrieron mayoritariamente en menores de 1 año, grupo que presenta mayor frecuencia de hospitalización, complicaciones y muerte por esta enfermedad; el mayor número se registró en el año 2011.1-6,24
Si bien en el período 2002-2011 las coberturas de vacunación nacionales alcanzaron niveles superiores al 80%, resulta importante destacar que se obtuvieron por el método administrativo que puede presentar errores: registros erróneos de las dosis aplicadas (edad, número de dosis, lugar de residencia), estimación a partir de las dosis enviadas a terreno en lugar de las efectivamente administradas o información parcial de las vacunas administradas en el sector privado.
En el año 2011, se registró una tasa de incidencia de 7 por 100 000 habitantes, similar a la reportada por los Estados Unidos (6 por 100 000 habitantes).17 Los menores de 1 año representaron el grupo predominante entre los casos confirmados (84%) con una tasa de incidencia específica muy superior a la general, en coincidencia con la literatura.1-5,17-23 Las bajas tasas registradas en los mayores de 1 año podrían ser reflejo del subdiagnóstico de la enfermedad en esos grupos etarios, situación por modificar para detectar potenciales fuentes de transmisión a lactantes y cambios en la epidemiología de la enfermedad. En las epidemias de California (2010)20 y Washington (2012),21 se registraron altas tasas de incidencia entre 10 y 14 años de edad; en los reportes de Estados Unidos de 2011, el 38% de los casos fueron entre 5 y 14 años y el 85% fueron mayores de 1 año.17
En Argentina, se ha fortalecido la vigilancia de coqueluche: se pasó de datos agrupados a fichas individuales, se aumentó la notificación y la sensibilidad del sistema mediante la realización de Talleres de Capacitación en las provincias y la inclusión de nuevos nodos clínicos y de laboratorios en la red de efectores; se aumentó la especificidad con el acceso a métodos de diagnóstico para B. pertussis ya que desde los LNR se promovió la implementación del diagnóstico molecular en otros laboratorios del país. La PCR fue adoptada como método confirmatorio por ser una técnica rápida, con buena sensibilidad y especificidad, como sucedió en Estados Unidos (1996), Francia, Alemania.4,25-27 A partir del año 2011, el SNVS, basándose en la mejora en el diagnóstico, incorpora la variable "clasificación epidemiológica" con la posibilidad de definir los casos de la enfermedad como confirmados, probables y descartados, en consecuencia, se pudo determinar con mayor precisión la incidencia de la enfermedad, que es el principal indicador del impacto de la inmunización y es útil para monitorear la tendencia.28 Por esta razón, no se cuenta con datos históricos de casos confirmados entre 2002 y 2010 ya que esta clasificación final no existía en el módulo C2.
En octubre de 2011, el Advisory Committee on Immunization Practices (ACIP) publicó la recomendación de la dTpa en las embarazadas en Estados Unidos29 y diversos estudios demostraron la transferencia transplacentaria de anticuerpos de embarazadas vacunadas a sus hijos.30 A fines de 2011, el ProNaCEI convocó a la Comisión Nacional de Inmunizaciones y se analizó esta estrategia: la Argentina fue el primer país de Latinoamérica en recomendar la vacuna dTpa para las embarazadas con el objetivo de disminuir la mortalidad en lactantes menores de un año.31
El fortalecimiento de la vigilancia epidemiológica y las estrategias de vacunación implementadas32,33 se contraponen al mayor número de casos y fallecimientos, sobre todo visualizando que las coberturas de vacunación del lactante y del ingreso escolar se mantuvieron estables en el período estudiado y en valores superiores al 80%. Esta situación podría ser consecuencia de distintos factores:
1. La eficacia de la vacuna para prevenir enfermedad grave, luego de la 3ra dosis, se estima entre el 70 y el 90%.3
2. Pérdida de la inmunidad debida a la enfermedad natural y la inducida por la vacuna; esta última se reduciría considerablemente tras 5-8 años posteriores al último refuerzo.3,4 La duración de la protección podría ser distinta según se empleen vacunas celulares o acelulares.34
3. Mayor sensibilidad y especificidad del sistema de vigilancia para la detección y confirmación de los casos.
4. Tasas de vacunación subóptimas con diferencias no reflejadas en el global del país.
5. Subestimación de la incidencia de la enfermedad en adolescentes y adultos jóvenes que presentan formas clínicas más leves, que actúan como reservorios y fuentes de infección.
6. Circulación en la población de cepas de B. pertussis antigénicamente diferentes a las contenidas en las vacunas en uso.35
Como debilidades de nuestro trabajo, podemos mencionar la falta de datos históricos de casos confirmados de 2002-2010 y las limitaciones de la información de coberturas vacunales por el método administrativo; actualmente, se está avanzando en la implementación de un registro nacional nominalizado de las dosis aplicadas.
Como fortalezas, podemos mencionar que presentamos un análisis de la serie histórica de 10 años de datos nacionales, el perfil epidemiológico de los casos confirmados del año 2011 y se detallan los avances que se han producido en la vigilancia de la enfermedad.
Los desafíos que plantea coqueluche están estrechamente relacionados con la complejidad de su control. Es necesario disponer de una vacuna que tenga mayor eficacia y confiera una inmunidad más duradera. La vacunación en las embarazadas fue una estrategia implementada para proteger a los lactantes más pequeños; su efectividad y seguridad deben ser monitoreadas. Mientras tanto, las acciones de control existentes no deben ser descuidadas.
CONCLUSIONES
• En el período 2002-2011, aumentaron los casos notificados de coqueluche, los fallecidos fueron en su mayoría menores de un año y las coberturas de vacunación de los lactantes y niños al momento del ingreso escolar fueron de 80 y 90%.
• En el año 2011, la distribución de casos en el país fue heterogénea, con mayor morbimortalidad en los menores de 4 meses y más de la mitad de los niños fallecidos no había alcanzado la edad suficiente para iniciar el esquema primario de vacunación.
• En el período estudiado, el MSN fortaleció la vigilancia epidemiológica de la enfermedad e incorporó dosis adicionales de vacunación antipertussis.
Notas:
* El Proyecto Latinoamericano de Pertussis es un proyecto colaborativo entre los Centros para el Control y Prevención de Enfermedades de Estados Unidos (CDC), la Organización Panamericana de la Salud, el Instituto de Vacunas Sabin y los Ministerios de Salud de países seleccionados para fortalecer la vigilancia de tos ferina en América Latina.
ANEXO
Definiciones de caso de coqueluche utilizadas entre los años 2002 y 2011:
Período 2002-200710 (modalidad de notificación numérica-semanal):
Caso sospechoso. Persona con tos paroxística que dura como mínimo 2 semanas, afebril, con uno de los siguientes síntomas: tos paroxística, estridor inspiratorio, vómito posterior al acceso de tos y expectoración mucosa y filante sin otra causa aparente.
Caso confirmado. Caso sospechoso con aislamiento de Bordetella pertussis a partir de secreción respiratoria o nexo epidemiológico con un caso confirmado por laboratorio.
Período 2007-20116 (modalidad individual-inmediata):
Caso sospechoso. Paciente que presenta tos durante al menos 14 días, afebril y con alguno de los siguientes síntomas: tos paroxística, estridor inspiratorio, vómito posterior al acceso de tos y expectoración mucosa y filante sin otra causa aparente.
En menores de 6 meses, pueden no observarse los paroxismos y presentar apneas y cianosis. En situaciones de brote, se ajustará la definición de caso.
Caso confirmado. Caso sospechoso con aislamiento de Bordetella pertussis a partir de secreción respiratoria o PCR positiva o seroconversión entre dos sueros tomados uno en la fase aguda y otro en la convaleciente o nexo epidemiológico con un caso confirmado.
Período 201111 (modalidad individual-inmediata):
Caso sospechoso
Menores de 6 meses. Toda infección respiratoria aguda, con al menos uno de los siguientes síntomas: apnea, cianosis, estridor inspiratorio, vómitos después de toser o tos paroxística.
Mayores de 6 meses hasta 11 años. Tos de 14 o más días de duración acompañado de uno o más de los siguientes síntomas: tos paroxística, estridor inspiratorio o vómitos después de la tos, sin otra causa aparente.
Mayores de 11 años. Tos persistente de 14 días de duración o más, sin otra sintomatología acompañante.
Caso confirmado
Paciente con infección respiratoria que presenta tos de cualquier duración y con cultivo positivo para el agente causal.
Paciente con clínica compatible de coqueluche y resultados positivos en el laboratorio mediante ensayos de PCR específicos.
Paciente con clínica compatible de coqueluche y resultados positivos (seroconversión) en el laboratorio mediante ensayo serológico específico.
Paciente con clínica compatible de coqueluche y nexo epidemiológico con caso confirmado por laboratorio.
Caso probable
Paciente con clínica compatible con coqueluche y sin confirmación por laboratorio (no estudiado o resultados de laboratorio no conclusivos) y sin nexo epidemiológico con un caso confirmado por laboratorio.
Paciente con clínica incompleta o datos insuficientes y con resultado positivo por PCR o por seroconversión.
Caso descartado
Clínica incompleta o datos insuficientes, y con resultado de laboratorio negativo y sin nexo epidemiológico con un caso confirmado.
1. American Academy of Pediatrics. Pertussis (Whooping Cough). En: Pickering LK, ed. Red Book: 2012 Report of the Committee on Infectious Diseases. 29th ed. Elk Grove Village, IL: American Academy of Pediatrics; 2012. Págs.553-66.
2. Sociedad Argentina de Pediatría. Comité Nacional de Infectología. Bordetella Pertussis. En: Libro Azul de Infectología Pediátrica. 4ta ed. Buenos Aires: SAP; 2012.Págs.484-93.
3. Centers for Disease Control and Prevention. Epidemiology and Prevention of Vaccine-Preventable Diseases. 12th ed. Washington DC: Public Health Foundation, 2012. Chapter 15 Pertussis. Disponible en: http://www.cdc.gov/vaccines/pubs/pinkbook/pert.html. Acceso: 10 de marzo de 2013. [ Links ]
4. Tan T, Trindade E, Skowronski D. Epidemiology of pertussis. Pediatr Infect Dis J 2005;24(5 Suppl):S10-8. [ Links ]
5. World Health Organization. Immunization, Vaccines and Biologicals. Pertussis. Geneva: World Health Organization, 2012. Disponible en: http://www.who.int/immunization/topics/pertussis/en/index.html. Acceso: 15 de abril de 2013. [ Links ]
6. Argentina. Ministerio de Salud de la Nación. Manual de normas y procedimientos de Vigilancia y Control de Enfermedades de Notificación Obligatoria. Revisión nacional 2007. Buenos Aires, 2007. Disponible en: http://www.msal.gov.ar/images/stories/epidemiologia/pdf/manual-normas-obligatorias.pdf. Acceso: 20 de abril de 2013. [ Links ]
7. Argentina. Ministerio de Salud de la Nación. Vigilancia Clínica (C2). Buenos Aires, 2013. Disponible en: http://www.msal.gov.ar/index.php/home/funciones/area-de-vigilancia/snvs-c2. Acceso: 20 de abril de 2013. [ Links ]
8. Argentina. Ministerio de Salud de la Nación. SIVILA. Sistema Nacional de Vigilancia Epidemiológica por Laboratorios de Argentina. Buenos Aires, 2013. Disponible en: http://www.msal.gov.ar/index.php/home/funciones/area-de-vigilancia/sivila. Acceso: 20 de abril de 2013. [ Links ]
9. Argentina. Ministerio de Salud de la Nación. Dirección de Estadística e Información en Salud. Defunciones de menores de 5 años. Indicadores seleccionados. Boletín número 139. Buenos Aires: Dirección de Estadística e Información en Salud; 2013. Disponible en: http://www.deis.gov.ar/publicaciones/Archivos/Boletin139.pdf. Acceso: 9 de junio de 2014. [ Links ]
10. Argentina. Ministerio de Salud. Manual de Normas y Procedimientos del Sistema Nacional de Vigilancia Epidemiológica. SI.NA.VE. - 1999. Revisión Internacional 2000. Buenos Aires, 2000.
11. Argentina. Ministerio de Salud de la Nación. Programa Nacional de Control de Enfermedades Inmunoprevenibles. Actualización de la Situación de coqueluche. Alerta N° 12. Buenos Aires, 2001.Consulta: 18 de junio de 2014. Disponible en: http://www.msal.gov.ar/images/stories/epidemiologia/inmunizaciones/alerta-sarampion/alerta-coqueluche_agosto19-5B1-5D.pdf.
12. Argentina. Ministerio de Salud de la Nación. Coqueluche sospechoso y coqueluche en estudios de contactos: normativa y tutorial para la vigilancia a través del sistema nacional de vigilancia laboratorial. SIVILA-SNVS. Actualización 2011. Buenos Aires, 2011. Disponible en: http://www.msal.gov.ar/images/stories/epidemiologia/vigilancia/sivila/tutoriales/coqueluche-tutorial-normativa-para-notificacion-sivila-2011.pdf. Acceso: 20 de abril de 2013. [ Links ]
13. World Health Organization. Immunization. Vaccines and Biologicals. Laboratory manual for the diagnosis of whooping cough caused by Bordetella pertussis/Bordetella parapertussis. Geneva: World Health Organization, 2007. Disponible en: http://whqlibdoc.who.int/hq/2004/WHO_IVB_04.14_eng.pdf. Acceso: 10 de marzo de 2013. [ Links ]
14. Glare EM, Paton JC, Premier RR, Lawrence AJ, et al. Analysis of a repetitive DNA sequence from Bordetella pertussis and its application to the diagnosis of pertussis using the polymerase chain reaction. J Clin Microbiol 1990;28(9):1982-7. [ Links ]
15. Grimprel E, Bégué P, Anjak I, Betsou F, et al.Comparison of polymerase chain reaction, culture, and western immunoblot serology for diagnosis of Bordetella pertussis infection. J Clin Microbiol 1993;31(10):2745-50. [ Links ]
16. Tatti KM, Sparks KN, Boney KO, Tondella ML. Novel multitarget real-time PCR assay for rapid detection of Bordetella species in clinical specimens. J Clin Microbiol 2011;49(12):4059-66. [ Links ]
17. Adams DA, Gallagher KM, Jajosky RA, Kriseman J, et al. Summary of Notifiable Diseases - United States, 2011. MMWR Morb Mortal Wkly Rep 2013;60(53):1-117. [ Links ]
18. Plotkin S. Aims, scope and findings of the global pertussis initiative. Pediatr Infect Dis J 2005;24(5 Suppl):S5-6. [ Links ]
19. Halperin SA. The control of pertussis - 2007 and beyond. N Eng J Med 2007;356(2):110-3. [ Links ]
20. Winter K, Harriman K, Zipprich J, Schechter R, et al. California pertussis epidemic, 2010. J Pediatr 2012;161(6):1091-6. [ Links ]
21. Centers for Disease Control and Prevention (CDC). Pertussis epidemic-Washington, 2012. MMWR Morb Mortal Wkly Rep 2012;61(28):517-22. [ Links ]
22. Chile. Ministerio de Salud. Departamento de Epidemiología. Informe de coqueluche año 2011. Santiago de Chile, 2011. Disponible en: http://epi.minsal.cl/epi/html/bolets/reportes/Coqueluche/Tos_Final_2011.pdf. Acceso: 25 de marzo de 2013. [ Links ]
23. Uruguay. Ministerio de Salud Pública. Dirección General de la Salud, División de Epidemiología. Informe de actualización. Situación tos convulsa (a la semana epidemiológica 37 de 2012). Montevideo: Ministerio de Salud Pública; 2012. Disponible en: http://www.msp.gub.uy/sites/default/files/archivos_adjuntos/Informe_ tos_convulsa_SETIEMBRE_2012%20(4).pdf. Acceso: 9 de junio de 2014. [ Links ]
24. Tanaka M, Vitek CR, Pascual FB, Bisgard KM, et al. Trends in pertussis among infants in the United States, 1980-1999. JAMA 2003;290(22):2968-75. [ Links ]
25. Cherry JD, Grimpel E, Guiso N, Heininger U, et al. Defining pertussis epidemiology: clinical, microbiologic and serologic perspectives. Pediatr Infect Dis J 2005;24(5 Suppl):S25-34. [ Links ]
26. Heininger U, Schmidt-Schläpfer G, Cherry JD, Stehr K. Clinical validation of a polymerase chain reaction assay for the diagnosis of pertussis by comparison with serology, culture, and symptoms during a large pertussis vaccine efficacy trial. Pediatrics 2000;105(3):E31. [ Links ]
27. Giammanco A, Nardone A, Pebody R, Kafatos G, et al. European Sero-Epidemiology Network 2: standardisation of immunoassay results for pertussis requires homogeneity in the antigenic preparations. Vaccine 2008;26(35):4486-93. [ Links ]
28. World Health Organization. Estimates of disease burden and cost-effectiveness. Geneva: World Health Organization: 2014. Disponible en: http://www.who.int/immunization/monitoring_surveillance/burden/estimates/en/. Acceso: 9 de junio de 2014. [ Links ]
29. Centers for Disease Control and Prevention (CDC). Updated recommendations for use of tetanus toxoid, reduced diphtheria toxoid and acellular pertussis vaccine (Tdap) in pregnant women and persons who have or anticipate having close contact with an infant aged <12 months -Advisory Committee on Immunization Practices (ACIP), 2011. MMWR Morb Mortal Wkly Rep 2011;60(41):1424-6. [ Links ]
30. Leuridan E, Hens N, Peeters N, de Witte L, et al. Effect of a pregnancy pertussis booster dose on maternal antibody titers in young infants. Pediatr Infect Dis J 2011;30(7):608-10. [ Links ]
31. Argentina. Ministerio de Salud de la Nación, Programa Nacional de Control de Enfermedades Inmunoprevenibles. Alerta epidemiológico 25/1/2012. Tos convulsa: aumento de casos y muertes. Buenos Aires; 2012. Disponible en: http://www.msal.gov.ar/images/stories/bes/graficos/0000000454cnt-2013-10_alerta-n01-tos-convulsa-2012.pdf. Acceso: 9 de junio de 2014. [ Links ]
32. Argentina. Ministerio de Salud de la Nación. Calendario Nacional de Vacunación de la República Argentina 2012. Buenos Aires; 2012. Disponible en: http://www.msal.gov.ar/images/stories/calendario-vacunacion/calendario-vacunacion-2012.pdf. Acceso: 9 de junio de 2014. [ Links ]
33. Argentina. Ministerio de Salud de la Nación, Secretaría de Promoción y Programas Sanitarios. Normas nacionales de vacunación. Edición 2008. Buenos Aires: OPS/OMS Argentina; 2008. Disponible en: http://publicaciones.ops.org.ar/pubKcaciones/otras%20pub/Normas-Nacionales-de-Vacunacion-2008.pdf. Acceso: 9 de junio de 2014.
34. Tartof SY, Lewis M, Kenyon C, White K, et al. Waning immunity to pertussis following 5 doses of DTaP. Pediatrics 2013;131(4):e1047-52. [ Links ]
35. Fingermann M, Fernández J, Sisti F, Rodríguez ME, et al. Differences of circulating Bordetella pertussis population in Argentina from the strain used in vaccine production. Vaccine 2006;24(17):3513-21. [ Links ]














