Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Archivos argentinos de pediatría
versão impressa ISSN 0325-0075
Arch. argent. pediatr. vol.113 no.4 Buenos Aires ago. 2015
http://dx.doi.org/10.5546/aap.2015.310
ARTÃCULOS ORIGINALES
http://dx.doi.org/10.5546/aap.2015.310
Influencia de los virus respiratorios en la evaluación de la efectividad de la vacuna neumocócica de 13 serotipos en menores de 5 años: estudio de series temporales 2001-2013
Dra. Ãngela Gentilea, Dra. MarÃa del Valle Juareza, Dra. MarÃa Florencia Luciöna, Dra. Viviana Sandra Romanina, Dr. Norberto Giglioa y Dra. Julia Bakina
a. Hospital de Niños Ricardo Gutiérrez, División Promoción y Protección de la Salud. Ciudad Autónoma de Buenos Aires.
Correspondencia: Dra. Ãngela Gentile: angelagentile@fibertel.com.ar
Financiamiento:Ninguno.
Conflicto de intereses: Ninguno que declarar.
Recibido: 19-12-2014
Aceptado: 9-3-2015
RESUMEN
Introducción. Streptococcus pneumoniae es el principal agente de las neumonÃas consolidantes de causa bacteriana. En 2012, se introdujo la vacuna contra neumococo de 13 serotipos al Calendario Nacional en Argentina para niños inmunocompetentes a partir de los dos meses de edad (2 + 1).
Objetivo. Analizar la influencia de los virus respiratorios en la evaluación de la efectividad de la vacuna conjugada contra el neumococo de 13 serotipos en relación con el número de hospitalizaciones por neumonÃas consolidantes confirmadas por radiologÃa (NCCR).
Métodos. Estudio observacional analÃtico de series temporales. Se incluyeron todos los niños internados con diagnóstico de NCCR según criterios de la Organización Mundial de la Salud, marzo-noviembre de 2001-2013. El diagnóstico viral (virus sincicial respiratorio, adenovirus, influenza y parainfluenza) se realizó por inmunofluorescencia indirecta de aspirados nasofarÃngeos o por reacción en cadena de la polimerasa con transcriptasa inversa. Se desarrollaron series temporales que compararon los perÃodos prevacunación 20012011 y posvacunación 2012-2013.
Resultados. De un total de 11 306 niños menores de 5 años con infecciones respiratorias agudas bajas, se incluyeron 4974 con NCCR. Promedio anual de internación por NCCR: 394,8 prevacunación; 315,5 posvacunación (reducción del 20,1%; IC 95% 13,13-26,49%; p <0,001). Promedio anual de internación por NCCR no viral: 255,5 prevacunación; 183 posvacunación (reducción del 28,4%; IC 95% 20,5-35,78%; p <0,001). Promedio anual de internación por NCCR viral: 139,2 prevacunación; 132 posvacunación (reducción del 4,8%; IC 95% 8,38-16,49%; p = 0,4758). La proporción de NCCR con diagnóstico viral positivo fue 35,3% prevacunación y 42% posvacunación (p = 0,001). Conclusiones. Se observó un descenso significativo de las internaciones por NCCR en forma global luego de la introducción de la vacuna contra neumococo de 13 serotipos, particularmente en aquellas de etiologÃa no viral. Es fundamental continuar la vigilancia epidemiológica para evaluar el impacto de esta medida y el comportamiento viral en relación con las NCCR.
Palabras clave: NeumonÃa; Streptococcus pneumoniae; Vacunas neumocöcicas; Estudios de series temporales; Efectividad.
INTRODUCCIÃN
Las infecciones neumocócicas son una causa importante de morbilidad, hospitalización y mortalidad en todo el mundo, con dos grupos de edad de mayor incidencia y gravedad: los niños menores de 2 años y los adultos mayores de 65 años de edad.1 La Organización Mundial de la Salud (OMS) estimó, en el año 2000, que el 20% de las muertes de menores de 5 años estaban relacionadas con infecciones respiratorias agudas; el 90% de estas eran neumonÃas agudas de la comunidad, de las cuales, en más del 50%, el agente causal era el Streptococcus pneumoniae.2,3 En Argentina, las enfermedades respiratorias son la tercera causa de muerte en niños menores de 5 años, con un porcentaje de internación de alrededor del 65% y una tasa de letalidad de 1,1%.4-6
Argentina introdujo al Calendario Nacional de Vacunación, en el año 2012, la vacuna conjugada contra el neumococo de 13 serotipos (VCN-13) con el propósito de controlar la enfermedad neumocócica invasiva (ENI) y disminuir la mortalidad por neumonÃa, ENI y sus respectivas secuelas.
Los datos de cobertura de vacunación según la OMS fueron, para el año 2012, 69% para la primera dosis y 22% para la tercera dosis y, en el año 2013, la cobertura fue 96% para la primera dosis y 81% para el refuerzo.7
En términos de serotipos circulantes en el paÃs, la VCN-13 presenta una cobertura del 85% para todas las enfermedades neumocócicas, de 88,4% para los serotipos involucrados en neumonÃas y de 83,3% para meningitis de acuerdo con los datos del Sistema de Redes de Vigilancia de los Agentes Responsables de NeumonÃas y Meningitis Bacterianas (SIREVA II) del año 2011.8
Al igual que en distintos paÃses del mundo,9-11 una vez incorporada la VCN-13 al Calendario Nacional de Vacunación, se implementaron los lineamientos para valorar su efectividad en el "mundo real".1213
Dada la dificultad de confirmar el diagnóstico bacteriológico de la enfermedad causada por Streptococcus pneumoniae, la utilización de los patrones clÃnicos y radiológicos de neumonÃa ha brindado la información adecuada para realizar diferentes estudios de efectividad.3
Para la medición de la eficacia y efectividad de la vacuna neumocócica en términos de reducción de las neumonÃas consolidantes confirmadas por radiologÃa (NCCR), existe la controversia sobre cuál es el valor predictivo positivo para inferir infección bacteriana teniendo en cuenta la capacidad de los virus de producir imágenes semejantes de consolidación radiológicas a los agentes bacterianos.
Por todo lo expresado anteriormente, consideramos que resulta de interés para los estudios de efectividad valorar la influencia de los virus sobre las NCCR.
El objetivo de este estudio es analizar la influencia de los virus respiratorios en la evaluación de la efectividad de la vacuna conjugada contra el neumococo de 13 serotipos en relación con el número de hospitalizaciones por NCCR.
MATERIAL Y MÃTODOS
Estudio observacional analÃtico de series temporales. Se incluyeron los niños menores de 5 años internados entre marzo y noviembre de los años 2001-2013, con diagnóstico de NCCR por todas las causas de acuerdo con las definiciones de la OMS de 2000.3
Todos los registros de NCCR se tomaron del programa de Vigilancia Epidemiológica Activa del Hospital de Niños Ricardo Gutiérrez.
Este programa se lleva a cabo en el Hospital desde el año 2000 y consiste en una vigilancia epidemiológica activa y prospectiva de infecciones respiratorias agudas bajas (IRAB) en los niños internados por esta causa. Al momento del ingreso hospitalario, se realiza radiografÃa de tórax y exámenes virológicos.
Criterio de inclusión: pacientes menores de 5 años internados en nuestro Hospital con diagnóstico de NCCR al ingresar.
Criterio de exclusión: pacientes internados por otra causa que desarrollaron NCCR después de las 48 horas de haber ingresado.
NCCR: opacidad densa habitualmente homogénea o de aspecto algodonoso, que compromete un segmento o un lóbulo pulmonar completo, por lo general, con broncograma aéreo y, a veces, asociada a derrame pleural.
NCCR con detección viral: son las neumonÃas consolidantes confirmadas radiológicamente que hayan tenido prueba de laboratorio (inmunofluorescencia indirecta), realizada dentro de las 48 horas de la internación positiva.
El diagnóstico virológico -virus sincicial respiratorio (VSR), adenovirus, influenza y parainfluenza- se realizó por inmunofluorescencia indirecta (IFI) o reacción en cadena de la polime-rasa con transcriptasa inversa (reverse transcription polymerase chain reaction; RT-PCR, por sus siglas en inglés) para influenza (a partir de 2009) en el aspirado nasofarÃngeo dentro de las 48 horas de haber ingresado.
Se consideró, para este estudio, el perÃodo 2001-2011 como prevacunación y el perÃodo 20122013 como posvacunación.
Se realizó, en primer lugar, un análisis descriptivo, calculando mediana y rango intercuartÃlico para las variables continuas y, para datos categóricos, proporciones con sus intervalos de confianza del 95%. Se utilizó la metodologÃa de las series temporales con el cálculo de las medias móviles para comparar los perÃodos prevacunación y posvacunación y la detección viral como punto de comparación.
Se realizó, además, un análisis estratificado de la serie temporal propuesta en términos de niños menores de 1 año de vida, asà como de NCCR con diagnóstico viral positivo detectado por inmunofluorescencia indirecta.
Datos meteorológicos: los valores medios mensuales de temperatura y humedad relativa del Observatorio de Buenos Aires del perÃodo 2001-2013 fueron provistos por el Servicio Meteorológico Nacional, Ministerio de Defensa de la Nación. La temperatura fue expresada en grados Celsius (°C) y la humedad relativa, en porcentaje.
Este estudio contó con la aprobación del Comité de Ãtica en Investigación del Hospital de Niños Ricardo Gutiérrez.
RESULTADOS
Entre los años 2001 y 2013, se internaron un total de 11 306 niños menores de 5 años con IRAB, de los cuales 4974 ingresaron con diagnóstico de NCCR. Las caracterÃsticas de los pacientes internados por NCCR en nuestro centro mostraron una población, en su mayorÃa, menor de 2 años de relación semejante entre ambos sexos, gran parte provenientes del Conurbano de la provincia de Buenos Aires, sin diferencias significativas entre ambos perÃodos (Tabla 1).
Tabla 1. CaracterÃsticas de los pacientes ingresados por neumonÃa consolidante confirmada por radiologÃa. PerÃodos pre (2001-2011) y posvacunación (2012-2013). Hospital de Niños R. Gutiérrez

De la muestra de pacientes con NCCR de acuerdo con el diagnóstico viral, un 63,8% (n= 3177) tuvieron diagnóstico viral negativo y 36,2% (n= 1797), diagnóstico viral positivo.
La serie temporal de los casos de NCCR y de virus respiratorios mostró un patrón estacional similar con predominio invernal. Los perÃodos de máxima detección viral coincidieron, en todos los años, con los perÃodos de mayor humedad y menor temperatura. Del mismo modo, la máxima detección viral coincidió con los picos de internación de casos de NCCR. Las NCCR sin detección viral predominaron en la época de primavera, a excepción del año 2013. En este año, se dejó de observar este predominio fuera del perÃodo de mayor detección (Figura 1).
Figura 1. Hospitalizaciones por neumonÃa consolidante confirmada por radiologÃa y detección viral en relación con las variaciones estacionales en niños menores de 5 años. Hospital de Niños R. Gutiérrez. Años 2001-2013

El promedio anual de internaciones por NCCR en el perÃodo prevacunación fue de 394,8 (DE 54,6). En el perÃodo posvacunación, el promedio fue de 315,5 (DE 36,1), lo cual representó una reducción del 20,1% (iC 95%: 13,13-26,49%; p < 0,001) respecto al perÃodo prevacunación. Esta reducción fue de 22% (IC 95%: 12,4-31,5%; p < 0,001) al analizar la población de menores de 1 año.
El promedio anual de internación por NCCR no viral en el perÃodo prevacunación fue 255,5 (DE 31,5) y, en el perÃodo posvacunación, 183 (DE 32,5), lo cual representó una reducción del 28,4% (IC 95%: 20,5-35,78%), que fue estadÃsticamente significativa (p < 0,001). El promedio anual de internación por NCCR viral en el perÃodo prevacunación fue 139,2 (DE 36,5) y, en el perÃodo posvacunación, 132 (DE 3,5). Esto mostró una reducción del 4,8%, sin significancia estadÃstica (Tabla 2).
Tabla 2. Casos y promedio anual de neumonÃa consolidante confirmada por radiologÃa y según rescate virológico en menores de 5 años. Hospital de Niños R. Gutiérrez. Años 2001-2013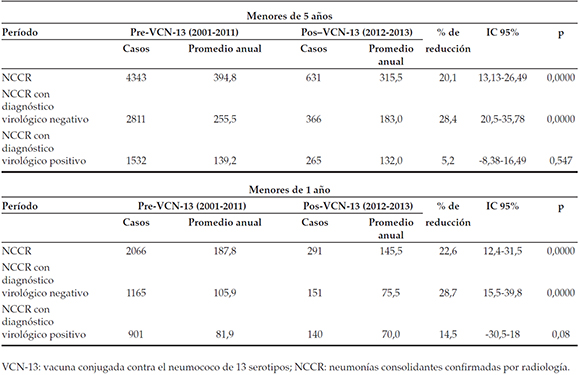
La proporción de neumonÃas consolidantes con diagnóstico viral en el perÃodo prevacunación fue de 35,3% (1532/4343), mientras que, en el perÃodo posvacunación, fue de 42% (265/631). La diferencia entre ambas proporciones resultó significativa (p = 0,0010) (Figura 2).
Figura 2. Número anual de neumonÃas consolidantes según diagnóstico virológico y proporción de neumonÃas consolidantes confirmadas por radiologÃa con diagnóstico viral positivo y negativo 2001-2013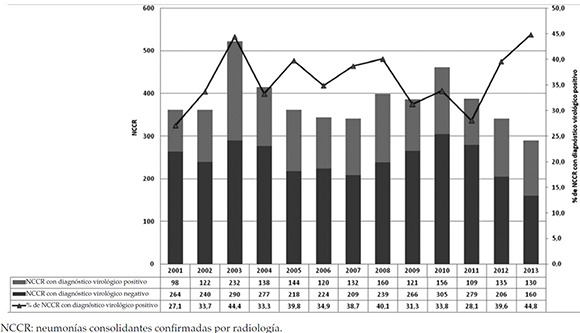
DISCUSIÃN
Nuestros resultados permiten evidenciar una reducción de los casos de NCCR hospitalizadas además de demostrar que la inclusión de los casos de NCCR con diagnóstico viral positivo modifica los resultados de efectividad de la VCN-13 para el perÃodo 2012-2013 en Argentina.
Los valores de efectividad se encuentran en coincidencia con otros estudios, como el de eficacia de la vacuna de 7 serotipos realizada por Black y col.,1415 que mostraba una reducción de 25,5% de las NCCR. En el mismo sentido, Grijalva describe una reducción de 39%, a través de series temporales interrumpidas con exclusión del año de transición y utilizando datos de fuente secundaria.11
Con relación a las diferencias encontradas en términos de efectividad para NCCR y NCCR con diagnóstico virológico positivo y negativo, Dagan y col.16 demuestran que la introducción de VCN en sus programas nacionales de vacunación ha generado un descenso significativo de las NCCR, que resulta mayor aun cuando se ajusta este resultado por la variación estacional del virus sincicial respiratorio.
Resulta plausible considerar, desde una perspectiva unicista, que dadas las caracterÃsticas de las vacunas conjugadas antineumocócicas, estas no tendrÃan impacto sobre las neumonÃas virales. Debido a esta condición, la inclusión de esta entidad clÃnica en los estudios de efectividad podrÃa sobrestimar o subestimar el efecto.
Contrariamente a lo expresado en el párrafo anterior, Klugman y col.,17 en el estudio aleatorizado controlado realizado en Soweto, describen, en el análisis por protocolo, una eficacia de 17% (IC 95% 2-30) para las neumonÃas lobares por toda causa, 14% (IC 95% 2-24) para las neumonÃas sin identificación viral y 31% (IC 95% 15-43) para las neumonÃas virales. El autor justifica la eficacia de la VCN-9 obtenida para la neumonÃa con confirmación radiológica y diagnóstico virológico positivo sobre la base de las hipótesis de coinfección de virus y bacterias en este tipo de infección respiratoria.
El tema de las NCCR con virológico positivo, asà como coinfección entre virus y bacterias en infecciones respiratorias bajas, ha sido abordado por diferentes autores.18-20 Un estudio con base poblacional, realizado en Uruguay por Hortal y col.21 antes de la introducción de la vacuna contra neumococo, demostró que el 17,1% de las neumonÃas no consolidantes presentaban alguna detección viral y que el 18% de las neumonÃas consolidantes (o probablemente bacterianas) presentaban diagnóstico viral. Destacamos que la búsqueda de etiologÃa viral se realizaba al azar, no en todos los casos.
En un estudio publicado por Gentile y col.22 en el marco del Comité Nacional de InfectologÃa de la Sociedad Argentina de PediatrÃa que describe la experiencia y las acciones en el perÃodo de la gripe pandémica, se observó que el 47,6% de los pacientes ingresados con diagnóstico de influenza pandémica presentaban un cuadro clÃnico de neumonÃa consolidante.
Estudios realizados en comunidades aborÃgenes de Australia central han encontrado un 39,8% de coinfección entre virus y bacterias, y el autor no ha podido demostrar un patrón de infección caracterÃstico a través de la detección nasal de virus respiratorios y bacterias entre las neumonÃas confirmadas por radiologÃa y el resto de las infecciones respiratorias bajas.23
En el mismo sentido, un estudio desarrollado en Francia demostró que el 28% de los niños con neumonÃa hospitalizada de la comunidad presentaron coinfección entre virus y bacterias.24
Resultados similares han sido descritos por Luchsinger y col.25 en un estudio desarrollado en Chile en población adulta, en el que los autores describen coinfección de neumonÃa de la comunidad entre Streptococcus pneumoniae y virus respiratorios en 25 casos de una muestra total de 356 casos de neumonÃas.
Finalmente, en relación con la efectividad valorada, nuestro estudio presenta algunas debilidades. En cuanto al perÃodo preintroducción, se incluye el año pandémico que podrÃa sobreestimar el diagnóstico de neumonÃa consolidante. Además, el perÃodo posintroducción de la vacuna resulta corto; con la inclusión de más años en este perÃodo, las estimaciones de efectividad seguramente serán de mayor solidez.
Dadas las caracterÃsticas de nuestro trabajo, no hemos podido estudiar las coinfecciones debido a que la detección de agentes bacterianos en esta forma clÃnica es baja, lo que no permite descartar las coinfecciones.
Condiciones como el tipo de diseño del estudio o el número de casos de neumonÃas virales valoradas podrÃan explicar la ausencia de impacto en este último grupo si la hipótesis de coinfección carece de relevancia.
La controversia está planteada ya que, a la fecha, la detección de virus en una neumonÃa lobar no es condición suficiente para descartar que, en estos cuadros clÃnicos, pudiera existir coinfección con Streptococcus pneumoniae.26
Estudios de mayor validez interna serán necesarios para confirmar estas últimas hipótesis.
CONCLUSIONES
Se observó un descenso significativo de las internaciones por NCCR luego de la introducción de la VCN-13 al Calendario Nacional, particularmente en aquellas NCCR con diagnóstico virológico negativo, y no se hallaron valores de efectividad significativos para las NCCR con diagnóstico viral positivo. â–
1. Gorrotxategi Gorrotxategi PJ, Iturrioz Mata A. Vacuna conjugada contra neumococo ¿es una prevención universal adecuada de la enfermedad neumocócica? Rev Pediatr Aten Primaria 2010;12(47):443-55. [ Links ]
2. World Health Organization. Global Health Observatory data. Care seeking for pneumonia. Situation and trends. Geneva, 2015. [Acceso: 9 de marzo de 2015]. Disponible en: http://www.who.int/gho/child_health/prevention/pneumonia_text/en/index.html. [ Links ]
3. World Health Organization Pneumonia Vaccine Trial Investigators' Group. Standardization of interpretation of chest radiographs for the diagnosis of pneumonia in children. Geneva, 2001. [Acceso: 9 de marzo de 2015]. Disponible en: http://apps.who.int/iris/bitstream/10665/66956/1/WHO_V_and_B_01.35.pdf. [ Links ]
4. Dirección de EstadÃsticas e Información de Salud. EstadÃsticas vitales. Información básica - Año 2012. Buenos Aires: Ministerio de Salud de la Nación Argentina; 2013. Serie 5 - Número 56.
5. Gentile A, Ruvinsky R, Bakir J, Gentile F, et al. Probable bacterial pneumonia in children less than five years old in two geographical areas of Argentina: two years of surveillance. En: 44th Interscience Conference on Antimicrobial Agents and Chemotherapy. Washington DC, USA: 2004 Oct 30 - Nov 2. [ Links ]
6. Gaiano A, Biscayart C, Vizzotti C. Introducción de la vacuna conjugada antineumocócica en el Calendario Nacional de Vacunación en Argentina. Rev Argent Salud Pública 2012;3(10):41-3. [ Links ]
7. World Health Organization. WHO vaccine-preventable diseases: monitoring system. 2014 global summary. Coverage time series for Argentina. Geneva, 2014. [Consulta: 9 de marzo de 2015]. Disponible en: http://apps.who.int/immunization_momtoring/globalsummary/coverages?c=ARG. [ Links ]
8. Organización Panamericana de la Salud. Informe Regional de SIREVA II, 2011: datos por paÃs y por grupos de edad sobre las caracterÃsticas de los aislamientos de Streptococcus pneumoniae, Haemophilus influenzae y Neisseria meningitidis, en procesos invasores. Washington DC, 2012. [ Links ]
9. Grijalva CG, GriffinMR. Population-based impact ofroutine infant immunization with pneumococcal conjugate vaccine in the USA. Expert Rev Vaccines 2008;7(1):83-95. [ Links ]
10. Pirez MC, Algorta G, Cedres A, Sobrero H, et al. Impact of universal pneumococcal vaccination on hospitalizations for pneumonia and meningitis in children in Montevideo, Uruguay. Pediatr Infect Dis J 2011;30(8):669-74. [ Links ]
11. Grijalva CG, Nuorti JP, Arbogast PG, Martin SW, et al. Decline in pneumonia admissions after routine childhood immunisation with pneumococcal conjugate vaccine in the USA: a time-series analysis. Lancet 2007;369(9568):1179-86. [ Links ]
12. Patel MM, Steele D, Gentsch JR, Wecker J, et al. Real-world impact of rotavirus vaccination. Pediatr Infect Dis J 2011;30(1 Suppl):S1-5. [ Links ]
13. Griffin MR, Zhu Y, Moore MR, Whitney CG, et al. U.S. hospitalizations for pneumonia after a decade of pneumococcal vaccination. N Engl J Med 2013;369(2):155-63. [ Links ]
14. Black S, Shinefield H, Fireman B, Lewis E, et al. Efficacy, safety and immunogenicity of heptavalent pneumococcal conjugate vaccine in children. Pediatr Infect Dis J 2000;19(3):187-95. [ Links ]
15. Hansen J, Black S, Shinefield H, Cherian T, et al. Effectiveness of heptavalent pneumococcal conjugate vaccine in children younger than 5 years of age for prevention of pneumonia: updated analysis using World Health Organization standardized interpretation of chest radiographs. Pediatr Infect Dis J 2006;25(9):779-81. [ Links ]
16. Weinberger DM, Givon-Lavi N, Shemer-Avni Y, Bar-Ziv J, et al. Influence of pneumococcal vaccines and respiratory syncytial virus on alveolar pneumonia, Israel. Emerg Infect Dis 2013;19(7):1084-91. [ Links ]
17. Madhi SA, Klugman KP, Vaccine Trialist Group. A role for Streptococcus pneumoniae in virus-associated pneumonia. Nat Med 2004;10(8):811-3. [ Links ]
18. Wolf DG, Greenberg D, Shemer-Avni Y, Givon-Lavi N, et al. Association of human metapneumovirus with radiologically diagnosed community-acquired alveolar pneumonia in young children. J Pediatr 2010;156(1):115-20. [ Links ]
19. Madhi SA, Ludewick H, Kuwanda L, Van Niekerk N, et al. Pneumococcal coinfection with human metapneumovirus. J Infect Dis 2006;193(9):1236-43. [ Links ]
20. Madhi SA, Kuwanda L, Cutland C, Klugman KP. The impact of a 9-valent pneumococcal conjugate vaccine on the public health burden of pneumonia in HIV infected and uninfected children. Clin Infect Dis 2005;40(10):1511-8. [ Links ]
21. Hortal M, Estevan M, Iraola I, De Mucio B. A population-based assessment of the disease burden of consolidated pneumonia in hospitalized children under five years of age. Int J Infect Dis 2007;11(3):273-7. [ Links ]
22. Gentile A, Bakir J, Russ C, Ruvinsky S, et al. Estudio de las enfermedades respiratorias por virus Influenza A H1N1 (pH1N1) en niños internados durante el año de la pandemia. Experiencia de 34 centros en la Argentina. Arch Argent Pediatr 2011;109(3):198-203. [ Links ]
23. O'Grady K, Torzillo PJ, Valery P, Smith-Vaughan H, et al. Viruses and bacteria associated with hospitalized, radiologically confirmed pneumonia in aboriginal children aged less than five years in Central Australia [abstract]. En: 9th International Symposium on Pneumococci and Pneumococcal Diseases. Hyderabad, India: 2014 March 9-13; p. [ Links ] 46.
24. Cantais A, Mory O, Pillet S, Verhoeven PO, et al. Epidemiology and microbiological investigations of community-acquired pneumonia in children admitted at the emergency department of a university hospital. J Clin Virol 2014;60(4):402-7. [ Links ]
25. Luchsinger V, Ruiz M, Zunino E, MartÃnez MA, et al. Community-acquired pneumonia in Chile: the clinical relevance in the detection of viruses and atypical bacteria. Thorax 2013;68(11):1000-6. [ Links ]
26. McCullers JA. The co-pathogenesis of influenza viruses with bacteria in the lung. Nat Rev Microbiol 2014;12(4):252-62. [ Links ]














