Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Archivos argentinos de pediatría
Print version ISSN 0325-0075On-line version ISSN 1668-3501
Arch. argent. pediatr. vol.114 no.6 Buenos Aires Dec. 2016
http://dx.doi.org/10.5546/aap.2016.563
ARTÍCULO ESPECIAL
http://dx.doi.org/10.5546/aap.2016.563
Enfermedad hepática grasa no alcohólica: una nueva epidemia en la edad pediátrica
Dra. Mirta Cioccaa, Dra. Margarita Ramonetb y Dr. Fernando Álvarezc
a. Hepatología y Trasplante Hepático Pediátrico. Hospital Alemán. Buenos Aires.
b. Miembro titular del Comité Nacional de Hepatología, Sociedad Argentina de Pediatría (SAP). Miembro del Comité Permanente de la International Pediatric Association (IPA).
c. Departamento de Pediatría. CHU Sainte-Justine. Universidad de Montreal. Canadá.
Correspondencia: Dra. Mirta Ciocca, mciocca@intramed.net
Financiamiento: Ninguno.
Conflicto de intereses: Ninguno que declarar.
Recibido: 18-3-2016
Aceptado: 4-5-2016
RESUMEN
La enfermedad hepática grasa no alcohólica es considerada una de las causas más frecuentes de enfermedad hepática en adultos y niños, lo que coincide con el aumento de la prevalencia de obesidad en ambas poblaciones, en el mundo. Es una enfermedad multifactorial que involucra un amplio espectro de afecciones hepáticas, que van desde la esteatosis simple hasta la esteatohepatitis, caracterizada por hallazgos histopatológicos de inflamación y fibrosis. La patogenia y la progresión están aún incompletamente comprendidas y un conocimiento más cabal de ellas podrá contribuir al desarrollo de pruebas diagnósticas no invasivas y nuevas terapéuticas. La biopsia hepática representa el patrón para el diagnóstico de la fase evolutiva. Aunque las modificaciones del estilo de vida constituyen el objetivo central del tratamiento, el desarrollo de nuevos agentes farmacológicos podría ser promisorio para pacientes que no responden a la terapia de primera línea.
Palabras clave: Enfermedad del hígado graso no alcohólico; Obesidad infantil; Esteatosis hepática.
INTRODUCCIÓN
La enfermedad hepática grasa no alcohólica (non-alcoholic fatty liver disease; NAFLD, por sus siglas en inglés) consiste en la infiltración grasa de más del 5% de los hepatocitos, en ausencia de consumo de alcohol, enfermedades hepáticas inducidas por virus, autoinmunes, metabólicas, drogas, etc.; mientras que la esteatohepatitis no alcohólica (nonalcoholic steatohepatitis; NASH, por sus siglas en inglés) se caracteriza, además, por hallazgos histopatológicos inflamatorios o fibrosis.1-3
Epidemiología
La NAFLD está considerada, durante las tres últimas décadas, como una de las causas más frecuentes de enfermedad hepática en adultos y niños, lo que coincide con el aumento en la prevalencia de obesidad en ambas poblaciones.4
Según la Organización Mundial de la Salud (OMS), la obesidad es una enfermedad crónica compleja y multifactorial que se presenta cuando el consumo de alimentos calóricos supera el gasto energético durante un período suficientemente prolongado. Se inicia, con frecuencia, en la infancia o en la adolescencia y está caracterizada por el aumento de grasa corporal, cuya magnitud y distribución condicionan la salud del individuo.
Es el trastorno nutricional crónico más frecuente en países desarrollados; su prevalencia global es del 16% en edades de entre los 6 y los 12 años. El incremento en las últimas décadas varió entre 2 y 4 veces.
Los niños obesos en edad preescolar tienen 5 veces más probabilidad de presentar sobrepeso en la adolescencia. El 40% de los niños de 7 años y el 70% de los adolescentes con obesidad mantienen la enfermedad en la adultez.5
La prevalencia de la NAFLD está influenciada por varios factores que se originan en una interacción genética y ambiental. Existe una fuerte relación con determinantes ambientales, particularmente en el ámbito familiar, que es el origen de factores que condicionan el balance energético en los niños pequeños. Los padres desempeñan un rol muy importante en la etiología de la obesidad: el estado socioeconómico, el nivel de educación, el trabajo de ambos, el sobrepeso, las relaciones intrafamiliares, la comunicación intrafamiliar, así como la elección de los alimentos y la práctica de actividad física.
El sobrepeso y la obesidad constituyen problemas generalizados en el mundo, específicamente, en América Latina y, sobre todo, en América del Norte y el Caribe, que indican que el sobrepeso afecta a un 23% de los adultos y a un 7% de los niños en edad preescolar.6 En la región, los países del Caribe muestran la más alta prevalencia en adultos. Los países con más obesos son San Cristóbal y Nieves (40,9%), seguido de Bahamas (35%) y Barbados (33,4%). En Latinoamérica, México es el país con mayor tasa de obesidad, que afecta al 32,8% de los adultos; en Venezuela, el 30,8%; en Argentina, el 29,4%; y, en Chile, el 29,1%. En el año 2013, más de 42 millones de niños menores de 5 años tenían sobrepeso en el mundo, de los cuales más del 80% vivía en países en desarrollo.7
¿Cuál es la causa del aumento de los índices de sobrepeso y obesidad infantil en los últimos años?
El crecimiento mundial de la obesidad infantil es producto de múltiples factores, entre los que se destacan los siguientes:
- El aumento del consumo de alimentos industrializados de bajo costo, ricos en grasa, azúcares y sal, pero pobres en fibra y otros nutrientes.
- Los elevados precios de las frutas, los vegetales frescos y otros alimentos de alta calidad nutricional.
- Las estrategias de las corporaciones para aumentar la disponibilidad y el acceso a los alimentos procesados y sus acciones de marketing para promover el consumo de alimentos no saludables y bebidas azucaradas en la infancia.
- La disminución de la actividad física, debida a los estilos de vida cada vez más sedentarios y a las características de la vida urbana.7
A causa del aumento de la incidencia de la obesidad, entre el 20% y el 30% de los adultos y entre el 3% y el 10% de los niños, con una relación masculino-femenino de 2:1 (países occidentales), pueden sufrir de NAFLD. Alcanzan, aproximadamente, del 70% al 80% si consideramos la población de niños obesos.8
En un estudio realizado en San Diego (EE. UU.), de 742 autopsias en una población de 2 a 19 años, entre 1993 y 2003, el 9,6% presentaba NAFLD, que se incrementó al 38% en niños obesos. En relación con las etnias, se observaron los siguientes porcentajes: hispánicos, 12%; asiáticos, 10,2%; anglosajones, 8,6%; y afroamericanos, 1,5%.9
La prevalencia de la NAFLD aumenta con la edad; es más frecuente entre los 11 y los 13 años, en asociación con los cambios hormonales y el desarrollo de una resistencia periférica a la insulina.10
Feldstein y col., en un estudio sobre la historia natural de la NAFLD, en una población de 66 niños, con una edad promedio de 13,9 ± 3,9 años, durante un período de 20 años, hallaron que, en cuatro niños, la enfermedad se desarrollaba hacia la cirrosis y la enfermedad hepática terminal, con la necesidad de un trasplante hepático en su evolución.11
Patogenia
La patogenia y la progresión de la NAFLD están aún comprendidas de manera incompleta. Fue considerada clásicamente como un proceso en dos etapas. Durante la primera etapa, se produce acumulación de grasa en el hígado (esteatosis), hiperinsulinemia e insulinorresistencia, influenciada por la existencia de susceptibilidad genética, mecanismos epigenéticos, un estilo de vida sedentario y dietas hipercalóricas. La esteatosis obedece a la liberación aumentada por el tejido adiposo, una lipogénesis aumentada y el metabolismo de los ácidos grasos alterado. Los triglicéridos acumulados en el hígado derivan, mayormente, de la lipólisis del tejido adiposo (60%) y lipogénesis hepática de novo (26%), y el aporte de la dieta como quilomicrones es mínimo (14%).
La acumulación de lípidos hepáticos exacerba la resistencia a la insulina al interferir en la fosforilación de los receptores de insulina. Esta situación predispone a la segunda etapa, caracterizada por la producción de estrés oxidativo, disfunción mitocondrial, alteración de citoquinas proinflamatorias y activación de las células estrelladas. Estos fenómenos van a conducir a la producción de necrosis, inflamación y fibrosis intrahepática.
Recientemente, se ha propuesto que una afectación de la microbiota y el aumento de la permeabilidad intestinal incrementan la exposición del hígado a productos bacterianos derivados de este, tales como los lipopolisacáridos. Estos productos estimulan los receptores del sistema inmune innatos, los cuales conducen a la activación de los procesos de inflamación y fibrogénesis hepática.
Las células estrelladas del hígado son consideradas la principal fuente productora de matriz extracelular durante el desarrollo de NASH. Además, el compartimento de células hepáticas progenitoras está expandido en niños con NAFLD y su activación participa en la respuesta hepática al estrés oxidativo, en la progresión de la enfermedad y el desarrollo de fibrosis.
Las adipocitoquinas están involucradas en la progresión de esteatosis simple a NASH. Los adipocitos o las células inflamatorias (fundamentalmente, los macrófagos), que infiltran el tejido adiposo en situación de resistencia a la insulina, son responsables de la secreción de adipocitoquinas. La expansión del tejido adiposo, particularmente de la grasa visceral, está asociada con una disminución en la liberación de citoquinas antiinflamatorias y un incremento de moléculas proinflamatorias.
En los últimos años, las teorías fisiopatológicas de la NAFLD se han complementado con el descubrimiento de nuevos polimorfismos genéticos, que podrían promover el desarrollo de NAFLD y luego la progresión a NASH. Cada polimorfismo participa de una etapa diferente, y, en el futuro, la fisiopatología podría considerarse como una "hipótesis de múltiples etapas".1,8,12-14
Clínica
La mayor parte de los niños con NAFLD no presentan síntomas. En algunos casos, se describen síntomas inespecíficos, como dolor abdominal y fatiga. Al momento del examen físico, se observa una circunferencia abdominal aumentada, estrías cutáneas y la presencia de acantosis nigricans en los pliegues cutáneos, las axilas y el cuello, signo característico de resistencia a la insulina. La hepatomegalia se puede detectar en el 50% de los casos, mientras que la esplenomegalia es menos frecuente y se asocia con signos de enfermedad hepática avanzada.
Los niveles de alanina transaminasa (ALT), fosfatasa alcalina y gamma glutamil transferasa pueden estar elevados. La resistencia a la insulina, dislipidemia e hiperuricemia son parámetros orientadores del síndrome metabólico.12,15,16
La medición de la circunferencia abdominal (medida sobre las crestas ilíacas superiores) representa un parámetro antropométrico importante para identificar la adiposidad central, y su incremento puede predecir el riesgo de resistencia a la insulina y el síndrome metabólico.
El índice de masa corporal (IMC) es una herramienta simple, de bajo costo y fácilmente disponible de la relación entre el peso y la talla, que se utiliza, con frecuencia, para identificar el sobrepeso y la obesidad.8
La complejidad del proceso multifactorial y la variedad de los hallazgos histopatológicos de la NAFLD dificultan los esfuerzos para diseñar una adecuada intervención terapéutica.
La aplicación de un algoritmo pediátrico puede ayudar a unificar criterios diagnósticos y a la derivación oportuna de estos pacientes4 (Figura 1).
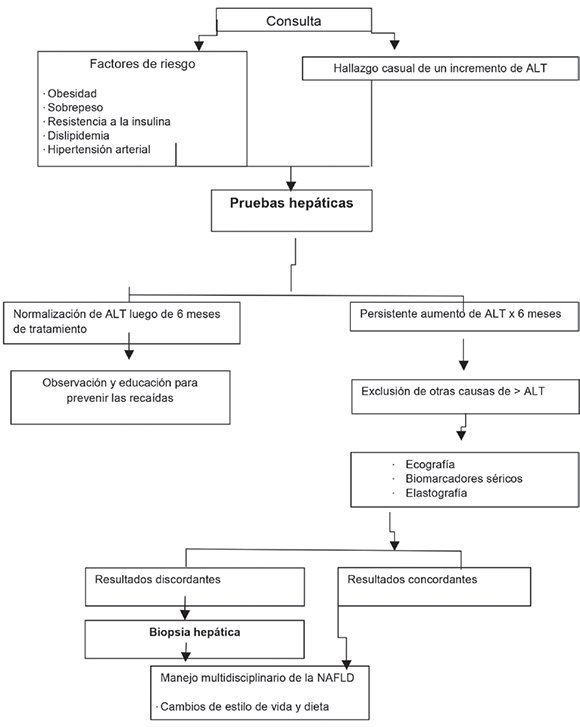
Figura 1. Algoritmo diagnóstico. Alisi, A.,4 adaptado por los autores
Diagnóstico
Debe sospecharse NAFLD en pacientes con sobrepeso u obesidad que presentan hallazgos ultrasonográficos compatibles o ALT elevada (de 2 a 3 veces el límite superior normal). Sin embargo, la ALT no es ni sensible ni específica de NAFLD, ya que los valores pueden fluctuar y hasta ser normales en pacientes con NAFLD, NASH y aun cirrosis.8,12,17
La biopsia hepática se considera el patrón para el diagnóstico de NAFLD y puede distinguir la esteatosis simple de la NASH, definir el grado de fibrosis y colaborar en el diagnóstico diferencial. No obstante, es un procedimiento invasivo, relativamente costoso y asociado a un número infrecuente pero significativo de complicaciones. Además, hay que considerar el error de muestreo al representar una mínima porción del órgano (aproximadamente, 1/50 000), en una patología con distribución desigual.1-3,8
Debido a la elevada prevalencia de la NAFLD, las limitaciones y dificultades de la biopsia hepática, surge la necesidad de contar con modalidades diagnósticas no invasivas. Para este fin, se estudiaron numerosos biomarcadores, pero ninguno resultó suficientemente preciso hasta el momento.7,8,12,16
La ultrasonografía hepática es uno de los estudios de imágenes más utilizado; es la prueba inicial en los pacientes en los que se sospecha NAFLD. Constituye un estudio muy atractivo por su disponibilidad amplia, bajo costo y ausencia de radiación. Sin embargo, no resulta efectiva para detectar esteatosis leve (aproximadamente, < 20% de infiltración grasa), por lo cual un hallazgo normal no descarta NAFLD. Además, depende del operador y del intérprete, con acuerdo intrae interobservador subóptimo. Su eficiencia también está limitada en pacientes con obesidad mórbida.12-16
La tomografía computada puede contribuir al diagnóstico de esteatosis hepática. Tiene mayor especificidad que la ultrasonografía, pero no se aconseja su uso rutinario, debido a la exposición a radiación que genera.12,15-18
La resonancia nuclear magnética (RNM) puede proporcionar una medida cuantitativa de la grasa infiltrada, aunque existen escasos estudios vinculados con su utilización en la población pediátrica. Puede detectar hasta un 3% de esteatosis y está sometida a menor variabilidad, lo que le otorga mayor sensibilidad que la ultrasonografía. Sus limitaciones radican en el elevado costo, el prolongado tiempo de realización del escaneo y la frecuente necesidad de sedación en niños pequeños.12,16,18-20
La espectroscopía de RNM es el método de imágenes más preciso para la detección y cuantificación de la esteatosis. En adultos, demostró una sensibilidad y especificidad del 100% y 97%, respectivamente. Sin embargo, este método tiene las mismas limitaciones que la RNM y necesita un equipo específico, disponible solamente en centros especializados.10,12,16
La elastografía es una técnica aprobada en EE. UU. por la Food and Drug Administration (FDA) para adultos. Consiste en la medición de la velocidad de propagación de ondas elásticas a través del hígado y sirve para evaluar el grado de fibrosis hepática en el paciente de forma no invasiva. En la edad pediátrica, hay estudios de investigación en marcha que nos van a permitir definir su utilidad en esta etapa.10,12,16
Diagnóstico diferencial
La presencia de transaminasas aumentadas en un paciente con sobrepeso u obesidad no es diagnóstico de NAFLD/NASH. Es necesario descartar otras enfermedades musculares o hepáticas antes de vincular al niño/adolescente con dicho diagnóstico.
La NAFLD, por lo general, no ocurre en niños muy pequeños (menores de 3 años) y es rara en menores de 10 años. Para establecer el diagnóstico diferencial, debemos considerar, primero, el cuadro clínico, luego, los hallazgos humorales y, finalmente, la biopsia hepática.
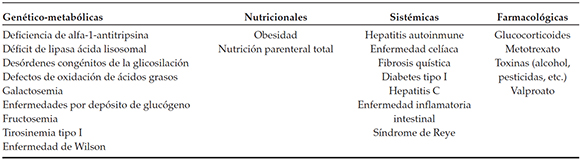
La presencia de esteatosis microvesicular debe alertar acerca de los siguientes diagnósticos posibles: enfermedades mitocondriales, defectos de la oxidación de ácidos grasos, trastornos del ciclo de la urea, deficiencia de lipasa ácida lisosomal (enfermedades de Wolman y de almacenamiento de ésteres de colesterol) y hepatotoxicidad por valproato de sodio. Si estamos frente a una enfermedad hepática crónica con esteatosis hepática que necesitamos diferenciar de NAFLD/NASH, debemos pensar en enfermedad de Wilson, hepatitis autoinmune, hepatitis C crónica, fibrosis quística, deficiencia de alfa-1-antitripsina, etc. En la Tabla 1, se completan los diagnósticos diferenciales más frecuentes de esta entidad.12,16,18
Tabla 1. Causas de esteatosis hepática en niños
Tratamiento
Considerando que la NAFLD puede progresar a enfermedad hepática avanzada y cirrosis, los pacientes deben ser tratados tempranamente.
- Dieta y modificaciones del estilo de vida
El objetivo principal del tratamiento es la implementación de modificaciones del estilo de vida para lograr una pérdida de peso gradual. Una pérdida de peso rápida puede acelerar el proceso inflamatorio a nivel hepático. Al reducir el aporte alimentario e incrementar la actividad física, los pacientes pueden ir perdiendo peso paulatinamente. Se ha demostrado que una reducción del 5% en el IMC se asocia con cambios significativos en la circunferencia abdominal y descenso de los niveles de colesterol, triglicéridos y resistencia a la insulina en niños y disminución de las enzimas hepáticas en adultos. El impacto en la resistencia a la insulina se asocia con la mejoría de la NAFLD. Además, con los cambios en el estilo de vida luego de 24 meses, puede observarse una mejoría histológica notable.
Las dietas infantiles deben estar bien balanceadas para promover un crecimiento armónico. Es aconsejable una reducción en el consumo de hidratos de carbono de liberación rápida (alimentos con fructosa), no solo para mejorar la resistencia a la insulina y reducir la lipogénesis, sino también para contrarrestar los efectos fibrogénicos y proinflamatorios de la fructosa.
En el tratamiento de la obesidad infantil, es fundamental el compromiso de los padres. Se ha demostrado que un cambio de conducta en la familia debe ser el principal objetivo del tratamiento del niño obeso.
Futuros estudios podrán definir el grado de descenso ponderal necesario en el niño para lograr una importante mejoría histológica, como así también cuál es la dieta más apropiada para lograr este objetivo.8,12,14,17,21-23
- Tratamiento farmacológico
El tratamiento farmacológico de la NAFLD ha sido un área de investigación en los últimos años. Ninguno de los fármacos estudiados ha demostrado ser útil en la edad pediátrica.
Los pacientes con NASH y diabetes tienen mayor riesgo de desarrollar una enfermedad hepática más agresiva. Entre los agentes capaces de aumentar la sensibilidad a la insulina en la edad pediátrica' se ha estudiado solamente la metformina, que resultó segura y efectiva en el tratamiento de la diabetes infantil. No se recomienda el uso de este fármaco en pacientes no diabéticos' fuera del campo de la investigación clínica.
Debido a que el estrés oxidativo es considerado un participante potencial en el desarrollo de NASH' se han estudiado una serie de antioxidantes como tratamientos posibles. Un estudio pediátrico, controlado, aleatorizado comparó los tratamientos con vitamina C, vitamina E y placebo, y demostró que 2 años de tratamiento en pacientes con NAFLD con antioxidantes no produjo más mejoría histológica que la dieta y el ejercicio.
Considerando el rol potencial de la flora microbiana en la patogenia de la NAFLD, la modificación de la microbiota intestinal puede colaborar en la prevención y desarrollo de esteatohepatitis. Los resultados preliminares de estudios que utilizan prebióticos y probióticos son promisorios.8,12,14,16,23
- Cirugía bariátrica
La cirugía bariátrica puede disminuir el grado de esteatosis, inflamación hepática y fibrosis en NAFLD. El bypass gástrico en Y de Roux es un procedimiento seguro y efectivo para adolescentes extremadamente obesos. Se debe considerar en pacientes seleccionados, con un IMC > 40 kg/m2 con comorbilidades graves, tales como NAFLD, o en aquellos con un IMC > 50 kg/m2 con comorbilidades más leves. En su indicación pediátrica, es necesario considerar la madurez física y psicológica del paciente, el deseo personal de ser sometido a este, los intentos previos destinados a disminuir el peso y la capacidad de cumplir con el seguimiento necesario.24,25
- La NAFLD es considerada la causa más frecuente de enfermedad hepática crónica en niños y adolescentes.
- Es fundamental su detección y tratamiento tempranos para evitar la progresión hacia una enfermedad hepática terminal.
- El sobrepeso y la obesidad constituyen hoy una verdadera epidemia, como consecuencia de una conducta esencialmente sedentaria, con actividad física insuficiente y el acompañamiento de una dieta hipercalórica y desequilibrada.
- Los Gobiernos, las asociaciones internacionales, las sociedades científicas, la sociedad civil, las organizaciones no gubernamentales y el sector privado tienen una función crucial en la prevención de la obesidad y, por ende, de la NAFLD.
- Los pediatras desempeñan un rol primordial en el reconocimiento oportuno de esta patología y en la implementación de las medidas adecuadas para su prevención.
1. Tiniakos DG, Vos MB, Brunt EM. Nonalcoholic fatty liver disease: pathology and pathogenesis. Annu Rev Pathol 2010;5:145-71. [ Links ]
2. Brunt EM. Pathology of nonalcoholic fatty liver disease. Nat Rev Gastroenterol Hepatol 2010;7(4):195-203. [ Links ]
3. Schwimmer JB, Behling C, Newbury R, Deutsch R, et al. Histopathology of pediatric nonalcoholic fatty liver disease. Hepatology 2005;42(3):641-9. [ Links ]
4. Alisi A, Feldstein AE, Vilani A, Raponi M, et al. Pediatric nonalcoholic liver disease: a multidisciplinary approach. Nat Rev Gastroenterol Hepatol 2012;9(3):152-61. [ Links ]
5. Nader PR, O'Brien M, Houts R, Bradley R, et al. Identifying risk for obesity in early childhood. Pediatrics 2006;118(3):e594-601. [ Links ]
6. Organización de las Naciones Unidas para la Alimentación y la Agricultura (FAO). Panorama de la Seguridad Alimentaria y Nutricional en América Latina y el Caribe 2013. [Acceso: 5 de mayo de 2016]. Disponible en: http://www.fao.org/docrep/019/i3520s/i3520s.pdf.
7. World Health Organization. Obesity and overweight. Geneva: WHO; 2015. [Acceso: 5 de mayo de 2016]. Disponible en: http://www.who.int/mediacentre/factsheets/fs311/en/.
8. Vajro P, Lenta S, Socha P, Dhawan A, et al. Diagnosis of nonalcoholic fatty liver disease in children and adolescents: position paper of the ESPGHAN Hepatology Committee. J Pediatr Gastroenterol Nutr 2012;54(5):700-13. [ Links ]
9. Schwimmer JB, Deutsch R, Kahen T, Lavine JE, et al. Prevalence of fatty liver in children and adolescents. Pediatrics 2006;118(4):1388-93. [ Links ]
10. Feldstein AE, Charatcharoenwitthaya P, Treeprasertsuk S, Benson JT, et al. The natural history of non-alcoholic fatty liver disease in children: a follow-up study for up to 20 years. Gut 2009;58(11):1538-44. [ Links ]
11. Berardis S, Sokol E. Pediatric non-alcoholic fatty liver disease: an increasing public health issue. Eur J Pediatr 2014;173(2):131-9. [ Links ]
12. Fusillo S, Rudolph B. Nonalcoholic fatty liver disease. Pediatr Rev 2015;36(5):198-205. [ Links ]
13. Marzuillo P, Grandone A, Perrone L, Miraglia del Giudice E. Understanding the pathophysiological mechanisms in the pediatric non-alcoholic fatty liver disease: the role of genetics. World J Hepatol 2015;7(11):1439-43. [ Links ]
14. Roberts EA. Pediatric nonalcoholic fatty liver disease (NAFLD): a "growing" problem? J Hepatol2007;46(6): 1133-42. [ Links ]
15. Shannon A, Alkhouri N, Carter-Kent C, Monti L, et al. Ultrasonographic quantitative estimation of hepatic steatosis in children with NAFLD. J Pediatr Gastroenterol Nutr 2011;53(2):190-5. [ Links ]
16. Feldstein Ae, Patton-Ku D, Boutelle KN. Obesity, nutrition and liver disease in children. Clin Liver Dis 2014;18(1): 219-31. [ Links ]
17. Mann JP, Goonetilleke R, McKiernan P. Paediatric nonalcoholic fatty liver disease: a practical overview for nonspecialists. Arch Dis Child 2015;100(7):673-7. [ Links ]
18. Marzuillo P, Grandone A, Perrone L, Miraglia del Giudice E. Controversy in the diagnosis of pediatric non-alcoholic fatty liver disease. World J Gastroenterol 2015;21(21):6444-50. [ Links ]
19. Vos MB. Is it time to advance pediatric NAFLD diagnosis to the magnetic resonance imaging era? Hepatology 2015;61(6):1779-80. [ Links ]
20. Schwimmer JB, Middleton MS, Behling C, Newton KP, et al. Magnetic resonance imaging and liver histology as biomarkers of hepatic steatosis in children with nonalcoholic fatty liver disease. Hepatology 2015;61(6):1887-95. [ Links ]
21. Koot BG, van der Baan-Slootweg OH, Tamminga-Smeulders CL, Rijcken TH, et al. Lifestyle intervention for nonalcoholic fatty liver disease: prospective cohort study of its efficacy and factors related to improvement. Arch Dis Child 2011;96(7):669-74. [ Links ]
22. De Bruyne RM, Fitzpatrick E, Dhawan A. Fatty liver disease in children: eat now pay later. Hepatol Int 2010;4(1):375-85. [ Links ]
23. Gibson PS, Lang S, Gilbert M, Kamat D, et al. Assessment of diet and physical activity in paediatric non-alcoholic fatty liver disease patients: a United Kingdom case control study. Nutrients 2015;7(12):9721-33. [ Links ]
24. Vos MB. NAFLD in the transition from adolescence to young adulthood. Clin Liver Dis 2014;4(4):93-5. [ Links ]
25. Nobili V, Vajro P, Dezsofi A, Fischler B, et al. Indications and limitations of bariatric intervention in severely obese children and adolescents with and without nonalcoholic steatohepatitis: ESPGHAN Hepatology Committee Position Satatement. J Pediatr Gastroenterol Nutr 2015;60(4):550-61. [ Links ]











 text in
text in 


