Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos argentinos de pediatría
versión impresa ISSN 0325-0075versión On-line ISSN 1668-3501
Arch. argent. pediatr. vol.115 no.4 Buenos Aires ago. 2017
http://dx.doi.org/10.5546/aap.2017.374
COMUNICACIONES BREVES
http://dx.doi.org/10.5546/aap.2017.374
Anidulafungina en niños: experiencia de un hospital pediátrico de tercer nivel en Argentina
Dra. María T. Rosanovaa, Dra. Claudia Sarkisa, Dra. Florencia Escarraa, Dra. Carolina Epelbauma, Farm. Norma Sbernab, Dra. Susana Carnovalec, Dr. Carlos Figueroad, Dra. Rosa Bolognaa y Dr. Roberto Ledee
a. Servicio de Infectología, Hospital de Pediatría "Profi Dr. J. P. Garrahan", Ciudad Autónoma de Buenos Aires, Argentina.
b. Servicio de Farmacia, Hospital de Pediatría "Prof. Dr. J. P. Garrahan", Ciudad Autónoma de Buenos Aires, Argentina.
c. Microbiología, Hospital de Pediatría "Prof. Dr. J. P. Garrahan", Ciudad Autónoma de Buenos Aires, Argentina.
d. Servicio de Trasplante de Médula Ósea, Hospital de Pediatría "Prof. Dr. J. P. Garrahan", Ciudad Autónoma de Buenos Aires, Argentina.
e. Universidad Abierta Interamericana (UAI), Buenos Aires, Argentina.
Correspondencia: Dra. María T. Rosanova: margris2@yahoo.com.ar
Financiamiento: Ninguno.
Conflicto de intereses: Ninguno que declarar.
Recibido: 5-1-2017
Aceptado: 21-2-2017
RESUMEN
La experiencia con anidulafungina en el tratamiento de infecciones fúngicas invasivas en pediatría es escasa.
Se presenta nuestra experiencia en 55 niños. La anidulafungina se administró por vía intravenosa en la dosis de carga de 3 mg/kg en una sola dosis diaria, seguida de 1,5 mg/kg cada 24 h durante una media de 14 días (rango, 7-22 d.). La mediana de edad de los pacientes fue de 114 meses (rango intercuartíhco, 32168 m.). Todos los pacientes tenían enfermedades subyacentes. En los trasplantados de médula ósea, la diferencia entre el valor inicial y al final de la administración del fármaco en el recuento de glóbulos blancos, valores de transaminasas y función renal no fue significativo. Ninguno de los pacientes tuvo eventos adversos o murió por causas relacionadas con anidulafungina. La anidulafungina podría ser una opción para la profilaxis o el tratamiento de las infecciones fúngicas invasivas en pediatría, aunque se requieren estudios metodológicamente sólidos para probarlo.
Palabras clave: Anidulafungina; Niños; Infeceionesfúngicas invasivas.
INTRODUCCIÓN
Las infecciones fúngicas invasivas (IFI) son un problema de salud cada vez mayor y se asocian con una alta morbilidad y mortalidad.1
Los últimos fármacos antifúngicos que han aparecido han sido las equinocandinas, que tienen un mecanismo de acción distintivo, ya que inhiben la síntesis del p-1, 3-D-glucano y danan la pared fúngica, sin que las células humanas se afecten, ya que dichas células no contienen p-1, 3-D-glucano.2-5 Estas nuevas opciones terapéuticas se han utilizado en la población adulta, pero, en pacientes pediátricos, la experiencia, sobre todo con anidulafungina, es escasa.
De esas drogas, la anidulafungina fue la última en ser introducida comercialmente y es una equinocandina que presenta un perfil farmacocinético diferente al resto de las equinocandinas. No se metaboliza en el hígado, sino que es degradada en más del 90%, con lentitud, en el plasma mediante un proceso de biotransformación por peptidasas no específicas que abren el anillo de la molécula y forman un sustrato que es degradado terciariamente por proteasas plasmáticas.5 No se excreta por vía renal y tampoco presenta interacciones farmacológicas con las drogas inmunosupresoras.5-8
Tiene una excelente actividad in vitro frente a Candida spp. y Áspergillus spp., incluso en cepas resistentes al fluconazol y a la anfotericina B.1,6
Debido al tipo de metabolismo de la anidulafungina y al modo de eliminación, no se requiere el ajuste de dosis en pacientes con insuficiencia hepática leve, moderada o grave ni tampoco en insuficiencia renal, lo que la hace una droga atractiva para su uso como profilaxis y/o tratamiento de IFI en pacientes trasplantados.
En niños, se informó de efectos adversos leves o moderados relacionados con la infusión, que incluían malestar, rubor y eritema facial, fiebre e hipotensión.2
A pesar de las características favorables de esta droga, la experiencia en pediatría es escasa.
OBJETIVO
El objetivo de este estudio descriptivo-prospectivo es presentar nuestra experiencia con el uso de la anidulafungina en una población pediátrica.
MATERIAL Y MÉTODOS
En el entorno de un hospital pediátrico de tercer nivel público, entre enero y junio de 2016, y debido a la falta temporal de anfotericinas lipídicas, a 55 pacientes se les indicó anidulafungina como profilaxis o tratamiento de IFI probada, probable o posible con un protocolo de seguimiento. Luego de una adecuada revisión bibliográfica y de haberse evaluado la falta de interacciones y los escasos efectos adversos reportados, su uso "off label" fue aprobado por el Comité de Drogas del Hospital.
Determinaciones de laboratorio: Entre los parámetros bioquímicos, se monitorizaron, al principio y al final del tratamiento, en todos los pacientes, el recuento de glóbulos blancos (que se expresó en valor de células/mm3), los niveles de transaminasas (que se expresaron en U/L), la bilirrubina (en mg/dl) y la creatinina (en mg/dl).
Definiciones: Se definieron las IFI de acuerdo con los criterios de la European ürganization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group and the National Institute of Állergy and Infectious Diseases Mycoses Study Group (EORTC/MSG).9
IFI probada: si la histocitopatología era positiva a partir de una biopsia con evidencia de lesión hística asociada o con cultivo microbiologico positivo de una zona estéril con clínica o radiología compatible con infección.
IFI probable: la suma de, al menos, un criterio relativo al huésped más un criterio micologico más un criterio clínico.
IFI posible: cuando existían factores del huésped y evidencia clínica de IFI sin criterios micológicos positivos.
Dosificación: La anidulafungina se administró por vía intravenosa en las dosis recomendadas (de carga de 3 mg/kg, una dosis diaria, seguida de 1,5 mg/kg cada 24 h, tanto fuera para profilaxis como para tratamiento). Se observaron y registraron todos los eventos adversos posibles o probables relacionados con la droga.
Los datos fueron procesados en la base Epi Info versión 6.0. Las variables continuas fueron informadas como mediana y rango intercuartílico (RIC). Las variables categóricas, como cantidad absoluta y frecuencia relativa porcentual.
RESULTADOS
Se incluyeron todos los pacientes que recibieron anidulafungina (n: 55). La mediana de edad de estos fue de 114 meses (RIC: 32168 m). Todos presentaban enfermedades subyacentes, de los cuales el trasplante de médula ósea (29 pacientes, 53%), el trasplante hepático (9 pacientes, 16%) y otros trastornos hematológicos-oncológicos (7 pacientes, 13%) fueron los más comunes (véase la Tabla 1).
Tabla 1. Características de los pacientes (n: 55)
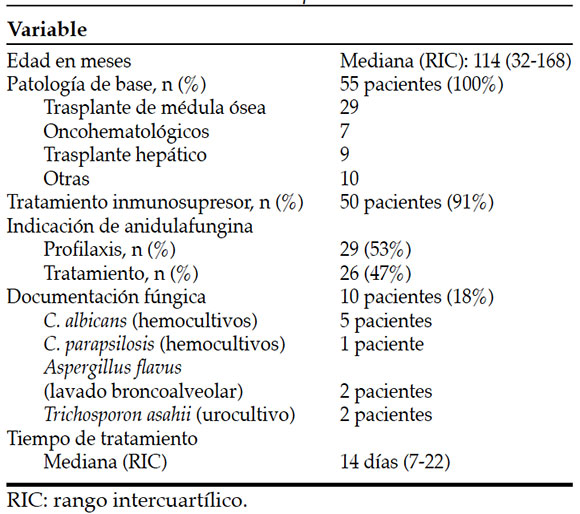
El tratamiento fue administrado durante una media de 14 días (RIC: 7-22 d.) e indicado como tratamiento en 27 pacientes (49%) y como profilaxis en 28 pacientes (51%). En 10 pacientes, se confirmó IFI y Candida albieans fue el hongo más comúnmente aislado (Tabla 1).
En los receptores de trasplante de médula ósea, que constituyeron el grupo más numeroso, se analizaron los valores medios de los parámetros bioquímicos en el inicio del tratamiento y al final. Estos fueron transaminasas: 29,5 U/L y 32 U/L (p: 0,44); bilirrubina: 0,35 y 0,30 mg/dl (p: 0,20); y creatinina: 0,52 y 0,60 mg/dl (p: 0,67). El recuento de glóbulos blancos mostró una gran variabilidad debido a la enfermedad subyacente, pero la diferencia de su valor entre el inicio y el final de la administración del fármaco no fue significativa: mediana de 2810 células/mm3 y 5160 células/mm3, respectivamente (p: 0,07) (véase la Tabla 2).
Tabla 2. Evolución de los parámetros bioquímicos en pacientes con trasplante de médula tratados con anidulafungina (n: 29 pacientes)

Al evaluar la eficacia, se observó que el 100% de los pacientes con IFI tratados con la droga resolvieron su situación infecciosa y el 100% de los pacientes a los cuales se les indicó como profilaxis no desarrollaron infección en el seguimiento a 30 días.
Ninguno de los pacientes presentó eventos adversos leves, moderados o graves o murió por causas relacionadas con anidulafungina. El seguimiento a 30 días fue completo y no hubo casos de recaídas ni mortalidad asociables al uso de la droga.
DISCUSIÓN
Este estudio comenzó a raíz de la falta temporal de anfotericina lipídica en nuestro Hospital. Su uso fue basado en la hipótesis de que la anidulafungina sería mejor tolerada y de eficacia no inferior a otras opciones de tratamiento o profilaxis.
Para decidir su indicación, también se consideró que, a diferencia de otros antifúngicos, no había interacciones conocidas entre la anidulafungina y los inmunosupresores, lo que favorecía su uso en pacientes trasplantados y que los efectos adversos relacionados con la infusión eran menos frecuentes y su costo era menor relacionado con las formulaciones lipídicas de anfotericina.1,5,10,12
Un estudio de fase II en el que se administró anidulafungina a 24 niños, entre 2 y 17 años, con dosis de 0,75 o 1,5 mg/kg de peso corporal por día, informó de efectos adversos leves o moderados, pero, en solo cuatro casos, pudieron calificarse como posible o probablemente relacionados con el fármaco.2
Estos efectos adversos incluían malestar, rubor y eritema facial, elevación de urea, fiebre e hipotensión, situaciones que no se observaron en esta serie. Los resultados mostraron que, en los receptores de trasplante de médula ósea, no hubo necesidad de descontinuar el uso de anidulafungina debido a efectos adversos. En particular, no hubo casos de hepatotoxicidad ni nefrotoxicidad grave directamente atribuible al uso de la droga. Las transaminasas permanecieron estables o disminuyeron durante el tratamiento.
El recuento de glóbulos blancos fue variable en la población estudiada debido a la patología de base de los pacientes y tampoco se constataron alteraciones significativas semejantes a lo reportado en la literatura.2
Tanto cuando fue indicada como tratamiento o como profilaxis, se observaron proporciones de éxito sugerentes de una eficacia suficiente tal como en otras series de pacientes, sobre todo en adultos.1,11,13,15
La poca literatura existente en pediatría avala nuestros hallazgos sobre la seguridad y eficacia de esta droga y enfatiza la necesidad de un mayor número de estudios para consolidar estas afirmaciones.1,3
CONCLUSIONES
Estos resultados justifican planificar estudios metodológicamente apropiados para probar la hipótesis de que la anidulafungina podría ser una opción válida para la profilaxis o el tratamiento de las IFI en los niños.
1. Wilke MW. Invasive Fungal Infections in Infants- Focus on Anidulafungin. Clin Med Insights Pediatr 2013;7:7-11. [ Links ]
2. Gobernado M, Cantón E. Anidulafungina. Rev Esp Quimioter 2008;21(2):99-114. [ Links ]
3. Benjamin DK Jr, Driscoll T, Seibel NL, et al. Safety and pharmacokinetics of intravenous anidulafungin in children with neutropenia at high risk for invasive fungal infections. Antimiorob Agents Chemother 2006;50(2):632-8. [ Links ]
4. Dowell JA, Stogniew M, Krause D, et al. Anidulafungin does not require dosage adjustment in subjects with varying degrees of hepatic or renal impairment. J Clin Pharmaool 2007;47(4):461-70. [ Links ]
5. Reboli AC, Rotstein C, Pappas PG, et al. Anidulafungin versus fluconazole for invasive candidiasis. N Engl J Med 2007;356(24):2472-82. [ Links ]
6. Acuna C. Anidulafungina. Actualización microbiológica y clínica. Drugs of Today 2008;44(Suppl 2):1-25. [ Links ]
7. Catalán González M, Montejo González JC. Nueva aportación en terapia antifúngica: Anidulafungina. Aspectos farmacológicos de la anidulafungina. Rev Iberoam Miool 2008;25:92-100. [ Links ]
8. Dowell JA, Stogniew M, Krause D, et al. Lack of pharmacokinetic interaction between anidulafungin and tacrolimus. J Clin Pharmaool 2007;47(3):305-14. [ Links ]
9. De Pauw B, Walsh TJ, Donnelly JP, et al. Revised definitions of invasive fungal disease from the European Organization for Research and Treatment of Cancer/Invasive Fungal Infections Cooperative Group and the National Institute of Allergy and Infectious Diseases Mycoses Study Group (EORTC/MSG) Consensus Group. Clin Infeot Dis 2008;46(12):1813-21. [ Links ]
10. Denning DW. Echinocandin antifungal drugs. Lanoet 2003;362(9390):1142-51. [ Links ]
11. Tapisiz A. Anidulafungin: is it a promising option in the treatment of pediatric invasive fungal infections? Expert Rev Anti Infeot Ther 2011;9(3):339-46. [ Links ]
12. Pappas PG, Kauffman CA, Andes DR, et al. Clinical Practice Guideline for the Management of Candidiasis: 2016 Update by the Infectious Diseases Society of America. Clin Infeot Dis 2016;62(4):e1-50. [ Links ]
13. Liu P, Ruhnke M, Meersseman W, et al. Pharmacokinetics of anidulafungin in critically ill patients with candidemia/invasive candidiasis. Antimiorob Agents Chemother 2013;57(4):1672-6. [ Links ]
14. Ghannoum M, D'Angelo M. Anidulafungin: A potent antifungal that targets Candida and Aspergillus. Infeot Dis Clin Praot 2005;13(4):165-78. [ Links ]
15. Azanza Perea JR. Equinocandinas: aspectos aplicados de la farmacología. Rev Iberoam Miool 2016;33(3):140-4. [ Links ]














