Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos argentinos de pediatría
versión impresa ISSN 0325-0075versión On-line ISSN 1668-3501
Arch. argent. pediatr. vol.115 no.5 Buenos Aires oct. 2017
http://dx.doi.org/10.5546/aap.2017.470
ARTÍCULO ORIGINAL
http://dx.doi.org/10.5546/aap.2017.470
Efectos adversos relacionados con la linezolida en la práctica clínica pediátrica
Prof. Asoc. Dr. Nuri Bayrama, Dra. Mine Düzgöla, Dra. Ahu Karaa, Dr. Fatih M. Özdemirb y Prof. Asoc. Dr. İlker Devrima
a. Departamento de Enfermedades Infecciosas Pediátricas, Hospital Pediátrico Dr. Behçet Uz, Esmirna, Turquía.
b. Hospital Pediátrico Dr. Behçet Uz, Esmirna, Turquía.
Correspondencia: Dr. Nuri Bayram: nuribayram@gmail.com
Financiamiento: Ninguno.
Conflicto de intereses: Ninguno que declarar.
Recibido: 2-2-2017
Aceptado: 24-4-2017
RESUMEN
Introducción. La linezolida puede causar efectos adversos, como trombocitopenia, que, según lo observado, se relacionan con la administración de linezolida durante más de 2 semanas. Se ha realizado una cantidad limitada de estudios sobre la seguridad y el momento de aparición de los efectos adversos relacionados con la linezolida en los niños. El objetivo de este estudio fue evaluar la incidencia de los efectos adversos asociados con la linezolida, especialmente en relación con el momento de su aparición.
Población y métodos. Se incluyeron a todos los niños (< 18 años de edad) que recibieron tratamiento con linezolida durante > 3 días. Se evaluaron los efectos adversos atribuidos a la linezolida y el momento de aparición de los efectos secundarios.
Resultados. En total, se incluyeron 179 niños. La mediana de edad de los pacientes fue 4 años (entre 6 días y 17 años). Durante el tratamiento con linezolida, 36 (20,1%) pacientes tuvieron efectos adversos. El efecto adverso más frecuente fue la trombocitopenia, detectada en 26 (14,5%) pacientes. Los demás efectos adversos fueron: elevación de las enzimas hepáticas en 4 pacientes, leucopenia y anemia en 2 pacientes, disfunción renal en 1 y reacciones cutáneas graves en 3 pacientes. Los efectos adversos se detectaron dentro de una mediana de 7,5 días de tratamiento (intervalo: de 4 a 18 días). Entre los 36 pacientes, 26 (72,2%) presentaron un efecto adverso en los primeros 10 días de tratamiento.
Conclusiones. Se detectaron efectos adversos transitorios en el 20,1% de los pacientes durante el tratamiento con linezolida. Estos efectos adversos podrían detectarse antes de los 10 días de tratamiento. La linezolida debe recetarse de manera segura a los niños siempre que se vigilen los efectos adversos, en especial el recuento de trombocitos y el nivel de enzimas hepáticas.
Palabras clave: Linezolida; Efectos adversos; Niño; Trombocitopenia.
INTRODUCCIÓN
La linezolida es el primer antibiótico de la clase de las oxazolidinonas aprobado y usado en niños, incluidos los recién nacidos prematuros.1,2 Tiene una actividad excelente contra la mayoría de las bacterias grampositivas sensibles a la meticilina y meticilino-resistentes.3 Inicialmente, la linezolida fue aprobada en 2002 por la Administración de Alimentos y Medicamentos de los Estados Unidos para su uso pediátrico, en el tratamiento de infecciones, como las cutáneas y de partes blandas, neumonías intra- y extrahopitalarias e infecciones por Enterococcus faecium resistente a la vancomicina.4 En comparación con los antibióticos glucopéptidos, las ventajas de la linezolida son su eficacia clínica y microbiológica, la excelente penetración tisular y el hecho de que no es necesario determinar la concentración plasmática del fármaco.5 Su perfil de toxicidad es bajo frente a los antibióticos glucopéptidos. Sin embargo, se ha informado que la linezolida causa efectos adversos graves, como neuropatía, elevación de las enzimas hepáticas y mielosupresión, incluso trombocitopenia y leucopenia.6
Los datos sobre los efectos adversos de la linezolida se basan principalmente en informes relacionados con su uso en adultos. En la actualidad, existe una cantidad limitada de estudios sobre la seguridad de la linezolida en los pacientes pediátricos. Por lo tanto, el objetivo de este estudio es evaluar la incidencia de los efectos adversos asociados con la linezolida, especialmente en relación con el momento de su aparición.
MATERIALES Y MÉTODOS
Este estudio retrospectivo se llevó a cabo entre junio de 2010 y junio de 2015 en el Hospital Pediátrico Dr. Behget Uz, un centro de referencia para enfermedades infecciosas pediátricas en la región del Egeo en Turquía. En este estudio se incluyó a todos los niños (< 18 años de edad) que recibieron tratamiento con linezolida durante > 3 días por una infección causada por bacterias grampositivas, ya fuera presunta o confirmada. Se excluyó a todos los pacientes con un recuento anormal de trombocitos (< 150 x 109/l) antes del tratamiento.
Los datos de los pacientes se obtuvieron a partir de las historias clínicas, e incluyeron características demográficas (edad, sexo, prematurez, antecedentes médicos); enfermedades preexistentes o comorbilidades; duración de la hospitalización; datos sobre el tipo de microorganismo e infección; posología y duración del tratamiento con linezolida; desenlace del tratamiento con linezolida.
La linezolida se administró por vía intravenosa en dosis de 10 mg/kg tres veces al día a niños de 0 a 11 años y de 10 mg/kg (dosis máxima: 600 mg) dos veces al día a los niños mayores.
Los datos de laboratorio, incluidas las características hemáticas (recuento de glóbulos blancos, valor de hemoglobina, recuento de trombocitos), los análisis bioquímicos de rutina y las pruebas funcionales hepáticas y renales se registraron a partir de las historias clínicas. También se evaluaron los efectos secundarios atribuidos a la linezolida. Los efectos adversos se definieron como eventos que ocurrieron durante el uso de linezolida que no podían explicarse a partir de la evolución clínica natural de las enfermedades preexistentes o por el uso de otros fármacos. Por este motivo, se evaluó lo siguiente: efectos hemáticos, que incluyeron leucopenia, trombocitopenia, anemia; disfunción hepática, que incluyó hiperbilirrubinemia, aumento de las transaminasas hepáticas (incremento de la alaninaaminotransferasa por encima de tres veces el límite superior normal); efectos gastrointestinales, que incluyeron náuseas, vómitos, pancreatitis y diarrea; nefrotoxicidad, que incluyó disfunción renal aguda (aumento de la creatinina de > 50% respecto del valor basal o un descenso de la tasa de filtración glomerular de > 25%, o disminución de la diuresis a menos de 0,5 ml/kg/h durante 6 horas o más); efectos cutáneos, que incluyeron sarpullido y picazón; y deterioro neurológico. La trombocitopenia se definió como recuento de trombocitos de < 150 x 109/l o una reducción del 50% en el recuento de trombocitos respecto del valor basal al inicio del tratamiento con linezolida.7
Los desenlaces de los pacientes se definieron como cura, mejoría clínica o fracaso según la respuesta al tratamiento con linezolida. La cura se definió como la resolución de las manifestaciones clínicas y de laboratorio de la infección para la cual se administró la linezolida. La persistencia o el avance de los signos de infección o la ausencia de erradicación microbiológica eran indicativos del fracaso del tratamiento. La mejoría clínica se definió como cualquier situación entre el fracaso y la cura. La mortalidad se definió como muerte durante el tratamiento y el seguimiento.
El análisis estadístico se realizó con el programa SPSS, versión 20.0 (IBM Corp., Somers, NY). Las variables categóricas se analizaron con la prueba de y2 o la prueba exacta de Fisher. Las variables continuas se analizaron con la prueba t de Student o la prueba U de Mann-Whitney. Un valor de P < 0,05 se consideró estadísticamente significativo.
RESULTADOS
Durante el período de estudio, se evaluaron los datos de 211 pacientes tratados con linezolida. De estos, se excluyó a 24 debido a datos inadecuados. También se excluyó a 8 pacientes que fallecieron en los tres primeros días del tratamiento con linezolida. En total, se incluyeron 179 niños en el estudio. La mediana de edad de los pacientes al momento del ingreso era de 4 años (de 6 días a 17 años); 106 (59,2%) eran varones y 73 (40,8%), mujeres. Entre los pacientes, 16 habían nacido de manera prematura; 3 (1,6%) de ellos con una edad gestacional de < 28 semanas, 8 (4,4%) entre las 28 y las 32 semanas de gestación, y 5 (2,7%), entre las 32 y las 36 semanas. La mediana de duración del tratamiento con linezolida fue de 12 días (intervalo: de 4 a 31 días). En la Tabla 1, se describen las características basales.
Tabla 1. Características clínicas y demográficas de los 179 pacientes incluidos en el estudio
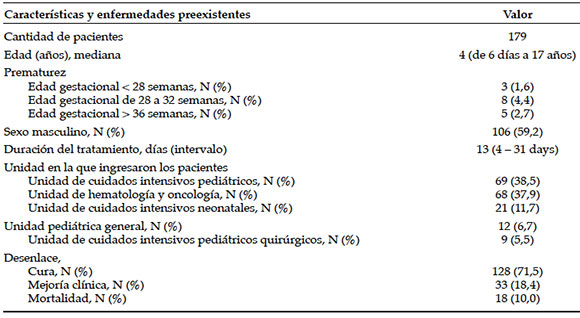
En relación con los tratamientos, 69 (38,5%) se administraron a pacientes internados en la unidad de cuidados intensivos pediátricos, 68 (37,9%) a pacientes de la unidad de oncología y hematología pediátricas, 21 (11,7%) a pacientes neonatales, 12 (6,7%) a pacientes con inmunodeficiencia y 9 (5,5%) a pacientes de la unidad de cuidados intensivos pediátricos. En la Tabla 2, se muestran la cantidad y las proporciones de pacientes con enfermedades preexistentes y comorbilidades.
Tabla 2. Indicaciones clínicas para el tratamiento con linezolida en los 179 pacientes

A todos los niños se les administró la linezolida como tratamiento de segunda línea, excepto a los pacientes en los que se documentó Enterococcus resistente a la vancomicina o Staphylococcus resistente a la vancomicina. La linezolida se administró principalmente debido al fracaso clínico de los pacientes mientras recibían tratamiento con glucopéptidos (85/179 casos, 47,4%). Se administró el tratamiento basado en el objetivo según el diagnóstico documentado microbiológicamente a 94 (52,5%) niños. Entre ellos, el microorganismo patógeno aislado con mayor frecuencia fue el estafilococo coagulasa negativo (53 casos, 29,6%), seguido del enterococo resistente a la vancomicina (39 casos, 21,7%) y el Staphylococcus aureus resistente a la meticilina (2 casos, 1,1%). Todos los microorganismos aislados eran susceptibles a la linezolida (concentración inhibitoria mínima < 2 mg/l) según las pautas del Instituto de Normas Clínicas y de Laboratorio (Clinical and Laboratories Standards Institute, CLSI).8
Las localizaciones de las infecciones clínica y microbiológicamente confirmadas fueron las siguientes: en 134 pacientes (74,9%), el torrente sanguíneo; en diez y nueve pacientes (10,6%), las vías urinarias; en diez pacientes (5,6%), el sistema nervioso central; en nueve pacientes (5,0%) neumonía asociada al respirador; en seis pacientes (3,3%), absceso de partes blandas; y en un paciente, peritonitis.
Durante el tratamiento con linezolida, 36 (20,1%) pacientes tuvieron efectos adversos. El efecto adverso principal del tratamiento con linezolida fue la trombocitopenia. Se detectó trombocitopenia inducida por linezolida en 26 (14,5%) pacientes. Se detectaron recuentos finales de trombocitos de < 50 x 109/l en 11 (6,1%) pacientes; 2 de ellos requirieron transfusión de plaquetas. En los 15 (8,3%) pacientes restantes, se detectaron disminuciones en el recuento de trombocitos de más del 50% respecto del valor inicial con un recuento de < 150 x 109/l. Se observaron leucopenia y anemia en dos (1,1%) pacientes. No se observaron casos de neutropenia durante el tratamiento.
Los demás efectos adversos fueron aumento transitorio de las enzimas hepáticas en cuatro (2,2%) pacientes, disfunción renal en uno y reacciones cutáneas graves con exantema y picazón en tres (1,6%). Todas ellos fueron reversibles. En la Tabla 3, se enumeran los efectos adversos asociados con el tratamiento con linezolida.
Tabla 3. Efectos adversos asociados con el tratamiento con linezolida (36/179 pacientes, 20,1%)
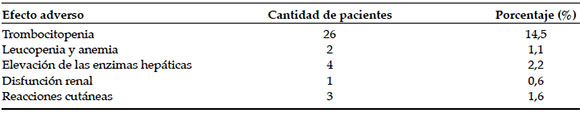
Se consideró que 128 (71,5%) pacientes se curaron y que 33 (18,4%) pacientes tuvieron una mejoría clínica. La tasa de mortalidad fue del 10,0% (18/179 pacientes) durante el tratamiento debido a choque séptico e insuficiencia respiratoria, mayormente atribuidos a las enfermedades preexistentes.
Correlación de los efectos adversos con la duración del tratamiento con linezolida:
La mediana de duración del tratamiento con linezolida fue de 13 días (de 4 a 31 días) en los niños sin efectos adversos causados por linezolida, y de 12 días (de 5 a 28 días) en los niños con efectos adversos; no se observaron diferencias significativas entre ambos períodos en relación con la duración del tratamiento con linezolida (p= 0,297). Los pacientes que recibieron tratamiento con linezolida tuvieron efectos adversos con una mediana de 7,5 días de tratamiento (de 4 a 18 días). Veintiséis (72,2%) de 36 pacientes tuvieron un efecto adverso en los primeros 10 días y el resto (27,8%), después de transcurridos los primeros 10 días de tratamiento (los datos se muestran en la Figura 1). La trombocitopenia fue el efecto adverso más frecuente en 17 (77,2%) pacientes en el primer período, mientras que en 5 (22,7%) pacientes apareció después de los primeros 10 días de tratamiento.

Figura 1. Efectos adversos acumulados durante los días de tratamiento con linezolida; la mayoría de los pacientes los acumularon en los primeros 10 días de tratamiento con linezolida (77,2% frente a 22,78%)
DISCUSIÓN
La linezolida tiene actividad antibacteriana contra las bacterias grampositivas. En estudios clínicos de gran tamaño, se evaluaron la seguridad y la eficacia de la linezolida en adultos.
Este informe incluye una de las poblaciones pediátricas más amplias tratada con linezolida. En este estudio, se señala que los efectos adversos asociados con la linezolida no son frecuentes y podrían detectarse durante la primera etapa del tratamiento.
La mayor parte de la población del estudio recibió linezolida como tratamiento basado en el objetivo según el diagnóstico documentado microbiológicamente y los desenlaces generales fueron favorables, con altas tasas de cura y mejoría clínica en el 90% de los pacientes. Las tasas de éxito son similares a las observadas en el estudio realizado por Garazzino y cols.9 Si bien la linezolida suele ser bien tolerada, existe cierta preocupación respecto de la toxicidad sanguínea, incluidas la neutropenia y la trombocitopenia, que, según lo observado, se relaciona con la dosis y la duración del tratamiento.10 L a trombocitopenia es un efecto adverso frecuente en los pacientes adultos y, según se ha señalado, la incidencia de trombocitopenia relacionada con linezolida ha sido del 15% al 50%.7,11,12 Los otros efectos secundarios frecuentes que se publicaron en relación con el tratamiento con linezolida fueron diarrea, náuseas, cefalea, neuropatía y pruebas funcionales hepáticas anormales.13 Estos efectos adversos se detectaron mayormente en los pacientes que recibieron linezolida durante más de dos semanas.13
A pesar de su uso cada vez mayor, los datos clínicos sobre la linezolida en la población pediátrica son limitados. En algunos estudios pediátricos, se documentó que entre el 18,8% y el 25,6% de los niños tuvieron efectos adversos asociados con el tratamiento con linezolida, en su mayoría, alteraciones de la función hepática, hematológicas y gastrointestinales.9 En el estudio actual, la trombocitopenia fue el efecto adverso más frecuente asociado con la linezolida compatible con la bibliografía. Si bien este efecto adverso fue leve y reversible en general, dos de los pacientes en quienes se detectó trombocitopenia requirieron la transfusión de plaquetas, por lo que es crucial supervisar los parámetros hematológicos. Los demás efectos adversos detectados en nuestra población fueron elevación de las enzimas hepáticas, reacciones cutáneas, leucopenia, anemia y disfunción renal, todos reversibles. Al contrario de lo indicado en la bibliografía, ninguno de los pacientes tuvo neutropenia o neuropatía, la cual también estuvo asociada con los niños tratados con linezolida.14,15 En este estudio, tampoco se detectaron efectos adversos asociados con alteraciones gastrointestinales, probablemente debido al uso exclusivo de linezolida por vía intravenosa.
En los adultos, se informó que el uso prolongado de linezolida estaba asociado con efectos adversos, en especial trombocitopenia a causa de la mielosupresión.5 En general, los efectos adversos se informaron con menor frecuencia en los niños que en los adultos tratados con linezolida, tal vez debido a la menor susceptibilidad de los niños a la toxicidad mitocondrial, y a la menor cantidad de casos de tratamiento prolongado.916 Se desconoce el mecanismo preciso de la trombocitopenia, aunque se ha propuesto un fenómeno mediado por el sistema inmunitario.6 Los datos de estudios clínicos indican que la mielosupresión está asociada con el tratamiento prolongado.17 La trombocitopenia y un leve aumento del riesgo de anemia fueron evidentes en los pacientes que recibieron tratamiento con linezolida durante más de 2 semanas.5 Según los estudios en adultos, existe un riesgo leve de trombocitopenia que aumenta con la mayor duración del tratamiento con linezolida, aunque es reversible al suspender la administración del fármaco.18 Sin embargo, según los datos de estudios clínicos pediátricos, el tratamiento más breve con linezolida también causaría trombocitopenia leve reversible en los niños.19 Al contrario de la mayoría de los datos, casi todos los pacientes en el estudio actual tuvieron efectos adversos dentro de los primeros 10 días de tratamiento. La trombocitopenia fue el efecto adverso más frecuente en ese período. De manera similar, también se informaron tratamientos más breves asociados con efectos adversos, en especial trombocitopenia. Zhang y cols., publicaron que el tratamiento con linezolida durante 7 días estuvo asociado con trombocitopenia y concluyeron que una duración menor a 2 semanas también podría causar efectos adversos.18 Orrick y cols., propusieron que el riesgo de trombocitopenia podría presentarse incluso antes del período de 14 días de tratamiento con linezolida.20 En un estudio con 108 pacientes pediátricos también se observó que la duración del tratamiento con linezolida no se correlacionaba con los efectos adversos.14 La acidosis láctica es un efecto adverso poco frecuente del tratamiento con linezolida que se produce en los pacientes adultos que reciben un tratamiento más prolongado con este fármaco.21 Sin embargo, la acidosis láctica relacionada con la linezolida en niños tiende a desarrollarse antes que en los adultos; según un par de informes, se detectó acidosis láctica en los primeros dos días de iniciada la administración de linezolida.22,23 Por lo tanto, puede suponerse que los efectos adversos en niños podrían ocurrir antes que en los adultos debido a las diferencias en la farmacocinética y la toxicodinámica de la linezolida en la población pediátrica.
En el estudio actual, 21 (11,7%) pacientes eran recién nacidos; de ellos, 16 eran prematuros. Se detectaron efectos adversos transitorios solamente en tres pacientes; dos de ellos tuvieron trombocitopenia y el otro, elevación de las enzimas hepáticas. El tratamiento con linezolida fue seguro y eficaz en el período neonatal, de manera similar a lo descrito en la bibliografía.2,14
Cabe destacar varias consideraciones a la hora de interpretar los resultados. En primer lugar, se trató de un estudio retrospectivo, con limitaciones inherentes en comparación con los estudios clínicos aleatorizados. En segundo lugar, en este estudio se incluyó a todos los niños con enfermedades preexistentes y comorbilidades diferentes. En tercer lugar, es muy difícil identificar ciertos efectos en la población pediátrica, como la neuropatía, por lo que los efectos adversos observacionales podrían pasar inadvertidos. No obstante, se debe notar que el estudio actual incluye una de las poblaciones pediátricas más grandes tratadas con linezolida. Teniendo en cuenta los datos, la linezolida debe indicarse de manera segura a los pacientes pediátricos siempre que se vigilen los efectos adversos, en especial el recuento de trombocitos y el nivel de enzimas hepáticas.
A modo de conclusión, en el estudio actual se detectaron efectos adversos transitorios en el 20,1% de los pacientes durante el tratamiento con linezolida. Los efectos adversos pudieron detectarse antes de los 10 días de tratamiento. Se debe evaluar el uso de linezolida en niños mediante estudios controlados aleatorizados y prospectivos para respaldar nuestros datos.
1. Chiappini E, Conti C, Galli L, et al. Clinical efficacy and tolerability of linezolid in pediatric patients: a systematic review. Clin Ther 2010;32(1):66-88. [ Links ]
2. Kocher S, Muller W, Resch B. Linezolid treatment of nosocomial bacterial infection with multiresistant Grampositive pathogens in preterm infants: a systematic review. Int J Antimicrob Agents 2010;36(2):106-10. [ Links ]
3. Gostelow M, Gonzalez D, Smith PB, et al. Pharmacokinetics and safety of recently approved drugs used to treat methicillin-resistant Staphylococcus aureus infections in infants, children and adults. Expert Rev Clin Pharmacol 2014;7(3):327-40. [ Links ]
4. Dotis J, Iosifidis E, Ioannidou M, et al. Use of linezolid in pediatrics: a critical review. Int J Infect Dis 2010;14(8):e638-48. [ Links ]
5. Bassetti M, Baguneid M, Bouza E, et al. European perspective and update on the management of complicated skin and soft tissue infections due to methicillin-resistant Staphylococcus aureus after more than 10 years of experience with linezolid. Clin Microbiol Infect 2014;20Suppl 4:3-18. [ Links ]
6. Vinh DC, Rubinstein E. Linezolid: a review of safety and tolerability. J Infect 2009;59 (Suppl 1):S59-74. [ Links ]
7. Natsumoto B, Yokota K, Omata F, et al. Risk factors for linezolid-associated thrombocytopenia in adult patients. Infection 2014;42(6):1007-12. [ Links ]
8. Tenover FC, Moellering RC Jr. The rationale for revising the Clinical and Laboratory Standards Institute vancomycin minimal inhibitory concentration interpretive criteria for Staphylococcus aureus. Clin Infect Dis 2007;44:1208-15. [ Links ]
9. Garazzino S, Krzysztofiak A, Esposito S, et al. Use of linezolid in infants and children: a retrospective multicentre study of the Italian Society for Paediatric Infectious Diseases. J Antimicrob Chemother 2011;66(10):2393-7. [ Links ]
10. Bradley JS, Sauberan JB. Antimicrobial agents. En: Long SS, Pickering LK, Prober CG, eds. Principles and Practice of Pediatric Infectious Diseases. 4th ed. New York: Elsevier Saunders; 2012.Pags.1453-84. [ Links ]
11. Chen C, Guo DH, Cao X, et al. Risk factors for thrombocytopenia in adult Chinese patients receiving linezolid therapy. Curr Ther Res Clin Exp 2012;73(6):195-206. [ Links ]
12. Takahashi Y, Takesue Y, Nakajima K, et al. Risk factors associated with the development of thrombocytopenia in patients who received linezolid therapy. J Infect Chemother 2011;17(3):382-7. [ Links ]
13. Rodvold KA, McConeghy KW. Methicillin-resistant Staphylococcus aureus therapy: past, present, and future. Clin Infect Dis 2014;58Suppl 1:S20-7. [ Links ]
14. Simon A, Mullenborn E, Prelog M, et al. Use of linezolid in neonatal and pediatric inpatient facilities: results of a retrospective multicenter survey. Eur J Clin Microbiol Infect Dis 2012;31(7):1435-42. [ Links ]
15. Nambiar S, Rellosa N, Wassel RT, et al. Linezolid-associated peripheral and optic neuropathy in children. Pediatrics 2011;127(6):1528-32. [ Links ]
16. Garcia-Prats AJ, Rose PC, Hesseling AC, et al. Linezolid for the treatment of drug-resistant tuberculosis in children: A review and recommendations. Tuberculosis(Edinb) 2014;94(2):93-104. [ Links ]
17. Gerson SL, Kaplan SL, Bruss JB, et al. Hematologic effects of linezolid: summary of clinical experience. Antimicrob Agents Chemother 2002;46(8):2723-6. [ Links ]
18. Zhang Z, Liang Z, Li H, et al. Comparative evaluation of thrombocytopenia in adult patients receiving linezolid or glycopeptides in a respiratory intensive care unit. Exp Ther Med 2014;7(2):501-7. [ Links ]
19. Meissner HC, Townsend T, Wenman W, et al. Hematologic effects of linezolid in young children. Pediatr Infect Dis J 2003;22(9):S186-92. [ Links ]
20. Orrick JJ, Johns T, Janelle J, et al. Thrombocytopenia secondary to linezolid administration: what is the risk? Clin Infect Dis 2002;35(3):348-9. [ Links ]
21. Boutoille D, Grossi O, Depatureaux A, et al. Fatal lactic acidosis after prolonged linezolid exposure for treatment of multidrug-resistant tuberculosis. Eur J Intern Med 2009;20(6):e134-5. [ Links ]
22. Ozkaya-Parlakay A, Kara A, Celik M, et al. Early lactic acidosis associated with linezolid therapy in paediatric patients. Int J Antimicrob Agents 2014;44(4):334-6. [ Links ]
23. Su E, Crowley K, Cardllo JA, et al. Linezolid and lactic acidosis: a role for lactate monitoring with long-term linezolid use in children. Pediatr Infect Dis J 2011;30(9):804-6. [ Links ]














