INTRODUCCIÓN
La tiroiditis linfocitaria crónica (TLC) es la causa más frecuentede hipotiroidismo adquirido en lainfancia y la adolescencia, con unaprevalencia cercana al 2 % en los niñosy predominio en el género femenino (4 : 1).1,2 El cuadro clínico es más gravecuanto más tardío es el diagnóstico, con mayor compromiso de la tallafinal.2
Existe escasa bibliografía acerca del impacto en la talla final en los niñoscon hipotiroidismo adquirido grave (HAG), por lo cual nuestro objetivofue detectar a aquellos pacientes quepresentaban mayor riesgo de baja talla adulta según el estadio puberal y latalla al momento del diagnóstico.
MATERIALES Y MÉTODOS
Estudio descriptivo retrospectivo de pacientes menores de 18 añoscon diagnóstico de HAG por TLC, atendidos desde 2008 a 2014 en uncentro pediátrico de alta complejidad.
Los criterios de inclusión al momento del diagnóstico fueronlos siguientes: hormona estimulantede la tiroides (thyroid stimulatinghormone; TSH, por sus siglas en inglés)> 50 µIU/ml con dosajes de hormonastiroideas bajos para los rangos dereferencia según la edad y anticuerposantitiroideos positivos (anticuerpoantitiroperoxidasa tiroidea -ATPO-y/o anticuerpo antitiroglobulinaultrasensible -ATGU). Se excluyeronaquellos pacientes con algunaotra causa que pudiera afectar elcrecimiento.
Las variables analizadas fueron género, edad, talla, estadio puberal, edad ósea (EO) al momento deldiagnóstico y, en las siguientes visitas, presencia de bocio. La talla se expresócomo puntuaciones de desviaciónestándar (SDE) y se normalizaron parala edad y el género.3 La EO fue evaluadapor el mismo endocrinólogo infantilcon el método de Greulich y Pyle. Enaquellos casos en los que se obtuvieronlas tallas de ambos padres, se calcularonlas tallas medias parentales.
Las determinaciones fueron realizadas por quimioluminiscencia, TSH, T3, T4L en plataforma Architect, i4000 Abbott y T4, ATPO y ATGU en plataforma IMMULITE 2000, Siemens. Para TSH y hormonas tiroideas, se utilizaron losvalores de referencia previamente publicados. 4 Eldesarrollo puberal fue evaluado según el métodode Tanner, y el volumen testicular, utilizando elorquidómetro de Prader. Todos los pacientes, luego del diagnóstico, iniciaron el reemplazo conlevotiroxina.
Se consideró talla cercana a la final cuando la velocidad de crecimiento era menor de 0,5 cm/año y/o presentaron EO adulta. Se definió tallabaja cuando era < -2,5 SDE y talla normal, cuandoera > -2,5 SDE. Los pacientes con talla cercana a lafinal fueron divididos en cuatro grupos:
Grupo 1 (G1): prepúber con talla baja.
Grupo 2 (G2): prepúber con talla normal.
Grupo 3 (G3): púber con talla baja.
Grupo 4 (G4): púber con talla normal.
Para analizar las asociaciones entre las distintas variables, se realizó el test de análisisde varianza (analysis of variance; ANOVA, por sussiglas en inglés). Se compararon en cada grupola talla al momento del diagnóstico y la cercana a la final.
El estudio fue aprobado por el Comité de Ética institucional y se garantizó la protección integralde datos de los pacientes.
RESULTADOS
Se evaluaron 79 pacientes; el 78 % (n: 62) fueron mujeres. La mediana de edad al momentodel diagnóstico fue de 10,9 años, con rango deentre 10 y 12 años.
Al analizar las asociaciones entre las variables, se encontró que los que presentaron bocio (n:45) mostraron mejor talla en el diagnóstico queaquellos que no lo presentaban; SDE medio detalla: 0,2 vs. -2,42 (T = -5,13; p < 0,0001).
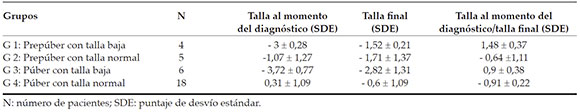
Solo se obtuvo la talla final de 33 pacientes, ya que, al momento actual, algunos no alcanzaron latalla final y otros perdieron seguimiento (Tabla 1).
Veintitrés pacientes (G2 y G4) se presentaron con talla normal al momento del diagnóstico;19 de ellos finalizaron con talla normal para lapoblación (8 dentro del rango genético, 2 debajode este y, en los 9 restantes, no se contó condatos antropométricos del padre). Los 4 restantesfinalizaron con talla baja por mala adherencia altratamiento.
Diez pacientes presentaron talla baja al momento del diagnóstico y los prepuberales (G1) finalizaron con una talla final significativamentemayor que los puberales (G3) (p = 0,0311). Losprepúberes tuvieron una mediana de tiempode seguimiento de 6,83 años, y los púberes, de 2.5 años.
En la Tabla 2, se muestran las características clínicas del G1. Los 4 pacientes finalizaroncon talla final normal para la población (SDE:1,48 ± 0,37). Las niñas presentaron su menarca 1.5 años más tarde que lo descrito en la poblaciónnormal según Tanner y col.
En la Tabla 3, se muestran las características clínicas del G3. La paciente 2 presentó muymala adherencia al tratamiento. El paciente 4 se diagnosticó a los 15,1 años con pubertad completa. Las pacientes 3 y 6, por presentartalla baja extrema al momento del diagnóstico, recibieron tratamiento con análogos del factorliberador de gonadotrofinas (gonadotropinreleasing hormone analogue; a Gn RH, por sus siglasen inglés). La paciente número 3 inició a Gn RH a los 10 años con Tanner 3 y talla -3,73 SDE, y suspendió el tratamiento a los 11,8 años con EO = 12,5 años. Presentando su menarca a los13 años, su talla final fue -3,13 SDE.
La paciente número 6 alcanzó una talla final normal para la población, pero debajo de surango genético (-0,76 SDE). Llamativamente, al momento del diagnóstico (13,8 años), yahabía presentado su menarca con un atraso de la EO de 6 años y una talla -3,77 SDE. Recibióa Gn RH durante 10 meses, que se suspendió pordificultades de provisión, y logró una talla finalde -1,9 SDE.
Cinco niñas (el 6,3 %) se presentaron con pubertad precoz (PP) al momento del diagnóstico (Tabla 4).
DISCUSIÓN
El HAG en los niños produce detención del crecimiento y un profundo retraso en lamaduración esquelética, como consecuenciade una osificación y mineralización retrasada, combinada con la atenuación y "down regulación"de la hormona de crecimiento y del factor decrecimiento insuline-Hke.5 ’ 6
Una vez iniciado el tratamiento con levotiroxina, los niños experimentan una fase decrecimiento compensador, durante el cual la tasade maduración esquelética supera la ganancia deestatura, lo que resulta en un déficit de la tallafinal. Este fenómeno es exacerbado por el iniciode la pubertad central, que, a menudo, ocurrepoco después de haber comenzado el reemplazohormonal.7
El objetivo de nuestro trabajo fue describir a la población de pacientes pediátricos con HAG por TLC y analizar el impacto en la talla cercana a lafinal, según el SDE de la talla y el estadio puberalal momento del diagnóstico, para detectar al grupode pacientes con mayor riesgo de baja talla adulta.
Las formas de presentación sin bocio tuvieron mayor afectación de la talla. Seguramente, sedebió a que su presencia fue un signo clínico quealertó sobre patología tiroidea.
El atraso de la EO al momento del diagnóstico no fue predictor de una mayor tasa decrecimiento, ya que, luego de haber iniciado elreemplazo hormonal, rápidamente, se produjoun avance en la maduración esquelética, quecoincidió con lo descrito por Pantsiouou y col.8
En nuestro trabajo, al igual que lo descrito por Chiesa y col.,9 se demostró que un determinantede la talla final no solo fue el déficit de talla almomento del diagnóstico, sino también el tenerla pubertad avanzada.
Existen diferentes propuestas de tratamientos coadyuvantes del crecimiento, tales como a Gn RH, somatocrinina (growth hormone-releasing hormone;GHrh, por sus siglas en inglés) o inhibidores de la aromatasa (IA). Nebesio y col. compararon latalla final de 13 niños con hipotiroidismo grave (TSH > 150 µUI/ml), 6 de los cuales recibierontratamiento con terapias coadyuvantes (IA, GHrh y/o a GnRH) y 7, solo levotiroxina. No seencontraron diferencias entre ambos grupos.10
Se reportaron 6 niños tratados con a Gn RH, con falla de crecimiento grave, mayor edadcronológica, progresión puberal y avance de la EO, quienes alcanzaron la misma estaturaque 17 niños con menor compromiso de talla al momento del diagnóstico tratados solo conlevotiroxina.11
Reportes de casos aislados12,15 demostraron que el tratamiento combinado de GHrh y a Gn RH, sumado a levotiroxina, lograba una importanteganancia de SDE de talla en los adolescentes conhipotiroidismo grave y mal pronóstico de tallafinal.
Los trabajos publicados acerca de la eficacia del uso de terapias adyuvantes de crecimiento enpacientes con HAG en la infancia y la adolescenciatienen varias limitaciones, como el bajo númerode pacientes, diseños retrospectivos, variables detiempos de seguimiento, diferentes dosis de iniciode levotiroxina y ajustes subsiguientes, sumadosa la falta de estandarización en el uso de terapiasadyuvantes.
Si bien la limitante de nuestra serie es el bajo número de pacientes de los subgruposque alcanzan la talla final, se considera que eldiagnóstico tardío del hipotiroidismo grave enpediatría tiene un impacto negativo en esta, especialmente en aquellos púberes con talla baja almomento del diagnóstico, en los cuales se deberíaconsiderar el uso de terapias adyuvantes delcrecimiento para mejorar su pronóstico de talla.
Estudios aleatorizados, controlados y prospectivos son necesarios para dilucidar losfactores modificables, relacionados con la pérdidadel potencial de talla en los niños con HAG.











 text in
text in