Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957versión On-line ISSN 1851-6114
Acta bioquím. clín. latinoam. v.39 n.1 La Plata ene./mar. 2005
PROGRAMA DE EVALUACIÓN EXTERNA DE CALIDAD
Efecto de la concentración de citrato de sodio sobre las pruebas de hemostasia
Cristina Duboscq1, Lucía Kordich2
1. Dra. en Ciencias Químicas, Universidad de Buenos Aires. Servicio de Hematología Hospital Británico de Buenos Aires. Coordinadora del subprograma Hemostasia del PEEC.
2. Dra. en Ciencias Químicas, Universidad de Buenos Aires. Facultad de Ciencias Exactas y Naturales, UBA Coordinadora del subprograma Hemostasia del PEEC.
Resumen
El objetivo de este trabajo es evaluar el efecto de diferentes concentraciones de citrato 3,2% (109 mM) o 3,8% (129 mM) utilizado como anticoagulante en la determinación del tiempo de protrombina (TP) y el tiempo de tromboplastina parcial activado (APTT). Se trabajó con tres tromboplastinas de distintos orígenes para el TP y cuatro reactivos de APTT que fueron empleados en tres sistemas de detección: manual, fotoóptico y electromecánico. Tres grupos fueron estudiados: voluntarios sanos, pacientes con tratamiento anticoagulante con dicumarínicos en fase estable y pacientes con tratamiento de anticoagulación con heparina no fraccionada. No se obtuvieron diferencias significativas entre las concentraciones de citrato estudiadas para los 9 pares de reactivo/sistemas de detección utilizados para el TP expresado en porcentaje. Los resultados del tiempo de protrombina obtenidos con las dos tromboplastinas de menor ISI muestran una diferencia estadísticamente significativa entre ambas concentraciones de citrato, lo cual corresponde a una diferencia de RIN (Relación Internacional Normatizada) promedio de 7,8%. Esta diferencia se hace más notoria a valores de RIN mayores de 3,5. Las diferencias obtenidas en el RIN están dentro del CV de la metodología utilizada, por lo que permite la elección indistinta de ambos citratos. Los valores de APTT obtenidos con citrato de sodio 3,8% son significativamente más largos que los obtenidos con citrato de sodio 3,2% cuando se utilizan reactivos de APTT sensibles a la presencia de inhibidor lúpico en los tres sistemas de detección en todos los grupos estudiados. Este efecto es aún mayor cuando se estudian pacientes en tratamiento con heparina no fraccionada.
Palabras clave: Concentración de citrato de sodio; Tiempo de protrombina; Tiempo de trombina parcial activado.
Summary
Effect of sodium citrate concentration on coagulation assays
The aim of this study was to assess the extent of influence of citrate concentration on the results of routine coagulation assays (prothrombin time (PT) and activated partial thromboplastin time (APTT). PT was evaluated using three tromboplastins of different origin and APTT was determined by four different APTT reagents. Three methods of clot detecction were used (manual, photo-optic and electromecanic).Three groups were studied: healthy volunteers, outpatients receiving stable dosis of oral anticoagulant therapy and hospitalized patients receiving non fractionated heparin therapy. There were no statistically significant differences of TP expressed in percentaje. In patients receiving dicumarinic therapy, the INR (International Normatized Ratio) obtained with two thromboplastins of lower ISI showed a statistically significant difference between two citrate concentrations. This difference is more important when the RIN is greater than 3.5. Effects of sodium citrate concentration on APTT were satistically significant in all groups when a reagent sensitive to aid the detection of lupus anticoagulant was used. For APTT the greatest change was observed in patients receiving heparin therapy.
Key words: Sodium citrate concentration; Prothrombin time; Activated partial thromboplastin time.
INTRODUCCIÓN
Las variables preanalíticas tanto como las analíticas afectan los resultados de las pruebas de hemostasia (1). Las variables preanalíticas son aquellas que afectan a la recolección, transporte y almacenamiento de la muestra. La mayoría de ellas están estandarizadas por la norma de la NCCLS (National Comittee for Clinical Laboratory Standards) (2). Las variables que afectan la recolección son múltiples: correcto cumplimiento del paciente de las normas del laboratorio para la realización del estudio, calidad de la punción, sistema empleado en la extracción, tiempo de éxtasis venoso, concentración de citrato de sodio utilizado como anticoagulante y relación hematocrito y volumen de anticoagulante.
Escasos estudios investigan el efecto de la variación de la concentración de citrato de sodio sobre las pruebas de coagulación y no existen recomendaciones que fijen la concentración de anticoagulante a utilizar (3-6). La NCCLS recomienda concentraciones de citrato de sodio entre 105 y 129 mM, mientras que el Comité de Expertos en Estandarización Biológica de la OMS (Organización Mundial de la Salud) recomienda la utilización de citrato 109 mM (7).
El tiempo de protrombina (TP) introducido por Quick en 1935 fue adoptado como el método de control de la terapia anticoagulante oral a través del
cálculo de la Relación Internacional Normatizada (RIN) (8-9).
El RIN fue introducido con el objeto de estandarizar los resultados del TP. A pesar de los esfuerzos a través de distintos trabajos colaborativos que se han realizado, aún hoy persisten diferencias entre los valores de RIN determinados con distintos sistemas (reactivo/instrumento) (10) (Tabla I).
Una de las variables que podría afectar el ISI y por ende el RIN es que la concentración de citrato utilizada en la recolección de las muestras de sangre que se utilizan para establecer el ISI de cada tromboplastina fuera diferente a la concentración de citrato de sodio empleada al procesar las muestras.
Las concentraciones de citrato utilizadas por los fabricantes en la calibración de cada tromboplastina no está definida estrictamente y varían entre 100-136 mM.
Duncan et al. demostraron que existía hasta un 10% de variación en el valor del ISI cuando se utilizan dos concentraciones diferentes de citrato (105 y 129 mM) para recolectar la sangre (6).
Van den Besselaar demostró que no hay diferencias significativas entre los ISI cuando se utilizan citrato 105 ó 109 mM (5).
El valor del tiempo de tromboplastina parcial activado (APTT) expresado en segundos, depende fuertemente del reactivo y del tipo de detección utilizado (11). Hay pocos reportes acerca de cómo afecta la variación de la concentración de citrato de sodio en el valor de APTT con los distintos tipos de reactivos (10).
El objetivo de este trabajo es evaluar el efecto de la concentración de citrato 109 mM (3,2%) y 129 mM (3,8%) sobre las pruebas básicas de coagulación utilizando tres tromboplastinas de distintos orígenes y tres reactivos de APTT de diferente sensibilidad en tres sistemas distintos de detección del coágulo (manual, foto-óptico y mecánico).

Tabla I. Causas que originan diferentes valores de RIN entre los laboratorios
MATERIALES y MÉTODOS
Población
Se investigaron tres grupos poblacionales.
GRUPO A: Veinticinco individuos sanos con edades comprendidas entre 20 y 65 años.
GRUPO B: Cincuenta pacientes con tratamiento anticoagulante con dicumarínicos en fase estable, cuyas edades iban de 35 a 71 años.
GRUPO C: Veinte pacientes con tratamiento anticoagulante con heparina no fraccionada, con edades que oscilan entre 38 y 87 años.
Cinco mililitros de sangre venosa se repartieron en forma randomizada en tubos plásticos nuevos del mismo lote que contenían citrato de sodio 109 mM (3,2%) ó citrato de sodio 129 mM (3,8%). Todas las muestras fueron centrifugadas a 2.500 g durante 15 min. a temperatura ambiente y procesadas antes de 4 horas de extraídas.
Tiempo de protrombina
Se determinó el tiempo de Quick por duplicado con tres tromboplastinas de diferentes orígenes de acuerdo a las instrucciones de cada inserto.
R1: tromboplastina de placenta humana (Thromborel S,ISI = 1,03, Dade Behring, Marburg, Alemania).
R2: tromboplastina recombinante (Innovin, ISI = 1.0, Dade Behring, Marburg, Alemania).
R3: tromboplastina de cerebro de conejo (Thromboplastin, ISI = 1,9,Biopool, Umeà, Suecia).
Tiempo de tromboplastina parcial activado (APTT)
Se determinó el APTT por duplicado con 4 reactivos de APTT diferentes (2 sensibles a la detección de inhibidor tipo lúpico) de acuerdo a las instrucciones de cada inserto por el método de Rapaport.
R4: PTTA (Diagnostica Stago, Asnières, Francia).
R5: Actin, (Dade Behring, Marburg, Alemania).
R6: Actin FSL (Dade Behring, Marburg, Alemania).
R7: PTTLA (Diagnostica Stago, Asnières, Francia).
SISTEMA DE DETECCIÓN DEL COÁGULO
La formación del coágulo se visualizó por tres métodos diferentes:
T1: Técnica manual.
T2: Detección foto-óptica/mecánica (Coagulómetro BCT, Dade Behring, Marburg, Alemania).
T3: Detección electromecánica: (Coagulómetro ST4, Diagnóstica Stago, Asnières, Francia).
Estadística
Los resultados fueron evaluados por el método de Mann-Whitney considerando una p < 0,05 como significativa. Las diferencias en segundos para el TP y en unidades RIN se determinaron como las diferencias aritméticas entre ambas concentraciones de citrato de sodio.
RESULTADOS
Influencia de la concentración de citrato sobre el tiempo de protrombina
Para los tres grupo estudiados, los tiempos de protrombina determinados en plasma anticoagulado con citrato de sodio 129 mM son más largos que los obtenidos con citrato de sodio 109 mM con R1 y R2 en los tres sistemas de detección empleados. Esta diferencia es más marcada en los pacientes anticoagulados (grupo B).
La concentración de protrombina expresada en porcentaje con una dada concentración de citrato, se extrapoló de la curva de calibración realizada con un pool de plasmas de 20 individuos normales extraídos con la misma concentración de citrato de sodio.
La Tabla II muestra los valores de TP expresados en porcentaje para los tres grupos estudiados con ambas concentraciones de citrato y para cada combinación de reactivo/instrumento. Si bien los valores de tiempo de protrombina expresados en segundos, cuando la muestra es extraída con citrato de sodio 129 mM, son ligeramente mayores, no se observan variaciones estadísticamente significativas entre ambas concentraciones de citrato cuando el tiempo de protrombina se expresa en porcentaje en ninguno de los grupos estudiados.
Tabla II. Valores del tiempo de protrombina expresado en porcentaje: media y desvío estándar.
Influencia de la concentración de citrato de sodio sobre el RIN
Para cada concentración de citrato de sodio se calculó en forma separada el RIN de cada paciente. Se determinó la media del TP normal para cada combinación tromboplastina/sistema de detección con los 25 plasmas normales estudiados a las distintas concentraciones de citrato de sodio. En todos los casos se utilizó el ISI asignado por el fabricante para cada sistema de detección.
La Tabla III muestra los resultados del RIN (media y desvío estándar) obtenidos para cada combinación reactivo/instrumento. Los resultados muestran que hay diferencias estadísticamente significativas (p < 0,001) al comparar las dos concentraciones de citrato de sodio cuando se utilizan tromboplastinas con ISI cercano a 1 (R1 y R2). La diferencia de RIN promedio es de 0,23 ± 0,04 que corresponde a 7,8% de variación, valor que está dentro del CV de la metodología utilizada.
El 64% (32/50) de los pacientes muestran una diferencia de RIN < 0,25; a medida que aumenta el RIN se incrementa la diferencia entre el valor de RIN calculado con ambas concentraciones de citrato (Fig. 1).
Los reactivos de menor ISI (R1 y R2) mostraron diferencias significativas (p < 0,001) entre el valor de RIN calculado con ambas concentraciones de citrato para los tres sistemas de detección utilizados.
Tabla III. Efecto de la concentración de citrato de sodio sobre el RIN en los pacientes del grupo B: media y DE.

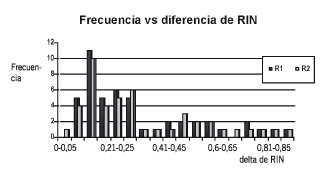
Figura1. Influencia de la concentración de citrato sobre el tiempo de tromboplastina parcial activado (APTT)
Los valores de APTT expresados en segundos con los reactivos R4 y R5 no mostraron diferencias significativas en todas las combinaciones reactivo/instrumentos utilizadas (Tabla IV).
Los valores de APTT con Actin FSL y PTT-LA son significativamente más largos cuando las muestras son extraídas en citrato 129 mM. Esta diferencia no tiene significación clínica, sino para establecer un valor de referencia para el APTT de acuerdo a la concentración de citrato de sodio que cada laboratorio utilice.
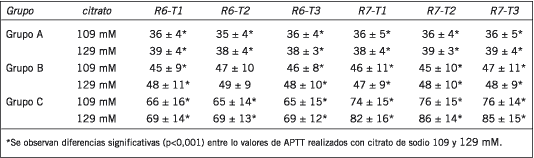
Sólo se observa diferencia significativa entre los valores de APTT para los reactivos sensibles a la detección de inhibidor lúpico (PTT-LA, Actin FSL). La mayor diferencia se observa en el grupo C; 5 de los pacientes con tratamiento con heparina no fraccionada muestran hasta 6 segundos de diferencia entre ambas concentraciones de citrato de sodio con los reactivos Actin FSL y PTT-LA (Tabla V). Este hecho hay que tenerlo en cuenta cuando se establece el rango terapéutico de APTT para monitorear el tratamiento con heparina no fraccionada (11).
Tabla IV. Valores de APTT utilizando reactivos de screening expresados en segundos. Media y desvío estándar.
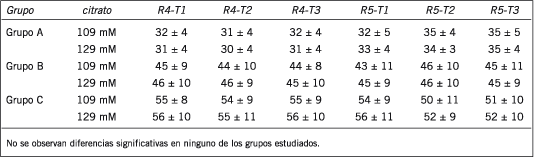
Tabla V. Valores de APTT utilizando reactivos sensibles fosfolípidos expresados en segundos. Media y desvío estándar.
DISCUSIÓN Y CONCLUSIONES
El presente estudio demuestra que la concentración de citrato de sodio utilizada como anticoagulante es una variable preanalítica importante en las determinaciones de rutina del laboratorio de hemostasia cuya influencia depende del reactivo/sistema de detección utilizado (12). La concentración de citrato de sodio empleada como anticoagulante puede variar el tiempo de coagulación del plasma porque la cantidad de citrato presente afecta la concentración de calcio utilizada en la prueba. A mayor concentración de citrato menor concentración de calcio disponible para promover la formación del coágulo y por lo tanto se obtienen tiempos de coagulación más largos.
Con las tromboplastinas R1 y R2 empleadas, los tiempos de protrombina obtenidos en citrato de sodio 129 mM son más largos que los obtenidos en citrato de sodio 109 mM. Las diferencias son mínimas en los valores normales pero son estadísticamente significativas en los pacientes en tratamiento con anticoagulación oral, lo cual conduce a que se obtengan valores de RIN mayores en citrato 129 mM. Si bien las diferencias entre los valores de RIN calculados con ambas concentraciones de citrato son estadísticamente significativas, las mismas no son clínicamente relevantes (el total de la diferencia de RIN es menor que el 10%).
En este trabajo los RIN fueron calculados con el valor de TP normal obtenido con cada concentración de citrato y los ISI suministrados por los fabricantes de cada tromboplastina para cada método de detección. En la mayoría de los casos los insertos no informan a qué concentración de citrato de sodio se realizó la calibración; existen reportes bibliográficos que demuestran que los valores del ISI son hasta un 10% menores cuando son determinados con plasmas obtenidos en citrato de sodio 129 mM. Las diferencias son mayores (hasta 0,6 unidades de RIN) si se calcula el RIN en citrato de sodio 129 mM y se utiliza el TP normal obtenido en citrato 109 mM. Por esta razón es importante que el laboratorio unifique la concentración de citrato a utilizar, en especial en aquellos laboratorios que centralizan muestras de varios lugares.
Los valores de tiempo de tromboplastina parcial activado son más largos en citrato 129 mM cuando se utilizan reactivos sensibles a fosfolípidos. La magnitud de la diferencia depende del sistema de detección utilizado. Este efecto es mayor en los plasmas de los pacientes con tratamiento anticoagulante con heparina no fraccionada Estos resultados muestran que es importante establecer el valor de referencia del APTT y el rango terapéutico para el control de pacientes anticoagulados con heparina a una dada concentración de citrato.
Los distintos organismos internacionales de estandarización no fijan la concentración de citrato de sodio a utilizar: ISTH (Internacional Society of Thrombosis and Haematology) y OMS recomiendan utilizar 109 mM (3,2%) (7-13) mientras que la NCCLS sugiere una concentración entre 109 mM y 130 mM (2). De los resultados expuestos que concuerdan con otros trabajos (2-6)(13) se puede inferir que sería conveniente un consenso mundial que permita estandarizar una única concentración de citrato de sodio en la recolección de los plasmas de los pacientes, en la calibración de las tromboplastinas y en la obtención de los plasmas liofilizados que se utilizan en los programas de control de calidad externo e interno.
Correspondencia
Dra. Cristina Duboscq
Hospital Británico
Servicio de Hematología
Perdriel 74
1280 Buenos Aires
E-mail: cristinaduboscq@speedy.com.ar
Referencias bibliográficas
1. Duboscq C, Castañon M. Control de calidad en el laboratorio de Hemostasia en: Fundamentos prácticos en el laboratorio de Hemostasia. Grupo Argentino de Hemostasia 1ª ed., La Plata, 2003: 47-56.
2. National Committee for Clinical Laboratory Standards. Collection, transport and processing of blood specimens for coagulation testing and performance of coagulation assays. 2ª ed. (approved guideline) NCCLS documents H21-A3 (ISBN 1-56238-363-9),1998. NCCLS, 940 West Vallery Road, Wayne, Pensylvania. 19087, USA, 1998.
3. Adcok D, Kressin D, Marlar R. Effect of 3,2% sodium citrate concentration on routine coagulation testing. Am J Clin Pathol 1997;107:105-10.
4. Chantarangkul V, Tripodi A, Clerici M, Negri B, Manucci P. Assesment of the influence of citrate concentration on the International Normalized Ratio (INR) determined with twelve reagent instrument combinations. Thromb Haemost 1998; 80: 258-62.
5. van den Besselaar AM, Chantarangkul V, Tripodi A. A comparison of two sodium citrate concentration in two evacuated blood collection systems for prothrombin time and ISI determination. Thromb Haemost 2000; 84: 664-7.
6. Duncan E, Casey C, Duncan B, Lloyd J. Effect of concentration of trisodium citrate anticoagulant on calculation of the international normalised ratio and the international sensitivity index of thromboplastin. Thromn and Haemost 1994; 72 (1): 84-8.
7. Guidelines for thromboplastin and plasma used to control oral anticoagulant therapy. In: WHO Expert Committee on Biological Standarization. Forty-Eighth Report. Anex 3. WHO Technical Report Series no 889. Geneva: World Health Organization 1999; 64-93.
8. Quick A, The prothrombin in hemophilia and in obstructive jaundice. J Biol Chem 1935; 109:73-4.
9. Poller L. International Normalized Ratios (RIN): The first 20 years. J Thromb Haemost 2004; 2: 849-60.
10. Naghibi F, Yangsook H, Dodds W, Lawrence C. Effects of reagent and instrument on prothrombin times, activated partial thromboplastin times and patients/control ratios.
11. Bjornsson D, Nash VP. Variability in heparin sensitivity of APTT reagents. Am J Clin Pathol 1986; 86: 199-204.
12. Lotin L, Woodhams BJ, Saureau C, Robert A, Aillaud MF, Arnaud E, et al. The clinical relevance of the citrate effect on international normalized ratio determinations depends on the reagent and instrument combination used. Blood Coagulation and Fibrinolysis 2001, 12: 399-404.
13. Loeliger EA. ICSH/ICTH recomendations for reporting prothrombin time in oral anticoagulant control. Thromb Haemost 1985; 54:155-66. [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ]














