Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957versión On-line ISSN 1851-6114
Acta bioquím. clín. latinoam. v.39 n.3 La Plata jun./sept. 2005
TEMAS DE INTERÉS
Guías del laboratorio para screening, diagnóstico y monitoreo de la lesión hepática*
* Este documento ha sido traducido con permiso de la Nacional Academy of Clinical Biochemistry (NACB), Washington, DC. La NACB no se hace responsable de la exactitud de la traducción. Los puntos de vista presentados son los de los autores y no necesariamente los de la NACB.
EDITOR
D. Robert Dufour
Chief, Pathology and Laboratory Medicine Service, VA Medical Center, Washington, DC;
Professor of Pathology, George Washington University School of Medicine.
GUIDELINES COMMITTEE
John A. Lott
Professor of Pathology, The Ohio State University College of Medicine
Frederick S. Nolte
Associate Professor of Pathology and Laboratory Medicine, Emory University School of Medicine
David R. Gretch
Associate Professor of Laboratory Medicine, University of Washington School of Medicine
Raymond S. Koff
Professor of Medicine, University of Massachusetts Medical Center
Leonard B. Seeff
Senior Scientist, Hepatitis C Programs, National Institute of Diabetes, Digestive, and Kidney Diseases, National Institutes of Health; Professor of Medicine, Georgetown University School of Medicine.
INTRODUCCIÓN
La lesión del hepatocito es un hallazgo común en la práctica médica. La incidencia de la hepatitis viral aguda ha disminuido marcadamente en la década pasada debido a la introducción de vacunas para las hepatitis A y B y al análisis de sangre de donantes para hepatitis C. Otras formas de lesión hepática aguda no han cambiado, prácticamente, en incidencia y las lesiones hepáticas crónicas han aumentado. En los Estados Unidos, se estima que un millón de individuos están infectados crónicamente con el virus de la hepatitis B y 2,1-2,8 millones lo están con el de la hepatitis C (1). La cirrosis es actualmente la 9º causa de muerte en los Estados Unidos (2); se predice que las muertes por cirrosis aumentarán del 223% en el 2008 al 360% en el 2028 debido a casos originados en una infección crónica por hepatitis C (3). La incidencia del carcinoma hepatocelular se ha duplicado en los últimos 20 años (4) y se espera que aumente otro 68% durante la próxima década a partir de cánceres que desarrollarán en individuos infectados con el virus de la hepatitis C (3).
La enfermedad hepática es a menudo clínicamente silente hasta períodos tardíos de su curso. Por esta razón, son generalmente necesarias las pruebas de laboratorio para el reconocimiento y caracterización del tipo de lesión hepática presente. La causa más común de lesión hepática en el mundo es la infección con virus que infectan primariamente al hígado, a menudo llamados virus de la hepatitis. Se necesitan pruebas serológicas y otras basadas en ácidos nucleicos para poner de manifiesto la exposición a estos virus y su presencia, así como para controlar el tratamiento de los individuos afectados. Un cierto número de otras enfermedades pueden también causar lesión hepática, particularmente los desórdenes inmunológicos y los desórdenes congénitos y adquiridos del metabolismo. Las pruebas de laboratorio son críticas para el reconocimiento de estas otras enfermedades, particularmente en pacientes sin evidencia de infección viral. Finalmente, la exposición a etanol y otras drogas puede causar lesión hepática; la información clínica es el medio más confiable para reconocer estas causas potenciales de daño hepático.
Las recomendaciones específicas en esta monografía se basan en información relevante publicada. La solidez de los datos científicos que apoyan cada recomendación se caracteriza usando el criterio de puntaje adoptado por el Practice Guidelines Comittee of the American Association for the Study of Liver Diseases (AASLD), como se resume en la Tabla I.
Para cada recomendación, los números romanos del I al IV describen la calidad de la evidencia en la que se basa cada una de ellas y las letras de la A a la E describen el significado de la recomendación. Debido a la naturaleza de estas guías sólo se usan en las recomendaciones las categorías B y E.

Tabla I. Categorías de la ASSLD que reflejan la calidad de las evidencias en las que se basan
las Recomendaciones (números romanos) y las guías de evidencias secundarias (letras).
SECCIÓN I
Pautas para la realización de pruebas de laboratorio de la función y lesión hepáticas
Especificaciones para las pruebas de laboratorio
Las pruebas de laboratorio son usadas por los médicos para el diagnóstico, seguimiento, y pronóstico en pacientes con enfermedad hepática. Un número de factores, primariamente preanalíticos y analíticos, afectan la certeza de los resultados de las pruebas. Las principales características de cualquier prueba son su desvío y su imprecisión. El desvío es primariamente una característica analítica, por la cual los resultados reportados difieren del valor verdadero. La imprecisión, o falta de reproducibilidad, se debe tanto a factores fisiológicos como analíticos. En el estado basal, los resultados de las pruebas fluctúan en un individuo debido al azar y a la variación predecible; esto se denomina variación intraindividual. El grado de variación puede estar incrementado bajo ciertas condiciones, tales como ingesta de comida, hora del día, ejercicio, enfermedad aguda, u otras formas de estrés. En general, para muchas pruebas, hay también diferencias significativas de una persona a otra, lo que se denomina variación interindividual. La variación intraindividual, interindividual, y las causas analíticas de variación deben ser consideradas en la interpretación de los resultados de las pruebas de laboratorio como indicando un cambio en el estado de salud de un individuo.
Las especificaciones para la realización de las pruebas sirven como una guía para el laboratorio del grado de variación analítica que permitirá al médico determinar con certeza el estado fisiológico de un individuo. Las especificaciones para la realización pueden ser establecidas por diferentes métodos, incluyendo (en orden decreciente de importancia) estudios médicos, datos de variación biológica, opiniones de médicos o de sociedades de profesionales, o datos de pruebas de aprovechamiento, o directivas gubernamentales (5).
Los objetivos de la realización deben especificar la imprecisión aceptable, el desvío, y el error total (desvío + 1.65 * imprecisión). Cuando los objetivos son derivados de datos biológicos, el objetivo target para la imprecisión es menos de la mitad de la variación intraindividual para la prueba, mientras que el objetivo para el desvío es menor que un cuarto del promedio de la variación intraindividual (cv1) e interindividual (cvg), calculado como 1/4 (cvi2 + cvg2) (6). La Tabla II resume los datos publicados sobre las especificaciones de realización y de precisión en el laboratorio para pruebas relacionadas a la función y lesión hepáticas.
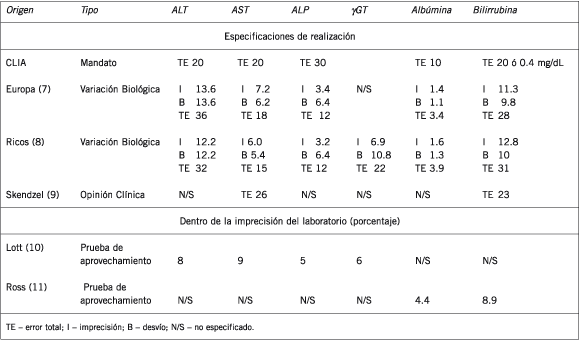
Tabla II. Especificaciones de realización y precisión para pruebas de hígado (porcentaje).
Intervalos de referencia
A fin de determinar la probabilidad de que una enfermedad esté presente, los resultados de una prueba son típicamente comparados con valores obtenidos a partir de individuos sanos; el rango de tales resultados es denominado intervalo de referencia, en tanto que los extremos superior e inferior del intervalo son denominados límites de referencia superior e inferior, respectivamente. La mayoría de los laboratorios publica un único intervalo de referencia para casi todas las pruebas de laboratorio, definido como el intervalo central con el 95% de los resultados, obtenidos a partir de personas sanas. En muchos casos, hay factores reconocidos que pueden afectar los resultados de las pruebas sin indicar la presencia de enfermedad, particularmente cuando sólo es usado un intervalo de referencia. Para cada una de las pruebas de laboratorio listadas existen factores que afectan a los resultados y que son resumidos en tablas y figuras.
Para algunas pruebas los límites de referencia son definidos por consecuencias en la salud; como ejemplos se incluyen los límites de referencia usados corrientemente para el colesterol y la glucosa en ayunas. El uso de límites de referencias basados en consecuencias. también requiere un alto grado de estandarización de la determinación entre laboratorios para asegurar que los resultados de todos los laboratorios tengan una relación similar con el límite superior del intervalo de referencia. Mientras datos de estudios acerca de la probabilidad de transmisión de infección luego de una transfusión sugieren que una consecuencia basada en el límite superior de referencia puede ser apropiada para ALT, no hay suficiente estandarización de las determinaciones ALT entre laboratorios para permitir el uso de tal aproximación. en la actualidad. No hay datos sobre límites de referencia basados en consecuencias para otras pruebas de función y lesión hepáticas.
Aminotransferasas
La aspartato aminotransferasa (AST, también algunas veces denominada SGOT) y la alanin aminotransferasa (ALT, también a veces denominada SGPT) se encuentran ampliamente distribuidas en las células del cuerpo. AST se encuentra primariamente en corazón, hígado, músculo esquelético y riñón, mientras que ALT se encuentra primariamente en hígado y riñón, con cantidades menores en corazón y músculo esquelético.
Las actividades de AST y ALT en hígado son aproximadamente 7.000 y 3.000 veces las actividades séricas, respectivamente (12). ALT es exclusivamente citoplasmática; tanto la forma mitocondrial como la citoplasmática de AST se encuentran en todas las células (13). La vida media de la AST total es 17±5 horas, mientras que la de ALT es 47±10 horas (14). La vida media de la AST mitocondrial promedia las 87 horas (15). En adultos, las actividades de AST y ALT son significativamente mayores en hombres que en mujeres, y los intervalos de referencia varían con la edad (Figura 1) (Figura 2).
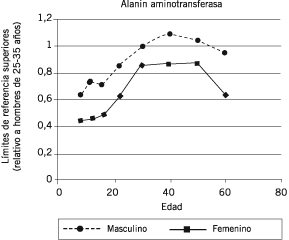
Figura 1. Efectos de la edad y el sexo sobre los límites de referencia superiores para ALT. El límite de referencia superior para hombres de 25-35 años es fijado en 1.0 unidades de valor relativo. Los límites superiores del intervalo de referencia para ALT aumentan desde la niñez hasta aproximadamente los 40 años de edad, con mayores aumentos en hombres que en mujeres; los límites superiores del intervalo de referencia son aproximadamente 10% mayores en hombres de 40 años que en los de 25 años. Luego de los 40 años, los límites superiores del intervalo de referencia de ALT nuevamente disminuyen, con una disminución más pronunciada en hombres que en mujeres. Datos tomados de la referencia 16.
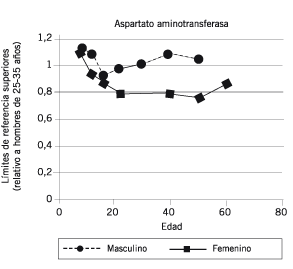
Figura 2. Efectos de la edad y el sexo sobre los límites de referencia superiores para AST. El límite de referencia superior para hombres de 25-35 años es fijado en 1.0 unidades de valor relativo. Los límites superiores del intervalo de referencia para AST aumentan desde la niñez hasta la juventud, pero cambian relativamente poco con el aumento de la edad en adultos hasta poco después de los 60 años. En todas las edades excepto en la niñez y en la vejez; los límites superiores del intervalo de referencia para AST son aproximadamente 25-30% mayores en hombres que en mujeres. Datos tomados de la referencia 16.
Hasta aproximadamente los 15 años de edad, la actividad de AST es ligeramente mayor que la de ALT, con un patrón inverso para la edad de 15 años para hombres, pero persistiendo hasta la edad de 20 años en mujeres (17). En adultos, la actividad de AST tiende a ser mas baja que la de ALT hasta alrededor de los 60 años, cuando ambas son groseramente iguales. Debido a que los límites de referencia superiores varían poco entre los 25 y 60 años no se necesita usar límites de referencia ajustados por la edad para esta población, que comprende a la mayoría de las personas con lesión hepática crónica. Límites de referencia separados se requieren para niños y ancianos; esto puede implicar esfuerzos en el orden nacional para obtener suficientes muestras de individuos sanos para determinar con certeza los límites de referencia.
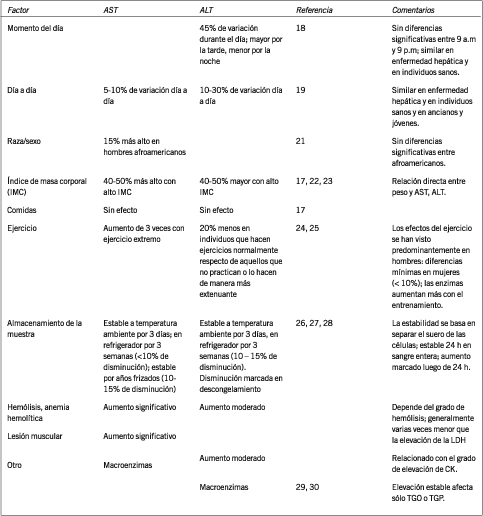
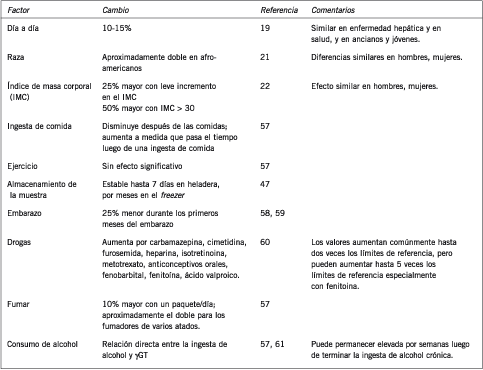
La enfermedad hepática es la causa más importante de aumento de la actividad de ALT y una causa común de aumento de actividad de AST. Hay otros factores distintos de la enfermedad hepática que afectan la actividad de AST y ALT; ellos se resumen en la Tabla III.
Tabla III. Factores que afectan la actividad de AST y ALT además de la lesión hepática.
Inesperadamente, resultados anormales aparecen como normales en pruebas repetidas. En muchos tipos de enfermedad hepática, la actividad de ALT es mayor que la de AST; una excepción se ve en la hepatitis alcohólica. Las razones para la mayor actividad de AST en la hepatitis alcohólica parecen ser múltiples. El alcohol incrementa la actividad de AST mitocondrial en plasma, mientras que otras formas de hepatitis no lo hacen (31). La mayoría de las formas de injuria hepática disminuyen la actividad en los hepatocitos de las formas citosólica y mitocondrial de AST, pero el alcohol sólo disminuye la actividad de la forma citosólica (32). La deficiencia de piridoxina, común en los alcohólicos, disminuye la actividad de ALT (33), y el alcohol induce la liberación de AST mitocondrial desde las células sin daño celular visible (34).
AST y ALT son típicamente medidas por su actividad catalítica (35); ambas requieren 5'-fosfato de piridoxal (P-5'- P) para la máxima actividad, aunque el efecto de la deficiencia de P-5'-P sobre la actividad de ALT es mayor que sobre la de AST (36). En caso de falla renal, las actividades de AST y ALT son significativamente menores que en individuos sanos, tal vez debido a los ligandos del suero para P-5'-P, dado que el P-5'-P total está elevado (37). Debido a las marcadas diferencias entre laboratorios, la estandarización de los métodos es una prioridad. En el ínterin, métodos alternativos para minimizar las diferencias entre laboratorios, tales como expresar los resultados como múltiplos del límite de referencia (38), han mostrado una disminución en la variación entre laboratorios (39).
Los valores usuales para el error total en las mediciones de ALT son de 20% (CLIA). Los datos clínicos sobre los cuales se basan estos objetivos no están disponibles para la mayoría de las pruebas de laboratorio de evaluación hepática, con la excepción de ALT. Existen pocos datos sobre la variación biológica de ALT en hepatitis crónica, particularmente en Hepatitis C, aunque comúnmente se acepta que los resultados de ALT son altamente variables. En un estudio de 275 pacientes con infección por VHC confirmada, el coeficiente de variación intraindividual promedio fue 38%, aunque en un cuarto de los pacientes, fue menos que 23% (Dufour, observaciones no publicadas). Varios estudios han mostrado que el tratamiento de la infección crónica por VHC no se indica si ALT está dentro del rango de referencia. Así, la determinación de la certeza de ALT en el límite de referencia es crítica para el correcto tratamiento de pacientes con infecciones con VHC. El consenso de los autores y del AASLD Practice Guidelines Committee es que los criterios de performance
para ALT deben ser definidos en los límites superiores de referencia, y que los objetivos actuales son inadecuados para uso clínico. Los datos en pacientes con ALT estable sugieren que se requiere un error total menor de 10% en los límites superiores de referencia para una detección exacta de pacientes que pueden beneficiarse con el tratamiento para VHC. Los datos actuales sobre la precisión intralaboratorio (Tabla II) sugieren que este objetivo no puede ser logrado por métodos corrientes. Es necesario desarrollar un programa de estandarización para determinaciones de ALT, similar al usado para CK-MB. Esto puede requerir el uso de otros métodos, tales como inmunoensayo, para lograr objetivo necesario en el error total para el manejo de pacientes con hepatitis crónica.
Los objetivos de la performance para el error total en las medidas de actividad AST son 15-20%, ambos de acuerdo a los requerimientos CLÍA y basados en la variación biológica. Esto cumple con las necesidades de los médicos para el diagnóstico y el manejo de la enfermedad hepática (9). Dichos objetivos no son tan críticos para AST como para ALT; un menor porcentaje de resultados de AST son anormales en VHC crónica comparados con ALT (66% vs. 71%). AST es anormal (6%) mientras ALT es normal, excepto en la cirrosis o en el abuso de alcohol (Dufour, observaciones no publicadas).
Los ensayos para la actividad de ALT deben tener un error analítico total ≤ del 10% en el límite de referencia superior (IIB). Los objetivos publicados para AST, con un error total de 15-20%, son adecuados para uso clínico (IIIB).
La estandarización de los valores de ALT entre métodos y entre laboratorios es una necesidad prioritaria para el cuidado de los pacientes. Hasta que esto sea logrado debe ser considerado el uso de resultados normalizados (IIIB).
Como mínimo, los laboratorios deben tener separados los límites de referencia superiores para hombres y mujeres adultas; los límites de referencia también deben ser establecidos para los niños y para los adultos con edad por encima de los 60 años a través de esfuerzos cooperativos (IIB).
Valores inesperadamente elevados de ALT y/o AST deberían ser evaluados por pruebas repetidas; en el caso de individuos sometidos a ejercicio intenso, la repetición debería ser realizada luego de un período de abstinencia de ejercicio. Se requiere investigación para determinar el intervalo de tiempo apropiado (IIB, E).
Fosfatasa alcalina
La fosfatasa alcalina (ALP), involucrada en el transporte de metabolitos a través de las membranas celulares, se encuentra en orden decreciente de abundancia en placenta, mucosa ileal, riñón, hueso e hígado. Las fosfatasas alcalinas de hueso, hígado y riñón comparten una estructura proteica común, codificada por el mismo gen (40)(41); difieren en su contenido en hidratos de carbono. La vida media de la isoenzima hepática es 3 días (42). La Figura 3 ilustra cambios relacionados con la edad y el sexo en los límites de referencia superiores para fosfatasa alcalina.
La interpretación de los resultados de fosfatasa alcalina usando poblaciones de referencia adecuadas es particularmente importante en niños; los límites de referencia difieren poco en los hombres y mujeres adultos entre las edades de 25 y 60 años. Luego de los sesenta años, los límites de referencia aumentan en las mujeres, aunque los estudios no han sido consistentemente evaluados para la presencia de osteoporosis, que puede incrementar la actividad de fosfatasa alcalina en suero. Se requieren rangos de referencia separados para niños y mujeres embarazadas.
La colestasis estimula la síntesis de ALP por los hepatocitos; las sales biliares, los detergentes u otros agentes tensioactivos facilitan la liberación de ALP desde las membranas celulares (43)(44). Otros factores que afectan la fosfatasa alcalina están resumidos en la Tabla IV.
El método para ALP total de mayor uso es el método con p-nitrofenilfosfato como sustrato, método de Bowers, McComb and Kelly (50).
Agentes complejantes tales como citrato, oxalato o EDTA unen cationes tales como zinc y magnesio, que son cofactores necesarios para la actividad de ALP, causando valores falsamente disminuidos, tan bajos como 0. La transfusión de sangre (que contenga citrato) causa disminución transitoria de la ALP a través de un mecanismo similar.
La separación de las formas de ALP no específicas de tejido (hueso, hígado y riñón) es dificultosa debido a su similitud estructural; la electroforesis de alta resolución y el isoelectroenfoque son las técnicas más útiles. La ALP hueso-específica puede ser medida por inactivación por calor (un método pobre), por métodos inmunológicos y electroforéticos. Los inmunoensayos de ALP de hueso están ahora disponibles a partir de varias fuentes (51), y pueden ser usados para monitorear los pacientes con enfermedad ósea. Debido a que hay concordancia entre aumentos de la fosfatasa alcalina de origen hepático y un incremento en la actividad de otras enzimas canaliculares tales como g-glutamil transferasa (gGT), sus valores elevados son una buena indicación de una fuente hepática, pero no excluye que coexista una enfermedad ósea (52).
En contraste a la mayoría de las enzimas, la variación intra individual en ALP es baja, estando ligeramente en promedio ligeramente sobre un 3% (Tabla II). El promedio corriente de la imprecisión entre laboratorios es de 5% y está próxima a las especificaciones recomendadas para la performance; un error total de 10-15% permitiría encontrar valores target del 12% basados en individuos sanos. El rango de error total especificado por CLIA del 30% parece demasiado amplio para uso clínico y debería ser más estrecho.

Figura 3. Efectos de la edad y el sexo sobre los límites de referencia superiores para fosfatasa alcalina. El límite de referencia superior para varones de 25 a 35 años de edad está fijado en 1.0 unidades de valor relativo. La fosfatasa alcalina es varias veces más alta en niños y adolescentes, alcanzando las actividades del adulto aproximadamente a los 25 años. Los valores son ligeramente mayores en hombres que en mujeres hasta los últimos años de vida. En los hombres adultos, los límites superiores del intervalo de referencia no cambian con la edad, mientras que en las mujeres los límites superiores del intervalo de referencia aumentan con la menopausia. Datos de la referencia 16.
Tabla IV. Factores que afectan la actividad de la fosfatasa alcalina además de la lesión hepática.
RECOMENDACIONES
Las técnicas para fosfatasa alcalina deben tener un error analítico total ≤ 10-15% en el límite de referencia superior (IIIB).
Se deben proveer límites de referencia separados para niños, basados en la edad y el sexo, y para mujeres embarazadas. Un rango de referencia único es adecuado para adultos mayores de 25 años (IIB).
Las muestras para determinar actividad de fosfatasa alcalina deben ser obtenidas con el paciente en ayunas; de no ser así, se pueden encontrar valores moderadamente elevados que deben ser reevaluados en estado de ayuna antes de proseguir con la evaluación (IIB, E)
Las determinaciones de las isoenzimas de fosfatasa alcalina o la medición de otras enzimas asociadas (tales como gGT) son necesarias sólo cuando la fuente de una actividad de fosfatasa alcalina elevada no es obvia a partir de datos clínicos y de laboratorio (IIIB, E)
Gamma glutamil transferasa
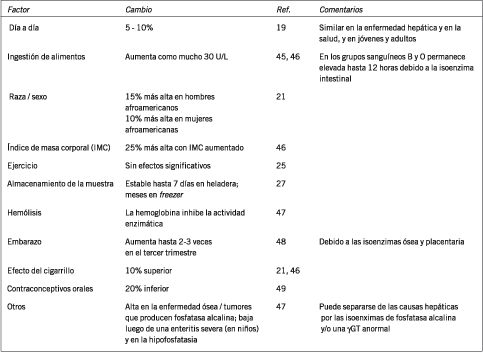
La gamma glutamil transferasa (gGT), una enzima unida a membranas, está presente en orden decreciente de abundancia en el túbulo renal proximal, hígado, páncreas (ductos y células del acino), e intestino. La actividad de gGT en suero proviene principalmente del hígado. La vida media de gGT en humanos es aproximadamente de 7 a 10 días; en la injuria hepática asociada al alcohol, la vida media aumenta hasta 28 días, sugiriendo una disminución en el clearance. En la Figura 4 se resumen diferencias relacionadas con la edad y el sexo en gGT.
En los hombres adultos es adecuado un único rango de referencia entre las edades de 25 y 80 años. Aunque los límites superiores del intervalo de referencia son aproximadamente 2 veces mayores en aquellos que tienen ascendencia africana, no se provee comúnmente a los laboratorios información sobre características raciales; sería dificultoso para los laboratorios reportar valores con el intervalo de referencia apropiado basado en la raza. En las mujeres y niños, los límites superiores de referencia para gGT aumentan gradualmente con la edad, y son considerablemente más bajos que los encontrados en los hombres adultos. Se deben establecer límites de referencia separados para hombres y mujeres, y para diferentes rangos de edad en mujeres y niños. En niños esto requerirá probablemente un esfuerzo cooperativo de los laboratorios para obtener un número adecuado de muestras de niños sanos.
La gGT es ligeramente más sensible que ALP en la enfermedad hepática obstructiva. La gGT aumenta en promedio 12 veces el límite superior de referencia en el 93-100% de pacientes con colestasis, mientras que ALP aumenta en promedio tres veces el límite de referencia superior en el 91% del mismo grupo (52-54). La gGT parece aumentar en colestasis por los mismos mecanismos que aumenta la ALP (54)(55). La gGT está aumentada en 80-95% de pacientes con alguna de las formas de hepatitis aguda (55)(56). Se resumen en la Tabla V otros factores que afectan la actividad de gGT.
Los pacientes con diabetes, hipertiroidismo, artritis reumatoidea y enfermedad pulmonar obstructiva a menudo tienen un incremento en gGT; las razones para estos hallazgos no se conocen bien. Luego del infarto agudo de miocardio, gGT puede permanecer anormal por semanas (62). Estos otros factores determinan un bajo valor predictivo de gGT (32%) para enfermedad hepática (63).
El método de la Federación Internacional de Química Clínica descrito por Shaw (64) es usado por la mayoría de los laboratorios. La precisión para actividades menores que la mitad del límite de referencia superior es aproximadamente del 10%; en el doble del límite de referencia superior, está próxima al 5%. Los objetivos de la performance para gGT se basan primariamente en la variación biológica, con límites de tolerancia del error total de aproximadamente 20%. Estos son adecuados para propósitos clínicos, dada la limitada utilidad clínica de las determinaciones de gGT.
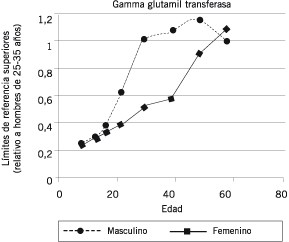
Figura 4. Efectos de la edad y el sexo sobre el límite de referencia superior para g-Glutamil Transferasa (GGT). El límite de referencia superior para hombres entre 25-35 años de edad es establecido como 1.0 unidades de valor relativo. Los límites de referencia superiores de GGT aumentan a lo largo de la vida, con el efecto más marcado en las mujeres que en los hombres. Antes de los 50 años, los límites superiores de referencia en los hombres son aproximadamente 25-40% mayores que en las mujeres, pero las diferencias disminuyen con el aumento de la edad. Datos de la referencia 16.
Tabla V. Factores que afectan la gGT aparte de la lesión hepática.
RECOMENDACIONES
Los ensayos para la actividad de gamma-glutamil transferasa deberían tener un error analítico total ≤ 20% en el límite de referencia superior (IIIB).
Se recomienda el uso de muestras tomadas en ayunas por la mañana (IIB).
Mientras que un límite único de referencia superior es apropiado para hombres adultos, para niños y mujeres adultas son necesarios límites de referencia basados en la edad (IIB)
Debido a la falta de especificidad la gGT debería ser reservada para indicaciones específicas tales como la determinación del origen de un aumento de fosfatasa alcalina (IIIB, E).
Bilirrubina
La producción diaria de bilirrubina no conjugada es de 250 a 350 mg, principalmente proveniente de eritrocitos senescentes (65). El clearance a valores normales es 5 mg/kg/día, o alrededor de 400 mg/día en adultos; la proporción no aumenta significativamente con hemólisis (66). La vida media de la bilirrubina no conjugada es < 5 min (67). La UDP-glucuronil transferasa cataliza la conjugación rápida de la bilirrubina en el hígado; la bilirrubina conjugada es excretada por bilis y está esencialmente ausente de la sangre en los individuos normales. La bilirrubina delta (d-bilirrubina, también a veces llamada biliproteína) se produce por reacción de la bilirrubina conjugada con albúmina (68); tiene una vida media de aproximadamente 17-20 días (la misma que la albúmina), presentándose en pacientes con ictericia prolongada que se recuperan de hepatitis o de una obstrucción (69). Los cambios relacionados con la edad y el sexo en los límites de referencia para bilirrubina se ilustran en la Figura 5.
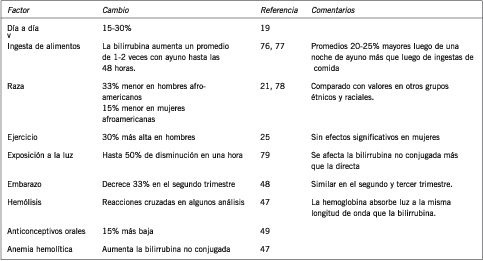
Los aumentos en la bilirrubina conjugada son altamente específicos para enfermedad hepática o de los ductos biliares (70). Los incrementos en la bilirrubina conjugada también pueden ocurrir con alteraciones de la excreción de bilirrubina, dependiente de energía en sepsis, nutrición parenteral total, y luego de una cirugía (71). En la recuperación de una hepatitis o de una obstrucción, la bilirrubina conjugada cae rápidamente, mientras que la d-bilirrubina declina más lentamente (72). El síndrome de Gilbert, encontrado en aproximadamente el 5% de la población, causa una leve hiperbilirrubinemia no conjugada debido a una alteración en la actividad de la UDP-glucuronil transferasa junto con una disminución en la captación de iones orgánicos (73)(74). La bilirrubina total raramente excede 68-85 µmol/L (4-5 mg/dL), aún durante el ayuno prolongado, a menos que otros factores que incrementan la bilirrubina se encuentren también presentes (75). En la Tabla VI se resumen otros factores que afectan a la bilirrubina.
La bilirrubina se mide típicamente usando dos ensayos, bilirrubina total y bilirrubina directa; sustrayendo la bilirrubina directa de la total se obtiene la "bilirrubina indirecta". El ensayo para bilirrubina directa mide la mayoría de la d-bilirrubina y la bilirrubina conjugada, y un porcentaje pequeño y variable de bilirrubina no conjugada (79)(80). Un valor alto de pH o la presencia de un agente humectante promueve la reacción de bilirrubina no conjugada en el ensayo de la "directa"; el reactivo para la bilirrubina "directa" debe contener al menos 50 µmol/L de HCl para prevenir la medición de bilirrubina no conjugada (81). La luz puede convertir la bilirrubina no conjugada en un fotoisómero que reacciona directamente (79); esto causa una disminución de la bilirrubina total de 0.34 µmol/L/h (0.02 mg/dL/h). La espectrofotometría directa (métodos en películas secas) mide bilirrubina conjugada y no conjugada individualmente, y luego calcula la d-bilirrubina como la diferencia entre la suma de éstas y la bilirrubina total. Algunos han sugerido que la bilirrubina conjugada es mejor que la bilirrubina "directa" para medir la recuperación de una enfermedad hepática (82).
Los objetivos de la performance de la medición de bilirrubina permiten de un 20% (CLIA) a 30% (variación biológica) de error total. Los médicos sienten que un 23% de cambio en los límites de referencia superiores de bilirrubina indican un cambio significativo en la condición (9). Así, CLIA parece alcanzar las necesidades de performance clínica. A concentraciones elevadas, un cambio de 2 mg/dL (5%) fue considerado clínicamente significativo. Valores targets para el error total deben, por lo tanto, especificar la concentración de bilirrubina.
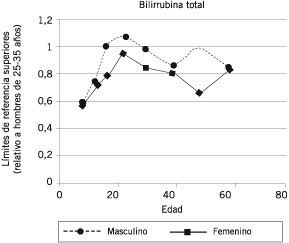
Figura 5. Efectos de la edad y el sexo sobre los límites de referencia para bilirrubina total. El límite superior de referencia para hombres de 25-35 años se toma como 1.0 unidades de valor relativas. Los límites superiores de referencia aumentan durante la niñez y la adolescencia, alcanzando valores picos a aproximadamente los 20 años; luego de esto, los valores disminuyen gradualmente con el aumento de la edad. A todas las edades, los límites de referencia superiores son mayores en los hombres que en las mujeres, aunque las diferencias son mínimas en los extremos de la vida. Datos de la referencia 16.
Tabla VI. Factores que afectan la bilirrubina aparte de la lesión hepática.
RECOMENDACIONES
Los ensayos para bilirrubina deben tener un error analítico total ≤ 20% (o 6.8 µmol/L [0.4 mg/dL]) en el límite superior de referencia (IIIB).
Deben usarse límites de referencia superiores separados para hombres y mujeres. Mientras los límites superiores de referencia de bilirrubina declinan con la edad en los adultos, hay poca significancia para elevaciones ligeras en la bilirrubina y no se requieren límites de referencia superiores ajustados por edad, separados, para adultos. En niños, deben ser usados rangos de referencia separados (IIIB).
Albúmina
La albúmina es la más abundante de las proteínas plasmáticas y es producida por los hepatocitos. La velocidad de producción es dependiente de varios factores, incluyendo la provisión de aminoácidos, la presión oncótica del plasma, niveles de citoquinas inhibitorias (particularmente IL-6) y el número de hepatocitos funcionantes (83). La vida media de la albúmina plasmática es normalmente de alrededor de 19-21 días. Las concentraciones de albúmina plasmática son bajas en los neonatos, típicamente de 28 a 44 g/L (2.8-4.4 g/dL). En la primera semana de vida, se alcanzan los valores del adulto de 37 a 50 g/L (3.7-5.0 g/dL), aumentando de 45 a 54 g/L (4.5-5.4 g/dL) a los 6 años y permaneciendo en estas concentraciones durante la juventud, antes de declinar a los valores típicos del adulto. No existen diferencias significativas en los límites de referencia entre hombres y mujeres (84). Valores incrementados de albúmina son típicamente debidos a hemoconcentración, causada, ya sea por deshidratación, uso de torniquete prolongado durante la recolección de la muestra, o evaporación de la misma. Las principales causas para valores disminuidos de albúmina incluyen pérdida de proteínas (síndrome nefrótico, quemaduras, enteropatía con pérdida de proteínas), un recambio incrementado de albúmina (estados catabólicos, glucocorticoides), disminución en la ingesta de proteínas (malnutrición, dietas muy bajas en proteínas), y enfermedad hepática. La albúmina plasmática está disminuida a veces en la hepatitis aguda, debido a su larga vida media, pero en la hepatitis crónica la albúmina gradualmente cae cuando la enfermedad progresa a la cirrosis. Las concentraciones de albúmina son un marcador de la descompensación y del pronóstico en la cirrosis.
La albúmina es comúnmente medida por métodos colorimétricos, particularmente con verde de bromocresol y púrpura de bromocresol; actualmente, alrededor del 50% de los laboratorios usan alguno de estos métodos. Los métodos con verde de bromocresol pueden sobreestimar la albúmina (85), aunque las diferencias entre los dos métodos son pequeñas (83). El púrpura de bromocresol subestima la albúmina en la falla renal (86) y en pacientes con un aumento de d-bilirrubina (87), tornando a este método inconveniente en pacientes con ictericia.
No se recomienda la estimación de la albúmina a partir de electroforesis de proteínas debido a la sobreestimación significativa de la misma basada en una mayor unión del colorante (83). Y los inmunoensayos en plasma para albúmina están disponibles pero no son muy utilizados (88).
Los objetivos de la performance para la determinación de albúmina basada en la variación biológica están típicamente alrededor del 4%, mientras que CLIA permite un error del 10%. El uso clínico de las determinaciones de albúmina para la enfermedad hepática está primariamente dirigido al reconocimiento de la cirrosis, y a determinar su severidad; esto requiere cambios significativos de los límites de referencia. Datos de fuentes CAP indican que sólo el 2% de los laboratorios pueden lograr los límites de error basados en la variación biológica. La opinión del Comité es que los objetivos de CLÍA son adecuados para propósitos clínicos.
RECOMENDACIONES
Un error total < 10% en el límite de referencia inferior es adecuado para propósitos clínicos; los objetivos de performance basados en la variación biológica no pueden ser logrados por la mayoría de los laboratorios (IIB)
En los ensayos para albúmina en pacientes con enfermedad hepática debe usarse verde de bromocresol. El púrpura de bromocresol y las determinaciones de albúmina por electroforesis pueden ser inexactas en pacientes con enfermedad hepática (IIB).
Tiempo de protrombina
El tiempo de protrombina (TP) mide el tiempo requerido para que el plasma coagule luego de la adición de Factor Tisular y fosfolípido; es afectado por cambios en la actividad de los factores X, VII, V, II (protrombina) y I (fibrinógeno). Todos estos factores son sintetizados en el hígado, y tres de ellos (II, VII y X) son activados por una enzima dependiente de vitamina K a través de la adición de un segundo grupo g-carboxilo sobre los residuos de ácido glutámico. La warfarina, un antagonista de la vitamina K, causa anticoagulación por inhibición de la g-carboxilación, produciendo factores incapaces de unir calcio y reduciendo su actividad. Los individuos con warfarina o con deficiencia de vitamina K sintetizan cantidades normales de los precursores de los factores de coagulación, pero en una forma inactiva denominada "proteínas inducidas por antagonistas de vitamina K (PIVKA)". Hay inmunoensayos disponibles para medir los PIVKA más abundantes, des-g-carboxi protrombina. El TP es relativamente insensible a la deficiencia de cualquier factor de coagulación individual; no hay aumento significativo hasta que las concentraciones caen por debajo del 10% de la concentración normal (89).
El TP es comúnmente reportado en segundos y comparado con valores de referencia de pacientes. El tiempo requerido para que una muestra coagule está inversamente relacionado a la cantidad de Factor Tisular presente en los reactivos. Para minimizar la variación en TP entre reactivos con diferentes cantidades de Factor Tisular, se le asigna a cada uno un Índice de Sensibilidad Internacional (ISI); a menor cantidad de factor tisular, menor valor de ISI y más largo tiempo de protrombina. Para ajustar por diferencias en el ISI de reactivos, es utilizada la relación internacional normalizada (RIN); el valor se calcula como
RIN= (TP paciente / TP media control)ISI
El uso de reactivos con bajo ISI mejora la reproducibilidad de la medición del RIN, haciendo que el uso de reactivos con bajo ISI sea ideal para monitorear la terapia anticoagulante (90).
El efecto del ISI es mucho mayor sobre el TP durante el uso de warfarina que en la enfermedad hepática, por eso el RIN no refleja exactamente la inhibición de la coagulación en la enfermedad hepática (89) (91)(92).
Una muestra de un paciente que recibe warfarina tiene un TP de 20 s con reactivos de alto ISI y un TP de 40 s cuando se prueba con reactivos de bajo ISI, pero el RIN es esencialmente idéntico con ambos reactivos (89). El RIN, entonces, normaliza los resultados en un paciente con warfarina, a pesar de las diferencias en el ISI de los reactivos usados. En la enfermedad hepática, la disminución del ISI de los reactivos usados causa sólo un ligero aumento en el TP. Por ejemplo, una muestra de un paciente con enfermedad hepática tiene un TP de 20 s con reactivos de alto ISI, pero un TP de 23.6 s con reactivos de bajo ISI. Al contrario que en los pacientes con warfarina, en donde el RIN es virtualmente idéntico cuando se usan reactivos con diferente ISI, el RIN fue 2.90 con reactivos de alto ISI y 1,86 con reactivos de bajo ISI (89). Si se usan reactivos con bajo ISI, entonces el RIN desestima marcadamente la alteración del grado de coagulación en la enfermedad hepática. Una posible causa para la discrepancia en la utilidad del RIN entre el uso de warfarina y la enfermedad hepática es la marcada diferencia en las cantidades relativas de protrombina nativa versus la protrombina des-g-carboxilada presente en ambas condiciones. Los pacientes con warfarina o con déficit de vitamina K tienen una marcada elevación de la des-g-carboxi-protrombina y una disminución de la protrombina nativa, mientras que los pacientes con hepatitis aguda o cirrosis han disminuido la protrombina nativa con sólo una ligera elevación de la des-g- protrombina (93). Algunas preparaciones de Factor Tisular son inhibidas por la des-g-protrombina (93).
En la hepatitis aguda isquémica (94)(95) y en la tóxica (96) el TP tiene un aumento de más de 3 segundos que la media de la población pero en las hepatitis virales (97) o alcohólicas (98)(99) raramente esté elevado más de 3 segundos. El TP a menudo está elevado en la ictericia obstructiva y puede responder a la administración parenteral de vitamina K. En la hepatitis crónica el TP está típicamente dentro de los límites de referencia pero aumenta a medida que progresa a cirrosis y está elevado en pacientes cirróticos (100). Otros factores que afectan el TP se resumen en la Tabla VII.
Reactivos con el mismo ISI típicamente brindan diferentes resultados sobre diferentes instrumentos aun del mismo modelo (103). Además, cuando se usan reactivos de diferentes fabricantes con el mismo ISI, la misma muestra puede dar diferentes RINs (104). La reproducibilidad de los resultados del TP en laboratorios que usan el mismo instrumento y reactivos es del 3-8% cuando los tiempos de protrombina son prolongados; la variación es mayor para el RIN que para el tiempo de protrombina en sí mismo. Dentro de un laboratorio, la variación promedio en el RIN está estimada en un ± 10% (105). La diferencia en el TP entre laboratorios que usan diferentes reactivos puede ser marcada; en un estudio, la diferencia promedio fue de 20% (104). Recientemente, el uso de plasmas calibradores para determinar el ISI en cada laboratorio para sus propios instrumentos y reactivos, ha demostrado mejorar significativamente la reproducibilidad del RIN (104)(106)(107).
Tabla VII. Factores que afectan el tiempo de protrombina.

RECOMENDACIONES
Debe usarse el TP (en segundos), más que el RIN, para expresar resultados del tiempo de protrombina en pacientes con enfermedad hepática; sin embargo, esto no estandariza resultados entre laboratorios (IIB).
Se necesita investigación adicional sobre estandarización de reactivos y uso de índices derivados (porcentaje de actividad, RIN) en la enfermedad hepática (IVB).
Amoníaco (NH3)
El amoníaco es producto del metabolismo de los aminoácidos, primariamente se depura a través de la síntesis de urea en el hígado. En pacientes con cirrosis, el Helicobacter pylori en el estómago, parece ser una fuente importante de amoníaco (108). En la enfermedad hepática, el aumento de NH3 es un signo típico de lesión hepática. Pueden observarse concentraciones altas en los casos de deficiencias de enzimas del ciclo de la urea (110), Síndrome de Reye (111), y con encefalopatía hepática aguda o crónica (112)(113). Leves incrementos plasmáticos de NH3 se observan en pacientes con hepatitis crónica, proporcionalmente a la extensión de la enfermedad (114). Está controvertido el uso de NH4 para monitoreo de pacientes con encefalopatía; algunos estudios han mostrado una buena correlación entre las concentraciones de amoníaco y el grado de encefalopatía (111)(113), mientras que otros lo han negado (115). El NH3 parece mejorar el efecto del ácido g-aminobutírico (GABA) (116) así como incrementar los receptores para las benzodiazepinas (117): ambos han sido implicados en la patogénesis de la encefalopatía hepática. Por otro lado, las características clínicas observadas en personas con hiperamoniemia aislada no son idénticas a las de la encefalopatía hepática (118). En la Tabla VIII se resumen otros factores que afectan al NH3.
En las muestras, debe separarse el plasma de las células dentro de la primera hora de obtención; en pacientes con enfermedad hepática es ideal la separación dentro de los quince minutos (120) (122).
Varios métodos han sido usados para medir el amoníaco (120); los ensayos enzimáticos han sido los más empleados. Un fabricante usa tecnología en placas
Tabla VIII. Factores que afectan el amoníaco además de la lesión hepática.

RECOMENDACIONES
La medición del amoníaco plasmático para diagnóstico o monitoreo de encefalopatía hepática no se recomienda como rutina en pacientes con enfermedad hepática aguda o crónica: puede ser útil en pacientes con encefalopatía de etiología desconocida (IIIB).
Para medidas más seguras debe usarse sangre arterial, más que venosa (IIB).
El plasma debería separarse de las células dentro de los 15 minutos de la obtención de la muestra para evitar aumentos artificiales de amoníaco (IIB).
Referencias bibliográficas
1. Alter MJ, Kruszon-Moran D, Nainan OV, McQuillan GM, Gao F, Moyer LA, et al. The prevalence of hepatitis C virus infection in the United States. 1988 through 1994. N Engl J Med 1999; 341: 556-62.
2. Staadatmand F. Stinson FS, Grant BF, Dufour MC. Surveillance Report #49 -liver cirrhosis mortality in The United States, 1970-1995. U.S. Department of Health and Human Services. Public Health Service. National Institutes of Health.
3. Davis GL, Albright JH, Cook SF, et al. Projecting the future healthcare burden from hepatitis C in the United States. Hepatology 1998; 28: 390A.
4. El-Serag HB, Mason AC. Rising incidence of hepatocellular carcinoma in the United States. N Engl J Med 1999; 340: 745-50.
5. Kaplan LA. Determination and application of desirable analytical performance goals: the ISO/TC 212 approach. Scand J Clin Lab Invest 1999; 59: 479-82.
6. Fraser CG. The application of theoretical goals based on biological variation data in proficiency testing. Arch Pathol Lab Med 1988; 112: 404-15.
7. Westgard JO, Seehafer JJ, Barry PL. European specifications for imprecision and inaccuracy compared with operating specifications that assure the quality required by US CLIA proficiency-testing criteria. Clin Chem 1994; 40: 1228-32.
8. Ricos C, Alvarez V, Cava F, García-Lario JV, Hernández A, Jiménez CV, et al. Current databases on biological variation: pros, cons and progress. Scand J Clin Lab Invest 1999; 59: 491-500.
9. Skendzel LP, Barnett RN, Platt R. Medically useful criteria for analytic performance of laboratory tests. Am J Clin Pathol 1985; 83: 200-5.
10. Lott JA, Tholen DW, Massion CG. Proficiency testing of enzymes. Charting the way toward standardization. Arch Pathol Lab Med 1988; 112: 392-8.
11. Ross JW, Lawson NS. Analytic goals, concentration relationships, and state of the art for clinical laboratory precision. Arch Pathol Lab Med 1995; 119: 495- 513.
12. Lott JA, Wolf PL. Alanine and aspartate amino-transferase (ALT and AST). Clinical enzymology: a case-oriented approach. Chicago: Year Book Medical Publishers, 1986, 111-38
13. Rej R. Measurement of aminotransferases: Part I. Aspartate aminotransferase. CRC Crit Rev Clin Lab Sci 1984; 21: 99-106.
14. Price CP, Alberti KGMM. Biochemical Assessment of I.iver Function. In Wright R. Alberti KGMM, Karran S. Millward Saldler GH (eds.): Liver and Biliary Disease- Pathophisiology, Diagnosis, Management. London: W.B. Saunders; 1979, 381-416.
15. Panteghini M. Aspartate aminotransferase isoenzymes. Clin Biochem 1990; 23: 311-9.
16. Siest G, Henry J, Schiele F, Young DS. Interpretation of Clinical Laboratory Tests: Reference Values and Their Biological Variation. Foster City, CA: Biomedical Publications; 1985.
17. Siest G, Schiele F, Galteau MM, Panek E, Steinmetz J, Fagnani F, et al. Aspartate aminotransferase and alanine aminotransferase activities in plasma: statistical distribution, individual variations, and reference values. Clin Chem 1975; 21: 1077-87.
18. Cordoba J, O'Riordan K. Dupuis J, Borensztajin J, Blei AT. Diurnal variation of serum alanine transaminase activity in chronic liver disease. Hepatology 1999; 28: 1724-5.
19. Fraser CG. Biological variation in clinical chemistry: an update: collated data, 1988-1991. Arch Pathol Lab Med 1992: 116: 916-23.
21. Manolio TA, Burke GL, Savage PJ, Jacobs DR Jr, Sidney S, Wagenknecht LE, et al. Sex- and race-related differences in liver-associated serum chemistry tests in young adults in the CARDIA study. Clin Chem 1992;38(9):1853-9.
22. Salvaggio A, Periti M, Miano L, Tavanelli M, Mazurati D. Body mass index and liver enzyme activity in serum. Clin Chem 1991; 37: 720-3.
23. Piton A, Poynard T, Imbert-Bismut F, Kalil L, Delattre J, Pelissier E, et al. Factors associated with serum alanine aminotransaminase activity in healthy subjects: consequences for the definition of normal values, for selection of blood donors, and for patients with chronic hepatitis C. MULTIVIRC group. Hepatology 1998; 27: 1213-9.
24. Nuttall FQ, Jones B Creatinine kinase and glutamic oxalacetic transaminase activity in serum: kinetics of change with exercise and effect of physical conditioning. J Lab Clin Med 1968; 257-61.
25. Dufour DR. Effects of habitual exercise on routine laboratory tests. Clin Chem 1998; 44: 136.
26. Ono T, Kitaguchi K, Takehara M, Shiiha M, Hayami K. Serum-constituents analyses: effect of duration and temperature of storage of clotted blood. Clin Chem 1981; 27: 35-8.
27. DiMagno EP, Corle D, O'Brien JF, Masnyk IJ, Go VL, Aamodt R. Effect of long-term freezer storage, thawing. and refreezing on selected constituents of serum. Mayo Clin Proc 1989; 27: 1226-34.
28. Prasad R, Firkins K, Fiorello J: Stability of AST and ALT assays in Tris buffers. Clin Chem 1990; 36: 407-8.
29. Litin S, O'Brien JF, Pruett S, Forsman RW, Burrit MF, Bartholomew LG, et al. Macroenzyme as a cause of unexplained elevation of aspartate aminotransferase. Mayo Clin Proc 1987; 62: 681-7.
30. Mifflin TE, Bruns DE, Wrotnoski U, Mac Millan RH, Stallings RG, Fólder RA, et al. Macroamylase, macro creatine kinase, and other macroenzymes. Clin Chem 1985; 31: 1743-8.
31. Nalpas B, Vassault A, Le Guillou A, Lesgourgues B, Ferry N, Lacour B, et al. Serum activity of mitochondrial aspartate aminotransferase: a sensitive marker of alcoholism with or without alcoholic hepatitis. Hepatology 1984; 4: 893-6.
32. Pol S, Nalpas B, Vassault A, Bousquet-Lemercier B, Franco D, Lacour B, et al. Hepatic activity and mRNA expression of aspartate aminotransferase isoenzymes in alcoholic and non alcoholic liver disease. Hepatology 1991; 14: 620-5.
33. Ludwig S, Kaplowitz N. Effect of serum pyridoxine deficiency on serum and liver transaminases in experimental liver injury in the rat. Gastroenterology 1980; 79: 545-9.
34. Zhou S-L, Gordon RE, Bradbury M, Stump D, Kiang C-L, Berk PD. Ethanol up-regulates fatty acid uptake and plasma membrane expression and export of mitochondrial aspartate aminotransferase in Hep G-2 cells. Hepatology 1998; 27: 1064-74.
35. Bergmeyer HU, Scheibe P, Wahlefeld AW. Optimization of methods for aspartate aminotransferase and alanine aminotransferase. Clin Chem 1978; 24: 58-73.
36. Vanderlinde RE. Review of pyridoxal phosphate and the transaminases in liver disease. Ann Clin Lab Sci 1986; 16: 79-93.
37. Allman MA, Pang E, Yau DF, Stewart PM, Tiller DJ, Truswell AS. Elevated plasma vitamers of vitamin B6 in patients with chronic renal failure on regular hemodialysis. Eur J Clin Nutr 1992; 46: 679-83.
38. Dybkaer R. International Federation of Clinical Expert Panel on Theory of Reference Values and International Committee for Standardization in Haematology Standing Committee on Reference Values: Approved recommendation (1987) on the Theory of Reference Values Part 6. Presentation of observed values related to reference values. Labmedica 1988 (Apr/May), 27-30.
39. Lott JA, Tholen DW, Massion CG. Determination of reference ranges for serum enzymes via a large interlaboratory survey. Arch Pathol Lab Med 1987; 111: 9-15.
40. Moss DW. Multiple forms of acid and alkaline phosphatases: genetics, expression and tissue modification. Clin Chim Acta 1986; 161: 123-35.
41. Weiss MJ, Ray K, Henthorn PS, et al. Structure of the human liver/bone/kidney alkaline phosphatase gene. J Biol Chem 1988; 263: 12002-10.
42. Clubb JS, Neale FC, Posen S. The behavior of infused placental alkaline phosphatase in human subjects. J Lab Clin Med 1965; 66: 493-507.
43. Moss DW. Physicochemical and pathophysiological factors in the release of membrane-bound alkaline phosphatase from cells. Clin Chim Acta 1997; 257: 133-40.
44. Schlaeger R, Haux D, Kattermann R. Studies on the mechanism of the increase in serum alkaline phosphatase activity in cholestasis: significance of the hepatic bile acid concentration for the leakage of alkaline phosphatase from rat liver. Enzyme 1982; 28: 3-13.
45. Bayer PM, Hotschek H, Knoth E. Intestinal alkaline phosphatase and the ABO blood group system: a new aspect. Clin Chim Acta 1980; 108: 81-7.
46. Gordon T. Factors associated with serum alkaline phosphatase level. Arch Pathol Lab Med 1993; 117: 87-190.
47. Young DS. Effects of Preanalytical Variables on Clinical Laboratory Tests, 2nd ed.. Washington, DC: AACC Press; 1997.
48. Yamada N, Kido K, Hayashi S, et al. Characteristics of blood biochemical constituents of pregnant women. Acta Obstet Gynaec Jpn 1977; 29: 447-50.
49. Dufour DR. Effects of oral contraceptives on routine laboratory tests. Clin Chem 1998; 44: 137.
50. Bowers GN Jr, McComb RB, Kelley ML. Measurement of total alkaline phosphatase activity in human serum. Sel Meth Clin Chem 1977; 8: 31-9.
51. Gomez B, Ardakani S, Ju J, et al. Monoclonal antibody assay for measuring bone-specific alkaline phosphatase activity in serum. Clin Chem 1995; 41: 1551-3.
52. Anciaux ML, Pelletier AG, Attali P, Meduri B, Liguory C, Etienne JP. Prospective study of clinical and bio-chemical features of symptomatic choledo-cholithiasis. Dig Dis Sci 1986; 31: 449-53.
53. Sheeman M, Maythorn P. Predictive value of gammaglutamyl transpeptidase in various liver diseases. In: Goldberg DM, Werner M, eds. Progress in Clinical Enzymology, New York: Masson; 1979, 184-7.
54. Ratanasavanh D, Tazi A, Gaspart E. Hepatic gammaglutamyl transferase release: effect of bile salt and membrane structure modification. Advan Biochem Pharmacol 1982; 3: 93-103.
55. Itoh S, Nakajima M. Liver gamma-glutamyl transferase activity in viral liver disease. Digestion 1986; 33: 121-5.
56. Nemesanszky E, Lott JA. Gamma-glutamyltransferase and its isoenzymes: progress and problems. Clin Chem 1985; 31: 797-803.
57. Nilssen O, Helge-Forde O, Brenn T. The Tromso studydistribution and population determinants of gammaglutamyltransferase. Am J Epidemiol 1990; 132: 318-26.
58. Schiele F. Guilmin AM, Detienne H, Siest G. Gamma-glutamyltransferase activity in plasma: statistical distributions, individual variations, and reference intervals. Clin Chem 1977; 23: 1023-8.
59. Combes B, Shore GM, Cunningham FG, Walker FB, Shorey JW, Ware A. Serum gamma-glutamyl transpeptidase activity in viral hepatitis: suppression in pregnancy and by birth control pills. Gastroenterology 1977; 72: 271-4.
60. Young DS. Effect of Drugs on Clinical Laboratory Tests, 4th ed.. Washington, D.C.: AACC Press; 1995.
61. Moussavian SN, Becker RC, Piepmeyer JL, Mezey E, Bozian RC. Serum gamma-glutamyl transpeptidase and chronic alcoholism - influence of alcohol ingestion and liver disease. Dig Dis Sci 1985; 30: 211-4.
62. Hedworth-Whitty RB, Whitfield JB, Richardson RW. Serum gamma-glutamyltranspeptidase activity in myocardial ischaemia. Brit Heart J 1967; 29: 432-8.
63. Burrows S, Feldman W, McBride F. Serum gammaglutamyl transpeptidase. Evaluation in screening of hospitalized patients. Am J Clin Pathol 1975; 64: 311-4.
64. Shaw LM, Stromme JH, London JL, Theodorsen L: International Federation of Clinical Chemistry. Scientific Committee, Analytical Section. Expert Panel on Enzymes. IFCC methods for measurement of enzymes. Part 4. IFCC methods for gamma-glutamyltransferase [(gamma-glutamyl)-peptide: amino acid gamma-glutamyltransferase, EC 2.3.2.2]. Clin Chim Acta 1983; 135: 315f-38f.
65 Chowdhury JR, Wolkoff AW, Chowdhury NR, Arias IM. Hereditary jaundice and disorders of bilirubin metabolism. In: The metabolic and molecular bases of inherited disease, Scriver CR, Beaudet AL, Sly WS, Valle D, Stanbury JB, Wyngaarden JB, Fredrickson DS, eds., New York: McGraw-Hill, Inc.; 1995; 2: 2161-208.
66. Berk PD, Martin JF, Blaschke TF, Scharchmidt BF, Plotz PH: Unconjugated hyperbilirubinemia: physiologic evaluation and experimental approaches to therapy. Ann Intern Med 1975; 82: 552-70.
67. Bloomer JR, Berk PD, Vergalla J, Berlin NI. Influence of albumin on the extravascular distribution of unconjugated bilirubin. Clin Sci Mol Med 1973; 45: 517-21.
68. McDonagh AF, Palma AA, Lauff JJ, Wu TW: Origin of mammalian biliprotein and rearrangement of bilirubin glucuronides in vivo in the rat. J Clin Invest 1984; 74: 763-70.
69. Fevery J, Blanckaert N. What can we learn from analysis of serum bilirubin. J Hepatol 1986; 2: 113-21.
70. Berk PD, Noyer C. Clinical chemistry and physiology of bilirubin. Sem Liver Dis 1994; 14: 46-355.
71. Zimmerman HJ. Intrahepatic cholestasis. Arch Intern Med 1979; 139: 1038-45.
72. Van Hootegem P, Fevery J, Blanckaert N. Serum bilirubins in hepatobiliary disease: comparison with other liver function tests and changes in the portobstructive period. Hepatology 1985; 5: 112-7.
73. Bosma PJ, Chowdhury JR, Bakker C, Gantla S, de Boer A, Oostra BA, et al. The genetic basis of the reduced expression of bilirubin UDP-glucuronosyltransferase 1 in Gilbert's syndrome. N Engl J Med 1995; 333 (18): 1171-5.
74. Persico P, Persico E, Bakker C, et al. Hyperbilirubinemia in subjects with Gilbert syndrome (GS) mutations is determined by the rate of hepatic uptake of organic anions. Hepatology 1999; 30: 501A.
75. Thomsen HF, Hardt F, Juhl E. Diagnosis of Gilbert's Syndrome. Scand J Gastroent 1981; 16: 699-703.
76. Barrett PVD. Bilirubinemia and fasting. N Engl J Med 1970; 283: 823.
77. Dufour, DR. Effects of food ingestion on routine laboratory tests. Clin Chem 1998; 44: 136.
78. Carmel R, Wong ET, Weiner JM, Johson CS. Racial differences in serum total bilirubin levels in health and in disease (pernicious anemia). JAMA 1985; 253: 3416-8.
79. Ihara H, Shino Y, Hashizume N, et al. Effect of light on total and direct bilirubin by an enzymatic bilirubin oxidase method. J Anal Biol Sci 1997; 20: 349-54.
80. Doumas BT, Wu T-W, Jendrzejcaz. Delta bilirubin: absorption spectra, molar absorptivity, and reactivity in the diazo reaction. Clin Chem 1987; 33: 769-74.
81. Doumas BT, Wu TW. The measurement of bilirubin fractions in serum. Crit Rev Clin Lab Sci 1991; 28: 415-46.
82. Kubasik NP, Mayer TK, Bhaskar AG, Sine HE, D'Souza JP. The measurement of fractionated bilirubin by Ektachem film slides - method validation and comparison of conjugated bilirubin measurements with direct bilirubin in obstructive and hepatocellular jaundice. Am J Clin Pathol 1985; 84: 518-23.
83. Doumas BT, Peters T. Serum and urine albumin: a progress report on their measurement and clinical significance. Clin Chim Acta 1997; 258: 3-20.
84. Dufour, DR. Gender related differences in liver function and integrity tests. Clin Chem 1998; 44: 137.
85. McGinlay JM, Payne RB. Serum albumin by dye-binding: bromcresol green or bromcresol purple? Ann Clin Biochem 1988; 25: 417-21.
86. Beyer C, Boekhout M, van Iperen H. Bromcresol purple dye-binding and immunoturbidimetry for albumin measurement in plasma or serum of patients with renal failure. Clin Chem 1994; 40: 844-5.
87. Bush V, Reed RG. Bromcresol purple dye-binding methods underestimate albumin that is carrying covalently bound bilirubin. Clin Chem 1987; 33: 821-3.
88. Pascucci MW, Grisley DW, Rand RN. Electro-immunoassay of albumin in human serum: accuracy and long-term precision. Clin Chem 1983; 29: 1787-90.
89. Ts'ao C, Swedlund J, Neofotistos D. Implications of use of low international sensitivity index thrombo-plastins in prothrombin time testing. Arch Pathol Lab Med 1994; 118: 1183-7.
90. Taberner DA, Poller L, Thomson JM, Darby KV. Effect of international sensitivity index (ISI) of thrombo-plastins on precision of international normalised ratios (INR). J Clin Pathol 1989: 42: 92-6.
91. Kovacs MJ, Wong A, MacKinnon K, Weir K, Keeney M, Boyle E, et al. Assessment of the validity of the INR system for patients with liver impairment. Thromb Haemost 1994; 71: 727-30.
92. Robert A, Chazouilleres O. Prothrombin time in liver failure: time, ratio, activity percentage, or International Normalized Ratio? Hepatology 1996; 24: 1392-4.
93. Blanchard RA, Furie BC, Jorgensen M, Kruger SF, Furie B. Acquired vitamin K-dependent carboxylation deficiency in liver disease. N Engl J Med 1981; 305: 242-8.
94. Dufour, DR, Teot, L. Laboratory identification of ischemic hepatitis (shock liver). Clin Chem 1988; 34: 1287.
95. Fuchs S, Bogomolski-Yahalom V, Paltiel O, Ackerman Z. Ischemic hepatitis: clinical and laboratory observations of 34 patients. J Clin Gastroenterol 1998; 26: 183-6.
96. Singer AJ, Carracio TR, Mofenson HC. The temporal profile of increased transaminase levels in patients with acetaminophen-induced liver dysfunction. Ann Emerg Med 1995; 26: 49-53.
97. Willner IR, Uhl MD, Howard SC, Williams EQ, Riely CA, Waters B. Serious hepatitis A: an analysis of patients hospitalized during an epidemic in the United States. Ann Intern Med 1998; 128: 111-4.
98. Mendenhall CL and the VA Cooperative Study Group on Alcoholic Hepatitis: Alcoholic hepatitis. Clin Gastroenterol 1981; 10: 417-41.
99. O'Grady JG, Alexander GJM, Hayllar KM, Williams R. Early indicators of prognosis in fulminant hepatic failure. Gastroenterology 1989; 97: 4439-45.
100. Bonacini M, Hadi G, Govindarajan S, Lindsay KL. Utility of a discriminant score for diagnosing advanced fibrosis or cirrhosis in patients with chronic hepatitis C infection. Am J Gastroneterol 1997; 92: 1302-4.
101. Baglin T, Luddington R. Reliability of delayed INR determination: implications for decentralized anticoagulant care with off-site blood sampling. Br. J. Haematol 1997; 96: 431-4.
102. Adcock DM, Kressen DC, Marlar RA. Effect of 3.2% vs. 3.8% sodium citrate on routine coagulation testing. Am J Clin Pathol 1997; 107: 105-10.
103. Cunningham MTA, Johnson GF, Pennell BJ, Olson JD: The reliability of manufacturer-determined, instrument specific international sensitivity index values for calculating the international normalized ratio. Am J Clin Pathol 1994; 102: 128-33.
104. Stevenson KJ, Craig S, Dufty JMK, Taberner DA. System ISI calibration: a universally applicable scheme is possible only when coumarin plasma calibrants are used. Br J Haematol 1997; 96: 435-41.
105. Lassen JF, Kjeldsen J, Antonsen S, Petersen PH, Brandslund I: Interpretation of serial measurements of international normalized ratio for prothrombin times in monitoring oral anticoagulant therapy. Clin Chem 1995; 41: 1171-6.
106. Poller L. Screening INR deviation of local prothrombin time systems. J Clin Pathol 1998; 51: 356-9.
107. Johnson M, Brigder M: A cross-Canada survey of prothrombin time testing - does the establishment of local ISI values improve the accuracy of International Normalized Ratio reporting? Am J Clin Pathol 1998; 110: 683-90.
108. Miyaji H, Ito S, Azuma T, Ito J, Yamazaki Y, Ohtoki Y, et al. Effects of Helicobacter pylori eradication therapy on hyperammonemia in patients with liver cirrhosis. Gut 1997; 40: 726-30.
110. Batsshaw ML. Inborn errors of urea synthesis. Ann Neurol 1994; 35: 133-41.
111. Heubi JE, Daugherty CC, Partin JS, Partin JC, Schubert WK. Grade 1 Reye's syndrome - outcome and predictors of progression to deeper coma grades. N Engl J Med 1984; 311: 1539-42.
112. Stahl J: Studies of the blood ammonia in liver disease - its diagnostic, prognostic, and therapeutic significance. Ann Intern Med 1963; 58: 1-23.
113. Butterworth RF, Giguere JF, Michaud J, Lavoie J, Layrargues GP. Ammonia: key factor in the pathogenesis of hepatic encephalopathy. Neurochem Pathol 1987; 6: 1-12.
114. Muting D, Kalk JF, Fischer R, Wuzel H, Reikowski J. Hepatic detoxification and hepatic function in chronic active hepatitis with and without cirrhosis. Dig Dis Sci 1988; 33: 41-6.
115. McClain CJ, Zieve L, Doizaki WM, Gilberstadt S, Onstad GR. Blood methanetriol in alcoholic liver disease with and without hepatic encephalopathy. Gut 1980; 21: 318-23.
116. Jones EA, Basile AS. The involvement of ammonia with the mechanisms that enhance GABA-ergic neurotransmission in hepatic failure. Adv Exp Med Biol 1997; 420: 75-83.
117. Norenberg MD, Itzhak Y, Bender AS. The peripheral benzodiazepine receptor and neurosteroids in hepatic encephalopathy. Adv Exp Med Biol 1997; 420: 95- 111.
118. Chamuleau RAFM, Vogels BAPM. Hyperammonemia without portal systemic shunting does not resemble hepatic encephalopathy. Adv Exp Med Biol 1997; 420: 173-83.
119. Diaz J, Tornel PL, Martinez P. Reference intervals for blood ammonia in healthy subjects, determined by microdiffusion. Clin Chem 1995; 41: 1048.
120. Huizenga JR, Tangerman A, Gips CH. Determination of blood ammonia in biological fluids. Ann Clin Biochem 1994; 31: 529-43.
121. Derave W, Bouckaert J, Pannier JL. Gender differences in blood ammonia response during exercise. Arch Physiol Biochem 1997; 105: 203-9.
122. da Fonseca-Wollheim F. Preanalytical increase of ammonia in blood specimens from healthy subjects. Clin Chem 1990; 36: 1483-7.
123. Davies SM, Szabo E, Wagner JE, Ramsay NK, Weisdorf DJ. Idiopathic hyperammonemia: a frequently lethal complication of bone marrow transplantation. Bone Marrow Transplant 1996; 17: 1119-25.
124. Xu SR, Yao EG, Dong ZR, Liu RS, Pan L, Lin FR, et al. Plasma ammonia in patients with acute leukemia. Chin Med J 1992; 105: 713-6.
125. Altunbasak S, Baytok V, Tasouji M, Herguner O, Burgut R, Kayrine L: Asymptomatic hyperammo-nemia in children treated with valproic acid. J Child Neurol 1997; 12: 461-3.
126. Shepard RL, Kraus SE, Babayan RK, Sirosky MB: The role of ammonia toxicity in the post transurethral prostatectomy syndrome. Br J Urol 1987; 60: 349- 51.
127. Ammonia. College of American Pathologists, 325 Waukegan Road, Northfield, IL 60093, Chemistry Survey Set C-B, 1999, 73.














