Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957versión On-line ISSN 1851-6114
Acta bioquím. clín. latinoam. v.43 n.1 La Plata ene./mar. 2009
MICOLOGÍA
Criptococosis pulmonar en una paciente con SIDA
Pulmonary cryptococcosis and AIDS
Mirta Beatriz Peralta1 *, Amadeo Javier Bava2 **
1. Médica Infectóloga
2. Doctor en Medicina
* Unidad de Cuidados Intensivos Respiratorios. Hospital de Enfermedades Infecciosas "Francisco Javier Muñiz". Uspallata 2272. Buenos Aires. Argentina.
** Cátedra de Micología. Facultad de Ciencias Exactas. Universidad Nacional de La Plata. Calle 115 y 47. La Plata. Buenos Aires. Argentina.
Resumen
Se comunica un caso de criptococosis pulmonar en una paciente de 30 años, VIH positiva desde 1997, hospitalizada, con deterioro del estado general, diarrea, mialgias generalizadas y fiebre. Como datos anormales de laboratorio presentó hematocrito de 28%, 1.900 leucocitos/mm3 y 100.000 plaquetas/mm3. Evolucionó con tos seca, disnea, dolor abdominal, ausencia de síntomas neurológicos, un estudio parasitológico positivo para Isospora belli y hemocultivos positivos para Cryptococcus neoformans. La radiografía de tórax reveló un infiltrado intersticial bilateral, similar al provocado por Pneumocystis jiroveci en los pacientes con SIDA. La microscopia en fresco de secreciones respiratorias obtenidas por lavado broncoalveolar, enviadas para la investigación de P. jiroveci, reveló levaduras capsuladas, identificadas luego como C. neoformans. Posteriormente, se observaron levaduras capsuladas en el sedimento del líquido cefalorraquideo (LCR). La paciente fue tratada con anfotericina B a las dosis habituales a pesar de lo cual falleció diez días después de su internación. La localización pulmonar es raramente diagnosticada en pacientes con criptococosis asociada al SIDA; su diagnóstico requiere la visualización microscópica y/o el aislamiento de C. neoformans de secreciones respiratorias. La presencia de C. neoformans en materiales respiratorios obliga a investigar su existencia en el LCR, a pesar de la ausencia de síntomas de afectación neurológica.
Palabras clave: Cryptococosis pulmonar; Criptococosis asociada al SIDA; Virus de la inmunodeficiencia humana.
Summary
A case of pulmonary cryptococcosis in a 30-year-old woman, HIV positive since 1997, who was hospitalized with malaise, diarrhea, generalized myalgias and fever is communicated. As laboratory abnormal data, the patient showed 28% hematocrite, 1,900 leukocytes/mm3 and 100,000 platelets/mm3. She evolved into dry cough, dyspnea and abdominal pain without neurological symptoms, a positive parasitological study for Isospora belli and positive blood cultures for Cryptococcus neoformans. Chest radiology showed a bilateral interstitial infiltrate, similar to that produced by Pneumocystis jiroveci in AIDS patients. Capsulated yeasts, later identified as C. neoformans, were observed in a wet mount examination of respiratory secretions obtained by bronchoalveolar lavage, sent for analysis of P. jiroveci. Subsequently, India ink microscopy of a CSF sample showed capsulated yeasts and the patient was treated with amphotericin B in the usual dose; in spite of that, she died ten days after admission. Pulmonary cryptococcosis is a rarely diagnosed localization of this mycosis in AIDS patient, and its diagnosis requires the microscopic visualization and/or isolation of C. neoformans from respiratory secretions. The presence of C. neoformans in respiratory samples compels the search for the likely localization of this yeast in the CSF, in spite of the absence of symptoms of the neurological condition.
Keywords: Pulmonary cryptococcosis; AIDS associated cryptococcosis; Human immunodeficiency virus.
Introducción
La criptococosis es la micosis sistémica más frecuente entre los pacientes con SIDA, con una prevalencia que oscila entre el 5-25%, dependiendo de las regiones geográficas evaluadas (1).
Si bien las manifestaciones clínicas de la enfermedad se relacionan con mayor frecuencia al compromiso del sistema nervioso central (SNC), otras localizaciones son también observables, entre ellas la pulmonar, que radiológicamente puede confundirse en los pacientes con SIDA con la neumocistosis (2).
El diagnóstico de la criptococosis pulmonar requiere la visualización del agente causal en secreciones respiratorias, o bien de su aislamiento por cultivos a partir de las mismas (3). La identificación de un aislamiento se realiza mediante el estudio de las características micromorfológicas y la ayuda de ciertas pruebas bioquímicas que permiten su diferenciación de levaduras de otros géneros (producción de ureasa) o aún del mismo género (crecimiento a 37 ºC y producción de fenol oxidasa) (4).
El sólo aislamiento de C. neoformans en cultivos debe interpretarse con cuidado, ya que puede no corresponder a un diagnóstico de criptococosis pulmonar; no obstante, obliga a la búsqueda de este hongo en otras localizaciones, fundamentalmente en pacientes inmunocomprometidos (2)(3).
En este trabajo se comunica un caso de criptococosis pulmonar ocurrido en una paciente con SIDA internada en la Unidad de Cuidados Respiratorios del Hospital Muñiz (UCIR), así como la metodología empleada para su diagnóstico.
Materiales y Métodos
PACIENTE
La paciente, una mujer de 30 años de edad, VIH positiva desde 1997, ingresó a la UCIR el 18 de julio de 2007, presentando deterioro del estado general, diarrea, mialgias generalizadas y fiebre. El examen físico reveló deshidratación, desnutrición, frecuencia respiratoria de 24/min, frecuencia cardíaca de 100/min, temperatura axilar de 36 ºC y presión arterial de 70/40 mm Hg.
La auscultación pulmonar reveló rales crepitantes en ambas bases, y la cardíaca, taquicardia sin descompensación hemodinámica. A nivel neurológico no presentaba cefalea ni signos meníngeos. En el paladar blando se observó una lesión blanquecina interpretada como una candidiasis orofaríngea.
El laboratorio general reveló un hematocrito de 28%, un recuento de 1.900 leucocitos/mm3 y otro de plaquetas de 100.000/mm3, siendo el resto de los parámetros normales.
Recibió tratamiento del síndrome diarreico con ciprofloxacina, y se inició tratamiento retroviral con zidovudina (AZT), didanosina (DDI) y la co-formulación de lopinavir + ritonavir (kaletra®), en las dosis habituales.
La paciente evolucionó con registros aislados de fiebre, tos seca con disnea clase funcional II a III y dolor abdominal difuso. Los hemocultivos y urocultivos fueron bacteriológicamente negativos, mientras que el estudio parasitológico de materia fecal reveló quistes de Isospora belli. Los hemocultivos para hongos fueron positivos para Cryptococcus neoformans.
En un primer estudio radiológico de tórax, se observó la existencia de infiltrados intersticiales bilaterales (Figura 1).

Figura 1. Radiografía de tórax de la paciente que revela infiltrados intersticiales bilaterales.
La microscopia del LCR y las secreciones respiratorias obtenidas por lavado broncoalveolar mostraron levaduras capsuladas, identificadas luego como C. neoformans, lo que determinó la administración de anfotericina B en las dosis habituales y la búsqueda del hongo en el LCR, aún en ausencia de síntomas.
La paciente evolucionó rápidamente con insuficiencia respiratoria por lo que fue derivada a la UCIR, donde requirió asistencia respiratoria mecánica por insuficiencia respiratoria acompañada de progresión radiológica con infiltrados alveolares bilaterales compatibles con síndrome de distrés respiratorio del adulto (Figura 2). La paciente falleció a las 48 h de su ingreso a esa Unidad (28 de julio de 2007).
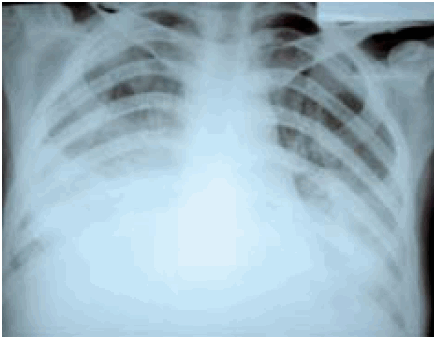
Figura 2. Radiografía de tórax de la paciente que revela infiltrados alveolares bilaterales compatibles con síndrome de distrés respiratorio del adulto.
ESTUDIO MICROBIOLÓGICO DE LAS SECRECIONES RESPIRATORIAS
Se remitieron al laboratorio de Parasitología del Hospital Muñiz las secreciones respiratorias obtenidas por lavado broncoalveolar contenidas en un tubo de plástico estéril con tapa a rosca, en cantidad aproximada de 10 mL, para investigar la presencia de Pneumocystis jiroveci.
La muestra fue centrifugada a 1.500 rpm durante 15 min y con el concentrado se realizaron extendidos que se fijaron a la llama del mechero y una preparación entre porta y cubreobjetos para el examen microscópico en fresco.
Los extendidos fijados a la llama del mechero fueron coloreados, en vista de los resultados de la microscopia en fresco, con las tinciones de Giemsa, Kinyoun, PAS, Mucicarmín de Mayer (5) y una modificación rápida de la técnica Grocott (6).
En base a los resultados de la microscopia en fresco, parte del concentrado fue sembrado en agar glucosado de Sabouraud y agar semillas de girasol (7), adicionados de cloranfenicol, e incubados en estufa de cultivo a 37 ºC durante 1 semana. Con parte de las colonias aisladas se investigó la producción de ureasa en medio de Christensen a 37 ºC.
Resultados
La microscopia en fresco reveló la presencia de levaduras capsuladas (Figura 3), identificadas como tales por el halo claro que rodeaba cada una de estas células, algunas de ellas con brotes únicos y otras con ubicación intracelular. Este estudio de la muestra fue negativo para otros hongos (incluyendo P. jiroveci) y zooparásitos.

Figura 3. Levadura capsulada presente en el concentrado del lavado broncoalveolar de la paciente, observada en fresco (400x).
Las cápsulas de las levaduras fueron evidenciadas con la aplicación de las coloraciones del Mucicarmín de Mayer, PAS y Giemsa (Figura 4). La coloración de Grocott mostró a las levaduras de color negro, en algunas oportunidades rodeada por un espacio claro, correspondiente a una imagen negativa de la cápsula.

Figura 4. Levadura capsulada brotada, presente en un extendido del lavado broncoalveolar de la paciente, teñido con la técnica de Giemsa (1.000x).
Los cultivos, tras 72 horas de incubación a 37 ºC, revelaron el desarrollo de colonias cremosas, de color blanco en agar glucosado de Sabouraud y de color pardo tras una semana en agar semillas de girasol.
La microscopia de las colonias desarrolladas en ambos medios permitió observar levaduras esféricas con cápsula de pequeño tamaño y escasos brotes únicos. La producción de ureasa fue positiva, luego de 48 h de incubación.
Discusión y Conclusiones
A pesar de ser reconocido el pulmón como la puerta de entrada del Cryptococcus neoformans, es proporcionalmente bajo el número de diagnósticos de la localización pulmonar que se realiza, respecto de la afectación del SNC.
Varias revisiones sobre el tema han comunicado la colonización asintomática del árbol respiratorio por parte de C. neoformans, condición que generalmente ocurre asociada a una enfermedad pulmonar favorecedora, tal como la enfermedad pulmonar obstructiva crónica (3).
Estas aseveraciones sugieren que el aislamiento de C. neoformans de secreciones respiratorias de un paciente sin síntomas o evidencias radiológicas de un infiltrado pulmonar debe ser interpretado con cuidado, así como la idea de administrarle un tratamiento antifúngico.
Sin embargo, el hallazgo de C. neoformans en secreciones respiratorias obliga, en todos los casos (aún en ausencia de evidencias de compromiso clínico), a la investigación de este hongo en el LCR a los efectos de descartar su localización más frecuente: el SNC.
El agar semillas de girasol adicionado de cloranfenicol es ideal para el aislamiento de C. neoformans a partir de materiales clínicos eventualmente contaminados, debido a que es un medio diferencial y permite el rápido reconocimiento de las colonias de C. neoformans por su color pardo (7).
En este medio, las colonias de las especies de Candida, las más frecuentemente recuperadas del aparato respiratorio humano, desarrollan de color blanco, así como las de otras especies de Cryptococcus, diferentes de C. neoformans. Estas últimas presentan una micromorfología similar a C. neoformans, pero no desarrollan a 37 ºC.
En la práctica clínica se puede decir que toda levadura redonda, ureasa positiva, que desarrolla a 37 ºC puede interpretarse como un C. neoformans hasta que se demuestre lo contrario, con muy poco margen de error.
En el caso aquí descrito, el resultado positivo para C. neoformans de 3 muestras de hemocultivo, motivó la búsqueda del hongo en LCR y lavado broncoalveolar.
A diferencia de lo observado en huéspedes inmunocompetentes, quienes pueden presentar una neumopatía inaparente, alrededor del 90% de los inmunosuprimidos, entre ellos los pacientes con SIDA, suelen tener síntomas (8).
Las manifestaciones clínicas más frecuentes de la localización pulmonar de la criptococosis son la presencia de fiebre (81%), tos (63%), disnea (50%), pérdida de peso (47%), cefalea (41%) y ocasionalmente dolor torácido por afectación de la pleura, ninguno de los cuales es patognomónico de la criptococosis pulmonar y muchos de los cuales estuvieron presentes en la paciente aquí descrita.
El diagnóstico de certeza requeriría, en todo caso, de la visualización y el aislamiento de C. neoformans a partir de muestras pulmonares obtenidas por métodos invasores, tales como broncoscopia, toracocentesis, aspiración con aguja o bien por biopsia a cielo abierto. No obstante estas aseveraciones teóricas, en la práctica diaria, la presencia de C. neoformans en las secreciones respiratorias de pacientes con SIDA es siempre tomada con mucho cuidado y asociada a la producción de enfermedad, más aún y como en el presente caso, cuando se acompaña de la localización del hongo en el SNC (3).
Los hallazgos radiológicos más frecuentes de la criptococosis pulmonar en los pacientes con SIDA son sumamente inespecíficos y consisten en la presencia de infiltrados alveolares o intersticiales focales o difusos, seguidos por lesiones con forma de cuña, masas, cavidades o derrame pleural, tal cual fuera observado en pacientes internados en el Hospital Muñiz en numerosas oportunidades (9). Los infiltrados intersticiales pueden confundirse fácilmente con aquellos provocados por la neumocistosis pulmonar, la cual es la patología que produce estas alteraciones con mayor frecuencia en los pacientes con SIDA y cuyo diagnóstico de certeza requiere de la observación microscópica de Pneumocystis jiroveci (10).
Teniendo en cuenta el carácter diseminado de la enfermedad, el diagnóstico de criptococosis puede lograrse por el aislamiento de C. neoformans a partir de materiales no respiratorios, tales como escarificación de lesiones cutáneas, orina, biopsias, cultivos de médula ósea, hemocultivos, etc. De hecho, la recuperación de C. neoformans fue lograda de muestras diferentes a secreciones respiratorias en 19/22 pacientes con SIDA y criptococosis pulmonar estudiados en el Hospital Muñiz (9).
Igualmente, estos autores encontraron a C. neoformans en secreciones respiratorias asociado con otros patógenos tales como Mycobacterium tuberculosis y Pneumocystis jiroveci y agregan que el hallazgo de estos últimos no invalida la importancia patógena de C. neoformans (9).
Finalmente, si bien teóricamente puede considerarse controvertido el hallazgo de C. neoformans en secreciones respiratorias, su presencia obliga a considerarlo como posible patógeno (sobre todo en pacientes inmunocomprometidos) y a su búsqueda en el LCR y otros materiales, a pesar de la ausencia de signos y síntomas neurológicos.
CORRESPONDENCIA
DRA. MIRTA BEATRIZ PERALTA
Colpayo 469, 5º "A"
1405 CIUDAD AUTÓNOMA DE BUENOS AIRES
Argentina
E-mail: mirperalta1@yahoo.com.ar
1. Bava AJ, Arechavala AI, Negroni R, Robles AM, Bianchi M. Cryptococcosis associated with AIDS in the Muñiz Hospital of Buenos Aires. Mycopathologia (Deen Haag) 1997; 140: 13-7. [ Links ]
2. Cameron ML, Bartlett JA, Gallis HA, Waskin HA. Manifestations of pulmonary cryptococcosis in patients with acquired immunodeficiency syndrome. Rev Infect Dis 1991; 13: 64-7. [ Links ]
3. Meyohas MC, Roux P, Bollens D, Chouaid C, Rozenbaum W, Meynard JL, et al. Pulmonary cryptococcosis: localized and disseminated infections in 27 patients with AIDS. Clin Infect Dis 1995; 21: 628-33. [ Links ]
4. Mitchell TG, Perfect JR. Cryptococcosis in the era of AIDS--100 years after the discovery of Cryptococcus neoformans. Clin Microbiol Rev 1995; 8: 515-48. [ Links ]
5. Negroni R, Guelfand L. Manual de Procedimientos para Laboratorios de Micología Médica. Acta Bioquím Clin Latinoam 1999; 34 Supl 1: 37-47. [ Links ]
6. Bava AJ. Coloración rápida para la identificación de quistes de Pneumocystis carinii en materiales respiratorios. Acta Bioquím Clín Latinoam 2003; 37: 189-92. [ Links ]
7. Pal M, Mehrotra BS. Studies on the efficacy of sunflower seed agar for the isolation and identification of Cryptococcus neoformans Arogya; J Health Sci 1982; 8: 74-9. [ Links ]
8. Chechani V, Kamholz SL. Pulmonary manifestations of disseminated cryptococcosis in patients with AIDS. Chest 1990; 98: 1060-6. [ Links ]
9. Helou S, Robles AM, Arechavala AI, Bianchi MH, Negroni R. Criptococosis respiratoria en pacientes HIV positivos. Rev Iberoam Micol 1999; 16: 126-9. [ Links ]
10. Delorenzo LJ, Huang CT, Maguire GP, Stone DJ. Roentgenographic patterns of Pneumocystis carinii pneumonia in 104 patients with AIDS. Chest 1987; 91: 323-7. [ Links ]
Aceptado para su publicación el 24 de octubre de 2008














