Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957
Acta bioquím. clín. latinoam. v.44 n.1 La Plata ene./mar. 2010
SECCIÓN PERMANENTE LATINOAMERICANA
Papel de los Dímeros D en la Enfermedad Venosa Tromboembólica (EVT)
L. Sitbon1
1. Laboratorio de Bioquímica y de Biología Molecular. Hospital Lariboisière, París.
Editor: Dr. Camilo Fernández Espina
Colaboración: Dr. Miguel Blasco Vega
Asociación Española de Farmacéuticos
Analistas Modesto Lafuente, 3 - 28010 Madrid
AEFA agradece a Biologiste et Praticien las facilidades y autorización desinteresada para la traducción al español y la inserción de sus artículos en Laboratorio y Clínica. Los autores de los originales no son, en ningún caso, responsables de la absoluta fidelidad en la traducción de los mismos.
Resumen
Los Dímeros D son una combinación de moléculas, todas diferentes, provenientes de la degradación de moléculas de fibrina, que se caracterizan por un mismo enlace proteico D=D. Su cuantificación se realiza con ayuda de métodos inmunológicos que utilizan anticuerpos monoclonales que reconocen un epitopo del enlace D=D.
En la práctica, una tasa de Dímeros D inferior a 500 ng/mL (cut-off) permite descartar el diagnóstico de enfermedad venosa tromboembólica en aproximadamente el 95% de los pacientes en caso de probabilidad clínica baja o intermedia. No obstante, su valor predictivo positivo es malo; un resultado positivo (> 500 ng/mL) no presenta especificidad alguna para este diagnóstico.

Introducción
En Francia, la Enfermedad Venosa Tromboembólica (EVT), que puede manifestarse clínicamente por una trombosis venosa profunda o una embolia pulmonar, se cifra en 200.000 casos al año, con hasta 20.000 defunciones. Se trata de un problema importante de salud pública.
El diagnóstico de la EVT es difícil. En efecto, los principales signos y síntomas clínicos (disnea y dolor basitorácico espontáneos y severos) son poco frecuentes, inespecíficos y a menudo desatendidos o subestimados por el paciente. La medicina moderna utiliza árboles de decisión que asocian clínica y exámenes complementarios de imagen tales como la escintigrafía pulmonar, el angioescáner torácico espiral o la angiografía pulmonar. Estos exámenes son molestos, caros y a veces invasivos, de ahí la utilidad de una prueba biodiagnóstica no invasiva como la determinación de los Dímeros D, productos de la degradación específica de la fibrina, en el diagnóstico de exclusión de la EVT.
2. Bosquejo fisiopatológico
2.1. ENFERMEDAD VENOSA TROMBOEMBÓLICA
La embolia pulmonar (EP) corresponde a la oclusión de la arteria pulmonar o de sus ramas por un émbolo, generalmente un coágulo de fibrina proveniente de una trombosis venosa profunda. Estas dos afecciones entran en el marco de la EVT.
La aparición de una trombosis en la red venosa profunda responde a diferentes factores patológicos reagrupados según la tríada de Virchow:
. Lesiones venosas parietales.
. Éstasis venoso.
. Trombofilia (estado de hipercoagulabilidad debido al exceso de factores procoagulantes o al déficit en factores anticoagulantes).

Cada uno de estos acontecimientos puede ser influenciado por diferentes circunstancias fisiopatológicas (Tabla I).
Tabla I. Diferentes factores de la trombosis venosa según la tríada de Virchow.

2.2. DÍMEROS-D
Los Dímeros D son unas especies moleculares heterogéneas con el mismo grupo proteico. Son el resultado de un ciclo que pone en juego la acción de tres enzimas sobre las moléculas de fibrinógeno en tres etapas (Figura 1):
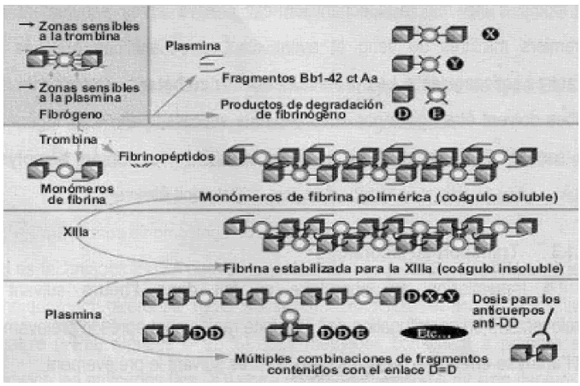
Figura 1. Transformación del Fibrinógeno en Dímeros D
. Acción de la trombina: insolubilización del fibrinógeno
La trombina elimina los fibrinopéptidos A y B (péptidos que aseguran la solubilidad del fibrinógeno) y transforma así el fibrinógeno en monómero de fibrina.
Éstos se amontonan unos sobre otros con el fin de formar filamentos (monómeros de fibrina polimerizados, coágulo soluble).
. Acción del factor XIII: consolidación de los monómeros de fibrina
El factor XIII permite que se entrelacen por un enlace covalente los extremos terminales de dos monómeros de fibrina adyacentes (llamados fragmentos D de la molécula de fibrinógeno). Así se forma el enlace D=D.
3. Dímeros D y fisiopatología
3.1. FASE PREANALÍTICA
3.1.1. Muestra
La determinación se realiza en plasma citratado, después de centrifugación de la sangre obtenida por punción venosa. La sangre puede también ser recogida en tubo CTAD (citrato, teofilina, adenina, dipiridamol). Cualquier otro anticoagulante está proscrito. Se recomienda la utilización de tubos de vidrio.
. Acción de la plasmina: lisis de monómeros de fibrina estabilizados
La plasmina corta este filamento largo de fibrina en pequeñas unidades, de aquí la formación de combinaciones múltiples de fragmentos heterogéneos que contiene el mismo motivo proteico D=D.
En resumen, los Dímeros D son unos productos heterogénos de degradación por la plasmina, de moléculas de fibrina polimerizadas y estabilizadas bajo la acción del factor XIII.
La presencia de un trombo en el marco de una EVT activa este ciclo explicando así el aumento de Dímeros D en caso de trombosis venosa profunda o en caso de embolia pulmonar.
3.1.2. Toma de muestra
Con la excepción de los casos de urgencia, la toma de muestra se hace por la mañana en ayunas (café, tabaco, alcohol suspendidos en la hora que precede a la toma de muestra) y en posición acostada o sentada los treinta minutos anteriores. La compresión del brazo debe limitarse a menos de un minuto. La muestra se recoge después de despreciar los primeros mililitros de sangre y antes de recoger otras muestras sobre otros anticoagulantes. Está proscrita la toma de muestra a través de catéter. Los tubos deben agitarse por vueltas sucesivas con el fin de homogeneizar la sangre y el anticoagulante. Las muestras lactescentes o hemolizadas deben ser rechazadas y se debe verificar la ausencia de microcoagulación.
3.1.3. Transporte al laboratorio
El envío al laboratorio se hace dentro de la hora de la toma de muestra. La centrifugación debe hacerse rápidamente después de la toma y el análisis en las dos horas siguientes.
En caso de análisis diferido, el plasma se puede congelar a -80 °C.
3.1.4. Resultados
El resultado se expresa en ng/mL o pg/mL o pg/L. Según los reactivos, pueden ser unidades fibrinógeno-equivalente (FEU) o unidades Dímeros D.
3.2. METODOLOGÍA
A causa de la naturaleza heterogénea de las moléculas de Dímeros D, su medición plasmática por métodos inmunológicos se hace con anticuerpos monoclonales específicos de un epitope que tiene la secuencia DD de los Dímeros D.
Hay tres grandes familias:
. Métodos semicuantitativos de aglutinación de partículas de látex (únicamente utilizables en el contexto de activación masiva de la coagulación, CIVD por ejemplo).
. Métodos cuantitativos inmunoenzimáticos de tipo ELISA de primera generación y luego de segunda generación.
. Métodos cuantitativos de aglutinación de micropartículas de látex con detección turbidimétrica, automatizables en autoanalizadores de hemostasia o de bioquímica.
Las técnicas ELISA convencionales (de primera generación) son las técnicas de referencia (gold standard): sensibilidad y valor predictivo negativo (VPN) elevado (> 95%). Estos métodos consisten en formar un sandwich con los antígenos (los DD) entre el primer anticuerpo, llamado «de captura», fijado en el fondo de una placa de medida y el segundo anticuerpo, llamado «de revelado» marcado con un sustrato cromógeno o fluorescente. La cantidad de anticuerpo retenido en este sandwich es proporcional a la cantidad de DD en la muestra analizada.
Sin embargo, aunque estas técnicas son los métodos de referencia, presentan poco interés de rutina habida cuenta de los inconvenientes de su realización técnica: tiempos largos, técnicas costosas.
Las técnicas ELISA de segunda generación (la más utilizada, Vidas D-Dimer® ), aparecidas a partir de 1995, aseguran una sensibilidad excelente de las pruebas ELISA y una comodidad suficiente para permitir su utilización en la rutina hospitalaria: pruebas unitarias, rápidas de realizar, de costo razonable y bastante fiables para ser incluidas en la estrategia diagnóstica de la EVT.
Sin embargo, la inmensa mayoría de los equipos comercializados hoy se basan en el principio de aglutinación de micropartículas de látex recubiertas con un anticuerpo monoclonal. Su principal interés reside en su automatización en los autoanalizadores de bioquímica y de hemostasia (los mismos analizadores usados para perfiles analíticos normalizados), su rapidez de ejecución (algunos minutos) y su costo menor que la prueba ELISA (Tabla II).
Tabla II. Prestaciones de los métodos analíticos de Dímeros D comercializados para el diagnóstico de la EVT.

3.3. INTERPRETACIÓN
Sea cual fuere el método, los resultados se informan con un umbral de positividad de alrededor de 500 ng/mL. En presencia de una trombosis establecida, la tasa de Dímeros D siempre está aumentada: los falsos negativos son muy raros. En cambio, la tasa plasmática de Dímeros D puede ser positiva (>500 ng/mL) en numerosas condiciones no trombóticas:
. Fisiológicas:
- Edad >70 años
- Embarazo. Patológicas:
- Cirugía reciente y período postoperatorio
- Afecciones coronarias
- Síndrome inflamatorio
- Tumores sólidos, hemopatías malignas
- Coagulación intravascular diseminada
- Infecciones virales, bacterianas o parasitarias
- Síndrome de lisis tumoral
Por otro lado, numerosas moléculas terapéuticas modifican la tasa de Dímeros D:
. Disminución: aspirina, algunas estatinas, warfarina y medicinas antitrombóticas.
. Aumento: estrógenos, contracepción oral, prostaciclina, lidocaína, uroquinasa, estreptoquinasa.
Las causas de falsos positivos pues son muy frecuentes. El análisis de Dímeros D se inscribe hoy en una estrategia de diagnóstico de exclusión de la EVT; sin embargo, esta estrategia no puede concebirse más que para un paciente que no presenta ningún factor de riesgo de aumento de Dímeros D.
Así, la dosificación en pacientes hospitalizados y clínicamente sospechosos de embolia pulmonar, es a menudo menos informativa que en pacientes ambulatorios, teniendo en cuenta que hay múltiples factores que pueden aumentar su tasa plasmática.
4. Interés de la determinación de Dímeros D en la EVT
4.1. INTERÉS DIAGNÓSTICO EN LA EMBOLIA PULMONAR
Delante de un cuadro típico de embolia pulmonar (disnea, dolor basitorácico espontáneo agudo, +/-hemoptisis), no hay estrategia diagnóstica alguna bien establecida que permita el diagnóstico cierto de embolia pulmonar. Sin embargo, la actitud general comprende en primera intención una evaluación clínica y el establecimiento de una puntuación como las obtenidas a partir de las escalas de Wells o de Geneva (Tabla III), ya que esta metodología no permite hacer un diagnóstico formal, aunque sí orientar en el enfoque diagnóstico.
Tabla III . Escalas de Wells y Geneva (para el riesgo de embolia pulmonar)

A partir de estas puntuaciones clínicas se han establecido algoritmos decisorios que integran la medición de Dímeros D al lado de exámenes de imagen tales como la escintigrafía pulmonar de ventilación y de perfusión, el angioescáner o la angiografía pulmonar (Figura 2). En la inmensa mayoría de los casos, la cuantificación de Dímeros D figura por encima de estos exámenes más costosos e invasivos y operador dependientes, que serán prescritos sólo en caso de que la tasa de Dímeros D sea superior al valor umbral definido (500 ng/mL). Por otro lado, esta dosificación es sobre todo útil en caso de probabilidad débil o moderada de embolia pulmonar (ver escala de puntuación). Ello permite excluir rápidamente en alrededor del 30% de los casos la presencia de una embolia pulmonar si el resultado es inferior al umbral de decisión. En cambio, en caso de gran probabilidad clínica, los exámenes de imagen se prescriben de entrada con el fin de optimizar el abordaje del paciente.

Figura 2. Algoritmo decisorio en la enfermedad venosa tromboembólica
En resumen, la determinación de Dímeros D, prueba biodiagnóstica no invasiva, permite excluir el diagnóstico de EVT si su tasa es inferior al valor umbral, en caso de probabilidad clínica débil o moderada.
Los beneficios esperados en los pacientes en los cuales la prueba sea negativa son:
. Reducir el tiempo de hospitalización;
. Reducir el número de exploraciones invasivas;
. Evitar un tratamiento anticoagulante, así como sus efectos secundarios;
. Reducir el costo.
4.2. OTROS INTERESES
Han sido propuestas otras indicaciones del análisis de Dímeros D :
• Vigilancia del tratamiento trombolítico en la embolia pulmonar;
• Seguimiento de la evolución de una flebitis o de embolia pulmonar tratada;
• Determinación del riesgo de recidiva de enfermedad venosa tromboembólica.

En cuanto a este último punto, un estudio mostró que los Dímeros D caían por debajo del umbral generalmente tres meses después de un episodio de trombosis venosa profunda o de embolia pulmonar. Su tasa cae desde el primer día de tratamiento con heparina y habitualmente continúa disminuyendo progresivamente bajo antivitamina K. Así, una tasa de Dímeros D por debajo del umbral en un paciente sospechoso de recidiva de EVT más allá de tres meses podría excluir la recidiva. Sin embargo, la eficacia clínica de tal estrategia todavía no está validada.

5. Conclusión
La determinación analítica de Dímeros D ha modificado el abordaje de la EVT, permitiendo excluir su diagnóstico cuando su tasa es inferior al valor umbral, evitando así la prescripción de exámenes de imagen pesados y costosos.
La aparición de nuevas técnicas ha contribuido al aumento de la prescripción de esta prueba en un contexto de urgencia: realización en Urgencias, las 24 horas del día, gracias a una técnica fiable, automatizada en los principales analizadores de bioquímica y de hematología, de costo razonable y sobre todo de tiempo de respuesta rápido, adaptado a la urgencia.


Referencias bibliográficas
1. Freyburger G, Saillour F, Trilluad H, Labrouche S, Constans J, Laurent F, et al. Les D-dimères dans l'exclusion de thrombose: théorie, réalité quotidienne et perspective d'intégration dans une stratégie globale. Sang Throm Vaiss 2000; 12 (9): 547-58. [ Links ]
2. Bordenave L. Aspect biologique: la place des D-dimères dans le diagnostic et le suivi de la maladie thromboembolique. Médecine Nucléaire- Imaginerie fonctionnelle et métabolique 2001 ; 25: 250-5. [ Links ]
3. Lecourvoisier C, Toulon P. Intérêt du dosage des Ddimères dans le diagnostic d'exclusion de l'embolie pulmonaire. Ann Biol Clin 2001; 59: 693-700. [ Links ]
4. Eichinger S, Minar E, Bialonczyk C, Hirschi M, Quehenberger P, Schneoder B, et al. D-Dimer levels and risks of recurrent venous thromboembolism. JAMA 2003; 290: 1071-4. [ Links ]
5. Piquet P. Intérêt du dosage des D-Diméres dans le diagnostic de la maladie veineus etheomboembolique (point de vue du biologiste). Réunion de I'APRAMEN. Disponible en www.vulgares-medical.com/forum/s319-dimere.html Fecha de acceso: 25 de marzo de 2006 [ Links ]
6. Denis I, Szymanowicz A, Fabre X, Neyron M-J. Etude du dosage plasmatique des D-Dimères sur Cobas Integra 800 dans le diagnostic d'exclusion des maladies veineuses trhomboemboliques. J d'information Biomédicale 2005; 72 : 430-3. [ Links ]
7. Mansencal N, Dubourg 0. Actualités et aspects évolutifs dans la maladie veineuse trhomboembolique. AMC pratique 2005; 140. [ Links ]
8. Wells P, Anderson D, Rodger M, Forgie M, Kearon C. Dreyer J, et al. Evaluation of D-dimer in the diagnosis of suspected deep-vein thrombosis: randomised controlled trial. N Engl J Med 2003; 349: 1227-35. [ Links ]
9. Laboratoire Mérieux. Les D-dimères: utilisation dans l'exclusion de la TVP/EP en pratique clinique (intérêts, actualités), Journée Formation Continue, Avril 2005. [ Links ]
10. Biologie: la phase pré-analytique. DRASS75. [ Links ]
11. Stein PD, Hull RD, Patel KC. Dimer for the exclusion of acute venous thrombosis and pulmonary embolism. Ann Intern Med 2004; 140: 589-602. [ Links ]














