Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957
Acta bioquím. clín. latinoam. vol.44 no.4 La Plata oct./dic. 2010
BIOQUÍMICA CLÍNICA
Estudio clínico de marcadores de hipermetilación indólica en las alteraciones de la percepción
Clinical studies of markers of the indolic hypermethylation in human perception alterations
Arturo Alberto Vitale1 a *, Jorge Ciprian-Ollivier2 b, Martín Gustavo Vitale3 c, Esther Romero4 d, Alicia Beatriz Pomilio5 a *
1. Doctor en Química, Investigador Independiente de CONICET
2. Médico especialista en Psiquiatría, Director del Centro de Psiquiatría Biológica, Universidad de Buenos Aires.
3. Bachiller en Ciencias; Estudiante de Medicina, Facultad de Ciencias Médicas, Universidad de Buenos Aires.
4. Licenciada en Psicología, Especialista en Psicología Cognitiva.
5. Doctora de la Universidad de Buenos Aires, Investigadora Superior de CONICET. Directora del Área de Bioquímica Estructural y Espectroscopía RMN de PRALIB (UBA y CONICET).
a. PRALIB (UBA y CONICET), Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires (UBA), Junín 956, C1113AAD Ciudad Autónoma de Buenos Aires. e-mails: avitale@ffyb.uba.ar; pomilio@ffyb.uba.ar.
b. Centro de Psiquiatría Biológica de Buenos Aires, Universidad de Buenos Aires, Argentina. prcoetal@fibertel.com.ar.
c. INIFTA (CONICET, UNLP), Facultad de Ciencias Exactas, Universidad Nacional de La Plata, B2900 La Plata, Argentina. mgvitale@gmail.com; vitale@inifta.unlp.edu.ar.
d. Psicología Cognitiva, Facultad de Psicología, Universidad Nacional de La Plata.
* Miembros de la Carrera de Investigador Científico de CONICET (Argentina).
Todos los autores contribuyeron de igual manera a este trabajo interdisciplinario.
Resumen
Se estudiaron los marcadores bioquímicos en 34 pacientes psicóticos frente a controles, efectuándose: dosaje de monoaminooxidasa (MAO) plaquetaria y aminooxidasa (AO) sérica, actividad transmetilante y dosaje de N,N-dimetilindolalquilaminas urinarias: bufotenina y N,N-dimetiltriptamina (DMT). Se realizaron simultáneamente tests neuropsicológicos para evaluar los parámetros psicométricos en los mismos sujetos de estudio. Los niveles urinarios de DMT y bufotenina fueron evaluados por cromatografía de gases-espectrometría de masas y por cromatografía líquida de alta resolución. Las enzimas fueron dosadas por métodos espectrofluorimétricos. Se establecieron relaciones entre los valores estadísticamente significativos de bufotenina urinaria y MAO plaquetaria, de DMT urinaria con MAO plaquetaria y con AO sérica. Los valores estadísticamente significativos de MAO plaquetaria y los de actividad de transmetilación fueron satisfactoriamente correlacionados lográndose así categorizar el 91,1% de los 34 sujetos participantes en cuatro tipos principales. La marcada disminución de MAO plaquetaria mostró concordancia con el aumento de bufotenina y DMT, y con la alteración perceptual observada en los tests neuropsicológicos. La disminución de AO sérica fue moderada, pero acorde con la actividad transmetilante registrada. Los resultados apoyan la teoría de transmetilación patológica de la esquizofrenia y muestran que estas indolalquilaminas metiladas son marcadores de estado para estas patologías.
Palabras clave: Esquizofrenia; Transmetilación; Monoaminooxidasa plaquetaria; Aminooxidasa sérica; Indolalquilaminas metiladas; N,N-dimetiltriptamina y bufotenina urinarias
Summary
Biochemical markers were studied in 34 psychotic patients compared to controls, e.g., dosage of platelet monoamine oxidase (MAO) and serum amine oxidase (AO), transmethylation activity, and dosage of the urinary N,N-dimethylindolealkylamines, bufotenine and N,N-dimethyltryptamine (DMT). Neuropsychological tests were simultaneously performed to evaluate psychometric parameters in the same subjects under study. Urinary levels of DMT and bufotenine were evaluated by gas chromatography-mass spectrometry and high-performance liquid chromatography. The enzymes were dosed by spectrofluorimetric methods. Relationships were established between the statistically significant values of urinary bufotenine and platelet MAO, and of urinary DMT and both platelet MAO and serum AO. The statistically significant values of platelet MAO and those of transmethylation activity were satisfactorily correlated, thus achieving the 91.1% categorization of the 34 subjects in four main types. The sharp decrease in platelet MAO was in agreement with the increase in bufotenine and DMT, and with the perceptual alteration observed in neuropsychological tests. The decrease in serum AO was moderate, but consistent with the transmethylating activity registered. The results support the pathologic transmethylation theory of schizophrenia, and show that these N,N-methylated indolealkylamines are state markers for these pathologies.
Key words: Schizophrenia; Transmethylation; Platelet monoamine oxidase; Serum amine oxidase; Schizophrenia; Methylindolealkylamines; Urinary N,N-dimethyltryptamine and bufotenin
Introducción
La esquizofrenia es un grupo de enfermedades heterogéneas de diferente etiología, con distintas manifestaciones sintomáticas, de evolución dispar y de pronóstico complejo, por lo que resulta más correcto hablar de "esquizofrenias". No obstante, se usa el término en singular de manera genérica. Por ello, DSM IV-TR (1) ha englobado patologías bien distintas bajo los apartados esquizofrenia, trastornos esquizoafectivos y reacción psicótica breve. En el mismo concepto se incluyen enfermedades tan distintas como las verdaderas esquizofrenias procesales, las psicosis marginales y las esquizofrenias sistemáticas. Resulta por lo tanto necesario realizar la diferenciación clara entre estas entidades (2).
Se considera entonces que la esquizofrenia es un conjunto de enfermedades del neurodesarrollo de origen multifactorial. Muchos mecanismos pueden interactuar para producir las manifestaciones psicóticas, como por ejemplo bases genéticas, enfermedades virales, disfunciones inmunológicas, complicaciones obstétricas o determinantes ambientales que produzcan factores de estrés temprano. Cada paciente y cada cuadro nosológico se diferencian por la variabilidad de síntomas (positivo, negativo, afectivo, cognitivo) que si bien son interdependientes, aparecen en distintos momentos de la enfermedad, en distintas formas clínicas, no responden del mismo modo al tratamiento e impactan en mayor o menor medida en la disfunción psico-social y de inter-relación de la enfermedad.
Desde hace muchos años se ha demostrado en los enfermos esquizofrénicos la existencia de alteraciones de neurotransmisores y péptidos, destacándose la alteración del sistema dopaminérgico (DA), hecho que surgió de la comprobación de que la mayoría de las drogas antipsicóticas son bloqueantes de los receptores dopaminérgicos centrales y que algunos agonistas, como la anfetamina, producen estados psicóticos paranoides.
Las teorías más recientes, de carácter complementario a las existentes, se basan en una disfunción glutamatérgica. Las primeras teorías sobre la hipoactividad glutamatérgica en esquizofrenia surgen de la observación de los estados psicóticos inducidos por fenilciclidina, que actúa por antagonismo NMDA. La hipoactividad glutamatérgica produce aumento de la actividad DA y disminución de la actividad gabaérgica.
Otras hipótesis postulan una disminución de la actividad de la colecistoquinina B, neuropéptido que co-localiza con vesículas de DA y que actúa como antagonista endógeno. También se han planteado alteraciones de la neurotensina en esquizofrenia.
Otras teorías que resurgieron con el advenimiento de los antipsicóticos de segunda generación, involucran a receptores serotoninérgicos, contemplando una alteración cuantitativa a nivel del receptor y otra cualitativa con la producción de compuestos metilados derivados de la serotonina (5-HT) (hipermetilación o hipodesmetilación).
La hipótesis de la transmetilación fue la primera hipótesis específica de la etiología bioquímica de la esquizofrenia. Fue explorada extensamente por Osmond y Smythies (3), Friedhoff y Van Winkle (4), Stam et al. (5), Fischer (6), Fischer y Spatz (7), Fischer et al. (8), Saavedra y Axelrod (9), Smythies (10) y Ciprian Ollivier et al. (11) (12), entre otros. Esta teoría se basa en la observación que las drogas alucinógenas como: mescalina, psilocibina y la dietilamida del ácido lisérgico (LSD) son químicamente parecidas a algunos neurotransmisores (13). Según esta hipótesis, un error congénito del metabolismo podría causar algunos casos de esquizofrenia debido a la producción y acumulación por trastornos enzimáticos (14) de indolalquilaminas metiladas, como bufotenina (5-hidroxi-N,N-dimetiltriptamina), 5-metoxi-N,N-dimetiltriptamina y N,N-dimetiltriptamina (DMT) (4) (8) (11). La mayoría de estos compuestos han demostrado ser alucinógenos potentes en sujetos sanos.
No obstante ser sustratos de la monoaminooxidasa (MAO), las indolalquilaminas metiladas se han detectado en muestras de orina de pacientes psiquiátricos, no sólo de esquizofrénicos, a pesar de su alto turn-over (9) (15) ya que treinta minutos después de administrar por vía endovenosa una dosis alta única, se puede recuperar sólo el 1% en muestras de sangre y/o de orina (16).
Este grupo de investigación ha informado previamente (11) (12) (17) (18) acerca de la relación de estos compuestos con alteraciones de la percepción, no sólo verdaderas alucinaciones, sino alteraciones perceptuales más sutiles que se observan en varias entidades. Por lo tanto, las indolalquilaminas metiladas, más que ser un rasgo para cualquier categoría de diagnóstico, pueden desempeñar el papel de "marcadores de estado" de psicosis clínicas o subclínicas. Su acumulación en pacientes podría ser debida a una aceleración de la cinética de su producción o bien, y más probablemente, a una disminución en la cinética de la enzima (MAO) responsable de la degradación de las indolalquilaminas metiladas (19). Con frecuencia se ha informado una disminución de la actividad de MAO en la esquizofrenia, estando por lo tanto de acuerdo con esta teoría (20). Esto permite la acumulación de indolalquilaminas, cruzando la barrera hematoencefálica (BHE) y actuando en el sistema nervioso central (SNC).
Dos aspectos de la hipótesis de la transmetilación patológica ameritan una discusión adicional. El primer aspecto se refiere a la relevancia de las alteraciones de la percepción en la fisiopatología de la psicosis (21). Una percepción distorsionada de la realidad no sólo causa los llamados síntomas positivos sino también puede contribuir al deterioro progresivo del paciente y a los denominados síntomas negativos (22). El segundo aspecto de la teoría tiene implicancias biológicas y farmacológicas. Desde hace unos años, se ha despertado un considerable interés en los antipsicóticos atípicos (23), no sólo porque actúan sobre los síntomas positivos y negativos, sino también porque tienen efectos potentes sobre los receptores serotoninérgicos. Así, clozapina, olanzapina, risperidona y ritanserina (24) muestran un mecanismo de acción, que también implica la capacidad de interactuar con varios receptores 5-HT (25), siendo los 5-HT2 los más importantes. Es decir que, como se postulara en la hipótesis de la transmetilación, los derivados del indol podrían desempeñar un papel importante en la fisiopatología de la esquizofrenia.
Esta teoría (ahora hipótesis) está apoyada por el hecho bien establecido que la mayoría de las drogas alucinógenas actúan vía los receptores serotoninérgicos (26). De hecho, DMT interactúa también con los receptores serotoninérgicos, pudiéndose hipotetizar que parte del efecto de los nuevos antipsicóticos puede estar relacionado con el bloqueo de la actividad de DMT en estos receptores.
A la luz de las investigaciones anteriores de este grupo (11) (12) (17) (18) (27-32), en las que la presencia de DMT en Ayahuasca, en consumidores de la misma y en las muestras de orina de pacientes esquizofrénicos confirma que los efectos biológicos y cognitivos registrados son producidos por estas indolalquilaminas metiladas, y las investigaciones de diversos autores sobre detección e identificacion de indolalquilaminas metiladas en fluidos biológicos, se llevó a cabo en este trabajo una investigación integral e interdisciplinaria. Este conjunto de experiencias tuvo como objetivo explorar la posibilidad de excreción de indolalquilaminas metiladas en 34 casos y 20 controles, eligiendo bufotenina y DMT en orina, y en el mismo grupo de análisis dosar la enzima AO sérica y en particular la MAO plaquetaria como marcador de MAO cerebral. Asimismo, se analizó la actividad de transmetilación y se efectuaron simultáneamente ensayos neuropsicológicos en los mismos sujetos de estudio. De esta manera, los resultados incluyen la formación de los compuestos N-metilados, los productos de ese metabolismo y la actividad de las enzimas que los degradan con el fin de evaluar su capacidad para modular los receptores serotoninérgicos, y así determinar en qué medida se afectan los procesos perceptuales y cognitivos, así como los parámetros neuroendocrinos.
Materiales y Métodos
PERFIL DE LOS PACIENTES
Se estudiaron 34 pacientes (11 mujeres y 23 hombres), blancos, no emparentados, no medicamentados, de 16 a 44 años de edad (promedio: 26,5), diagnosticados por especialistas, de acuerdo al DSM IV-TR (1).
Criterios de exclusión: abuso o dependencia pasada o actual de alcohol u otras sustancias dentro de los 3 meses, anomalías clínicamente significativas en el electrocardiograma o en análisis de laboratorio, incluyendo análisis de orina positivo para drogas ilícitas.
El grupo control consistió en 20 controles sanos de 41,8 ± 12,2 años de edad, sin antecedentes personales o familiares de psicopatología, sin desórdenes neurodegenerativos ni psiquiátricos y sin tratamiento médico.
Todos los participantes respondieron las preguntas formuladas en los cuestionarios sobre su historial médico, hábitos de bebida y tabaquismo. Todos dieron su consentimiento por escrito para participar en el estudio y dar muestras de sangre y orina.
Los procedimientos utilizados fueron aprobados por el Comité de Ética del Centro de Psiquiatría Biológica y las autoridades de la Facultad de Farmacia y Bioquímica (Universidad de Buenos Aires).
Los pacientes fumaban en promedio unos 40 cigarrillos (rango 24-56) por día, mientras que los sujetos controles sanos fumaban un promedio de 20 cigarrillos (rango 2-60) por día.
ENSAYOS NEUROPSICOLÓGICOS
Se realizó una evaluación neuropsicológica sólo para controlar y analizar los procesos de memoria y la coordinación visuo-espacial. Los tests utilizados fueron: Wais- R Digit Symbol Test (Wais-R DST) [Escala Revisada de Inteligencia de Wechsler para Adultos (Escala de Performance): Wechsler Adult Intelligent Scale-revised], Complex- Figure (Ray-Osterrieth) y Buschke Selective Reminding Task (Test de Recuerdo Selectivo de Buschke-Memoria).
ANÁLISIS BIOQUÍMICOS
Consistieron en la determinación de los niveles de bufotenina (5-hidroxi-N,N-dimetiltriptamina = N,N-dimetilserotonina) y N,N-dimetiltriptamina (DMT) en orina. Se determinaron monoaminooxidasa en plaquetas (MAO plaquetaria), aminooxidasa en suero (AO sérica) y la actividad N-metilante o de transmetilación.
DETERMINACIÓN DE LA ACTIVIDAD N-METILANTE
Se utilizó nicotinamida (niacinamida) como sustrato pues se transforma en un solo subproducto N-metilado: N1-metilnicotinamida, según Buscaino et al. (14) y aplicada por el grupo de Spatz (33).
Se agregaron 5,0 μL de una solución acuosa de nicotinamida (Sigma-Aldrich, St. Louis, EE.UU.) 0,4 M y de S-adenosilmetionina (SAM) 0,3 M preparada en biotina 3,2 mM a 0,5 mL de sangre con EDTA (sal disódica), como anticoagulante. Una primera muestra (tiempo 0) fue desproteinizada de inmediato. Las restantes se incubaron a 37 °C con agitación, de las cuales se extrajeron alícuotas cada 10 min, luego de los 30 min hasta completar los 90 min. A cada muestra se agregaron 3,5 mL de agua bidestilada y 1,0 mL del reactivo precipitante (ácido fosfotúngstico) para la separación de las lipoproteínas de alta densidad (HDL) (Wiener Lab, Rosario, Argentina). Las muestras se analizaron inmediatamente, o bien se guardaron a -20 °C hasta su análisis. Al realizar el análisis, las muestras a temperatura ambiente fueron centrifugadas durante 20 min a alta velocidad. Finalmente, 1 mL de cada sobrenadante fue analizado junto con una serie de estándares por espectrofotofluorometría mediante la técnica modificada de Pelletier y Campbell (34) que se basa en la formación de un producto fluorescente de condensación entre la N-metilnicotinamida y cetonas. Establecido el valor basal de N-metilnicotinamida se calculó su porcentaje máximo de incremento a lo largo del tiempo frente al tubo de lectura más alta.
EVALUACIÓN DE MAO PLAQUETARIA
Se extrajo sangre (4 mL) de la vena cubical en una jeringa descartable de plástico de 1 mL con citrato dextrosa fosfato (CDP) como anticoagulante (citrato de sodio 7,5 g, ácido cítrico 0,5 g, dextrosa 2,5 g y fosfato de sodio dibásico 0,5 g en agua destilada csp 100 mL). El plasma rico en plaquetas (PRP) se obtuvo por centrifugación (935 × g) durante 70 s a temperatura ambiente. Las plaquetas sedimentaron mediante centrifugación adicional de PRP a 10.000 x g durante 5 min. El precipitado de plaquetas fue lavado con solución fisiológica y centrifugado nuevamente.
Las plaquetas fueron destruidas por sonicación (20 kHz, amplitud de 8 × 10-3mm durante 30 s). La actividad de la MAO-B plaquetaria fue determinada mediante el método espectrofluorimétrico, utilizando kinuramina [3-amino-1-(2-aminofenil)propan-1-ona] como sustrato, mediante el método de Krajl (35), modificado por Pivac et al. (36). Las muestras del estándar, blanco (agua) y los sonicados de plaquetas (100 μL) se analizaron por duplicado en buffer fosfato (0,5 M; pH 7,4) y se incubaron durante 60 min a 37 °C con kinuramina. La reacción se detuvo mediante el agregado de NaOH 1N enfriado con hielo. La medición de la fluorescencia de 4-hidroxiquinolina (4-HOQ), un producto de kinuramina, se realizó en un espectrofluorímetro (Varian Cary Eclipse, Waldnut Creek, California, EE.UU.) con una longitud de onda de excitación de 310 nm y longitud de onda de emisión de 380 nm.
EVALUACIÓN DE AO SÉRICA
La sangre se recogió por punción venosa y se dejó coagular a temperatura ambiente. Se centrifugó durante aproximadamente 5 min a 3000 rpm para separar el suero, que se usó para los análisis.
Para la determinación de AO sérica se usó el método microfluorométrico de Krajl (35) modificado, con kinuramina como sustrato (37), en forma análoga al procedimiento descripto.
Análisis químico de las muestras de orina
Se usaron como patrones DMT y bufotenina sintetizados en estos laboratorios (38). Las muestras fueron examinadas por cromatografía en capa delgada (CCD; thin-layer chromatography: TLC) en placas de vidrio recubiertas con silicagel GF254 (Merck, Darmstadt, Alemania) y cromatografía en capa delgada de alta resolución (CCD-AR; high-performance thin-layer chromatography: HPTLC) de silicagel (Merck, Darmstadt, Alemania). Las manchas se visualizaron con el reactivo de Dragendorff.
Análisis de bufotenina y DMT en orina
Se analizaron DMT y bufotenina en las muestras de orina de pacientes y controles. Se procedió a la recolección de orina de 24 horas, incluyendo la primera de la mañana. Cada muestra fue filtrada por una membrana de poro 0,22 μm (Millipore, Billerica, Massachusetts, EE.UU.). Se agregaron 32 μL de HCl 5N a 3,2 mL de orina con los estándares adecuados según el método de análisis a utilizar como se describiera anteriormente (39-41) y se sembraron en una columna de extracción en fase sólida (solid phase extraction: SPE) Oasis (Waters Corporation, Milford, Massachusetts, EE.UU.) neutra.Se lavó la columna con 2,0 mL de buffer carbonato 0,15 M (pH 9,3) y a continuación, con 2,0 mL de agua desionizada. Se agregaron 4,0 mL de n-hexano. La elución se realizó con 3 mL de 2-propanol/cloruro de metileno (75:25). Se realizó la evaporación del eluyente bajo nitrógeno, dejando una mínima cantidad para el análisis posterior por CG-EM y también por HPLC.
Técnica de cromatografía de gases-espectrometría de masas (CG-EM)
Se usó un equipo VG-2 TRIO-2 Mass Lab (VG Mass- Lab, Cheshire, Inglaterra) con helio como gas portador para el análisis de CG-EM. Divisor: 100:1. Presión en la columna: 10 psi. Los datos fueron procesados mediante el sistema Lab Base GC-MS Data System (VG MassLab, Cheshire, Inglaterra). El barrido de masas se realizó en el rango de 30-500 por cada pico de la muestra en estudio. Se usó una columna capilar de sílice fundida SPB-1 (Sigma-Aldrich, St. Louis, EE.UU.), de 30 m de longitud x 0,20 mm de d.i., con el programa siguiente de temperatura del horno: 60 °C durante 1 min, 60-290 ºC (rampa: 10 oC/min) y 5 min a 290 oC.
TÉCNICA DE CROMATOGRAFÍA LÍQUIDA DE ALTA RESOLUCIÓN (HPLC)
Bufotenina y DMT se determinaron por HPLC. Los procedimientos detallados ya han sido ampliamente descriptos por este grupo (27) (28) (39-41) utilizando un cromatógrafo LKB (LKB, Bromma, Suecia) equipado con una bomba de distribución del solventes LKB Bromma 2249, un inyector Rheodyne y un detector fluorimétrico Chrompack (18 nm de ancho de rendija, constante de tiempo de 1,5 s) acoplado a un integrador LKB Bromma 2221 [columna: μBondapak C18 (Waters Corporation, Milford, Massachusetts, EE.UU.), 10 μm, 250 mm de longitud x 4,6 mm, d.i.]; 10 μL de volumen inyectado.
MÉTODOS ESTADÍSTICOS
La evaluación estadística de los datos (expresados como valor medio ± desviación estándar) se hizo mediante el análisis de varianza de una vía (one-way analysis of variance: ANOVA), seguido por el test de comparación múltiple de Tukey. Se usó ANOVA de dos vías para probar la asociación entre la actividad de MAO-B plaquetaria y distintas variables, y para ensayar las interacciones entre ellos. La correlación entre parámetros se determinó mediante el coeficiente de correlación de Pearson. Los resultados fueron considerados significativos cuando p<0,01.
Resultados
ENSAYOS NEUROPSICOLÓGICOS
Se realizó una evaluación neuropsicológica de los 34 pacientes participantes frente a los sujetos controles con el fin de analizar los procesos de memoria y la coordinación visuo-espacial. Para ello, se utilizaron el test de Ray-Osterrieth, el test de Wais-R DST y el test de de Buschke (42).
El test de Ray-Osterrieth se usa comúnmente para evaluar la memoria visual inmediata y diferida. En este caso, se privilegió la evaluación de los aspectos de coordinación visual-perceptiva y visual-motora. Se requirió que el paciente fuera capaz de analizar la situación, de descubrir los métodos para resolverla, de sintetizar los detalles de una unidad coherente. En este test los pacientes mostraron, en comparación con los controles, alteraciones de la capacidad perceptiva y de análisis, así como de la capacidad organizadora del espacio. Es decir que, los procesos visuo-perceptuales se vieron afectados significativamente.
La capacidad de atención sostenida fue evaluada mediante el ensayo Wais-R DST, mientras que la memoria verbal explícita fue evaluada por el ensayo de Buschke (43). En este ensayo cada sujeto tuvo que elaborar una estrategia para evocar lo aprendido, lo cual está relacionado con la memoria de trabajo (44). Se observó que el comportamiento promedio de los sujetos que participaron en esta experiencia fue algo menor en el momento de repetir el ensayo comparativo que en la evaluación previa. Los defectos de copia encontrados en esta segunda evaluación fueron los siguientes: a) Tendencia a la macro-reproducción. b) Omisión de algunos detalles internos. c) Defecto de programación y falta de control de acción.
Se destacan los siguientes resultados: En el ensayo de atención sostenida, o ensayo de Wais-R DST, se observó que los pacientes participantes presentaron una disminución significativa con respecto a los controles, indicando interferencia con la atención sostenida. El comportamiento fue ligeramente inferior en la repetición del test, en general, debido a un retraso psicomotor y dificultades para ser sostenido en una tarea continua.
El test de Buschke permitió evaluar diferentes aspectos del aprendizaje y la memoria. En particular, los sujetos mostraron una disminución en CLTR (Consistent Long Term Retrieval, o sea: recuperación consistente a largo plazo), pero no cambios significativos en LTS (Long Term Storage, o sea: almacenamiento a largo plazo), LTR (Long Term Retrieval, o sea: recuperación a largo plazo de lo almacenado) y TR (Total Recall: Recuerdo total). En el ensayo de memoria los puntajes más bajos fueron los de coherencia y consolidación de lo recordado a lo largo de las pruebas. Este déficit sugiere una ligera disminución en la función de la memoria de tarea en relación con el sistema de ejecución, a los que sustentan las estructuras prefrontales.
Los cambios de corta duración en percepción, cognición y otras funciones psicológicas se analizaron en los 34 sujetos psicóticos. Los resultados están de acuerdo con los obtenidos anteriormente por este grupo de investigación (18) (27) (28).
En resumen, se observaron efectos fuertes sobre la construcción visuo-espacial.
Al analizar las muestras de orina por CG-EM, se pudo categorizar a los sujetos participantes en cuatro grupos de acuerdo a la respuesta de DMT. Por lo tanto, la presencia de DMT en la orina (tR promedio: 15,73 min) de los pacientes participantes se correlacionó significativamente con las alteraciones perceptivas observadas.
ANÁLISIS BIOQUÍMICOS
Se determinaron los niveles de bufotenina (5-hidroxi-N,N-dimetiltriptamina = N,N-dimetilserotonina) y N,N-dimetiltriptamina (DMT) en orina, así como la actividad de monoaminooxidasa [EC 1.4.3.4] en plaquetas (MAO plaquetaria), aminooxidasa en suero [EC 1.4.3.6] (AO sérica) y la actividad de transmetilación.
En este trabajo se analizaron 34 casos. El perfil de los pacientes y el histograma de la edad de los pacientes se muestran en la Fig. 1, mientras que el gráfico estadístico del género de los pacientes en la Fig. 2.

Figura 1: Perfil de los pacientes. Histograma de la edad de los pacientes.

Figura 2: Representación estadística del género de los pacientes.
DETERMINACIÓN DE MAO PLAQUETARIA Y DE AO SÉRICA
En este tipo de estudios resultó importante determinar la actividad de la enzima MAO en plaquetas y de AO en suero.
Como MAO-B se expresa sólo, o predominantemente, en las plaquetas y linfocitos periféricos (45), la evaluación de MAO plaquetaria, corresponde en realidad a dosar MAO-B en plaquetas, las cuales constituyen un modelo periférico de los sinaptosomas centrales serotoninérgicos (5-HT), ya que comparten procesos bioquímicos similares con las neuronas 5-HT (46). Por lo tanto, la actividad de MAO plaquetaria es un índice de la actividad serotoninérgica cerebral.
En el presente trabajo se dosó MAO plaquetaria en los 34 pacientes frente a los controles, mediante el método espectrofluorimétrico utilizando kinuramina como sustrato. Se utilizó primeramente citrato dextrosa fosfato (CDP) que es considerado un anticoagulante ideal porque preserva las células sanguíneas y los factores de coagulación por mayor tiempo, permitiendo así obtener las plaquetas intactas en el primer paso de la técnica, ya que al mezclar CDP con la sangre se obtuvo un pH de 7,46 que es muy cercano al pH fisiológico y además contiene glucosa (47).
Dado que el tabaquismo disminuye la actividad de MAO-B plaquetaria (48), se registraron qué sujetos eran fumadores y cuántos cigarrillos fumaban por día. En este estudio, todos los pacientes y los controles eran fumadores, pero los pacientes fumaban el doble en promedio, que los sujetos control. También se registró el número de cigarrillos fumados diariamente, pero la actividad de MAO-B plaquetaria no se vio afectada por el número de cigarrillos fumados por día y no se encontró correlación entre la actividad de MAO-B plaquetaria y el número de cigarrillos diarios, en concordancia con resultados anteriores (49).
Dado que la actividad de MAO-B plaquetaria se encuentra bajo la influencia del género (48) (50), edad (51), etnia o raza (52), tabaquismo, alcoholismo (53), enfermedades neurodegenerativas, sustancias psicotrópicas, medicamentos (54) y el tratamiento con litio o haloperidol, para controlar estos efectos se incluyeron sólo sujetos de raza blanca, libres de medicamentos, de edad no avanzada y no alcohólicos. En cuanto al alcoholismo, otros autores (53) estudiaron su influencia sobre MAO-B plaquetaria, demostrando que el tabaquismo y no el alcoholismo, reducía la actividad de MAO-B en sujetos alcohólicos.
Los valores normales de MAO plaquetaria obtenidos en el presente estudio correspondieron en promedio a: 13,5 ± 3,3 nmoles/mL/h/109 plaquetas para hombres; 14,7 ± 4,8 nmoles/mL/h/109 plaquetas para mujeres, comparables con los descriptos en la literatura (55).
Si se observan los valores estadísticamente significativos (p < 0,01) de MAO plaquetaria se encuentra que: el 17,6% están dentro del rango normal (hombres: 10,2- 16,8 nmoles/mL/h; mujeres: 9,9-19,5 nmoles/mL/h), 8,9% por encima y 73,5% por debajo de los valores normales (Fig. 3).

Figura 3: Representación estadística de los niveles de MAO plaquetaria
Se observa que en los pacientes el porcentaje significativamente mayor: 73,5% (p < 0,01) corresponde a un marcado descenso en MAO plaquetaria (MAO-B) (Fig. 3), lo cual está de acuerdo con observaciones previas de disminución en algunos desórdenes mentales y neurodegenerativos, esquizofrenia, enfermedad de Alzheimer, enfermedad de Parkinson, corea de Huntington (54), trastorno obsesivo compulsivo y obsesiones agresivas (56). En cambio, se registraron aumentos de MAO plaquetaria en pacientes depresivos (57).
En el presente trabajo se ha determinado también AO sérica que corresponde a un conjunto de aminooxidasas solubles, sin FAD, sensibles a semicarbazida con una alta afinidad por bencilamina: SSAO [EC 1.4.3.6; amina: oxido-reductasa de oxígeno (desaminante) que contiene cobre] por eso se la ha denominado, con frecuencia, bencilamino-oxidasa (BAO) (58), que se encuentran en muchos tejidos y órganos de humanos (59).
SSAO se encuentra en una forma soluble que circula en el plasma sanguíneo: SSAO circulante (AO circulante o plasmática), que puede metabolizar las aminas extracelulares, y en una forma unida a membrana: SSAO tisular, que está presente en los tejidos. Ambas formas comparten similitudes bioquímicas y catalizan la misma reacción general de desaminación oxidativa de aminas primarias alifáticas, de cadena larga y corta, para dar los correspondientes aldehídos, amoníaco y peróxido de hidrógeno.
Hasta hace varios años estas aminooxidasas solubles (SSAO) se mencionaban como MAO plasmática o MAO sérica, o bencilaminoxidasa, pero para evitar confusiones varios autores la indican como SSAO sérica o bien, AO sérica, como se hace en este trabajo.
Así, en este trabajo se dosó AO sérica (SSAO), que actúa extracelularmente, para determinar su posible rol dentro de las características de los trastornos psiquiátricos bajo estudio. Los valores normales de AO sérica obtenidos en el presente estudio correspondieron en promedio a: 16,4 ± 3,8 nmoles/mL/h para hombres y 17,5 ± 4,1 nmoles/mL/h para mujeres.
Debido a que se ha observado que la actividad de AO sérica (SSAO circulante) es estable en adultos sanos (59) y que no existen diferencias por género, ni por la posición del cuerpo (de pie, sentado, recostado, en cuclillas), ni por la hora del día de toma de muestras de sangre (60) (61), no fue necesario controlar estas condiciones.
En el presente trabajo, se determinaron los valores estadísticamente significativos (p< 0,01) de AO sérica en los 34 pacientes frente a controles (Fig. 4), observándose que el 23,5% se encontraba dentro del rango normal (hombres: 16,4 nmoles/h; mujeres: 13,4-21,6 nmoles/h), 32,4% por encima y 44,1% por debajo de los valores normales.

Figura 4: Representación gráfica de la estadística de los niveles de AO sérica.
Ninguno de estos porcentajes parece destacarse marcadamente sobre el resto, excepto en el caso del porcentaje inferior a los valores normales que corresponde a casi el doble de los datos normales (44,1% vs. 23,5%).
De acuerdo con los resultados obtenidos en el presente trabajo, en estos 34 casos, el porcentaje significativamente más destacado (p < 0,01) de los niveles de aminooxidasas está por debajo del valor normal. Esta hipoactividad de las aminooxidasas es más intensa en la MAO plaquetaria (MAO-B) (73,5%) que en la AO sérica (44,1%).
Teniendo en cuenta la hipótesis de las monoaminas con respecto a la fisiopatología de la esquizofrenia y otros trastornos relacionados, al evaluar en este trabajo la actividad de SSAO sérica en los 34 pacientes frente a los controles, se puso de manifiesto la existencia de una cinética de MAO disminuida en un porcentaje de los pacientes, conduciendo, por lo tanto, a la no-destrucción y acumulación de las indolalquilaminas metiladas, como por ejemplo: DMT, en estos pacientes. Esto está en concordancia con lo indicado por varios autores respecto a la esquizofrenia (20) (52) (62) (63).
Las diferencias en la actividad de las aminoxidasas encontradas en los distintos trastornos mentales, incluyendo MAO en esquizofrenia, pueden también observarse en SSAO y se puede buscar una correlación entre ambas.
DETERMINACIÓN DE LA ACTIVIDAD TRANSMETILANTE
Triptamina y serotonina son dos indolalquilaminas que, en presencia de dadores de grupos metilo se pueden transformar en compuestos mono- y dimetilados, es decir N-metiltriptamina, N,N-dimetiltriptamina, N-metilserotonina, N,N-dimetilserotonina, O-metilserotonina, O-metil- N-metilserotonina y O-metil-N,N-dimetilserotonina, con la presencia de algunos de estos compuestos metilados o bien todos, según las condiciones experimentales. Por lo tanto, para un dosaje de estas indolalquilaminas resulta difícil controlar el grado de metilación alcanzado. Es por eso que para un análisis cuantitativo reproducible y confiable se eligió utilizar como sustrato a la nicotinamida ya utilizada por Buscaino et al. (14), y aplicada por el grupo de Spatz (33), pues se obtiene un solo producto de metilación: N1-metilnicotinamida. La actividad N-metilante es considerada normal cuando su valor no supera el 10% de incremento, sospechosa cuando el valor hallado se encuentra entre un 10,1 y 15% y anormal cuando la actividad supera el 15,1%.
La representación de los valores estadísticamente significativos de la actividad de transmetilación se muestra en la Fig. 5. Se puede observar que 5,9% de los casos presentan actividad metilante normal, 38,2% actividad border (pacientes con trastorno fronterizo esquizo- afectivo) y 55,9% anormal, mostrando así en estos 34 casos un 94,1% de actividad de transmetilación superior a la normal. La transmetilación implica la producción de compuestos indólicos N,N-dimetilados de la ruta serotoninérgica, por ejemplo: bufotenina y DMT, debido a un error metabólico, por actuar la enzima amina-N-metiltransferasa (nombre sistemático: S-adenosil- L-metionina:amina-N-metiltransferasa; sinónimo: triptamina- N-metiltransferasa) [EC 2.1.1.49] que se encuentra en la sangre, en los pulmones y en el cerebro.

Figura 5: Representación gráfica de la estadística de la actividad de transmetilación.
RELACIÓN ENTRE MAO PLAQUETARIA Y ACTIVIDAD METILANTE
Categorización de los sujetos participantes
Se pudo categorizar el 91,1% de los 34 casos en cuatro tipos principales tomando en consideración los valores estadísticamente significativos de MAO plaquetaria y de actividad de transmetilación.
La correlación de los valores significativos de MAO plaquetaria y de actividad de transmetilación correspondió a: 11,7% del Tipo 1, 26,5% del Tipo 2, 44,1% del Tipo 3 y 8,8% del Tipo 4 (Fig. 6). El Tipo 1 se refiere a MAO plaquetaria por debajo de los valores normales y una actividad de transmetilación border. El Tipo 2 se refiere a valores normales de MAO plaquetaria y una actividad de transmetilación border. El Tipo 3 se refiere a MAO plaquetaria por debajo de los valores normales y una actividad de transmetilación anormal. El Tipo 4 se refiere a MAO plaquetaria por encima de los valores normales y una actividad de transmetilación anormal.

Figura 6: Tipologías: Valores de correlación de MAO plaquetaria y actividad de transmetilación.
Esta categorización estadísticamente significativa, basada en la actividad de la MAO-B plaquetaria, y de acuerdo con lo expresado respecto a la actividad de transmetilación, después de controlar el tabaquismo, puede ser utilizada como un marcador periférico del fenotipo específico, como fuera sugerido anteriormente (49) (64).
DOSAJE DE BUFOTENINA Y DMT URINARIAS
La excreción urinaria de bufotenina y DMT del tipo 3 (15 casos del total) se indican en la Fig. 7, siendo el tipo 3 el grupo principal de esta tipología. Hay un 33,3% de la excreción urinaria de bufotenina que está por encima del rango normal (1-8,9 μg/24 h), mientras que el 46,7% de la excreción urinaria de DMT está por debajo del rango normal (< 0,5 μg/24 h).
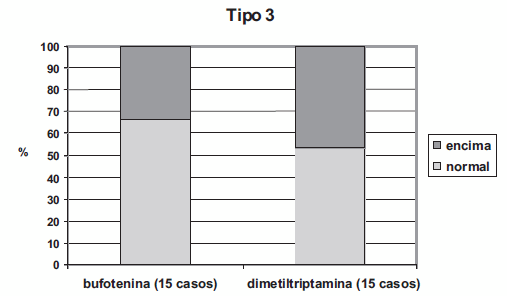
Figura 7: Excrecion de bufotenina y DMT en pacientes del tipo 3.
En 15 casos correspondientes al Tipo 3, el 33,3% excreta bufotenina en cantidades superiores a los valores normales, y el 46,7% excreta DMT en cantidades superiores a los valores normales. En resumen, bufotenina y DMT se excretaron en la orina de los pacientes del tipo 3, observándose que DMT se excretaba en un porcentaje mayor en comparación con bufotenina.
A modo de ejemplo se muestra un cromatograma de orina de un paciente psicótico con presencia de DMT (tR 15,53 min) (Fig. 8).

Figura 8: Cromatograma de orina de un paciente psicótico con pico con un tiempo de retención (tR) de 15,53 min correspondiente a excreción de DMT.
RELACIÓN DE BUFOTENINA URINARIA Y MAO PLAQUETARIA
Si se considera la excreción urinaria de bufotenina con respecto a los pacientes con actividad de MAO plaquetaria inferior a la normal (25 casos), sólo el 36% de los casos excreta bufotenina por encima del rango normal. Para los que tienen actividad normal de MAO plaquetaria (6 casos), sólo el 17% excreta bufotenina en cantidades superiores a la normal. Para aquellos con actividad de MAO superior a la normal (3 casos), el 100% excreta cantidades normales de bufotenina (Fig. 9).

Figura 9: Excreción urinaria de bufotenina: A) MAO plaquetaria inferior a los niveles normales. B) MAO plaquetaria con valores normales. C) MAO plaquetaria superior a los niveles normales.
RELACIÓN DE DMT URINARIA Y MAO PLAQUETARIA
En los pacientes con actividad de MAO plaquetaria inferior a la normal (25 casos), sólo el 32% excreta DMT por encima del rango normal (<0,5 μg/24 h). En los que tienen actividad normal de MAO plaquetaria (6 casos), sólo el 33% excreta DMT en cantidad superior a la normal. En los que tienen actividad de MAO plaquetaria superior a la normal (3 casos), el 100% excreta cantidades normales de DMT (Fig. 10).

Figura 10: Excreción urinaria de DMT: A) MAO plaquetaria por debajo de los niveles normales. B) MAO plaquetaria con valores normales. C) MAO plaquetaria por encima de los valores normales.
RELACIÓN DE DMT URINARIA Y AO SÉRICA
En los pacientes con actividad de AO sérica inferior a la normal (15 casos), el 53% excreta DMT por encima del rango normal (<0,5 μg/24 h). En los que tienen actividad normal de AO sérica (8 casos), sólo el 25% excreta DMT en cantidad superior a la normal. En los que tienen actividad de AO sérica superior a la normal (11 casos), el 100% excreta cantidades normales de DMT (Fig. 11).

Figura 11: Excreción urinaria de DMT: A) AO sérica por debajo de los niveles normales. B) AO sérica con valores normales. C) AO sérica por encima de los valores normales.
En las Figuras 9, 10 y 11, se observa que el 100% de los pacientes con actividad de MAO plaquetaria superior a la normal, excretaron cantidades normales de DMT y bufotenina. Esto se debió a la desaminación oxidativa de ambas indolalquilaminas por la MAO. Cuando los niveles de MAO estuvieron por debajo de los valores normales, debido a una marcada hipoactividad de esta enzima en los pacientes, o incluso cuando los niveles de MAO fueron normales, se detectó un aumento de la excreción urinaria de DMT y de bufotenina (Figs. 9-11).
Discusión y Conclusiones
Este trabajo consistió en un análisis integral de marcadores bioquímicos, dosaje de enzimas como MAO plaquetaria y AO sérica, determinación de la actividad N-metilante o transmetilante y búsqueda de la presencia de indolalquilaminas metiladas, como DMT y bufotenina, y su dosaje urinario en las muestras de 34 pacientes psicóticos no medicados, a quienes además se les hizo tests neuropsicológicos.
ENSAYOS NEUROPSICOLÓGICOS
La esquizofrenia se podría definir como una anomalía en una función básica cognitiva que sería la consecuencia de una mala operación en la conectividad de las regiones corticales, el cerebelo y el tálamo, y esta alteración de la activación se observa en diversos ensayos cognitivos (65) y/o tests neuropsicológicos (66).
Bajo estas premisas, en este trabajo se utilizaron: el test de Ray-Osterrieth, el subtest de Wais-R DST y el test de Buschke (42). Las alteraciones de la capacidad perceptiva y de análisis, así como de la capacidad organizadora del espacio que presentaron los pacientes en el test de Ray-Osterrieth se debieron al hecho que la percepción lleva a un reconocimiento derivado de una información visual y, a continuación, tiene lugar un análisis y una organización mental de los datos percibidos hasta que se origina una estructura central. Si existe una alteración en la capacidad de elaboración del estímulo, se observa que éste se guarda como una imagen incoherente y vaga, y el sujeto falla en la reproducción correcta.
La capacidad de atención sostenida fue evaluada mediante el ensayo de Wais-R DST, mientras que la memoria verbal explícita fue evaluada por el test de Buschke. Este test de recuerdo verbal selectivo es uno de los procedimientos más utilizados en la evaluación de la memoria y el aprendizaje verbal. Se ha empleado para estudiar los problemas de memoria asociados a un gran número de enfermedades neurológicas y condiciones patológicas, tales como el daño cerebral traumático, enfermedad de Alzheimer, esclerosis múltiple, síndrome de Korsakoff, así como en niños con problemas de aprendizaje (43) (67).
La disminución de la activación frontal dorsolateral, el área motora suplementaria y el cíngulo anterior, corroboran la hipótesis de una disfunción frontal en la esquizofrenia (65). Como es sabido, el Cingulus girus está relacionado con la atención y las funciones de la emoción. Los pacientes participantes mostraron un déficit de la activación de este circuito, especialmente en aquellas situaciones en las que hay una mayor demanda de atención. Se han corroborado también alteraciones del flujo sanguíneo en pacientes esquizofrénicos durante la realización de los ensayos de memoria que estaban centrados en el circuito córtico-cerebelo-talámico-cortical (68). Estos resultados se repiten en los estudios realizados por otros autores y son independientes del tipo de ensayos cognitivos usados. El déficit en la conexión normal de este circuito sería responsable de la dificultad expresada en estos pacientes para la introducción, procesamiento, recuperación y explicitación de la información.
En los tests empleados se puso de manifiesto cómo se ven afectadas las funciones visuo-espaciales más que los procesos cognitivos per se, debido a la interferencia perceptual sutil en este tipo de pacientes.
DETERMINACIÓN DE MAO PLAQUETARIA Y DE AO SÉRICA
La enzima MAO [EC 1.4.3.4], como es sabido, cataliza la reacción de desaminación oxidativa de varios neurotransmisores, aminas biogénicas y xenobióticas, así como de aminas dietarias, a aldehídos y juega un papel importante en la regulación de sus niveles (69). Altos niveles de la isoforma MAO-B son expresados en astrocitos y neuronas serotoninérgicas (5-HT), mientras que la isoforma MAO-A está expresada en altos niveles en las neuronas catecolaminérgicas (45) (54).
En el cerebro, MAO-A tiene un papel crítico en la regulación de la disponibilidad de los neurotransmisores monoaminérgicos para el secuestro vesicular y en su subsiguiente inactivación extrasináptica después de la liberación, tanto para serotonina y norepinefrina vs. dopamina. La desaminación de estos neurotransmisores por MAO inactiva sus funciones fisiológicas y controla eficazmente sus niveles en el cerebro. La MAO hepática tiene un papel defensivo crucial en la desactivación de las monoaminas circulantes o aquellas que, como la tiramina, se originan en el intestino y son absorbidas por la circulación portal.
Los inhibidores selectivos de MAO-A han demostrado ser eficaces antidepresivos, mientras que algunos inhibidores de MAO-B resultaron ser beneficiosos en el tratamiento de las enfermedades de Parkinson y Alzheimer. Por lo tanto, es importante contar con procedimientos precisos para la determinación de las actividades de cada isoenzima MAO en tejidos que puedan contenerlas.
En este trabajo resultó importante determinar la actividad de MAO plaquetaria y AO sérica.
En especial, la MAO plaquetaria es considerada un biomarcador de los diferentes rasgos de personalidad tales como comportamiento agresivo, adicción, búsqueda de sensaciones, trastornos afectivos, psicosis afectiva y depresión neurótica (54) (64) y se han encontrado niveles alterados de MAO plaquetaria en varias psicopatologías. Además de actuar en la fisiología de la hemostasia, las plaquetas son herramientas importantes en la investigación psiquiátrica sobre el estrés físico y psicológico, para la comprensión de ciertas condiciones psiquiátricas y de las propiedades farmacológicas de algunos medicamentos psicotrópicos. En realidad, ofrecen una variedad de perspectivas bioquímicas en neuropsiquiatría (46). Entonces, por todo lo expresado, la actividad de MAO plaquetaria es un índice de la actividad serotoninérgica cerebral.
Se observó que en los pacientes el porcentaje significativamente mayor: 73,5% (p < 0,01) corresponde a un marcado descenso en MAO plaquetaria (MAO-B), lo cual está de acuerdo con observaciones previas de disminución en algunos desórdenes mentales y neurodege nerativos, alcoholismo, esquizofrenia, enfermedad de Alzheimer, enfermedad de Parkinson, corea de Huntington, anemia perniciosa (54), trastorno infantil de hiperactividad con déficit de atención (attention deficit hyperactivity disorder: ADHD) (70), conductores de alto riesgo que admiten el riesgo, veteranos de guerra con trastorno de estrés postraumático (71) relacionado con el combate (49), trastorno obsesivo compulsivo y obsesiones agresivas (56). En cambio, se registraron aumentos de MAO plaquetaria en pacientes depresivos (57).
En el presente trabajo se ha determinado también AO sérica que corresponde a un conjunto de aminooxidasas solubles: SSAO, relacionadas con la barrera hematoencefálica, además de la más conocida MAO que actúa intracelularmente (72). SSAO o AO sérica, que puede metabolizar las aminas extracelulares y una forma unida a membrana: SSAO tisular, catalizan la misma reacción general de desaminación oxidativa (73).
En condiciones normales, la actividad de SSAO es constante y la variación inter-individual es pequeña. Sin embargo se ve alterada ante ciertas condiciones fisiopatológicas.
Los valores experimentales de AO sérica obtenidos en este trabajo están de acuerdo con lo observado por otros autores, que encontraron un aumento de la actividad de SSAO sérica, en: diabetes mellitus (tipo 1 y tipo 2) (74), enfermedades inflamatorias del hígado, trastornos vasculares, enfermedad de Alzheimer y demencia vascular, enfermedad de Alzheimer moderada-grave y grave (75). Un aumento en la actividad de AO sérica podría contribuir al estrés oxidativo y al daño vascular en la enfermedad de Alzheimer avanzada. La actividad aumentada de AO sérica también dio lugar a complicaciones tipo diabetes, incluyendo la formación de productos finales de glicación avanzada, presión arterial elevada, progresión alterada de aterosclerosis y nefropatía (76).
Si bien la relación entre AO sérica (SSAO circulante), analizada en el presente estudio, y la forma ligada a membrana no es aún totalmente clara (59), en la actualidad sólo es justificable examinar AO sérica, ya que el examen de la forma unida a membrana en humanos está restringida a técnicas muy invasivas de extracción de tejidos. Por lo tanto, el presente análisis de la actividad de AO sérica refleja sólo una porción del sistema de SSAO implicada en las anomalías monoaminérgicas en pacientes psicóticos. No obstante, los presentes resultados apoyan la hipótesis del metabolismo monoaminérgico disfuncional en la patogénesis de los trastornos psicóticos, si bien la asociación entre los diferentes trastornos y el metabolismo monoaminérgico requiere continuar investigando especialmente en lo que respecta a la actividad de SSAO.
Como SSAO (AO sérica) actúa extracelularmente, puede considerarse complementaria a la actividad intracelular de MAO (MAO plaquetaria). Adicionalmente, hay interacción fisiológica directa entre las actividades de SSAO y MAO, en concordancia con lo encontrado por otros autores (77).
DOSAJE DE BUFOTENINA Y DMT URINARIAS
Se ha sugerido que las moléculas endógenas psicotomiméticas bufotenina y DMT pueden jugar un papel en la patogénesis de trastornos mentales severos, como en esquizofrenia, trastorno del espectro autista (autistic spectrum disorder: ASD) entre otros, y se puede correlacionar con el puntaje de hiperactividad en el autismo (78). Como puede observarse en el presente trabajo las concentraciones en orina de esta molécula están asociadas con las características clínicas de los pacientes psiquiátricos.
DMT EN ORINA Y RELACIÓN ENTRE LOS DISTINTOS PARÁMETROS
Los trabajos anteriores de este grupo de investigación están relacionados con la aparición de este compuesto DMT en la orina de pacientes psiquiátricos y el nivel de las alteraciones perceptuales (11) (17), que también se confirma ahora. Esto también se ha demostrado en estos laboratorios (18) (27) (28) sobre los consumidores de Ayahuasca, debido a los fuertes efectos sobre la percepción.
El estudio interdisciplinario sobre el mismo grupo permitió establecer correlaciones de valor estadístico entre los distintos parámetros estudiados.
Dado que DMT ejerce efectos agonistas en 5-HT2A y parcialmente agonistas en 5-HT2C en el SNC, este agonismo permite explicar las perturbaciones biológicas y de comportamiento observadas, en forma análoga a lo que sucede con bufotenina.
Los resultados obtenidos en este estudio apoyan la hipótesis de que los metabolitos metilados indólicos: bufotenina y DMT, reflejan procesos de transmetilación patológica, por lo cual estas indolalquilaminas metiladas serían marcadores de estado. Estos marcadores son útiles para correlacionar las alteraciones bioquímicas que sufre el paciente con su cuadro clínico, para un correcto diagnóstico, evolución del mismo y para efectuar un tratamiento adecuado, por medio de la medicación que no aumente la actividad serotoninérgica.
La búsqueda de marcadores biológicos de las psicosis funcionales ha sido el objetivo fundamental de la investigación psiquiátrica biológica, buscando primero marcadores específicos de la enfermedad para distinguir las distintas tipologías y para facilitar el diagnóstico de la esquizofrenia. Se esperaba así establecer la etiología o, al menos, contar con un elemento relacionado con la patogénesis. Desde entonces, se establecieron los conceptos de marcador de rasgo, que se refieren a los hallazgos invariables que pueden observarse en los pacientes con trastornos mentales endógenos en la fase aguda, y aún en su remisión; y el de marcador de estado, que indica que sólo va a manifestarse en grado variable mientras esté presente la sintomatología de la enfermedad.
Justamente aquí se presenta el segundo tipo de marcadores.
En cuanto a la actividad de las aminooxidasas, aquí se analizaron MAO plaquetaria y AO sérica. Varias aminas biogénicas de los sistemas dopaminérgicos, noradrenérgicos y serotoninérgicos son degradadas por desaminación oxidativa vía MAO intracelular del grupo de las monoaminooxidasas, las cuales juegan un papel importante respecto a la modificación de la transducción de señales dentro de estos sistemas de neurotransmisores (79). Otras aminoxidasas, como AO sérica, también pueden estar implicadas en estos procesos, pero actuando extracelularmente. Ambas metabolizan las aminas circulantes para mantener la homeostasis del cerebro.
La presencia de SSAO en tejido cerebrovascular humano y en las células endoteliales de la microvasculatura (incluyendo BHE) (74) (80) es compatible con su impacto sobre el metabolismo del SNC y la convierte en un marcador de interés en los casos psiquiátricos.
En resumen, este estudio in vivo demuestra que existe concordancia entre los parámetros neuropsicológicos y la presencia de DMT y bufotenina en muestras de orina de los pacientes como marcadores de la actividad de transmetilación. Más aún, el presente estudio ha demostrado una categorización en cuatro tipos, siendo dos de ellos los más significativos.
Hasta donde llega nuestro conocimiento éste es el primer trabajo que relaciona en conjunto, mediante determinaciones bioquímicas, la actividad transmetilante, la hipoactividad de MAO, la alteración de las AOs intra-y extracelulares, la presencia de indolaquilaminas metiladas en orina y los tests neuropsicológicos, con varias tipologías esquizofrénicas.
Previamente, como se indica en la bibliografía, se han hecho estas relaciones en general una o dos por separado, pero nunca en conjunto como se plantea en este trabajo que brinda un panorama más acabado de toda la batería de análisis cuantitativos que habría que hacer para establecer un diagnóstico más certero y confiable.
AGRADECIMIENTOS
Los autores desean agradecer a CONICET (Argentina) y a la Universidad de Buenos Aires (Argentina) por el apoyo financiero brindado. También al Ministerio de Ciencia, Tecnología e Innovación Productiva (MINCYT, Argentina) por el acceso a la Biblioteca Electrónica (ScienceDirect). A.B.P. y A.A.V. son Miembros de la Carrera de Investigador Científico de CONICET (Argentina).
CORRESPONDENCIA
PROF. DR. ARTURO ALBERTO VITALE
Instituto PRALIB (UBA y CONICET)
Facultad de Farmacia y Bioquímica
Universidad de Buenos Aires (UBA)
Junín 956, C1113AAD CIUDAD AUTÓNOMA DE BUENOS AIRES
E-mail: avitale@ffyb.uba.ar.
1. American Psychiatric Association: Diagnostic and Statistical Manual of Mental Disorders. (DSM IV-TR), 4th ed. Text Revision, Washington, DC: American Psychiatric Association Press; 2000. [ Links ]
2. López Mato A, Vázquez G. Esquizofrenias. En: López Mato A. Psiconeuroinmunoendocrinología II. Buenos Aires: Polemos; 2004. [ Links ]
3. Osmond H, Smythies J. Schizophrenia: a new approach. J Ment Sci 1952; 98 (411): 309-15. [ Links ]
4. Friedhoff AJ, Van Winkle E. Biological O-Methylation and Schizophrenia. Psychiatric Research Report 19. Washington, DC: American Psychiatric Association; 1964 December. p. 149-53. [ Links ]
5. Stam FC, Heslinga FJ, van Tilburg W. Schizophrenia and pink spot. Psychiatr Neurol Neurochir 1969; 72 (6): 513-24. [ Links ]
6. Fischer E. Biogenic amines in schizophrenia. En: Hawkins D, Pauling L, editors. Orthomolecular Psychiatry: Treatment of Schizophrenia. San Francisco: Freeman WH; 1970. p. 179-201. [ Links ]
7. Fischer E, Spatz H. Studies on urinary elimination of bufotenine- like substances in schizophrenia. Biol Psychiatry 1970; 2 (3): 235-40. [ Links ]
8. Fischer E, Spatz H, Fledel T. Bufotenine-like substances in form of glucuronide in schizophrenic and normal urines. Psychosomatics 1971; 12 (4): 278-80. [ Links ]
9. Saavedra JM, Axelrod J. Psychotomimetic N-methylated tryptamines: Formation in brain in vivo and in vitro. Science 1972; 175 (28): 1365-6. [ Links ]
10. Smythies JR. The transmethylation and one-carbon cycle hypotheses of schizophrenia. Psychol Med 1983; 13 (4): 711-4. [ Links ]
11. Ciprian-Ollivier J, Cetkovich-Bakmas MG, Boullosa O. Abnormally methylated compounds in mental illness. En: Shagass C, Josiassen RC, Bridger WH, Weiss KJ, Stoff D, Simpson GM, editors. Biological Psychiatry 1985. New York: Elsevier Science Pub Co; 1986. p. 243-5. [ Links ]
12. Ciprian-Ollivier J, Cetkovich-Bakmas MG, Boullosa O, López-Mato A Psicosis esquizofrénicas.Teoría de la Trasmetilación Patológica. En: Ciprian-Ollivier J, editor. Psiquiatría Biológica. Fundamentos y Aplicación Clínica. Buenos Aires: Científica Interamericana; 1988. p. 75-87. [ Links ]
13. Fischman LG. Dreams, hallucinogenic drug states, and schizophrenia: A psychological and biological comparison. Schizophr Bull 1983; 9 (1): 73-94. [ Links ]
14. Buscaino GA, Spadetta V, Carella A. Il test de la metilazione nella schizofrenia. Considerazione su una casuistica de 500 sperimentazioni. Acta Neurol 1969; 24 (2): 113-8. [ Links ]
15. Tanimukai H, Ginther R, Spaide J, Bueno JR, Himwich HE. Detection of psychotomimetic N,N-dimethylated indoleamines in the urine of four schizophrenic patients. Br J Psychiatry 1970; 117 (539): 421-30. [ Links ]
16. Sitaram BR, McLeod WR. Observations on the metabolism of the psychomimetic indolealkylamines: Implications for future clinical studies. Biol Psychiatry 1990; 28 (10): 841-8. [ Links ]
17. Ciprian-Ollivier J. Delusional status and abnormally methylated compounds. En: Racagni G, Brunello N, Fukuda T, editors. Biological Psychiatry. Proceedings of the 5th. World Congress of Biological Psychiatry. Florence, 1991 9-14 june. Amsterdam: Excerpta Medica; 1991. p. 627-9. [ Links ]
18. Pomilio AB, Vitale AA, Ciprian-Ollivier J. Cult-Hoasca: A model for Schizophrenia. Mol Med Chem 2003; 1: 1-7. [ Links ]
19. Räisänen M, Kärkkäinen J. Mass fragmentographic quantification of urinary N,N-dimethyltryptamine and bufotenine. J Chromatogr 1979; 162 (4): 579-84. [ Links ]
20. Davis BA, Yu PH, Carlson K, O'Sullivan K, Boulton AA. Plasma levels of phenylacetic acid, m- and p-hydroxyphenylacetic acid, and platelet monoamine oxidase activity in schizophrenic and other patients. Psychiatry Res 1982; 6 (1): 97-105. [ Links ]
21. de Beaurepaire R. Bases biochimiques et neurobiologiques de la psychiatrie. EMC-Psychiatrie 2005; 2: 4- 39. [ Links ]
22. Kay S. Positive and Negative Syndromes in Schizophrenia. New York: Brunner/Mazel; 1991. [ Links ]
23. Müller-Spahn F. Risperidone in the treatment of chronic schizophrenic patients: An international double blind parallel group study versus haloperidol. Proceedings of the 18th. Collegium Internationale Neuropsychopharmacologicum Congress. New York: Raven Press; 1992. Clinical Neuropharmacology 1992; 15 (Suppl 1A): 90-1. [ Links ]
24. Ciudad A, Álvarez E, Bousoño M, Olivares JM, Gómez JC. Seguridad y tolerabilidad de olanzapina y risperidona: un estudio aleatorizado de 1 año de duración en pacientes con esquizofrenia y sintomatología negativa prominente tratados de manera ambulatoria. Actas Esp Psiquiatr 2007; 35 (2): 105-14. [ Links ]
25. Strassman RJ. Human psychopharmacology of N,N-dimethyltryptamine. Behav Brain Res 1995; 73 (1-2): 121-4. [ Links ]
26. Glennon RA, Dukat M. Serotonin receptor subtypes. En: Bloom FE, Kupfer DJ, editors. Psychopharmacology: The Fourth Generation of Progress. New York: Raven Press; 1995. p. 415-29. [ Links ]
27. Pomilio AB, Vitale AA, Ciprian-Ollivier J, Cetkovich- Bakmas M. A chemical approach to the understanding of Schizophrenia. An Asoc Quim Argent 1998; 86: 320-35. [ Links ]
28. Pomilio AB, Vitale AA, Ciprian-Ollivier J, Cetkovich- Bakmas M, Gómez R, Vázquez R Ayahoasca: An experimental psychosis that mirrows the Transmethylation Hypothesis of Schizophrenia. J Ethnopharmacol 1999; 65 (1): 29-51. [ Links ]
29. Ciprian Ollivier J, Spatz H. Aminas N- y O-metiladas en orina de esquizofrénicos y controles normales. Daimon 1981; 138: 28-31. Editum: Ediciones de la Universidad de Murcia. [ Links ]
30. Ciprian-Ollivier J. Bioquímica de la esquizofrenia (en correlaciones psicobiológicas). En: Actas del 1º Congreso Argentino, Buenos Aires: Editorial Belgrano; 1982. p. 33-9. [ Links ]
31. Ciprian Ollivier J, Cetkovich Bakmas M. Teoría de la trasmetilación patológica. En: Ciprian Ollivier J, editor. Psiquiatría Biológica. Buenos Aires: Interamericana; 1992. [ Links ]
32. Ciprian-Ollivier J, Cetkovich-Bakmas M. Altered consciousness states and endogenous psychoses: a common molecular pathway? Schizophr Res 1997; 28 (2-3): 257-65. [ Links ]
33. Umbricht D, Kane JM. Risperidone: Efficacy and safety. Schizophr Bull 1995; 21 (4): 593-606. [ Links ]
34. Pelletier O, Campbell JA. A rapid method for the determination of N'-methylnicotinamide in urine. Anal Biochem 1962; 3: 60-7. [ Links ]
35. Krajl M. A rapid microfluorimetric determination of monoamine oxidase. Biochem Pharmacol 1965; 14 (11): 1684-5. [ Links ]
36. Pivac N, Knezevic J, Mustapic M, Dezeljin M, Muck-Seler D, Kozaric-Kovacic D, et al. The lack of association between monoamine oxidase (MAO) intron 13 polymorphism and platelet MAO-B activity among men. Life Sci 2006; 79 (1): 45-9. [ Links ]
37. Matsumoto T, Suzuki O, Furuta T, Asai M, Kurokawa Y, Nimura Y, et al. A sensitive fluorometric assay for serum monoamine oxidase with kynuramine as substrate. Clin Biochem 1985; 18 (2): 126-9. [ Links ]
38. Sintas JA, Vitale AA. Synthesis of 131I derivatives of indolealkylamines for brain mapping. J Labelled Compnds Radiopharm 1997; 39 (8): 677-84. [ Links ]
39. Pomilio AB. Separación de aminas biogénicas mediante cromatografía líquida de alta resolución. Acta Bioquím Clín Latinoam 1995; 29 (1): 3-36. [ Links ]
40. Vitale AA, Calviño MA, Ferrari C, Pomilio AB, Ciprian- Ollivier J, Cetkovich-Bakmas M. Método rápido y sensible para detectar aminas primarias y secundarias no fenólicas en orina humana. Acta Bioquím Clín Latinoam 1995; 29 (1): 37-46. [ Links ]
41. Pomilio AB, Vitale AA. Técnicas para determinación cuali/cuantitativa de drogas de abuso en fluidos biológicos. Acta Bioquím Clín Latinoam 2006; 40 (3): 347-82. [ Links ]
42. Spreen O, Strauss E. A Compendium of Neuropsychological Tests. NewYork: Oxford University Press; 1991. [ Links ]
43. Buschke H. Selective reminding analysis of memory and learning. J Verb Learn Verb Behav 1973; 12 (5): 543-50. [ Links ]
44. McClure MM, Romero MJ, Bowie CR, Reichenberg A, Harvey PD, Siever LJ. Visual-spatial learning and memory in schizotypal personality disorder: Continued evidence for the importance of working memory in the schizophrenia spectrum. Arch Clin Neuropsychol 2007; 22 (1): 109-16. [ Links ]
45. Shih JC, Grimsby J, Chen K, Zhu Q-s. Structure and promoter organization of the human monoamine oxidase A and B genes. J Psychiatr Neurosci 1993; 18 (1): 25-32. [ Links ]
46. Camacho A, Dimsdale JE. Platelets and psychiatry: lessons learned from old and new studies. Psychosom Med 2000; 62 (3): 326-36. [ Links ]
47. Vives JL, Aguilar JL. La sangre, características generales y métodos de extracción sanguínea. Empleo de anticoagulantes. En: Manual de técnicas de laboratorio en hematología. Barcelona: Salvat Editores; 1987. [ Links ]
48. Fowler JS, Logan J, Wang GJ, Volkow ND. Monoamine oxidase and cigarette smoking. Neurotoxicology 2003; 24: 75-82. [ Links ]
49. Pivac N, Knezevic J, Kozaric-Kovacic D, Dezeljin M, Mustapic M, Rak D, Matijevic T, Pavelic J, Muck-Seler D. Monoamine oxidase (MAO) intron 13 polymorphism and platelet MAO-B activity in combat-related posttraumatic stress disorder. J Affect Disord 2007; 103: 131-8. [ Links ]
50. Costa-Mallen P, Costa LG, Checkoway H. Genotype combinations for monoamine oxidase-B intron 13 polymorphism and dopamine D2 receptors TaqIB polymorphism are associated with ever-smoking status among men. Neurosci Lett 2005a; 385: 158-62. [ Links ]
51. Nicotra A, Pierucci F, Parvez H, Senatori O. Monoamine oxidase expression during development and aging. Neurotoxicology 2004; 25: 155-65. [ Links ]
52. Sobell JL, Lind TJ, Hebrink DD, Heston LL, Sommer SS. Screening the monoamine oxidase B gene in 100 male patients with schizophrenia: a cluster of polymorphisms in African-American but lack of functionally significant sequence changes. Am J Med Genet (Neuropsychiatric Gen) 1997; 74: 44-9. [ Links ]
53. Anthenelli RM, Tipp J, Li T-K, Magnes L, Schuckit MA, Rice J, Daw W, Nurnberger Jr JI. Platelet monoamine oxidase activity in subgroups of alcoholics and controls: results from the collaborative study on the genetics of alcoholism. Alcohol Clin Exp Res 1998; 22 (3): 598-604. [ Links ]
54. Oreland L. Platelet monoamine oxidase, personality and alcoholism: the rise, fall and resurrection. Neurotoxicology 2004; 25 (1-2): 79-89. [ Links ]
55. Meltzer HY, Arora RC. Skeletal muscle MAO activity in the major psychoses: Relationship with platelet and plasma MAO activities. Arch Gen Psychiatry 1980; 37 (3): 333-9. [ Links ]
56. Arrojo M, Baca-García E, Pérez-Rodríguez MM, Dolengevich-Segal H, Navio-Acosta M, Rodríguez-Salgado B, Saiz-Ruiz J. Actividad de la monoaminooxidasa plaquetaria en el trastorno obsesivo compulsivo. Eur Psychiatry 2007; 22 (8): 525-9. [ Links ]
57. White K, Shih JC, Fong TL, Young H, Gelfand R, Boyd J. Elevated platelet monoamine oxidase activity in non-endogenous depressives. Am J Psychiatry 1980; 37: 1258-9. [ Links ]
58. Buffoni F, Ignesti G. Biochemical aspects and functional role of the copper-containing amine oxidases. Inflammopharmacology 2003; 11 (3): 203-9. [ Links ]
59. Boomsma F, Hut H, Bagghoe UM, van der Houwen A, van den Meiracker A. Semicarbazide-sensitive amine oxidase (SSAO): from cell to circulation. Med Sci Monit 2005; 11 (4): RA122-6. [ Links ]
60. Mátyuz P, Dajka-Halász B, Földi A, Haider N, Barlocco D, Magyar K. Semicarbazide-sensitive amine oxidase: current status and perspectives. Curr Med Chem 2004; 11: 1285-98. [ Links ]
61. Boomsma F, Bagghoe UM, van der Houwen AMB, van den Meiracker AH. Plasma semicarbazide-sensitive amine oxidase in human (patho)physiology. Biochim Biophys Acta 2003; 1647 (1-2): 48-54. [ Links ]
62. Spatz H, Spatz N. Trastornos bioquímicos en algunos desórdenes psiquiátricos. En: Psiquiatría biológica. Fundamentos y aplicación clínica. Buenos Aires: Interamericana; 1988. p. 37-47. [ Links ]
63. Spatz N, Spatz H, Mesones Arroyo HL, Rosan T, Brengio F. Eliminación de N,N-dimetiltriptamina por orina. Acta Psiquiatr Psicol Am Lat 1993; 39 (3): 212-6. [ Links ]
64. Ruchkin VV, Koposov RA, af Klinteberg B, Oreland L, Grigorenko EL. Platelet MAO-B, personality, and psychopathology. J Abnorm Psychol 2005; 114 (3): 477-82. [ Links ]
65. Goldstein G, Allen DN, van Kammen DP. Individual differences in cognitive decline in schizophrenia. Am J Psychiatry 1998; 155 (8): 1117-8. [ Links ]
66. Crespo-Facorro B, Kim JJ, Andreasen NC, O'Leary DS, Magnotta V. Regional frontal abnormalities in schizophrenia: A quantitative grey matter volume and cortical surface size study. Biol Psychiatry 2000; 48 (2): 110-19. [ Links ]
67. Hannay HJ, Levin HS. Selective Reminding Test: An examination of the equivalence of four forms. J Clin Exper Neuropsychol 1985; 7 (3): 251-63. [ Links ]
68. Voglmaier MM, Seidman LJ, Niznikiewicz MA, Dickey CC, Shenton ME, McCarley RW. A comparative profile analysis of neuropsychological function in men and women with schizotypal personality disorder. Schizophr Res 2005; 74 (1): 43-9. [ Links ]
69. Castagnoli N, Dalvie D, Kalgutkar A, Taylor T. Interactions of nitrogen containing xenobiotics with monoamine oxidase (MAO) isozymes A and B: SAR studies on MAO substrates and inhibitors. Chem Res Toxicol 2001; 14 (9): 1139-62. [ Links ]
70. Roessner V, Uebel H, Becker A, Beck G, Bleich S, Rothenberger A. Serum level of semicarbazide-sensitive amine oxidase in children with ADHD. Behav Brain Functions 2006; 2: 5. [ Links ]
71. Nemeroff CB, Bremner JD, Foa EB, Mayberg HS, North CS, Stein MB. Posttraumatic stress disorder: a state-of-the science review. J Psychiatr Res 2006; 40: 1-21. [ Links ]
72. Smeraldi C, Castillo V, Lizcano JM, Unzeta M. Some properties of semicarbazide-sensitive amine oxidase (SSAO) from human cerebrovascular tissues. Inflamm Res 2001; 50 (Suppl 2): S144-5. [ Links ]
73. Ohman J, Jakobsson E, Källström U, Elmblad A, Ansari A, Kalderén C, et al. Production of a truncated soluble human semicarbazide-sensitive amine oxidase mediated by a GST-fusion protein secreted from HEK293 cells. Protein Expr Purif 2006; 46: 321-31. [ Links ]
74. Obata T. Diabetes and semicarbazide-sensitive amine oxidase (SSAO) activity: a review. Life Sci 2006; 79 (5): 417-22. [ Links ]
75. Unzeta M, Solé M, Boada M, Hernández M. Semicarbazide- sensitive amine oxidase (SSAO) and its possible contribution to vascular damage in Alzheimer's disease. J Neural Transm 2007; 114 (6): 857-62. [ Links ]
76. Nemcsik J, Szökö E, Soltész Z, Fodor E, Toth L, Egresits J, et al. Alteration of serum semicarbazide-sensitive amine oxidase activity in chronic renal failure. J Neural Transm 2007; 114 (6): 841-3. [ Links ]
77. Fitzgerald DH, Tipton KF. Inhibition of monoamine oxidase modulates the behaviour of semicarbazide-sensitive amine oxidase (SSAO). J Neural Transm 2002; 109 (3): 251-65. [ Links ]
78. Emanuele E. Colombo R, Martinelli V, Brondino N, Marini M, Boso M, et al. Elevated urine levels of bufotenine in patients with autistic spectrum disorders and schizophrenia. Neuro Endocrinol Lett 2010; 31 (1): 117-21. [ Links ]
79. Billett EE. Monoamine Oxidase (MAO) in human peripheral tissues. Neurotoxicology 2004; 25: 139-48. [ Links ]
80. Obata T. Semicarbazide-sensitive amine oxidase (SSAO) in the brain. Neurochem Res 2002; 27 (4): 263-8. [ Links ]
Aceptado para su publicación el 3 de diciembre de 2010














