Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957
Acta bioquím. clín. latinoam. vol.44 no.4 La Plata oct./dic. 2010
INMUNOLOGÍA
Efecto producido por Ascaris lumbricoides sobre la carga superficial eritrocitaria utilizando el Método de Polibrene
Effect of Ascaris lumbricoides on the erythrocyte superficial charge using Polybrene Method
Patricia Ponce de León1 a, Claudia Biondi2 b, Juana Valverde2 b
1. Bioquímica.
2. Doctora en Ciencias Bioquímicas.
a Laboratorio de Parasitología. Facultad de Cs. Bioquímicas y Farmacéuticas. UNR.
b Laboratorio de Inmunohematología, Hemorrelogía e Inmunogenética. Facultad de Cs. Bioquímicas y Farmacéuticas. UNR, Rosario, Argentina.
Resumen
Los ácidos siálicos (AS) contenidos en glucoproteínas y glucolípidos participan en diversas funciones biológicas y su presencia en el eritrocito tiene importancia hemorreológica y hemodinámica. Se considera que los AS intervendrían en la interacción parásito-hospedador. El objetivo de este trabajo fue estudiar el efecto producido por A. lumbricoides sobre la carga superficial eritrocitaria utilizando el Método de Polibrene. Se trabajó con 51 extractos de parásito adulto ([EA]) y con 4 concentrados larvales ([CLAL]: 2000/ 1000/ 500/ 250 larvas/ mL). El método fue aplicado en eritrocitos no tratados (Control) y tratados con [EA]/ los 4 [CLAL] de forma simultánea. El tratamiento con las larvas se realizó en 18 experiencias. Los eritrocitos tratados con el 37, 25% de los [EA] presentaron menor agregación en relación al Control. Los análisis estadísticos mostraron que este efecto no se relacionó con la concentración proteica del [EA]. La disminución de agregado en el tratamiento con [CLAL] fue dependiente de la concentración larvaria y se relacionó a concentraciones ≥ a 500 larvas/ mL. Se observó que la fijación [EA]/ [CLAL] al eritrocito no era fuerte. Los resultados demostraron que A. lumbricoides secuestra AS eritrocitario. Esta captación podría influir en la patología y / o participar en la evasión de la respuesta inmune del hospedador.
Palabras clave: Ascaris lumbricoides; Carga eritrocitaria; Polibrene
Summary
Sialic acids (SA) contained in glycoproteins and glycolipids participate in various biological functions; besides, its presence on the erythrocyte surface has both hemodynamical and hemorheological importance. SA are thought to intervene in the parasite-host interaction. The aim of this work was to study the effect of Ascaris lumbricoides on the erythrocyte superficial charge by using Polybrene Method. Work was carried out on 51 adult parasite extracts ([AE]) and 4 (larvae) larvae concentrates ([ALLC]: 2000 / 1000 / 500 / 250 larvae/ mL). The method was applied to non-treated (Control) and treated red cells with [AE] / all 4 [ALLC] simultaneously. Larvae´ treatment was conducted over 18 experiences. Erythrocytes treated with 37. 25% of the [AE] had lower aggregation than the Control. The statistical analysis showed that this effect was not related to the protein concentration of [AE]. The aggregate decrease in the treatment with [ALLC] was dependent on larvae concentration and it was related to larvae concentrations ≥ 500 larvae/ mL. It was observed that the [AE]/ [ALLC] fixation to the erythrocyte was not strong. The results have shown that A. lumbricoides sequestrates SA erythrocyte. This capture could affect the pathology and/or participate in the escape of the host's immune response.
Key words: Ascaris lumbricoides; Erythrocyte charge; Polybrene
Introducción
La glicobiología es el estudio de los aspectos estructurales y funcionales de los glicoconjugados presentes en las células.
Durante la última década, las tecnologías de secuenciación y síntesis, que son de uso común en el estudio de ácidos nucleicos y proteínas, también pasaron a formar parte del estudio de los glicoconjugados, demostrando la participación de los oligosacáridos en las vías de señalización (1).
La comprensión a nivel molecular del enlace hidrato de carbono/proteína, ha posibilitado el conocimiento de las funciones biológicas de los primeros. Su estudio ha permitido relacionarlos con enfermedades, y ya existen ejemplos concretos en infecciones bacterianas y virales. Lo mismo sucede con enfermedades parasitarias como malaria, leishmaniasis y tripanosomiasis (1).
Los ácidos siálicos son azúcares carboxilados con nueve carbonos. El más común es el ácido N-acetilneuramínico (Neu5Ac), el cual es considerado precursor de los otros miembros de la familia, como por ejemplo, del ácido N-glicolilneuramínico (Neu5Gc) y del ácido 2-deoxi-2,3-didehidro-N-acetilneuramínico (Neu5Ac2en).
Los ácidos siálicos presentes en glucoproteínas y glucolípidos están involucrados en funciones biológicas tales como procesos de reconocimiento celular, vida media de células y proteínas plasmáticas, modulación del sistema inmune y apoptosis. También son ligandos de moléculas de adhesión, como por ejemplo, selectinas o sialoadhesinas, mediando adhesión celular o transducción de señales. Actualmente se considera que tendrían un papel importante en la interacción parásito-hospedador (1).
El ácido siálico también tiene importancia hemorreológica y hemodinámica, debido a que es responsable de la carga negativa de la membrana eritrocitaria y contribuye a las propiedades estructurales de las glicoforinas. Su disminución promueve la agregación eritrocitaria, la formación de rouleaux, la disminución del flujo sanguíneo y el aumento de la viscosidad de la sangre, favoreciendo de este modo la interacción de los glóbulos rojos con el endotelio vascular (2).
Ascaris lumbricoides es un nematodo patógeno muy común en este medio. En el ciclo de vida tiene etapas larvarias en donde las larvas circulan por el torrente sanguíneo. Cuando desarrolla a estado adulto, si bien su localización es intestinal, puede migrar y provocar obstrucción biliar, pancreatitis, apendicitis obstructiva, perforación de la pared intestinal, abscesos hepáticos, o penetrar en los canales venosos hepáticos o cavales para ser transportado a cerebro, corazón o pulmones produciendo trombosis (3), por lo tanto las fases larvales tienen contacto directo con los eritrocitos del hospedador, y eventualmente también lo podría tener el parásito adulto.
En experiencias preliminares, aplicando el Método de Partición en Sistemas Bifásicos Acuosos (Dx/ PEG), se demostró que A.lumbricoides altera la carga superficial eritrocitaria, lo que indicó que tendría la capacidad de captar ácido siálico del glóbulo rojo (4).
El único método directo de cuantificación de ácido siálico en el eritrocito, es su dosaje en la membrana eritrocitaria. Debido a que la implementación de esta técnica, no es accesible a todos los laboratorios, surgieron varios métodos que permiten estudiar de manera indirecta la carga y el contenido de ácido siálico superficial del glóbulo rojo. Uno de ellos es el que utiliza bromuro de hexadimetrina (Polibrene). Este polímero sintético, cargado positivamente, tiene la propiedad de aglutinar los eritrocitos normales, pero no los glóbulos con carga negativa reducida (5).
Debido a la importancia que podría tener la captación de ácido siálico en la interacción párasito- hospedador, el objetivo de este trabajo fue estudiar el efecto producido por A.lumbricoides sobre la carga superficial eritrocitaria utilizando el Método de Polibrene.
Materiales y Métodos
MUESTRAS
Extractos de A. lumbricoides ([EA]): Se trabajó con 51 extractos parasitarios obtenidos a partir de la remoción de la cutícula de ejemplares adultos y ruptura mecánica refrigerada (6).
Concentrados de Larvas ([CLAL]): Se utilizaron 4 Concentrados de Larvas (L1/L2) obtenidos de la embrionación in vitro (7) y posterior eclosión de huevos de A. lumbricoides (8). Las larvas fueron recolectadas a 37 ºC por el método de Baermann-Moraes (9) en buffer fosfato. Completada la recolección fueron concentradas por centrifugación y se procedió al recuento de las mismas ([CLAL1]: 2000 larvas/mL; [CLAL2]: 1000 larvas/mL; [CLAL3]: 500 larvas/mL; [CLAL4]: 250 larvas/mL).
MÉTODOS
Método de Polibrene Modi.cado en placa de vidrio (10)
Se utilizaron suspensiones de eritrocitos humanos frescos Grupo "O", lavados 3 veces en solución fisiológica (SF). Previo al lavado de los glóbulos, se separó el plasma autólogo (PA) por centrifugación.
El método se aplicó simultáneamente en eritrocitos no tratados (Control) y en los mismos eritrocitos tratados con el parásito.
El tratamiento consistió en incubar 100 μL del sedimento globular con igual volumen de [EA] o [CLAL], durante 1 hora en baño termostatizado a 37 ºC. Los eritrocitos Control fueron incubados de la misma manera con igual volumen de SF.
Los eritrocitos tratados y Control fueron lavados 3 veces en SF y se prepararon a partir del sedimento globular, suspensiones al 20% en solución salina.
Se colocaron, en una placa de vidrio, 3 gotas de LIM (solución de baja fuerza iónica), 2 gotas de PA y 1 gota de la suspensión eritrocitaria. Se mezcló con varilla de vidrio y se agregó 1 gota de Polibrene, volviendo a mezclar con la varilla. Se homogeneizó mediante movimientos circulares de la placa de vidrio durante 1 min. En esta primera etapa se produjo la agregación de los eritrocitos.
A los fines de comparar la agregación de los glóbulos tratados con la del respectivo Control, se semicuantificó con cruces (3+; 2+: 1+; +/-; +/ - -).
En la segunda etapa del método, se agregó una gota de solución de resuspensión, se mezcló con varilla y se realizaron nuevamente, durante un minuto, movimientos circulares de la placa. En este paso se observó si los eritrocitos permanecían o no agregados.
La técnica fue desarrollada para detectar aloanticuerpos dirigidos contra los glóbulos rojos, que se evidencian por la no desagregación (10).
REACTIVOS
- LIM, dextrosa 25 g, EDTA disodio 1 g, agua destilada 500 mL
- Polibrene 0,1%.
Solución de reserva 10% (1 g de Polibrene + 10 mL de SF)
Solución de Trabajo (5 mL solución de reserva + 495 mL de SF)
- Solución de resuspensión
0,4 M de citrato trisódico (35,28 g de citrato trisódico + 300 mL de agua destilada)
dextrosa 5% (10 g de dextrosa + 200 mL de agua destilada)
Mezclar ambos.
MÉTODO PARA DETERMINAR LA CONCENTRACIÓN PROTEICA TOTAL DE LOS [EA] (11)
Se usó un método colorimétrico automatizado que se fundamenta en la formación de un complejo, a pH alcalino, entre el ión cúprico y las proteínas totales. El máximo de absorbancia del complejo es a 540 nm y su intensidad es proporcional a la concentración proteica de la muestra.
ANÁLISIS ESTADÍSTICOS DE LOS RESULTADOS
Se aplicó el test de Mann-Whitney para determinar si la concentración proteica del [EA] estaba relacionada con la alteración en la agregación de los glóbulos tratados (12).
El test de Cochran se empleó para analizar si la concentración de larvas usada en el tratamiento se asociaba a la disminución de agregación eritrocitaria, con respecto a la agregación del Control (13).
Resultados
RESULTADOS OBTENIDOS DEL TRATAMIENTO DE LOS ERITROCITOS CON [EA]
La experiencia se realizó en forma simultánea para los eritrocitos tratados y los correspondientes eritrocitos Controles.
Los glóbulos rojos tratados con 19 de los 51 [EA] (37, 25%) mostraron en la primera etapa del método, una diferencia notable en la agregación con respecto a los Controles. Este comportamiento se evidenció no sólo por la menor cantidad de agregado formado, sino también por la velocidad de agregación que fue más lenta que la velocidad del Control.
En la segunda etapa de la técnica, todos los eritrocitos tratados y Controles desagregaron al incorporar la solución de resuspensión.
La Tabla I muestra los resultados obtenidos en la primera etapa de agregación con eritrocitos Controles/eritrocitos tratados con extracto, así como también la concentración de proteínas totales de cada [EA] utilizado en la experiencia.
Tabla I. Primera etapa del Método de Polibrene Modificado: Agregación de eritrocitos Controles y tratados con [EA]

ANÁLISIS ESTADÍSTICO
Se aplicó el test de Shapiro-Wilk para verificar el cumplimiento del supuesto de normalidad.
El test de Mann-Whitney se utilizó para comparar los valores centrales de la concentración proteica de los 19 [EA] que provocaron diferencias en la agregación de los eritrocitos tratados con respecto a la agregación del Control, y de los 32 [EA] que no alteraron la agregación en el tratamiento de los glóbulos en relación a lo observado en sus correspondientes Controles.
La mediana de los [EA] que tuvieron efecto sobre la agregación eritrocitaria fue 0,2 (RI: 0,490) y de los extractos que no modificaron la agregación con respecto a la del Control fue 0,2 (RI: 0,525). La Figura 1 muestra el análisis estadístico del efecto de la concentración proteica del [EA] sobre la alteración de la carga eritrocitaria.
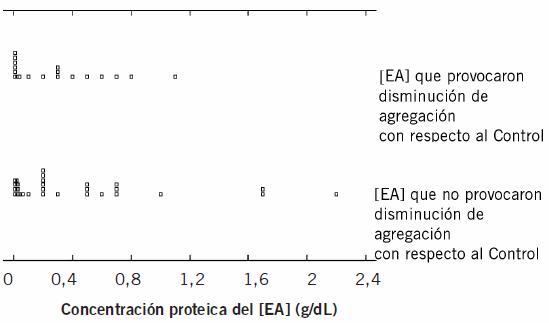
Figura 1. Estudio del efecto que el [EA] produce sobre la agregación eritrocitaria, en la concentración proteica del mismo.
Se concluye, por el test de Mann-Whitney, que la concentración proteica del extracto parasitario no está relacionada con el efecto que el [EA] produce sobre la agregación eritrocitaria (p>0,50).
RESULTADOS OBTENIDOS DEL TRATAMIENTO DE LOS ERITROCITOS CON [CLAL]
Se realizaron 18 experiencias con distintas suspensiones de glóbulos rojos. En cada una de ellas se procesaron en forma simultánea los eritrocitos no tratados (Control) y los mismos eritrocitos tratados con los 4 concentrados de larvas.
El tratamiento con [CLAL1] (2000 larvas/mL) provocó, en la primera etapa del método, alteración de la agregación del total de las suspensiones estudiadas, mostrando en casi todos los glóbulos tratados, una marcada disminución del agregado formado y menor velocidad de agregación con respecto al Control correspondiente (18/ 18= 100%).
Los resultados obtenidos con [CLAL2] (1000 larvas/ mL) fueron similares a los anteriores con 17 de las suspensiones de glóbulos tratados (17/ 18= 94,44%).
Los resultados mostraron que el tratamiento con [CLAL3] (500 larvas/mL) alteró la agregación eritrocitaria en 9 de las experiencias realizadas (9/ 18= 50%), las cuales presentaron velocidades de agregación un poco más lentas que las de sus Controles. La cantidad de agregado formado fue menor en relación a los glóbulos no tratados, aunque sólo en 4 de las 9 se observó una marcada disminución.
El tratamiento de los eritrocitos con [CLAL4] (250 larvas/ mL) provocó alteraciones en la agregación de 5 suspensiones (5/ 18= 27,78%), de las que sólo 2 mostraron una evidente disminución de la cantidad de agregado formado y de la velocidad de agregación al compararlas con el Control.
Los resultados de la primera etapa del método se muestran en la Tabla II.
Tabla II. Primera etapa del Método de Polibrene Modificado: Agregación de eritrocitos Controles y tratados con [CLAL]

En la segunda etapa de la técnica, la adición de la solución de resuspensión, desagregó todos los Controles y los eritrocitos tratados con los 4 [CLAL] en las 18 experiencias realizadas.
ANÁLISIS ESTADÍSTICO
Se aplicó el test de Cochran para analizar si la concentración larvaria estaba relacionada con el efecto de modificar la agregación de los eritrocitos tratados.
Se compararon sólo las proporciones de resultado 3+ o no, es decir la agregación observada en el Control con otra agregación diferente (2+: 1+; +/-; +/ - -).
Los resultados del análisis se muestran a continuación; las proporciones que difieren son aquellas cuyos * no están alineados (p< 0,05).

Se concluye, por aplicación del test de Cochran, que [CLAL1] y [CLAL2] no difieren entre sí, pero son diferentes al Control, por lo tanto estas dos concentraciones larvarias están relacionadas con la disminución de la agregación con respecto a la observada en el Control. No hay diferencia significativa entre ambas en la proporción de experiencias en las que el tratamiento provocó disminución de carga.
[CLAL3] y [CLAL4] tampoco difieren entre sí, pero sólo el primero mostró una proporción significativamente diferente al Control.
Los resultados estadísticos mostraron que la disminución de la agregación en los glóbulos tratados con larvas, se relaciona con concentraciones ≥ a 500 larvas/ mL. No se encontró una variación significativa entre la agregación del Control y de los eritrocitos tratados con 250 larvas/ mL (p<0,001).
Discusión y Conclusiones
Los ácidos siálicos pertenecen a una familia de azúcares que se localizan en las posiciones terminales de una gran variedad de glucoconjugados. Naturalmente, muestran una inmensa diversidad de estructuras que reflejan su participación en importantes procesos biológicos de crecimiento y desarrollo, tanto normal como patológico (14)(15). Estos azúcares juegan un papel destacado regulando los procesos de reconocimiento celular y molecular, dado que en muchas situaciones son componentes esenciales de receptores implicados en la transducción de señales. Pueden funcionar también como enmascadores biológicos, que por efectos estéricos y/o de repulsión electrostática, pueden impedir o reducir la accesibilidad de los ligandos a sus receptores sobre la superficie celular. Adicionalmente, los diferentes tipos de ácidos siálicos son importantes en la carga neta de la superficie celular de los mamíferos y protistas parásitos, siendo relativamente abundantes en el glucocálix de distintas células mamíferas tales como los enterocitos, eritrocitos y células caliciformes maduras de intestino delgado, así como también se encuentran en grandes cantidades en el moco de las mucosas (15). Su presencia en la superficie del eritrocito determina la carga negativa, y su disminución tiene consecuencias hemorreológicas y hemodinámicas que son fundamentales en el desarrollo de distintas patologías humanas (2).
Los distintos grupos de ionización presentes en la superficie externa de la membrana plasmática son responsables de que todas las células vivas tengan globalmente una carga negativa superficial expuesta al medio acuoso que las rodea. Este potencial eléctrico negativo condiciona la estabilidad física de la célula en la circulación sanguínea (16).
El Método de Polibrene permite estudiar, de forma indirecta, la carga y el contenido de ácido siálico superficial del glóbulo rojo. Este policatión induce la agregación inespecífica de los eritrocitos y facilita el acercamiento de las moléculas de anticuerpos IgG. Dicha agregación inespecífica es reversible tras el agregado de un inhibidor del policatión pero irreversible ante una verdadera reacción antígeno - anticuerpo (5).
La Técnica de Polibrene en tubo descripta por Mollison (5) utiliza la misma concentración de polímero que fue empleada en la experiencia en placa (0,1%). Este autor ha comunicado que la deficiencia de ácido siálico debe superar el 12% para que los hematíes no sean agregados (5). El uso del polímero en una concentración de 0,6 g/dL puede producir fenómenos de prozona y por lo tanto, eritrocitos con importantes pérdidas de ácido siálico (del 30% o más), tampoco serían agregados (5).
En la experiencia realizada se observó, en la primera etapa de la técnica de Polibrene, disminución en la cantidad de agregado, presentando distintos grados de agregación con respecto al correspondiente Control, tanto para glóbulos tratados con [EA] como con [CLAL]. Ninguno de los tratamientos provocó que los hematíes no fueran agregados. Por lo tanto, los resultados obtenidos sugieren que en los glóbulos tratados en los que se visualizó disminución de carga superficial, la pérdida de ácido siálico debería ser inferior al 12%.
Se demostró que el 35, 27% de los [EA] captó ácido siálico de los eritrocitos, en las condiciones experimentales establecidas en este estudio.
En los nematodos, el cuerpo está recubierto por una cutícula resistente en la que predominan proteínas similares al colágeno y una proteína del tipo de las queratinas.
El crecimiento se acompaña normalmente de cuatro mudas de la cubierta superficial, donde la antigua se separa y el parásito segrega la nueva cubierta. La antigua se desprende entera o en fragmentos, pero puede ser absorbida parcialmente por la nueva. En el ejemplar adulto no hay mudas, pero la cutícula continúa expandiéndose mientras el parásito crece (17).
Los extractos utilizados en la experiencia fueron preparados a partir de la remoción de la cutícula de ejemplares adultos del parásito. Se determinó el contenido proteico del extracto, a modo de estimación del grado de crecimiento y desarrollo del nematodo, con el objeto de estudiar si se relacionaba con la capacidad del parásito de captar ácido siálico.
El estudio estadístico concluyó que no hay relación entre la concentración proteica de [EA] y la diferencia de agregación observada en los glóbulos tratados con respecto a la agregación del Control. Por lo tanto, la captación de ácido siálico producida por el extracto de A. lumbricoides y la consecuente alteración de la carga superficial eritrocitaria sería independiente del grado de crecimiento y desarrollo del helminto.
El tratamiento con [CLAL] provocó también, disminución de la carga globular que fue dependiente de la concentración de larvas utilizada.
Los resultados del análisis estadístico concluyeron que hay diferencia significativa en la proporción de experiencias en las que se observó menor agregación en los eritrocitos tratados respecto a la agregación de los no tratados, cuando se utilizaron concentraciones larvarias ≥ a 500 larvas/ mL.
Además, se observó que la concentración larvaria se relacionaba significativamente con la proporción de experiencias en las que los glóbulos tratados presentaron menor agregación que los glóbulos Controles, ya que el contacto con 500 larvas/ mL provocó disminuciones de carga superficial eritrocitaria en el 50% de las experiencias realizadas, mientras que el tratamiento con 1000 y 2000 larvas/ mL mostró este efecto en el 94,44% y 100%, respectivamente, de las experiencias. No se encontró diferencia estadísticamente significativa entre estas dos últimas concentraciones.
En la segunda etapa de la técnica, cuando hay una reacción antígeno- anticuerpo, la desagregación es irreversible debido a que se establece entre ambos una fuerza de unión intensa. Diversos autores, por lo tanto, han empleado este método para detectar aloanticuerpos anti-eritrocitarios en estudios pre-tranfusionales (10)(18)(19), en anemias hemolíticas autoinmunes (20)(23) y en embarazos (21)(22).
En las experiencias realizadas, esta etapa fue utilizada para evaluar la unión del parásito al glóbulo rojo durante el tratamiento.
Ninguno de los eritrocitos tratados con [EA]/ [CLAL] permaneció agregado cuando se adicionó la solución de resuspensión. Estos datos sugieren que no hubo una fuerte fijación del parásito a los eritrocitos.
Los resultados obtenidos con el Método de Polibrene Modificado en placa son coincidentes con los comunicados previamente utilizando el Método de Partición en Sistemas Bifásicos Acuosos (4). Con ambas técnicas se observó que A. lumbricoides, tanto en su fase larval como adulta, es capaz de disminuir la carga superficial del glóbulo rojo a temperatura fisiológica.
La captación de ácido siálico del eritrocito por A. lumbricoides sugiere que también podría secuestrarlo a partir de otros glucoconjugados que posean residuos sialisados, tal como fue comunicado para Trypanosoma cruzi (24). Este flagelado, como no tiene la capacidad de sintetizar acido siálico de novo, lo capta de los glicoconjugados del hospedador para transferirlo a moléculas aceptoras tipo mucina de su propia superficie (24).
El ácido siálico es el mayor componente responsable de la carga neta negativa superficial de los tripanosomátidos (25) y se ha demostrado que está involucrado en los fenómenos de adhesión parasitaria. En la tripanosomiasis debida a T. congolense la adhesión del parásito a eritrocitos y células endoteliales es mediada por estructuras filamentosas emitidas por los tripomastigotes hematozoicos que establecen contactos con la superficie de la célula hospedadora. Se ha demostrado que estos filamentos contienen residuos de ácido siálico (26). Este fenómeno de adhesión también ha sido descrito para T. brucei con eritrocitos y plaquetas (26) y para T. evansi con glóbulos rojos (27).
Debido a que se ha demostrado que A. lumbricoides capta ácido siálico, habría que determinar cuál es el objetivo del parásito para realizar este secuestro. En este contexto, considerando las funciones del mismo, su captación podría ser utilizada para inhibir la vía alternativa del complemento (24)(28)(29), alterar los procesos de reconocimiento celular, la vida media de células y proteínas plasmáticas, modular el sistema inmune y la apoptosis celular, y/ o modificar la adhesión de moléculas cuyo ligando fuera el ácido siálico (1).
Por otro lado, la remoción de los residuos de ácido siálico del glóbulo rojo, no sólo promueve la agregación eritrocitaria, la formación de rouleaux, la disminución del flujo sanguíneo y el aumento de la viscosidad de la sangre (2), sino que también se ha comunicado que altera la superficie del glóbulo rojo, modificándola antigénica y bioquímicamente, y en consecuencia produce un incremento de la fagocitosis hepática de los eritrocitos (30).
Desde otro punto de vista, al relacionar algunos aspectos de la patología producida por A. lumbricoides con la disminución del ácido siálico eritrocitario, se debería considerar la formación de trombos ocasionados por migraciones erráticas del parásito (3) y las comunicaciones frecuentes de asociación con anemia (31-33). Por lo tanto, sería también importante determinar si la disminución de ácido siálico en el glóbulo rojo causada por el parásito, participa en la formación de trombos y en la modificación bioquímica o antigénica de la superficie eritrocitaria. Este último efecto, contribuiría al estado de anemia, aumentando la destrucción hepática de glóbulos rojos por fagocitosis.
Debido a que la captación de ácido siálico por A. lumbricoides podría afectar a una amplia diversidad de procesos biológicos, sería posible, en consecuencia, que este efecto causado por el parásito, no sólo interviniese en la patología, sino que también estuviese involucrado en la evasión de la respuesta inmune del hospedador.
CORRESPONDENCIA
DRA. PATRICIA PONCE DE LEÓN
Laboratorio de Parasitología. Dpto de Microbiología
Facultad de Cs. Bioquímicas y Farmacéuticas
Suipacha 531
2000 ROSARIO, Argentina
E-mail: tefu1958@hotmail.com
1. Previato L, Todeschini AR, Previato JO. Enfermedad de Chagas. Macromoléculas: Carbohidratos, lípidos y glucoproteínas. Disponible en: http://www.fiocruz.br/chagas_esp/cgi/cgilua.exe/sys/start.htm?sid=79. (Fecha de acceso: 10 de noviembre de 2009). [ Links ]
2. Foresto PG, D'Arrigo M, Filipini F, Gallo R, Rasia R, Valverde JR. Estudio de parámetros hemorreológicos en hipertensión esencial. Rev Fed Argent Cardiol 2002; 31: 69-73. [ Links ]
3. Beaver PCH, Jung RC, Cupp EW. Parasitología Clínica. Barcelona: Salvat; 1986. [ Links ]
4. Ponce de León P, Lebensohn N, Foresto P, Valverde J. Ascaris lumbricoides: alteration of the erythrocyte superficial charge using the Partition Method in aqueous two-phase system. Rev Inst Med trop S Paulo 2009; 51 (4): 219-21. [ Links ]
5. Mollison PL. Transfusión de sangre en Medicina Clínica. Barcelona: Reverté; 1987. [ Links ]
6. Ponce de León P, Valverde J, Zdero M. Preliminary studies on antigenic mimicry of Ascaris lumbricoides. Rev Inst Med Trop S Paulo 2000; 42: 295-6. [ Links ]
7. Fairbairn D. The in vitro hatching of Ascaris lumbricoides eggs. Canad J Zool 1961; 39: 153-62. [ Links ]
8. Geenen PL, Bresciani JB, Pedersen A, Eirksen H, Fagerholm PN. The morphogenesis of Ascaris suum to the infective third-stage larvae within the Egg. J Parasitol 1999; 85 (4): 616-22. [ Links ]
9. Shore García L, Ash L. Diagnóstico parasitológico. Buenos Aires: Médica Panamericana; 1983. [ Links ]
10. Lin M. A safe, simple and efficient cross matching using the slide polybrene method. Transfusion Today 2006; 66: 28. [ Links ]
11. Kachmar JF, Moss DV. Fundamentals of Clinical Chemistry. Philadelphia, WB Saunders Co; 1976. [ Links ]
12. Wackerly D, Mendenhall W, Scheaffer R. Estadística matemática con aplicaciones. México: Thomson Learning; 2003. [ Links ]
13. Fleiss JL, Levin B, Paik MC. Statistical Methods for Rates and Proportions. New York: Wiley and Sons; 2003. [ Links ]
14. Lehmann F, Tiralongo E, Tiralongo J. Sialic acid-specific lectins: occurrence, specificity and function. Cell Mol Life Sci 2006; 63(12):1331-54. [ Links ]
15. King TP. Lectin cytochemistry and intestinal epithelial cell biology. Londres: Pusztai A. and B Taylor; 1995. [ Links ]
16. Riquelme B, Foresto P, Relancio F, Lebensohn N, Di Tullio L, Grandfils C, et al. Evaluación de la acción de nuevos policationes sintéticos sobre las propiedades viscoelásticas de la membrana eritrocitaria. Anales AFA 2005; 17: 325-7. [ Links ]
17. Campbell NA, Reese JB, Lawrence G, M Reese. Biología: conceptos y relaciones, México: Pearson Educación; 2001. [ Links ]
18. De Chirinos SM, LichtigerB. Prueba manual de polibrene frente a prueba en salina como medio de detección de aloanticuerpos de glóbulos rojos en examen pre-transfusional. Sangre 1991; 36(1): 43-6. [ Links ]
19. Gioseffi O, Piacquadio E, Borello O, Fernández de Cieza J M. Reacción hemolítica transfusional por anticuerpo anti-JKa demostrado sólo por el método manual de baja concentración iónica y agregado de polibrene (LIM-P). Rev Argent Transfus 1985; 11(4):205-8. [ Links ]
20. Braga GW, Bordin JO, Moreira Júnior G, Kuroda A. Laboratory diagnosis of auto-immune hemolytic anemia: characteristics of the manual direct test of Polybrene. Rev Assoc Med Bras 1998; 44(1): 16-20. [ Links ]
21. Alfonso Valdez ME, Muñiz E, Bencomo Hernández A, López de Roux MR, Cruz Tamayo F, Morena Barios LM, et al. Aloanticuerpos contra células sanguíneas en embarazadas nulíparas antes y después de abortos provocados. Disponible en: http://scielo.sld.cu/pdf/hih/v24n2/hih07208.pdf. (Fecha de acceso: 20 de noviembre de 2009. [ Links ])
22. Alfonso ME, Muñiz E, Bencomo A, López de Roux R, Cruz F, Lam RM, et al. Aloinmunización contra células sanguíneas en el primer trimestre del embarazo. Rev Cubana Hematol Inmunol Hemoter [online]. 2006; 22 (2). Disponible en: http://bvs.sld.cu/revistas/hih/vol24_2_08/hih07208.htm. (Fecha de acceso: 23 de noviembre de 2009. [ Links ])
23. Biondi C, Arriaga S, Valverde J. Técnica manual utilizando bromuro de hexadimetrina (polibrene) para la determinacion de crioaglutininas. Sangre 1988; 33(4): 320. [ Links ]
24. Buscaglia C. Trans- sialidasa de Tripanosoma cruzi: un blanco potencial para el tratamiento de la enfermedad de Chagas. Rev Hosp Mat Inf Ramón Sardá 2002; 21 (1): 24-7. [ Links ]
25. Souto Padron T. The surface charge of trypanosomatids. An Acad Bras Ciênc 2002; 74 (4): 649-75. [ Links ]
26. Hemphil A, Ross CA. Flagellum-mediated adhesion of Trypanosoma congolense to bovine aorta endotelial cells. Parasitol Res 1995; 81: 412-20. [ Links ]
27. Boada Sucre A, Rossi S, Marcello S, De Stefano H. Alteraciones en el patrón de enlazamiento de lectinas en el riñón de ratones infectados experimentalmente con una cepa venezolana de Trypanosoma evansi. Rev Cient 2004; 14 (5): 431-9. [ Links ]
28. Murray PR, Rosenthal K , Pfaller MA. Microbiología Médica, Madrid : Gea Consultoría Editorial; 2006. [ Links ]
29. Chabalgoity J, Pereira M, Rial A. Inmunidad contra los agentes infecciosos. Disponible en: http://www.higiene.edu.uy/cefa/2008/Inmunidadcontralosagentesinfecciosos.pdf. (Fecha de acceso: 25 de noviembre de 2009. [ Links ])
30. Anosa VO, Kaneko JJ. Pathogenesis of Trypanosoma brucei infection in deer mice (Peromyscus maniculatus): light and electron microscopic studies on erythrocyte pathologic changes and phagocytosis. Am J Vet Res 1983; 44: 645-51. [ Links ]
31. Bardenwerper HE. Ascaris lumbricoides infestation with extreme anemia. J Am Med Assoc 1928; 91(14): 1037. [ Links ]
32. García-Leiva J, Barreto-Zuñiga R, Estradas J, Torre A. Ascaris lumbricoides and iron deficiency anemia. Am J Gastroenterol 2008; 103: 1051-2. [ Links ]
33. Amuga GA, Onwuliri COE, Oniye SJ. Relative contribution of hookworm and Ascaris lumbricoides to iron deficiency anemia among school pupils in Nasarawa area, Nigeria. Int J Nat Appl Sc 2006; 2 (3): 205-9. [ Links ]
Aceptado para su publicación el 2 de julio de 2010














