Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957
Acta bioquím. clín. latinoam. vol.45 no.1 La Plata ene./mar. 2011
PARASITOLOGÍA
El diagnóstico de la leishmaniasis cutánea: a propósito de un caso
Diagnosis of cutaneous leishmaniasis: a case report
Susana Lloveras1,a, Daniel Moreno2,b, Amadeo Javier Bava3,b, Tomás Orduna4,a
1. Médica Infectóloga.
2. Bioquímico.
3. Doctor en Medicina.
4. Médico Infectólogo.
a. Centro Municipal de Patología Regional Argentina y Medicina Tropical (CEMPRA-MT), Sala 9.
b. Sección Parasitología. Hospital de Enfermedades Infecciosas "Francisco Javier Muñiz". Uspallata 2272. (1282)Buenos Aires. Argentina.
Resumen
Se describe el caso de un paciente con leishmaniasis cutáneo-mucosa proveniente de Israel, quien viajó por regiones endémicas de esta enfermedad en América Latina durante el último año. Consultó por la presencia de lesiones úlcero-costrosas, levemente dolorosas, de 45 días de evolución, una en la región del mentón (acompañada de inflamación local y adenopatía regional submentoniana), de aproximadamente 2 cm de diámetro, y otra, más pequeña, en el borde lateral del ojo derecho. Con material tomado por escarificación de los bordes de las lesiones, se realizaron extendidos que fueron fijados y coloreados con la técnica de Giemsa. La microscopia reveló la presencia de amastigotes de Leishmania. Conocida la etiología, se inició tratamiento específico con antimonio de meglumina (Glucantime®), a razón de 20 mg/kg/día, durante 21 días, con buena tolerancia y cicatrización de las lesiones. Las lesiones de leishmaniasis cutáneo-mucosa deben incluirse en el diagnóstico diferencial de las úlceras tropicales y su diagnóstico etiológico requiere de un procedimiento sencillo, al alcance de laboratorios de baja complejidad.
Palabras clave: Leishmaniasis tegumentaria; Leishmania brasiliensis; Úlcera tropical
Summary
An Israeli patient with cutaneous leishmaniasis who had been travelling in Latin America during the previous year was described. The patient presented with two lesions, one crusty ulcer in the chin region which was slightly painful and with regional adenopathy, and a smaller ulcer in the lateral edge of the right eye. The diagnosis was established by microscopic observation of Leishmania sp. in skin scrapings stained with Giemsa. Systemic treatment with meglumine antimony (Glucantime ®), 20 mg / kg / day during 21 days was administered without adverse events and ulcer reepithelialization. Cutaneous leishmaniasis should be included in the differential diagnosis of tropical ulcers, and etiologic diagnosis requires a simple procedure, available to low-complexity laboratories.
Key words: Cutaneous leishmaniasis; Leishmania brasiliensis; Tropical ulcer
Introducción
Las leishmaniasis constituyen un grupo de enfermedades causadas por protozoarios flagelados del género Leishmania, presentes en el citoplasma de los macrófagos de humanos y otros vertebrados en la forma de amastigotes, y como promastigotes en el intestino de los dípteros vectores (1).
El ciclo biológico de Leishmania sp. se cumple en dos hospederos: uno vertebrado (el ser humano y otros mamíferos) y en la hembra hematófaga de un insecto de los géneros Lutzomya (Nuevo Mundo) o Phlebotomus (Viejo Mundo), que actúa como vector transmisor del parásito (1).
Las manifestaciones clínicas son variables y dependen de una compleja interacción entre la estructura antigénica, las características patogénicas del parásito y el sistema inmune del huésped. La enfermedad tiene cuatro formas clínicas: visceral (Kala azar), cutánea, mucocutánea y dérmica post kala-azar, causadas por diferentes especies de Leishmania.
En América, el área endémica de esta antropozoonosis, abarca desde el sur de los Estados Unidos hasta el norte de Argentina, en donde el área endémica de la leishmaniasis tegumentaria (cutánea y mucocutánea) incluye diferentes regiones de las provincias de Salta, Jujuy, Tucumán, Santiago del Estero, Chaco, Catamarca, Corrientes, Misiones y Formosa. Leishmania (V) braziliensis es la especie más frecuente en Argentina y agente etiológico de la leishmaniasis cutánea o mucocutánea (1)(2).
La conjunción de los antecedentes epidemiológicos (procedencia, residencia, viajes y/o el trabajo rural dentro de las áreas endémicas) y los hallazgos clínicos son de gran importancia en la presunción diagnóstica.
Las lesiones cutáneas de la leishmaniasis pueden ser únicas o múltiples y se presentan, en general, como úlceras de bordes elevados, indoloras, de fondo granuloso que pueden o no estar cubiertas por un exudado. Pueden cicatrizar espontáneamente en el término de semanas o meses, o persistir durante un año o más. También se pueden presentar como formas vegetantes, verrugosas, o en placas (3).
Clínicamente, puede confundirse con histoplasmosis, paracoccidioidomicosis, sífilis terciaria, frambesia o pian, carcinoma basocelular, granuloma de la línea media y ciertos linfomas. (4) Es importante tener en cuenta que las lesiones presentes en las mucosas nasal, bucal, faríngea o laríngea, pueden aparecer meses o años después que las lesiones cutáneas de primoinfección, ubicadas en el sitio de entrada del parásito, han cicatrizado (3).
El diagnóstico de certeza de la leishmaniasis cutánea se confirma cuando los amastigotes de Leishmania sp. se reconocen microscópicamente en las preparaciones convenientemente teñidas (de preferencia con la coloración de Giemsa o similares), realizadas con material clínico obtenido de las lesiones por raspado, aspirado (tomado con jeringa y solución fisiológica estéril) o biopsia del borde de las lesiones (5-7).
En laboratorios de mayor complejidad puede lograrse el desarrollo de las formas promastigotes en medios de cultivo especializados (medio NNN), a partir de las muestras antes mencionas, siendo sin embargo éste un procedimiento poco rentable por la eventual contaminación, y con una sensibilidad que oscila entre 50-70%, al igual que también puede realizarse inoculación y aislamiento posterior en animal sensible (hámster dorado) (8).
Existen métodos de diagnóstico indirecto (inmunológicos) que se basan en la detección de la respuesta inmune celular, o humoral por anticuerpos específicos, desarrollados como consecuencia de la infección. Estas técnicas son: intradermorreacción de Montenegro y la serología por ELISA/ DOT-ELISA e inmunofluorescencia indirecta. La primera, efectuada con antígeno proveniente de cultivos "in vitro" de promastigotes de Leishmania, pone de manifiesto el estado de la hipersensibilidad retardada del paciente a los antígenos del parásito (9). Produce reacciones positivas en cerca del 80-100% de los casos, aunque su valor diagnóstico es escaso, ya que puede ser negativa en pacientes enfermos con la forma anérgica de la leishmaniasis o en estadios tempranos de la misma, y positiva en personas de áreas endémicas que han estado expuestas al parásito sin enfermar o que han curado la leishmaniasis espontáneamente o con tratamiento. En las poblaciones de áreas endémicas, sin lesión activa o cicatriz, la positividad de la reacción varía entre 20-30% (10)(11). Los métodos serológicos no se utilizan de rutina, debido a la superposición con el área endémica para Chagas y la ocurrencia de reacciones cruzadas (11).
Las técnicas moleculares, basadas en la amplificación de genes, constituyen una herramienta poderosa y sensible por su elevada especificidad y tienen relevancia en la identificación de los aislamientos de Leishmania, al nivel de especie (12)(13).
Caso clínico
Paciente de sexo masculino, 22 años, oriundo del Estado de Israel, desde donde partió en julio de 2009 hacia Sudamérica. Se encontraba en el momento de la consulta en tránsito por Buenos Aires, luego de haber realizado viajes por diversas regiones de Ecuador (Quito, Galápagos, Baños y Montañita), Perú (Cuzco, Lima y Huaras), Bolivia (La Paz, Rurrenabaque, Coroico y Salar de Uyuni) y Argentina (Salta y Jujuy), Consultó el 21 de diciembre de 2009 en el Centro Municipal de Patología Regional Argentina y Medicina Tropical (CEMPRA-MT, Sala 9), del Hospital de Enfermedades Infecciosas "Francisco J. Muñiz", por la presencia de dos lesiones úlcero-costrosas de 45 días de evolución, una en la región del mentón (acompañada de importante inflamación local y adenopatía regional submentoniana), de aproximadamente 2 cm de diámetro, y otra, más pequeña, presente en el borde lateral del ojo derecho. (Figura 1). Ambas lesiones eran levemente dolorosas, en especial la ubicada en la región mentoniana. En el Laboratorio de Parasitología del mencionado Hospital se realizó la escarificación de las lesiones, obteniéndose material de los bordes, con el cual se efectuaron preparaciones microscópicas, que una vez fijadas con alcohol metílico, fueron coloreadas con Giemsa. La microscopia con objetivo de inmersión reveló la presencia, dentro de las células fagocitarias, de amastigotes de Leishmania sp (Figura 2). De manera adicional, los estudios de laboratorio general (hemograma, hepatograma, amilasemia, uremia y creatininemia) revelaron valores dentro de los límites normales y el electrocardiograma fue también normal. Una vez establecido el diagnóstico etiológico, se inició tratamiento específico con antimoniales pentavalentes (antimonio de meglumina, Glucantime ®), a razón de 20 mg/kg/día durante 21 días, con buena tolerancia del mismo y cicatrización de las lesiones.
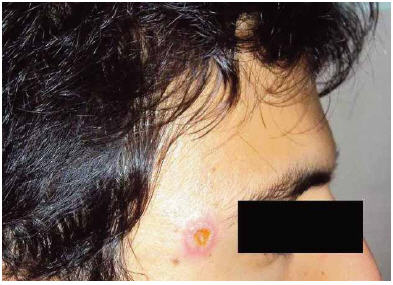
Figura 1. Lesión ulcerosa con bordes sobreelevados en el borde lateral del ojo derecho.
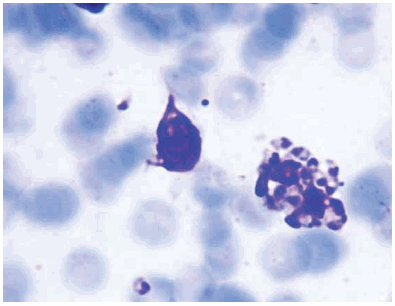
Figura 2. Amastigostes de Leishmania sp. en la preparación microscópica de material obtenido de las lesiones, teñidos con Giemsa (1.000 x).
Comentario
La leishmaniasis tegumentaria (cutánea y mucosa) constituye una patología regional endémica de extensas regiones de Argentina y del resto de Latinoamérica. Teniendo en cuenta el traslado frecuente de individuos desde y hacia estas regiones se hace necesaria la presunción clínica del cuadro, en el contexto del diagnóstico diferencial de "úlcera tropical", y el reconocimiento microbiológico del agente causal en materiales provenientes de estas lesiones, el cual requiere de un procedimiento sencillo, al alcance de laboratorios de baja complejidad.
AGRADECIMIENTOS
A las técnicas de laboratorio Luciana Rivas, Alejandra Ambrogio y Karina Funes, por su desinteresada colaboración en el procesamiento de las muestras.
CORRESPONDENCIA
DRA. SUSANA LLOVERAS
Uspallata 2272
1282 - BUENOS AIRES, Argentina
slloveras@intramed.net
1. Lainson R, Shaw JJ. Evolution, classification and geographical distribution. In: Peters W, Killick - Kendrick R, editors. The leishmaniases in biology and medicine. London: Academic Press; 1987 pp. 1-120. [ Links ]
2. Jones TC, Jhonson WD, Barretto AC, Lago E, Badaro R, Cerf B, et al. Epidemiology of American cutaneous leishmaniasis by Leishmania brasiliensis brasiliensis. J Infect Dis 1987; 156: 73-83. [ Links ]
3. Pearson RD, Sousa AQ. Clinical spectrum of leishmaniasis. Clin Infect Dis 1996; 22: 1-13. [ Links ]
4. Zeegelaar JE, Faber WR. Imported tropical infectious ulcers in travelers. J Clin Dermatol 2008; 9: 219-32. [ Links ]
5. Singh S. New development in the diagnosis of leishmaniasis. Indian J Med Res 2006; 123: 311-30. [ Links ]
6. Salomón OD, Sosa Stani S, Canini L, Córdoba Lanús E. Leishmaniasis tegumentaria en un área con niveles epidémicos de transición, Salta, Argentina. Medicina (Buenos Aires) 2001; 58: 685-91. [ Links ]
7. Murray HW, Berman JD, Davies CR, Saravia NG. Lancet 2005; 366: 1561-77. [ Links ]
8. Cuba Cuba CA. Diagnóstico parasitológico de la leishmaniasis tegumentaria americana. Rev Med Exp 2000; 17: 39-52. [ Links ]
9. Kalter DC. Laboratory tests for the diagnosis and evaluation of leishmaniasis. Dermatologic Clinics 1994; 12: 37-50. [ Links ]
10. Manual de Vigilancia da Leishmaniose Tegumentar Americana / Ministerio da Saude, Secretaria de Vigilancia em Saude, Departamento de Vigilancia Epidemiologica. 2a ed. Brasilia: Editora do Ministerio da Saude, 2007. 182 p. (Serie A. Normas e Manuais Tecnicos). [ Links ]
11. Resolución Nº 898/02 Programa Nacional de Garantía de Calidad de la Atención Medica. El Manual de Procedimientos de Nivel Gerencial y Profesional sobre leishmaniasis. Buenos Aires. Revisión 2006. [ Links ]
12. Tavares CAP, Fernández AP, Melo MN. Molecular diagnosis of leishmaniasis. Expert Rev Mol Diagn 2003; 3: 657-67. [ Links ]
13. Barrio A, García Bustos MF, Mora MC, Parodi CM, Ramos F, Moreno S,.Basombrío MA. Identificación por PS-PCR de especies de Leishmania y su correlación con características clínicas, epidemiológicas y terapéuticas en Salta, Argentina). Rev Argent Salud Pública 2009; 1: 30-3. [ Links ]
Aceptado para su publicación el 8 de noviembre de 2010














