Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957
Acta bioquím. clín. latinoam. vol.45 no.4 La Plata oct./dic. 2011
Homenajes
Reconocimiento a la trayectoria institucional del IBYME
Relato histórico del Instituto de Biología y Medicina Experimental
Eduardo Charreau
El IBYME nace en un momento de incomprensión e intolerancia en la vida político-científica argentina.
El 16 de octubre de 1943, poco antes de mediodía, la radio anunció que el gobierno había resuelto dejar cesantes a los profesores universitarios y demás firmantes de un manifiesto publicado en los diarios del día anterior, en el que se expresaban anhelos de democracia efectiva y solidaridad americana. Pero también es cierto que el IBYME surgió del altruismo y la buena voluntad de gente comprometida con la Argentina.
Alrededor de las tres de la tarde del 18 de octubre, el Profesor Bernardo A. Houssay recibió la visita de dos caballeros que ofrecieron ayuda pecuniaria para que él y su equipo prosiguieran con entera libertad las investigaciones desinteresadas, en vista de que el equipo de investigaciones había quedado privado de trabajo. Creían de esta forma servir al país.
La proposición fue formulada por el Dr. Miguel F. Laphitzondo y el Sr. Pablo F. Perlender en su nombre y en el del Sr. Fernando Capdevielle y el Ing. Carlos Sauberan, todos ellos en memoria de Juan Bautista Sauberan.
Casi simultáneamente, Houssay y sus colaboradores recibieron numerosos ofrecimientos, para ocupar cátedras o posiciones en Uruguay, Chile, Brasil y los Estados Unidos, pero aunque eran tentadores prefirieron la proposición de nuestros compatriotas porque creyeron que era su deber seguir luchando en el país, por su adelanto científico y la formación de investigadores, obra a la cual habían consagrado sus vidas a pesar de constantes dificultades. Testimonio elocuente de ello es la carta que el Dr Houssay le dirige desde Washington a un amigo: "...Nos quieren hacer quedar y hasta ofrecen traer todo el personal de Buenos Aires, si quiero... Los recursos son amplios, la gente amable, ávida para aprender, llena de interés científico. Pero no olvido que mi vida está consagrada a cosas casi imposibles, muchas de las cuales y otras inesperadas han ido llegando. Quiero dedicarme al desarrollo científico del país donde nací, me formé, tengo amigos, nacieron mis hijos, luché, aprendí, enseñé, etc.".
Esta extraordinaria fidelidad y compromiso con la Argentina se hace más admirable si se contempla desde la óptica de las circunstancias del momento, la tensión, angustia e incertidumbre sobre el futuro, en el cual peligraba la tranquilidad personal y familiar.

Dr. Bernardo A. Houssay Director: 1944-1970
Fue precisamente en esos días de conflictos que Houssay redactó ese tipo de "credo" ampliamente divulgado, en el que expresaba sus convicciones con firmeza.

El sueño de Houssay de fundar un Instituto privado de investigación, que no existía en el continente, dedicado al estudio de los problemas fundamentales de la medicina y biología, comenzaba a hacerse realidad y así se refería a ese proyecto: "Este Instituto es una de las iniciativas más importantes realizadas en el país para establecer un centro de investigaciones científicas de carácter privado e independiente de recursos del gobierno." y agregaba: "estamos convencidos que este Instituto debe tener vida permanente para lo cual deberán hallarse recursos y asignarle un personal competente y consagrado".
La primera gran dificultad fue encontrar un lugar adecuado para su establecimiento y les correspondió a los Dres. Braun Menéndez y Foglia esa tarea preliminar.
Si bien las circunstancias eran favorables para adquirir o alquilar una vivienda con las comodidades que se requerían, ya que muchas familias estaban deseosas de reducir sus espaciosas mansiones, tan pronto como se enteraban del posible destino del inmueble, la negociación terminaba. Laboratorio era para la época sinónimo de explosión, y bioterio, ratas y perros, por consiguiente ruidos y olores.
Según contara el Dr. Foglia, quien más sufrió la ansiedad provocada por este forzoso período de espera fue la esposa de Houssay, doña María Angélica Catán, que veía a su esposo abatido por no poder continuar con su trabajo experimental y les suplicó que encontraran urgente un lugar para laboratorio como única alternativa terapéutica.
Finalmente, lo tan anhelado se concretó en una casona de Costa Rica 4185. El garaje situado en la esquina y separado de la casa por un jardín cubierto de arbustos y árboles se transformó en bioterio central. En el piso superior nacieron tres laboratorios; en el central el comedor se transformó en biblioteca y sala de lectura y hubo espacio suficiente para otros tres laboratorios y dos escritorios. En el sótano, la cocina fue laboratorio de histología y lamentablemente la bodega, bioterio secundario.
Rápidamente comenzaron a recibirse donaciones de profesores universitarios, ciudadanos, empresarios, Fundaciones y Laboratorios Farmacéuticos con amplia generosidad. Con los fondos adquiridos se compraron equipamiento, instrumentos y reactivos. La biblioteca se inició con los libros y publicaciones de los fundadores que vieron rápidamente completarse con donaciones realizadas por los fisiólogos Cannon, Evans, Fulton y Wiggeers quienes junto a otros organizaron en Estados Unidos el Committee on the Houssay Journal Fund, con el que se pagaron suscripciones de 18 revistas por cinco años y se adquirieron numerosos libros.
El trabajo mayor se había completado y el Instituto de Biología y Medicina Experimental comenzaba a funcionar regular y oficialmente el 14 de marzo de 1944, sólo cuatro meses después de haber decidido su creación; integrado inicialmente por los doctores Bernardo A. Houssay, Juan T. Lewis, Oscar Orías, Eduardo Braun Menéndez y Virgilio G. Foglia luego se incorporaron Carlos Martínez, Roberto Pinto, José G. Sara, E. Moisset de Espanés y Dora Potick.

Miembros del IBYME en 1945
Con guardapolvo blanco, de izquierda a derecha:
1ra. fila: E. Braun Menéndez, O. Orias, B.A. Houssay, J.T. Lewis; 2da. fila: G. Sara, C. Martínez, R. M. Pinto, V. G. Foglia; 3ra. fila: A. Bernárdez
Muchas personas del país y del extranjero pidieron trabajar en el Instituto, pero sólo fue posible aceptar contados casos, debido fundamentalmente a limitaciones de espacio, situación que aún hoy persiste. No obstante ello, una brillante generación de científicos argentinos y extranjeros participaron del establecimiento del IBYME y de su progreso: E. Chiodi, S. Gitter, M. R. Covian, C. Cardini, A. Paladini, R. Caputto, M. Burgos, C. T. Rietti, R. Gerchman, R. R. Rodriguez, E. De Robertis, R. Mancini, P. Bazerque, H. Prieto Díaz, J. M. Afani, E. Porta, E. Urgoiti, J. C. Penhos, A. di Pietro, E. Ashkar, A. O. Donoso, F. Stefano, M. Barontini, G. Waserman, H. Hartmann, E. M. Krieger, E. Marusic, R. O. Scout, Ulf S. von Euler, y otros.
Nuestro especial agradecimiento a todos ellos.

Premio Nobel de Fisiología y Medicina, 1947

Medalla
En 1946 el edificio es comprado por Mauricio Braun Menéndez y un comité de ayuda coordinado por Joaquín de Anchorena, Pedro Baliña, Marcelino Herrera Vegas y Jorge M. Bullrich obtiene numerosos fondos para financiar las actividades.
Seguramente el año 1947 dejó marcas imborrables en aquellos que trabajaban en el Instituto.
Permítanme suponer que la vida transcurría quizá en ritmo provinciano, siguiendo una plácida rutina diaria, cuando repentinamente ocurrió el sobresalto de una noticia fantástica. Houssay había sido distinguido con el premio Nobel de Fisiología por sus contribuciones al conocimiento de la influencia de la hipófisis en el metabolismo de los hidratos de carbono. La prensa de la época dio escasa divulgación a esta noticia y por curiosidad quise informarme cómo había sido registrado en las memorias del IBYME este acontecimiento, que no sólo era una distinción sobresaliente como tributo a su carrera científica sino que también constituía un honor para la Argentina, que por primera vez en su historia obtenía tan importante premio en Ciencias.
Con enorme sorpresa transcribo la única mención que se refiere a tal acontecimiento: "Los miembros del Instituto han recibido distinciones significativas entre las que figuran el Premio Nobel de Fisiología y Medicina de 1947 acordado al Dr. Bernardo A. Houssay".
El 23 de septiembre de 1949, el Superior Gobierno Nacional por decreto 23.551, reconoce a nuestro Instituto como Fundación con persona jurídica de existencia posible que tiene por principal objetivo el bien común. La medida tiene efecto retroactivo al 14 de marzo de 1944, día de la creación original. El primer triunvirato directivo estuvo integrado por Bernardo Houssay, Eduardo Braun Menéndez y Virgilio Foglia.
Hasta 1955 el personal científico técnico y auxiliar fue subvencionado con fondos privados, pero a partir de entonces y en forma progresiva, los fondos fueron aportados por la Universidad de Buenos Aires que lo reconoce en 1959 como Instituto de Investigaciones de su competencia al designar al Dr Bernardo A. Houssay Profesor de Investigaciones en Fisiología, dependiente primeramente del Rectorado y posteriormente en 1973 de la Facultad de Medicina. En este año, establece asociaciones legales con el CONICET del que depende casi totalmente desde hace 38 años.

Sede, en Vuelta de Obligado 2490, 1959
Las necesidades de espacio fueron apremiantes y el local no resultó suficiente para el crecimiento de la Institución. En 1959, el Ministerio de Asistencia Social y Salud Pública proporcionó un edificio más amplio en la calle Vuelta de Obligado 2490 y gracias a un subsidio del Gobierno Nacional e innumerables donaciones privadas se logró terminar de arreglar las instalaciones. Allí funcionamos desde entonces.

Dr. Virgilio Foglia Director: 1971-1993
El 16 de enero de ese año, (día en que cumplía 56 años) el Profesor Eduardo Braun Menéndez perdía la vida en un trágico accidente de aviación. Hombre eminente de ciencia cuyo nombre quedó vinculado para siempre a adelantos importantes de la Fisiología y Medicina experimental, fue uno de los puntales de este Instituto y era uno de los hombres más brillantes y progresistas de nuestra Universidad, cuyos problemas y orientaciones conocía como pocos y por cuyo adelanto bregó incesante e infatigablemente. Su posición en el colegiado Directivo fue ocupada por Luis F. Leloir.

Dr. Luis Federico Leloir Director: 1970-1971
Houssay continuó en la dirección del Instituto hasta aproximadamente un año antes de su fallecimiento en 1971, convencido de que los científicos tienen patria y por ella deben trabajar. Desarrolló investigación científica donde no existía, probando la falsedad de los prejuicios que declaraban la imposibilidad de investigar donde las dificultades económicas parecían insuperables. Durante ese año, ocuparon la dirección interina Luis Federico Leloir y Virgilio Foglia, quien asume la dirección efectiva el 22 de septiembre de 1971. El 15 de enero de 1973, la doctora Julia V. M. Uranga es incorporada al triunvirato directivo.
La década del ochenta encontró nuevamente al Instituto limitado en espacios y presionado por una generación de jóvenes que crecían, acompañando al conocimiento del siglo. Fue entonces cuando el CONICET y la cooperación efectiva de un nuevo comité de Ayuda coordinado por el Dr. Jorge Blaquier, por entonces investigador de Instituto y artífice de lo logrado, y la invalorable colaboración de los señores Federico Amadeo, Fredy Cameo, Sergio Enaudi, Mario Piñeiro, Oscar Puiggrós y Mario Vazquez, hicieron posible la ampliación edilicia inaugurada en 1983.
No sólo los avatares políticos influyeron en la historia del IBYME. Una madrugada de enero de 1985, la fuerza incontenible del agua, como consecuencia de un temporal, arrasó con instalaciones, equipamiento y protocolos de gran parte del IBYME.
Motivados por la adversidad y herederos de un pasado de esfuerzos, los miembros del Instituto reconstruyeron lo dañado y continuaron trabajando con el entusiasmo de siempre quizá aunque en forma inconsciente para que sea verdad el postulado de los fundadores "La mejor manera de convencer a los demás es predicar con el ejemplo".

Nuevo edificio del IBYME inaugurado en 1983

Un laboratorio del subsuelo del edificio nuevo luego de la inundación de 1985
El fallecimiento del Dr. Luis Federico Leloir en 1987 y el crecimiento del Instituto, ocasionaron la necesidad de aumentar el número de miembros de la Comisión Administradora. Esto trajo como resultado la presentación ante la Dirección General de Personas Jurídicas, de una Reforma de Estatutos. Desde entonces y mientras se resolvía dicho pedido, colaboraron con la administración juntamente con el Dr. Virgilio Foglia y la Dra. Julia Uranga, los Dres. Alberto Baldi, Jorge Blaquier, Ricardo Calandra, Eduardo Charreau, Alejandro De Nicola, Enrique Segura, Alicia Roldán, Enrique del Castillo y Marta Tesone.

Dr. Eduardo H. Charreau Director: 1993-2002 / 2008-2010

Dr. Alejandro F. De Nicola Director: 2002-2008
El 7 de agosto de 1991 Eduardo Charreau es designado por los doctores Foglia y Uranga para integrar la terna administradora, ocupando el lugar dejado por el doctor Leloir. A la renuncia de la Dra. Julia Uranga en 1992, el Dr. Alejandro F. De Nicola completa el colegiado.
El 15 de julio de 1993 falleció el Dr. Virgilio G. Foglia. Con su desaparición, la ciencia argentina perdía a uno de sus firmes propulsores durante más de medio siglo y al último miembro fundador del Instituto de Biología y Medicina Experimental. Su carácter amable, su entusiasmo, su incansable dedicación al trabajo (concurrió al Instituto hasta el último día previo a su desaparición desarrollando la actividad diaria con su habitual dinamismo), le valieron el aprecio de todos los que acompañamos su gestión. Con su partida se cierra un capítulo brillante de la Ciencia Argentina.
Eduardo Charreau asume la posición de presidente de la Fundación Instituto de Biología y Medicina Experimental y de Director ante el CONICET del Instituto de Biología y Medicina Experimental de doble dependencia Fundación IBYME-CONICET. El Dr. Alejandro F. De Nicola ejerce la vice-Dirección y el Dr. Alberto Baldi se incorpora como miembro permanente del Colegiado Directivo, incorporándose como miembros transitorios los Dres. José Lino Barañao, Damasia Becú y Juan Carlos Calvo, posiciones previstas en la modificación estatutaria aprobada el 4 de septiembre de 1992.
La posibilidad de favorecer la participación institucionalizada del sector científico tecnológico en el asesoramiento al sector productivo de bienes y servicios, sean públicos o privados, en la selección y adaptación de tecnologías disponibles y en la transferencia de los resultados de la investigación, propulsó la solicitud para la aprobación de la Fundación Instituto de Biología y Medicina Experimental como Unidad de Vinculación Tecnológica (UVT), otorgada por la resolución 314 del 12 de junio de 1993, de la entonces Secretaría de Ciencia, Tecnología e Innovación Productiva. Fue la primer UVT registrada al amparo de la ley de Transferencia de Tecnología.
En la subsecuente renovación de autoridades que tuvo lugar el 20 de diciembre de1996 los Dres. Juan Carlos Calvo, Carlos Libertun y Ricardo Calandra fueron electos como vocales.
En virtud de la designación del Dr. Eduardo Charreau en el cargo de Presidente del Directorio del CONICET (decreto Nº 255/2002 del 8 de febrero de 2002), pasó a desempeñarse como presidente interino de la Fundación y vicedirector a cargo del Instituto el Dr. Alejandro F. De Nicola, acompañado por los Dres. Alberto Baldi, Juan Carlos Calvo, Claudia Lanari y Damasia Becú.

Dra. Damasia Becú Directora: Desde 2010
En las elecciones de fines de 2004 la Dra. Patricia Cuasnicú reemplazó al Dr. Juan Carlos Calvo y en 2006 Victoria Lux reemplaza a Claudia Lanari, en 2008 Juan Carlos Calvo sustituye a la Dra. Victoria Lux.
Con motivo de la finalización de la designación de Presidente del CONICET, el 8 de abril de 2008 el Dr. Eduardo H. Charreau reasume la dirección del Instituto y el Dr. De Nicola la vicedirección.
Con el alejamiento del Dr. Eduardo Charreau de la dirección del IBYME, el CONICET junto con la fundación IBYME, mediante concurso, designa a la Dra. Damasia Becú Directora por el término de cuatro años, quien elige al Dr. Gabriel Rabinovich como vice-Director. El Dr. Charreau reasume como Presidente de la Fundación Instituto de Biología y Medicina Experimental.
Asimismo, en el mes de diciembre de 2010 una nueva elección define la constitución del Colegiado Directivo de la Fundación IBYME de la siguiente manera: Eduardo H. Charreau como Presidente, Alejandro F. De Nicola como secretario, Alberto Baldi como tesorero y los doctores Juan Carlos Calvo, Victoria Lux-Lantos y Gabriel Rabinovich como vocales. Este mismo cuerpo actúa como Consejo Directivo del Instituto de Biología y Medicina Experimental dirigido por la Dra. Damasia Becú.
Es también la hora del recuerdo y del halago para los que custodiaron el esfuerzo de los que hoy son honrados. Es por ello que deseamos hacer nuestro sincero homenaje a Francisco Gómez, celoso custodio del patrimonio material del IBYME desde 1946 a 1980, a Josefina Yanguas, que no sólo fue la más eficiente administradora de la Fundación desde 1946 a 1992, sino que también nuestra constante consejera, amiga leal y generosa. A nuestra querida Zulema Rinaldo quien fuera desde 1949 hasta el 2005 el alma de la biblioteca y la más eficiente secretaria administrativa de la Sociedad Argentina de Biología, con sede en el IBYME.
El IBYME creció en espíritu y en obras, de aquel pequeño grupo que le dio origen, más de tres centenares usufructuamos hoy su obra y al cumplir 67 años con la ciencia, corona su trayectoria con alrededor de 3000 publicaciones de alcance internacional, 6000 presentaciones orales de sus trabajos científicos y varias centenas de tesis doctorales. Testimonio elocuente de la calidad de entrenamiento desarrollado, es el número de profesores que, formados en el IBYME fueron simiente de conocimientos en otros lugares del país y del extranjero, sumado a ello, el reconocimiento internacional que nuestra Institución tiene como centro de excelencia.

Miembros del IBYME

Nuevos laboratorios 2011
En la actualidad 82 investigadores de carrera, 97 becarios, 36 técnicos, 45 pasantes, 27 consultores y administrativos y 15 auxiliares de servicios, componen el plantel de trabajo. Cuarenta y siete miembros del IBYME realizan docencia de grado y postgrado en Universidades Argentinas, ocupando 17 de ellos las posiciones académicas más destacadas de nuestro sistema universitario.
El incremento de los recursos humanos del IBYME, sin duda debido a una agresiva política nacional al respecto, lo han llevado a una nueva crisis de infraestructura. Así, con la colaboración público-privada entre el CONICET y las Fundaciones Sales, Bunge y Born, IBYME, Cherny y aportes desinteresados de particulares como los del empresario Jorge Ferioli, y las señoras Silvia de Ostri, Raquel Oddone de Ostri, Patricia y Emilse Ostri y María Elvira Varela, se ha logrado edificar

Nueva Biblioteca 2011
alrededor de 2500 metros cuadrados cubiertos de áreas destinadas a nuevos laboratorios, biblioteca y servicios, permitiendo repatriar a 8 investigadores y lograr la expansión natural interna de otros tantos grupos que crearán unidades de investigación independientes.
Los fines del Instituto pueden agruparse en cuatro categorías:
1) investigaciones básicas y aplicadas en fisiología, bioquímica y biología molecular;
2) entrenamiento de estudiantes y becarios pre y posdoctorales;
3) realización de cursos de nivel de pre y posgrado; y
4) desarrollos biotecnológicos y transferencia de tecnologías.
Históricamente, los principales descubrimientos fueron en el campo de la Fisiología y la Endocrinología. Las áreas actuales incluyen Neurociencias, Biología de la Reproducción, Oncología Experimental e Inmunología. Los resultados se publican en revistas de jerarquía internacional, que demuestran el nivel de excelencia alcanzado por los distintos grupos de investigación de esta Institución.
El Instituto de Biología y Medicina Experimental cuenta en la actualidad con 21 grupos de investigación independientes cuyos objetivos e integrantes son:
LABORATORIO DE ESTEROIDES
Director del laboratorio:
Ricardo Saúl Calandra
Integrantes: Silvia Gonzalez-Calvar, Mónica Frungieri, Susana Rulli, Betina Gonzalez, María Matzkin, Laura Ratner, Soledad Rossi, Guillermina Stevens
El grupo de investigación estudia los fenómenos reproductivos a nivel fisiopatológico, que permitirán esclarecer los mecanismos bioquímicos y moleculares involucrados en las interacciones entre los factores endógenos intratesticulares, impulsando el desarrollo de nuevos protocolos enfocados a la optimización de la actividad reproductiva en especies fotoperiódicas de relevancia ganadera (ej.: oveja, cabra).
Por otro lado, los resultados obtenidos en estudios realizados en muestras humanas permitirán desarrollar nuevos enfoques en el tratamiento de patologías que involucran los cuadros denominados como Infertilidad Idiopática Masculina.
La disponibilidad de un modelo de ratones transgénicos que sobreexpresa hCG permitirá estudiar los mecanismos que conducen a una alteración del eje hipotálamo-hipófiso-gonadal y al desarrollo de tumores gonadales.
En cuanto a transferencia del conocimiento, cabe destacar que los integrantes de este Laboratorio participan activamente en el dictado de Cursos de pre y post-grado (UBA, Universidad Austral, etc) y en la dirección de una Maestría en Fisiopatología Endocrina (Facultad de Ciencias Biomédicas, Universidad Austral, Acreditada por CONEAU).
LABORATORIO DE MECANISMOS MOLECULARES DE LA FERTILIZACIÓN
Director del laboratorio:
Patricia S. Cuasnicu
Integrantes: Débora Cohen, María Agustina Battistone, Juan Ernesto, Mariana Weigel-Muñoz, Claudio Augusto Curia, Vanina Da Ros
Nuestros estudios permitirán una mayor comprensión del proceso por el cual un espermatozoide interactúa con el ovocito brindando información esencial tanto para el desarrollo de nuevas técnicas de regulación de la fertilidad como para el diagnóstico y tratamiento de los problemas de infertilidad humana.
LABORATORIO DE FISIOLOGÍA OVÁRICA
Directora del laboratorio
Marta Tesone
Integrantes: Fernanda Parborell, Griselda Irusta, Dalhia Abramovich, Fátima Hernández, Leopoldina Scotti, Diana Bas
En los últimos años la angiogénesis ha sido estudiada con intensidad, ya que está involucrada en condiciones patológicas como el cáncer y en enfermedades reproductivas como ser la Poliquistosis Ovárica (PCOS) y el Síndrome de Hiperestimulación Ovárica (OHSS). El esclarecimiento de este proceso sin duda redundará en el tratamiento de estas enfermedades al explorar nuevas estrategias terapéuticas.
LABORATORIO DE ENDOCRINOLOGÍA MOLECULAR
Director del laboratorio:
Eduardo Charreau
Integrantes: Liliana Dain, Violeta Chiauzzi, Cecilia Fernandez, Ianina Ferder, Melisa Taboas, Ana Rosa De La Cámara
En las últimas décadas los países desarrollados han experimentado un proceso de transición epidemiológica, caracterizado por el creciente control de la desnutrición y las enfermedades infectocontagiosas y el incremento relativo de las afecciones crónico-degenerativas. Aunque el mundo subdesarrollado aún se enfrenta a las llamadas enfermedades de la pobreza, en ciertas naciones las enfermedades crónicas y los trastornos genéticos comienzan a ser un problema de salud pública. En Argentina, donde la mortalidad infantil (MI) es de 13,3 por mil, los defectos congénitos constituyen su segunda causa, explicando el 25,1% de la MI total.
Los defectos congénitos incluyen a las alteraciones morfológicas (malformaciones congénitas) y/o funcionales presentes en la infancia o en etapas posteriores de la vida y causados por eventos que preceden al nacimiento, heredados o adquiridos durante la vida prenatal. Los defectos congénitos que pueden identificarse al nacimiento son generalmente las malformaciones y tienen una prevalencia de aproximadamente 3%. Sin embargo, debido al diagnóstico de impedimentos fisiológicos y mentales de aparición más tardía, la prevalencia de estos defectos asciende al 8% a los 5 años de edad. Por otra parte, ciertas afecciones congénitas se manifiestan en la edad adulta, incluyendo tanto enfermedades genéticas de baja frecuencia, como enfermedades comunes de origen multifactorial (enfermedades cardiovasculares y neurodegenerativas, cáncer, etc.), responsables de la mayor parte de la morbimortalidad actual.
El gran desarrollo tecnológico de los últimos años ha permitido llevar a cabo diversos estudios moleculares de enfermedades genéticas gracias a los cuales se han podido identificar muchos genes involucrados en la etiopatología de varios desórdenes de origen exclusivamente genético, así como proponer genes asociados a enfermedades de origen parcialmente genético o multifactorial.
Por otra parte, investigaciones epidemiológicas han sugerido que los diferentes tipos de defectos congénitos y las frecuencias con que los mismos se presentan, varían entre poblaciones según la distribución geográfica y el origen étnico de las mismas. De manera similar, los estudios moleculares han demostrado que las variantes alélicas supuestamente relacionadas con genes de predisposición pueden ser diferentes según el acervo genético de las poblaciones. Estas observaciones han conducido a la necesidad de realizar estudios genéticos-moleculares para cada población en particular con el propósito de determinar los factores de riesgo que se asocian con estas patologías.
En muestro laboratorio proponemos estudiar genes implicados en la etiología de enfermedades de origen monogénico y multifactorial en nuestra población. Se enfoca el estudio en dos enfermedades relacionadas con el sistema reproductivo y endócrino: la deficiencia de 21-hidroxilasa y la falla ovárica prematura (FOP). La deficiencia de 21-hidroxilasa es la enfermedad autosómica recesiva de mayor incidencia. Por su parte, dentro de las enfermedades de origen multifactorial, la FOP afecta al 1% de las mujeres en edad fértil. Los estudios comprenden la identificación de variantes asociadas a estas enfermedades, así como estudios de las consecuencias fisiopatológicas de los genes implicados en ellas.
LABORATORIO DE INMUNOLOGÍA DE LA REPRODUCCIÓN
Directora del laboratorio:
Rosa Inés Barañao
Integrantes: Gabriela Meresman, Mariela Bilotas, Analía Ricci, Carla Olivares, Juan Ignacio Bastón
La endometriosis se define como la presencia de tejido endometrial fuera de la cavidad uterina. Esta enfermedad afecta a un 10-15 % de mujeres en edad reproductiva. Los dos síntomas más comunes de la endometriosis son el dolor y la infertilidad que se manifiesta como dispareunia, dismenorrea o dolor abdominal crónico. Este dolor puede ser tan intenso que afecte la calidad de vida de la mujer, desde sus relaciones hasta sus actividades diarias. Por otra parte, alrededor de un 30 a 40% de las mujeres con endometriosis son infértiles, por lo cual es una de las tres principales causas de infertilidad femenina.
Nuestros estudios tienen como objetivo la evaluación del efecto in vitro e in vivo de nuevas alternativas terapéuticas para tratar esta patología con el fin de hallar tratamientos más simples, con medicamentos que actúen en forma más directa sobre los implantes, que inhiban los mecanismos involucrados en el desarrollo de la enfermedad, y que potencialmente sean más eficaces en su acción de erradicar las lesiones endometriósicas.
En nuestro modelo murino evaluamos también la relación entre endometriosis e infertilidad y hemos comenzado el estudio de los posibles mecanismos involucrados en la tolerancia inmunológica hacia los implantes de tejido endometrial ectópico que se produciría durante el establecimiento de la endometriosis.
LABORATORIO DE ENDOCRINOLOGÍA MOLECULAR Y TRANSDUCCIÓN DE SEÑALES
Director del laboratorio:
Omar P. Pignataro
Integrantes: Carolina Mondillo, Marcos Besio Moreno, Romina Pagotto, Casandra Monzón
REGULACIÓN DE LA FUNCIÓN ESTEROIDOGÉNICA EN TESTÍCULO Y GLÁNDULA ADRENAL
Las hormonas adenohipofisarias LH (luteinizante) y ACTH (adrenocorticotrofina) son los factores tróficos principales de la esteroidogénesis testicular y adrenal, respectivamente.
Sin embargo, debido a que en ambos órganos hay diferentes poblaciones celulares, éstas secretan factores que son capaces de regular las acciones mencionadas.
Nuestro grupo de trabajo ha demostrado que los sistemas óxido nítrico sintasa/óxido nítrico (NOS/NO) y hemo oxigenasa/monóxido de carbono (HO/CO), y la histamina (HA) modulan los efectos de las hormonas adenohipofisarias mencionadas, en ambos sistemas.
Tanto en testículo como en la corteza suprarrenal, los factores descriptos pueden actuar a través de distintos (o similares) mecanismos de transducción para activar o inhibir la síntesis de esteroides, a nivel del camino esteroidogénico y/o en la expresión de la proteína StAR, regulatoria en el transporte de colesterol a la mitocondria. Además de la conocida participación del AMPc en la transducción de la señal de ambas hormonas hipofisarias, otros segundos mensajeros pueden estar involucrados en la respuesta biológica final.
Sin duda, la existencia de interacciones celulares locales capaces de modular las acciones de LH y ACTH, provee un eficiente mecanismo de regulación de las funciones testicular y adrenal, evitando la generación de respuestas de tipo todo o nada y permitiendo a las glándulas responder en forma fina y ajustada a los distintos estímulos, sean éstos fisiológicos o patológicos. Así, el objetivo general del proyecto es el estudio de la regulación de la esteroidogénesis en testículo y glándula adrenal por factores producidos localmente: HA, NO y CO, la interrelación entre los mismos y los mecanismos moleculares involucrados. Asimismo, se evalúa la posible participación de dichos factores como moduladores de la proliferación y/o diferenciación de las células esteroidogénicas,
Los resultados obtenidos permitirán lograr una mejor comprensión de los procesos relacionados con la fertilidad humana y con la producción de hormonas esenciales para la vida.
LABORATORIO DE ESTUDIOS DE LA INTERACCIÓN CELULAR EN REPRODUCCIÓN Y CÁNCER
Directora del laboratorio:
Mónica H. Vazquez-Levin
Integrantes: Clara Marin-Briggiler, María Laura Matos, Lara Lapyckyi, Marina Rosso, María Matilde Arzondo, Nadia Edelsztein, María José Besso
El grupo de investigación estudia las bases moleculares de los mecanismos involucrados en la adhesión celular, así como los eventos que se desencadenan como resultado de las interacciones célula-célula en procesos fisiológicos y patológicos.
Nuestro interés actualmente se centra en el estudio de miembros de la familia de cadherinas clásicas y moléculas relacionadas, utilizando gametas de diversas especies (humano, murino y bovino), así como en líneas celulares establecidas, en muestras de tejidos no tumorales y tumorales de diversos orígenes y más recientemente en células stem de origen embrionario. Para nuestros estudios utilizamos estrategias celulares, bioquímicas, moleculares y estudios funcionales y colaboramos con referentes nacionales e internacionales de trayectoria en los temas de estudio.
Los hallazgos de nuestros estudios podrán contribuir a comprender las bases moleculares de procesos tan importantes como lo son la fecundación y la progresión tumoral. Esperamos, asimismo, con nuestros estudios contribuir a mejorar el diagnóstico de la infertilidad y de la patología del cáncer y, eventualmente, proponer alternativas para su tratamiento.
LABORATORIO DE BIOTECNOLOGÍA ANIMAL Y FISIOLOGÍA DE LA GLÁNDULA MAMARIA
Director del laboratorio:
Leonardo Bussmann
Integrantes: Inés Bussmann, Ursula Bussmann, Juan Manuel Perez Saez.
PÉPTIDOS ANTIMICROBIANOS EN LA RESISTENCIA A LA MASTITIS
La mastitis es la inflamación de la glándula mamaria producida predominantemente por la infección bacteriana a través del conducto del pezón. La mastitis bovina es una de las enfermedades de mayor impacto económico para la actividad lechera. La glándula mamaria responde a las infecciones con mecanismos específicos y no específicos. Los mecanismos no específicos constituyen la forma de defensa en los estadios tempranos de la infección e involucran, entre otros, a péptidos y proteínas como la lactoferrina (LF) y las defensinas. La digestión de LF genera distintos péptidos, como por ejemplo la lactoferricina (LFcin), siendo algunos de ellos aún más eficientes que la molécula original contra patógenos mamarios. El objetivo de esta línea de investigación es lograr nuevos enfoques de diagnóstico, prevención y tratamiento de la mastitis bovina a través del uso de moléculas con acción antimicrobiana como LF y LFcin, aunque no de manera excluyente. La expresión recombinante de análogos de LFcin en la glándula mamaria como forma de obtener leche diferenciada con acción antibiótica local y como alimento funcional aparece como un logro de gran atractivo tanto científico como tecnológico. Dado que el péptido tendrá mayor actividad desde su secreción en la glándula mamaria, los potenciales animales transgénicos que expresen este péptido serán altamente resistentes a la mastitis, disminuyendo la utilización de antibióticos en los tambos y brindando los consecuentes beneficios para la salud humana y el medioambiente. Por otro lado, dadas las características extraordinarias de los péptidos derivados de la LF en cuanto a sus propiedades nutracéuticas, esta leche será altamente beneficiosa para el consumidor, modulando el sistema inmune, colaborando con la prevención del desarrollo de tumores y combatiendo infecciones en el tracto digestivo.
DESARROLLO DE MÉTODOS PARA LA GENERACIÓN DE GALLINAS TRANSGÉNICAS COMO BIORREACTORES
La producción de animales transgénicos que expresen proteínas terapéuticas permite la producción de moléculas de interés por medios a largo plazo más económicos que la obtención por métodos tradicionales (expresión en líneas celulares/bacterias). A su vez, en numerosos casos la molécula de interés producida en animales transgénicos es mejor y más apta, o muchas veces es la única opción de obtener las modificaciones post-transduccionales necesarias. Actualmente se han podido obtener en nuestro país vacas que expresan proteínas terapéuticas en su glándula mamaria; sin embargo, el uso de vacas, ovejas o cabras para tales fines resulta en un proceso costoso que exige una alta inversión en tiempo y en dinero para poder conseguir un significativo plantel productor de la molécula de interés. Frente a esta dificultad, las aves transgénicas se presentan como una alternativa muy atractiva, pues poseen una serie de grandes ventajas que las convierten en excelentes posibles biorreactores para la industria farmacéutica. El impacto de la realización del proyecto global de esta línea de investigación será de gran importancia, ya que permitirá desarrollar a nivel nacional una tecnología que redundará en beneficios económicos y sanitarios, permitiendo la generación de un sistema único de producción de proteínas recombinantes de valor farmacéutico que poseerá grandes ventajas, incluso frente a los existentes actualmente en el mundo. Para lograr estos objetivos globales, en el laboratorio se trabaja también en una línea de investigación que se centra en el análisis de promotores tejido-específico y desarrollo de vectores y sistemas de cultivos destinados a la generación de gallinas transgénicas como biorreactores.
LABORATORIO DE BIOTECNOLOGÍA DE LA REPRODUCCIÓN ANIMAL Y DE LA REGULACIÓN HORMONAL DEL TRACTO REPRODUCTIVO FEMENINO
Director del laboratorio:
José Lino S. Barañao
A cargo:
Patricia Saragüeta
Integrantes: Griselda Vallejo, Ana Mestre-Citrinovit, Adrián Sestelo, Alejandro J. Lagreca, Inti Tarifa
Nuestro laboratorio trata de comprender los mecanismos celulares y moleculares de acción de las hormonas ováricas, estradiol y progesterona sobre la proliferación y diferenciación celular El endometrio experimenta procesos cíclicos de proliferación, diferenciación y muerte celular regulados por las hormonas ováricas. Nuestro proyecto se centra en el estudio de los mecanismos de regulación de la expresión génica durante la proliferación y diferenciación inducidas por progesterona y estradiol. En nuestro laboratorio hemos demostrado la participación de progesterona en la proliferación de células de endometrio mediante la activación transitoria de Erk y Akt por la interacción del receptor de progesterona y estradiol, hemos encontrado que progesterona a tiempos cortos de estimulación down-regula la expresión de Factores de Transcripción e inhibidores del ciclo celular por lo que proponemos que el efecto proliferativo de progesterona se produce por la inhibición de estos represores de ciclo celular y de la acción de los factores de transcripción y/o sus genes blancos. Asimismo, proponemos la especificidad tisular para dicho mecanismo por lo que caracterizaremos la expresión génica tipo celular específica inducida por la activación de cascadas de señalización citoplasmáticas dependiente de progestinas en células endometriales humanas y las compararemos con resultados previamente obtenidos en células de cáncer de mama humanas T47D. Por otra parte, en nuestro laboratorio hemos caracterizado la expresión génica asociada a la transdiferenciación decidual in vitro y en este proyecto nos proponemos caracterizar la diferenciación y reprogramación de células estromales a células deciduales que tiene lugar fisiológicamente bajo el efecto de estrógenos y progesterona. Estos estudios proveerán nuevo conocimiento acerca de los mecanismos por los cuales la progesterona actúa en la fisiología de las células endometriales y permitirán un nuevo abordaje para la fisiopatología de varias enfermedades ginecológicas asociadas con proliferación endometrial anormal, entre ellas el cáncer y la hiperplasia endometrial.
LABORATORIO DE QUÍMICA DE PROTEOGLICANOS Y MATRIZ
Director del laboratorio:
Juan Carlos Calvo
Integrantes: Lucrecia Piñeiro De Calvo, Valeria Careaga, Virginia Pistone Creydt, Marina Romanato, Vanina Julianelli, Melisa Celeste Sanchez, Amelia Julieta Tesone, Bárbara Ferrando, Sabrina Fletcher, Paula Sacca
En nuestro laboratorio comenzamos estudiando los componentes de la matriz extracelular, en particular los glicosaminoglicanos (ácido hialurónico, condroitín sulfato, dermatán sulfato, heparán sulfato y heparina) como moléculas aisladas o en el contexto de la matriz extracelular. Esta experiencia la plasmamos ahora en dos proyectos de investigación que tienen a estos compuestos como nexo: 1-el estudio de la descondensación de la cromatina del núcleo espermático y, 2-el papel de la matriz extracelular y el entorno celular en la aparición, progresión y metástasis tumoral.
DESCONDENSACIÓN DE LA CROMATINA DEL NÚCLEO ESPERMÁTICO
En este proyecto analizamos las etapas y componentes involucrados en el proceso que ocurre una vez que el espermatozoide penetra hacia el interior del ovocito. Para que la cromatina quede en situación apta para su utilización en la formación de pronúcleo y posterior singamia, hace falta la reducción de puentes disulfuro de las protaminas por GSH y la disociación de las mismas con reemplazo por histonas. En nuestro laboratorio, en modelo humano, encontramos que el heparán sulfato es la molécula responsable de esto último. Actualmente estamos estudiando el metabolismo de este glicosaminoglicano en el folículo en diversos estadios de desarrollo.
EFECTO DEL ENTORNO CELULAR SOBRE EL DESARROLLO TUMORAL
En dos modelos de cáncer, mamario y prostático, estudiamos el papel del tejido adiposo como principal exponente del estroma en el caso de la glándula mamaria y como tejido periprostático en el caso de la próstata. El primer modelo permite estudiar la interacción bidireccional entre epitelio y estroma, mientras que el segundo modelo podría ayudar a comprender el papel del tejido adiposo en la metástasis prostática, aunque no pueda descartarse una acción directa sobre el epitelio tumoral a través de moléculas solubles.
LABORATORIO DE MECANISMOS MOLECULARES DE CARCINOGÉNESIS
Directora del laboratorio:
Patricia Virginia Elizalde
Integrantes: Eduardo Charreau, Roxana Schillaci, Cecilia Proietti, Violeta Chiauzzi, María Celeste Díaz Flaqué, Martín Rivas, Mercedes Tkach, Franco Izzo, Lucía Romero, Leandro Venturutti, Florencia Mercogliano, Rosalía Cordo Russo
El cáncer de mama es una enfermedad compleja y devastadora que tiene sin duda un impacto muy significativo sobre la salud en el mundo entero. Una importante cantidad de descubrimientos a lo largo de la última década ha puesto en evidencia que en el desarrollo de los tumores mamarios hay dos actores clave: los receptores de las hormonas esteroideas estrógenos (ER) y progesterona (PR) y los receptores de factores de crecimiento (GFs) con actividad de tirosina quinasa (RTKs). Particularmente, existe una familia de receptores con actividad de tirosina quinasa, la familia ErbBs, que tiene un rol clave en el desarrollo del carcinoma mamario. Uno de sus miembros, el ErbB-2, es utilizado actualmente en la terapia del cáncer de mama, con relativo éxito, en un tipo particular de tumor mamario que tiene altos niveles de expresión de ErbB-2. La terapia consiste en suprimir la actividad de este receptor mediante un anticuerpo monoclonal humanizado, Trastuzumab, cuyo nombre comercial es Herceptina. Si bien es conocido que los ErbBs interactúan con el PR y el ER para estimular la proliferación del cáncer de mama, los mecanismos que regulan esa interacción y las posibles moléculas activadas por la acción conjunta de ErbBs y de hormonas esteroideas permanecen muy poco conocidos. El objetivo de nuestro laboratorio es identificar mecanismos moleculares de convergencia entre la proteína Heregulina (HRG), ligando de los receptores ErbBs, y el PR con el objeto de encontrar nuevas herramientas moleculares para inhibir el crecimiento del cáncer de mama resistente a la terapia endocrina tradicional de primera línea y a terapias de segunda línea basadas en el bloqueo de tirosina quinasas tales como la Herceptina.
LABORATORIO DE CARCINOGÉNESIS HORMONAL
Directora del laboratorio:
Claudia Lanari
Integrantes: Caroline Lamb, Victoria Fabris, Virginia Novaro, Paola Rojas, María Gorostiaga, Pablo Docampo, Sebastián Giulianelli, Ana Sahores, Victoria Wargon, María Laura Polo, Marina Riggio, Tomás Guillardoy, Gonzalo Sequeira, María May
El objetivo general del laboratorio es investigar los mecanismos que conducen a la hormono independencia en cáncer de mama. Un 75% de las pacientes presentan tumores que expresan receptores hormonales y la enfermedad es, por lo tanto, susceptible a terapias endócrinas. Sin embargo, un alto porcentaje de estas pacientes sufre con el tiempo la pérdida de esta respuesta como parte de la progresión de la enfermedad. Comprender los mecanismos por los cuales los receptores hormonales regulan el crecimiento tumoral podría facilitar el desarrollo de nuevas terapias para prevenir o retardar la aparición de resistencia al tratamiento. En particular, nuestras investigaciones están orientadas a conocer los mecanismos por los cuales se activa el receptor de progesterona y cómo el mismo podría ser utilizado como blanco terapéutico.
LABORATORIO DE HORMONAS Y CÁNCER
Directora del laboratorio:
Isabel Alicia Lüthy
Integrantes: Ariana Bruzzone, Lilian Fedra Castillo, Cecilia Pérez Piñero
Los compuestos adrenérgicos, adrenalina y noradrenalina son importantes hormonas/neurotransmisores liberados durante el estrés. Sus respuestas están mediadas por la activación de receptores adrenérgicos (RA). Nuestro grupo ha descripto la presencia de α2-RA en líneas tumorales y no tumorales de cáncer de mama humano y murino. La estimulación de estos receptores está asociada a un aumento significativo de la proliferación celular y el crecimiento tumoral. Los compuestos adrenérgicos son ampliamente utilizados en la clínica, aun en pacientes con historia previa de cáncer de mama. Sin embargo, no existían estudios que evaluaran el efecto de estos compuestos sobre modelos in vivo de cáncer de mama.
El objetivo de nuestro trabajo es el estudio de estos compuestos sobre diferentes modelos de cáncer de mama, in vitro e in vivo y el estudio de los mecanismos de señalización intracelulares implicados en estas respuestas. También evaluamos la regulación del loop autócrino-parácrino de la prolactina y su receptor en células tumorales mamarias humanas por parte de compuestos adrenérgicos.
Comprendiendo estos mecanismos, se podría determinar qué compuestos (agonistas y antagonistas) podrían ser útiles como tratamiento adyuvante del cáncer de mama. Muchos de estos compuestos se utilizan ampliamente en la clínica con efectos secundarios mínimos, y podrían eventualmente complementar terapias existentes, sobre todo en aquellos casos en los que se desarrolla resistencia a las mismas.
LABORATORIO DE PATOLOGÍA Y FARMACOLOGÍA MOLECULAR
Director del laboratorio:
Alberto Baldi
Integrantes: Carina Shayo, Adrián Góngora, Martín Gomez, Ramiro Vazquez, Sabrina Copsel, Gabriela Bravo, Natalia Alonso, Carolina Flumian, Luís A. Haro Duran
En el Laboratorio de Patología y Farmacología Molecular llevamos a cabo diferentes líneas de investigaciones que comprenden áreas involucradas en el desarrollo de anticuerpos monoclonales humanizados (AcMh) contra diversos moléculas implicadas en la angiogénesis asociada al desarrollo neoplásico. Es así que hemos obtenido una serie de AcM recombinantes que bloquean la actividad del factor de crecimiento del endotelio vascular (VEGF), y del factor de crecimiento fibroblástico básico (FGFb), similares procedimientos se llevan a cabo para neutralizar a otras moléculas pro-angiogénicas que evaden la acción de dichos reactivos. El AcM anti-VEGF redujo muy significativamente el crecimiento de células endoteliales tanto in vitro como in vivo, con la concomitante reducción del volumen tumoral especialmente en melanomas xenotransplantados en ratones atímicos.
También hemos emprendido una serie de ensayos tendientes a silenciar la expresión de genes para disminuir la síntesis de proteínas que no pueden ser neutralizadas por AcMh. Demostramos que construcciones oligonucleotídicas en formato shRNA (small hair-pinRNA) resultaron muy efectivas en silenciar la expresión del FGFb y VEGF. Comenzamos además, con el uso de nanopartículas paramagnéticas como vehículos de los reactivos mencionados, las que pueden ser direccionadas en forma tejido-específico mediante un campo magnético, de forma que el fármaco se reclute de manera selectiva.
Otra área de trabajo se basa en el estudio sobre la transducción de señales relacionadas con la diferenciación celular. En este sentido, la histamina modula numerosos procesos fisiológicos y patológicos a través de cuatro clases de receptores de la familia de receptores acoplados a proteínas G (GPCRs) y juegan un importante papel en la modulación de los procesos de proliferación y diferenciación en células leucémicas que son de nuestro interés. Parte de los objetivos en este campo es definir novedosos blancos terapéuticos.
Además, investigamos las propiedades antiproliferativas de estructuras de origen natural y sintético y sus mecanismos de acción, con el fin de desarrollar nuevos protocolos terapéuticos basados en compuestos innovativos que puedan contribuir al desarrollo de estrategias para tratamiento de dicha patología.
En resumen, el conjunto de estos estudios contribuirán probablemente a un mejor entendimiento de algunos de los mecanismos moleculares implicados en el desarrollo neoplásico y la forma con que estas patologías puedan ser controladas para el beneficio de los pacientes.
LABORATORIO DE INMUNOPATOLOGÍA
Director del laboratorio:
Gabriel Adrián Rabinovich
Integrantes: Norberto Zwirner, Marta Toscano, Mariana Salatino, Diego Laderach, Victoria Sundblad, Iván Mascanfroni, Juan Pablo Cerliani, Carolina Domaica, Diego O. Croci, Lucas Rossi, Damián Avila, Sebastián Dergan-Dylon, Germán Spallanzani, Laura Giribaldi, Andrea Ziblat, Tomás Dalotto Moreno, Verónica Martinez Allo, Mercedes Fuertes, Gimena Raffo, Santiago Mendez Huergo
Los resultados de las investigaciones de nuestro laboratorio podrían contribuir a la generación de nuevas estrategias antiinflamatorias o antitumorales de interés para la comunidad, compañías de biotecnología y/o farmacéuticas. Nuestros proyectos tienen como objetivo el desarrollo de inmunomoduladores que mimeticen las funciones biológicas de lectinas endógenas y /o interfieran con las interacciones entre proteínas y glicanos, modulando así las respuestas inmunológicas asociadas a diversas patologías. Asimismo, a partir de estudios básicos, pretendemos identificar factores endógenos y exógenos que modulen la actividad funcional de diferentes células del sistema inmune y que podrían ser de relevancia durante procesos fisiopatológicos tales como el crecimiento tumoral, las enfermedades autoinmunes, las enfermedades inflamatorias crónicas, infecciones, etc. Mediante la adecuada capitalización de tales conocimientos pretendemos realizar un aporte para la optimización de estrategias inmunoterapéuticas y contribuir, de este modo, al mejoramiento de la salud humana.
LABORATORIO DE INMUNOHEMATOLOGÍA
Directora del laboratorio:
Norma Alejandra Chasseing
Integrantes: Vivian Labovsky, Valeria Fernandez Vallone, Leandro Martínez, Julián Otaegui
El laboratorio tiene como objetivo general encontrar en médula ósea y sangre periférica factores pronóstico del desarrollo de futuros desórdenes óseos en pacientes con cáncer de mama y pulmón. Y entender la contribución del microambiente tumoral, en particular las células madre mesenquimales, en la evolución del tumor primitivo y metástasis óseas.
LABORATORIO DE BIOQUÍMICA NEUROENDÓCRINA
Director del laboratorio:
Alejandro F. De Nicola
Integrantes: Flavia Eugenia Saravia, Susana Laura Gonzalez, María Claudia González Deniselle, María Florencia Labombarda, María Florencia Coronel, Luciana Pietranera, Juan Beauquis, Laura Inés Garay, María Meyer, Maria Elvira Brocca, Gisella Gargiulo Monachelli, Analía Ethel Lima, Paulina Roig, Liliana Zugasti
Las investigaciones realizadas por el Laboratorio de Bioquímica Neuroendocrina muestran la posibilidad de transferencia de los resultados obtenidos en modelos animales a la clínica humana. Trabajando con modelos de neuropatologías, tales como envejecimiento, traumatismo de la médula espinal, esclerosis múltiple y esclerosis lateral amiotrófica, hemos demostrado el beneficio terapéutico que brinda el tratamiento con progesterona y/o estrógenos. Estudios realizados en animales hipertensos demuestran una encefalopatía originada en la hiperfunción del sistema mineralocorticoide, la cual se corrige por tratamiento con estrógenos. En la encefalopatía de la diabetes experimental, tanto los estrógenos como los antidepresivos actúan como neuroprotectores. En el caso de esclerosis lateral amiotrófica, los datos obtenidos en un ratón mutante se han extrapolado a pacientes que mostraron mayor sobrevida luego de recibir progesterona.
LABORATORIO DE NEUROENDOCRINOLOGÍA
Director del laboratorio:
Carlos Libertun
Directora Adjunta:
Victoria Ar Lux Lantos
Integrantes: Silvia Bianchi, Paolo Catalano, Marina Fernandez, Maria Marta Bonaventura, Natalia Isabel Cataldi, Noelia Paula Di Giorgio, Martín Crivello, Nadia Bourguignon, Verónica Calvo, Paula Lopez, Diego Rodriguez
El control neurológico de la hipófisis tiene importancia por su potencial aplicación en medicina reproductiva, y también para establecer la etiopatogenia de los adenomas hipofisarios.
Los estudios sobre regulación de la ingesta y balance energético son fundamentales para entender la etiopatogenia y tratamientos de patologías con alteraciones del peso corporal.
Aquellos resultados referidos a Bisfenol A son relevantes para dilucidar los efectos de los contaminantes ambientales en la salud pública.
Los estudios de la participación de los receptores GABAB en el control del eje hipotálamo-hipofisario y en la regulación de la fisiología pancreática son de suma importancia para comprender patologías endocrinas de gran prevalencia, como la diabetes, y dado el amplio uso farmacológico de agonistas y antagonistas de dichos receptores, los efectos deseables e indeseables de los mismos.
Los estudios referentes a la regeneración de islotes pancreáticos por oligodeoxinucleótidos son muy alentadores y pueden ser de gran interés para el tratamiento de la diabetes juvenil.
LABORATORIO DE REGULACIÓN HIPOFISARIA
Directora del laboratorio:
Damasia Becu
Integrantes: Isabel Lacau, Graciela Díaz, Isabel García Tornadu, Ana Ornstein, Victoria Recouvreux, Maria Cecilia Ramirez, Guillermina Luque, Carolina Cristina, Rodrigo Lorenzo, María Andrea Camilletti
El laboratorio estudia la fisiopatología de la función hipofisaria usando modelos murinos transgénicos, líneas celulares en cultivo, muestras de tumores hipofisarios humanos, y bovinos de importancia económica.
Nuestro laboratorio estudia funciones no convencionales del receptor dopaminérgico tipo 2 (RD2). Los RD2 son fundamentales en la coordinación motora, la actividad de locomoción, el planeamiento, la motivación o aversión y la dominancia social. Por otro lado, diversos mecanismos que aumentan la probabilidad de consumir alimentos nutritivos y aparearse recurrentemente usan la estimulación de este subtipo de receptor. La participación del RD2 en la función endocrina, motivo de nuestras investigaciones, refuerza su papel en la reproducción y supervivencia.
Demostramos la participación de este receptor no sólo en el desarrollo de prolactinomas hipofisarios, sino también en el eje del crecimiento, la ingesta y el metabolismo de glucosa usando en forma combinada ensayos farmacológicos y ratones transgénicos con mutación nula del RD2 en todo el organismo, o con mutación tejido específica en lactotropos. Asimismo, complementamos el enfoque estudiando otros modelos murinos de prolactinomas, y adenomas humanos obtenidos por cirugía.
Nuestros resultados demuestran que este receptor participa en un complejo repertorio de funciones adaptativas que mejoran el desempeño del individuo, su éxito reproductivo y supervivencia
LABORATORIO DE NEUROBIOLOGÍA
Director del laboratorio:
Héctor Coirini
Integrantes: María Sol Kruse, Mariana Rey, María Cristina Vega, Marina Roxana Di Pilla
Los estudios que se efectúan en el laboratorio están dirigidos a evaluar de qué manera una patología severa durante la preñez o un evento perinatal agudo son capaces de preacondicionar al sistema nervioso central para responder ante un evento estresante de una manera anómala y encontrarse directamente relacionados con procesos neurodegenerativos que ocurren en los animales adultos. Paralelamente estudiamos la acción protectora de ciertos agentes de naturaleza sintética que podrían llegar a utilizarse en un futuro para prevenir o revertir las lesiones producidas en etapas tempranas. La relevancia de estos estudios radica en que los mismos permitirán conocer y correlacionar cambios bioquímicos y morfológicos tempranos altamente relacionados con el desarrollo de patologías neurodegenerativas como la enfermedad de Alzheimer y/o la esquizofrenia que presentan una incidencia mayor en la población occidental y que afectan significativamente la calidad de vida del individuo y el entorno cercano.
LABORATORIO DE BIOLOGÍA DEL COMPORTAMIENTO
Director del laboratorio:
Enrique Segura
Integrantes: Marcelo Cassini, Rubén Muzio, Silvano Zanutto, Alejandro Waiselboim, Luciana Frick, Claudia Marro, Alberto Yorio, Maximiliano Rapanelli, Mariana Iurman, Valeria Natacha Peszano, Martín Puddington, Ángel Tabullo, Francisco Mannara, Cecilia Imperioso, Pamela Lopes Da Cunha, Anabel Miguelez Fernandez, Marcia Caruso, Federico Sanchez, Camilo Mininni
Con una larga tradición en el terreno de las regulaciones fisiológicas centradas en el control neuroendócrino de funciones cardiovasculares y reproductivas, se trabaja actualmente en hipótesis originales relacionadas con el estrés en tanto estrategia evolutivamente estable en diversas especies de vertebrados. Sobre esa base se han logrado esclarecer ciertos mecanismos de funcionamiento en mamíferos y anfibios, referidos a las condiciones de regulación en situaciones fisiológicamente críticas. Consecuentemente se está en condiciones de ofrecer conocimiento básico y aplicado con relación a los mecanismos homeostáticos y sus perturbaciones en diversas enfermedades de sistema como hipertensión arterial y alteraciones de la regulación del metabolismo hidrosalino.
Por otra parte, actualmente se llevan a cabo estudios con el objeto de contribuir al debate sobre las bases cognitivas y neurobiológicas de la adquisición del lenguaje en humanos. Los resultados del grupo señalan la importancia de los mecanismos de aprendizaje estadístico en la adquisición de términos y reglas gramaticales nuevas.
UNIDAD DE VINCULACIÓN Y TRANSFERENCIA DE TECNOLOGÍA
En 1983 la Fundación IBYME tomó la decisión de comprometerse con la gestión de proyectos de I+D y fomentar la transferencia tecnológica del conocimiento surgido a partir de la investigación básica en el amplio rango de las investigaciones que se realizaban en la institución. Fue pionera y en el marco de la resolución 314 de la SETCYP del 12 de julio de 1993 como ya se mencionó, se designó a la Fundación Unidad de Vinculación Tecnológica, habilitando su participación al sector productivo de bienes y servicios (tanto públicos como privados) y a la transferencia de los resultados de sus investigaciones.
Esta transferencia tiene distintas modalidades según el tipo de servicio que presta y los destinatarios de los mismos. En nuestro caso, se trata de Servicios Tecnológicos de Alto Nivel (STAN-CONICET), prestaciones que se encuentran reguladas por resoluciones otorgadas por el Consejo Nacional de Investigaciones Científicas y Técnicas, o convenios específicos con empresas o instituciones públicas o privadas.
Entre los primeros, merecen citarse.
- Medición de hormonas en bovinos, ovinos, camélidos, equinos y porcinos
- Testeo de construcciones bajo promotor de beta-caseina bovino.
- Transfección y clonado de fibroblastos fetales bovinos para transferencia nuclear (Institución tomadora del servicio: BioSidus S.A,)
- Determinación de anticuerpos anti-receptor de la hormona folículo estimulante.
- Determinación de anticuerpos anti-ovario en suero humano
- Servicio de microdisección láser
Entre los convenios con empresas figuran:
- Obtención de insulina recombinante humana (Laboratorios Beta, S.A.).
- Modificación genética de levaduras recombinantes para optimizar la producción de proteínas heterólogas (Laboratorios Beta, S.A.).
- Obtención de anticuerpos monoclonales humanizados para el tratamiento en patologías humanas (Casara).
- Desarrollo de un sistema de obtención de aves transgénicas (BioSidus).
- Progestágenos y factores de crecimiento en cáncer de mama humano (Oncomed Reno, S.A.).
- Evaluación de péptidos contra cadherina epitelial y neural en el proceso de interacción de gametas (ADHEREX Technologies Inc- Canada).
- Plataforma biotecnológica para la producción de proteínas recombinantes de uso en salud humana en leche de bovinos transgénicos (BioSidus S.A.).
AGRADECIMIENTO
La invalorable colaboración de la Lic. Flavia Hernández en la coordinación y corrección del material recibido para este número de homenaje al Instituto de Biología y Medicina Experimental es especialmente reconocida.
A continuación contribuciones de los laboratorios que conforman el IBYME
LABORATORIO DE ESTEROIDES
Avances en la fisiología y patología de la célula de Leydig
Advances on Leydig Cell physiology and pathology
Avanços na fisiologia e patologia da célula de Leydig
Mónica B. Frungieri, Silvia I. Gonzalez-Calvar, María E. Matzkin, Soledad P. Rossi, Artur Mayerhofer, Ricardo S. Calandra
Resumen
Con el sustento de datos de la literatura y propios, se describe la interacción entre distintos neurotransmisores (noradrenalina (NA), adrenalina (A), ácido γ-aminobutírico (GABA) y serotonina (5-HT), melatonina y prostaglandinas y su influencia sobre la actividad de las células de Leydig y la posible repercusión sobre la espermatogénesis. Brevemente, se analizan las interrelaciones entre los sistemas testiculares serotoninérgico y melatoninérgico y su participación en la modulación de la expresión testicular de la ciclooxigenasa (COX), enzima clave en la biosíntesis de prostaglandinas. En síntesis, los estudios propuestos, además de brindar un mejor conocimiento sobre la fisiología testicular, permiten dilucidar aspectos fisiológicos del testículo en una especie fotosensible (hámster Dorado) y por el otro, posibilitan describir en el humano hallazgos originales en ciertos cuadros de Infertilidad Idiopática (Síndrome de Sertoli Solo, Arresto Germinal o Hipoespermatogénesis severa). En este contexto, se ha observado en pacientes con distintos grados de Oligospermia y/o Azoospermia, la expresión de COX en células de Leydig, mientras que dicha enzima no se detecta en testículos humanos con morfología normal. De este modo, los avances descriptos pueden contribuir en el estudio de los mecanismos involucrados en el desarrollo de patologías testiculares y permitirían el diseño de nuevas estrategias terapéuticas.
Palabras clave: testículo; neurotransmisores; melatonina; prostaglandinas; infertilidad.
Summary
Data from other authors and our own group describe the presence of different Neurotransmitters-noradrenaline (NA), adrenaline (A) gamma aminobutyric acid (GABA) and serotonin (5-HT), Melatonin and Prostaglandins-in testis and their role in male gonadal function. This review describes interactions between testicular serotoninergic, catecholaminergic and corticotropin-releasing factor systems, and their participation in the regulation of testis expression of ciclo-oxigenase (COX), a key enzyme for steroidogenesis. Moreover, studies on COX expression and Prostaglandin production in Golden hamster Leydig cells are shown. The absence of COX-2 in normal human testes also is discussed, as well as its expression in biopsies from infertile patients (Sertoli cell-only Syndrome, Germ cell arrest or severe hypospermatogenesis) and its potential relevance. Within this context, COX expression in Leydig cells has been observed in patients with some degree of Oligospermia and/or Azoospermia, while this enzyme cannot be detected in normal human testes. Consequently, the advances described can contribute to the study of the mechanisms involved in the develpment of testis pathologies and would enable the design of new therapeutic strategies.
Key words: testis; neurotransmitters; melatonin; prostaglandins; infertility.
Resumo
Com base em dados da literatura e próprios, descreve-se a interação entre diversos neurotransmissores (noradrenalina (NA, adrenalina (A), ácido γ-aminobutírico (GABA) e seroto-nina (5-HT), melatonina e prostaglandinas e sua influência na atividade das células de Leydig e a possível repercussão na espermatogênese. Brevemente, são analisadas as interrelações entre os sistemas testiculares serotoninérgico e melatoninérgico e sua participação na modulação da expressão testicular da ciclooxigenase (COX), enzima chave na biossíntese de prostaglandinas. Em síntese, os estudos pro-postos, além de oferecerem um melhor conhecimento sobre a fisiologia testicular, permitem elucidar aspectos fisiológicos do testículo numa espécie fotossensível (hamster Dourado) e por outra parte, possibilitam descrever no humano achados originais em certos quadros de Infertilidade Idiopática (Síndrome de Sólo Células de Sertoli, Presença de Células Germinais ou Hipoespermatogênese severa). Neste contexto, foi observado em pacientes com diversos graus de Oligospermia e/ou Azoospermia, a expressão de COX em células de Leydig, enquanto que dita enzima não é detectada em testículos humanos com morfologia normal. Deste modo, os avanços descritos podem contribuir no estudo dos mecanismos envolvidos no desenvolvimento de patologias testiculares e permitiriam o desenho de novas estratégias terapêuticas.
Palavras chave: testículo; neurotransmissores; melatonina; prostaglandinas; infertilidade.
Introducción
De manera creciente se ha ido demostrando que la infertilidad masculina es debida, sólo en un reducido número de casos, a alteraciones en el eje hipotálamo-hipófiso-gonadal (H-H-G). Aproximadamente, un 48% de hombres cursa con esterilidad sin causa aparente y el desconocimiento de la causa de cualquier patología hace difícil e ineficaz su tratamiento (1). Por otro lado, los diferentes tipos celulares en el testículo (células de Leydig, Sertoli, germinales, mastocitos, macrófagos, etc) y el avance en el conocimiento en las características estructurales y productos de su secreción, ha llevado a que progresivamente los mecanismos que intervienen en la regulación local del testículo adquieran significancia. Así, nuevos factores intratesticulares fisiológicos, establecidos o potenciales, se involucran en la regulación de la función testicular y eventualmente en la fisiopatología testicular. Han sido descriptos numerosos compuestos como participantes a nivel paracrino (difusión entre células vecinas) en el control de la función gonadal. Entre los principales compuestos se incluyen los siguientes:
A) Neurotransmisores (N-T):Noradrenalina(N-A), Adrenalina(A), Ácido γ-aminobutírico (GABA), Acetilcolina (Acet), Serotonina (5-HT), y B) Otros compuestos: Histamina, Neuropéptido Y (NPY), Factor Liberador de Corticotrofina (CRF), Melatonina (Mel), Prostaglandinas (PGs), Opiodes, Taquininas (SP, NKA, NPK, NPG, NKB), Arginina-Vasopresina (AVP), Ocitocina, GnRH, Leptina, Orexina, Grelina, etc.
Este capítulo se refiere a: N-A, A, GABA, 5-HT, CRF, Mel y PGs y estudios sobre los restantes compuestos pueden ser consultados, entre otras, en las siguientes revisiones específicas: (2-8).
I- NORADRENALINA/ADRENALINA
El testículo no posee nervios somáticos y la inervación es provista a través de nervios autonómicos. Sin embargo, aunque se ha descripto en algunas especies la presencia de un escaso número de fibras colinérgicas en la cápsula testicular (9) la mayoría de los nervios testiculares son de origen simpático. En este sentido, el principal N-T asociado a las fibras simpáticas post-ganglionares es la N-A y en menor grado neuropéptidos (péptido intestinal vasoactivo, VIP y neuropéptido Y, NPY).
Los nervios simpáticos se hallan a lo largo de las arterias que llegan al testículo y constituyen el nervio espermático superior e inferior, localizándose en el espacio intersticial en el hombre, mono Rhesus, perro, gato y cobayo. En cambio, en la rata las fibras nerviosas exhiben una alta densidad sólo en la cápsula testicular, pero ello no es menos importante por cuanto hay células de Leydig próximas a zonas de la cápsula y a vasos sanguíneos muy inervados por varicosidades y vesículas con N-T. Esto se considera una "inervación indirecta", en donde los N-T liberados por la inervación simpática alcanzan a las células vecinas (células de Leydig), inmersas en el líquido intersticial (10). También se ha observado en el mono otro posible orígen de las catecolaminas en el testículo y se refiere por un lado a la detección de la enzima tirosina-hidroxilasa (TH) y dopamina-hidroxilasa (DH), y por el otro, al relacionado a la presencia de células similares a neuronas (neuronlike cells).
En el mismo sentido, se comprobó en las células de Leydig correspondientes a distintos roedores (ratas adultas, ratón, ratón del desierto, hámster y cobayos) inmunoexpresión de marcadores neuronales y gliales (neurofilamento de 200 kD, proteína ácida gliofibrilar, vimentina, citoqueratina, etc) y otros marcadores, los cuales son típicos de células neuroendocrinas y gliales (11). Otra manera de demostrar la participación de N-A y A, ha sido realizada en nuestro laboratorio, donde se demostró luego de la denervación quirúrgica uni y bilateral del testículo de rata, con preservación de la estructura celular, una disminución en la producción de andrógenos post-estímulo con hCG y un descenso exclusivo y simultáneo en los receptores de LH en las células de Leydig (12).
En algunos estudios se han utilizado testículos de hámster debido a la versatilidad del modelo, al permitir estudiar al animal en diferentes estadíos de la función gonadal, según el fotoperíodo de exposición (13). Este modelo en la adultez presenta cambios morfológicos y fisiológicos que son compatibles con una involución testicular severa cuando los animales son expuestos a un fotoperíodo de 6 h de luz y 18 h de oscuridad durante al menos 16 semanas. Luego de 28 semanas en foto-restricción, los animales inician una reactivación espontánea que los lleva a restituir su perfil hormonal y fertilidad. Esto es importante por cuanto previamente se señaló que las catecolaminas son más activas durante el desarrollo y la reactivación que ocurre luego de la involución por exposición a un fotoperíodo breve, que en cierta manera semeja el desarrollo puberal. Así, inicialmente indicamos que la estimulación por N-A y A no es mediada a través de AMPc (14) y, según la edad, el antagonista del receptor adrenérgico α1 prazosin, bloquea dicho estímulo, mientras que propanolol, un β bloqueante, no lo modifica. Estos resultados indican un efecto directo de las catecolaminas sobre el testículo, diferenciándose este efecto según el grado de funcionalidad gonadal, al punto que en testículos prepuberales o en involución, la sensibilidad a las catecolaminas es mayor, lo cual coincide con niveles muy disminuídos de LH/FSH.
En resumen, es posible referir que ante la casi ausencia de gonadotrofinas, se postula que las catecolaminas intervendrían en las situaciones referidas con un rol predominante sobre la esteroidogénesis.
II-ÁCIDO γ-AMINOBUTÍRICO (GABA)
GABA es un potente N-T en el SNC y participa en la proliferación neuronal y modulación de la producción de neuroesteroides. En relación a este N-T, en el laboratorio se ha identificado GABA en el testículo de rata, preferentemente en el estadío prepuberal (15), demostrando un efecto estimulatorio en la esteroidogenésis y la presencia de receptores-GABA (Rs-GABA) en células de Leydig purificadas (16). Además de su localización en el intersticio testicular, se describe la presencia de GABA y Rs-GABA tipo A en espermatozoides humanos eyaculados, facilitando la iniciación de la reacción acrosomal y una mayor motilidad espermática. Más recientemente, en colaboración con el Grupo del Dr. Mayerhofer (Munich, Alemania), hemos descripto por medio de técnicas de biología molecular: a) Rs-GABA-A/B y sus diferentes subunidades en células de Leydig purificadas del testículo en distintas especies incluido el humano, b) la enzima GABA-glutamato decarboxilasa (GAD65 y/o 67) y c) la expresión del transportador vesicular inhibitorio de aminoácidos (VIAAT/VGAT). A su vez, la presencia de la subunidad α1 del Rs-GABA-A- en las células de Leydig de rata fue confirmada por la técnica de microdisección por captura láser y RT-PCR (17).
En resumen, GABA podría : 1) regular la función esteroidogénica de las células de Leydig ; 2) intervenir en la maduración y diferenciación de las células germinales y participar en la reacción acrosomal y 3) influir en la proliferación y diferenciación del intersticio testicular, debido a hallazgos que señalan al GABA como un regulador trófico.
III-SEROTONINA (5-HT)/CORTICOTROPIN RELEASING FACTOR (CRF)
Otros autores autores han descripto previamente elevadas concentraciones de 5-HT en el testículo de rata, pero de manera especial al nacimiento. En nuestro grupo se observó inicialmente un efecto directo de esta indolamina sobre la esteroidogénesis testicular así como la presencia de sitios específicos de unión de la 5-HT-3H a membranas testiculares (18). Más tarde fue descripta la presencia de 5-HT en la cápsula testicular y células intersticiales y ausencia en los túbulos seminíferos. Se indicó que en un porcentaje considerable, el origen del N-T es a partir de una inervación serotoninérgica. También, fue llamativa la elevada concentración de 5-HT y ácido 5-hidroxiindolácetico en el líquido intersticial, indicando esto último la presencia de actividad monoamino oxidasa (19). Estudios posteriores, y correspondientes a otros autores, indican que las células de Leydig de rata producen 5-HT, su síntesis es estimulada por AMPc y de manera autocrina/paracrina, la indolamina interviene en la liberación testicular de
CRF por las células de Leydig (20). Este péptido es un inhibidor en la producción de testosterona post-hCG y por lo tanto, se ha postulado que la 5-HT modularía en forma indirecta la esteroidogénesis testicular.
A través de la utilización del modelo fotosensible del hámster, en nuestro grupo se observó no sólo la síntesis local de 5-HT y su localización celular, sino que también se demostró su variación durante el desarrollo sexual y durante el proceso de involución/reactivación fotoinducible (21).
En el origen testicular de la 5-HT pueden estar involucrados los mastocitos, los que también secretan, al menos en roedores, una serie de compuestos entre los que se hallan: histamina, citoquinas, prostaglandinas (PGs), factores de crecimiento y proteasas. Estas células están en la proximidad de las fibras nerviosas y de los elementos neuronales testiculares. La interacción entre estos elementos y las células de Leydig, al menos en el testículo de mono, sería mediada por los mastocitos (22) y vía sus productos secretorios influirían sobre la función testicular. Estudios de otros grupos y este Laboratorio, han descripto en el testículo humano que los mastocitos se hallan localizados en el compartimento intersticial y en la pared de los túbulos seminíferos. Así, en biopsias testiculares y por técnicas inmunohistoquímicas, se observó un aumento significativo en la población de mastocitos en muestras de pacientes con el Síndrome de Sertoli Solo (o Del Castillo, Trabucco y de la Balze) y Arresto Germinal (22).También se halló que los mastocitos testiculares contienen triptasa, una proteasa de serinas (23). En ese sentido, se describió que ejerce una acción fibroproliferativa que involucra la activación del receptor activado por proteasas 2 (PAR2), un aumento en la expresión de la enzima ciclo-oxigenasa 2 (COX2, clave en la biosíntesis de PGs) y unión de 15-deoxi-Δ12,14-PGJ12 (15d-PGJ2) a sus receptores nucleares PPARγ.
En consecuencia, la triptasa se halla estrechamente ligada a la relación entre mastocitos y los procesos fi-bróticos (24).Es interesante resaltar, que el testículo humano presenta los componentes del sistema triptasa-PAR2-COX2-15d-PGJ2-PPARγ, y en consecuencia un aumento en la población mastocitaria podría estar involucrada en la fibrosis peritubular en las patologías mencionadas.
IV-MELATONINA (MEL)
Es reconocido el efecto de la Mel sobre el eje H-H en especies fotosensibles y en especial en la regulación de la actividad reproductiva en modelos con variación estacional (25). El efecto de Mel depende de la especie, tiempo, extensión y niveles hormonales alcanzados. Además de su efecto en el eje H-H, la Mel ejerce un efecto directo sobre las células de Leydig. Esta hormona influencia la capacidad reproductiva a nivel cerebral y sobre la hipófisis regula la síntesis de gonadotrofinas. La señal fótica (impulso lumínico) llega a través de la retina a la glándula pineal modulando la síntesis de Mel. Además de este mecanismo melatoninérgico central sobre el control de la reproducción, también hemos demostrado en el hámster Dorado un efecto intratesticular de la Mel vía receptores mel1a en las células de Ley-dig y una regulación inhibitoria en la expresión génica de la proteína StAR y enzimas esteroidogénicas (P450scc, 3β-HSD, 17β-HSD). Más aún, en las células de Leydig ha sido posible establecer la presencia de las enzimas específicas que intervienen en la síntesis de Mel, sugiriendo un origen gonadal (26).
Se ha observado que la Mel regula el número de mastocitos testiculares. En estudios de este Laboratorio, se observó en hámsteres expuestos a un fotoperíodo reducido (8h luz-día), simultáneamente un aumento en el número de mastocitos testiculares y en los niveles de Mel (26). En este sentido, previamente se señaló la interacción entre el sistema serotoninérgico-catecolaminérgico-CRF en las células de Leydig de hámster (22). Recientemente, se describió en estas células la expresión de la serotonina N-acetiltransferasa, enzima pívot en la síntesis de Mel. También se detectaron Rs-Mel1a, una inhibición por Mel en la producción post-estímulo con hCG de AMPc y andrógenos así como en la expresión de StAR y enzimas relacionadas (26). Por lo tanto, los resultados indican la existencia de un sistema melatoninérgico testicular y un rol de Mel a distintos niveles en el camino de la esteroidogénesis gonadal. En síntesis, los nuevos conocimientos en la regulación de la esteroidogénesis testicular, sugieren un fine tunning o tono fino, ejercido por compuestos locales (ej. N-T, Mel, 5-HT), los que bien podrían ser de relevancia en una mejor comprensión de la fisiología a nivel celular.
V-PROSTAGLANDINAS (PGs)
Las PGs son compuestos derivados del ácido araquidónico vía la intervención en sus etapas iniciales por dos isoenzimas tales como la ciclooxigenasa tipo 1 (COX-1) y ciclooxigenasa tipo 2 (COX-2) y a posteriori por otras enzimas (PGE sintasa, PGD sintasa, etc). La COX-1 es constitutiva, se halla en la mayoría de las células y en cambio la isoenzima COX-2 es inducible y se expresa en estadíos tempranos de la diferenciación celular. El desarrollo de ratones deficientes en COX-1 y COX-2, ha permitido delimitar el rol de ambas isoenzimas en la reproducción. En ratones machos deficientes en COX-1 y COX-2 no se observan trastornos de la fertilidad. Sin embargo, estudios previos señalaron en ratones machos y en la línea celular de testículo MA-10, que las PGs podrían estar inhibiendo la esteroidogenésis. Más recientemente, se indica que el descenso en la biosíntesis de testosterona testicular en la rata Brown-Norway en envejecimiento, se relaciona con la actividad de la isoenzima COX-2. En este sentido, hemos indicado que diferentes especies que incluyen monos Rhesus adultos, cerdo, ratas Wistar y Sprague Dawley, y ratones BALBc y hamsteres prepuberales o en involución gonadal por fotorestricción, no mostraron expresión de la isoenzima COX-2, mientras que células de Leydig de hamsteres adultos y puberales en fotoperíodo normal indicaron expresión positiva (27). PGD2 y PGF2α, modulan la síntesis de testosterona en estas células. Además, estudios recientes nos señalan que la expresión de COX-2 y la síntesis de PGs en células de Leydig del hámster, son reguladas por testosterona a través de un mecanismo no clásico (28).
Finalmente, es importante señalar que en testículos de pacientes con ciertos cuadros de infertilidad, tales como el Síndrome de Sertoli Solo y en el Síndrome de Arresto Germinal, hemos hallado expresión de COX-2. Por el contrario, en muestras de testículos provenientes de pacientes sin anormalidades morfológicas del testículo la expresión es negativa (29). Conectado a estos hallazgos, el número total de macrófagos se encuentra aumentado. Estas células inmunes, localizadas en el espacio intersticial y los túbulos seminíferos, expresan interleuquina 1α/β y TNFα (30). Al respecto, recientemente hallamos una significativa correlación entre los niveles de interleuquina 1β y la expresión de COX-2 en el testículo humano (31). De este modo, ciertas citoquinas serían capaces de modificar la función de las distintas células del testículo y en consecuencia podrían estar involucradas en el desarrollo de cuadros de infertilidad que se clasifican como idiopáticos.
AGRADECIMIENTOS
Los estudios descriptos han sido apoyados con Subsidios provenientes del Consejo Nacional de Investigaciones Científicas y Técnicas (CONICET), Agencia Nacional de Promoción Científica y Técnica (ANPCYT), Facultad de Medicina-Universidad de Buenos Aires, Fundación Antorchas, Fundación A.J.Roemmers, Deutsche Forsschungsgemeinschaft (DFG) (Alemania), Academy of Sciences for the Developing World (TWAS).
1. Randolph J. Unexplained Infertility. Clin Obstet Gynecol 2000; 43: 897-901.
2. Fabbri A, Knox G, Buczko E, Dufau ML. Beta-endorphin production by the fetal Leydig cell regulation and implications for paracrine control of Sertoli cell function. Endocrinology 1988; 122: 749-755.
3. Sharpe RM. Intratesticular control of steroidogenesis. Clin Endocrinol 1990; 33: 787-807.
4. Spiteri-Grech J, Nieschlag E. Paracrine factors to the regulation of spermatogenesis.- A Review. J Reprod Fertil 1993; 98: 1-14.
5. Gnesi L, Fabbri A, Spera G. Gonadal peptides as mediators of development and functional control of the testis: an integrated system with hormones and local environment. Endocrine Rev 1997; 18: 541-609.
6. Debeljuk L, Rao JN, Bartke A. Tachykinins and their possible modulatory role on testicular function : a Review. Int J Androl 2003; 26: 202-10.
7. Frungieri MB, Gonzalez-Calvar SI, Matzkin ME, Mayer-hofer A, Calandra RS. Sources and functions of prostaglandins in the testis : evidence for their relevante in male (in) fertility. Anim Reprod 2007; 4: 63-9.
8. Nieschlag E, Behre HM, Nieschlag S. Andrology: Male Reproductive Health and Dysfunction. 3rd Edition. Springer; 2010.
9. Setchell BP, Maddocks S, Brooks DE. Anatomy, Vasculature, Innervation and Fluids of the Male Reproductive Tract. En: The Physiology of Reproduction; E. Knobil, JD Neill (eds). New York: Raven Press; 1994; págs. 1063-175.
10. Mayerhofer A. Leydig cell regulation by catecholamines and neuroendocrine messengers. En: The Leydig Cell, AH Payne, MPP Hardy, LD Russell (eds.), Viena: Cache River Press; 1996; 407-17.
11. Ortega HH, Lorente JA, Salvetti NR. Immunohisto-chemical study of intermediate filaments and neuroendocrine marker expresión in Leydig cells of Laboratory rodents. Anat Histol Embriol 2004; 33: 309-15.
12. Campos MB, Chiocchio SR, Calandra RS, Ritta MN. Effect of bilateral denervation of the immature testis on testicular gonadotroppin receptors and in vitro androgen production. Neuroendocrinology 1993; 57: 189-94.
13. Bartke A, Male hamster reproductive endocrinology. En: The Hamster, HI Spigel (editor). New York: Plenum; 1985. p. 73-98.
14. Mayerhofer A, Calandra R, Bartke A. Cyclic adenosine monophosphate (c-AMP) does not mediate the stimulatory action of norepinephrine on testosterone production in the testis of the golden hamster. Life Sci 1991; 48: 1109-14.
15. Ritta MN, Campos MN, Calandra RS. Effect of GABA and Benzodiazepines on testicular androgen production. Life Sci 1987; 40: 791-8.
16. Ritta MN, Campos MB, Calandra RS. Coexistence of γ-aminobutyric acid Type A and Type B receptors in testicular interstitial cells. J Neurochem 1991; 56: 1236-40.
17. Geigerseder Ch, Doepner R, Thalhammer A, Frungieri MB, Gamel-Didelon K, Calandra RS, et al. Evidence for a GABAergic system in rodent and human testis: local GABA production and GABA receptors. Neuroendocrinology 2003; 77: 314-23.
18. Campos MB, Vitale ML, Ritta MN, Chiocchio SR, Calandra RS. Involvement of serotonin in testicular androgen production. En: Proc 5th Eur.Workshop on Molecular and Cellular Endocrinology of the Testis. Brighton, Cheney and Sons Ltd; 1988.
19. Campos MB, Vitale ML, Calandra RS, Chiocchio SR. Serotoninergic innervation of the rat testis. J Reprod Fert 1990; 88: 475-9.
20. Tinajero JC, Fabri A, Ciocca DR, Dufau ML. Serotonin secretion from rat Leydig cells. Endocrinology 1993; 133: 3026-9.
21. Frungieri MB, Gonzalez-Calvar SI, Rubio M, Ozu M, Lustig L, Calandra RS. Serotonin in golden hamster : testicular levels, immunolocalization and role during sexual development and photoperiodc regression-recrudescence transition. Neuroendocrinology 1999; 69: 299-308.
22. Frungieri MB, Zitta K, Pignataro OP, Gonzalez-Calvar SI, Calandra RS. Interactions between testicular serotoninergic, catecholaminergic and corticotropin-releasing factor systems modulating the cAMP and testosterone production in the Golden hamster. Neuroendocrinology 2002; 76: 35-46.
23. Meineke V, Frungieri MB, Jessberger B, Vogt HJ, May-erhofer A. Human testicular mast cells contain tryptase: increased mast cell number and altered distribution in the testes of infertile men. Fert Steril 2000; 74: 239-44.
24. Frungieri MB, Weidinger S, Meineke V, Köhn FM, May-erhofer A. Proliferative action of mast-cell tryptase is mediated by PAR2, COX2, prostaglandins, and PPARy: Possible relevance to human fibrotic disorders. Proc Natl Acad Sci 2002; 9: 15072-7.
25. Reiter RJ. Pineal Melatonin: Cell biology of its synthesis and of its physiological interactions. Endocrine Rev 1991; 12: 151-80.
26. Frungieri MB, Mayerhofer A, Zitta K, Pignataro OP, Calandra RS, Gonzalez-Calvar SI. Direct effect of melatonin on syrian hamster testes: melatonin subtype1a receptors, inhibition of androgen production and interaction with the local corticotropin-releasing hormone system. Endocrinology 2005; 146: 1541-52.
27. Frungieri MB, Gonzalez-Calvar SI, Parborell F, Al-brecht M, Mayerhofer A, Calandra RS. Cyclooxyge-nase-2 (COX-2) and prostaglandin F2a (PGF2a) in Syrian Hamster Leydig cells: inhibitory role on LH/hCG stimulate testosterona production. Endocrinology 2006; 147: 4476-85.
28. Matzkin ME, Gonzalez-Calvar SI, Mayerhofer A, Calandra RS, Frungieri MB. Testosterone induction of prostaglandin-endoperoxide synthase 2 expression and prostaglandin F2a production in hamster Leydig cells. Reproduction 2009; 138: 163-75.
29. Schell C, Frungieri MB, Albrecht M, Gonzalez-Calvar SI, Kôhn FM, Calandra RS, et al. A prostaglandin D2 system in the human testis. Fertil Steril 2007; 88: 233-6.
30. Frungieri MB, Calandra RS, Lustig L, Meineke V, Kôhn FM, Vogt HJ, et al. Number, distribution pattern, and identification of macrophages in the testes of infertile men. Fertil Steril 2002; 78: 298-306.
31. Matzkin ME, Mayerhofer A, Rossi SP, Gonzalez B, Gonzalez CR, Terradas C, et al. Cyclooxygenase-2 in testes of infertile men: evidence for the induction of prostaglandin synthesis by interleukin-1p. Fertil Steril 2010; 94: 1933-6.
LABORATORIO DE ESTEROIDES
Efectos gonadales y extra-gonadales de la hipersecreción de la hormona gonadotrofina coriónica humana: evaluación en un modelo de ratones transgénicos.
Gonadal and extra-gonadal effects of human chorionic gonadotropin hypersecretion: evaluation in a transgenic mouse model
Efeitos gonadais e extra-gonadais da hipersecreção do hormônio gonadotrofina coriônica humana: avaliação num modelo de camundongos transgênicos
Susana B. Rulli, Laura D. Ratner, Guillermina Stevens, Betina González, Ricardo S. Calandra
Resumen
Nuestro grupo de investigación está enfocado en estudiar los efectos gonadales y extra-gonadales que ejerce la hormona gonadotrofina coriónica humana (hCG) sobre la función endocrina y reproductiva, particularmente en condiciones de secreción desregulada y persistente. La tecnología transgénica ha resultado ser una herramienta fundamental a la hora de proveer nuevas evidencias sobre el rol de las gonadotrofinas en la patofisiología reproductiva. En este sentido, los ratones transgénicos hipersecretores de hCG han resultado un excelente modelo para llevar a cabo dichas investigaciones. Hemos realizado estudios de caracterización del modelo, que nos han permitido tener un profundo conocimiento del mismo e identificar un gran número de anomalías en distintos niveles de regulación endocrina, que serán el foco de atención en futuras investigaciones. Las mismas tienen un considerable potencial en el campo de la biomedicina, ya que ayudarán a identificar los mecanismos regulatorios afectados por un estímulo disruptivo como puede ser una hipersecreción hormonal, y permitirán la exploración de nuevas estrategias terapéuticas que interfieran en las patologías endocrinas asociadas. Nuestras investigaciones sobre el modelo de hipersecreción crónica de hCG en ratones muestran claramente que niveles elevados y persistentes de esta hormona promueven múltiples anomalías endocrinas que están acompañadas de tumores gonadales y extra-gonadales.
Palabras clave: gonadotrofina coriónica humana; ratones transgénicos; reproducción; hormona; tumores.
Summary
This investigation is focused in studying the gonadal and extra-gonadal effects that the human chorionic gonadotropin hormone (hCG) exerts on endocrine and reproductive functions, particularly under deregulated and persistent secretion conditions. Transgenic technology has turned out to be a fundamental tool when providing new evidences on the role of gonadotropins in reproductive physiopathology. In this sense, transgenic mice hCG hypersecretion has been an excellent model to perform these investigations. Characterization studies of the model have been developed to identify a great number of anomalies in different levels of endocrine regulation, which will be the center of attention in subsequent investigations. These have a considerable potential in the field of biomedicine and will help to identify the regulatory mechanisms affected by a disruptive stimulus, such as hormonal hypersecretion, and will enable the exploration of new therapeutic strategies to interfere with endocrine pathologies. Our investigations on the model of chronic hypersecretion of hCG in mice show clearly that high and persistent levels of this hormone promote manifold endocrine anomalies that are accompanied by gonadal and extra-gonadal tumors.
Key words: human chorionic gonadotropin; transgenic mice; reproduction; hormone; tumors.
Resumo
Nosso grupo de pesquisa está focado em estudar os efeitos gonadais e extra-gonadais que exerce o hormônio gonadotrofina coriônica humana (hCG) sobre a função endócrina e reprodutiva, particularmente em condições de secreção desregulada e persistente. A tecnologia transgênica tem resultado ser uma ferramenta fundamental na hora de fornecer novas evidências sobre o papel das gonadotrofinas na patofisiologia reprodutiva. Nesse sentido, os camundongos transgênicos hipersecretores de hCG têm resultado um excelente modelo para levar a cabo tais pesquisas. Temos realizado estudos de caracterização do modelo, que nos têm permitido ter um profundo conhecimento do mesmo e identificar um grande número de anomalias em diferentes níveis de regulação endócrina, que serão o foco de atenção em futuras pesquisas. As mesmas têm um considerável potencial no campo da biomedicina, visto que ajudarão a identificar os mecanismos regulatórios afetados por um estímulo disruptivo como pode ser uma hipersecreção hormonal, e permitirão a exploração de novas estratégias terapêuticas que interfiram nas patologias endócrinas associadas. Nossas pesquisas sobre o modelo de hipersecreção crônica de hCG em camundongos mostram claramente que níveis elevados e persistentes deste hormônio promovem múltiplas anomalias endócrinas que estão acompanhadas de tumores gonadais e extra-gonadais.
Palavras chave: gonadotrofina coriônica humana; camundongos transgênicos; reprodução; hormônio; tumores.
El eje hipotálamo-hipófiso-gonadal es el pilar fundamental en la regulación endocrina de la función reproductiva. Cualquier alteración en la regulación de las diferentes hormonas o receptores involucrados en el funcionamiento de este eje puede provocar cambios en el inicio de la pubertad, infertilidad, y también cáncer, desórdenes metabólicos o disfunciones cardiovasculares. La acción fisiológica de las gonadotrofinas está bien caracterizada y se sabe que son esenciales en la foliculogénesis, ovulación y esteroidogénesis en las hembras, y en el desarrollo testicular, espermatogénesis y esteroidogénesis en los machos. Existen condiciones fisiológicas y patológicas donde la secreción y/o acción de las gonadotrofinas están elevadas. Por ejemplo, durante el primer trimestre de embarazo, cuando la hormona gonadotrofina coriónica humana (hCG) es esencial en el mantenimiento de la preñez y la masculinización del feto (1). La posmenopausia es una condición fisiológica donde las mujeres están expuestas a niveles elevados de gonadotrofinas durante décadas, y se ha propuesto que éste es un factor de riesgo para el desarrollo de tumores de ovario (2). Por último, condiciones patológicas con elevada secreción/acción de gonadotrofinas incluye tumores hipofisarios, mutaciones activantes de sus receptores, síndrome de ovario poliquístico, enfermedades trofoblásticas y tumores testiculares.
La tecnología transgénica ha resultado ser una herramienta fundamental a la hora de proveer nuevas evidencias sobre el rol de las gonadotrofinas en la pato-fisiología reproductiva. La hCG, normalmente secretada por la placenta, está estructural y funcionalmente relacionada con la hormona luteinizante (LH), y produce el mismo efecto biológico a través de la unión a un mismo receptor, estimulando la esteroidogénesis gonadal. Los descubrimientos que vinculan a la acción de LH con actividad de promotor tumoral, fueron el incentivo para esclarecer las consecuencias fenotípicas de una acción aumentada de LH/hCG (3-8). Con el fin de lograr una elevada actividad de LH/hCG circulante, se han desarrollado dos líneas de ratones transgénicos que sobreexpresan hCG: 1) simple transgénicos portadores del gen de la subunidad β de hCG (hCGβ+); 2) doble transgénicos portadores de los genes de las subunidades α y β de hCG (hCGαβ+). Ambos transgenes se encuentran bajo el promotor universal Ubiquitina C.
Nuestro grupo de investigación está enfocado en estudiar los efectos gonadales y extra-gonadales que ejerce la hCG sobre la función endócrina y reproductiva, particularmente en condiciones de secreción desregulada y persistente. En este sentido, los ratones transgénicos hipersecretores de hCG han resultado un excelente modelo para llevar a cabo dichas investigaciones. Estos animales se han desarrollado en la Universidad de Turku, Finlandia, bajo la dirección y coordinación de los Dres. I. Huhtaniemi y M. Poutanen, con quienes se mantiene una activa colaboración. Hemos realizado estudios de caracterización del modelo, que nos han permitido tener un profundo conocimiento del mismo e identificar un gran número de anomalías en distintos niveles de regulación endocrina, que serán el foco de atención en futuras investigaciones. Las mismas tienen un considerable potencial en el campo de la biomedicina, ya que ayudarán a identificar los mecanismos regulatorios afectados por un estímulo disruptivo como puede ser una hipersecreción hormonal, y permitirán la exploración de nuevas estrategias terapéuticas que interfieran en las patologías endocrinas asociadas.
Hemos descrito que en el modelo de ratones transgénicos hCGβ+ se producen moderados niveles de hCG bioactiva, producto de la dimerización de la subunidad hCGβ transgénica y la subunidad α expresada endógenamente en la hipófisis (9)(10). Mientras que los machos hCGβ+ son fértiles, las hembras presentan pubertad precoz y son infértiles debido a alteraciones en el ciclo estral y defectos en la estructura uterina. Los ovarios se muestran con quistes hemorrágicos ocasionales y altamente luteinizados como consecuencia de la activa estimulación con hCG. Estos animales producen elevados niveles circulantes de andrógenos, estrógenos y progesterona desde edades tempranas del desarrollo sexual. Se han detectado también varios fenotipos extragonadales en este modelo: a edades avanzadas, las hembras desarrollan hiperprolactinemia acompañada de macroprolactinomas y tumores mamarios metastásicos (9)(11)(12). Los complejos cambios hormonales, y consecuentemente el desarrollo de dichos tumores se atribuyen a la hiperestimulación crónica del ovario por hCG, ya que la ovariectomía impide su formación, a pesar de mantener una persistente y elevada secreción de hCG.
El modelo de ratones doble transgénicos hCGαβ+ produce una excesiva secreción de la forma dimérica bioactiva de hCG (3)(4)(10)(13). Esta condición permitió identificar fenotipos patológicos que no se habían manifestado en el modelo de simples transgénicos con moderada expresión de hCG. Hemos observado que las hembras también presentan pubertad precoz, infertilidad y significativas alteraciones en el perfil de hormonas esteroideas circulantes desde edades tempranas de la maduración sexual. La principal característica que diferencia este modelo con el del simple transgénico es el desarrollo de tumores de ovario de tipo teratoma (3)(4). Al inicio de la edad adulta, hemos detectado la presencia de células gigantes del trofoblasto en el ovario hCGαβ+, normalmente involucradas en la implantación del feto y vascularización de la decidua materna, así como la formación de una masa tumoral compuesta de tejidos derivados de las tres capas embrionarias, que imita desordenadamente el desarrollo embrionario. Estos tumores surgen a partir de la activación partenogenética de los ovocitos dentro del ovario. Hemos analizado si el desarrollo tumoral está influenciado por la acción de los esteroides gonadales producidos en exceso por dichos ovarios, a través de tratamientos in vivo con el antiandrógeno flutamida, el antiestrógeno fulvestrant y el antiprogestágeno mifepristone en ratones hembras hCGαβ+ (14). Si bien los tratamientos antihormonales no lograron impedir la activación teratogénica, los mismos tuvieron un claro efecto sobre la progresión tumoral, frenando el crecimiento explosivo del teratoma. Por otra parte, hemos estudiado la capacidad ovulatoria y la expresión de distintos factores involucrados en la ovulación en hembras inmaduras hCGαβ+ sometidos a un protocolo de inducción de la ovulación con PMSG/hCG. Observamos que el mecanismo de ovulación resultó significativamente afectado en las hembras transgénicas, indicando que niveles elevados de hCG estarían produciendo una alteración en la correcta expresión de los factores involucrados en el proceso de señalización intrafolicular, que conllevaría a la anovulación (15).
En cuanto a los machos, la hipersecreción crónica de hCG causa hiperplasia/hipertrofia de las células de Leydig de origen fetal, hiperandrogenismo, infertilidad y severas alteraciones en los órganos reproductivos masculinos (10)(13). Hemos demostrado además, que la hipersecreción de hCG en machos produce una inhibición persistente sobre la síntesis y secreción de FSH, a través de alteraciones a nivel de la hipófisis y del hipotálamo, que no revierten con la castración o con el bloqueo de la acción androgénica por flutamida (16). Dado que la sobreexpresión de hCG en este modelo ocurre desde el estadío fetal, este efecto se debería a una mayor exposición a esteroides del sistema neuroendócrino durante etapas tempranas de diferenciación sexual, revelando nuevos roles de los andrógenos y/o sus metabolitos producidos localmente en la (des)regulación de la unidad hipotálamo-hipofisaria masculina.
Nuestras investigaciones sobre el modelo de hipersecreción crónica de hCG muestran claramente que niveles elevados y persistentes de esta hormona promueven en ratones múltiples anomalías endocrinas que están acompañadas de tumores gonadales y extra-gonadales.
Estas investigaciones han sido financiadas con subsidios de la Agencia Nacional de Promoción Científica y Tecnológica, el Consejo Nacional de Investigaciones Científicas y Técnicas de la República Argentina y Fundación Roemmers.
Referencias bibliográficas
1. Huhtaniemi I. Fetal testis-a very special endocrine organ. Eur J Endocrinol 1994; 130: 25-31.
2. Konishi I Gonadotropins and ovarian carcinogenesis: a new era of basic research and its clinical implications. Int J Gynecol Cancer 2006; 16: 16-22.
3. Rulli SB, Huhtaniemi I. What have gonadotrophin over-expressing transgenic mice taught us about gonadal function? Reproduction 2005; 130: 283-91.
4. Huhtaniemi I, Rulli S, Ahtiainen P, Poutanen M. Multiple sites of tumorigenesis in transgenic mice overproducing hCG. Mol Cell Endocrinol 2005; 234: 117-26.
5. Huhtaniemi I, Ahtiainen P, Pakarainen T, Rulli SB, Zhang FP, Poutanen M. Genetically modified mouse models in studies of luteinising hormone action. Mol Cell Endocrinol 2006; 252: 126-35.
6. Ahtiainen P, Rulli S, Pakarainen T, Zhang FP, Poutanen M, Huhtaniemi I. Phenotypic characterisation of mice with exaggerated and missing LH/hCG action. Mol Cell Endocrinol 2007; 262: 55-63.
7. Pakarainen T, Ahtiainen P, Zhang FP, Rulli S, Poutanen M, Huhtaniemi I. Extragonadal LH/hCG action- Not yet time to rewrite textbooks. Mol Cell Endocrinol 2007; 269: 9-16.
8. Peltoketo H, Zhang FP, Rulli SB. Animal models for aberrations of gonadotropin action. Rev Endocr Metab Disord 2011 (en prensa).
9. Rulli SB, Kuorelahti AI, Karaer 0, Pelliniemi L, Poutanen M, Huhtaniemi IT. Reproductive disturbances, pituitary lactotrope adenomas, and mammary gland tumors in transgenic female mice producing high levels of human chorionic gonadotropin. Endocrinology 2002; 143: 4084-95.
10. Rulli SB, Ahtiainen P, Makela S, Toppari J, Poutanen M, Huhtaniemi IT. Elevated steroidogenesis, defective reproductive organs and infertility in transgenic male mice over-expressing human chorionic gonadotropin. Endocrinology 2003; 144: 4980-90.
11. Kuorelahti A, Rulli S, Huhtaniemi I, Poutanen M. hCG upregulates wnt5b and wnt7b in the mammary gland and hCG{beta} transgenic female mice present with mammary gland tumors exhibiting characteristics of the Wnt/{beta}-catenin pathway activation. Endocrinology 2007; 148: 3694-703.
12. Ahtiainen P, Sharp V, Rulli SB, Rivero-Müller A, Mamaeva V, Röyttä, et al. Enhanced LH action in transgenic female mice expressing hCGβ subunit induces pituitary prolactinomas; the role of high progesterone levels. Endocrine-Related Cancer 2010; 17: 611-21.
13. Ahtiainen P, Rulli S, Pelliniemi LJ, Toppari J, Poutanen M, Huhtaniemi I. Fetal but not adult Leydig cells are susceptible to adenoma formation in response to persistently high hCG level; a study on hCG overexpressing transgenic mice. Oncogene 2005; 24: 7301-9.
14. Gonzalez B, Calandra RS, Poutanen M, Huhtaniemi I, Rulli SB. Expression of key steroidogenic genes and the role of androgens in the development of ovarian tumors in hCG transgenic mice. Endocrinologia e Metabologia 2008; 52, supl.6, S924.
15. Ratner LD, Gonzalez B, Poutanen M, Huhtaniemi I, Calandra RS, Rulli SB. The ovulatory capacity and related genes are altered in transgenic mice hypersecreting the human chorionic gonadotrophin hormone (hCG). 12nd European Congress of Endocrinology, Praga, República Checa, 2010. Endocrine Abstracts 2010; 22: P485.
16.Gonzalez B, Ratner LD, Di Giorgio NP, Poutanen M, Huhtaniemi I, Calandra RS, et al. Effect of chronically elevated androgens on the developmental programming of the hypothalamic-pituitary axis in male mice. Mol Cell Endocrinol 2011; 332: 78-87.
LABORATORIO DE ENDOCRINOLOGÍA MOLECULAR
Falla ovárica prematura
Premature ovarian failure
Falência ovariana prematura
Violeta Chiauzzi, Victoria Sundblad, Ianina Ferder, Liliana Dain, Eduardo Charreau
Resumen
La falla ovárica prematura (FOP) es un sindrome caracterizado por amenorrea hipergonadotrófica antes de los 40 años. Las causas del desarrollo de FOP pueden ser autoinmunes, genéticas, cromosómicas e idiopáticas. Es importante identificar marcadores para predecir la cesación prematura de los ciclos y planear una concepción temprana.
Palabras clave: falla ovárica prematura; síndrome de ovario resistente a las gonadotrofinas; autoinmunidad ovárica; gen R-FSH; gen inhibina α; gen FMR-1.
Summary
Premature ovarian failure (POF) is defined as hyper-gonadotropic amenorrhea before the age of 40. The causes of POF development could be autoimmune, genetic, chromosomic and idiopathic. It is important to identify markers that can predict the premature cessation of menses and enable early conception planning.
Key words: premature ovarian failure; resistant ovary syndrome; ovarian autoimmunity; R-FSH gen; inhibin-α gen; FMR-1 gen.
Resumo
A falência ovariana prematura (FOP) é uma síndrome caracterizada por amenorreia hipergonadotrófica antes dos 40 anos. As causas do desenvolvimento de FOP podem ser autoimunes, genéticas, cromossômicas e idiopáticas. É importante identificar marcadores para predizer a cessação prematura dos ciclos e planificar uma concepção precoce.
Palavras chave: falência ovariana prematura; síndrome de ovário resistente às gonadotrofinas; autoimunidade ovariana; gene R-FSH; gene inibina α; gene FMR-1.
Introducción
La falla ovárica prematura (FOP) es una patología que afecta al 1% de las mujeres en edad fértil, caracterizada por presentar amenorrea primaria o secundaria antes de los 40 años, hipoestrogenismo e hipergonadotrofismo, con distintos grados de atresia folicular. Es un sindrome muy heterogéneo y de patogénesis multicausal. Entre las causas de FOP se hallan alteraciones cromosómicas, enzimáticas, causas iatrogénicas, infecciosas o autoinmunidad. Asimismo y debido a la presencia de varios casos de FOP en una misma familia, se ha sugerido que este sindrome podría ser de origen genético.
Se ha propuesto al sindrome de ovario resistente a las gonadotrofinas (SOR) como una forma folicular de FOP, el cual se caracteriza por la presencia de numerosos folículos primordiales morfológicamente normales en los ovarios. Dado que las estructuras foliculares se encuentran conservadas en el SOR, sería teóricamente posible la recuperación de la función ovárica, ya sea de forma espontánea o inducida.
Presentación clínica
La FOP puede presentarse con amenorrea primaria o secundaria. Las mujeres con defectos cromosómicos en general presentan amenorrea primaria. Sin embargo, si el defecto se presenta con cierto grado de mosaicismo, las pacientes pueden poseer algo de tejido gonadal funcional que conduciría a distintos grados de desarrollo sexual y a ciclicidad menstrual transitoria.
En muchos casos, la falla ovárica se desencadena después de una historia menstrual normal con posibilidades incluso de fertilidad. En otras mujeres, la amenorrea ocurre después del parto o de la suspensión de tratamientos con anticonceptivos orales. Su aparición no es un fenómeno de "todo o nada" y el diagnóstico definitivo de su comienzo es difícil de establecer. En los últimos años, algunos autores prefieren el término "disfunción ovárica prematura" (DOP) o "insuficiencia ovárica prematura" (IOP) para describir un curso clínico progresivo hacia la cesación de la función ovárica. Asimismo, la deficiencia en los esteroides sexuales que se observa en este síndrome puede conducir a un riesgo elevado de osteoporosis, de enfermedad cardiovascular, así como a la pérdida de fertilidad debida en la mayoría de los casos, a la ausencia de folículos.
Etiología
La falla ovárica prematura puede ocurrir como consecuencia de: a) una reducción del tamaño del reservorio folicular inicial; b) un aumento de la atresia folicular; c) una interrupción en la maduración de los folículos. Las causas del desarrollo de FOP pueden ser: autoinmunes (~15%), genéticas (~ 20%), cromosómicas (~5%) e idiopáticas (~60%). Nuestro grupo de trabajo se ha dedicado al estudio de las causas inmunológicas y genéticas del desarrollo de FOP.
I- CAUSAS INMUNOLÓGICAS
El ovario humano puede ser blanco de procesos autoinmunes en varias circunstancias. Uno de los elementos en la identificación de la etiología autoinmune de FOP es la detección de anticuerpos circulantes dirigidos hacia antígenos del ovario, junto con la asociación a otras enfermedades autoinmunes, sistemáticas u órgano-específicas. En algunas pacientes, hay también una documentación histológica de infiltrado linfocitario en sus ovarios (1). Cuando la FOP se asocia a autoinmunidad adrenal (2-10% de los casos) las pacientes presentan anticuerpos circulantes a células esteroideas (SCA) (2). Los mismos reconocen células productoras de esteroides en la corteza adrenal, testículo, placenta y ovario, y se correlacionan con la falla gonadal.
Sin embargo, en los casos de FOP no asociado a autoinmunidad adrenal y en los casos de FOP aislado, es necesario detectar autoanticuerpos circulantes dirigidos a antígenos del ovario como marcadores de autoinmunidad ovárica. En estudios previos de nuestro laboratorio, mediante una técnica de Western blot en fracción citosólica de ovarios humanos, detectamos reacción positiva hacia una proteína de aproximadamente 54 KDa, en el 19,1% de una población de 110 pacientes FOP. Esta proteína fue identificada como enolasa-α (3). No se ha podido establecer aún si estos anticuerpos anti-ovario son causa o consecuencia del proceso que conduce a la FOP y actualmente, su utilidad clínica es controvertida.
Por otro lado, el SOR puede considerarse un caso raro de FOP autoinmune dado que el mismo presenta inmunoglobulinas circulantes dirigidas al receptor de la hormona folículo estimulante (Ig-RFSH) (4). En un estudio retrospectivo de 247 pacientes FOP, 23 de las cuales fueron diagnosticadas como SOR, hallamos que todas las pacientes SOR presentaron este anticuerpo (5). Esta inmunoglobulina bloquea la unión de FSH a sus receptores o a un sitio muy próximo, impidiendo su acción (4). Estos datos son consistentes con las manifestaciones histopatológicas de las pacientes SOR y podrían explicar la resistencia de los folículos a la acción de la FSH.
II- CAUSAS GENÉTICAS
El gen del R-FSH ha sido uno de los genes candidatos más estudiados. La primera mutación fue descripta en el exón 7 de este gen, en mujeres con disgenesia ovárica hipergonadotrófica pertenecientes a 6 familias de Finlandia (6). Hasta el presente se han descripto 8 mutaciones inactivantes del gen del R-FSH, todas ellas en casos aislados. En nuestros trabajos, no detectamos mutaciones en la secuencia codificante completa del gen R-FSH en los individuos analizados (7). Estos datos son coincidentes con estudios realizados en otras poblaciones, sugiriendo que las mutaciones en el gen del R-FSH son poco frecuentes en las pacientes FOP. Asimismo, se conocen dos sitios polimórficos en el exón 10 del gen del R-FSH que dan lugar a 2 isoformas del receptor. Nuestros resultados indicaron que los polimorfismos del exón 10 no representan un factor de riesgo para el desarrollo de FOP, si bien, la presencia de una isoforma particular del receptor estaría asociada a una forma más severa del sindrome (8).
Por su parte, el gen de la inhibina alfa ha sido propuesto como otro gen candidato para el desarrollo de FOP, debido al rol de las inhibinas en la regulación de la FSH. En este gen se han descripto un polimorfismo y una sustitución, los cuales se han asociado al desarrollo de la enfermedad. Sin embargo, resultados de nuestro laboratorio estarían indicando que estas variantes no constituyen un factor de riesgo para la enfermedad ya que no hallamos asociación de los mismos con la aparición de FOP en nuestra población (9).
Otro de los genes candidatos propuestos es el gen FMR-1. Este gen se encuentra en el cromosoma X y se caracteriza por poseer en su región 5´ no codificante un número variable de trinucleótidos CGG. Los individuos normales poseen hasta 50 repeticiones CGG, mientras que la expansión en más de 200 repeticiones (mutación completa) es responsable del "síndrome de fragilidad del X" (SFX), una forma de retardo mental. Los alelos que contienen entre 50-200 repeticiones son considerados premutados y pueden expandirse a mutación completa en una generación. Las mujeres con alelos premutados en el gen FMR-1 tienen un riesgo aumentado de desarrollar FOP. De hecho, se ha estimado que la incidencia de FOP entre las mujeres portadoras de la premutación es de alrededor del 15% (10). Por otro lado, aproximadamente 4% de las mujeres afectadas de FOP son portadoras de la premutación en el gen FMR-1. Nuestros estudios sobre 100 pacientes FOP y 156 controles, mostraron la presencia de tripletes expandidos de este gen en 7 pacientes FOP de nuestra población. Teniendo en cuenta la posibilidad de descendencia del SFX, se aconseja solicitar el estudio de la zona repetitiva CGG del gen FMR-1 a las pacientes FOP, a los efectos de brindar asesoramiento genético (11).
Tratamiento
El criterio actual para mujeres con FOP es la terapia de reemplazo hormonal hasta la edad fisiológica de la menopausia (50 años) con el objeto de cubrir el déficit estrogénico de sus ovarios y disminuir el riesgo de osteoporosis y enfermedad cardiovascular. Además, se suplementa con testosterona para mejorar la función sexual. Alrededor de 5-10% de las mujeres con FOP logran ovulación y embarazos espontáneos, razón por la cual se debe proteger al ovario con esta terapia y no privar a la paciente de esa posible fertilidad. Los tratamientos con clomifeno, gonadotrofinas, agonistas de GNRH o inmunosupresores, no mejoraron significativamente la posibilidad de embarazos, y en consecuencia, se han dejado de usar. Existen sólo algunos casos reportados de pacientes FOP autoinmunes que han recuperado el ciclo menstrual y embarazo con la terapia inmunosupresora (12). Actualmente, el tratamiento de elección para recuperar la fertilidad de la mujer con FOP es la donación de óvulos mediante el proceso de reproducción asistida. También se propone la criopreservación de ovocitos para su posterior crecimiento y maduración in vitro.
Desarrollos futuros
El entendimiento de los posibles mecanismos que conducen a la FOP contribuirían al diagnóstico temprano de esta condición, para así lograr la protección de los folículos antes del desarrollo de la misma. Es importante identificar marcadores que puedan predecir la cesación prematura de los ciclos y planear una concepción temprana.
Referencias bibliográficas
1. Coulam CB. The prevalence of autoimmune disorders among patients with primary ovarian failure. Am J Reprod Immunol 1983; 4: 63-6.
2. Betterle C, Volpato M. Adrenal and ovarian autoimmunity. Eur J Endocrinol 1998; 138: 16-25.
3. Sundblad V, Bussmann L, Chiauzzi VA, Pancholi V, Charreau EH. Alpha-enolase: a novel autoantigen in patients with premature ovarian failure. Clin Endocrinol (Oxf) 2006; 65(6): 745-51.
4. Chiauzzi VA, Cigorraga S, Escobar ME, Rivarola MA, Charreau EH. Inhibition of follicle-stimulating hormone receptor binding by circulating immunoglobulins. J Clin Endocrinol Metab 1982; 54: 1221-8.
5. Chiauzzi VA, Bussmann L, Calvo JC, Sundblad V, Charreau EH. Circulating immunoglobulins that inhibit the binding of follicle-stimulating hormone to its receptor: a putative diagnostic role in resistant ovary syndrome? Clin Endocrinol 2004; 61: 46-54.
6. Aittomaki K, Lucena JL, Pakarinen P, Sistonen P, Tapanainen JS, Gromoll J, et al. Mutation in the follicle-stimulating hormone receptor gene causes hereditary hypergonadotropic ovarian failure. Cell 1995; 82: 959-68.
7. Sundblad V, Chiauzzi VA, Escobar ME, Dain L, Charreau EH. Screening of FSH receptor gene in Argentine women with premature ovarian failure (POF). Mol Cell Endocrinol 2004; 222 (1-2): 53-9.
8. Sundblad V, Chiauzzi VA, Andreone L, Campo S, Charreau EH, Dain L. Role of polymorphisms 919A>G and 2039A>G of FSH receptor (FSHR) gene in premature ovarian failure (POF) development. Curr Trends Endocrinol 2010; 4: 21-7.
9. Sundblad V, Chiauzzi VA, Andreone L, Campo S, Charreau EH, Dain L. Controversial role of inhibin alpha-subunit gene in the aetiology of premature ovarian failure. Hum Reprod 2006; 21: 1154-60.
10. Wittenberger MD, Hagerman RJ, Sherman SL, McConkie-Rosell A, Welt CK, Rebar RW, et al. The FMR1 premutation and reproduction. Fertil Steril 2007; 87 (3): 456-65.
11. Chiauzzi VA, Ferder I, Alba L, Belli S, Escobar ME, Charreau EH, Dain L. Estudios de la región 5´UTR en pacientes con falla ovárica prematura. Revista Argent de Endocrinol y Metab 2010; 47(4): 3-10.
12. Sundblad V, Chiauzzi VA, Charreau EH. Autoimmune Diseases in Endocrinology. Premature Ovarian Failure. Weetman AP, Editor. Totowa NJ: Human Press Inc., 2007; Chapter 13, 297-321.
LABORATORIO DE MECANISMOS MOLECULARES DE LA FERTILIZACIÓN
Mecanismos moleculares involucrados en el proceso de fertilización
Molecular mechanisms involved in the fertilization process
Mecanismos moleculares envolvidos no processo de fertilização
Débora J. Cohen, Julieta A. Maldera, Mariana Weigel Muñoz, Juan I. Ernesto, Gustavo Vasen, María A. Battistone, Patricia S. Cuasnicu
Resumen
El proceso de fertilización en mamíferos involucra una serie de interacciones entre el espermatozoide y el ovocito mediadas por mecanismos de tipo ligando-receptor. Una de las moléculas mediadoras del proceso de fertilización es la proteína epididimaria CRISP1 (Cysteine Rich Secretory Protein 1), la cual se asocia con dos afinidades diferentes a los espermatozoides durante la maduración. Mientras la población débilmente unida al espermatozoide se libera durante la capacitación, la población fuertemente unida, se comporta como una proteína integral de membrana, permanece en el espermatozoide luego de la capacitación, y participa en el proceso de interacción de gametas. Recientes estudios indican que, si bien los ratones knockout para CRISP1 son fértiles, sus espermatozoides exhiben menores niveles de fosforilación de proteínas en tirosina durante la capacitación, como así también una significativamente menor capacidad de interactuar tanto con la zona pellucida como con la membrana plasmática del ovocito (fusión). Dado que la proteína testicular CRISP2 también participa en el proceso de fusión, la misma sería la candidata más probable a compensar la falta de CRISP1 en el animal knockout. En conjunto, nuestros resultados apoyan la idea de diferentes roles para una misma proteína CRISP, y la cooperación entre proteínas CRISP homólogas con el fin de garantizar el éxito de la fertilización.
Palabras clave: espermatozoide; ovocito; fertilización.
Summary
Mammalian fertilization involves a series of sperm-egg interactions mediated by ligand-receptor mechanisms. One of the molecules proposed to participate in this process is epididymal protein CRISP1 (Cysteine Rich Secretory Protein 1) which associates with two different affinities with sperm during maturation. While the loosely bound population is released from the cell during capacitation, the strongly bound population behaves as an integral protein, remains on the sperm after capacitation, and participates in gamete interaction. Recent results revealed that although CRISP1 knockout mice are fertile, their sperm exhibit lower levels of protein tyrosine phosphorylation during capacitation as well as a significantly reduced ability to interact with both ZP and the oolema (fusion). Considering evidence showing that testicular CRISP2 also participates in gamete fusion, this protein is a likely candidate to compensate for the lack of CRISP1 in knockout mice. Together, these results support the idea of different roles for the same CRISP protein, and a functional cooperation between homologous CRISP proteins to ensure the success of fertilization.
Key words: sperm; egg; fertilization.
Resumo
O processo de fertilização em mamíferos envolve uma série de interações entre o espermatozoide e o ovócito mediados por mecanismos de tipo ligando-receptor. Uma das moléculas mediadoras do processo de fertilização é a proteína epididimária CRISP1 (Cysteine Rich Secretory Protein 1), a qual se associa com duas afinidades diferentes aos espermatozoides durante a maduração. Enquanto a população unida de forma fraca ao espermatozoide se libera do espermatozoide durante a capacitação, a população fortemente unida se comporta como uma proteína integral de membrana, permanece no espermatozoide depois da capacitação, e participa no processo de interação de gametas. Recentes estudos indicam que embora os camundongos knockout para CRISP1 sejam férteis, seus espermatozoides exibem menores níveis de fosforilação de proteínas em tirosina durante a capacitação, bem como uma significativamente menor capacidade de interagir tanto com a zona pelúcida quanto com a membrana plasmática do ovócito (fusão). Visto que a proteína testicular CRISP2 também participa no processo de fusão, a mesma seria a candidata mais provável a compensar a falta de CRISP1 no animal knockout. Em conjunto, nossos resultados apoiam a ideia de diferentes papéis para uma mesma proteína CRISP, e a cooperação entre proteínas CRISP homólogas visando a garantir o êxito da fertilização.
Palavras chave: espermatozoide; ovócito; fertilização.
El proceso de fertilización involucra una serie de interacciones entre el espermatozoide y el ovocito mediadas por mecanismos de tipo ligando-receptor entre moléculas complementarias presentes en las membranas de ambas gametas (1). Sin embargo, a pesar de la importancia de este proceso, la información acerca de la identidad de las moléculas involucradas es aún muy escasa (2).
Una de las proteínas postuladas como mediadoras del proceso de fertilización es la proteína epididimaria CRISP1 (32 kDa) (3), la cual se asocia a los espermatozoides a medida que los mismos transitan por el epidídimo (4). Originalmente localizada en la región dorsal de la cabeza del espermatozoide, CRISP1 migra al segmento ecuatorial con la ocurrencia de la reacción acrosomal (5). Dado que el segmento ecuatorial es la región por la cual el espermatozoide se fusiona con el ovocito, se investigó el posible papel de CRISP1 en este paso específico de la fertilización. Los resultados indicaron que tanto la presencia de anti-CRISP1, como de la proteína CRISP1 purificada, durante la co-incubación de gametas, inhibía significativamente la fusión espermatozoide-ovocito sin afectar la etapa de unión entre ambas gametas (6). Estos resultados no sólo confirmaron la participación de CRISP1 en la etapa de fusión sino también la existencia de sitios complementarios para esta proteína en la membrana plasmática del ovocito (oolema). Ensayos posteriores de inmunoflorescencia indirecta permitieron detectar la presencia de dichos sitios en toda la superficie del ovocito, excepto en una región a la que se denominó área negativa y que resultó coincidente con la región por la cual el espermatozoide no se fusiona con el ovocito (6). De este modo, mientras la proteína CRISP1 estaría localizada en la región fusogénica del espermatozoide, sus sitios complementarios se localizarían en la región fusogénica del ovocito. Estos resultados representaron una importante contribución al campo de la fusión de gametas ya que constituyeron la primera evidencia de la existencia de sitios específicos para una proteína del espermatozoide en la superficie del ovocito de mamíferos. Posteriores resultados indicaron que CRISP1 se asociaría a la membrana del espermatozoide con dos afinidades diferentes, dando lugar a la presencia de dos poblaciones sobre la gameta: una población mayoritaria, asociada débilmente por interacciones iónicas y que se libera de la célula durante el proceso de capacitación, y una población fuertemente unida que corresponde a la proteína que migra al segmento ecuatorial y que participa en el proceso de fertilización (7). La relevancia de CRISP1 para la fertilidad fue confirmada por experimentos en los cuales ratas inmunizadas con CRISP1 presentaban anticuerpos específicos contra la proteína, y una inhibición significativa de la fertilidad en ambos sexos (8).
CRISP1 recibe este nombre por haber sido el primer miembro descripto de la familia de proteínas denominadas CRISP (Proteínas Secretorias Ricas en Cisteínas), las cuales poseen un total de 16 cisteínas, 10 de las cuales se localizan en el extremo C-terminal de la molécula. Resultados de nuestro laboratorio indican que, al igual que CRISP1 de rata, las proteínas homólogas de ratón y humano también participan en el proceso de fusión de gametas a través de sitios de unión en la superficie de los respectivos ovocitos (9)(10). Posteriores estudios de nuestro grupo revelaron que, además de su rol en el proceso de fusión de gametas, CRISP1 también participaría en la etapa previa de interacción espermatozoide-zona pellucida (ZP) a través de su interacción con sitios complementarios presentes en la ZP (11).
Mientras se ha encontrado que el dominio C-terminal de varias proteínas CRISP presenta la capacidad de regular canales iónicos (12), resultados de nuestro laboratorio indican que el dominio N-terminal contendría el sitio por el cual CRISP1 se une a la membrana plasmática del ovocito (13). Más aún, hemos encontrado que dicha actividad reside en una región de sólo 12 aminoácidos que corresponde a una secuencia consenso compartida por todas las proteínas CRISP, denominada Signature 2 (13). Por su parte, nuestras observaciones indican que la capacidad de CRISP1 de interactuar con la ZP no residiría en una región específica de la molécula sino que dependería de su conformación (11). En conjunto, no sólo habría dos poblaciones de CRISP1 sobre el espermatozoide sino también dos dominios en la molécula con dos actividades diferentes. Mientras la capacidad de unirse al ovocito se encontraría asociada a la proteína fuertemente unida y residiría en el dominio N-terminal, la proteína débilmente unida al espermatozoide cumpliría un rol en el proceso de capacitación regulando canales iónicos a través del dominio C-terminal. Recientes resultados de nuestro grupo indican que la población de CRISP1 débilmente unida al espermatozoide, se asociaría a través de la formación de un complejo entre la proteína y el zinc (14), mientras que la población fuertemente unida, lo haría a través de los epididimosomas presentes en el fluido epididimario (resultados no publicados).
Con el fin de confirmar la importancia de CRISP1 para la fertilización, nuestro laboratorio generó animales knockout (KO) para la proteína CRISP1 estudiando posteriormente su fenotipo. Los estudios indicaron que, si bien los animales KO eran fértiles, los espermatozoides presentaban una marcada disminución en el nivel de fosforilación de proteínas en tirosina, evento clave dentro del proceso de capacitación de los espermatozoides como así también exhibían una disminución significativa en su capacidad de interactuar con la ZP y fusionarse con el oolema, consistente con los roles propuestos para CRISP1 en el proceso de fertilización (15). Asimismo, la exposición de ovocitos a espermatozoides KO en presencia de diversas proteínas CRISP disponibles en el laboratorio indicó que, además de CRISP1, otras proteínas homólogas estarían cooperando con CRISP1 para garantizar el éxito de la fertilización. En base a resultados de nuestro grupo indicando que la proteína testicular CRISP2, altamente homóloga a CRISP1, también participa en el proceso de fusión (16), CRISP2 sería la candidata más probable a compensar la falta de CRISP1 en el animal KO.
En conjunto, nuestros resultados apoyan la idea de diferentes roles para una misma proteína CRISP, y la participación de diferentes proteínas CRISP en un mismo evento reproductivo (Figura 1). Dado que los espermatozoides son células inactivas a nivel transcripcional, es probable que esta redundancia funcional exista en el espermatozoide como un mecanismo para garantizar el éxito de un evento esencial como lo es la fertilización.
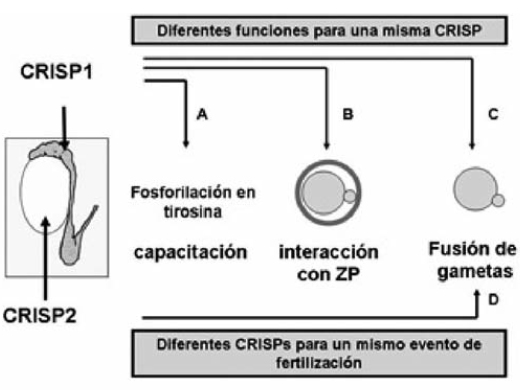
Figura 1. Representación esquemática de las funciones de las proteínas CRISP en fertilización: La proteína epididimaria CRISP1 cumpliría funciones a nivel de A: la regulación de la fosforilación de proteínas en tirosina durante la capacitación, B: la unión del espermatozoide a la zona pellucida (ZP) y C: la fusión de gametas, mientras que la proteína testicular CRISP2 cooperaría con CRISP1 en el evento de fusión (D).
Referencias bibliográficas
1. Kaji K, Kudo A. The mechanism of sperm-oocyte fusion in mammals. Reproduction 2004; 127: 423-9.
2. Okabe M, Cummins JM. Mechanisms of sperm-egg interactions emerging from gene-manipulated animals. Cell Mol Life Sci 2007; 64(15): 1945-58.
3. Cameo MS, Blaquier JA. Androgen-controlled specific proteins in rat epididymis. J Endocr 1976; 69: 317-24.
4. Kohane AC, Cameo MS, Piñeiro L, Garberi JC, Blaquier JA. Distribution and site of production of specific proteins in the rat epididymis. Biol Reprod 1980; 23: 181-7.
5. Rochwerger L, Cuasnicu PS. Redistribution of a rat sperm epididymal glycoprotein after in vivo and in vitro capacitation. Mol Reprod Dev 1992; 31: 34-41.
6. Rochwerger L, Cohen DJ, Cuasnicú PS. Mammalian sperm-egg fusion: The rat egg has complementary sites for a sperm protein that mediates gamete fusion. Dev Biol 1992; 153: 83-90.
7. Cohen DJ, Rochwerger L, Ellerman DA, Morgenfeld M, Busso D, Cuasnicu PS. Relationship between the association of rat epididymal protein DE with spermatozoa and the behavior and function of the protein. Mol Reprod Dev 2000; 56(2): 180-8.
8. Ellerman DA, Brantua VS, Martinez SP, Cohen DJ, Conesa D, Cuasnicu PS. Potential contraceptive use of epididymal proteins: immunization of male rats with epididymal protein DE inhibits sperm fusion ability. Biol Reprod 1998; 59: 1029-36.
9. Cohen DJ, Ellerman DA, Busso D, Morgenfeld M, Piazza A, Hayashi M, et al. Evidence that human epididymal protein ARP plays a role in gamete fusion through complementary sites on the surface of the human egg. Biol Reprod 2001; 65: 1000-5.
10. Cohen DJ, Ellerman DA, Cuasnicú PS. Mammalian sperm-egg fusion: evidence that epididymal protein DE plays a role in mouse gamete fusion. Biol Reprod 2000; 63: 462-8.
11. Busso D, Cohen DJ, Maldera JA, Dematteis A, Cuasnicu PS. A novel function for CRISP1 in rodent fertilization: Involvement in sperm-zona pellucida interaction. Biol Reprod 2007; 77(5): 848-54.
12. Gibbs GM, Roelants K, O'Bryan MK. The CAP super-family: cysteine-rich secretory proteins, antigen 5, and pathogenesis-related 1 proteins roles in reproduction, cancer, and immune defense. Endocr Rev 2008; 29(7): 865-97.
13. Ellerman DA, Cohen DJ, Da Ros VG, Morgenfeld MM, Busso D, Cuasnicu PS. Sperm protein "DE" mediates gamete fusion through an evolutionarily conserved site of the CRISP family. Dev Biol 2006; 297(1): 228-37.
14. Maldera JA, Vasen G, Ernesto JI, Weigel-Munoz M, Cohen DJ, Cuasnicu PS. Evidence for the Involvement of zinc in the association of crisp1 with sperm during epididymal maturation in rats. Biol Reprod 2011.
15. Da Ros VG, Maldera JA, Willis WD, Cohen DJ, Goulding EH, Gelman DM, et al. Impaired sperm fertilizing ability in mice lacking Cysteine-RIch Secretory Protein 1 (CRISP1). Dev Biol 2008; 320(1): 12-8.
16. Busso D, Goldweic NM, Hayashi M, Kasahara M, Cuasnicu PS. Evidence for the involvement of testicular protein CRISP2 in mouse sperm-egg fusion. Biol Reprod 2007; 76(4): 701-8.
LABORATORIO DE BIOLOGÍA CELULAR Y MOLECULAR DE LA REPRODUCCIÓN
Mecanismos moleculares relacionados con la exocitosis acrosomal en espermatozoides de mamíferos
Molecular mechanisms associated with mammalian sperm acrosomal exocytosis
Mecanismos moleculares relacionados com a exocitose acrossomal em espermatozoides de mamíferos
Mariano G. Buffone, Ana Romarowski, Florenza A. La Spina.
Resumen
Los espermatozoides de mamífero adquieren capacidad fecundante durante su paso por el tracto femenino en un proceso denominado ¨capacitación¨ espermática. Durante este proceso, el espermatozoide adquiere la capacidad de realizar la ¨exocitosis acrosomal¨ que permite penetrar la zona pellucida (matriz extracelular que rodea al ovocito). En el proceso de exocitosis acrosomal, la membrana acrosomal externa y la membrana plasmática se fusionan en múltiples puntos, produciéndose la liberación y dispersión del contenido acrosomal. Esta exocitosis es un tipo particular de secreción regulada, que comparte mucho de los mismos mecanismos básicos que se han descrito en otras células secretoras, como neuronas o células del sistema endocrino. Durante la capacitación, se ha observado que el espermatozoide atraviesa estadios intermedios de exocitosis acrosomal con una exposición gradual de componentes intra-acrosomales. Este fenómeno se da coincidentemente con una estabilización de las estructuras involucradas, de manera tal que la exocitosis se produzca sólo en respuesta al estímulo adecuado. A pesar de que se han descripto numerosos cambios bioquímicos asociados al proceso de capacitación y exocitosis, la pregunta que aún no ha podido ser contestada es: ¿cuáles son los cambios bioquímicos esenciales que transforman un espermatozoide sin capacidad de realizar exocitosis acrosomal ante un estímulo fisiológico (no capacitados) en una célula capaz de hacerlo (capacitados)? Asimismo, durante la capacitación se produce una polimerización de la actina globular (G) en filamentosa (F) en la cabeza del espermatozoide, sitio donde además, han sido identificados numeroso componentes relacionados con el citoesqueleto de actina. El citoesqueleto de actina actúa como un modulador de la exocitosis en diversos sistemas celulares. Nuestros resultados preliminares indican que la polimerización de la actina es necesaria para que los espermatozoides puedan formar los estadios intermedios de exocitosis y eventualmente, reaccionar ante el estímulo adecuado.
Palabras clave: espermatozoide; exocitosis acrosomal; citoesqueleto de actina.
Summary
Mammalian sperm must undergo a process termed capacitation in order to become competent to fertilize an egg. Capacitation renders the sperm competent by priming the cells to undergo an exocytotic event called acrosomal exo-cytosis that is stimulated by the zona pellucida (ZP) of the egg. During exocytosis, the outer acrosomal membrane (OAM) and the plasma membrane (PM) fuse, resulting in the release of the acrosomal components. Although many aspects of acrosomal exocytosis are similar to exocytosis in other cell types, there are also some major differences. As incubation under capacitating conditions proceeds, sperm progresses through intermediate stages of acrosomal exocytosis that lead to the incremental exposure and eventual release of selected acrosomal components. The formation of these intermediate stages is coincidental with stabilization of a primed event (membrane docking/fusion) so that the exocytosis is restricted to and occurs only in response to a specific stimulus (ZP). Over many years, several biochemical events have been associated with the capacitation process; however, the question that has remained unanswered in investigations of capacitation is: what is the underlying reaction or set of reactions that transform the sperm cell from a state unresponsive to ZP-stimulated acrosomal exocytosis to the state primed to respond to these stimuli? During the course of capacitation, sperm intracellular globular (G)-actin is polymerized to filamentous (F)-actin. In other systems, the cortical actin network acts as a dominant negative clamp which blocks constitutive exocytosis. Preliminary results suggest that actin polimerization is essential for acrosomal exocitosis to occur.
Key words: spermatozoon; acrosomal exocytosis; actin cytoskeleton.
Resumo
Os espermatozoides de mamífero adquirem capacidade fecundante durante sua passagem pelo trato feminino num processo denominado ¨capacitação¨ espermática. Durante este processo, o espermatozoide adquire a capacidade de realizar a ¨exocitose acrossomal¨ que permite penetrar a zona pelúcida (matriz extracelular que rodeia o ovócito). No processo de exocitose acrossomal, a membrana acrossomal externa e a membrana plasmática se fundem em múltiplos pontos, produzindo-se a liberação e dispersão do conteúdo acrossomal. Esta exocitose é um tipo particular de secreção regulada, que muito compartilha dos mesmos mecanismos básicos que se têm descrito em outras células secretoras, como neurônios ou células do sistema endócrino. Durante a capacitação, foi observado que o espermatozoide atravessa estádios intermediários de exocitose acrossomal com uma exposição gradual de componentes intra-acrossomais. Este fenômeno se dá em coincidência com uma estabilização das estruturas envolvidas de maneira tal que a exocitose seja produzida só em resposta ao estímulo adequado. Apesar de que foram descritas numerosas alterações bioquímicas associadas ao processo de capacitação e exo-citose, a pergunta que ainda não pôde ser respondida é: quais são as alterações bioquímicas essenciais que transformam um espermatozoide sem capacidade de realizar exocitose acrossomal diante de um estímulo fisiológico (não capacitados) numa célula capaz de fazê-lo (capacitados)? Do mesmo modo, durante a capacitação se produz uma polimerização da actina globular (G) em filamentosa (F) na cabeça do espermatozoide, lugar onde também, têm sido identificados numerosos componentes relacionados com o citoesqueleto de actina. O citoesqueleto de actina age como um modulador da exocitose em diversos sistemas celulares. Nossos resultados preliminares indicam que a polimerização da actina é necessária para que os espermatozoides possam formar os estádios intermediários de exocitose e eventualmente, reagir diante do estímulo adequado.
Palavras chave: espermatozoide; exocitose acrossomal; citoesqueleto de actina.
Exocitosis acrosomal
Los espermatozoides de mamíferos adquieren capacidad fecundante durante su paso por el tracto femenino en un proceso denominado capacitación espermática (1). Este proceso puede también ocurrir in vitro en medios definidos que emulan la composición del fluído oviductal. Varios eventos han sido asociados al proceso de capacitación, entre los que se encuentran los cambios en el patrón de movimiento (hiperactividad), cambios en la localización de proteínas, incremento en la fluidez de membrana y en la permeabilidad a ciertos iones como calcio y bicarbonato, fosforilación de proteínas, principalmente en tirosina, y polimerización de la actina G a F en la cabeza del espermatozoide (2).
Mediante la capacitación, el espermatozoide adquiere la competencia para realizar la exocitosis acrosomal que le permite penetrar la zona pelúcida, matriz extracelular que rodea al ovocito, en donde la membrana acrosomal externa (MAE) y la membrana plasmática (MP) se fusionan en múltiples puntos produciéndose la liberación y dispersión del contenido acrosomal. Este mecanismo de exocitosis es un tipo particular de secreción regulada que comparte características similares con mecanismos básicos descriptos en otras células secretoras, como neuronas o células del sistema endócrino. Las diferencias esenciales son: 1) el acrosoma es una vesícula secretoria única; 2) se forman múltiples puntos de fusión entre la membrana acrosomal externa (MAE) y la plasmática (MP); 3) esta fusión forma vesículas híbridas que son liberadas al medio circundante durante la exocitosis; 4) no existe reciclado de las membranas luego de la exocitosis acrosomal, siendo éste un proceso irreversible.
ESTADÍOS INTERMEDIOS DE EXOCITOSIS ACROSOMAL
Durante la capacitación, el espermatozoide atraviesa estadíos intermedios de exocitosis acrosomal con una exposición gradual de componentes intra-acrosomales. Estudios realizados mediante microscopía electrónica de transmisión sobre espermatozoides humanos en proceso de exocitosis acrosomal revelaron seis estadios intermedios (3). Más recientemente, Zanetti y Mayorga (4) han mostrado cambios morfológicos graduales en la formación de vesículas híbridas previo a la exocitosis completa, con un hinchamiento del acrosoma durante la capacitación que disminuye la distancia entre las dos membranas y que, posiblemente, facilite el anclaje o formación de los poros de fusión.
En especies como ratón y cobayo, se han descripto cuatro estadíos intermedios que representan sucesivos pasos hacia una exocitosis completa (5). Utilizando ratones transgénicos que expresan en forma soluble la proteína fluorescente verde (GFP) en sus acrosomas como herramienta para evaluar la integridad acrosomal, Kim y Gerton (5) han demostrado mediante el uso de esferas conjugadas con anticuerpos anti-sp56 (proteína de la matriz acrosomal) la relación temporal entre cuatro estadíos intermedios de exocitosis. Los espermatozoides comienzan con proteína GFP en sus acrosomas y sin unir esferas con el anticuerpo anti-sp56. Luego, atraviesan dos estadíos intermedios en los cuales comienzan a mostrar unión a las esferas demostrando la exposición de la proteína sin perdida del contenido acrosomal para, posteriormente, perder la proteína GFP y seguir mostrando unión a las esferas, ya que la matriz acrosomal continúa asociada a la cabeza del espermatozoide por un cierto tiempo luego de realizada la exocitosis acrosomal. Finalmente, todos los espermatozoides pierden la asociación con las esferas anti-sp56 debido a la completa liberación de la matriz acrosomal.
Consistente con la idea de que existen estadíos intermedios de exocitosis, reportes previos han definido cuatro patrones de tinción con el colorante clortetraciclina (6). Los espermatozoides no capacitados poseen el patrón "N", los capacitados sin reaccionar el patrón "B", los capacitados en vías de sufrir exocitosis acrosomal el patrón "S" y los reaccionados el patrón "AR". Los patrones B y S representan estadíos intermedios de exocitosis y los espermatozoides pueden ser atrapados químicamente en estos estadíos mediante el uso de diferentes sustancias. Estudios electromicroscópicos del estadío "S" revelaron que las membranas MAE y MP comienzan a unirse.
El espermatozoide capacitado podría formar pequeñas regiones de fusión que llevan a una creciente exposición y eventual liberación de los componentes acrosomales. Dos modelos celulares para estudiar este fenómeno son las células lactotropas de la glándula pituitaria de rata y las células secretoras de insulina INS-I. Ambas células forman poros estables de fusión que persisten por períodos prolongados de tiempo. En estos dos modelos hay un retraso entre la apertura del poro de fusión y la liberación de los contenidos vesiculares (7). En espermatozoides de mamíferos existen evidencias que apoyarían este concepto como son los estudios de Flaherty y Olson (8). Estos autores preincubaron espermatozoides de cobayo en un medio libre de calcio y en presencia de lisolecitina. Luego, agregaron calcio para estimular la exocitosis acrosomal de manera sincronizada. Utilizando microscopía electrónica, observaron que la fusión entre la MAE y la MP no ocurría en el segmento apical del acrosoma y sí en las zonas periféricas.
La formación de estadíos intermedios durante la capacitación podría representar el anclaje de la membrana acrosomal externa con la membrana plasmática, que es necesario para que se lleve a cabo el proceso de fusión de membranas de la exocitosis acrosomal. Este proceso de formación de estadíos intermedios se da conjuntamente con una estabilización de estas estructuras por mecanismos aún no conocidos, de manera tal que la exocitosis se produzca sólo en respuesta al estímulo adecuado.
CITOESQUELETO DE ACTINA EN ESPERMATOZOIDES Y SU RELACIÓN CON LA EXOCITOSIS
En otros sistemas celulares, se ha demostrado que el citoesqueleto de actina actúa como una barrera que bloquea la exocitosis constitutiva. Mediante el uso de un sistema de imágenes con excitación por dos fotones, se ha observado que los gránulos de fusión de células acinares del páncreas son rápidamente recubiertos de actina-F. Esta malla de actina-F disminuye la tasa de fusión sin afectar el proceso fisiológico global de exocitosis, estabilizando las estructuras participantes en la fusión.
En espermatozoides de mamíferos, la actina se encuentra presente en su forma monomérica (actina-G) y polimerizada o filamentosa (actina-F). La actina ha sido identificada en el espacio acrosomal, la región ecuatorial y postacrosomal así como también en la cola del espermatozoide (8). Durante la capacitación se produce una polimerización de la actina globular (G) en filamentosa (F) en la cabeza del espermatozoide (2). Este fenómeno, sumado a la presencia de numerosas proteínas relacionadas con actina en el espermatozoide, sugeriría que el citoesqueleto de actina participa activamente en la función espermática.
Usando membranas aisladas de espermatozoides, Spungin y colaboradores (9) demostraron que la inducción de la exocitosis acrosomal en espermatozoides capacitados de ratón, produce una rápida desaparición de la actina-F. Esta despolimerización sería promovida por el marcado aumento de calcio que se produce durante la exocitosis acrosomal. La inhibición de la polimerización de actina que ocurre durante la capacitación inhibe la exocitosis acrosomal. Estos resultados sugerirían que la polimerización de actina es necesaria para que la exocitosis ocurra, y que una vez que la actina ha sido polimerizada a la forma F, debe ocurrir una rápida despolimerización para que la exocitosis pueda ocurrir. Si bien otros han demostrado el rol de las proteínas SNAREs y la synaptotagmina en los estadíos finales de fusión de las dos membranas (10), aún no se conoce el mecanismo que explique el movimiento o acercamiento de las membranas que precede a la formación de los puntos de fusión. El citoesqueleto de actina juega un papel importante en la exocitosis de diversos tipos celulares, y se piensa que el mismo es importante para posicionar las membranas de los gránulos secretorios en proximidad con la membrana plasmática, pero que en un estadío posterior, los filamentos de actina deben disociarse para permitir el contacto entre las dos membranas. Esta polimerización de la actina durante la capacitación espermática podría estar participando en este acercamiento de las membranas intervinientes en la fusión, para que los demás eventos moleculares puedan llevarse a cabo.
Referencias bibliográficas
1. Austin CR. Observations on the penetration of the sperm in the mammalian egg. Aust J Sci Res 1951 (B); 4(4): 581-96.
2. Brener E, Rubinstein S, Cohen G, Shternall K, Rivlin J, Breitbart H. Remodeling of the actin cytoskeleton during mammalian sperm capacitation and acrosome reaction. Biol Reprod 2003.; 68(3): 837-45.
3. Stock CE, Fraser LR. The acrosome reaction in human sperm from men of proven fertility. Hum Reprod 1987; 2(2): 109-19.
4. Zanetti N, Mayorga LS. Acrosomal swelling and membrane docking are required for hybrid vesicle formation during the human sperm acrosome reaction. Biol Reprod 2009; 81(2): 396-405.
5. Kim KS, Gerton GL. Differential release of soluble and matrix components: evidence for intermediate states of secretion during spontaneous acrosomal exocytosis in mouse sperm. Dev Biol 2003; 264(1): 141-52.
6. Lee MA, Storey BT. Evidence for plasma membrane impermeability to small ions in acrosome-intact mouse spermatozoa bound to mouse zonae pellucidae, using an aminoacridine fluorescent pH probe: time course of the zona-induced acrosome reaction monitored by both chlortetracycline and pH probe fluorescence. Biol Reprod 1985; 33(1): 235-46.
7. Angleson JK, Cochilla AJ, Kilic G, Nussinovitch I, Betz WJ. Regulation of dense core release from neuroen-docrine cells revealed by imaging single exocytic events. Nat Neurosci 1999; 2(5): 440-6.
8. Flaherty SP, Olson GE. Membrane domains in guinea pig sperm and their role in the membrane fusion events of the acrosome reaction. Anat Rec 1988; 220(3): 267-80.
9. Spungin B, Margalit I, Breitbart H. Sperm exocytosis reconstructed in a cell-free system: evidence for the involvement of phospholipase C and actin filaments in membrane fusion. J Cell Sci 1995; 108 ( Pt 6): 2525-35.
10. De Blas GA, Roggero CM, Tomes CN, Mayorga LS. Dynamics of SNARE assembly and disassembly during sperm acrosomal exocytosis. PLoS Biol 2005; 3(10): e323.
LABORATORIO DE QUÍMICA DE PROTEOGLICANOS Y MATRIZ EXTRACELULAR
El papel de los glicosaminoglicanos en el proceso de descondensación cromatínica del espermatozoide humano
Role of glycosaminoglycans in sperm chromatin decondensation in humans.
O papel dos glicosaminoglicanos no processo de descondensação cromatínica do espermatozoide humano
Marina Romanato, Vanina Julianelli, Bárbara Farrando, Lucrecia Calvo, Juan Carlos Calvo
Resumen
En el núcleo del espermatozoide, la cromatina se encuentra de 6 a 8 veces más condensada que en los núcleos de las células somáticas. Esta condensación es el resultado del intercambio de histonas por protaminas durante el proceso de formación de los espermatozoides, otorgando al material genético una resistencia única al ataque por especies reactivas de oxígeno como también al estrés que significa el trayecto hasta su encuentro con el ovocito en el oviducto. Esta condensación tan alta debe ser relajada, una vez producida la fecundación del ovocito, para permitir la formación del pronúcleo masculino y la posterior singamia. Para que ocurra la descondensación es necesaria la reducción de los puentes disulfuro de las protaminas, reacción que lleva a cabo el glutatión y, además, la remoción de las protaminas con intercambio posterior o concomitante por las histonas ovocitarias. En este punto, todavía no hay consenso sobre la molécula involucrada. En nuestro laboratorio postulamos que sería el heparán sulfato, basados en análisis de descondensación in vitro, en las características estructurales de la molécula y en su presencia en el ovocito murino, con evidencias preliminares de su presencia también en el ovocito humano (datos no mostrados).
Palabras clave: glicosaminoglicanos; cromatina; descondensación; espermatozoides; heparán sulfato.
Summary
In the sperm nucleus, chromatin is 6 to 8 times more condensed than in the nuclei of somatic cells. This high condensation is the result of the exchange between histones and protamines during the process of spermatogenesis, and provides the genetic material with unique resistance to the attack of reactive oxygen species, as well as to the stress of the voyage towards the encounter with the oocyte in the oviduct. This high condensation must be relaxed, once the fertilization of the oocyte has taken place, in order to allow for the formation of male pronucleus and subsequent syngamy. For the decondensation to occur, it is necessary to reduce the disulfide bonds in the protamines, reaction that takes place with the assistance of glutathione, and also to remove the pro-tamines with the subsequent or concomitant exchange with oocyte histones. At this point, there is no consensus regarding the molecule involved in this process. In these studies, it has been postulated that this molecule is heparan sulfate, based on in vitro decondensation studies, on the structural characteristics of the molecule and the fact that it is present in the murine oocyte, with preliminary evidence of its presence also in the human oocyte (data not shown).
Key words: glycosaminoglycans; chromatin; decondensation; spermatozoa; heparan sulfate.
Resumo
No núcleo do espermatozoide, a cromatina se encontra de 6 a 8 vezes mais condensada que nos núcleos das células somáticas. Esta condensação é o resultado da troca de histonas por protaminas durante o processo de formação dos espermatozoides, outorgando ao material genético uma resistência única ao ataque por espécies reativas de oxigênio bem como ao estresse que significa o trajeto até seu encontro com o ovócito no oviduto. Esta condensação tão alta deve ser relaxada, assim que é produzida a fecundação do ovócito, para permitir a formação do pronúcleo masculino e a posterior singamia. Para que ocorra a descondensação é necessária a redução das pontes dissulfeto das protaminas, reação que leva a cabo o glutation e, também, a remoção das protaminas com troca posterior ou concomitante pelas histonas oocitárias. Neste ponto, ainda não há consenso sobre a molécula envolvida. No nosso laboratório postulamos que seria o heparan sulfato, baseados em análises de descondensação in vitro, nas características estruturais da molécula e em sua presença no ovócito murino, com evidências preliminares de sua presença também no ovócito humano (dados não mostrados).
Palavras chave: glicosaminoglicanos; cromatina; descondensação; espermatozoides; heparan sulfato.
Introducción
La función de la gameta masculina en el proceso de fertilización no culmina con la penetración al ooplasma, sino que requiere además la fusión de su material genético con el material genético del ovocito. Para lograrlo, el núcleo del espermatozoide, una vez ingresado al ovocito, sufre una serie de cambios ultraestructurales que culminan con la formación del pronúcleo masculino. Es conocido el alto grado de condensación de la cromatina espermática, comparado con el de las células somáticas, y el impacto que la misma tiene en la protección del material genético de las especies reactivas de oxígeno, como también de los daños físicos durante el tránsito hacia el encuentro con el ovocito en las trompas. Con el objetivo de explicar las fallas de fertilización observadas en procedimientos de reproducción asistida, surgió en la última década, el interés por estudiar más detalladamente el núcleo del espermatozoide, el proceso de descondensación nuclear y los factores espermáticos y ovocitarios involucrados en dicho proceso. Esto es particularmente cierto con el advenimiento del ICSI, pues ya no interesa si el espermatozoide puede interactuar eficazmente con el cúmulus, la zona pelúcida o el oolema y cobran especial importancia todos los procesos que ocurren una vez que el espermatozoide se encuentra dentro del ooplasma.
ORGANIZACIÓN CROMATÍNICA DEL NÚCLEO ESPERMÁTICO
El núcleo del espermatozoide presenta una organización muy particular de la cromatina, diferente de la de las células somáticas (1)(2). La cromatina espermática se encuentra altamente condensada debido a que durante la espermatogénesis testicular, la mayor parte de las histonas es reemplazada por proteínas transicionales y luego por protaminas. Estas son proteínas más pequeñas (50-60 aminoácidos), más básicas que las histonas y con un alto contenido de residuos de cisteína y arginina que neutralizan muy eficazmente las cargas del ADN y permiten su mayor compactación. El complejo altamente condensado de protamina - ADN es estabilizado por uniones disulfuro intra e intermoleculares entre los residuos de cisteína de las protaminas, confiriendo al núcleo espermático de una extraordinaria estabilidad mecánica y química. De esta forma se impediría la descondensación prematura de la cromatina durante el tránsito del espermatozoide por el tracto genital masculino y el femenino, antes de incorporarse definitivamente al ooplasma, y además se protegería al ADN espermático de la acción de agentes mutagénicos.
Se han descripto dos grupos de protaminas, P1 y P2. Las P1 están presentes en los espermatozoides de todas las especies y tienen un alto contenido de cisteína y arginina, mientras que las P2 que están presentes en algunas especies (incluyendo el humano), contienen histidina además de cisteína y arginina y pueden unir Zn2+.
La importancia de una adecuada interacción protamina /ADN espermático en el proceso de fertilización ha quedado confirmada por la observación que ratones knockout para P1 o P2 son infértiles (3). En el hombre, se ha documentado la presencia de una relación P1/P2 alterada o incluso la ausencia de P2 en individuos infértiles (4)(5). Por otra parte, el eyaculado comúnmente contiene cantidades variables de espermatozoides que no han reemplazado la mayoría de sus histonas o proteínas transicionales por protaminas (6-8), cuyos núcleos se conocen generalmente como núcleos inmaduros (9), observándose que el eyaculado de hombres infértiles contiene una mayor proporción de los mismos que el de hombres fértiles (10)(11).
LA DESCONDENSACIÓN DEL NÚCLEO ESPERMÁTICO
El núcleo del espermatozoide se descondensa rápidamente luego de su penetración en el ovocito (12). La reducción de los puentes disulfuro, por el glutatión (GSH) presente en el ovoplasma, sería el primer paso de la descondensación del núcleo espermático en el ovocito. Esta reducción es necesaria pero no suficiente para que se produzca la descondensación nuclear. Se ha propuesto la participación de una macromolécula con fuerte carga negativa que pueda competir con el ADN por las protaminas, y actuar como aceptora de las mismas, posibilitando así el reemplazo de las protaminas espermáticas por histonas ovocitarias.
La descondensación de la cromatina del espermatozoide humano in vitro puede inducirse utilizando heparina y GSH (13)(14). No existe duda de la participación del GSH como tiorreductor en este proceso, pero el papel de la heparina es aún motivo de controversia, proponiéndose una interacción de tipo ligando-receptor (15-18) o un efecto directo sobre la cromatina del espermatozoide, ya que se ha demostrado que la heparina posee una fuerte afinidad por las protaminas y es capaz de combinarse con éstas formando un complejo insoluble (19). Sin embargo, ninguna de las evidencias existentes es directa y contundente. Unos de los puntos a considerar es que no se ha encontrado heparina en el complejo cumulus-ovocito y que la única célula capaz de sintetizar heparina in vivo es el mastocito. Sin embargo, existen en la literatura numerosas evidencias de la presencia de otros glicosaminoglicanos (GAGs) en el complejo cumulus - oocito en distintas especies (20-23). Entre ellos, el heparán sulfato (HS) es un análogo estructural de la heparina que posee en muchos sistemas biológicos acciones equivalentes a la misma (24-27). Las evidencias experimentales acumuladas en nuestro laboratorio en los últimos años, nos han llevado a plantear la hipótesis de que el HS efectivamente podría actuar como aceptor de protaminas durante la descondensación cromatínica del espermatozoide humano in vivo (14)(28).
EL HEPARÁN SULFATO COMO ACEPTOR DE PROTAMINAS
En nuestro laboratorio, estudiamos desde hace varios años, la descondensación nuclear del espermatozoide humano in vitro, a fin de dilucidar el papel de la heparina en este proceso. Utilizando muestras de semen de donantes normospérmicos de acuerdo con los criterios establecidos por la Organización Mundial de la Salud (29) y mediante un ensayo de descondensación nuclear originariamente descrito por Reyes et al. (13) y luego modificado en nuestro laboratorio (14), se evaluó la capacidad descondensante de distintas heparinas y otros GAGs sobre espermatozoides humanos capacitados y sobre núcleos aislados a partir de dichos espermatozoides. El comportamiento de los núcleos aislados, situación que se asemeja más a lo que ocurre in vivo debido a que el núcleo se encuentra desnudo dentro del ooplasma antes de descondensarse, fue, en todos los casos, semejante al de los espermatozoides enteros.
La actividad descondensante de la heparina se vio fuertemente afectada por la sulfatación de la molécula, y los resultados sugirieron que se trata no sólo de un efecto de carga neta sino que también es importante la posición de las cargas en la molécula (14)(28). También evaluamos el efecto del tamaño de la molécula de heparina sobre su capacidad descondensante, encontrándose que la actividad descondensante de la heparina era independiente de su peso molecular, por lo menos dentro del rango de pesos moleculares estudiado (3000-18800 Da) (14)(28)).
Una vez demostrado que la actividad descondensante de la heparina in vitro está relacionada con características estructurales de la molécula, evaluamos la actividad descondensante de otros GAGs presentes en el complejo cumulus-ovocito con el fin de encontrar algún equivalente a la heparina in vivo. Sólo el HS, análogo estructural de la heparina, mostró actividad descondensante in vitro, mientras que el ácido hialurónico, el condroitín sulfato y el dermatán sulfato fueron inactivos (14)(28). Más aún, la actividad descondensante de la heparina y del heparán sulfato fueron similares, a pesar del hecho que el heparán sulfato se encuentra levemente menos sulfatado que la heparina, y posee menor carga negativa neta.
El conjunto de estos resultados nos llevó a proponer que el HS, presente en el complejo cumulus-oocito y además análogo estructural de la heparina (25)(30)(31), podría estar funcionando como aceptor de protaminas en el proceso de descondensación del núcleo espermático humano in vivo. Recientemente (32) encontramos que el heparán sulfato se encuentra presente en el citoplasma del ovocito murino, siendo este un punto clave para nuestros estudios presentes y futuros. Mientras tanto, el papel del heparán sulfato en la descondensación nuclear in vivo es una hipótesis factible.
Referencias bibliográficas
1. Balhorn R. A model for the structure of chromatin in mammalian sperm. J Cell Biol 1982; 93: 298-305.
2. Ward WS, Coffey D. DNA packaging and organization in mammalian spermatozoa: comparison with somatic cells. Biol Reprod 1991; 44: 569-74.
3. Cho C, Willis WD, Goulding EH, Jung-Ha H, Choi YC, Hecht NB, et al. Haploinsufficiency of protamine 1 or 2 causes infertility in mice. Nat Genet 2001; 28: 82-6.
4. Belokopytova IA, Kostyleva EI, Tomilin AN, Vorob'ev VI. Human male infertility may be due to a decrease of the protamine P2 content in sperm chromatin. Mol Reprod Dev 1993; 34: 53-7.
5. Yebra L, Ballesca JL, Vanrell JA, Bassas L, Oliva R. Complete selective absence of protamine P2 in humans. J Biol Chem 1993; 268: 10553-7.
6. Tanphaichitr N, Sobhon P, Taluppeth N, Chalermis-arachai P. Basic nuclear proteins in testicular cells and ejaculated spermatozoa in man. Exp Cell Res 1978; 117: 347-56.
7. Chevaillier PH, Mauro N, Feneux D, Jouannet P, David G. Anomalous protein complement of sperm nuclei in some infertile men. The Lancet 1987. Octubre, 3.
8. Gatewood JM, Cook GR, Balhorn R, Bradbury EM, Schmid CW. Sequence-specific packaging of DNA in human sperm chromatin. Science 1987; 236: 962-4.
9. Kramer JA, Krawetz SA. RNA in spermatozoa: implications for the alternative haploid genome. Mol Hum Reprod 1997; 3: 473-8.
10. Foresta C, Zorzi M, Rossato M, Varotto A. Sperm nuclear instability and staining with aniline blue: abnormal persistence of histones in spermatozoa in infertile men. Int J Androl 1992; 15: 330-7.
11. Auger J, Schoevaert D, Negulesco I, Dadoune JP. The nuclear status of human sperm cells by TEM image cytometry: nuclear shape and chromatin texture in semen samples from fertile and infertile men. J Androl 1993; 14: 456-63.
12. Jager S. Sperm nuclear stability and male infertility. Arch Androl 1990; 25: 253-9.
13. Reyes R, Rosado A, Hernandez O, Delgado NM. Heparin and glutathione: physiological decondensing agents of human sperm nuclei. Gamete Res 1989; 23: 39-47.
14. Romanato M, Cameo MS, Bertolesi G. Heparan sulphate: a putative decondensing agent for human spermatozoa in vivo. Hum Reprod 2003; 18: 1868-73.
15. Delgado NM, Reyes R, Huacuja L, Merchant H, Rosado A. Heparin binding sites in the human spermatozoa membrane. Arch Androl 1982; 8: 87-95.
16. Handrow RR, Boehm SK, Lenz RW, Robinson JA, Ax RL. Specific binding of the glycosaminoglycan 3H-heparin to bull, monkey, and rabbit spermatozoa in vitro. J Androl 1984; 5: 51-63.
17. Lalich RA, Vedantham S, McCormick N, Wagner C, Prins GS. Relationship between heparin binding characteristics and ability of human spermatozoa to penetrate hamster ova. J Reprod Fertil 1989; 86: 297-302.
18. Lassalle B, Testart J. Relationship between fertilizing ability of frozen human spermatozoa and capacity for heparin binding and nuclear decondensation. J Reprod Fertil 1992; 95: 313-24.
19. Chargaff E, Olson KB. Studies on the chemistry of blood coagulation. VI. Studies on the action of heparin and other coagulants. The influence of protamine on the anticoagulant effect in vivo. J Biol Chem 1938; 122: 153-67.
20. Gebauer H, Lindner HR, Amsterdam A. Synthesis of heparin-like glycosaminoglycans in rat ovarian slices. Biol Reprod 1978; 18: 350-8.
21. Salustri A, Yanagishita M, Hascall VC. Synthesis and accumulation of hyaluronic acid and proteoglycans in the mouse cumulus cell-oocyte complex during follicle-stimulating hormone-induced mucification. J Biol Chem 1989; 264: 13840-7.
22. Ball GD, Bellin ME, Ax RL, First NL. Glycosaminoglycans in bovine cumulus-oocyte complexes: morphology and chemistry. Mol Cell Endocrinol 1982; 28: 113-22.
23. Bellin ME, Ax RL. Chondroitin sulfate: an indicator of atresia in bovine follicles. Endocrinology 1984; 114: 428-34.
24. Delgado NM, Sanchez-Vazquez ML, Reyes R, Merchant-Larios H. Nucleons, I: A model for studying the mechanism of sperm nucleus swelling in vitro. Arch Androl 1999; 43: 85-95.
25. Jackson RL, Busch SJ, Cardin AD. Glycosaminoglycans: molecular properties, protein interactions, and role in physiological processes. Physiol Rev 1991; 71: 481-539.
26. Rosemberg RD, Shworak NW, Liu J, Schwartz JJ, Zhang LJ. Heparan sulfate proteoglycans of the cardiovascular system. J Clin Invest 1997; 99: 2062-70.
27. Yanagishita M, Hascall VC. Cell surface heparan sulfate proteoglycans. J Biol Chem 1992; 267: 9451-4.
28. Romanato M, Regueira E, Cameo MS. Further evidence on the role of heparan sulfate as protamine acceptor during the decondensation of human spermatozoa. Hum Reprod 2005; 20: 2784-9.
29. OMS. WHO Laboratory Manual for the Examination of Human Semen and Sperm-Cervical Mucus Iinteraction, 4th edn. Cambridge, UK, Cambridge University Press; 1999.
30. Bellin ME, Ax RL, Laufer N, et al. Glycosaminoglycans in follicular fluid from women undergoing in vitro fertilization and their relationship to cumulus expansion, fertilization, and development. Fertil Steril 1986; 45: 244-8.
31. Eriksen GV, Malmstrom A, Uldbjerg N. Human follicular fluid proteoglycans in relation to in vitro fertilization. Fertil Steril 1997; 68: 791-8.
32. Romanato M, Julianelli V, Zappi M, Calvo L, Calvo JC. The presence of heparan sulfate in the mammalian oocyte provides a clue to human sperm nuclear decondensation in vivo. Human Reproduction 2008; 23: 1145-50.
LABORATORIO DE INMUNOLOGÍA DE LA REPRODUCCIÓN
Caracterización del endometrio y del ambiente peritoneal de mujeres que padecen endometriosis. Estudios in vivo e in vitro de nuevas alternativas terapéuticas para esta enfermedad
Characterization of endometrial and peritoneal environment of women with endometriosis. In vivo and in vitro studies of new therapeutic alternatives for this disease
Caracterização do endométrio e do ambiente peritoneal de mulheres que padecem endometriose. Estudos in vivo e in vitro de novas alternativas terapêuticas para esta doença
Gabriela Meresman, Mariela Bilotas, Carla Olivares, Analía Ricci, Juan Ignacio Bastón, Rosa Inés Barañao
Resumen
El tema de estudio de nuestro laboratorio es la endometriosis, patología benigna que afecta alrededor de un 15% de las mujeres en edad reproductiva y que se caracteriza por la presencia de tejido endometrial fuera de la cavidad uterina, provocando fuertes dolores pélvicos, metrorragia y, en un 50% de los casos, infertilidad. Hemos realizado investigaciones básicas sobre el ambiente peritoneal de las mujeres con endometriosis y analizamos las características del tejido endometrial de estas pacientes. En la actualidad continuamos con nuestros estudios tendientes a esclarecer no sólo la posible etiología de la endometriosis sino también a mejorar su tratamiento. Nuestros estudios tienen como objetivo la evaluación del efecto in vitro e in vivo de nuevos mecanismos para tratar esta patología en la búsqueda de nuevas alternativas terapéuticas que ofrezcan tratamientos más simples, con medicamentos que actúen en forma más directa sobre los implantes, que inhiban los mecanismos involucrados en el desarrollo de la enfermedad, y que potencialmente sean más eficaces en su acción de erradicar las lesiones endometriósicas. Además, comenzamos a evaluar los posibles mecanismos involucrados en la tolerancia inmunológica hacia los implantes de tejido endometrial ectópico que se produciría durante el establecimiento de la endometriosis.
Palabras clave: macrófagos; citoquinas; tratamiento; factor de crecimiento del endotelio vascular; ciclooxigenasa 2; aromatasa P450.
Summary
The subject matter of our laboratory is endometriosis, a benign disease that affects around 15% of women of reproductive age, characterized by the presence of endometrial tissue outside the uterine cavity, causing severe pelvic pain, metrorrhagia, and infertility in 50% of the cases. Basic research on the peritoneal environment of women with endometriosis has been conducted and the characteristics of these patients' endometrial tissue was analyzed. Currently, studies to clarify the etiology of the endometriosis but also to improve its treatment still continue. Said studies aim to assess the in vitro and in vivo effects of new mechanisms to treat the condition in the search for new therapeutic alternatives that provide simple treatments with drugs that act more directly on the implants, that inhibit the mechanisms involved in the development of the disease, and which are potentially more effective in their efforts to eradicate endometriotic lesions. Furthermore, the likely mechanisms involved in the immunological tolerance to ectopic endometrial tissue implants that would occur during the establishment of endometriosis started to be assessed.
Key words: macrophages; cytokines; treatment; vascular endotellium growth factor; ciclooxygenase 2; aromatase P450.
Resumo
O tema de estudo de nosso laboratório é a endometriose, patologia benigna que afeta aproximadamente 15% das mulheres em idade reprodutiva e que se caracteriza pela presença de tecido endometrial fora da cavidade uterina, provocando fortes dores pélvicas, metrorragia e, em 50% dos casos, infertilidade. Temos realizado pesquisas básicas sobre o ambiente peritoneal das mulheres com endometriose e analisamos as características do tecido endometrial destas pacientes. Na atualidade continuamos com nossos estudos tendentes a esclarecer não apenas a possível etiologia da endometriose, mas também a melhorar seu tratamento.
Nossos estudos têm como objetivo a avaliação do efeito in vitro e in vivo de novos mecanismos para tratar esta patologia na busca de novas alternativas terapêuticas que ofereçam tratamentos mais simples, com medicamentos que atuem em forma mais direta sobre os implantes, que inibam os mecanismos envolvidos no desenvolvimento da doença, e que potencialmente sejam mais eficazes em sua ação de erradicar as lesões endometrióticas. Também começamos a avaliar os possíveis mecanismos envolvidos na tolerância imunológica para os implantes de tecido endometrial ectópico que se produziria durante o estabelecimento da endometriose.
Palavras chave: macrófagos; citocinas; tratamento; fator de crescimento do endotélio vascular; ciclooxigenase 2; aromatase P450.
El principal tema de investigación de nuestro laboratorio es la endometriosis. Esta patología se caracteriza por la presencia de tejido endometrial fuera de la cavidad uterina formando quistes y/o lesiones ectópicas principalmente en el peritoneo pélvico y ovarios. Es una de las enfermedades ginecológicas benignas más frecuentes en mujeres de edad reproductiva y su etiología aún se mantiene sin elucidar.
En un intento de esclarecer la posible causa de esta enfermedad comenzamos nuestros estudios evaluando el ambiente peritoneal. Como resultado de estas evaluaciones concluimos que el ambiente peritoneal de las pacientes con endometriosis presenta alteraciones tanto en los niveles de citoquinas, estradiol (E2), progesterona (P4) y prostaglandina E2 (PGE2) y en el número y funcionalidad de macrófagos. Este ambiente peritoneal alterado facilitaría la implantación y crecimiento del tejido endometriósico fuera del útero (1)(2). Además observamos que mientras el líquido peritoneal de las pacientes con endometriosis mínima producía un efecto mitogénico sobre la proliferación celular en cultivos de endometrio normal, el líquido peritoneal de pacientes con endometriosis avanzada o severa producía un efecto inhibitorio de dicha proliferación (3)
A continuación evaluamos el tejido endometrial eutópico de estas pacientes y nuestros resultados demostraron que el mismo era menos susceptible a morir apoptosis y que además poseía una proliferación celular aumentada, hechos que lo predispondría a crecer en un sitio ectópico (4).
Posteriormente observamos que, en mujeres con endometriosis, el tratamiento con anticonceptivos orales combinados o bien con progestágenos solos como el desogestrel, producía una disminución de la proliferación celular y un aumento de la apoptosis del tejido endometrial eutópico (5).
Puesto que dentro de los tratamientos comúnmente empleados para esta patología se destacan los agonistas y antagonistas de GnRH, decidimos evaluar el efecto in vitro de ambos análogos de GnRH en cultivos de células de epitelio endometrial y observamos que los agonistas de GnRH estimulaban la apoptosis e inhibían la proliferación celular endometrial (6). Empleando el mismo modelo evaluamos también el efecto de los análogos de GnRH sobre la producción de interleuquina 1 β (IL-1β) y el factor de crecimiento de endotelio vascular (VEGF), como factores promitogénicos, en relación con la apoptosis de las células endometriales en cultivo (7). Asimismo observamos que existiría una regulación de la expresión de proteínas pro y anti-apoptóticas por parte de los agonistas y antagonistas de GnRH (8).
Además de continuar con nuestros estudios in-vitro sobre cultivos primarios de tejido endometrial hemos desarrollado un modelo de endometriosis experimental murina que se basa en el transplante autólogo de tejido endometrial en un sitio ectópico. Este modelo nos permite realizar estudios in-vivo y evaluar el efecto de posibles tratamientos médicos.
El tejido endometrial expresa aromatasa P450, esencial en la biosíntesis de estrógenos. En nuestro laboratorio hemos observado que existe expresión de la enzima aromatasa P450 en las lesiones endometriósicas peritoneales rojas y negras y que la expresión de la aromatasa está significativamente aumentada en el tejido endometrial eutópico de pacientes con endometriosis con respecto a las mujeres controles. Por lo tanto, la actividad de esta enzima favorecería la generación de un ambiente hiperestrogénico que permitiría mayor desarrollo y expansión de la enfermedad. Esto llevó a pensar que el uso de inhibidores de la aromatasa podría tener un potencial terapéutico en estas pacientes.
En nuestros estudios in vitro observamos que los inhibidores de aromatasa (Letrozole y Anastrozole) producen un efecto beneficioso induciendo una significativa disminución de la proliferación celular y un aumento en la apoptosis (9) y en el modelo de endometriosis murino, observamos que el tratamiento con estos inhibidores al inicio de la inducción de las lesiones no impidió el desarrollo de las mismas pero causó una disminución significativa de su tamaño, inhibición de la proliferación celular y aumento de la apoptosis (10). Estos resultados refuerzan la idea de que la inhibición de la aromatasa podría ser una estrategia novedosa de tratamiento de la endometriosis.
Tal como hemos observado en nuestros primeros estudios, en las mujeres con endometriosis existe una alteración del ambiente peritoneal debido al estado inflamatorio producido por la presencia de los focos de tejido endometrial ectópico. Esta inflamación suele producir fuertes dolores y en la actualidad uno de los tratamientos anti-inflamatorios empleados en estas pacientes es el celecoxib, un inhibidor selectivo de la actividad de la ciclo-oxigenasa 2 (COX-2). Por estos motivos decidimos evaluar el efecto de celecoxib sobre la proliferación celular, la apoptosis, la expresión de COX-2 y los niveles de VEGF y PGE2 en cultivos primarios de células epiteliales endometriales. Observamos que el celecoxib indujo una significativa disminución de la proliferación celular y aumento de apoptosis, tanto en los cultivos celulares de pacientes con endometriosis como de controles. De la misma manera, el celecoxib aumentó significativamente la expresión de COX-2 en cultivos de células de epitelio endometrial de pacientes con endometriosis. Además, inhibió significativamente la secreción de VEGF y de PGE2 en células epiteliales endometriales de estas pacientes (11).
Por otra parte, es un hecho conocido que en cualquier tejido u órgano autotransplantado es imprescindible una adecuada irrigación sanguínea para que pueda sobrevivir. Por este motivo, en los últimos años comenzó a cobrar mayor importancia la posibilidad de la regulación de la angiogénesis en endometriosis ya que ésta podría ser una nueva opción terapéutica para esta patología. Uno de los principales factores involucrados en la neovascularización del tejido endometrial ectópico es el VEGF, el cual no sólo sería producido por el mismo tejido endometrial sino también por los macrófagos peritoneales. Por otra parte, la secreción de este factor angiogénico sería estimulada por los esteroides ováricos, particularmente por el aumento de estradiol.
Estos antecedentes nos llevaron a evaluar el efecto de la terapia anti-angiogénica con bevacizumab (un anticuerpo monoclonal humanizado, anti VEGF) en el modelo de endometriosis murino. Observamos que el tratamiento con bevacizumab indujo una disminución significativa en el volumen promedio de las lesiones desarrolladas por ratón así como en los niveles de VEGF del líquido peritoneal. Sin embargo, no se observaron diferencias significativas en el número de lesiones desarrolladas por ratón. Por otra parte, el bevacizumab indujo un aumento altamente significativo de la apoptosis en las lesiones endometriósicas así como una disminución significativa de la proliferación celular en estas lesiones. Nuestros resultados sugieren que si bien el bevacizumab no disminuiría el número de lesiones endometriósicas desarrolladas, reduciría su tamaño, a través de un aumento en la apoptosis y una inhibición en la proliferación celular. Consistentemente, la acción del anticuerpo se ve reflejada en una disminución de los niveles de VEGF.
Actualmente estamos evaluando tanto in vivo como in vitro la acción de dos tratamientos con polifenoles naturales: el resveratrol (Res), una fitoalexina presente en las uvas, y el galato de epigalocatequina (EGCG), catequina más abundante del té verde. Se ha visto que ambos polifenoles poseen propiedades antioxidantes, antiinflamatorias y anticarcinogénicas. Observamos in vivo que EGCG en las distintas dosis ensayadas disminuyó el número y el tamaño de las lesiones desarrolladas por ratón, sin embargo el Res sólo en una concentración de 25 mg/kg disminuyó el tamaño de las lesiones. Por otra parte, observamos in vitro que ambos compuestos indujeron una inhibición de la proliferación de las células de epitelio endometrial. Nuestros resultados sugieren un efecto inhibitorio de Res y EGCG, in vivo e in vitro, sobre el crecimiento del tejido endometrial y avalan seguir investigando estos compuestos como estrategias novedosas para tratar la endometriosis (12).
Finalmente, estamos evaluando una de las posibles vías de escape inmunológico de los implantes endometriósicos. Nuestra hipótesis plantea que la expresión de Galectina-1 (Gal-1) en las lesiones endometriósicas facilita la implantación y sobrevida de las células endometriales en un sitio ectópico. Para ello, en un estudio preliminar, se indujeron lesiones endometriósicas en ratones hembras adultos C57BL/6 wild-type y knock-out para Gal-1 (Lgals1-/-). Luego de cuatro semanas se contó el número de lesiones, se midió el tamaño promedio, se analizó su histopatología y se determinó la proliferación celular en las mismas. Los resultados muestran una reducción significativa del tamaño promedio de las lesiones en los ratones Lgals1-/-, aunque el número de lesiones no fue diferente entre ambos grupos. Asimismo, la tasa de proliferación celular fue significativamente menor en las lesiones de ratones deficientes de Gal-1. Estos resultados sustentan nuestra hipótesis sobre el rol de Gal-1 facilitando el crecimiento y desarrollo de las lesiones endometriósicas al promover la proliferación de las células endometriales ectópicas que forman la lesión.
En síntesis, nuestro laboratorio apunta a investigar los mecanismos fisiopatológicos implicados en la etiología de la endometriosis y estos conocimientos sustentan a su vez, nuestros estudios de nuevas alternativas terapéuticas para tratar esta enfermedad.
Referencias bibliográficas
1. Raiter-Tenenbaum A, Baranao RI, Etchepareborda JJ, Meresman GF, Rumi LS. Functional and phenotypic alterations in peritoneal macrophages from patients with early and advanced endometriosis. Arch Gynecol Obstet 1998; 261(3): 147-57.
2. Tenenbaum A, Barañao RI, Etchepareborda JJ, Lavarello M, Kesseru E, Rumi LS. Functional alterations of peritoneal macrophages in patients with mild endometriosis. Fertility and Sterility. Progress in Research and Practice. Parthenon Publications; 1994.
3. Meresman GF, Baranao RI, Tenenbaum A, Singla JJ, Neuspiller NR, Rumi LS. Effect of peritoneal fluid from patients with mild and severe endometriosis on endometrial stromal cell proliferation. Arch Gynecol Obstet 1997; 259(3): 109-15.
4. Meresman GF, Barañao RI, Buquet RA, Ortiz, J. C-OO, Rum iLS. "Apoptosis of eutopic endometrial tissue is deficient in women with endometriosis" . Proceedings of the 10TH World Congress on Human Reproduction. Monduzzi Editore 1999; 159-65.
5. Meresman GF, Auge L, Baranao RI, Lombardi E, Tesone M, Sueldo C. Oral contraceptives suppress cell proliferation and enhance apoptosis of eutopic endometrial tissue from patients with endometriosis. Fertil Steril 2002; 77(6): 1141-7.
6. Meresman GF, Bilotas M, Buquet RA, Baranao RI, Sueldo C, Tesone M. Gonadotropin-releasing hormone agonist induces apoptosis and reduces cell proliferation in eutopic endometrial cultures from women with endometriosis. Fertil Steril 2003; 80 Suppl 2:702-7.
7. Meresman GF, Bilotas MA, Lombardi E, Tesone M, Sueldo C, Baranao RI. Effect of GnRH analogues on apoptosis and release of interleukin-1beta and vascular endothelial growth factor in endometrial cell cultures from patients with endometriosis. Hum Reprod 2003; 18(9):1767-1771.
8. Bilotas M, Baranao RI, Buquet R, Sueldo C, Tesone M, Meresman G. Effect of GnRH analogues on apoptosis and expression of Bcl-2, Bax, Fas and FasL proteins in endometrial epithelial cell cultures from patients with endometriosis and controls. Hum Reprod 2007; 22(3): 644-53.
9. Meresman GF, Bilotas M, Abello V, Buquet R, Tesone M, Sueldo C. Effects of aromatase inhibitors on proliferation and apoptosis in eutopic endometrial cell cultures from patients with endometriosis. Fertil Steril 2005; 84(2): 459-63.
10. Bilotas M, Meresman G, Stella I, Sueldo C, Baranao RI. Effect of aromatase inhibitors on ectopic endometrial growth and peritoneal environment in a mouse model of endometriosis. Fertil Steril 2010; 93(8): 2513-8.
11. Meresman G, Olivares C, Bilotas M, Buquet R, Sueldo C, Tesone M. Ciclooxygenase-2 (COX-2) inhibitor induces apoptosis and inhibits cell proliferation in endometrial epithelial cells from patients with endometriosis. Fertil Steril 2006; 88(Suppl.2): S264.
12. Ricci AG, Olivares CN, Bilotas MA, Singla JJ, Meresman GF, Barañao RI. Estudio de nuevas terapéuticas naturales posibles para el tratamiento de la endometriosis (EDT). Medicina (Bs As ) 2010; 70(Suppl. II): O69.
LABORATORIO DE FISIOLOGÍA OVÁRICA
Mecanismos fisiológicos y patológicos involucrados en la función y angiogénesis ovárica
Physiological and pathological mechanisms involved in ovarian angiogenesis and funcion
Mecanismos fisiológicos e patológicos envolvidos na função e angiogênese ovariana
Marta Tesone, Fernanda Parborell, Griselda Irusta, Dalhia Abramovich, Diana Bas, Fátima Hernandez, Leopoldina Scotti.
Resumen
El desarrollo y regresión del folículo ovárico es un proceso continuo y cíclico que depende de señales endocrinas, paracrinas, autocrinas y de interacciones célula-célula. El reclutamiento y selección de folículos lleva a la formación de uno o más folículos preovulatorios, cuyo número varía en cada especie. Estos procesos involucran la síntesis de factores locales que producen la selección y maduración de los folículos dominantes desencadenando la ovulación. Luego de la ovulación, se forma el corpus luteum (CL), que es una glándula transciente que se forma de las paredes remanentes del folículo. Si la preñez o embarazo no ocurre, el CL no sigue produciendo progesterona y regresiona en un proceso llamado luteólisis. Aunque todos estos procesos (crecimiento y regresión folicular, desarrollo del CL y luteólisis) requieren cambios en la red vascular ovárica, su regulación aún es debate de investigación. En este estudio, hemos investigado el papel del sistema Notch y su ligando DLL4 en la angiogénesis y su relevancia en la fisiología ovárica. Estos datos se complementaron estudiando si cambios en la regulación de los procesos angiogénicos están involucrados en las alteraciones vasculares observadas en modelos de PCOS (poliquistosis ovárica) y OHSS (síndrome de hiperestimulación ovárica) desarrollados en roedores.
Palabras clave: ovario; angiogénesis; poliquistosis ovárica; síndrome de hiperestimulación ovárica; sistema Notch.
Summary
Ovarian follicular development and regression is a continuous and cyclic process that depends on a number of endocrine, paracrine and autocrine signals. The cyclic recruitment and selection of follicles eventually leads to the formation of one or more preovulatory follicles, whose number varies in each species. These processes, involving a number of locally-produced factors, result in the selection and maturation of the dominant follicles that finally ovulate. After ovulation, the corpus luteum (CL) is the transient endocrine gland that forms from the remaining wall of the ovarian follicle, and if pregnancy does not occur (at the end of each nonfertile ovarian cycle) or when it is no longer required for maintenance of pregnancy, the CL ceases to produce progesterone and regresses in a process called luteolysis. Although all these processes (follicular growth and regression and CL development and luteolysis) require dynamic changes in the ovarian vascular network, their regulation is not well understood. The role of the Notch ligand DLL4 system in angiogenesis and its relevance in ovarian physiology were investigated in this study. These data were complemented by studying whether changes in the angiogenesis regulation are associated with the vascular ovarian alterations observed in PCOS and OHSS models developed in rodents.
Key words: ovary; angiogenesis; polycystic ovaric syndrome; ovarian hyperstimulation syndrome; Notch system.
Resumo
O desenvolvimento e regressão do folículo ovariano é um processo contínuo e cíclico que depende de sinais endócrinos, parácrinos, autócrinos e de interações célula-célula. O recrutamento e seleção de folículos levam à formação de um ou mais folículos pré-ovulatórios, cujo número varia em cada espécie. Estes processos envolvem a síntese de fatores locais que produzem a seleção e amadurecimento dos folículos dominantes desencadeando a ovulação. Depois da ovulação, forma-se o corpus luteum (CL), que é uma glândula transiente que se forma das paredes remanescentes do folículo. Se a prenhez ou gravidez não ocorrer, o CL não continua produzindo progesterona e regride num processo chamado luteólise. Embora todos estes processos (crescimento e regressão folicular, desenvolvimento do CL e luteólise) precisem de modificações na rede vascular ovariana, sua regulação ainda é debate de pesquisa. Neste estudo, temos pesquisado o papel do sistema Notch e seu ligando DLL4 na angiogênese e sua relevância na fisiologia ovariana. Estes dados foram complementados estudando se modificações na regulação dos processos angiogênicos estão envolvidas nas alterações vasculares observadas em modelos de PCOS (policistose ovariana) e OHSS (síndrome de hiperestimulação ovariana) desenvolvidos em roedores.
Palavras chave: ovário; angiogênese; policistose ovariana; síndrome de hiperestimulação ovariana; sistema Notch.
El desarrollo y regresión del folículo ovárico es un proceso continuo y cíclico que depende de señales endocrinas, paracrinas, autocrinas y de interacciones célula-célula. Estos procesos involucran la síntesis de factores locales que producen la selección y maduración de los folículos dominantes desencadenando la ovulación. Luego de la ovulación, las células remanentes del folículo ovárico formarán una glándula endocrina transitoria: el cuerpo lúteo (CL). La principal función del CL en mamíferos es la de secretar progesterona, la cual es esencial para la implantación del blastocisto y mantenimiento de la preñez/embarazo. Sin embargo, si ésta no ocurre o cuando ya no es necesario para el mantenimiento de la placenta, el CL cesa de producir progesterona y regresiona en un proceso llamado luteólisis. La apoptosis juega un papel crítico en la luteólisis y atresia folicular. Además, todos estos procesos (crecimiento y regresión folicular, desarrollo del CL y luteólisis) requieren cambios dinámicos en la red vascular ovárica cuya regulación aún plantea interrogantes.
La apoptosis es un proceso fisiológico que regula el mantenimiento de la homeostasis en organismos multicelulares. Las señales apoptóticas ocurren a través de múltiples caminos independientes que convergen en una maquinaria de destrucción celular. Los factores de crecimiento disparan distintos caminos de transducción de señales que promueven la supervivencia celular o inhiben la apoptosis. Entre éstos, se destacan los mediados por Erk ½ y por PI3K/Akt .
Durante el desarrollo embrionario los vasos sanguíneos se diferencian de precursores endoteliales por medio de una activa vasculogénesis, mientras que en el adulto se originan de vasculatura pre-existente por un proceso denominado angiogénesis. Este proceso ha sido estudiado en patologías como el cáncer, aunque en condiciones fisiológicas la angiogénesis se limita a algunos aspectos de la reproducción, como los cambios cíclicos en el ovario y endometrio uterino. La diferencia entre la angiogénesis patológica y fisiológica recae en la regulación precisa del balance de factores pro- y antiangiogénicos. Durante la neovascularización fisiológica los vasos formados maduran, se estabilizan y detienen su proliferación. Por el contrario, los vasos en condiciones patológicas pierden el balance apropiado entre los reguladores positivos y negativos, no detienen su crecimiento y se encuentran en constante remodelación, dando lugar a un sistema vascular aberrante. En el caso del ovario, los folículos primordiales y primarios reciben nutrientes y oxígenos por difusión pasiva, pero para continuar con su crecimiento más allá de estos estadios los folículos requieren de una vasculatura que se forma alrededor de cada uno de ellos. Esta vasculatura está confinada a la teca de los folículos, siendo la capa de células de la granulosa avascular durante todo el proceso de foliculogénesis. Entre los factores que se encuentran regulando la angiogénesis folicular, uno de los principales es el VEGF (Factor de crecimiento del endotelio vascular). Además, este factor actúa en coordinación con otros factores angiogénicos como ANGPT (Angiopoyetinas), PDGF (Factor de crecimiento derivado de plaquetas) y FGF2 (Factor de crecimiento fibroblástico). A medida que el desarrollo folicular continúa estos factores aumentan sus niveles permitiendo así, un intenso desarrollo de la vasculatura luego de la ovulación. En nuestro laboratorio hemos demostrado que factores angiogénicos ováricos (VEGF y Angiopo-yetina 1) tienen un papel protector de la atresia folicular mediado por inhibición de la apoptosis [1-3], además que el camino PI3K/Akt está involucrado en el efecto de VEGF [3].
El sistema Notch es un camino de señalización que incluye comunicación intercelular y regula la homeostasis de células embrionarias, la proliferación y la muerte celular. El sistema está formado por cuatro receptores (Notch1-4) y cinco ligandos (Jagged1, -2; Deltalike 1 (DLL1), DLL3 y DLL4), todas proteínas de membrana. Los receptores Notch, una vez que interactúan con los ligandos, sufren una serie de clivajes por diferentes enzimas. Estos culminan, por acción de la enzima γ-secretasa, en la liberación del dominio intracelular del receptor el cual se transloca al núcleo donde actúa sobre genes blanco de la familia Hes y Hey. Los ratones deficientes en alguno de estos componentes, mueren durante la embriogénesis con defectos en el remodelamiento vascular [4]. En estudios realizados en mamíferos donde los receptores Notch están constitutivamente activos, se ha observado que los mismos regulan la proliferación, diferenciación y apoptosis de varios tipos celulares.
Se ha descripto la interacción entre componentes del sistema Notch y la angiogénesis. En particular el ligando DLL4, los receptores Notch1, Notch4 y el Factor de Crecimiento del Endotelio Vascular A (VEGF) están involucrados en este proceso. Se demostró que la inhibición de la señalización de Notch en ovario de ratón neonatal, disminuyó la formación de folículos primordiales [5].
En carcinomas ováricos se ha observado que tanto Notch 3 como Jagged 2 se encuentran aumentados comparado a epitelio de ovario normal [6] y en tumores de ovario epiteliales se ha observado la presencia de varios elementos de la familia de Notch y la existencia de las formas activadas de estos receptores [7].
Uno de los objetivos del laboratorio es evaluar la acción del sistema Notch sobre el desarrollo folicular, función de las células de granulosa y la angiogénesis ovárica. En relación a esto hemos demostrado que la administración de un inhibidor de la γ secretasa (DAPT) a ratas preñadas, disminuye los niveles séricos de Progesterona, y que este fenómeno está vinculado a la regulación de la vía de Notch, lo cual conduce a la apoptosis del CL [8]. Estos resultados demuestran por primera vez, que la supresión de la vía de Notch causa un efecto directo sobre la función luteal.
En relación a la participación del sistema Notch en el crecimiento e invasión de células de granulosa tumorales (línea celular KGN), resultados preliminares de nuestro grupo demuestran que el DAPT es capaz de inhibir estos procesos en cultivos de esta línea celular.
Otro de los objetivos es dilucidar la participación de diferentes sistemas angiogénicos en la fisiopatología del síndrome de hiperestimulación ovárica (OHSS) y del síndrome de ovario poliquístico (PCOS) y evaluar novedosas alternativas terapéuticas para el tratamiento de estas patologías reproductivas. En estas patologías ha sido descripto un aumento en la producción ovárica de VEGF.
El OHSS es una complicación iatrogénica severa del crecimiento y maduración folicular ocasionada por la inducción de la ovulación con gonadotrofinas en tratamientos de fertilización asistida (ART). Aunque la prevalencia de la forma severa de OHSS es baja (0,3-5% de ciclos de estimulación), es importante destacar que el OHSS es una complicación causada por ART que en algunos casos puede tener resultados fatales. Las características de la enfermedad involucran: aumento en el tamaño del ovario, sobreproducción de hormonas esteroideas y sustancias vasoactivas, contribuyendo de esta manera al aumento de permeabilidad vascular, presencia de ascitis y formación de quistes. Estos quistes son de tejido luteal y hemorrágicos, y probablemente el mecanismo se deba o bien a un aumento de la proliferación/diferenciación de las células foliculares o a la inhibición de la apoptosis.
Cabe resaltar que las concentraciones de VEGFA en fluido peritoneal y folicular en pacientes con riesgo a OHSS se correlacionan con el desarrollo del síndrome.
Varios autores han mostrado que el VEGFA en pacientes que desarrollan OHSS, proviene de un ovario hiperestimulado, siendo la concentración de VEGFA en fluido folicular 100 veces mayor que la observada en suero [9]. También se ha observado en mujeres que desarrollan la enfermedad, que el VEGFA se expresa en células de granulosaluteínicas y se libera al fluido folicular en respuesta a hCG, aumentando la permeabilidad vascular y, por consiguiente, la presencia de ascitis.
En los últimos años, se propuso en el laboratorio el estudio de enfermedades reproductivas femeninas con una angiogénesis alterada como es el caso de OHSS y PCOS. Para ello, se desarrolló en el laboratorio un modelo animal que manifiesta OHSS en ratas inmaduras. Uno de los objetivos fue evaluar como posible estrategia terapéutica, el efecto in vivo de un agonista de GnRH, Acetato de Leuprolide (LA), sobre el desarrollo folicular y la formación del cuerpo lúteo, ya que este tipo de molécula es ampliamente utilizada en la clínica ginecológica. Los resultados mostraron que en el modelo de OHSS desarrollado en rata, el agonista disminuía la expresión de P450scc, StAR, ANGPT-1 y su receptor Tie-2 y afectaba la estabilidad vascular como la proliferación de células del cuerpo lúteo conduciéndolo a la regresión [10]. Por otro lado, en nuestro laboratorio se han observado altos niveles de ANGPT-1 en pacientes sometidas a ART con alta probabilidad de desarrollar OHSS comparado a pacientes controles, lo cual también se ha detectado en folículos periovulatorios provenientes de ratas que desarrollaron la patología de OHSS (resultados preliminares).
El PCOS, por su parte, afecta a un 5 a 10% de las mujeres en edad reproductiva causando infertilidad y se caracteriza porque las pacientes presentan alteraciones endocrinas, metabólicas y reproductivas. Los principales signos y síntomas son hiperplasia de la teca interna y del estroma con excesiva producción de andrógenos, hirsutismo, obesidad, resistencia a insulina, fertilidad disminuida y ovarios poliquísticos hipertrofiados. A pesar de que este síndrome fue descripto hace más de 50 años, aún no se conoce exactamente su etiología. Varios estudios demuestran que las pacientes con PCOS tienen altos niveles de VEGFA en suero y se cree que este factor proviene de una elevada producción ovárica [11]. Se ha demostrado que las mujeres que presentan PCOS tienen aumentado el flujo sanguíneo del estroma ovárico y que esto estaría relacionado al aumento sérico de VEGFA. Además existen mayores niveles de VEGFA en fluido folicular de pacientes con PCOS comparadas con pacientes control [12]. Cabe destacar que las mujeres que presentan PCOS, tienen mayor riesgo de desencadenar OHSS cuando son sometidas a técnicas de fertilización asistida y esto estaría relacionado al aumento de la permeabilidad vascular dada por los altos niveles de VEGFA ováricos y séricos descriptos en estas pacientes. Todas estas características estarían indicando que la angiogénesis juega un rol muy importante en el desarrollo de estas patologías. Cabe mencionar que la hCG no posee actividad vasoactiva por sí misma, por lo tanto, sus acciones deben estar mediadas a través de una o más sustancias angiogénicas liberadas por los ovarios en respuesta a gonadotrofinas. Uno de los candidatos es el VEGF, que es un mediador de la angiogénesis ovárica.
Con estos antecedentes se comenzó a estudiar el efecto del Trap (inhibidor de VEGF) en un modelo de PCOS desarrollado en ratas. Para ello, ratas Sprague Dawley prepúberes fueron inyectadas con DHEA, 6 mg/100 g de peso corporal durante 15 días consecutivos. Este modelo ha sido utilizado para mimetizar el PCOS humano en roedor [13]. Tiene la ventaja de exhibir las principales características ováricas del PCOS, como ser quistes ováricos y alteraciones en la foliculo-génesis, anovulación, ausencia de ciclos menstruales e hiperandrogenismo.
Las ratas PCOS mostraron un aumento en el porcentaje de área de células periendoteliales. El Trap disminuyó el reclutamiento de estas células hasta niveles inferiores a los normales. Se realizó además un recuento folicular para caracterizar las alteraciones en el desarrollo de los folículos ováricos que presentan las ratas PCOS y el efecto del Trap sobre el mismo.
Se observa que en las ratas PCOS, hay un mayor % de folículos primarios a expensas de los FPO y CLs. También se observa una gran cantidad de quistes. El Trap fue capaz de revertir la acumulación de folículos primarios y disminuyó el número de quistes, a pesar de que esto no se vio reflejado en un aumento en el % de folículos ovulados o capaces de ovular. Sin embargo, cuando analizamos el número de ratas que presentaba CLs en cada uno de los grupos, vimos que el Trap logró revertir la disminución en el número de ratas que ovularon hasta un valor no diferente del grupo control.
Estos resultados resultan prometedores para estudiar la interrelación entre distintos mecanismos angiogénicos en el ovario y diseñar novedosas estrategias terapéuticas en patologías reproductivas femeninas con angiogénesis alterada.
Referencias bibliográficas
1. Abramovich D, Parborell F, Tesone M. Effect of a vascular endothelial growth factor (VEGF) inhibitory treatment on the folliculogenesis and ovarian apoptosis in gonadotropin-treated prepubertal rats. Biol Reprod 2006; 75: 434-41.
2. Parborell F, Abramovich D, Tesone M. Intrabursal administration of the antiangiopoietin 1 antibody produces a delay in rat follicular development associated with an increase in ovarian apoptosis mediated by changes in the expression of BCL2 related genes. Biol Reprod 2008; 78: 506-13.
3. Abramovich D, Irusta G, Parborell F, Tesone M. Intra-bursal injection of vascular endothelial growth factor trap in eCG-treated prepubertal rats inhibits proliferation and increases apoptosis of follicular cells involving the PI3K/AKT signaling pathway. Fertil Steril 2010; 93: 1369-1377.
4. Li JL, Harris AL. Notch signaling from tumor cells: a new mechanism of angiogenesis. Cancer Cell 2005; 8: 1-3.
5. Trombly DJ, Woodruff TK, Mayo KE. Suppression of Notch signaling in the neonatal mouse ovary decreases primordial follicle formation. Endocrinology 2009; 150: 1014-24.
6. Lu KH, Patterson AP, Wang L, Marquez RT, Atkinson EN, Baggerly KA, et al. Selection of potential markers for epithelial ovarian cancer with gene expression arrays and recursive descent partition analysis. Clin Cancer Res 2004; 10: 3291-300.
7. Hopfer O, Zwahlen D, Fey MF, Aebi S. The Notch pathway in ovarian carcinomas and adenomas. Br J Cancer 2005; 93: 709-18.
8. Hernandez F, Peluffo MC, Stouffer RL, Irusta G, Tesone M. Role of the DLL4-NOTCH System in PGF2 alpha-induced luteolysis in the pregnant rat. Biol Reprod 2011; 84: 859-65
9. Artini PG, Monti M, Fasciani A, Tartaglia ML, D'Ambrogio G, Genazzani AR. Correlation between the amount of follicle-stimulating hormone administered and plasma and follicular fluid vascular endothelial growth factor concentrations in women undergoing in vitro fertilization. Gynecol Endocrinol 1998; 12: 243-47.
10. Scotti L, Irusta G, Abramovich D, Tesone M, Parborell F. Administration of a gonadotropin-releasing hormone agonist affects corpus luteum vascular stability and development and induces luteal apoptosis in a rat model of ovarian hyperstimulation syndrome. Mol Cell Endocrinol 2011; 335: 116-25.
11. Agrawal R, Jacobs H, Payne N, Conway G. Concentration of vascular endothelial growth factor released by cultured human luteinized granulosa cells is higher in women with polycystic ovaries than in women with normal ovaries. Fertil Steril 2002; 78: 1164-9.
12. Artini PG, Monti M, Matteucci C, Valentino V, Cristello F, Genazzani AR. Vascular endothelial growth factor and basic fibroblast growth factor in polycystic ovary syndrome during controlled ovarian hyperstimulation. Gynecol Endocrinol 2006; 22: 465-70.
13. Bas D, Abramovich D, Hernandez F, Tesone M. Altered expression of Bcl-2 and Bax in follicles within dehydroepiandrosterone-induced polycystic ovaries in rats. Cell Biol Int 2011; 35: 423-9.
LABORATORIO DE ENDOCRINOLOGÍA MOLECULAR TRANSDUCCIÓN DE SEÑALES
Regulación de la función esteroidogénica en testículo y glándula adrenal
Regulation of steroidogenic function in testis and adrenal gland
Regulação da função esteroidogênica em testículo e glândula adrenal
Omar P. Pignataro, Romina Pagotto, Casandra M. Monzón, Marcos Besio, Carolina Mondillo.
Resumen
Si bien las hormonas hipofisarias LH y ACTH son los reguladores primarios de la esteroidogénesis tanto en células de Leydig (CL) como en la zona fasciculada (ZF) adrenal, respectivamente, evidencias crecientes indican que diversos factores, locales y externos, modulan sutilmente (regulación fina) la fisiología de las glándulas esteroidogénicas. El paso regulatorio de la esteroidogénesis es el transporte del colesterol a la membrana interna de la mitocondria para ser transformado a pregnenolona y la proteína StAR es muy importante en este proceso. La presencia de otras poblaciones en testículo (células de Sertoli, peritubulares, macrófagos y mastocitos) y en corteza adrenal (células endoteliales, macrófagos, mastocitos y células de la médula adrenal) llevó a enfocar el estudio hacia compuestos que son secretados por esos tipos celulares o incluso por las propias CL o ZF y que regulan las acciones respectivas de la LH y de la ACTH en forma autócrina y/o parácrina. Nuestro grupo de trabajo ha demostrado que factores tales como óxido nítrico (NO), monóxido de carbono (CO) e Histamina (HA) modulan los efectos de las hormonas adenohipofisarias mencionadas. En ambos órganos, los diversos factores pueden actuar a través de distintos (o similares) sistemas transductores, ya sea para activar o inhibir la síntesis de esteroides. Además de la conocida participación del AMPc, otros segundos mensajeros están involucrados en la respuesta biológica final
Palabras clave: célula de Leydig; células corticoadrenales; esteroidogénesis; óxido nítrico; hemo oxigenasa; histamina.
Summary
Although steroidogenesis in both Leydig (CL) and zona fasciculata (ZF) adrenal cells are under the primary control of pituitary hormones LH and ACTH, respectively, increasing evidence suggests that local or external factors modulate (fine tunning) the physiology of steroidogenic glands. The limiting step in the synthesis of all steroid hormones is the transport of the substrate-cholesterol-from the outer to the inner mitochondrial membrane, where it is converted into pregnenolone. The participation of StAR protein in the mechanism is very important in this process. The presence of other cell types in testis (Sertoli and peritubular cells, macrophages and mast cells) and in the adrenal cortex (endothelial cells, macrophages, mast cells and the near medullary cells) led to focus this study in factors secreted by these cell types or even the same Leydig or ZF cells that are able to modulate LH and ACTH actions in an autocrine or paracrine way. These studies have shown that the NO/NOS, HO/CO and histamine systems modulate the effect of the above mentioned pituitary hormones. These factors can act through similar or different signal transduction pathways to activate or inhibit steroid synthesis. In addition to the very well documented participation of cAMP in the mechanism of action of both hormones, other second messengers are also involved in the generation of the final biological effect.
Key words: Leydig cells; corticoadrenal cells; steroidogenesis; nitric oxide; heme oxygenase; histamine.
Resumo
Embora os hormônios hipofisários LH e ACTH sejam os reguladores primários da esteroidogênese tanto em células de Leydig (CL) quanto na zona fasciculada (ZF) adrenal, respectivamente, evidências crescentes indicam que diversos fatores, locais e externos modulam sutilmente (regulação fina) a fisiologia das glândulas esteroidogênicas. O passo regulatório da esteroidogênese é o transporte do colesterol para a membrana interna da mitocôndria para ser transformado em pregnenolona e a proteína StAR é muito importante neste processo. A presença de outras populações em testículo (células de Sertoli, peritubulares, macrófagos e mastócitos) e em córtex adrenal (células endoteliais, macrófagos, mastócitos e células da medula adrenal) levou a focar o estudo em compostos que são secretados por esses tipos celulares ou inclusive pelas próprias CL ou ZF e que regulam as ações respectivas da LH e da ACTH em forma autócrina e/ou parácrina. Nosso grupo de trabalho tem demonstrado que fatores tais como óxido nítrico (NO), monóxido de carbono (CO) e Histamina (HA) modulam os efeitos dos hormônios adenohipofisários mencionados. Em ambos os órgãos, os diversos fatores podem atuar através de diferentes (ou similares) sistemas transdutores, seja para ativar ou inibir a síntese de esteroides. Além da conhecida participação do AMPc, outros segundos mensageiros estão envolvidos na resposta biológica final
Palavras chave: célula de Leydig; células córtico-adrenais; esteroidogênese; óxido nítrico; hemo oxigenase; histamina.
La función normal del testículo, dependiente de las gonadotrofinas hipofisarias, involucra la producción de espermatozoides en los túbulos seminíferos y la síntesis de andrógenos, principalmente testosterona, en las células intersticiales de Leydig (CL). La producción de testosterona es imprescindible para la función sexual normal, el mantenimiento de los caracteres sexuales secundarios, la espermatogénesis normal, y el mantenimiento de la hematopoyesis y de la masa muscular y ósea.
En los últimos años se ha aceptado que, si bien la hormona luteinizante hipofisaria (LH) es el regulador principal de la esteroidogénesis testicular, factores producidos por las diversas poblaciones celulares del testículo (células de Sertoli, peritubulares, macrófagos y mastocitos) modulan las acciones de la hormona, actuando de forma autócrina y/o parácrina. Dichos factores serían también capaces de modular a la LH en su papel como regulador de la diferenciación y proliferación de las CL inmaduras.
En forma semejante a lo descripto para testículo, si bien la esteroidogénesis adrenal es regulada principalmente por la hormona ACTH, los diversos tipos celulares que conforman la estructura de la corteza y de la médula suprarrenal, secretan compuestos que pueden modular la acción hormonal. Los corticosteroides producidos en respuesta a ACTH (aldosterona en la zona glomerulosa, y cortisol - o corticosterona en roedores-en la zona fasciculada) están implicados en una variedad de mecanismos fisiológicos, incluyendo aquellos que regulan la inflamación, el sistema inmune, el metabolismo de hidratos de carbono, el catabolismo de proteínas, los niveles electrolíticos en plasma y los que caracterizan la respuesta frente al estrés. ACTH es, además, responsable del mantenimiento de la integridad anatómica y funcional de la glándula adrenal, lo cual también estaría sujeto a regulación local.
Sobre la base de publicaciones previas de nuestro grupo de trabajo, los sistemas óxido nítrico sintasa/óxido nítrico (NOS/NO) y hemo oxigenasa/monóxido de carbono (HO/CO) y la histamina (HA), modulan los efectos de las hormonas adenohipofisarias mencionadas
1- SISTEMAS NOS/NO Y HO/CO
El NO es un radical libre inorgánico gaseoso, cuya función como mensajero intracelular ha sido ampliamente establecida en una gran variedad de tipos celulares. La enzima oxido nítrico sintasa (NOS) cataliza la síntesis de NO y L-citrulina a partir de L-arginina. Se han identificado al menos tres isoformas de NOS, producto de tres genes distintos: la nNOS (NOSI), la iNOS (NOSII) y la eNOS (NOSIII). El NO modula la esteroidogénesis en células granulosas-luteales del ovario humano y en células de zona glomerulosa adrenal. Trabajos propios y de otros grupos han demostrado que el NO regula la síntesis de esteroides en CL, en ZF de rata y en células glomerulosas bovinas (1-4). En particular, el trabajo de Del Punta et al. de 1996 tiene 137 citaciones según la base de datos Scopus, de las cuales 52 son en los últimos 5 años, lo cual muestra la vigencia y reconocimiento de nuestros resultados
Por su parte, se ha propuesto al CO, producido por el clivaje oxidativo del hemo, como un modulador con funciones semejantes a las del NO. El CO es producido en la reacción catalizada por la HO, en la que se genera asimismo biliverdina e hierro. Clásicamente se ha asociado esta actividad enzimática con el catabolismo de hemoproteínas. Sin embargo, en forma más reciente, se han descripto efectos citoprotectores relacionados con la actividad de HO. Hasta el momento se han caracterizado tres isoformas de la enzima: la HO-1 o inducible y las HO-2 y 3 que son constitutivas. Resultados de nuestro grupo y de otros han permitido la identificación de HO-1 y de HO-2 en células de ZF adrenal de rata, en la línea celular Y1, y en CL tumorales MA-10 y normales de rata (5)(6). Dado que la HO regula los niveles celulares de hemoproteínas, su actividad modularía los niveles de las enzimas dependientes de citocromo P450, esenciales en el camino esteroidogénico. La expresión constitutiva de HO-2 en testículo y glándula adrenal probablemente cumpla esa función.
Evidencias experimentales de los últimos años demuestran que los sistemas de generación y los mecanismos de acción del NO y del CO coinciden en diversos aspectos. Ambos mediadores comparten al menos un blanco de acción común como es el grupo hemo de la guanilil ciclasa soluble, y su acción se ha asociado a un aumento en los niveles de GMPc. Una estrategia biológica para evitar esta redundancia podría consistir en la regulación mutua y coordinada entre ambos sistemas enzimáticos. En este sentido, resulta cada vez más evidente que ambos mediadores no actúan siempre en forma independiente, sino que uno puede modular la actividad del otro. Se ha demostrado que el NO induce la expresión de HO-1 y que la HO podría regular los niveles de la hemoproteína NOS. En macrófagos obtenidos de animales inyectados con LPS, la HO-1 actuaría como un inhibidor fisiológico de NOS disminuyendo la disponibilidad del grupo hemo para la actividad de la iNOS. También se ha sugerido que hay un sinergismo entre CO y NO para proveer citoprotección. Se están desarrollando experimentos que intentarán ver si estos mecanismos son posibles en nuestros modelos experimentales.
Los procesos infecciosos e inflamatorios comprometen fuertemente las funciones testicular y adrenal. Sin embargo, los mecanismos involucrados en estos efectos aún no han sido elucidados. La inflamación involucra, entre otros procesos, la activación de monocitos, macrófagos y mastocitos, lo que lleva a la producción de citoquinas proinflamatorias y especies reactivas de oxígeno (ROS) citotóxicas, las cuales modulan la síntesis de esteroides en CL y en células adrenales. La producción de estos mediadores, que ocurre en forma sistémica y también localmente, se incrementa ante un estímulo como el LPS. Al respecto, el aumento en la muerte celular programada (apoptosis, autofagia) o no programada (necrosis) ocurre durante la injuria celular y puede contribuir a la etiología de varios estados fisiopatológicos. La HO-1 (a través de alguno de sus productos: CO, biliverdina y/o bilirrubina) confiere citoprotección en varios tipos celulares inhibiendo la apoptosis, la inflamación y la proliferación celular. Dicho efecto de la HO-1 puede involucrar diferentes sistemas de transducción de la señal que incluye, entre otros, p38MAPK, PI-3-K/AKT o NFkB (7-9). Estamos estudiando si la inducción de HO regula la proliferación de células de Leydig testiculares.
2- HISTAMINA
Clásicamente reconocida como mediadora en procesos inflamatorios, la histamina (HA) ha sido generalmente asociada a los mastocitos presentes en casi todos los tejidos. Sin embargo, también se ha descripto síntesis de HA en basófilos, plaquetas, células endoteliales y neuronas, y existen evidencias de su participación en una gran variedad de procesos fisiológicos y patológicos. La síntesis de HA se produce a partir del aminoácido L-histidina, en una reacción catalizada por la enzima L-histidina descarboxilasa (HDC). HA ejerce sus múltiples efectos a través de la unión a receptores acoplados a proteínas G en la membrana de sus células blanco. Los mismos han sido designados HRH1, HRH2, HRH3 y HRH4, y se diferencian en su patrón de expresión y mecanismos de transducción de la señal (10, 11). Varios de los procesos en los que HA interviene como modulador involucran proliferación celular y/o apoptosis. Más aún, HA tendría efectos pro apoptóticos o anti apoptóticos según el tipo celular.
Tanto en condiciones fisiológicas como patológicas, el efecto final de HA sobre la proliferación celular y/o apoptosis estaría definido por el subtipo de receptor con el que la amina interactúa en la membrana de sus células blanco, lo cual desencadena la activación de mecanismos de transducción de la señal específicos según el tipo celular. Estos incluyen la activación o inhibición de las vías MAPK/ERK, IKK/NF-KB, SAPK/JNK y JAK/STAT, en el caso de la regulación de la proliferación celular, y cambios en la expresión de proteínas de la familia BCL2 en el caso de inducción de apoptosis. La mayoría de los trabajos realizados hasta el momento involucran receptores HRH1 y HRH2, pero en los últimos años se centró la atención en los subtipos HRH3 y HRH4 y su papel en la regulación de la proliferación celular. Al respecto, cabe destacar que evidencias recientes indican que HRH3 y HRH4 se expresan en diferentes líneas celulares de glándula mamaria humana, tanto normales como transformadas, siendo la expresión de HRH3 significativamente mayor en estas últimas. Además, se demostró una correlación entre la expresión de HRH3, HDC y el antígeno nuclear de proliferación celular (PCNA), y un efecto estimulatorio de HA mediado por HRH3 sobre la migración de las células malignas. Por su parte, la activación de receptores HRH4 mostró un efecto inhibitorio sobre la proliferación celular, induciendo apoptosis (12, 13). Se están realizando estudios relacionados con los subtipos HRH3 y HRH4 y con la regulación de la proliferación celular
Existen muy pocas evidencias en la literatura acerca del posible papel de la HA como modulador de la fisiología de las células esteroidogénicas. Se vio que HA estimula la síntesis de progesterona a través de receptores del subtipo HRH2 por un mecanismo mediado por AMPc, en folículos preovulatorios de rata. También se ha reportado que HA tiene un efecto estimulatorio directo sobre la secreción de progesterona y estradiol en células de la granulosa humana, sugiriendo un rol fisiológico en la regulación de la función de dichas células durante el ciclo menstrual. Respecto a las funciones reproductivas en el macho, Mayerhofer et al. (14) han sugerido que HA estimula la esteroidogénesis a través de los receptores HRH1 en el parénquima testicular del hámster dorado. Además, dos trabajos recientes sugieren, por un lado, la existencia de un sistema histaminérgico en testículo humano (15) y por otra parte, que la HA estaría involucrada en la maduración del testículo, ya que en ratones KO para HDC, se observó atrofia testicular parcial, alteraciones morfológicas de las CL y esteroidogénesis disminuída (16). Al respecto en este punto, en nuestro conocimiento, los 3 trabajos publicados por nuestro grupo en células de Leydig, representan las mayores contribuciones en el tema (17-19). Además, hemos publicado, por invitación del Editor, un capítulo de libro (20).
Los niveles testiculares de HA presentan variaciones a diferentes edades, siendo considerablemente mayores en ratas prepúberes, donde predominan formas inmaduras de células de Leydig, en forma simultánea con un mayor número de mastocitos intersticiales. Los altos niveles de HA hallados en animales prepúberes estarían asociados a un incremento en la proliferación y/o una inhibición de la diferenciación, mientras que los niveles más bajos, hallados en los animales adultos, estarían asociados a una disminución de la proliferación, a un aumento de la diferenciación, y a la regulación de las funciones diferenciadas. Estas diferentes concentraciones de HA en distintos estadíos estarían de alguna manera correlacionadas con los efectos bifásicos que hemos observado previamente.
Considerando los estudios que realizó nuestro grupo en CL y dada la escasa, contradictoria y poco actualizada bibliografía acerca de la acción directa de la HA sobre la corteza adrenal, es que se están realizando estudios en células córticoadrenales (21). Los efectos de ACTH en la glándula adrenal incluyen la estimulación de la síntesis de esteroides y una marcada vasodilatación reflejada por el aumento en el flujo sanguíneo a través de la glándula. Se han localizado mastocitos en las paredes
de arteriolas en el punto de contacto de la corteza adrenal con la cápsula de tejido conectivo, y se ha sugerido que la HA y la serotonina producidas por dichas células incrementan el flujo del medio de perfusión y la secreción de esteroides en la glándula aislada perfundida en ausencia de ACTH. También se sugiere que la HA causa relajación de arteriolas córticoadrenales y que estimula la síntesis de aldosterona en células glomerulosas (ZG) adrenales bovinas. En lo que respecta a proliferación, un trabajo reciente (22) compara la expresión de proteínas y genes relacionados con la HA entre cortezas adrenales humanas normales y tumores adrenocorticales, demostrando un patrón de expresión diferencial entre ambos, en cuanto a la expresión de la enzima HDC, contenido de histamina y perfil de expresión de los receptores.
Uno de los puntos de integración entre los factores mencionados consiste en investigar si alguno de los efectos de la HA involucra a la modulación del sistema de las hemo oxigenasas (HO). Tal estudio se fundamenta en que recientemente hemos descripto (19) que concentraciones de HA inhibitorias de la esteroidogénesis en CL actúan, al menos en parte, a través de la activación del sistema NOS/NO. Esto concuerda con resultados anteriores de Del Punta y col (1) acerca de que el NO inhibe el proceso esteroidogénico. Si hubiere una regulación recíproca entre los sistemas NOS/NO y HO/CO y su relación con los parámetros de estrés oxidativo (incluyendo la producción de ROS) tal como planteamos en el bloque 1, entonces la HA regularía ambos sistemas a través de uno o más de sus subtipos de receptores. Si así fuere, los resultados representarían un novedoso sistema de regulación multifactorial que podría extrapolarse no sólo a otros sistemas esteroidogénicos, sino también a varios tipos celulares con diferentes funciones biológicas.
Otro punto de vista de la importancia de estos estudios radica en que los resultados obtenidos atraerán atención hacia nuevos efectos colaterales potenciales del uso de antihistamínicos, que podrían alterar el normal funcionamiento del testículo y la glándula adrenal, comprometiendo la fertilidad humana y la producción de hormonas esenciales para la vida.
Referencias bibliográficas
1. Del Punta K, Charreau EH, Pignataro OP. Nitric oxide inhibits Leydig cell steroidogenesis. Endocrinology 1996; 137: 5337-43
2. Cymeryng CB, Dada LA, Podesta EJ. Effect of nitric oxide on rat adrenal zona fasciculata steroidogenesis. J Endocrinol 1998; 158(2): 197-203.
3. Sainz JM, Reche C, Rábano M, Mondillo C, Patrignani ZJ, Macarulla JM, Pignataro OP, et al. Effects of nitric oxide on aldosterone synthesis and nitric oxide synthase activity in glomerulosa cells from bovine adrenal gland. Endocrine 2004; 24: 61-72.
4. Reche C Tesis Doctoral. Universidad Nacional de Quilmes. 2005.
5. Pomeraniec Y, Grion N, Gadda L, Pannunzio V, Podesta EJ, Cymeryng CB Adrenocorticotropin induces heme oxygenase-1 expression in adrenal cells. J Endocrinol 2004; 180(1):113
6. Piotrkowski B, Monzón C, Pagotto R, Reche C, Besio M, Cymeryng C, Pignataro OP, et al. Effects of heme oxygenase isozymes on Leydig cells steroidogenesis. J Endocrinol 2009; 203: 155-65.
7. Morse D, Lin L, Choi A, Ryter S. Heme oxygenase-1, a critical arbitrator of cell death pathways in lung injury and disease. Free Radical Biology and Medicine 2009; 47: 1-12.
8. Was H, Dulak J, Jozkowicz A. Heme oxygenase-1 in tumor biology and therapy. Current Drug Targets 2010; 11: 1551-70.
9. Leffler CW, Parfenova H, Jaggar J. Carbon monoxide as an endogenous vascular modulator. Am J Physiol Heart Circ 2011; 301(1): H1-H11.
10. Falus A, Darvas S, Grossman N (eds.) Histamine: Biology and Medical Aspects. Budapest: Karger; 2004.
11. Mohammed Shahid, Nancy Khardori, Rahat Ali Khan, (eds.). Biomedical Aspects of Histamine: Current Perspectives. Springer Science+Business Media B.V. 2010.
12. Medina V, Croci M, Crescenti E y col The role of histamine in human mammary carcinogenesis. H3 and H4 receptors as potential therapeutic targets for breast cancer treatment. Cancer Biol Ther 2008; 7: 27-35.
13. Medina V, Brenzoni P, Martinel Lamas D, Massari1 N, Mondillo C, Nunez M, et al. Role of histamine H4 receptor in breast cancer cell proliferation. Frontiers in Biosciences 2011; 3: 1042-60.
14. Mayerhofer A, Bartke A, Amador A, Began T. Histamine affects testicular steroid production in the golden hamster. Endocrinology 1989; 125: 2212-4.
15. Albrecht M, Frungieri M, Gonzalez-Calvar S, Meineke V, Kohn F, Mayerhofer A. Evidence for a histaminergic system in the human testis. Fertil Steril 2005; 83: 1060.
16. Pap E, Racz K, Kovacs JK, et al. Histidine decarboxylase deficiency in gene knockout mice elevates male sex steroid production. J Endocrinol 2002; 175 (1): 193-9
17. Mondillo C, Patrignani Z, Reche C, Rivera E, Pignataro OP. Dual role of histamine in modulation of Leydig cell steroidogenesis via H1 and H2 receptor subtypes. Biol Reprod 2005; 73(5): 899-907.
18. Mondillo C, Falus A, Pignataro O, Pap E. Prolongued histamine deficiency in histidine decarboxilase gene knockout mice affects regulation of Leydig cell function by LH/hCG. J Androl 2007; 28(1): 86-91.
19. Mondillo C, Pagotto RM, Piotrkowski B, Reche CG, Patrignani ZJ, Cymeryng CB, et al. Involvement of nitric oxide synthase in the mechanism of histamine-induced inhibition of Leydig cell steroidogenesis via histamine receptor subtypes in Sprague-Dawley Rats. Biol Reprod 2009; 80(1): 144-52.
20. Mondillo C, Pignataro OP. Novel role for Histamine through classical H1 and H2 receptors: regulation of Leydig cell steroidogenesis and its implications for male reproductive function. In: "Biomedical Aspects of Histamine: Current Perspectives". Chapter 17. 2010 Ed: M. Shahid-Springer. pp: 383-94.
21. Pagotto R, Mondillo C, Piotrkowski B, Besio M, Cymeryng C, Pignataro OP. La histamina como modulador directo de la esteroidogénesis en células córtico-adrenales. Medicina 2007; Vol 67: 82.
22. Szabó PM, Wiener Z, Tömböl Z, et al. Differences in the expression of histamine-related genes and proteins in normal human adrenal cortex and adrenocortical tumors. Virchows Arch 2009; 455(2): 133-42.
LABORATORIO DE ENDOCRINOLOGÍA MOLECULAR
Estudios genéticos y moleculares en hiperplasia suprarrenal congénita por déficit de 21-hidroxilasa
Molecular and Genetic studies in 21-hydroxylase deficiency
Estudos Genéticos e Moleculares em Hiperplasia Suprarrenal Congênita por Déficit de 21-Hidroxilase
Liliana Dain1,2, Cecilia Fernández1,2, Melisa Taboas2, Noemí Buzzalino2, Liliana Alba2, Eduardo Charreau1,
1. Instituto de Biología y Medicina Experimental, CONICET.
2. Centro Nacional de Genética Médica, ANLIS.
Resumen
La Hiperplasia Suprarrenal Congénita (HSC) por déficit de 21-hidroxilasa representa la enfermedad autosómica recesiva de mayor frecuencia y la causa del 90-95% de los casos de HSC. El objetivo de nuestro trabajo es la caracterización molecular de los defectos genéticos asociados a este déficit. En la actualidad 650 familias han sido caracterizadas, entre las cuales hallamos 7 mutaciones noveles ubicadas en regiones codificantes, sitios de splicing y en una región regulatoria. Estudios de modelado molecular indican diferencias en la estabilidad de la proteína mutada y/o de la carga de aminoácidos de superficie y resultados preliminares demostrarían una disminución de la actividad residual in vitro. Por su parte, estudios in silico predicen que la variante de la región regulatoria alteraría la topología y curvatura del ADN. Los ensayos funcionales sugieren diferencias en la tasa transcripcional del gen. Asimismo, hemos observado una gran variabilidad en la estructura genómica que contiene al CYP21A2 (módulo RCCX) y hemos podido establecer que muchas de las pacientes No Clásicas poseen sólo un alelo con mutación o bien ninguno, lo que sugeriría que los valores hormonales considerados para la inclusión de estos pacientes estarían sobreestimando la frecuencia de la patología.
Palabras clave: deficiencia de 21-hidroxilasa; caracterización molecular; mutaciones noveles.
Summary
Congenital adrenal hyperplasia (CAH) due to 21-hydroxylase deficiency is the most frequent inborn error of metabolism, and it accounts for 90-95% of CAH cases. The goal of our study is to fully determine all the molecular defects leading to 21 hydroxylase deficiency in Argentinian patients. So far, 650 families have been characterized. Our analysis revealed the presence of 7 novel mutations not previously described in the literature, located in the coding region, splicing sites and a variant located in a distal regulatory region. In silico analyses of novel coding point mutations revealed changes in protein stability or in the surface charge of the mutant enzymes. Functional preliminary results suggest that the enzymatic activity is impaired. Similarly, bioinformatic studies predict that the variant in the distal regulatory region introduces distortions in the local conformation of DNA. In vitro assays suggest differences in the transcriptional activity of the gene. In addition, a great variability in the genomic structure of the RCCX module was found where the CYP21A2 gene is located. On the other hand, our analyses revealed that the cut-off value in the ACTH-stimulated 17- hydroxyprog-esterone test might overestimate the diagnosis of the non-classical form by including some patients with heterozygous status.
Key words: 21-hydroxylase deficiency; molecular characterization; novel mutations.
Resumo
A Hiperplasia Suprarrenal Congênita (HSC) por déficit de 21-hidroxilase representa a doença autossômica recessiva de maior frequência e a causa de 90-95% dos casos de HSC. O objetivo do nosso trabalho é a caracterização molecular dos defeitos genéticos associados a este déficit. Na atualidade, 650 famílias têm sido caracterizadas, dentre as quais encontramos 7 mutações novéis localizadas em regiões codificantes, sítios de splicing e numa região regulatória. Estudos de modelagem molecular indicam diferenças na estabilidade da proteína mutada e/ou da carga de aminoácidos de superfície e resultados preliminares demonstrariam uma diminuição da atividade residual in vitro. Por sua vez, estudos in silico predizem que a variante da região regulatória alteraria a topologia e curvatura do DNA. Os ensaios funcionais sugerem diferengas na taxa transchcional do gene. Do mesmo modo, temos observado grande variabilidade na estrutura genómlca que contém o CYP21A2 (módulo RCCX) e pudemos estabelecer que multas das pacientes Náo-Clásslcas possuem apenas um alelo com mutacao ou entáo nenhum, o que sugerirla que os valores hormonals considerados para a inclusáo destes pacientes estarlam superestlmando a frequênce da patología.
Palavras chave: deficiência de 21-hidroxilase; caracteriza-gao molecular; mutagóes novéis.
Con el nombre de Hiperplasia Suprarrenal Congénita (HSC) se conoce a un conjunto de enfermedades hereditarias de origen autosómico recesivo que presentan trastornos en la esteroidogénesis suprarrenal y que causan déficit en la biosíntesis del cortisol y aldosterona. La deficiencia de la enzima 21-hidroxilasa es el desorden más común, representando al 90-95% de los casos de HSC (1). La sintomatología clínica del déficit de 21-hidroxilasa comprende un amplio espectro de manifestaciones que van desde formas severas con pérdida salina hasta aquellas con signos leves de hiperandrogenismo. La variabilidad de expresión es una manifestación del grado de actividad residual que presenta la enzima. Así, la deficiencia de 21-hidroxilasa puede valorarse clínicamente como severa o clásica y leve o no clásica o de presentación tardía. La clásica, que posee dos variantes Virilizante simple (VS) y Perdedora de sal (PS), se manifiesta durante el período perinatal con signos clínicos debido a la falta de producción de aldosterona y/o cortisol, mientras que la no clásica (NC) presenta manifestaciones clínicas menos severas después del nacimiento, en la primera infancia, en la pubertad o en la edad adulta y sus signos son principalmente el hiperandrogenismo. Las prevalencia han sido estimadas en 1/15.000 para la forma clásica y de 1/100 a 1/1.000 para la NC, dependiendo del origen étnico de los afectados. Esta patología es pasible de un tratamiento de bajo costo que permite una calidad de vida normal. Asimismo, el tratamiento prenatal con dexametasona, puede evitar la virilización en las formas clásicas, sin que se hayan descripto efectos teratogénicos con las dosis usadas.
El gen codificante, CYP21A2, está ubicado en el cromosoma 6p21.3 conformando un bloque que se encuentra normalmente duplicado. Este bloque denominado RCCX (AP, A4, A21 y TNa comprende parte del gen RP1, los genes del factor 4 del Complemento, los genes CYP21 y una región del gen TNXB que codifica para una proteína del citoesqueleto. Las regiones duplicadas de TNXB y RP1 constituyen pseudogenes truncados llamados TNXA y RP2, respectivamente(1)(2). Aproximadamente el 60% de los cromosomas contienen 2 módulos RCCX, conformando el siguiente arreglo de telómero a centrómero: RP1-C4A-CYP21A1P-TNXA (Módulo largo)- RP2-C4B-CYP21A2-TNXB (Módulo corto), con un gen activo (CYP21A2) en uno de ellos y un pseudogen inactivo (CYP21A1P) en el otro, ambos con 98% de identidad de secuencia. Sin embargo, se han descripto cromosomas monomodulares, trimodulares y tetramodulares, por duplicación/deleción del módulo que contiene al gen o al pseudogen.
Gran parte de los defectos genéticos responsables de la deficiencia son producto del apareamiento desigual entre el gen y el pseudogen, causando deleciones del gen o bien la transferencia de mutaciones deletéreas del pseudogen al gen por conversión génica. Si bien la mayor parte de los afectados poseen mutaciones que provienen del pseudogen, en los últimos años se han identificado más de 130 mutaciones espontáneas como causantes de la patología (3).
Nuestro grupo de trabajo inició el estudio molecular de la deficiencia de 21-hidroxilasa en el año 1996. Los primeros estudios nos permitieron estimar la distribución de las 10 mutaciones más frecuentes en una muestra preliminar de afectados (4)(5). Actualmente, más 650 familias han sido estudiadas, detectando entre el 85 y el 95% de los alelos clásicos y alrededor del 70% de los alelos pertenecientes a pacientes NC. En un grupo de pacientes en los que restaba identificar al menos una alelo, hemos llevado a cabo una búsqueda de mutaciones menos frecuentes y/o noveles por secuenciación. Nuestros resultados demostraron la presencia de 12 mutaciones poco frecuentes previamente descriptas, algunas de ellas asociadas a una diferente forma de presentación de la patología (6) y 7 mutaciones noveles, 5 en regiones codificantes, 1 en un sitio dador de splicing y 1 variante en una región regulatoria distal. Las variantes en la región proteica involucran a residuos aminoacídicos muy conservados evolutivamente en la proteína (7-8). Estudios de modelado molecular indican diferencias en la estabilidad de la proteína y/o de la carga de aminoácidos de superficie como consecuencia de estas mutaciones (8). Asimismo, estudios preliminares de la actividad residual in vitro de las variantes mutadas demostrarían una disminución en la capacidad de conversión de los sustratos de la enzima en sus productos. Por su parte, estudios bioinformáticos predicen una alteración de la topología y curvatura del ADN para la variante hallada en una de las regiones regulatorias analizadas. Los estudios preliminares de su expresión in vitro, sugerirían una diferencia en la tasa transcripcional del gen (9).
Estudios previos de nuestro grupo han demostrado también, una gran variabilidad en la estructura de la región genómica en donde está ubicado el gen CYP21A2 (bloque RCCX). Las mismas incluyen deleciones y duplicaciones del gen y pseudogen, así como la presencia de genes quiméricos (10). Estos resultados demuestran la gran complejidad que posee esta región genómica y su caracterización contribuye a una mejor comprensión de los mecanismos patológicos de la deficiencia.
Finalmente, nuestro estudio de búsqueda de mutaciones menos frecuentes o noveles en los pacientes, nos ha permitido establecer que muchas de las pacientes diagnosticadas como NC poseen sólo un alelo con mutación o bien ninguno (11). Estos resultados cobran importancia dado que demostrarían que el hiperandrogenismo que se observa en estos pacientes se debe a otras causas y no a la deficiencia de 21-hidroxilasa, y que los valores hormonales considerados como límite de corte para su inclusión, estarían sobreestimando la frecuencia de la patología. De hecho, todos aquellos pacientes analizados que presentan valores de 17 OH- progesterona post-estímulo con ACTH menores a 14 ng/mL (valor de corte: 10 ng/mL(4) poseen sólo un alelo del gen mutado o bien ninguno (4) (11)(12).
Referencias bibliográficas
1. White PC, Speiser PW: Congenital adrenal hyperplasia due to 21 hydroxylase deficiency. Endocr Rev 2000; 21: 245-91.
2. Koppens PFJ, Hoogennoezem T, Degenhart HJ: Duplication of the CYP21A2 gene complicates mutation analysis of steroid 21-hydroxylase deficiency: characteristics of three unusual haplotypes. Hum Genetics 2002; 111: 405-10.
3. Human Gene Mutation Database (HGMD) Cytochrome P450, subfamily XXIA (steroid 21-hydroxylase, congenital adrenal hyperplasia), peptide 2. http://uwcmml1s.uwcm.ac.uk/uwcm/mg/search/120605.html.
4. Dain L, Buzzalino N, Onetto A, Belli S, Oneto A, et al. Classical and nonclassical 21-hydroxylase deficiency: A molecular study of argentine patients. Clin Endocrinol 2002; 56:239-45.
5. Pasqualini T, Alonso G, Tomasini R, Galich A, Buzzalino N, et al. Congenital adrenal hyperplasia: Clinical characteristics and genotype in newborn, childhood and adolescense. Medicina 2007; 67: 253-61.
6. Taboas M, Fernández C, Belli S, Buzzalino N, Alba L, Dain L. Isolated p.H62L in a classical 21-hydroxylase deficient patient. Eur J Obst Gynecol Reprod Biol (en prensa).
7. Dain L, Minutolo C, Buzzalino N, Belli S, Oneto A, et al. A novel CYP21A2 point mutation in a 21-hydroxylase deficient patient. In: Novel human pathological mutations. Hum Genet 2006; 119: 359-64.
8. Minutolo C, Nadra A, Fernández C, Buzzalino N, Belli S, et al. Structure-based analysis of five novel disease-causing mutations in 21-hydroxylase-deficient patients PLoS ONE 2011; 6: e15899. doi:10.1371/ journal.pone.0015899.
9. Fernández C, Buzalino N, Belli S, Oneto A, Stivel M, et al. Novel allelic variant within the Z promoter: putative miss-regulation effect on CYP21A2 transcription. Manuscrito en preparación.
10. Fernández C, Buzzalino N, Oneto A, Stivel M, Belli S, et al. Caracterización del módulo RCCX en una muestra de pacientes argentinos con deficiencia de 21-hdroxilasa. XX Congress Brasileiro de Genética Médica y III Congresso Brasileiro de Enfermagem em Genética 2008.
11. Buzzalino N, Fernández C, Taboas M, Minutolo C, Belli S, et al. Caracterización molecular del gen CYP21A2 en una muestra de 241 pacientes con Hiperplasia Suprarrenal Congénita de nuestra población. RAEM 2009; 46 Sup I: 130 (manuscrito en preparación).
12. Taboas M, Minutolo C, Fernández C, Buzzalino N, Casali B, et al. Caracterización molecular por secuenciación de pacientes con hiperplasia suprarrenal congénita (HSC) por deficiencia de 21 hidroxilasa en nuestra población. Medicina 2010; 70 Sup.II: 132.
LABORATORIO DE ESTUDIOS DE LA INTERACCIÓN CELULAR EN REPRODUCCIÓN Y CÁNCER
Bases moleculares de la interacción celular en modelos de reproducción y cáncer: identificación de proteínas y mecanismos involucrados
Molecular basis of cell-cell interaction in reproduction and cancer models: identification of proteins and mechanisms involved
Bases moleculares da interação celular em modelos de reprodução e câncer: identificação de proteínas e mecanismos envolvidos
Mónica H. Vazquez-Levin, Laura I. Furlong, Clara I. Marín-Briggiler, Carolina Veaute, María F. Veiga, María L. Matos, Lara Lapyckyj, Nieves Gabrielli, Marina Rosso, María M. Arzondo, Nadia Y. Edelsztein, María J. Besso
Resumen
La interacción entre las células somáticas y entre las gametas involucra una serie de eventos moleculares que no han sido dilucidados totalmente. Nuestro grupo de investigación ha desarrollado proyectos dirigidos a profundizar el conocimiento de dichos eventos. Los estudios han comprendido el análisis de moduladores de la funcionalidad espermática (ej. efecto de la temperatura de incubación, las concentraciones del ión calcio, los anticuerpos antiespermáticos de fluidos biológicos en la motilidad, la capacitación y la exocitosis acrosomal). Asimismo, hemos caracterizado componentes del espermatozoide (ej. CaM Kinasa IV, proacrosina/acrosina) y de secreciones del tracto femenino (ej. Grp78/BiP), evaluado su rol en el desarrollo de capacidad fecundante y, en algunos casos, investigado su relación con la infertilidad. En años recientes, nuestros proyectos se han extendido al estudio de las cadherinas en eventos de adhesión celular durante la fecundación; hemos caracterizado la expresión de cadherina epitelial y neural en tejidos reproductivos y gametas y evaluado su participación en la fecundación. Dada su reconocida relevancia en el cáncer, hemos abordado estudios en diversos modelos tumorales. Nuestras investigaciones han contribuido a la comprensión de los eventos de interacción de las gametas durante la fecundación así como entre las células somáticas durante la progresión tumoral.
Palabras clave: interacción celular; fecundación; progresión tumoral; proacrosina/acrosina; Grp78/Bip; cadherinas clásicas.
Summary
Cell-cell interaction between somatic cells as well as gametes involves molecular events that have not been completely elucidated. Our research group has developed projects aimed at studying proteins and mechanisms participating in these interactions. Several modulators of sperm functions have been analyzed (i.e. incubation temperature, calcium ion concentration, and antisperm antibodies present in biological fluids upon sperm motility, capacitation and acrosomal exocytosis). In addition, proteins from spermatozoa (i.e. CaM Kinase IV, proacrosin/acrosin) and from secretions of the female tract (Grp78/BiP) have been characterized, and their role in the development of sperm fertilizing ability assessed. In some cases, their relationship with infertility was evaluated. In recent years, our projects have been extended to study members of the cadherin superfamily and related proteins; in particular, the expression of epithelial and neural cadherin in reproductive tissues and gametes was characterized and evidence of their participation in fertilization-related cell-cell adhesion events shown. Based on the vast evidence of the role of these proteins in tumor progression, our current research also involves studies of cancer models. Our projects have contributed to the understanding of the molecular basis of cell-cell interaction during fertilization as well as during tumor progression.
Key words: cell-cell interaction; fertilization; tumor progression; proacrosin/acrosin; Grp78/Bip; classical cadherins.
Resumo
A interação entre as células somáticas e entre os gametas envolve uma série de eventos moleculares que não têm sido elucidados totalmente. Nosso grupo de pesquisa tem desenvolvido projetos encaminhados a aprofundar o conhecimento de tais eventos. Os estudos têm compreendido a análise de moduladores da funcionalidade espermática (ex. efeito da temperatura de incubação, as concentrações do íon cálcio, os anticorpos antiespermáticos de fluidos biológicos na motilidade, a capacitação e a exocitose acrossomal). Do mesmo modo, caracterizamos componentes do espermatozoide (ex. CaM Kinase IV, proacrosina /acrosina) e de secreções do trato feminino (ex. Grp78/BiP), avaliamos seu papel no desenvolvimento de capacidade fecundante e, em alguns casos, investigamos sua relação com a infertilidade. Em anos recentes, nossos projetos se têm estendido ao estudo das caderinas em eventos de adesão celular durante a fecundação; temos caracterizado a expressão de caderina epitelial e neural em tecidos reprodutivos e gametas e avaliamos sua participação na fecundação. Dada sua reconhecida relevância no câncer, temos abordado estudos em diversos modelos tumorais. Nossas pesquisas têm contribuído à compreensão dos eventos de interação dos gametas durante a fecundação bem como entre as células somáticas durante a progressão tumoral.
Palavras chave: interagáo celular; fecundagáo; progressáo tumoral; proacrosina/acrosina; Grp78/Bip; caderinas clássicas.
Introducción
La interacción entre las células somáticas y entre las gametas involucra una serie de eventos moleculares complejos que no han sido dilucidados totalmente. Desde su constitución hace 15 años, nuestro grupo de investigación ha desarrollado proyectos de investigación dirigidos al estudio de los mecanismos moleculares y las entidades que participan en el reconocimiento de las gametas durante la fecundación. Como parte de los proyectos, hemos estudiado el rol de diversos componentes del espermatozoide y de las secreciones del tracto femenino en el desarrollo de su capacidad fecundante, así como hemos evaluado requerimientos in vitro (ej. el rol de la temperatura de incubación y del ión calcio (Ca2+) del medio de cultivo de espermatozoides para el desarrollo de estrategias de abordaje de algunos de los eventos de este proceso). En años recientes nuestras investigaciones están enfocadas en el estudio de miembros de la superfamilia de moléculas de adhesión llamadas cadherinas y proteínas relacionadas a éstas en eventos de adhesión celular durante la fecundación. Dada la reconocida relevancia de miembros de esta familia de moléculas de adhesión en la progresión del cáncer, nuestras investigaciones se han extendido a su estudio en diversos modelos tumorales. Los diseños experimentales han involucrado el uso de gametas y tejidos reproductivos de distintas especies de mamíferos (modelo humano, murino y bovino) así como líneas celulares y muestras de tejidos no tumorales y tumorales de diversos orígenes. En los abordajes de estudio empleamos estrategias celulares, bioquímicas, moleculares y funcionales. En los párrafos siguientes se presenta una revisión de algunos de los proyectos realizados.
GENERALIDADES DEL PROCESO DE LA FECUNDACIÓN
La fecundación involucra una secuencia coordinada de interacciones moleculares entre el espermatozoide y el óvulo que dan origen a una zigota. Los espermatozoides son células altamente especializadas y polarizadas, que se forman de manera continua en el epitelio seminífero del testículo durante la espermatogénesis. Sin embargo, el espermatozoide que deja la gonada es inmótil o presenta motilidad no progresiva y no puede fecundar al ovocito; ambas propiedades son adquiridas durante su tránsito por el epidídimo en un proceso conocido como maduración epididimaria. Luego de la eyaculación, los espermatozoides deben permanecer un tiempo en el tracto reproductivo femenino donde sufren una serie de cambios metabólicos y funcionales conocidos en conjunto como capacitación espermática. Los espermatozoides interactúan con las células del tracto reproductivo de la hembra y sus secreciones y desarrollan un patrón de motilidad llamado hiperactivación, que facilita su acercamiento y la penetración de las envolturas del ovocito. Una vez en el sitio de fecundación, los espermatozoides comienzan una serie compleja de interacciones con el ovocito y sus envolturas, particularmente las células del cumulus y la corona radiata y la zona pellucida (ZP) hasta alcanzar el citoplasma. Los espermatozoides sufren la exocitosis acrosomal (EA), evento que permite la liberación de enzimas acrosomales que asisten al espermatozoide en el proceso, así como la redistribución de proteínas en diferentes subregiones de la gameta y el consecuente desarrollo de capacidad fusogénica del segmento ecuatorial, que participaría en la fusión con el oolema (1-3).
En las últimas décadas, mucho se ha avanzado en relación al conocimiento de las bases de este proceso; sin embargo, los mecanismos moleculares involucrados aún no han sido dilucidados en su totalidad. La identificación y caracterización de las moléculas que participan en el proceso de fecundación así como la comprensión de los mecanismos que regulan su expresión y funciones pueden contribuir no solo a comprender los mecanismos involucrados en la interacción espermatozoide-ovocito, sino también al mejoramiento de las herramientas actuales para el manejo de las gametas, el desarrollo de nuevas alternativas para el diagnóstico y tratamiento para la infertilidad humana y nuevos métodos anticonceptivos.
REQUERIMIENTOS DE TEMPERATURA Y DE IONES CALCIO EN LOS PROCESOS DE CAPACITACIÓN Y DE EXOCITOSIS ACROSOMAL
Los eventos de la capacitación y la EA se encuentran estrechamente relacionados, situación que hace dificultosa la evaluación de los mecanismos y los componentes involucrados de manera independiente. En un proyecto orientado a disociar estos procesos, evaluamos los requerimientos de temperatura e iones Ca2+ para su ocurrencia en condiciones in vitro en el modelo del espermatozoide humano. Los resultados de estos estudios revelaron que la incubación de los espermatozoides a 20 °C impide la capacitación espermática pero es suficiente para sontener una respuesta a la inducción de la EA por un inductor fisiológico (fluido folicular) en espermatozoides previamente capacitados (4). Los estudios permitieron determinar además el requerimiento de concentraciones diferenciales de iones Ca2+ en el medio de incubación de los espermatozoides in vitro para la ocurrencia de ambos eventos: mientras 0,22 mM es suficiente para el desarrollo de eventos asociados a la capacitación (niveles de fosforilación en proteínas fosforiladas en residuos tirosina y motilidad hiperactivada), se necesitan concentraciones mayores del catión divalente (al menos 0,58 mM) para producir la máxima respuesta de las gametas a la inducción de la EA mediada por el fluido folicular y para obtener la máxima tasa de union a la ZP (5). La formulación de medios de cultivo con cantidades diferenciales de ión Ca2+ permitió abordar otros estudios, entre ellos identificar anticuerpos antiespermáticos inductores de la EA en sueros de mujeres en consulta/tratamiento por infertilidad y determinar su efecto sobre la interacción espermática sobre componentes de la ZP (6)(7), así como determinar que la chaperona Grp78/Bip, que se incoporaría al espermatozoide durante la capacitación, modula la interacción entre ambas gametas de manera dependiente de los iones Ca2+ (8 ver en detalle más adelante). Teniendo en cuenta que los medios de cultivo para manejo de espermatozoides en general tiene concentraciones milimolares de iones Ca2+ (2 mM), la formulación de medios de cultivo con cantidades diferenciales del catión divalente podrán impactar en el manejo de patologías espermáticas, entre ellas la ocurrencia prematura de la capacitación y/o EA.
PROTEÍNAS INVOLUCRADAS EN LA MOTILIDAD DEL ESPERMATOZOIDE: KINASAS DEPENDIENTES DEL IÓN CALCIO EN EL ESPERMATOZOIDE HUMANO
Los mecanismos involucrados en la regulación de la motilidad del espermatozoide de mamíferos no se conocen totalmente. Los estudios mencionados en la sección anterior (5) revelaron que los iones Ca2+ juegan un rol clave en el mantenimiento de la motilidad. Sin embargo, los mecanismos subyacentes a este fenómeno no han sido dilucidados. Dado que los iones Ca2+ pueden unirse a calmodulina y este complejo regula la actividad de muchas enzimas, entre ellas las proteinas kinadas dependiente de Ca2+/calmodulina (CaM kinasas), desarrollamos un estudio iniciado como parte de la tesis doctoral de la Dra. C. Marín Briggiler y luego completado de manera conjunta con el grupo liderado por el Dr. P. Visconti, en ese momento miembro de la Univ. de Virgina, EEUU. En el mismo, evaluamos la relevancia de la presencia de iones Ca2+ en el medio de incubación para la motilidad de los espermatozoides humanos y estudiamos la participación de las proteínas CaM kinasas en la motilidad. Los estudios confirmaron el requerimiento de los iones Ca2+ en el medio de incubación para el mantenimiento de la motilidad, determinándose que una concentración de 0,22 mM del ión divalente es suficiente para su mantenimiento. La participación de las CaM kinasas en la regulacion de la motilidad espermática dependiente de los iones Ca2+ fue confirmada a través del uso de inhibidores de estas kinasas (activos: KN62, KN93; inactivos: KN04 y KN92), observándose una disminución significativa en el porcentaje de espermatozoides mótiles; en particular, la incubación con el KN62 condujo a una reducción significativa en los valores de los parámetros cinemáticos y afectaron negativamente de manera significativa la cantidad de ATP en la gameta, pero no alteraron la viabilidad celular, la fosforilación global en residuos tirosina y la respuesta de las células a inductores fisiológicos de la EA. Finalmente, estudios adicionales permitieron a detectar una forma de 61 KDa para la proteína kinasa IV Ca2+ /calmodulina-dependiente (CaM kinasa IV) espermática, que fue localizada en el flagelo; los estudios además demostraron un aumento de su actividad durante la capacitacion y su inhibición con KN62 (9).
ADQUISICIÓN DE PROTEÍNAS DURANTE LA CAPACITACIÓN: LA CHAPERONA Grp78/BiP
Como se mencionara previamente, los espermatozoides completan la adquisición de su capacidad fecundante durante su tránsito por el tracto reproductor de la hembra (1-3). Numerosas evidencias sugieren que el entorno oviductal tiene un rol esencial en las etapas finales de la adquisición de competencia funcional de las gametas que llevan al éxito de la fecundación. Los espermatozoides que llegan al oviducto, interactuan con las células del epitelio oviductal y con sus secreciones, habiéndose observado un efecto del medio condicionado de cultivos de estas células en la preservación de la vitalidad y motilidad espermáticas, así como en la estimulación de eventos relacionados con la capacitación en animales, especialmente en el modelo bovino (10). Sin embargo, los efectos sobre la capacitación en el modelo humano no son concluyentes (11). Teniendo en cuenta evidencias previas que demostraron la detección de una forma secretoria la chaperona Grp78/BiP (Glucose regulated protein 78/ Binding immunoglobulin Protein) y hallazgos preliminares en nuestro laboratorio sobre su detección en el fluido folicular, realizamos un proyecto en colaboración con la Dra. V. Corrigal y col. del King's College London School of Medicine (Londres, Reino Unido) para estudiar su expresión en tejidos y secreciones del oviducto humano y evaluar su asociación al espermatozoide y su rol en eventos relacionados con la fecundación. En cortes histológicos de las secciones del isthmus y ampulla del oviducto humano, la Grp78/BiP fue inmunolocalizada en las células oviductales de ambas regiones, presentando mayor señal en la última. La forma secretoria de esta chaperona fue inmunodetectada en perfiles electroforeticos de proteínas de fluido oviductal y de medio condicionado de cultivos de células de tejido tubario humano. El análisis de los fluidos recuperados en diferentes momentos del ciclo menstrual además reveló la presencia de mayores niveles de Grp78/BiP en el período periovulatorio. Asimismo, Grp78/BiP recombinante se asoció a la región acrosomal de la cabeza del espermatozoide humano capacitado y demostró tener un rol modulador de la interacción entre las gametas de manera dependiente de los iones. Ca2+. Los resultados obtenidos concordaron con dos informes publicados durante el curso de la investigación en el modelo humano que describieron formas secretorias de la chaperona, su expresión en el oviducto y su capacidad de interactuar con el espermatozoide (12)(13). El estudio completado por nuestro grupo reportó, por primera vez, la secreción de la Grp78 por las células epiteliales oviductales humanas, así como demostró su asociación a la región del capuchón acrosomal del espermatozoide y presentó evidencias de su rol modulador de la activación de la gameta en eventos de la fecundación (Figura 1).
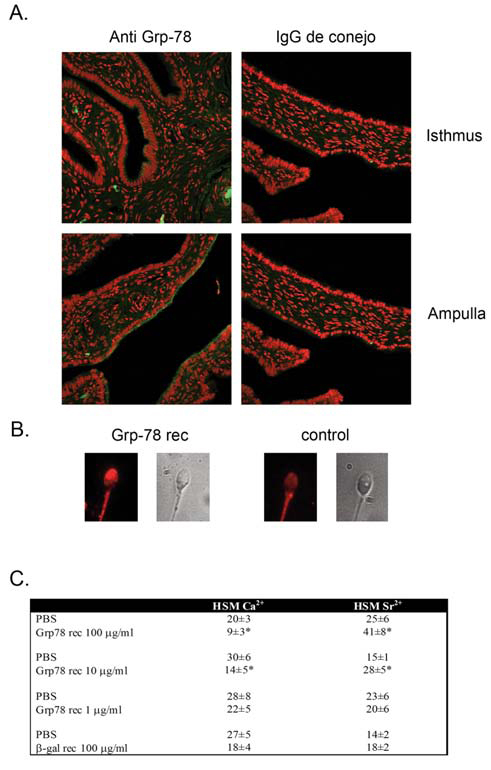
Figura 1. Expresión de Grp78 en el oviducto humano, su incorporación al espermatozoide humano y efecto sobre la interacción de las gametas. A. Inmunolocalización de Grp78 en secciones de trompa de Fallopio (isthmus y ampulla) humanas utilizando anticuerpo anti Grp78 (Santa Cruz Biotech) 2 mg/mL, anti conejo marcado con FITC (1:100), y contratinción con ioduro de propidio. Como control se incluye tinción con IgG de conejo 2 μg/mL. B. Unión de Grp78 recombinante (Grp78 rec) a espermatozoides humanos. Los espermatozoides capacitados por 4 h se incubaron con Grp78 rec (100 μg/mL) o PBS (control) por 4 h adicionales, fueron lavados para eliminar la proteína no unida y procesados para inmunocitoquímica. Se utilizó anti Grp78(Santa Cruz Biotech) 20 μg/mL, anti conejo marcado con CY3 (1:750). C. Efecto de la incubación de espermatozoides sobre la interacción con la ZP. Los espermatozoides mótiles fueron incubados por 4 h en condiciones capacitantes y expuestos a Hemizonae (HZ) en presencia de diferentes concentraciones de Grp78 rec. La HZ correspondiente fue incubada con PBS como control. Luego de 4 h de incubación, se removieron los espermatozoides débilmente unidos y se contaron los espermatozoides unidos por HZ. Se realizaron ensayos con 100 μg/mL de β-galactosidasa como control. Los resultados se expresan como media ± EEM; n ≥ 7. * P < 0.05 vs. control. El experimento fue realizado en medio conteniendo Ca2+ o Sr2+ (datos de ref. 8).
PROTEASAS ESPERMÁTICAS Y EL PROCESO DE LA FECUNDACIÓN: PROACROSINA/ACROSINA
La participación de proteasas de tipo tripsina en la interacción de gametas fue propuesta a partir de estudios que revelaron la capacidad de los inhibidores de tripsina de bloquear la penetración espermática del ovocito (14). De las proteasas acrosomales de este tipo, una de las más abundantes y estudiadas es Acrosina (EC 3.4.21.10), una endoproteasa con sitio activo de serina y especificidad por las uniones peptídicas de residuos Arginina o Lisina. Acrosina se sintetiza y almacena como zimógeno inactivo (proacrosina) en el acrosoma de las espermátidas redondas de todos los mamíferos estudiados y se activaría durante la EA en el sitio de la fecundación (15)(16).
En estudios realizados por nuestro grupo de investigación, el sistema proacrosina/acrosina fue immunolocalizado en la región apical de la cabeza y correspondiente al gránulo acrosomal de espermatozoides permeabilizados no capacitados y capacitados, mientras que luego de la EA se observó inmunoreactividad en la región ecuatorial o desaparición de la señal para la proteasa. Dado que la secuencia aminoacídica de proacrosina no indica la presencia de regiones transmembrana, la proteasa no estaría asociada directamente a la membrana del acrosoma y sería un componente de la matriz acrosomal. La proenzima humana puede ser extraída de espermatozoides utilizando soluciones ácidas que permiten disociar complejos formados con proteínas acrosomales y con el agregado de inhibidores de proteasas para prevenir su activación. En electroforesis bajo condiciones reductoras, proacrosina humana migra como una forma doble de Mr 53.000-55.000 y 58.000-61.000, igual tamaño molecular que el observado en ensayos de zimografía de extractos ácidos. La activación de la proenzima seguiría el mecanismo propuesto para la isoforma de cerdo, observándose formas de 52 kDa y 34 kDa que representarían el intermediario α-acrosina y la proteasa activa β-acrosina, respectivamente, además de otras formas de procesamiento de 22-24 y 16 KDa. Su activación puede ser completamente inhibida en presencia de benzamidina, sugiriendo la participación de serina proteasas en el mecanismo de activación. Si bien proacrosina purificada tiene capacidad de autoactivarse in vitro, el proceso de activación en el acrosoma estaría regulado por otros factores. En particular, estudios conjuntos entre nuestro laboratorio con el grupo del Dr Coronel de la Universidad de Córdoba, Argentina, revelan que tanto la activación como la actividad de la proteasa humana presente en extractos ácidos serían inhibidas por la proteína caltrin del plasma seminal (16-18).
En relación a las funciones del sistema proacrosina/acrosina, estudios realizados utilizando el modelo de knock out indicaron que esta enzima no sería esencial para el proceso de fecundación (19)(20). Sin embargo, los espermatozoides deficientes en proacrosina/acrosina mostraron un retraso en la penetración de la ZP normales y en ensayos de competencia espermática no fecundaron al ovocito (20). Estudios complementarios llevaron a proponer su participación en la activación/liberación de los contenidos acrosomales durante la EA. En concordancia con estas observaciones, se identificaron alteraciones en los patrones de activación de proacrosina de espermatozoides de individuos subfértiles sin alteraciones en los parámetros seminales y con una capacidad disminuida de fecundar ovocitos in vitro (21) así como un anticuerpo monoclonal dirigido contra el dominio de activación de la proenzima produjo una inhibición del porcentaje de espermatozoides humanos reaccionados sobre la ZP homóloga (22).
Además de su función de proteasa, el sistema proacrosina/acrosina tendría un rol en el reconocimiento y unión del espermatozoide a glicoproteínas de la ZP homóloga (15); sin embargo, los estudios en el modelo humano eran escasos. Empleando ensayos de unión en fase sólida (Ligand blot y ensayo en placa de poliestireno) se completaron una serie de experimentaciones para caracterizar la interacción entre proacrosina/acrosina humana y glicoproteínas de la ZP homóloga. Para los estudios se utilizó proacrosina/acrosina recuperada de espermatozoides y glicoproteínas obtenidas de ovocitos humanos de descarte de programas de fecundación in vitro, así como formas recombinantes de proacrosina (Rec-40) y productos truncados de su expresión (Re-30, Rec-20, Rec-10. Rec-6) generados en bacterias y glicoproteínas recombinantes de la ZP expresadas en células CHO (rec-hZPA, rec-hZPB, rec-hZPC). Los estudios revelaron la capacidad máxima de Rec-40 de interactuar principalmente con rec-hZPA, en concordancia con estudios en otras especies y demostraron el rol de los azúcares fucosa y manosa, presentes en los oligosacáridos de la ZP, en la interacción con la proenzima (23-25).
Teniendo en cuenta las funciones identificadas para el sistema de proacrosina/acrosina y que anticuerpos contra proteínas espermáticas han sido asociados a infertilidad humana, resultó relevante determinar la incidencia de anticuerpos contra el sistema proacrosina/acrosina en el suero de las mujeres en consulta por infertilidad. Empleando un ensayo de ELISA con la proacrosina humana recombinante (Rec-40) como antígeno (ELISA-Acro), se determinó una incidencia del 19% sobre un total de 179 sueros con anticuerpos contra el sistema de la proteasa. Una evaluación en paralelo realizada con el método de rutina de diagnóstico de infertilidad inmunológica (ensayo de immunobeads, IBT), arrojó resultados similares (incidencia de anticuerpos antiespermáticos contra proteínas espermáticas de superficie: 20%). Sin embargo, de los sueros antiacrosina positivos, sólo 6 fueron IB positivos, indicando que el ensayo clínico de rutina no permite predecir la presencia de anticuerpos antiacrosina. Estudios complementarios permitieron identificar un grupo de sueros que sólo reconocieron la región C-terminal de proacrosina, involucrada en el mecanismo de activación de la proenzima y en la interacción de proacrosina con componentes de la ZP. Todos esos sueros afectaron la unión de proacrosina recombinante a la proteína ZPA y en algunos casos también inhibieron la activación de la proenzima (26) (Figura 2). Estos estudios, en conjunto con los que realizamos usando un anticuerpo monoclonal contra la proenzima que mostraron un comportamiento similar y que inhibieron la EA (22), sugirieron el posible efecto deletéreo de los anticuerpos anticrosina sobre la fertilidad. Empleando un modelo experimental murino de inmunización genética contra proacrosina humana, se comprobó la respuesta humoral hacia la proacrosina/acrosina humana en los animales inmunizados, determinándose además la capacidad de esos anticuerpos generados de afectar la activación de proacrosina y de bloquear la interacción con la rec-hZPA; asimismo, los anticuerpos inhibieron de forma dosis-dependiente la fecundación in vitro y afectaron la fertilidad in vivo de los ratones, observándose un menor número de crías en las hembras inmunizadas y de un tamaño significativamente menor que las nacidas de hembras controles (27), confirmando su efecto negativo sobre la fertilidad e indirectamente la relevancia de este complejo enzimático en el proceso de la fecundación.
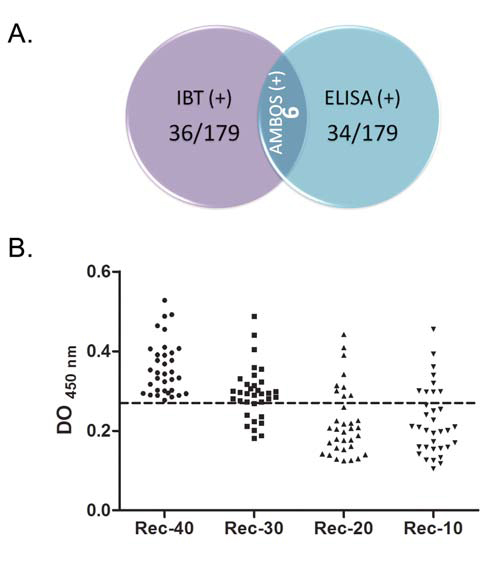
Figura 2: El sistema proacrosina/acrosina. Detección de anticuerpos en el suero de mujeres en consulta por infertilidad y reactividad a distintas regiones de la proenzima. A. Detección de anticuerpos antiproteínas espermáticas de superficie, mediante "Immunobead Binding Test" (IBT) y anticuerpos anti-proacrosina/acrosina, mediante ELISA indirecto (ELISA-Acro). Se analizaron los sueros de 179 mujeres en consulta por infertilidad, 36 (20%) presentaron anticuerpos contra antígenos de superficie según ensayo de IBT (>50% de espermatozoides unidos a microesferas) y en 34 (19%) se detectaron anticuerpos anti-proacrosina, según ensayo de ELISA-Acro. Sólo en 6 pacientes se encontró concordancia entre ambos ensayos. B. Análisis de las regiones de proacrosina reconocidas por los anticuerpos presentes en pacientes en consulta por infertilidad. Los sueros en los que se detectaron anticuerpos anti-proacrosina (n=34) utilizando proacrosina recombinante humana (Rec-40; aa 1-402) como antígeno fueron enfrentados a segmentos de la proteína truncados en el extremo C-terminal: Rec-30 (aa 1-300), Rec-20 (aa 1-190) y Rec-10 (aa 1-160). De los 34 sueros analizados, 25 presentaron reactividad contra Rec-30 y 9 reconocieron a Rec-20 y Rec-10. En línea de puntos se indica el valor de corte establecido para el ensayo (DO=0,270) (datos de ref. 26).
EXPRESIÓN DE MIEMBROS DE LAS CADHERINAS CLÁSICAS EN TEJIDOS REPRODUCTIVOS Y GAMETAS Y EVALUACIÓN DE SU PARTICIPACIÓN EN LA FECUNDACIÓN
La adhesión célula-célula regula numerosos procesos como el crecimiento, la movilidad, la diferenciación y la supervivencia de las mismas. Las cadherinas conforman una superfamilia de glicoproteínas transmembrana que intervienen en la unión célula-célula en forma dependiente de iones Ca2+. Dentro de la familia de las cadherinas Tipo I o clásicas, se encuentran la cadherina epitelial (uvomorulina, CAM120/80; cadE) y la cadherina neural (cadN). Como el resto de los miembros de la familia, poseen 5 dominios extracelulares cadherina (EC1-EC5), un dominio único transmembrana y un dominio citoplasmático. Los dominios cadherina extracelulares participan en las interacciones con moléculas de cadherina en la superficie de células adyacentes; una vez más los iones Ca2+ cumplen un rol clave, dado que su unión a sitios específicos cambia la conformación de la proteína haciendo que el dominio EC1 adquiera rigidez y permita la interacción entre cadherinas. Por su parte, el dominio citoplasmático une a la cadherina con moléculas adaptadoras, entre ellas β-catenina, y a través de ellas interactua con la red de filamentos de actina, para estabilizar la adhesión celular; esta región de la proteína también está involucrada en el tráfico y señalización celular (28)(29).
Dado que cadE y cadN participan en la adhesión celular dependiente de iones Ca2+y que el proceso de la fecundación involucra eventos de adhesión celular entre células somáticas y gametas y entre gametas entre sí que requieren de la presencia de este catión divalente, surgió el interés de caracterizar la expresión de ambas moléculas de adhesión en tejidos reproductivos y gametas y evaluar su posible participación en la fecundación; al inicio del proyecto, los estudios reportados sobre su presencia en las gametas eran escasos y el estudio de su rol en la fecundación no tenía antecedentes. La expresión de cadE en el epidídimo fue confirmada, determinándose la presencia del transcripto, así como la proteína en las células principales del epitelio epididimario y la forma completa de Mr 120.000 en extractos proteicos del epidídimo y de espermatozoides. CadE fue inmunolocalizada en espermatozoides no capacitados, capacitados y reaccionados, en regiones subcelulares que participan en la interacción gamética en particular en la membrana plasmática del ovocito; la proteína adaptadora β-catenina acompañó la localización de cadE. En ensayos in vitro de interacción de gametas (ensayo de Hemizona para evaluar la interacción espermática con la ZP y ensayo de penetración de ovocitos de hámster sin ZP para evaluar la unión y fusión del espermatozoide al ovocito) los anticuerpos anti-cadE inhibieron de manera significativa la unión del espermatozoide a componentes asociados a la estructura de la ZP y la penetración de los espermatozoides a ovocitos de hámster (30). Asimismo, se identificó la presencia y colocalización en el espermatozoide de un modulador negativo de las funciones de cadE, la proteína disadherina e inicialmente identificada principamente en células tumorales invasivas (31).
Los estudios sobre cadN confirmaron la expresión de la molécula de adhesión en el testículo y permitieron determinar los niveles de expresión del transcripto en la gonada y el epidídimo. Asimismo, las evaluaciones revelaron la presencia de la forma completa de cadN de 135 KDa en extractos de testículo y espermatozoides eyaculados. La proteína fue inmunolocalizada en el capuchón acrosomal de espermatozoides no capacitados y capacitados, mientras que se localizó en el segmento ecuatorial de los reaccionados. Asimismo, cadN fue localizada en la superficie del ovocito. La preincubacion de los espermatozoides con anticuerpos específicos no afectó su capacidad de interactuar con la ZP pero produjo una inhibición significativa de la penetración de los ovocitos de hámster, permitiendo proponer un rol para cadN en eventos que llevan a la fusión del espermatozoide al ovocito (32) (Figura 3).
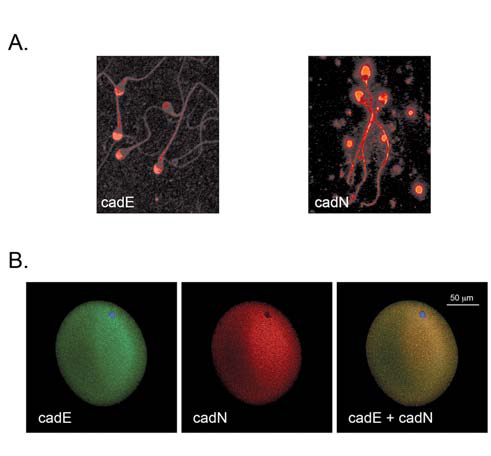
Figura 3. Cadherinas epitelial y neural. Inmunodetección en gametas humanas. Inmunolocalización de cadE y cadN en espermatozoides y ovocitos humanos A. Los espermatozoides fueron seleccionados y posteriormente fijados y sometidos a ensayos de inmunocitoquímica y registro por microscopía laser confocal. B. Inmunodetección de cadE y cadN en ovocitos humanos de descarte de programas de reproducción asistida sin ZP (estudios realizados en colaboración con el centro CEGYR) y evaluación empleando microscopía laser confocal. En A. y B. se emplearon los anticuerpos anti cadE (H-108) y anti cadN (H-63) (2 μg/mL, Santa Cruz Biotech) seguido de incubación con anti conejo marcado con CY3 (1:750). Como control se incluyó tinción con IgG de conejo 2 μg/mL (datos no mostrados) (datos de ref. 30 y 32).
Los estudios para ambas proteínas se han extendido a los modelos murino (Veiga et al, resultados no publicados) y bovino (Caballero et al., en consideración; Arzondo et al., resultados no publicados), obteniéndose resultados que apoyan los encontrados en el modelo humano.
CADHERINA EPITELIAL Y LA PROGRESIÓN TUMORAL. ALTERACIONES EN LA ADHESIÓN CELULAR MEDIADA POR CADHERINA EPITELIAL. ESTUDIOS EN LÍNEAS CELULARES
La alteración de la adhesión celular es un mecanismo clave en la progresión tumoral y en los procesos de metástasis; como parte de ese proceso, en numerosos cánceres se han identificado anormalidades en la expresión de cadE, la que se asocia de manera inversa a la agresividad del tumor. La pérdida de cadE en las células transformadas impide la formación de las uniones adherentes y les permite ignorar el ordenamiento tisular, infiltrar el estroma y eventualmente migrar hacia otros sitios. La supresión de la adhesión célula-célula puede disparar la liberación de células tumorales del tumor primario y conferirle propiedades invasivas. Los cambios en la expresión de cadE inducen respuestas celulares que llevan a la conversión de las células epiteliales en células con características mesenquimales, con un aumento de la motilidad y la invasividad, en un proceso llamado transición epitelio-mesenquimal (EMT, por sus siglas en inglés Epithelial-Mesenchymal Transition) (33).
La presencia de alteraciones en la expresión de cadE ha sido documentada en numerosos tumores de diversos orígenes tisulares. Particularmente, el cáncer de mama es la causa principal de mortalidad por cáncer en mujeres, representando el 14%; es el tipo de cáncer más común en las mujeres y representa el 23% de los canceres femeninos. Se ha descripto que la disminución parcial o total de cadE se asocia con la pérdida de características de diferenciación, la adquisición de invasividad celular, un mayor grado tumoral, un comportamiento metastásico de las células y un pronóstico pobre. Los estudios in vitro demuestran que las líneas celulares de cáncer humano con morfología epiteloide y diferenciada expresan cadE y son poco invasivas, mientras que las líneas con una morfología del tipo fibroblastoide son invasivas y han perdido la expresión de cadE. Como parte de los proyectos desarrollados por nuestro grupo en este área de investigación, se caracterizó la expresión de cadE y de proteínas relacionadas en las líneas celulares IBH-6 e IBH-4. Ambas líneas celulares fueron desarrolladas en el IBYME por la Dra. I.Luthy y col. a partir de carcinomas ductales infiltrantes de mama humanos. Como parte de los resultados, se identificó una forma distintiva de cadE de 89 KDa, truncada en el extremo C-terminal y presente en bajos niveles (<30% de la forma completa en células MCF-7), determinándose además la presencia de niveles de transcripto de cadE aproximadamente 1000 veces menores que en MCF-7. CadE presentó una localización intrace-lular puntillada y se contrapuso a la típica localización proteica en los bordes celulares y sitios de contacto en MCF-7; β-catenina acompañó a cadE y se identificaron cambios en la estructura de los filamentos de actina con detección de fibras de estrés de actina y una disminución de las adhesiones focales. Estos cambios son característicos de la transformación celular y sugieren una reorganización dinámica del citoesqueleto celular (Figura 4). Los estudios se han extendido a la evaluación de modelos experimentales de cáncer murino de mama (Lapyckyj et al, manuscrito en elaboración), y de vejiga (Lapyckyj et al., manuscrito en elaboración). En colaboración con el grupo liderado por el Dr. J Reventós y col. del Hospital de Vall d'Hebron de Barcelona, España, nos encontramos estudiando diversos modelos de estudio de cáncer de endometrio y de ovario (análisis en curso). Los modelos serán empleados en el estudio de las bases moleculares del cáncer y podrán ser utilizados en el diseño de estrategias y herramientas para su diagnóstico y tratamiento.

Figura 4. Expresión de miembros del complejo adherente: cadherina epitelial, β-catenina y actina filamentosa en líneas celulares de cáncer de mama humano. Análisis de localización de miembros del complejo adherente (cadE, β-catenina y actina filamentosa) líneas celulares de cáncer de mama humano IBH-4, IBH-6 y MCF-7. A. Inmunocito-química de fluorescencia y análisis por microscopía laser confocal de cadE (HECD-1, Zymed seguido de incubación con anti conejo marcado con CY3 1:750) en células IBH-6, IBH-4 y MCF-7. B. Detección de actina filamentosa (F-actina, verde) con faloidina-FITC (Invitrogen Life Technologies) en ensayos de colocalización con β-catenina (610153, BD Biosciences 1:1000), seguido de incubación con anti conejo marcado con CY3 1:750). Como control se incluyó tinción con IgG de conejo o ratón agregado a la misma concentración que el primer anticuerpo específico (datos no mostrados) (datos de ref. 34).
En conclusión, los proyectos abordados por nuestro grupo de investigación han contribuido a la comprensión de los eventos de interacción de las gametas durante la fecundación, así como entre las células somáticas durante la progresión tumoral.
Referencias bibliográficas
1. Yanagimachi R. Mammalian fertilization. En: The Physiology of Reproduction. Editores: Knobil E y Neill JD. Nueva York: Raven Press; 1994.
2. Wassarman PM, Jovine L, Litscher ES. A profile of fertilization in mammals. Nat Cell Biol (2001);3:E59-E64.
3. Vazquez-Levin MH, Marin-Briggiler CI. An overview on the molecular mechanisms involved in human fertilization. En: Infertility in the Male (4ta Edición). Editores: L. Lipshultz, S. Howards, y C. Niederberger. Nueva York: Cambridge University Press; 2009.
4. Marín-Briggiler CI, Tezón JG, Miranda PV, Vazquez-Levin MH. Effect of incubating human sperm at room temperature on capacitation-related events. Fertil Steril 2002; 77(2): 252-9.
5. Marín-Briggiler CI, Gonzalez-Echeverría F, Buffone M, Calamera JC, Tezón JG, Vazquez-Levin MH. Calcium requirements for human sperm function in vitro. Fertil Steril 2003; 79(6): 1396-403.
6. Marín-Briggiler CI, Vazquez-Levin MH, Gonzalez-Echev-erría F, Blaquier JA, Miranda PV, Tezón JG. Effect of an-tisperm antibodies present in human follicular fluid upon the acrosome reaction and sperm-zona pellucida interaction. Am J Reprod Immunol 2003; 50(3): 209-19.
7. Marín Briggiler CI, Gonzalez Echeverria MF, Blaquier J, Tezon JG, Vazquez-Levin MH. Identifican proteínas es-permáticas involucradas en la fecundación humana. Pagina de la Sociedad Iberoamericana de Información Científica (SIIC). http://www.siicsalud.com/dato/autor.php/81116
8. Marín-Briggiler CI, González-Echeverría MF, Munuce MJ, Ghersevich S, Caille AM, Hellman U, et al. Glucose-regulated protein 78 (Grp78/BiP) is secreted by human oviduct epithelial cells and the recombinant protein modulates sperm-zona pellucida binding. Fertil Steril 2010; 93(5): 1574-84.
9. Marín-Briggiler CI, Chertihin O, Buffone M, Herr JC, Vazquez-Levin MH, Visconti P. Evidence of the presence of calcium/calmodulin-cependent protein Kinase IV in human sperm and its involvement in motility regulation. J Cell Sci 2005; 118(Pt9): 2013-22.
10. Hunter RHF, Fléchon B, Fléchon JE. Distribution, morphology and epithelial interactions of bovine spermatozoa in the oviduct before and after ovulation: A scanning electron microscope study. Tissue Cell 1991; 23(5): 641-56.
11. De Jonge C. Biological basis for human capacitation. Hum Reprod Update 2005; 11(3): 205-14.
12. Delpino A, Castelli M. The 78 kDa glucose-regulated protein (GRP78/BIP.is expressed on the cell membrane, is released into cell culture medium and is also present in human peripheral circulation. Biosci Rep 2002; 22(3-4): 407-20.
13. Lachance C, Bailey JL, Leclerc P. Expression of Hsp60 and Grp78 in the human endometrium and oviduct, and their effect on sperm functions. Hum Reprod 2007; 22(10): 2606-14.
14. Llanos M, Vigil P, Salgado AM, Morales P. Inhibition of the acrosome reaction by trypsin inhibitors and prevention of penetration of spermatozoa through the human zona pellucida. J Reprod Fertil 1993; 97(1): 173-8.
15. Urch UA. Biochemistry and function of acrosin. En: Elements of Mammalian Fertilization. Wassarman P. (Editor). Boca Raton, Florida, US: CRC Press, p. 233-48; 1991.
16. Vazquez-Levin MH, Furlong LI, Veaute C, Ghiringhelli PD. An overview of the proacrosin/acrosin system in human spermatozoa. En: Treballs (Proceedings) de la So-cietat Catalana de Biología Endocrinologia molecular. Volumen especial, p. 1-16; 2005.
17. Zahn A, Furlong LI, Biancotti JC, Ghiringhelli PD, Marín-Briggiler CI, Vazquez-Levin MH. Evaluation of the proacrosin/acrosin system and its mechanism of activation in human sperm extracts. J Reprod Immunol 2002; 54(1-2): 43-63.
18. Biancotti JC, Furlong LI,Miranda S, Novella ML, Coronel CE, Vazquez-Levin MH. Caltrin-like proteins are found in human semen and may modulate proacrosin activation (en consideración).
19. Adham IM, Nayernia K, Engel W. Spermatozoa lacking acrosin protein show delayed fertilization. Mol Reprod Dev 1997; 46(3): 370-6.
20. Baba T, Azuma S, Kashiwabara S; Toyoda Y. Sperm from mice carrying a targeted mutation of the acrosin gene can penetrate the oocyte zona pellucida and effect fertilization. J Biol Chem 1994; 269(50): 31845-9.
21. Marí SI, Rawe V, Biancotti JC, Charreau EH, Dain L, Vazquez-Levin MH. Biochemical and molecular studies of the proacrosin/acrosin system in patients with unexplained infertility. Fertil Steril 2003; 79(Suppl 3): 1676-9.
22. Veaute C, Liu de Y, Furlong LI, Biancotti JC, Baker HW, Vazquez-Levin MH. Anti-human proacrosin antibody inhibits the zona pellucida (ZP)-induced acrosome reaction of ZP-bound spermatozoa. Fertil Steril 2010; 93(7): 2456-9.
23. Furlong LI, Hellman U, Krimer A, Tezón JG, Charreau EH, Vazquez-Levin MH. Expression of human proacrosin in Escherichia coli and binding to zona pellucida. Biol Reprod 2000; 62(3): 606-15
24. Furlong LI, Harris JD, Vazquez-Levin MH. Binding of re-combinant human proacrosin/acrosin to zona pellucida (ZP) glycoproteins. I. Studies with recombinant human ZPA, ZPB, and ZPC. Fertil Steril 2005; 83(6): 1780-90
25. Furlong LI, Veaute C, Vazquez-Levin MH. Binding of re-combinant human proacrosin/acrosin to zona pellucida glycoproteins. II. Participation of mannose residues in the interaction. Fertil Steril 2005; 83(6): 1791-6.
26. Veaute C, Furlong LI, Bronson R, Harris JD, Vazquez-Levin MH. Acrosin antibodies and infertility. I. Detection of antibodies towards proacrosin/acrosin in women consulting for infertility and evaluation of their effects upon the sperm protease activities. Fertil Steril 2009; 91(4): 1245-55.
27. Veaute C, Furlong LI, Cameo M, Harris JD, Vazquez-Levin MH. Antiacrosin antibodies and infertility. II. Gene immunization with human proacrosin to assess the effect of immunity toward proacrosin/acrosin upon protein activities and animal fertility. Fertil Steril 2009; 91(4): 1256-68.
28. Angst BD, Marcozzi C, Magee AI. The cadherin super-family. J Cell Sci 2001; 114(Pt4): 629-41.
29. van Roy F, Berx G. The cell-cell adhesion molecule Ecadherin. Cell Mol Life Sci 2008; 65(23): 3756-88.
30. Marín-Briggiler CI, Veiga MF, Matos ML, Echeverría MF, Furlong LI, Vazquez-Levin MH. Expression of epithelial cadherin in the human male reproductive tract and gametes and evidence of its participation in fertilization. Mol Hum Reprod 2008; 14(10): 561-71.
31. Gabrielli NM, Veiga MF, Matos ML, Quintana S, Chemes H, Blanco G, Vazquez-Levin MH. Expression of Dysadherin in the human male reproductive tract and in spermatozoa. Fertil Steril 2011; Jul 19. [Epub ahead of print]).
32. Marín-Briggiler CI, Lapyckyj L, González Echeverría MF, Rawe VY, Alvarez Sedó C, Vazquez-Levin MH. Neural cadherin is expressed in human gametes and participates in sperm-oocyte interaction events. Int J Androl 2010; 33(1): e228-39.
33. Thiery JP. Epithelial-mesenchymal transitions in tumour progression. Nat Rev Cancer 2002; 2(6): 442-54.
34. Lapyckyj L, Castillo LF, Matos ML, Gabrielli NM, Lüthy IA, Vazquez-Levin MH. Expression analysis of epithelial cadherin and related proteins in IBH-6 and IBH-4 human breast cancer cell lines. J Cell Physiol 2010; 222(3): 596-605.
LABORATORIO DE MECANISMOS MOLECULARES DE CARCINOGÉNESIS
Interacciones entre factores de crecimiento (GFs) y el receptor de progesterona (PR) en cáncer de mama.
Growth factors (GFs) and progesterone receptor (PR) crosstalks in breast cancer
Interações entre fatores de crescimento (GFs) e o receptor de progesterona (PR) em câncer de mama.
Patricia V. Elizalde, Cecilia Proietti, Roxana Schillaci, Maria E. Balaña, Leticia Labriola, Mariana Salatino, Wendy Béguelin, Romina Carnevale, Celeste Díaz Flaqué, Eduardo H. Charreau
Resumen
En trabajos previos hemos demostramos la existencia de interacciones bi-direccionales entre las vías de los progestá-genos y de la heregulina (HRG) en cáncer mamario. Encontramos que los progestágenos regulan la actividad y expresión del ErbB-2 y de la HRG. Describimos que la interacción entre la vía de la progesterona y de la HRG ocurre a nivel del PR que es activado transcripcionalmente por la HRG. Además encontramos que los progestágenos inducen la activación transcripcional de la proteína transductora de señales y activadora de la transcripción 3 (Stat3), que es un requisito para el crecimiento inducido por progestágenos en cáncer mamario. Demostramos que Stat3 es un punto de convergencia entre las vías de PR y de HRG/ErbB-2 en cáncer de mama, ya que la HRG, a través del ErbB-2, induce la activación de Stat3 mediante la integración del PR como molécula señalizadora. En línea con estos resultados, describimos la función de Stat3 como coactivador del PR activado por progesterona y como integrante de un complejo trans-cripcional en donde ErbB-2 actúa como coactivador de Stat3 sobre el promotor de ciclina D1. Estos resultados proveen nuevos blancos moleculares como terapéuticas alternativas para el tratamiento del cáncer de mama resistente a las terapias anti-hormonales y anti-tirosina quinasa.
Palabras clave: cáncer de mama; receptor de progesterona; ErbB2; heregulina.
Summary
Accumulating findings, including ours, have proven the presence of bidirectional interactions between progestins and heregulin (HRG) signaling pathways in breast cancer. On the one hand, we showed that PR activates the HRG/ErbB-2 pathway. On the other, we found that HRG induces PR trans-criptional activation. We have provided the first demonstration that progestins induced transcriptional activation of the signal transducer and activator of transcription 3 (Stat3), which is an absolute requirement for progestin-mediated in vitro and in vivo breast cancer growth. We have identified Stat3 as a convergence point between PR and HRG/ErbB-2 signaling pathways in breast cancer, given that Stat3 is activated by HRG via ErbB-2 and through the co-option of PR function as a signaling molecule. In line with these results, we have described Stat3 as a coactivator of ligand activated-PR and as part of a novel transcriptional complex where ErbB-2 functions as a Stat3 coactivator in progestin-induced cyclin D1 promoter activation. These results provide novel molecular targets as alternative therapies for breast cancer resistant to anti-hormonal and anti-tyrosine kinase therapies.
Key words: Breast cancer; progesterone receptor; ErbB2; heregulin ErbB2.
Resumo
Em trabalhos prévios temos demonstrado a existência de interações bidirecionais entre as vias dos progestágenos e da heregulina (HRG) em câncer mamário. Encontramos que os progestágenos regulam a atividade e expressão do ErbB-2 e da HRG. Descrevemos que a interação entre a via da proges-terona e da HRG ocorre em nível do PR que é ativado trans-cricionalmente pela HRG. Além disso encontramos que os pro-gestágenos induzem a ativação transcricional da proteína transdutora de sinais e ativadora da transcrição 3 (Stat3), que é um requisito para o crescimento induzido por progestágenos em câncer mamário. Demonstramos que Stat3 é um ponto
de convergência entre as vias de PR e de HRG/ErbB-2 em câncer de mama, já que a HRG, através do ErbB-2, induz a ativação de Stat3 mediante a integração do PR como molécula sinalizadora. Em linha com estes resultados, descreve-mos a função de Stat3 como coativador do PR ativado por progesterona e como integrante de um complexo transcri-cional onde ErbB-2 atua como coativador de Stat3 sobre o promotor de ciclina D1. Estes resultados fornecem novos alvos moleculares como terapêuticas alternativas para o tra-tamento do câncer de mama resistente às terapias anti-hor-monais e anti-tirosina quinase.
Palavras chave: câncer de mama; receptor de progestero-na; ErbB2; heregulina.
Los efectos de la progesterona en la glándula mamaria son controversiales debido a la complejidad estructural y funcional de este órgano. Dependiendo del modelo experimental, del contexto celular y de la duración del tratamiento, la progesterona puede ejercer efectos proliferativos o antiproliferativos en el crecimiento del epitelio mamario. Se ha hipotetizado que, luego de una ronda de proliferación, el pulso inicial de progesterona actúa como un factor iniciador para las acciones de factores secundarios involucrados en vías pro-liferativas, de diferenciación o apoptóticas. Entonces, serían los múltiples factores secundarios que regulan el crecimiento y desarrollo de un tumor de mama, en combinación con la progesterona, los que contribuyen con esta variedad de efectos (1).
Nuestro laboratorio trabaja en el estudio de las interacciones funcionales entre hormonas esteroideas, en particular la progesterona, GFs y factores de transcripción en cáncer de mama. En este campo de investigación hemos demostrado la existencia de interacciones bi-direccionales entre los caminos de transducción de señales de los progestágenos y de la heregulina (HRG), proteína ligando de los receptores con actividad de tirosina quinasa tipo I (RTKs tipo I). Específicamente hemos encontrado que los pro-gestágenos regulan la actividad y expresión de los RTKs, tipo I (ErbB-1, ErbB-2, ErbB-3 y ErbB-4) y de su ligando, HRG, en cáncer de mama, en modelos de ratón y humanos (2). Encontramos también que existe una interacción jerárquica funcional entre el ErbB-2 y el receptor del factor de crecimiento semejante a la insulina tipo I (IGF-IR), perteneciente a los RTKs tipo II, en el cáncer de mama (3). Este trabajo demostró por primera vez que el IGF-IR dirige la activación del ErbB-2, abriendo una nueva posibilidad de intervención terapéutica en cáncer de mama resistente a estrategias de bloqueo del ErbB-2.
Con el fin de investigar la participación de los pro-gestágenos y del PR en la progresión tumoral, estudiamos la regulación de caveolina-1, componente estructural de las caveolas y cuya expresión está asociada a la progresión y metástasis de tumores de mama y de próstata. Reportamos la inducción de caveolina-1 en cáncer de mama y demostramos su rol en la proliferación inducida por progestágenos, constituyendo así un posible blanco en el tratamiento del cáncer de mama (4).
Nuestro grupo describió que la interacción entre la vía de la progesterona y de la HRG ocurre a nivel del PR que es activado transcripcionalmente por la HRG (5). Esta activación requiere la presencia de un ErbB-2 funcional y activo. Esta fue la primera demostración en literatura de la activación transcripcional ligando-inde-pendiente del PR.
En nuestra línea de trabajo más reciente nos encontramos investigando la formación de complejos multimé-ricos entre receptores de hormonas esteroideas y proteínas transductoras de señales y activadoras de transcripción (Stats) en los promotores de genes que participan en la regulación del crecimiento y capacidad metastásica del cáncer de mama. En este campo, hemos demostrado la capacidad de los progestágenos de activar transcripcional-mente a Stat3 (6). Dicha activación es un evento necesario para la proliferación inducida por progestágenos en las células de cáncer de mama humanas y murinas. En línea con estos resultados, probamos que Stat3 y PR forman un complejo transcripcional en donde Stat3 actúa como coactivador del PR en la transcripción de los genes bcl-X y p21CIP1, involucrados en la regulación del ciclo celular inducida por progestágenos (7). Evaluamos además la participación de Stat3 en la red de interacciones bi-direccio-nales entre PR y HRG/ErbB-2 en cáncer de mama. Probamos que la HRG, a través del ErbB-2, induce la activación de Stat3 mediante la integración necesaria del PR como molécula señalizadora (8). Más aún, demostramos que la activación de Stat3 es un requisito absoluto en la proliferación inducida por HRG en células de cáncer de mama. Stat3 activada actúa así como un factor efector río abajo de la vía HRG/ErbB-2 y del PR activado independiente de su ligando para estimular la proliferación del cáncer de mama. Esta interacción entre ErbB-2, PR y Stat3 necesaria para el crecimiento del cáncer de mama, junto con los novedosos y recientes resultados sobre la localiza-ción nuclear del ErbB-2 y su función como regulador transcripcional, nos impulsaron a estudiar la localización nuclear del ErbB-2 inducida por progestágenos y la asociación física y funcional con Stat3 a nivel nuclear (9). Nuestros resultados describen por primera vez que los progestágenos inducen el ensamblado de un complejo transcripcional integrado por Stat3/ErbB-2 en donde ErbB-2 actúa como coactivador de Stat3. Dilucidamos además la presencia del PR en este complejo. Probamos que la función de ErbB-2 como coactivador de Stat3 regula la transcripción del gen de ciclina D1, inducido por proges-tágenos y esencial para el crecimiento del cáncer de mama. El bloqueo de la translocación de ErbB-2 mediante la transfección de una forma mutante dominante negativa incapaz de migrar al núcleo, inhibió la expresión de ciclina D1 y la proliferación inducida por progestágenos en células de cáncer de mama. Nuestros hallazgos revelan una nueva intervención terapéutica para tumores mamarios PR+/ErbB-2+ que consiste en el bloqueo específico de la translocación de ErbB-2 al núcleo. Otro campo de activa investigación en nuestro laboratorio son los efectos no ge-nómicos de los progestágenos en el desarrollo del cáncer de mama. Demostramos que los progestágenos inducen el crecimiento celular, regulan la actividad de las metalo-proteasas y la metástasis a través de la capacidad del PR de activar vías de señalización dependientes de la quinasa c-Src (10). Estos resultados sugieren una intervención terapéutica para tumores PR+ que consiste en el bloqueo específico de la función del PR como activador de las vías de señalización.
Actualmente estamos estudiando los efectos no ge-nómicos de los progestágenos en el factor de transcripción AP-1, dímero compuesto por Jun y Fos, activados por fosforilación y cuya presencia en tumores mamarios está asociada a mal pronóstico. Nuestro objetivo es demostrar la activación de AP-1 por progestá-genos y demostrar su participación en la transcripción del gen de ciclina D1 que contiene elementos respondedores a AP-1 en su promotor.
Referencias bibliográficas
1. Lange CA, Richer JK, Horwitz KB. Hypothesis: Progesterone primes breast cancer cells for cross-talk with proliferative or antiproliferative signals. Mol En-docrinol 1999; 13(6): 829-36.
2. Balana ME, Lupu R, Labriola L, Charreau EH, Eli-zalde PV. Interactions between progestins and hereg-ulin (HRG) signaling pathways: HRG acts as mediator of progestins proliferative effects in mouse mammary adenocarcinomas. Oncogene 1999; 18(46): 6370-9.
3. Balana ME, Labriola L, Salatino M, Movsichoff F, Peters G, Charreau EH, et al. Activation of ErbB-2 via a hierarchical interaction between ErbB-2 and type I insulin-like growth factor receptor in mammary tumor cells. Oncogene 2001; 20(1): 34-47.
4. Salatino M, Beguelin W, Peters MG, Carnevale R, Proietti CJ, Galigniana MD, et al. Progestin-induced caveolin-1 expression mediates breast cancer cell proliferation. Oncogene 2006; 25(59): 7723-39.
5. Labriola L, Salatino M, Proietti CJ, Pecci A, Coso OA, Kornblihtt AR, et al. Heregulin induces transcrip-tional activation of the progesterone receptor by a mechanism that requires functional ErbB-2 and mi-togen-activated protein kinase activation in breast cancer cells. Mol Cell Biol 2003; 23(3): 1095-111.
6. Proietti C, Salatino M, Rosemblit C, Carnevale R, Pecci A, Kornblihtt AR, et al. Progestins induce transcriptional activation of signal transducer and activator of transcription 3 (Stat3) via a Jak- and Src-dependent mechanism in breast cancer cells. Mol Cell Biol 200; 25(12): 4826-40.
7. Proietti CJ, Beguelin W, Flaque MC, Cayrol F, Ri-vas MA, Tkach M, et al. Novel role of signal transducer and activator of transcription 3 as a progesterone receptor coactivator in breast cancer. Steroids 2011; 76(4): 381-92.
8. Proietti CJ, Rosemblit C, Beguelin W, Rivas MA, Diaz Flaque MC, Charreau EH, et al. Activation of Stat3 by heregulin/ErbB-2 through the co-option of progesterone receptor signaling drives breast cancer growth. Mol Cell Biol 2009; 29(5): 1249-65.
9. Beguelin W, Diaz Flaque MC, Proietti CJ, Cayrol F, Rivas MA, Tkach M, et al. Progesterone receptor induces ErbB-2 nuclear translocation to promote breast cancer growth via a novel transcriptional effect: ErbB-2 function as a coactivator of Stat3. Mol Cell Biol 2010; 23: 5456-72.
10. Carnevale RP, Proietti CJ, Salatino M, Urtreger A, Peluffo G, Edwards DP, et al. Progestin effects on breast cancer cell proliferation, proteases activation, and in vivo development of metastatic phenotype all depend on progesterone receptor capacity to activate cytoplasmic signaling pathways. Mol Endocri-nol 2007; 21(6): 1335-58.
LABORATORIO DE CARCINOGÉNESIS HORMONAL
Crecimiento del cáncer de mama dependiente de receptores hormonales: aportes de un modelo experimental
Growth of hormone receptor dependent breast cancer: Contributions of an experimental model
Crescimento do câncer de mama receptor de hormônio dependente: contribuições de um modelo experimental
Claudia Lanari, Virginia Novaro, Carolina Lamb, Victoria Fabris, Paola Rojas, Sebastián Giulianelli, María Gorostiaga, Victoria Wargon, Tomás Guillardoy, María Laura Polo, Marina Riggio, Gonzalo Sequeira, Ana Sahores, María Pampera
Resumen
Si bien los estrógenos han demostrado tener un rol protagónico en el cáncer de mama, hoy se sabe que la progesterona, así como sus derivados sintéticos, ejercen roles proliferativos tanto en la glándula mamaria normal como neoplásica. Utilizando un modelo experimental de cáncer mamario murino, iniciado en la Academia Nacional de Medicina y trasladado al IBYME en el año 1995, demostramos la importancia de los fibroblastos asociados a tumor en la provisión de factores de crecimiento que activan en forma ligando-independiente a los receptores de progesterona (RPs) en las células tumorales. En este artículo mencionamos la importancia por un lado de la proporción de isoformas del RP en la determinación de la respuesta al tratamiento hormonal, y por otro, los mecanismos por los cuales el factor de crecimiento fibroblástico 2 (FGF2) estromal participaría en el crecimiento tumoral imitando la acción de la hormona.
Palabras clave: cáncer de mama; receptores de progesterona; hormono independencia; estroma; factor de crecimiento fibroblástico; receptores de factor de crecimiento fibroblástico.
Summary
It is well known that estrogens are key players regulating breast cancer growth. In addition, there is compelling evidence pointing out that progestins induce proliferative effects in normal and in neoplastic mammary glands. Using a murine breast cancer model, first developed in the National Academy of Medicine in Buenos Aires, and then moved to the IBYME in 1995, we demonstrated that carcinoma associated fibroblasts provide growth factors such as fibroblast growth factor 2 (FGF2), which are involved in the ligand independent activation of progesterone receptors (PR) of tumor cells. This article briefly describes, on one hand, the relevance of the evaluation of the PR isoform ratio to predict hormone responsiveness, and on the other hand, the mechanisms by which stromal FGF2 mimics the effects of progesterone to stimulate tumor growth.
Key words: breast cancer; progesterone receptors; hormone independence; stroma, fibroblast growth factor; fibroblast growth factor receptors.
Resumo
Embora os estrógenos tenham demonstrado ter um papel protagônico no câncer de mama, hoje se sabe que a progesterona, bem como seus derivados sintéticos, exerce papéis proliferativos tanto na glândula mamária normal quanto neoplásica. Utilizando um modelo experimental de câncer mamário murino, iniciado na Academia Nacional de Medicina e trasladado ao IBYME no ano 1995, demonstramos a importância dos fibroblastos associados a tumor na provisão de fatores de crescimento que ativam em forma ligando-independente os receptores de progesterona (RPs) nas células tumorais. Neste artigo mencionamos a importância, de um lado, da proporção de isoformas do RP na determinação da resposta ao tratamento hormonal, e do outro, dos mecanismos pelos quais o fator de crescimento fibroblástico 2 (FGF2) estromal participaria no crescimento tumoral imitando a ação do hormônio.
Palavras chave: câncer de mama; receptores de progesterona; hormônio independência; estroma; fator de crescimento fibroblástico (FGF); receptores de FGF (FGFR).
Cuando en el año 1983, trabajando en el Laboratorio de Leucemia Experimental de la Academia Nacional de Medicina con el Dr. A Molinolo y la Dra. CD Pasqualini, teníamos ratones BALB/c tratados con acetato de medroxiprogesterona (MPA) para inhibir la fibromatogénesis inducida por un cuerpo extraño, y aparecieron carcinomas mamarios, nos sorprendimos. Si bien había datos que vinculaban a los progestágenos con cáncer de mama, la mayoría de ellos apuntaban a los estrógenos como hormonas promotoras y/o iniciadoras en cáncer de mama. Hoy, casi treinta años después, no quedan dudas que los progestágenos participan en el desarrollo del cáncer de mama. El uso de MPA en la terapia de reemplazo hormonal fue lo que marcó la diferencia. Las evidencias experimentales estaban a la vista sin embargo el consenso se obtuvo después de la publicación del WHI Study en Estados Unidos en el 2002 (1) y del Million Study en Inglaterra 2003 (2)(3), que mostraron claramente un aumento de cáncer de mama en mujeres tratadas con ambas hormonas.
Las investigaciones en nuestro laboratorio se basaron en caracterizar este nuevo modelo experimental en el cual la mayor parte de los tumores de mama se clasificaron como carcinomas mamarios ductales infiltrantes con expresión de receptores de estrógenos (RE) y de progesterona (RP) y se mantenían por transplantes singeneicos en ratones tratados con hormona. Ocasionalmente surgían variantes tumorales con crecimiento autónomo, llamadas hormono-independientes por su capacidad de crecer sin el aporte exógeno de hormona. Cuando se evaluó la capacidad de los tumores de responder a distintos tratamientos hormonales descubrimos que muchos de ellos desaparecían casi completamente con tratamiento con antiprogestágenos o estrógenos y parcialmente con tamoxifeno. Otros tumores eran resistentes desde el comienzo; sin embargo, todos mantenían la expresión de RE y RP. Esto motivó que la mayor parte de las investigaciones de nuestro laboratorio, ya mudado en 1995 al IBYME se han dedicado a tratar de comprender los mecanismos por los cuales los tumores se vuelven hormono independientes o se hacen resistentes a la terapia hormonal (revisado en (4)).
Correlación de expresión de isoformas de receptor de progesterona y respuesta al tratamiento hormonal
Existen dos isoformas del RP ampliamente reconocidas que se transcriben a partir del mismo gen: la más grande es la isoforma B (RP-B) de 115 kDa y la más pequeña la isoforma A (RP-A) de 83 kDa en ratón y 94 kDa en humanos. La isoforma RP-A se ve más comprometida en cáncer de mama, ya que hay un mayor porcentaje de tumores RP positivos que expresan mayores niveles de isoforma A que B. A su vez éstos responderían menos al tamoxifeno en comparación con los que expresan más isoforma B que A (5). Nuestro grupo demostró que el perfil de isoformas de RP es diferente en carcinomas mamarios con distinta respuesta hormonal. Los tumores HI que regresionaban con antiprogestágenos o estrógenos expresaban altos niveles de RP-A, mientras que los resistentes constitutivos o los que fueron experimentalmente manipulados para ser resistentes (resistencia adquirida) mostraban mayores niveles de RP-B. Eso nos llevó a evaluar el porqué del silenciamiento de RP-A en tumores resistentes. Lo que sabemos al día de hoy es que los tumores resistentes constitutivos muestran metilación del promotor. Por lo tanto, el tratamiento de estos tumores con agentes desmetilantes, induce la reexpresión de RP-A y la consiguiente recuperación de la sensibilidad a los antiprogestágenos (6). No ocurre lo mismo con los resistentes adquiridos, pero en éstos, el tratamiento con estrógenos induce la reexpresión de RP-A, respondiendo ahora a la terapia conjunta de estrógenos y antiprogestágenos (7). Esta ida y vuelta de RP-A sugiere la presencia de mecanismos regulatorios epigenéticos más allá de la metilación que se están estudiados actualmente en el laboratorio. El mensaje clínico de esta parte de nuestro trabajo, es la sugerencia que aun los tumores que se hicieron resistentes a la terapia endócrina pueden ser direccionados para otro ciclo de tratamiento.
Quién activa a los receptores hormonales cuando las hormonas no están presentes o lo están en muy pequeña cantidad?
El otro tema que nos interesó es conocer qué es lo que activa a los receptores hormonales en tumores HI de modo tal que el bloqueo de los receptores permite frenar al crecimiento tumoral. Utilizamos nuestro modelo experimental para tratar de contestar este interrogante. Observaciones del laboratorio nos mostraban primero, que es muy difícil cultivar estos tumores en ausencia de fibroblastos, cuando los cultivos estaban contaminados con fibroblastos crecían mucho mejor y por otro lado, cuando las células tumorales purificadas de un tumor HD o de uno HI eran cultivados en plástico, eran indistinguibles entre sí. Esto sugería claramente que factores del huésped participan en el crecimiento HI. Uno de los componentes que conforma el estroma tumoral son los fibroblastos asociados a carcinoma (CAF). Postulamos entonces que los CAF de un tumor HI producirían factores de crecimiento que activarían a receptores de las células epiteliales que a su vez interactuarían con RP para activar la proliferación celular. Nos concentramos en el factor de crecimiento fibroblástico 2 (FGF2) y sus receptores FGFR. Elegimos este factor porque de los varios estudiados en su momento, fue el único capaz de reemplazar al MPA en su efecto proliferativo in vitro.
De acuerdo a la hipótesis planteada, demostramos que el estroma del tumor HI es diferente al del tumor HD (8) y que in vitro los CAF de los tumores HI producen más FGF2 que los tumores HD. El FGF2 por otra parte induce la activación de los RP. Demostramos asimismo que el FGF2 activa al FGFR2 e induce la traslocación nuclear del mismo de modo que interaccionaría con el RP junto con STAT5 induciendo la transcripción de genes blanco, como MYC y Ciclina D1, y la expresión de diversas proteínas reguladas por progesterona. La interacción entre FGFR-2 y RP fue confirmada por estudios de microscopía confocal, coinmunoprecipitaciones y ensayos de EMSA en placa. Para confirmar la hipótesis planteada que el eje FGF2-FGFR-2 está involucrado en el crecimiento HI demostramos que el inhibidor de FGFR (PD173074) inhibe el crecimiento HI y que la administración exógena de FGF2 a un tumor HD es capaz de estimular el crecimiento de un tumor imitando la acción de la hormona (9)(10).
Todos estos estudios fueron corroborados en la línea celular humana T47D que se comportó de manera muy similar a los tumores de nuestro modelo experimental. Más aun, la transfección constitutiva de un dominante activo del FGFR-2 a células T47D logró volverlas tumorigénicas al implantarlas en ratones inmunosuprimidos en ausencia de hormona (11).
En conjunto estos resultados muestran la participación del estroma en el crecimiento tumoral y sugieren el uso de terapias combinadas incorporando a inhibidores de FGFR en conjunto con la terapia endocrina para demorar la resistencia endocrina.
Referencias bibliográficas
1. Women's Health Initiative. Risks and benefits of estrogen plus progestin in healthy postmenopausal women: principal results From the Women's Health Initiative randomized controlled trial. JAMA 2002; 288(3): 321-3.
2. Beral V. Breast cancer and hormone-replacement therapy in the Million Women Study. Lancet 2003; 362(9382): 419-27.
3. Beral V, Reeves G, Bull D, Green J. Breast Cancer Risk in Relation to the Interval Between Menopause and Starting Hormone Therapy. J Natl Cancer Inst 2011; 16: 103(4): 296-305.
4. Lanari C, Lamb CA, Fabris VT, Helguero LA, Soldati R, Bottino MC, et al. The MPA mouse breast cancer model: evidence for a role of progesterone receptors in breast cancer. Endocr Relat Cancer 2009; 16(2): 333-50.
5. Hopp TA, Weiss HL, Hilsenbeck SG, Cui Y, Allred DC, Horwitz KB, et al. Breast cancer patients with progesterone receptor PR-A-rich tumors have poorer disease-free survival rates. Clin Cancer Res 2004; 10(8): 2751-60.
6. Wargon V, Fernandez SV, Goin M, Giulianelli S, Russo J, Lanari C. Hypermethylation of the progesterone receptor A in constitutive antiprogestin-resistant mouse mammary carcinomas. Breast Cancer Res Treat 2011; 126(2): 319-32.
7. Wargon V, Helguero LA, Bolado J, Rojas P, Novaro V, Molinolo A, et al. Reversal of antiprogestin resistance and progesterone receptor isoform ratio in acquired resistant mammary carcinomas. Breast Cancer Res Treat 2009; 116(3): 449-60.
8. Giulianelli S, Herschkowitz JI, Patel V, Lamb CA, Gutkind JS, Molinolo A, et al. MPA-induced gene expression and stromal and parenchymal gene expression profiles in luminal murine mammary carcinomas with different hormonal requirements. Breast Cancer Res Treat 2011; 129(1): 49-67.
9. Giulianelli S, Cerliani JP, Lamb CA, Fabris VT, Bottino MC, Gorostiaga MA, et al. Carcinoma-associated fibroblasts activate progesterone receptors and induce hormone independent mammary tumor growth: A role for the FGF-2/FGFR-2 axis. Int J Cancer 2008; 123(11): 2518-31.
10. Cerliani JP, Giulianelli S, Sahores A, Wargon V, Gongora A, Baldi A, et al. Mifepristone inhibits MPA-and FGF2-induced mammary tumor growth but not FGF2-induced mammary hyperplasia. Medicina (B Aires) 2010; 70(6): 529-32.
11. Cerliani JP, Guillardoy T, Giulianelli S, Vaque JP, Gutkind JS, Vanzulli SI, et al. Interaction between FGFR-2, STAT5 and progesterone receptors in breast cancer. Cancer Res 2011; 15; 71(10): 3720-31.
LABORATORIO DE HORMONAS Y CÁNCER
Receptores α2-adrenérgicos y cáncer de mama
α2-adrenoceptors and breast cancer
Receptores α2-adrenérgicos e câncer de mama
Isabel Alicia Lüthy, Ariana Bruzzone, Cecilia Pérez Piñero, Lilian Castillo
Resumen
El cáncer de mama es la neoplasia más frecuente entre las mujeres. Las experiencias estresantes causan la liberación de adrenalina y noradrenalina, que se unen a 9 receptores adrenérgicos. Nuestro grupo ha trabajado durante los últimos años en la caracterización de los receptores α2-adrenérgicos y en el efecto de su estimulación en diferentes modelos experimentales de cáncer de mama para contribuir a mejorar la calidad de vida de las pacientes. En células tumorales y no tumorales mamarias humanas encontramos que las catecolaminas endógenas adrenalina y noradrenalina y el agonista específico α2-adrenérgico clonidina estimulan significativamente la proliferación celular. La inhibición de los niveles de AMP cíclico correlacionan con la estimulación de dichos receptores. Hemos descripto la expresión de por lo menos un subtipo de receptor α2-adrenérgico en estas líneas tanto a nivel de ARNm (medida por RT-PCR) como de proteína (por inmunocitoquímica y unión de un antagonista radiactivo). Además hemos demostrado que los agonistas α2-adrenérgicos aumentan el crecimiento tumoral en modelos experimentales de cáncer de mama (tumores inducidos originalmente por acetato de medroxiprogesterona y xenotransplantes de células tumorales humanas). En todos los casos el antagonista α2-adrenérgico rauwolscina inhibió el crecimiento de los tumores control, pudiendo pensarse en utilizarlo como terapia adyuvante.
Palabras clave: cáncer de mama; receptores adrenérgicos; clonidina; rauwolscina.
Summary
Breast cancer is the most frequent women neoplasia. Stressing experiences enhance adrenalin and noradrenalin release. These catecholamines bind to 9 different adrenoceptors. Our group has described and characterized the α2-adrenoceptors and analyzed their effect in breast cancer models in order to contribute to a better quality of life in patients. The stimulation of these receptors with adrenalin, noradrenalin or α2-adrenergic agonists in both tumor and non-tumor human breast cells significantly stimulates cell proliferation, in correlation with inhibited cyclic AMP levels. At least one α2-adrenergic subtype in expressed in every cell line studied at the mRNA level (by RT-PCR) and at the protein level (immunocytochemistry and a radioactive antagonist binding). We have also found that the α2-adrenergic agonists enhance tumor growth in experimental models of breast cancer (transplanted mouse tumors originally induced by medroxyprogesterone acetate and human breast cancer cells xenotransplanted in nude mice). In every tumor model the α2-adrenergic antagonist rauwolscine inhibited tumor growth, suggesting the possibility of its utilization as an adjuvant therapy.
Key words: breast cancer; adrenoceptors; clonidine; rau-wolscine.
Resumo
O câncer de mama é a neoplasia mais frequente entre as mulheres. As experiências estressantes causam a liberação de adrenalina e noradrenalina, que se unem a 9 receptores adrenérgicos. Nosso grupo tem trabalhado durante os últimos anos na caracterização dos receptores α2 -adrenérgicos e no efeito de sua estimulação em diferentes modelos experimentais de câncer de mama para contribuir a melhorar a qualidade de vida das pacientes. Em células tumorais e não tumorais mamárias humanas encontramos que as catecolaminas endógenas adrenalina e noradrenalina e o agonista específico α2-adrenérgico clonidina estimulam significativamente a proliferação celular. A inibição dos níveis de AMP cíclico se correlaciona com a estimulação de tais receptores. Temos descrito a expressão de pelo menos um subtipo de receptor α2-adrenérgico nestas linhas tanto em nível de ARNm (medida por RT-PCR) quanto de proteína (por imunocito-química e união de um antagonista radiativo). Além disso temos demonstrado que os agonistas α2-adrenérgicos aumentam o crescimento tumoral em modelos experimentais de câncer de mama (tumores induzidos originalmente por acetato de medroxiprogesterona e xenotransplantes de células tumorais humanas). Em todos os casos o antagonista α2 -adrenérgico rauwolscine inibiu o crescimento dos tumores controle, podendo pensar em utilizá-lo como terapia adjuvante.
Palavras chaves: câncer de mama; receptores adrenérgicos; clonidina; rauwolscine
El cáncer de mama es la neoplasia más frecuente entre las mujeres (23%) (1). En la Argentina, cada año, mueren aproximadamente 5.400 mujeres y se estima que se diagnostican alrededor de 17.000 casos nuevos (2). Es, además, el cáncer más prevalente en la mayoría de las áreas geo grá ficas. Por lo tanto el cán cer de mama es un problema relevante para la salud en nuestro país así como en la mayoría de los países del mundo. Los antiestrógenos han sido la terapia más im por tante para las pacientes con cáncer de mama con receptores positivos y han logrado un indu dable progreso en el tratamiento, mejorando significativamente la sobrevida (3). Sin embargo, en una gran proporción de pacientes, sobre todo en aquellas con recurrencia o metás ta sis, se produce resistencia al tratamiento (3). Por esta razón es de importancia clínica encontrar otros tratamientos con mecanismos de acción diferente para complementar las terapias disponibles.
Las experiencias estresantes activan componentes del sistema límbico, que incluye el hipotálamo, el hipocampo y la amígdala entre otras regiones. En respuesta a señales neurosensoriales, se activa por un lado el eje hipotálamo-hipófiso-suprarrenal y por otro lado el sistema simpático. Los ganglios cercanos a la médula espinal liberan noradrenalina, mientras que las células cromoafines de la médula suprarrenal liberan adrenalina (4). Las catecolaminas naturales adrenalina y noradrenalina se unen a 9 receptores adrenérgicos, que se dividen en tres grandes grupos, receptores α1, α2 y β-adrenérgicos, ejerciendo su acción a través de esta unión. Los receptores adrenérgicos pertenecen a la familia de receptores de siete pasos trans mem bra na acopla dos a proteína G (GPCR). Lue go de la unión de los ligandos endógenos epine fri na y nor epi ne fri na, se produce un cambio conformacional que lleva a la activa ción de pro teí nas heterotriméricas que unen GTP. Los receptores α2-adrenérgicos se acoplan fundamen tal men te con pro teí nas G de la familia Gi/o. La se ñalización es tanto por la subunidad Gαin hibitoria co mo por las sub uni dades βγ. La activación de la pro teína G i lleva a una in hibición de la adenilil ci clasa que resulta en una disminución de los ni ve les intra ce lu la res de ade no sina mono fos fato cíclico (AMPc). En cambio, la liberación de las sub unidades βγcum ple im por tantes roles en la función celular (por ejemplo neu ro nal) me dian te la regula ción de cana les de Ca2+ y la activación de proteína kinasas activadas por mitó ge nos (MAPK) fun da men talmente kinasas reguladas por señales extracelulares (Erk) 1/2 (5).
Nuestro grupo ha estado trabajando durante los últimos años en la caracterización de los receptores α2-adrenérgicos y en el efecto de su estimulación en diferentes modelos experimentales de cáncer de mama para contribuir a mejorar la calidad de vida de las pacientes. El objetivo de estos trabajos es contribuir al conocimiento de la influencia de estos receptores sobre la progresión de estos tumores.
En un primer trabajo sobre acción adrenérgica en células tumorales mamarias humanas MCF-7 (6), encontramos que las dos catecolaminas endógenas, adrenalina o epinefrina y noradrenalina o norepinefrina, así como también el agonista específico α2-adrenérgico clonidina estimulan significativamente la proliferación celular (medida por incorporación de timidina tritiada) a concentraciones ente 10 pM y 10 nM. Al incubar las células en presencia de antagonistas de los receptores adrenérgicos, se observó que el antagonista α-adrenérgico propanolol no revertía este aumento de la proliferación celular, mientras que el antagonista α-adrenérgico fentolamina y el antagonista α2-adrenérgico yohimbina sí lo hacían. Para corroborar un efecto α2-adrenérgico, se analizaron los niveles de AMP cíclico (AMPc) con las diferentes incubaciones. Se observó que adrenalina, noradrenalina y clonidina provocaban una inhibición de estos niveles, que era revertida por la presencia simultánea del antagonista α2-adrenérgico yohimbina.
Posteriormente hemos descripto los receptores α2-adrenérgicos en diversas líneas celulares de mama humana, tanto tumorales como no tumorales (7). Las líneas mamarias humanas IBH-6 e IBH-7 desarrolladas en el laboratorio a partir de tumores primarios de pacientes (8), la línea MCF-7 y la no tumoral HBL-100 expresan los subtipos de receptor a2B y a2C-adrenérgicos. En cambio expresan un solo subtipo las células malignas HS-578T (a2A) y MDA-MB-231 y la línea no tumoral MCF-10A (a2B). Todos los compuestos αy α2-adrenérgicos compitieron efectivamente en ensayos de binding por los receptores α2-adrenérgicos, incluyendo adrenalina o epinefrina, noradrenalina o norepinefrina, yohimbina, clonidina, rauwolscina y prazosin (que es un antagonista α1-adrenérgico con alta afinidad por los subtipos α2B y α2C). Se comprobó la expresión de dichos receptores mediante inmunocitoquímica. En todas las líneas celulares los agonistas α2-adrenérgicos provocaban un incremento en la proliferación celular.
Además hemos demostrado que los compuestos α2-adrenérgicos aumentan el crecimiento tumoral en modelos experimentales de cáncer de mama (9). Se confirmó la expresión de receptores α2-adrenérgicos en la línea tumoral mamaria murina MC4-L5 mediante inmunocitoquímica, inmunofluorescencia y RT-PCR. La incubación de esta línea tumoral por 2 días con agonistas α2-adrenérgicos (clonidina y dexmedetomidina) incrementa significativamente la proliferación celular. Estos agonistas también estimularon significativamente el crecimiento de todos los tumores analizados (C4-HD, CC4-2-HD y CC4-3-HI) independientemente de la sensibilidad al acetato de medroxiprogesterona y de la inoculación de esta hormona a los ratones. Estos tumores fueron desarrollados en el laboratorio de la Dra. Claudia Lanari (10). Los antagonistas α2-adrenérgicos yohimbina y rauwolscina revirtieron completamente el efecto del agonista clonidina. Sin embargo, el grupo que recibió solamente yohimbina mostró en todos los casos un incremento constante aunque no significativo del crecimiento tumoral mientras que la rauwolscina sola disminuyó en todos los casos significativamente el crecimiento tumoral, comportándose como un agonista inverso. En los tumores CC4-3-HI, el tratamiento con rauwolscina aumentó la apoptosis y disminuyó el índice mitótico, mientras que la clonidina tuvo la acción inversa. Posteriormente (11) se analizó el efecto de las líneas tumorales mamarias humanas desarrolladas en el laboratorio y creciendo en ratones desnudos (12). Se comprobó que la clonidina también aumentó el crecimiento tumoral de las células IBH-4 e IBH-6 creciendo en ratones inmunodeficientes. En este modelo experimental también se observó una reversión del efecto del agonista α2-adrenérgicos por parte del antagonista rauwolscina, que en ausencia del agonista inhibió el crecimiento tumoral, comportándose nuevamente como agonista inverso. Se realizaron cultivos primarios de estos tumores, separando las células epiteliales de las estromales. Al incubar las células en cultivo con clonidina, se observó que la misma estimulaba la proliferación celular de la fracción en ri quecida en células epiteliales, de la fracción enriquecida en fibroblastos asociados a tumor y del cocultivo de ambas fracciones en ambos tumores (IBH-4 e IBH-6). El antagonista α2-adrenérgico rauwolscina revirtió en todas las fracciones el efecto de clonidina. Sin embargo cuando se incubaron las células solamente en presencia de rauwolscina todas las fracciones procedentes de tumores IBH-4 evidenciaron una inhibición de la proliferación celular, mientras que no se observó este efecto en las fracciones provenientes de tumores IBH-6. En ese mismo trabajo describimos que los fibroblastos murinos normales y asociados a tumor expresaban receptores α2-adrenérgicos mediante inmunocito química e inmuno histo quí mica. Esta marcación era también visible en tumores murinos y humanos tanto en células epiteliales como estromales. Los compuestos α2-adrenérgicos en todos los casos estimularon la proliferación de ambos tipos celulares.
En conjunto, estos trabajos demuestran que los receptores α2-adrenérgicos se expresan en tumores de mama tanto humanos como murinos y que su activación está asociada a un incremento de la proliferación celular y del crecimiento tumoral. En todos los casos el antagonista α2-adrenérgico rauwolscina revirtió el efecto proliferativo, y, lo que es más importante aun, en ausencia de agonistas inhibió la proliferación celular y el crecimiento tumoral al compararlo con el control, sugiriendo la posibilidad de su empleo como terapia complementaria para el cáncer de mama.
Referencias bibliográficas
1. Ferlay J, Shin HR, Bray F, Forman D, Mathers C, Parkin DM. Estimates of worldwide burden of cancer in 2008: GLOBOCAN 2008. Int J Cancer 2010; 127: 2893-917.
2. Viniegra M, Paolino M, Arrossi S. Cáncer de mama en Argentina: organización, cobertura y calidad de las acciones de prevención y control. Organización Panamericana de la Salud; 2010.
3. Borley AC, Hiscox S, Gee J, Smith C, Shaw V, Barrett-Lee P, et al. Anti-oestrogens but not oestrogen deprivation promote cellular invasion in intercellular adhesion-deficient breast cancer cells. Breast Cancer Res 2008; 10(6): R103.
4. Antoni MH, Lutgendorf SK, Cole SW, Dhabhar FS, Sephton SE, McDonald PG, et al. The influence of bio-behavioural factors on tumour biology: pathways and mechanisms. Nat Rev Cancer 2006; 6(3): 240-8.
5. Hein L. Adrenoceptors and signal transduction in neurons. Cell Tissue Res 2006; 326(2): 541-51.
6. Vazquez SM, Pignataro O, Luthy IA. Alpha2-adrenergic effect on human breast cancer MCF-7 cells. Breast Cancer Res Treat 1999; 55(1): 41-9.
7. Vazquez SM, Mladovan AG, Perez C, Bruzzone A, Baldi A, Luthy IA. Human breast cell lines exhibit functional alpha(2)-adrenoceptors. Cancer Chemother Pharmacol 2006; 58: 50-61.
8. Vazquez SM, Mladovan A, Garbovesky C, Baldi A, Luthy IA. Three novel hormone-responsive cell lines derived from primary human breast carcinomas: functional characterization. J Cell Physiol 2004; 199(3): 460-9.
9. Bruzzone A, Pinero CP, Castillo LF, Sarappa MG, Rojas P, Lanari C, et al. Alpha(2)-Adrenoceptor action on cell proliferation and mammary tumour growth in mice. Br J Pharmacol 2008; 155(4): 494-504.
10. Lanari C, Lamb CA, Fabris VT, Helguero LA, Soldati R, Bottino MC, et al. The MPA mouse breast cancer model:
evidence for a role of progesterone receptors in breast cancer. Endocr Relat Cancer 2009; 16(2): 333-50.
11. Bruzzone A, Pérez Piñero C, Rojas P, Romanatto M, Gass H, Lanari C, et al. α2-adrenoceptors enhance cell proliferation and mammary tumor growth acting through both the stroma and the tumor cells. Current Cancer Drug Targets 2011.
12. Bruzzone A, Vanzulli SI, Soldati R, Giulianelli S, Lanari C, Luthy IA. Novel human breast cancer cell lines IBH-4, IBH-6, and IBH-7 growing in nude mice. J Cell Physiol 2009; 219(2): 477-84.
LABORATORIO DE SEÑALIZACIÓN EN MELANOMA
El receptor Ror1 y su rol en cáncer
The role of Ror1 receptor in cancer
O receptor Ror1 e seu papel em câncer
Pablo López Bergami
Resumen
Las proteínas Wnt son ligandos que activan señales involucradas en proliferación, sobrevida, adhesión, migración, diferenciación y polaridad celular y como tal están involucradas en una amplia variedad de patologías. A diferencia de la vía Wnt canónica (o dependiente de beta-catenina) la vía no canónica posee numerosas ramificaciones y ha sido muy poco estudiada. Evidencias obtenidas en los últimos años sugieren que la vía Wnt no canónica (a través de Wnt5a) jugaría un importante rol en la progresión de numerosos tipos de tumores, incluyendo melanoma. Tradicionalmente, la mayor parte de la señalización por Wnt ha sido atribuida a la activación de Fzd y LRP. Sin embargo, evidencias mas recientes indican que Wnt puede ejercer sus efectos a través de receptores alternativos Ror1 y 2 (receptor huérfano 1 y 2 similar a tirosina quinasa). Estas proteínas son receptores de Tirosina Quinasa con una arquitectura funcional excepcional dentro de su familia ya que son los únicos en poseer dominios Kringle y dominios ricos en serina y treonina en el extremo C-terminal. Originalmente clonados como receptores huérfanos, su caracterización como receptores Wnt es relativamente reciente por lo cual su rol está en proceso de ser dilucidado.
Palabras clave: Wnt no-canónico; receptores Ror; cáncer.
Summary
Wnts are ligands that stimulate several signal transduction pathways involved in cell proliferation, survival, migration, and differentiation. Wnt pathway malfunction has been implied in various forms of disease. The most extensively studied Wnt pathway, termed canonical, results in stabilization of β-catenin and activation of gene expression by TCF and LEF transcription factors. However, Wnts can also activate numerous non-canonical pathways which are independent of β-catenin. These non-canonical pathways have been much less studied. Recent evidences suggest that the Wnt non-canonical pathway (via Wnt5a) would play an important role in several types of cancer, including melanoma. The Wnt signaling has usually been related to activation of Fzd and LRP receptors. However, more recent data indicate that Wnt can activate the alternative receptors Ror1 and 2 (receptor tyrosine kinase-like orphan receptor 1 and 2). These proteins belong to the Tyrosine kinase family and have particular functional domain such as the Kringle domains and Serine/Threonine domains at the C-terminal. Originally cloned as orphan receptors, they were more recently characterized as Wnt receptors and their cellular role is being elucidated.
Key words: non-canonical Wnt; Ror receptors; cancer.
Resumo
As proteínas Wnt são ligandos que ativam sinais envolvidos em proliferação, sobrevida, adesão, migração, diferenciação e polaridade celular e como tal estão envolvidas numa ampla variedade de patologias. À diferença da via Wnt canônica (ou dependente de beta-catenina) a via não canônica possui numerosas ramificações e tem sido muito pouco estudada. Evidências obtidas nos últimos anos sugerem que a via Wnt não canônica (através de Wnt5a) teria um importante papel na progressão de numerosos tipos de tumores, incluindo melanoma. Tradicionalmente, a maior parte da sinalização por Wnt tem sido atribuída à ativação de Fzd e LRP. Entretanto, evidências mais recentes indicam que Wnt pode exercer seus efeitos através de receptores alternativos Ror1 e 2 (Receptor tyrosine kinase-like orphan receptor 1 and 2). Estas proteínas são receptores de Tirosina Quinase com uma arquitetura funcional excepcional dentro de sua família já que são os únicos em possuir domínios Kringle e domínios ricos em serina e treonina no extremo C-terminal. Originalmente clonados como receptores órfãos, sua caracterização como receptores Wnt é relativamente recente pelo qual seu papel está em processo de ser elucidado.
Palavras chave: Wnt não-canônico; receptores Ror; câncer.
El melanoma es un grave problema sanitario debido a su creciente incidencia (es el quinto tumor más frecuente), su pésimo diagnóstico en el estadio metastásico y la falta de terapias efectivas. Distintos enfoques terapéuticos han fallado debido, entre otros motivos, a que en este tumor se observa una activación simultánea de varias vías de señalización. El objetivo general de los estudios que lleva adelante nuestro laboratorio es contribuir a mejorar el conocimiento de las vías de transducción de señales activas en melanoma. La suma de estos esfuerzos, sin duda, resultará en más y mejores alternativas terapéuticas contra esta enfermedad. A continuación se resumen los actuales proyectos del laboratorio.
Proyecto 1: Estudio del rol biológico de la vía de señalización Wnt/Ror1 en melanoma.
Proyecto 2: Caracterización de la vía de señalización Wnt no canónica.
Proyecto 3: Estudio del rol de GDF9 en cáncer.
Proyecto 4: Identificación y caracterización de blancos transcripcionales de STAT3.
Las vías de señalización Wnt no canónico, JAK/STAT3 y TGF-β se encuentran activas en forma constitutiva en melanoma y se ha demostrado su contribución a distintos aspectos del desarrollo y progresión de melanoma.
La vía de señalización Wnt no canónica ha sido muy poco estudiada y los mecanismos biológicos y moleculares involucrados se conocen sólo superficialmente. El primero de los proyectos tiene como objetivo determinar los mecanismos por los cuales la activación de esta vía contribuye al desarrollo y progresión de melanoma. El segundo proyecto complementa al anterior ya que pretende identificar los ligandos Wnt, los receptores y los mediadores celulares involucrados en esta vía de señalización.
GDF9 (Growth Differentiation Factor 9) es un miembro de la familia de TGF-β que ha sido caracterizado como un factor de crecimiento ovárico. Sin embargo, hemos observado que GDF9 es sobreexpresado en melanoma y podría contribuir al desarrollo tumoral. Actualmente, nos encontramos avocados a determinar el rol biológico de este factor de crecimiento en melanoma.
El factor de transcripción STAT3 cumple un importante rol en tumorigénesis. Nuestro objetivo es identificar nuevos blancos transcripcionales de STAT3 y caracterizar sus funciones en el contexto del desarrollo y progresión tumoral. Trabajos realizados en el laboratorio han establecido que la proteína scaffold RACK1 y la proteína quinasa PDK1 son reguladas por STAT3 y al aumentar su expresión incrementan la actividad de otras vías de señalización tales como PKC, JNK y PI3K/Akt.
El receptor Ror1 y su rol en cáncer
La señalización Wnt canónica y no-canónica
Las glicoproteínas Wnt forman una familia de 19 miembros que poseen entre 20% y 85% de identidad de aminoácidos entre sí. Estas proteínas son secretadas y actúan como ligandos extracelulares en forma autócrina y parácrina activando diferentes vías de señalización involucradas en proliferación, adhesión, sobrevida, migración, diferenciación y polaridad celular (1). Las proteínas Wnt se unen básicamente a tres tipos de receptores de membrana: Frizzled (Fzd o Fz, perteneciente a la familia de Receptores acoplados a proteína G), LRP (Low-density lipoprotein receptor-related protein) y ciertos receptores de tirosina quinasa (Ror1, Ror2 y Ryk) (1)(2). La unión de Wnt a sus receptores lleva a la fosforilación y activación de la proteína citosólica Disheveled (Dvl) mediante mecanismos no completamente esclarecidos. Dvl (particularmente Dvl2) juega un rol clave, ya que río abajo de esta proteína la señal se ramifica hacia la denominada vía canónica y múltiples vías no canónicas (1).
La vía canónica involucra la unión de Wnt a receptores de tipo Fzd en presencia de coreceptores LRP. En esta vía, la activación de Dvl estabiliza β-catenina, que de otra manera es ubiquitinada y degradada. β-catenina puede así translocar al núcleo, activar al factor de transcripción Tcf/Lef y regular la expresión de numerosos genes. Más recientemente se ha demostrado que Wnt puede activar vías alternativas, independientes de β-catenina y por lo tanto denominadas no-canónicas. En estos casos, las proteínas LRP no son necesarias y Wnt se une a receptores Fzd y, como se estableció mas recientemente, a los de tipo Tirosina Quinasa Ror1/2 o Ryk. El término "vías no canónicas" es utilizado en realidad para referirse a un conjunto numeroso de vías de señalización alternativas, tales como Wnt/calcineurina/NFAT, Wnt/PKC, Wnt/CAMKII, Wnt/Rho/ROCK, Wnt/proteína Gβ/γ/fosfodiesterasa/ cGMP (PDE), Wnt/proteína Gβ/γ/ fosfolipasa C (PLC) y Wnt/JNK que se activan en respuesta a señales no canónicas (2). Esta sobresimplificación pone de manifiesto la superficialidad de nuestro conocimiento de estas vías no canónicas. Aspectos tales como los factores que determinan la activación de una vía por sobre las otras o el grado de superposición entre ellas no han sido elucidados aún.
Otro interrogante clave que no ha sido esclarecido aún es porque algunos Wnts inducen alternativamente distintas vías de señalización y regulan aspectos tan diversos de la vida celular en distintos sistemas. Sin dudas, el elevado número de genes intervinientes ha dificultado su estudio. En mamíferos, se han identificado 19 genes Wnt y 10 genes Fzd además de un inusual número de moduladores solubles como sFRP, Dickkopf (Dkk) y WIF1, entre otros. El sistema se torna aún mas complejo por el hecho de que varios Fzd pueden actuar como receptores de un Wnt particular y que ciertos Fzd puede unir varios Wnts. Inicialmente, se consideró que algunos Wnts eran específicos para la vía canónica o no-canónica (por ejemplo, Wnt1, Wnt3a, Wnt3b, Wnt7a y Wnt8 para la canónica y Wnt2, Wnt4 Wnt5a, Wnt5b, Wnt6, Wnt7b y Wnt11 para la no canónica) pero más recientemente se ha demostrado en forma concluyente que esta especificidad no es tal y que en ciertas circunstancias aún los Wnts considerados "más específicos" pueden afectar ambas vías (1). Wnt5a, por ejemplo, además de activar la vía no-canónica suele inhibir la vía canónica. Estas y otras evidencias similares han dado origen a un nuevo paradigma que sostiene que la capacidad de activar una u otra vía no reside solo en los ligandos Wnt sino que además esta dada por el conjunto de receptores expresados por la célula (2).
Los Receptores de Tirosina Quinasa Ror1 y Ror2
Tradicionalmente, la mayor parte de la señalización por Wnt ha sido atribuida a la activación de Fzd y LRP. Sin embargo, evidencias más recientes indican que Wnt puede ejercer sus efectos a través de receptores alternativos como Ryk y Ror. Los receptores Ror1 y Ror2 (Receptor tyrosine kinase-like orphan receptor 1 and 2) fueron clonados hace 19 años y caracterizados como Receptores de Tirosina Quinasa huérfanos por desconocerse sus ligandos (3). Ror1 y Ror2 poseen 58% de identidad a nivel de aminoácidos y comparten todos sus dominios funcionales. Estos receptores poseen una arquitectura funcional excepcional dentro de su familia ya que son los únicos en poseer dominios Kringle y dominios ricos en Serina y Treonina en el extremo C-terminal. Gracias a estos dominios (involucrados en la formación de uniones proteína-proteína), se especula que estos receptores podrían regular y/o ser regulados por proteínas hasta ahora no involucradas en la señalización por receptores de Tirosina Quinasa. Interesantemente, los dominios de Serina/Treonina se encuentran conservados entre ortólogos de Ror2 pero no entre ortólogos de Ror1. Estudios en roedores demuestran patrones definidos de expresión espaciotemporal de Ror1 y Ror2 en tejidos embrionarios, congruentes con su rol crítico en desarrollo y organogénesis (4). Los diferentes fenotipos observados en estos estudios sugieren que Ror1 y Ror2 cumplen distintos roles en el organismo. Luego del nacimiento estas proteínas dejan de expresarse (4) y no son detectadas en tejidos normales adultos (5).
El descubrimiento en 2003 de que estas proteínas actuaban como receptores de Wnt (a través de su dominio rico en cisteínas, CRD) (6) aumentó el interés en ellas. La mayoría de los estudios hasta la fecha se han focalizado en Ror2. Recientemente, se ha propuesto un modelo por el cual Ror2 (y probablemente también Ror1) cumplirían en la vía no canónica un rol similar al del co-receptor LRP5/6 en la vía canónica (7). De esta manera, distintos Wnt, al unirse con receptores Ror o LRP activarían la vía no canónica o la canónica. De esta manera la competencia de estos coreceptores por Fzd produce una inhibición recíproca. Este modelo resalta la importancia de la expresión diferencial de receptores y permite explicar el hecho de que Ror2 puede activar la vía canónica o la no canónica en distintos tipos celulares. Estas y otras observaciones abonan el concepto de que la señalización por Wnt es fuertemente dependiente del balance entre los distintos Wnts expresados y sobretodo de la cohorte de receptores en la célula (2). Por razones difíciles de comprender, los trabajos que involucraron a Ror1 son muchísimo menos numerosos que los que tratan sobre Ror2, a pesar de que evidencias genéticas y bioquímicas sugieren que ambos receptores poseen funciones distintas. Por este motivo, se ha profundizado muy poco en las funciones y características de la señalización de este receptor en una célula humana adulta. Se ha demostrado que Ror1 se une a Wnt5a pero no a Wnt3, Wnt5b, o Wnt16 en células HEK293 y que es capaz de activar Rac en respuesta a Wnt5a en células HeLa y L. Se ha descripto que la activación de Ror1 por Wnt5a requiere la fosforilación de Ror1 por GSK3 (7), aunque también se ha descripto la transfosforilación de Ror1 por parte del receptor Met. Recientemente se determinó que Ror1 sufre procesos de glicosilación y monoubiquitinación pero no se ha establecido como estos afectan su funcion.
Participación de Ror1 en cáncer
Las evidencias que proponen un rol de Ror1 en cáncer son escasas aunque muy importantes desde el punto de vista funcional. Debe destacarse sin embargo, que la mayoría de los hallazgos que aquí se describen son muy recientes, reflejando el creciente interés en las funciones de Ror1. Se ha establecido claramente que Ror1 (pero no Ror2) esta sobreexpresado en leucemias (5) y cáncer renal. Dada su falta de expresión en tejidos normales adultos se ha propuesto el uso de Ror1 como marcador o como posible blanco terapéutico en leucemia linfocítica crónica (LLC). Mas allá de estos trabajos realizados en leucemias, Ror1 juega un rol importante en la célula tumoral (8). Se ha demostrado que la inhibición de Ror1 mediante RNA de interferencia induce muerte celular en dos tipos de células muy disímiles: HeLa y linfocitos B provenientes de LLC. La inhibición de Ror1 también ha sido asociada a una reducción en la proliferación y en la capacidad tumorigénica de células de carcinoma gástrico y cáncer de pulmón. Se determino que Ror1 podria intervenir en la activación de la vía Wnt no canónica en metástasis cerebrales de cáncer de mama. Estas observaciones se han producido en paralelo con el reconocimiento del importante rol en cáncer de Ror2 (9). Otro punto a tener muy en cuenta es que el rol de Ror1 debe ser analizado conjuntamente con el de las proteínas Wnt, sus únicos ligandos conocidos. Este aspecto será detallado en la siguiente sección.
La vía Wnt en melanoma
La activación de la vía canónica en melanoma se debe en muchos casos a modificaciones en intermediarios de esta vía como APC e ICAT que llevan a la activación y localización nuclear de β-catenina. Los Wnt que más frecuentemente activan esta vía en melanoma son Wnt1 y Wnt3a. Originalmente se considero que la vía canónica tenía un rol prooncogénico pero en la actualidad su rol se encuentra sujeto a debate (10).
La activación constitutiva de la vía no-canónica, fundamentalmente a través de Wnt5a, también es una característica distintiva de melanoma aunque se desconocen en profundidad los mecanismos moleculares involucrados. La expresión de otros Wnt "no canónicos" asociados a otros tipos de tumores como Wnt2, Wnt4, Wnt7b y Wnt11 no ha sido estudiada en melanoma. Wnt5a se encuentra sobreexpresada en melanoma (presumiblemente por la acción de STAT3) e induce aumentos en la adhesión, motilidad e invasión, la activación de EMT (Transición Epitelial-Mesenquimal), la inhibición de la expresión de supresores de metástasis como Kiss-1 y el aumento de expresión de activadores de metástasis como CD44 (11). Muchos de estos efectos son mediados por la activación de PKC, aunque persisten dudas sobre que isoforma es la involucrada. Sin embargo, debe hacerse notar que algunos de los experimentos en estos trabajos fueron realizados induciendo la sobreexpresión de Wnt5a en células que naturalmente expresaban altos niveles de este ligando, lo cual relativiza el significado de estas conclusiones. Interesantemente, la detección de Wnt5a en biopsias se correlacionó directamente con estadíos más avanzados e inversamente con la sobrevida del paciente. La sobreexpresión de Wnt5a en los tumores es localizada y ocurre en sitios de invasión activa y las células muestran características morfológicas asociadas a un comportamiento agresivo. Los receptores de Wnt5a caracterizados hasta el presente en melanoma son Fzd5 y Ror2. La expresión de este ultimo no solo correlaciona con la de Wnt5a sino que es necesaria para la inducción de metástasis de células B16 dependiente de Wnt5a.
Referencias bibliográficas
1. Rao TP, Kühl M. An updated overview on Wnt signaling pathways: a prelude for more. Circ Res 2010; 106: 1798-806.
2. van Amerongen R, Mikels A, Nusse R. Alternative wnt signaling is initiated by distinct receptors. Sci Signal 2008; 1: re9.
3. Masiakowski P, Carroll RD. A novel family of cell surface receptors with tyrosine kinase-like domain. J Biol Chem 1992; 267: 26181-90.
4. Green JL, Kuntz S, Sternberg PW. Ror receptor tyrosine kinases: orphans no more. Trends Cell Biol 2008; 18: 536-44.
5. Baskar S, Kwong KY, Hofer T, Levy JM, et al. Unique cell surface expression of receptor tyrosine kinase Ror1 in human B-cell chronic lymphocytic leukemia. Clin Cancer Res 2008; 14: 396-404.
6. Oishi I, Suzuki H, Onishi N, Takada R, Kani S, Ohkawara B, et al. The receptor tyrosine kinase Ror2 is involved in non-canonical Wnt5a/JNK signalling pathway. Genes Cells 2003; 8: 645-54.
7. Grumolato L, Liu G, Mong P, Mudbhary R, Biswas R, Arroyave R, et al. Canonical and noncanonical Wnts use a common mechanism to activate completely unrelated coreceptors. Genes Dev 2010; 24: 2517-30.
8. MacKeigan JP, Murphy LO, Blenis J. Sensitized RNAi screen of human kinases and phosphatases identifies new regulators of apoptosis and chemoresistance. Nat Cell Biol 2005; 7: 591-600.
9. O'Connell MP, Weeraratna AT. Hear the Wnt Ror: how melanoma cells adjust to changes in Wnt. Pigment Cell Melanoma Res 2009; 22: 724-39.
10. McDonald SL, Silver A.. The opposing roles of Wnt-5a in cancer. Br J Cancer 2009; 101: 209-14.
11. O'Connell MP, Fiori JL, Xu M, Carter AD, Frank BP, Camilli TC, French AD, et al. The orphan tyrosine kinase receptor, Ror2, mediates Wnt5A signaling in metasta-tic melanoma. Oncogene 2010; 29: 34-44.
LABORATORIO DE PATOLOGÍA Y FARMACOLOGÍA MOLECULAR
siARN y shARN: Aspectos básicos y aplicados. Su uso como agentes terapeúticos
siRNA and shRNA: basic and applied aspects. Their use as therapeutic agents
siARN e shARN: aspectos básicos e aplicados. Seu uso como agentes terapêuticos
Carolina Flumian, Gabriela Levy, Gabriela Bravo, Carla Gatto Cáceres, Martín Gómez, Adrián Góngora, Alberto Baldi
Resumen
La interferencia del ARN es un fenómeno por el cual pequeñas moléculas de ARN doble cadena inhiben la expresión génica de manera secuencia específica. Esta vía se encuentra altamente conservada en los organismos eucariotas. Existen varios tipos de ARN interferentes, entre ellos se encuentran los shARN (del inglés short hairping RNA) que a su vez, dan lugar a los siARN (del inglés small interfering RNA). La activación de esta vía de manera exógena constituye una estrategia prometedora para el tratamiento de múltiples enfermedades humanas tales como el cáncer, las infecciones virales, las enfermedades autoinmunes y neurodegenerativas. En el presente artículo se realiza la descripción de estas pequeñas moléculas, así como también de la vía involucrada y cuáles son los efectos de su activación. También se explican los problemas que presenta su aplicación y las perspectivas de su uso como agentes terapéuticos.
Palabras clave: iARN; siARN; shARN; silenciamiento génico; vectores virales; cáncer.
Summary
RNA interference is a phenomenon in which small double stranded RNAs mediate sequence-specific regulation of gene expression. This pathway is highly preserved in eukaryotic organisms. There are many types of interfering RNAs, among them, shRNAs (short hairping RNA) which give rise to siRNA (small interfering RNA). The exogenous activation of this pathway is a promising strategy as a treatment for various human diseases such as cancer, viral infections, autoimmune, and neurodegenerative diseases. In this article these small molecules, the pathway involved and the effects of their activation are described. In addition, the problems and perspectives of their application as therapeutic agents are presented.
Key words: iRNA; siRNA; shRNA; gene silencing; viral vectors; cancer.
Resumo
A interferência do ARN é um fenômeno pelo qual pequenas moléculas de ARN cadeia dupla inibem a expressão gênica de maneira sequência específica. Esta via se encontra altamente conservada nos organismos eucariotas. Existem vários tipos de ARN interferentes, entre eles se encontram os shARN (do inglês short hairping RNA) que por sua vez, dão lugar aos siARN (do inglês small interfering RNA). A ativação desta via de maneira exógena constitui uma estratégia promissora para o tratamento de múltiplas doenças humanas tais como o câncer, as infecções virais, as doenças autoimunes e neurodegenerativas. No presente artigo é realizada a descrição destas pequenas moléculas, bem como da via envolvida e quais são os efeitos de sua ativação. Também se explicam os problemas que apresenta sua aplicação e as perspectivas de seu uso como agentes terapêuticos.
Palavras chave: iARN; siARN; shARN; silenciamento gênico; vetores virais; câncer.
Interferencia del ARN
La interferencia del ARN (iARN) es un mecanismo muy conservado en el cual moléculas pequeñas de ARN silencian la expresión génica de manera post-trascripcional (1). Esta vía ha sido reconocida como una de las principales formas de regulación de la expresión génica en células eucariotas (2). Existen varios tipos de ARN pequeños regulatorios. Entre ellos, se encuentran los ARNs pequeños interferentes (siARN, del inglés small interfering RNAs) que consisten en moléculas de ARN doble cadena de 21-23 nucleótidos con 2 ó 3 nucleótidos libres en el extremo 3´ de manera simétrica (3). También existen los shARN (del inglés short hairping RNA) que son ARNs doble cadena que poseen una zona perfectamente complementaria y un rulo que no presenta complementariedad. Los shARNs son tomados en el citoplasma por una enzima llamada Dicer, que es una ribonucleasa tipo III, que corta el shARN dando lugar al siARN (4). Entonces, los siARNs son incorporados a un complejo llamado RISK (del inglés RNA-induced silencing complex) cuyo núcleo catalítico está constituido por la proteína Argonauta 2 (Ago2) que degrada una de las dos hebras. Cuál de las dos hebras es degradada se determina por las propiedades termodinámicas de las terminales del siARN que, a su vez, determinan su orientación dentro del Ago2 y cuál de las dos hebras va a servir como hebra guía (5). Esto da lugar a un complejo RISK activado que contiene un fragmento de ARN simple cadena que es antisentido con respecto al ARN mensajero (ARNm) blanco (6). Este complejo permite la unión con el ARNm y Ago2 rompe la unión fosfodiéster del ARNm que se ubica en el medio del sitio de reconocimiento siARN:ARNm. Los fragmentos del ARNm resultantes son liberados, y, por ende, son degradados al ser reconocidos como transcriptos aberrantes. El complejo activado puede actuar sobre varias moléculas de ARNm de manera sucesiva, ampliando el efecto de silenciamiento (7).
Por otro lado, además del efecto post-transcripcional, los siARNs promueven la modificación del ADN, facilitando el silenciamiento de la cromatina, mediante la expansión de segmentos de heterocromatina, a través del complejo RITS (del inglés RNA-induced transcriptional silencing) (8).
Silenciamiento génico selectivo
Conociendo la existencia de este tipo de mecanismo en los organismos, se pensó en la posibilidad de regular la expresión de ciertos genes induciendo esta vía por medio de la introducción de siARNs de manera exógena. Esto podría permitir contrarrestar la sobreexpresión de genes que se observa en distintas patologías, entre ellas, el cáncer. La interferencia de la expresión del ARN pude ser lograda de dos formas: 1) mediante la introducción al citoplasma de siARNs, o 2) mediante la incorporación al núcleo de casetes que codifiquen shARNs. En ambos casos, el mecanismo de ARNi sólo permite una inhibición parcial o knock down de la expresión del gen de interés, a diferencia de las técnicas existentes de knock out (9).
Se debe tener en cuenta que la eficacia del siARN diseñado depende de la accesibilidad de la zona de apareamiento en el ARNm, de la presencia de estructuras secundarias o de su asociación con proteínas.
Efectos inespecíficos (off-target)
Los siARNs y los shARNs, pueden producir una reducción no deseada de la expresión de algunos genes cuya secuencia es similar a la reconocida por siARN, debido al corte del ARNm correspondiente o por la inhibición de su traducción (10)(11). Estos efectos pueden reducirse mediante la modificación química del segundo residuo de la hebra activa del siARN, sin afectar al silenciamiento del ARNm específico (12). Además, es necesario eliminar en el diseño todos los siARNs que presenten una cierta similitud con las moléculas de ARNm no buscadas, mediante la utilización de BLAST.
El problema de la llegada a destino
Los siARNs son moléculas cargadas negativamente que no pueden a penetrar fácilmente las membranas lipídicas celulares sin algún compuesto carrier que las asista. Además, los siARNs que no se modifican químicamente generalmente son degradados por las ARNasas presentes en el suero. A su vez, se debe tener en cuenta la dificultad adicional que representa la administración in vivo de siARNs, ya sea que se realice de manera sistémica o localizada.
In vitro, estas dificultades pueden ser superadas para la mayoría de los tipos celulares si los siARNs se unen a reactivos lipídicos catiónicos. Sin embargo, existen muchas limitaciones en el uso de esta estrategia debido a la falta de especificidad con respecto al tipo celular que se pretenda como blanco del tratamiento, como así también, debido a la toxicidad de muchos de estos reactivos.
Con el fin de lograr una mayor especificidad de los siARNs por la población celular blanco in vivo, se ha desarrollado una serie de estrategias que incluyen la conjugación de los siARNs a agentes que reconocen de manera específica moléculas presentes en la superficie celular de la población blanco, como por ejemplo anticuerpos, ligandos y aptámeros.
La duración del efecto de silenciamiento
Las formas antes mencionadas de administración de los siARNs llevan a un silenciamiento transitorio, ya que la concentración intracelular de los siARNs va a ir disminuyendo debido a las divisiones celulares y a su degradación. Por el contrario, si se logra que la población blanco exprese los shARNs de interés, esto va a permitir que el efecto de silenciamiento dure hasta tanto la célula los transcriba. Esto es una cualidad ideal para el tratamiento de enfermedades crónicas. En este contexto, los virus y vectores derivados de los mismos constituyen un sistema que permite no sólo superar el problema de atravesar la membrana plasmática, sino también de penetrar la envoltura nuclear resultando en la incorporación de la secuencia que codifica para el shARN al genoma, posibilitando la expresión de los shARNs de manera estable.
El diseño de vectores virales fue posible gracias al descubrimiento de que la expresión de shRNAs induce la maquinaria de ARNi (13). Esta estrategia involucra el clonado de un oligonucleótido que codifica para el shARN en un plásmido o vector viral que permite la expresión endógena del shARN, que luego es procesado en el citoplasma de la célula hospedadora, dando lugar a los siARNs.
Perspectivas terapéuticas
Un gran número de trabajos constituyen la prueba de que el mecanismo de ARNi puede ser potencialmente utilizado para el tratamiento de una gran variedad de enfermedades (14)(15). Más aún, algunos siARNs ya están siendo utilizados en pruebas clínicas (16). Particularmente, en nuestro laboratorio, teniendo como modelo de trabajo al melanoma humano, nos propusimos estudiar los beneficios del silenciamiento de factores proangiogénicos que se encuentran sobreexpresados en este tipo de cáncer como posible terapia, ya que estos genes contribuyen al desarrollo y progresión de la enfermedad. Con este fin, hemos desarrollado algunos shARNs que tienen como blanco a uno de estos factores y, utilizando vectores virales derivados de retrovirus, se lograron establecer líneas celulares que expresan de manera estable el shARN y que muestran un silenciamiento de entre el 75 y el 95% que, a su vez, correlaciona con un aumento en la apoptosis.
Sin embargo, y a pesar del gran potencial de estas técnicas, existen grandes limitaciones en el uso de siARNs debido a las fallas con respecto a la seguridad y efectividad de los métodos para su administración específica en los tejidos o tipos celulares deseados. A pesar de estas dificultades consideramos que, con el continuo avance en las investigaciones, estas dificultades podrán ser superadas y que el uso de siARNs y shARN dará lugar a tratamientos efectivos contra enfermedades humanas.
Referencias bibliográficas
1. Bartel DP. MicroRNAs: genomics, biogenesis, mechanism, and function. Cell 2004; 116: 281-97.
2. Plasterk RH. Micro RNAs in animal development. Cell 2006; 124: 877-81.
3. Kim VN: MicroRNA biogenesis: coordinated cropping and dicing. Nat Rev Mol Cell Biol 2005; 6: 376-85.
4. Bernstein E. Caudy AA, Hammond SM, Hannon GJ. Role for a bidentate ribonuclease in the initiation step of RNA interference. Nature 2001; 409: 363-6.
5. Schwarz DS, Hutvagner G, Du T, Xu Z, Aronin N, Zamore PD. Asymmetry in the assembly of the RNAi enzyme complex. Cell 2003; 115(2): 199-208.
6. Rana TM. Illuminating the silence: understanding the structure and function of small RNAs. Nat Rev Mol Cell Biol 2007; 23-36.
7. Hutvagner G, Zamore PD. A microRNA in a multiple-turnover RNAi enzyme complex. Science 2002; 297: 2056-60.
8. Matzke MA, Matzke AJM. Planting the seeds of a new paradigm. PLoS Biol 2004; 2(5): E133.
9. Bartlett DW, Davis ME. Insights into the kinetics of siRNA-mediated gene silencing from live-cell and live-animal bioluminescent imaging. Nucleic Acids Res 2006; 34: 322-33.
10. Li C, Parker A, Menocal E, Xiang S, Borodyansky L, Fruehauf J. Delivery of RNA interference. Cell Cycle 2006; 5(18): 2103-9.
11. Takeshita F, Ochiya T. Therapeutic potential of RNA interference against cancer. Cancer Sci 2006; 97(8): 689-96.
12. Tong A, Zhang Y, Nemunaitis J. Small interfering RNA for experimental cancer therapy. Curr Opin Mol Ther 2005; 7(2): 114-24.
13. Brummelkamp TR, Bernards R, Agami R. A System for Stable Expression of Short Interfering RNAs in Mammalian Cells. Science 2002; 296:550-3.
14. Dykxhoorn DM, Lieberman J. Knocking down disease with siRNAs. Cell 2006; 126(2): 231-5.
15. Castanotto D, Rossi JJ. The promises and pitfalls of RNA-interference-based therapeutics. Nature 2009; 457(7228): 426-33.
16. Tiemann K, Rossi JJ. RNAi-based therapeutics-current status, challenges and prospects. EMBO Mol Med 2009; 1(3): 142-51.
LABORATORIO DE PATOLOGÍA Y FARMACOLOGÍA MOLECULAR
Potencial proangiogénico de los productos de disolución de materiales vítreos bioactivos
Angiogenic potential of bioactive glasses ionic dissolution products
Potencial proangiogênico dos produtos de dissolução de materiais vítreos bioativos
Luis A. Haro Durand1,2, Adrián Góngora1, Martín Gomez1, Alberto Baldi1, Alejandro Gorustovich2
1 Instituto de Biología y MedicinaExperimental IByME-CONICET,
2 Buenos Aires, Argentina; Grupo Interdisciplinario en Materiales, IE-SIING-UCASAL, INTECIN, UBA-CONICET, Salta, Argentina
Resumen
La angiogénesis es un proceso complejo caracterizado por una cascada de eventos que llevan a la activación, proliferación y migración de células endoteliales y al remodelado y estabilización del tejido vascular. Recientes intentos por estimular angiogénesis se han enfocado en la entrega de factores de crecimientos tales como el factor de crecimiento endotelial (VEGF) y el factor de crecimiento fibroblástico básico (bFGF), terapia génica y terapia basada en células, pero estos procedimientos son caros y los mecanismos de entrega óptimos son aún poco comprendidos, por lo tanto, contar con estrategias más sencillas y menos costosas para inducir angiogénesis, representarían una muy buena alternativa al uso de factores de crecimientos costosos para estimular la neovascularización en un tejido en reparación. Los vidrios bio-activos han sido ampliamente investigados para la regeneración de tejido óseo, sin embargo ha habido poca investigación en la aplicación de los vidrios biactivos para reparar tejidos blandos altamente vascularizados y particularmente, la influencia que tienen sobre la neovascularización. Sin embargo recientes trabajos han mostrado la habilidad de los vidrios bioactivos para promover angiogénesis lo cual es crítico para numerosas aplicaciones en la reparación de herida y en estrategias para la ingeniería de tejidos. Este artículo, en la primera parte; presenta una visión general de los vidrios bioactivos haciendo énfasis en las características que determinan la bioactividad de los vidrios de silicato bio-activos y en la segunda parte, revisa la evidencia existente en la bibliografía sobre estudios que han demostrado el potencial de los vidrios bioactivos, particularmente el 45S5 Bioglass® de estimular la angiogénesis, a través de sus productos de disolución iónica.
Palabras clave: angiogénesis; vidrios bioactivos; bioglass; reparación y regeneración de tejidos; ingeniería de tejidos.
Summary
Angiogenesis is complex multi-step process that involves endothelial cell activation, dissolution of surrounding basement membrane, increased endothelial cell proliferation and migration, tube formation to form a vascular network. Recent attempts to stimulate angiogenesis have focused on the delivery of growth factors and cytokines, such us vascular endothelial growth factor (VEGF) and basic fibroblast growth factor (bFGF), gene therapy and cells-based therapy. However the growth factors are expensive and the optimal delivery strategies are unclear. Therefore use others easier and cheaper strategies to induce angiogenesis could provide and alternative approach to the use of expensive growth factor for stimulating neovascularization of wound repair. While the bioactive glasses have been extensively investigated for bone repair and regeneration, there has been relatively little research on the application of bioactive glass to highly vascularized soft tissues repair and particularly, the effect on the neovascularization. However, there is emerging evidence in the literature that the use of bioactive glasses in biomaterial-based tissue engineering strategies may improve the vascularization, it is the major limitation of tissue engineering approaches for the replacement of diseased or damaged tissue. This article, in the first part, reviews the bioactivity characteristics of silicate bioactive glasses. In the second part, discusses the evidences in the literature showing the angiogenic potential of bioactive glasses ionic dissolution products, focusing on 45S5 bioglass®.
Key words: angiogenesis; bioactive glasses; bioglass; wound repair and tissue engineering.
Resumo
A angiogênese é um processo complexo caracterizado por uma cascata de eventos que levam à ativação, proliferação e migração de células endoteliais e à remodelagem e estabilização do tecido vascular. Recentes tentativas por estimular angiogênese têm se focado na entrega de fatores de crescimentos tais como o fator de crescimento endotelial (VEGF) e o fator de crescimento fibroblástico básico (bFGF), terapia gênica e terapia baseada em células, mas estes procedimentos são caros e os mecanismos de entrega ótimos são ainda pouco compreendidos, portanto, poder contar com estratégias mais simples e menos custosas para induzir angiogênese, representariam uma muito boa alternativa ao uso de fatores de crescimentos custosos para estimular a neovascularização num tecido em reparação. Os vidros bioativos têm sido amplamente pesquisados para a regeneração de tecido ósseo, entretanto tem havido pouca pesquisa na aplicação dos vidros bioativos para reparar tecidos moles altamente vascularizados e particularmente, a influência que têm sobre a neovascularização. Entretanto recentes trabalhos têm mostrado a habilidade dos vidros bioativos para promover angiogênese o qual é crítico para numerosas aplicações na reparação de ferida e em estratégias para a engenharia de tecidos. Este artigo, na primeira parte; apresenta uma visão geral dos vidros bioativos fazendo ênfase nas características que determinam a bioatividade dos vidros de silicato bioativos e, na segunda parte, revisa a evidência existente na bibliografia sobre estudos que têm demonstrado o potencial dos vidros bioativos, particularmente o 45S5 Bioglass® de estimular a angiogênese, através de seus produtos de dissolução iônica.
Palavras chave: angiogênese; vidros bioativos; bioglass; reparação e regeneração de tecidos; engenharia de tecidos.
Biomateriales
Los biomateriales son materiales sintéticos o naturales modificados que tienen la habilidad de coexistir en contacto con tejidos del cuerpo humano sin causar ningún grado de daño al cuerpo (1). Los biomateriales han sido categorizados, según el comportamiento biológico desencadenado por los mismos, en: biomateriales de primera, segunda y tercera generación. Los materiales de primera generación han demostrado un comportamiento bioinerte (no-bioactivo), mientras que los de segunda y tercera generación poseen propiedades bioactivas (2). La nueva generación de materiales bioactivos, denominada tercera generación, comprende a todos aquellos materiales biorreabsorvibles y/o biodegradables que tienen la capacidad de estimular respuestas celulares específicas a nivel molecular como resultado de la liberación de iones a partir de los mismos (3).
Vidrios Bioactivos
Un material bioactivo ha sido definido como un material que ha sido diseñado para inducir un respuesta biológica específica (4). La característica común que comparten todos los materiales bioactivos es una modificación cinética, dependiente del tiempo que ocurre bajo implantación (5). La superficie forma una capa de hidroxicarbonatoapatita (HCA) biológicamente activa que provee la interfase de unión con los tejidos. La HCA que se forma sobre el implante bioactivo es estructural y químicamente equivalente a la fase mineral del hueso (5). La habilidad de un material de precipitar sobre su superficie una capa de HCA cuando es sumergido en un fluido fisiológico simulado in vitro, es a menudo tomado como un indicador de bioactividad (6), pero este concepto esta siendo cuestionado debido a la creciente evidencia de que no siempre la bioactividad observada in vitro, implique estrictamente una bioactividad in vivo (4). La unión al tejido óseo fue primero demostrado para ciertos rangos de composición de vidrios bioactivos que contenían SiO2, Nα2O, CaO y P2O5 en proporciones especificas, estos presentaban tres características composiciónales claves que los distinguían de los vidrios tradicionales: [1] menos del 60% de SiO2, [2] alto contenido de Nα2O y CaO y (3) alta relación CaO/P2O5. Estas características composicionales hacen a la superficie del material altamente reactiva cuando es expuesta a medios acuosos (5).
Vidrios de Silicato Bioactivos
Desde su descubrimiento hace aproximadamente 40 años, el vidrio de silicato bioactivo 45S5 Bioglass (composición en %; 45% SiO2 24,5% Nα2O, 24,5% CaO, y 6% P2O5) ha sido el más ampliamente investigado para aplicaciones biomédicas (4). Este material inorgánico provee un medioambiente ideal para la colonización, proliferación y diferenciación de osteoblastos para formar hueso nuevo exhibiendo, una unión mecánicamente fuerte a la superficie del implante. Por otro lado, las reacciones sobre la superficie del vidrio bioactivo induce la liberación de concentraciones criticas de iones solubles, por ejemplo, Si, Ca y P, los cuales han mostrado favorecer respuestas intacelulares y extracelulares que promueven una respuesta rápida de formación de hueso (7), genéticamente controlada, por la sobreregulación de genes que participan en la proliferación de osteblastos (8-10). Si bien los vidrios bioactivos, particularmente el 45S5, han sido ampliamente investigados para la regeneración y reparación de hueso, hay relativamente pocos estudios respecto a la aplicación de los vidrios bioactivos para reparar o regenerar tejidos blandos. Sin embargo, recientes trabajos han mostrado la habilidad de los vidrios bioactivos de promover angiogénesis in vitro (11-13), lo cual es un obstáculo cuando se precisa establecer un sistema vascular maduro en un tejido en regeneración. Recientes intentos por estimular angiogénesis se han enfocado en la entrega de factores de crecimientos tales como el factor de crecimiento endotelial (VEGF) y el factor de crecimiento fibroblástico básico (bFGF), terapia génica y terapia basada en células (13), pero estos procedimientos son caros y los mecanismos de entrega óptimos son aun poco comprendidos. Por lo tanto la habilidad de un vidrio bioactivo para inducir angiogénesis podría proveer una buena alternativa al uso de factores de crecimiento caros, para estimular la neovascularización de un tejido en reparación (4).
Vidrios de boro-silicatos bioactivos
Nuevos vidrios bioactivos basados en el 45S5 Bioglass®, han sido desarrollados, reemplazando completamente el SiO2 en el 45S5 por B2O3 (generando un vidrio de boro bioactivo), reemplazando parcialmente el SiO2 por B2O3 en el vidrio 45S5 o simplemente agregando a la formula 45S5 ciertas concentraciones de B2O3 (produciendo vidrios de borosilicato bioactivos) (14)(15). Estos vidrios bioactivos debido a su baja durabilidad química se degradan más rápido y se convierten más completamente en un material similar a la HCA en un medio fisiológico cuando son comparados con el 45S5. Por lo tanto, la fácil fabricación, la posibilidad de controlar la tasa de degradación de estos vidrios variando la concertación de B y por otro lado, ya que ha sido bien establecido que el boro desempeñaría funciones en la angiogénesis y la reparación tisular (16-18), estas características lo hacen especialmente útil para aplicaciones en ingeniería de tejidos (4). Si bien se puede establecer que la bioactividad de los vidrios 45S5 Bioglass® dopados con Boro ha sido bien documentada, los datos existentes con especto a los efectos biológicos son escasos y controversiales por lo que son necesarios más estudios tanto, in vitro como in vivo para poder clarificar esta cuestión.
Productos de Disolución Iónica IDPs
Por mucho tiempo se asumió que la formación de una capa de HCA superficial era el requerimiento crítico para la bioactividad de un material. Sin embargo, hoy se sabe que la formación de HCA es útil, pero no es un fenómeno crítico para determinar la bioactividad (19). Nueva evidencia científica indica que los productos de disolución de los vidrios bioactivos son la clave para comprender el comportamiento bioactivo de un vidrio tanto in vitro como in vivo (20). La liberación de iones a partir de un vidrio bioactivo, se da como resultado de una secuencia de reacciones químicas que se llevan a cabo en la superficie del material bioactivo, que en ultima instancia llevan a la precipitación de una capa de HCA policristalina (5). Resumidamente, cuando el vidrio bioactivo toma contacto con un fluido fisiológico del cuerpo o simulado se produce una rápida reacción de intercambio iónico de Na+ y Ca2+ desde el material con H+ (o H3O+) desde la solución llevando a la formación de grupos silanoles (Si-OH) sobre la superficie del vidrio. Esta etapa eleva el pH de la solución lo que genera el ataque de SiO2 liberándose el Si en forma de acido salicílico Si(OH)4. La continua liberación Si(OH)4 y formación de Si-OH, lleva a la condensación y polimerización de una capa rica en SiO2 en el material carente de Na+ y Ca2+. La disolución del material continúa, y ahora acoplado al intercambio iónico de Ca2+ y (PO4)3- entre el vidrio y la solución se forma una capa de fosfato de calcio amorfa (ACP) sobre la capa rica en SiO2. Esta capa altamente reactiva, una vez formada, incorpora (OH)- y (CO3)- desde la solución cristalizando como una capa de HCA policristalina. Como implante y en contacto con fluidos fisiológicos del cuerpo y luego de formada la capa de HCA, sobre el vidrio se genera una superficie de reacción que incrementa la adsorción y desorción de factores de crecimientos y el periodo de tiempo de permanencia de macrófagos en la zona tratada que son requeridos para preparar el sitio de implante para la reparación tisular, el proceso de unión del vidrio con el tejido y la posterior diferenciación y proliferación de las células involucradas en la regeneración del tejido. La mineralización de la matriz que le sigue a la maduración de osteocitos luego que se encapsulan en una matriz de HCA-colágeno es el producto final observado in vivo cuando el tejido en cuestión es el tejido óseo (4)(19).
Mecanismos de acción de los productos de disolución iónica
Como se expuso anteriormente, el fenómeno clave de bioactividad de los vidrios bioactivos y en particular el Bioglass®, era la tasa controlada de liberación de iones, especialmente concentraciones criticas de Si, Ca, P y Na (19). La subsecuente liberación de estos iones luego de la exposición de los vidrios bioactivos a un ambiente fisiológico incrementaría la bioactividad de estos materiales y serian los responsables de la respuesta biológica observada hasta ahora. Con respecto a la osteogénesis ya ha sido bien establecido, con estudios in vitro e in vivo, el potencial osteogénico del Bioglass® (5)(19). Si bien aún no está muy claro el mecanismo de acción a nivel molecular de los IDPs se cree que estos actuarían regulando la expresión génica de ciertas moléculas relevantes, que intervienen en los procesos de control del ciclo celular de osteoblastos y en la proliferación y diferenciación, promoviendo además, la producción de componentes de la matriz ósea (8)(9) posiblemente a través de señales celulares que involucrarían las vías de señalización de las MAP Kinasas (10). La bibliografía actual sobre el efecto de los vidrios sobre el proceso angiogénico es escasa y la mayoría de los estudios fueron realizados en modelos in vitro de cultivo de células relevantes en contacto directo con el material. Hoppe (20) postula, basado en la bibliografía, que los IDPs actuarían estimulando la secreción de factores de crecimiento angiogénicos desde los fibroblastos como el VEGF y bFGF lo que llevaría a un incremento en la proliferación, diferenciación y migración de células endoteliales generando una red de túbulos de células endoteliales conectadas. Hasta ahora se ha postulado, basado en la bibliografía existente, que los vidrios bioactivos estimularían la proliferación de células endoteliales, pero estos trabajos son escasos y fueron basados en la respuesta observada de células endoteliales humanas en contacto directo con el material (7). Por lo tanto, son necesarios más trabajos futuros que analicen la respuesta angiogénica, tanto in vitro como in vivo, a los productos de disolución iónica de los vidrios bioactivos.
Referencias bibliográficas
1. Williams DF. On the mechanisms of biocompatibility. Biomaterials 2008; 29:2941-53.
2. Hench LL, Polak JM. Third-generation biomedical materials. Science 2002; 295(5557): 1014-7.
3. Rezwan K, Chen QZ, Blaker JJ, Boccaccini AR. Biodegradable and bioactive porous polymer/inorganic composite scaffolds for bone tissue engineering. Biomaterials 2006; 27(18): 3413-31.
4. Rahaman MN, Day DE, Sonny Bal B, Fu Q, Jung SB, Bonewald LF, et al. Bioactive glass in tissue engineering. Acta Biomater 2011; 6: 2355-73.
5. Hench LL. Bioceramics: From concept to clinic. J Am Ceram Soc 1991; 74(7): 1487-510.
6. Kokubo T, Kushitani H, Sakka S, Kitsugi T, Yamamuro T. Solutions able to reproduce in vivo surface-structure changes in bioactive glass-ceramic. J Biomed Mater Res 1990; 24: 721-34.
7. Gorustovich AA, Roether JA, Boccaccini AR. Effect of bioactive glasses on angiogenesis: A review of in vitro and in vivo evidence. Tissue Eng 2010; 16(2): 199-207.
8. Xynos ID, Edgar AJ, Buttery LDK, Hench LL, Polak JM. Ionic products of bioactive glass dissolution increase proliferation of human osteoblast and induce insulin-like growth factor II mRNA expression and protein synthesis. Biochem Biophys Res Commun 2000; 276(2): 461-5.
9. Xynos ID, Edgar AJ, Buttery LDK, Hench LL, Polak JM. Gene expression profiling of human osteoblast following treatment with the ionic products of Bioglass® 45S5 dissolution. J Biomed Mater Res 2001; 55(2): 151-7.
10. Au AY, Au RY, Demko JL, McLaughlin RM, Eves BE, Frondoza CG. Consil® bioactive glass particles enhance osteoblast proliferation and selectively module cell signaling pathways in vitro. J Biomed Mater Res 2010; 86(3): 678-84.
11. Day RM. Bioactive glass stimulates the secretion of angiogenic growth factors and angiogenesis in vitro. Tissue Eng 2005; 11(5/6):768-77.
12. Leach JK, Kaigler D, Wang Z, Krebsbach PH, Mooney DJ. Coating of VEGF-releasing scaffolds with bioactive glass for angiogenesis and bone regeneration. Biomaterials 2006; 27(17): 3249-55.
13. Leu A, Leach JK. Proangiogenic potential of collagen bioactive glass substrate. Pharm Res 2008; 25(5): 1222-9.
14. Yao A, Wang DP, Huang W, Rahaman MN, Day DE. In vitro bioactive characteristics of borate-based glasses with controllable degradation behavior. J Am Ceram Soc 2007; 90: 303-6.
15. Huang W, Day DE, Kittiratanapiboon K, Rahaman MN. Kinetics and mechanisms of conversion of silicate (45S5), borate, and borosilicate glass to hydroxyapatite in dilute phosphate solution. J Mater Sci Med 2006; 17: 583-96.
16. Benderdour M, Bui-Van T, Dicko A, Belleville F. In vivo and in vitro effects of boron and boranated compounds. J Trace Elem Med Biol 1998; 12(1): 2-7.
17. Mayap Nzietchueng R, Dousset B, Franck P, Benderdour M, Nabet P, Hess K. Mechanisms implicated in the effects of boron on wound healing. Trace Elem Med Biol 2002; 16: 239-44.
18. Gorustovich AA, Steimetz T, Nielsen FH, Guglielmotti MB. Histomorphometric study of alveolar bone healing in rats fed a boron-deficient diet. Anat Rec 2008; 291(4): 441-7.
19. Hench LL. The story of Bioglass®. J Mater Sci: Mater Med 2006; 17: 967-78.
20. Hoppe A, Guldal NS, Boccaccini AR. A review of biological response to ionic dissolution products from bioactive glasses and glass-ceramics. Biomaterials 2011; 32: 2757-74.
LABORATORIO DE PATOLOGÍA Y FARMACOLOGÍA MOLECULAR
El sistema eph/ephrin, un ejemplo de versatilidad y diversidad funcional en biología molecular del cáncer y la angiogénesis
The eph/ephrin system, an example of versatility and functional diversity in molecular biology of cancer and angiogenesis
O sistema eph/ephrin, um exemplo de versatilidade e diversidade funcional em biologia molecular do câncer e a angiogênese
Martín C. Gómez, Gabriela B. Bravo, Carla Gatto Cáceres, Adrián Góngora, Alberto Baldi
Resumen
Los receptores Eph y Ephrin son moléculas altamente versátiles, reguladoras de procesos tan diversos como la guía de axones, la modulación de plasticidad sináptica, la morfogénesis del sistema vascular y el tamaño y organización de órganos. Los receptores Eph comprenden la familia más numerosa de receptores de tirosina quinasa y sus ligandos Ephrin están anclados o atraviesan la membrana plasmática. El sistema Eph/Ephrin se caracteriza por desencadenar vías de señalización bi-direccional, tanto a través del receptor como a través del ligando. Mediante contacto célula-célula, y dependiendo del repertorio de receptores expresados, del tipo y el contexto celular, pueden controlar respuestas celulares muy diversas como la adhesión, morfología, proliferación y migración. Estos roles no están confinados a procesos fisiológicos, sino su importancia resalta aún más en una variedad de patologías humanas y, en particular, en cáncer. El receptor EphB4 está sobre-expresado en varios tipos tumorales y, con respecto a su funcionamiento, diversos artículos publicados muestran discrepancias, ya que su activación puede desencadenar señales pro- o anti-tumorales según la naturaleza del contexto celular. La expresión de su ligando EphrinB2, tanto en las células tumorales como en el endotelio asociado, está relacionado a su alta vascularización. Entender los mecanismos que controlan la función del sistema Eph/Ephrin proporcionaría conocimientos profundos para comprender los principios biológicos y permitir el desarrollo de nuevas drogas terapéuticas. Por ejemplo, mientras que anticuerpos contra VEGF ya son utilizados para el tratamiento del cáncer, la interferencia simultánea del sistema EphB4/EphrinB2 sería útil para actuar durante la angiogénesis tumoral y la progresión del cáncer.
Palabras clave: Eph/Ephrin; angiogénesis.
Summary
Eph receptors and Ephrins are highly versatile regulators of processes as diverse as axon guidance, modulation of synap-tic plasticity, morphogenesis of the vascular system or the patterning of organs. The Eph receptors are the largest family of receptor tyrosine kinases and their Ephrin ligands are bound to the plasmatic membrane or are transmembrane. The Eph/Ephrin system is characterized by activating bi-directional signals, throughout both the receptor and the ligand. By cell-cell contact, and depending on the expressed receptors set, cell type and context, it can trigger a wide array of cellular responses like cell adhesion, morphology, proliferation and migration. These roles are not confined to physiological processes, but are highly relevant for a variety of human pathologies and, in particular, cancer. EphrB4 receptor is overexpressed in various tumor types and with respect to its function, several published articles have shown discrepancies, since its activation can trigger pro- or anti-tumoral signals. The expression of its EphrinB2 ligand in both tumor cells and in the associated endothelium is related to its high vascularity. Thus, understanding the key mechanisms controlling Eph/Ephrin function would not only provide deeper insight into interesting biological principles, but it might also enable the development of new therapeutic reagents. For example, while antibodies against VEGF are already used for the treatment of cancer, inhibition of ephrin-B2 might be useful to simultaneously interfere with the function of VEGFR2 and VEGFR3, which act together during angiogenesis.
Key words: Eph/Ephrin; angiogenesis.
Resumo
Os receptores Eph e Ephrin são moléculas altamente versá-teis, reguladoras de processos tão diversos como guia de axô-nios, modulação de plasticidade sináptica, morfogênese do sistema vascular e o tamanho e organização de órgãos. Os receptores Eph compreendem a família mais numerosa de receptores de tirosina quinase e seus ligandos Ephrin estão ancorados ou atravessam a membrana plasmática. O sistema Eph/Ephrin se caracteriza por desencadear vias de sinaliza-ção bidirecional, tanto através do receptor quanto através do ligando. Mediante contato célula-célula, e dependendo do re-pertório de receptores expressos, do tipo e o contexto celular, podem controlar respostas celulares muito diversas como a adesão, morfologia, proliferação e migração. Estes papéis não estão confinados a processos fisiológicos, mas sua im-portância salienta mais ainda numa variedade de patologias humanas e, em particular, em câncer. O receptor EphB4 está sobre-expresso em vários tipos tumorais e, com relação a seu funcionamento, diversos artigos publicados mostram diver-gências, visto que sua ativação pode desencadear sinais pró ou anti-tumorais conforme a natureza do contexto celular. A expressão de seu ligando EphrinB2, tanto nas células tu-morais quanto no endotélio associado, está relacionada com sua alta vascularização. Entender os mecanismos que con-trolam a função do sistema Eph/Ephrin proporcionaria co-nhecimentos profundos para compreender os princípios biológicos e permitir também o desenvolvimento de novas drogas terapêuticas. Por exemplo, enquanto anticorpos contra VEGF já são utilizados para o tratamento do câncer, a interferência simultânea do sistema EphB4/EphrinB2 seria útil para atuar durante a angiogênese tumoral e a progressão do câncer.
Palavras chave: Eph/Ephrin; angiogênese.
Familias de Eph y Ephrin
Los receptores denominados Eph (erytropoietin-pro-ducing hepatocellular carcinoma) comprenden la familia más numerosa de receptores de tirosina quinasa del reino animal y están presentes en la mayoría de los tipos celulares. Los receptores Eph han sido subdivididos en dos clases, EphA y EphB, basándose en la homología de sus secuencias y en las propiedades de sus ligandos Eph-rins (Eph receptor interacting protein). Estos ligandos se dividen en EphrinA, los cuales se encuentran anclados a la membrana plasmática por glucosil-fosfatidil-inositol (GPI), y EphrinB, caracterizados por ser proteínas transmembrana. A diferencia de los clásicos receptores de factores de crecimiento, la unión del receptor/ligando Eph/Ephrin desencadena transducciones de señales bi-direccionales, tanto en las células que presentan el receptor (proceso denominado "señalización forward") como también en las células que presentan el ligando ("señalización reverse")(1). La interacción del receptor Eph con su ligando Ephrin conduce a la regulación de la morfología, adhesión y migración a través de la modificación de la organización del citoesqueleto e influenciando las actividades de moléculas de adhesión intercelular. Recientes trabajos han mostrado que además participan en el control de la proliferación y la sobrevida, como también en otras funciones celulares específicas tales como plasticidad neuronal, secreción de insulina, remodelación del hueso y regulación inmunológica (2).
En humanos, nueve receptores EphA (EphA1-EphA9) se unen en forma promiscua a cinco EphrinA (EphrinA1-EphrinA5), y cinco receptores de la subclase EphB (EphB1-B4 y EphB6) se unen a tres ligandos Eph-rinB (EphrinB1-EphrinB3), con la única excepción que EphB4 sólo es activado por EphrinB2. La parte extrace-lular de los receptores Eph incluye un dominio de unión a Ephrin N-terminal que es necesario y suficiente para el reconocimiento y la unión al ligando, una región rica en cisteína y dos repeticiones similares a fibronectina tipo III las cuales podrían estar involucradas en las interacciones de dimerización receptor-receptor (3). Separado por un dominio transmembrana, el dominio ci-toplasmático incluye un segmento yuxtamembrana, un dominio tirosina quinasa y un dominio SAM. Los ligan-dos de Ephrin están caracterizados por la presencia de un único dominio de unión al receptor en el extremo N-terminal separado de la membrana por un segmento de 40 aminoácidos. Las moléculas de la subclase EphrinA, ancladas a la célula por GPI, se encuentran agrupadas en dominios de membrana tipo lipid rafts, las cuales estarían asociadas con proteínas citoplasmáticas. Los ligandos de EphrinB atraviesan la membrana y poseen un dominio citoplasmático que incluye un motivo PDZ C-terminal, capaz de activar la vía de la familia de quinasa Src (2).
Recientes estudios estructurales y biofísicos sugieren que el mecanismo para la iniciación de la señalización bidireccional involucra inicialmente un contacto célula-célula y posteriormente la unión de ligandos y receptores en una relación estequiométrica de 1:1. Estos complejos de heterodímeros Eph-Ephrin crean superficies de interacción que juntan pares de dímeros en estructuras tetraméricas desencadenando la señalización "forward" y "reverse". Aunque la formación de estos complejos de tetrámeros Eph-Ephrin es suficiente para la fosforilación del receptor, la agregación de varios de estos tetrámeros y el tamaño de estos agregados serían absolutamente esenciales para determinar la intensidad de la señal y su naturaleza fisiológica. Sin embargo, se ha descrito que existen otros mecanismos que definen la señalización del sistema Eph/Ephrin, como la activación en cis entre moléculas receptor y ligando de una misma célula, la interacción con otros receptores (por ejemplo: Erb2, E-cadherina) (4) y la trans-endocitosis, haciendo que el estudio de este sistema sea un tanto complejo.
Si bien los receptores Eph y sus ligandos Ephrin están presentes en la mayoría de los tipos celulares, sus actividades se encuentran mejor caracterizadas en el sistema nervioso central y en el desarrollo embrionario del sistema circulatorio. En el sistema nervioso central regulan varios procesos tales como guía de direcciona-miento de axones, la migración de células de la cresta neural y la sinaptogénesis. La activación de receptores Eph en las células de la cresta neural o en los conos de crecimiento axonal dispara la retracción ante los tejidos que expresan las moléculas de ligando Ephrin complementarias a los mismos (5).
El corte enzimático de las moléculas de Ephrin por la metaloproteasa ADAM10 unida a membrana presenta otra posible explicación molecular para cambiar entre adhesión y repulsión. Se ha mostrado que la unión de EphA3 con EphrinA5 expone un motivo de reconocimiento de metaloproteasas y dispara el corte de EphrinA5 por ADAM10. Esta liberación de Ephrin de la superficie del axón conduce a la retracción de las células que expresan EphA5, mientras que el bloqueo de la escisión conduce a una interacción adhesiva extensa (6).
Otro mecanismo que media la conversión de interacciones adhesivas en señales repulsivas consiste en retirar el complejo Eph-Ephrin de la superficie celular por endocitosis. Durante este proceso denominado trans endocitosis, el complejo receptor-ligando intacto, y posiblemente las proteínas citoplasmáticas asociadas, junto con la membrana circundante son endocitados por la célula que expresa Eph o Ephrin. Estructuras intrace-lulares revestidas por doble membrana fueron observadas por microscopía electrónica en hipocampo de rata (7). La trans endocitosis cesa la adhesión y permite la retracción celular. Este proceso de despegado de células que requiere tanto de la activación de Eph (vía forward) como de la internalización del complejo de señalización, depende de la polimerización de moléculas de actina y de la actividad de la GTPasa pequeña Rac1. Recientes descubrimientos han evidenciado que la interacción Eph-Ephrin no está confinada a la zona de contacto entre dos células adyacentes, sino que además se han reportado interacciones en cis entre receptores y ligandos expresados en la misma célula. Mientras las interacciones convencionales en trans entre células distintas involucran el dominio de Ephrin y el correspondiente dominio de unión a ligando del receptor, Eph-rinA5 puede unirse en cis al dominio extracelular de fibronectina tipo III del receptor EphA3 en la misma célula, bloqueando la activación del mismo y contrarrestando la señalización forward desencadenada por el contacto célula-célula. Este modelo de inhibición en cis podría explicar cómo se generan gradientes de receptores activos parcialmente solapados durante el desarrollo del sistema visual (8).
Eph y ephrin en el sistema cardiovascular
El posicionamiento espacial y temporal apropiado de células endoteliales durante el nacimiento de los vasos es un requerimiento necesario para la formación de anastomosis y redes diferenciadas de vasos sanguíneos que eventualmente permitirían la dirección del flujo sanguíneo. Diversas moléculas Eph-Ephrin son expresadas en el sistema cardiovascular, sin embargo EphB4 y su ligando EphrinB2 han atraído mayor interés. Eph-rinB2 es expresada principalmente en el endotelio arterial, mientras que EphB4 es específica del endotelio venoso. Por esto, se ha propuesto a estas dos moléculas como marcadores candidatos para la diferenciación ar-terio-venosa (9). La relevancia del funcionamiento de EphB4 y EphrinB2 durante la vasculogénesis es indis-cutida, dado que ratones transgénicos knockout para EphB4 o EphrinB2 mueren en estadíos embrionarios tempranos por una desorganización de vasos sanguíneos. Recientemente se demostró que el calibre de arterias y venas y la localización de células endoteliales cuyo destino es la aorta o las venas cardinales está finamente regulado por un balance entre Notch y el sistema EphB4/EphrinB2 (10).
Durante etapas tardías del desarrollo embrionario y en el adulto, la formación regenerativa o patológica de nuevos vasos se caracteriza por el remodelamiento y la generación de nuevos capilares por brotación de la vas-culatura existente, proceso denominado angiogénesis. La expresión de EphrinB2 está aumentada durante el remodelamiento activo de vasos, sin embargo su rol durante la angiogénesis no es tan claro. La activación de EphB4 en células endoteliales en cultivo y en la córnea de ratón induce la proliferación, la migración, la formación de túbulos y la angiogénesis (9) lo que indicaría que la vía forward puede promover la brotación de nuevos vasos. En modelos de isquemia cardíaca se observó que EphrinB2 señalizando a través de EphB4 es capaz de estimular la mitosis de cardiomiocitos, aumentar la densidad de capilares y el desarrollo de vasos colaterales funcionales (11), sugiriendo a EphrinB2 como un candidato potencial para la terapia angiogé-nica en enfermedades de isquemia de corazón.
Eph y Ephrin en cáncer
EphA1 fue el primer miembro de la familia de receptores Eph en ser clonado a partir de una línea celular de carcinoma hepatocelular humano productor de eritropoyetina. EphA1 se encuentra sobre-expresado en esta línea celular en niveles relativamente elevados, lo que sugirió a esta nueva familia de tirosina quinasa un rol en la tumorigénesis (12). Desde entonces, cada miembro de la familia Eph ha sido identificado por sus características de expresión o desregulación en diferentes tipos de tumores humanos (13). Entre los receptores EphA, EphA2 ha sido el más intensamente estudiado en oncología y sus altos niveles de expresión están correlacionados con el estadío y la progresión del tumor. Además, la sobre-expresión de EphA2 en células epiteliales no transformadas de mama induce transformación maligna y confiere potencial tumorigénico (14).
Las funciones durante la tumorigénesis de los receptores y ligandos de la clase B parecen más complejas. La sobre-expresión de EphrinB2 en células de cáncer parece estar correlacionada con un aumento de invasión y una alta vascularización de tumores humanos conduciendo a un pobre pronóstico. El receptor EphB4 se encuentra sobre-expresado en diversos tumores humanos y con respecto a su funcionamiento, diversos artículos publicados muestran discrepancias, ya que su activación puede desencadenar tanto señales pro-oncogénicas como también señales anti-tumorales, según la naturaleza del contexto celular. EphB4 incrementa el crecimiento tumoral, la motilidad de células cancerosas y la metástasis en la próstata, mesotelio y útero. Por otra parte, también parece actuar como supresor de tumores en cáncer de mama y colon. Diversas estrategias han sido exploradas para evidenciar el funcionamiento de EphB4. Mediante la inhibición de la señalización por EphB4 utilizando receptores EphB4 truncados solubles, sobre-expresando un dominante negativo del receptor, o bien mediante técnicas de interferencia de ARN se observó una disminución de la proliferación, migración y del crecimiento tumoral en modelos de melanoma y de próstata (15)(16). Hemos observado en nuestro modelo de células de melanoma humano que el estímulo con moléculas solubles de EphrinB2 activa el receptor EphB4 e induce la proliferación y migración (datos aun no publicados). En células de cáncer de mama, sorpresivamente se observó que a pesar de los niveles de expresión de EphB4, la fosforilación en tirosinas es mucho más baja comparada con células epiteliales MCF-10A no transformadas (17), y la activación del receptor EphB4 y señalización mediante la vía Abl-Crk inhibe la capacidad tumoral de células de cáncer de mama.
El efecto promotor de tumores durante el crecimiento de un tumor de mama podría no depender exclusivamente de la señalización forward de EphB4. Se observó que la expresión de un receptor EphB4 con su dominio citoplasmático defectivo resultó en un incremento del crecimiento del tumor y un fuerte desarrollo de la angiogénesis tumoral (18). Este descubrimiento resalta a la señalización reverse mediante la molécula de EphrinB2 e implica la participación de interacciones EphB4/EphrinB2 entre células tumorales y células del estroma. Además, la señalización por EphrinB2 también promueve la interacción entre células endoteliales, pe-ricitos y células de la musculatura lisa vascular (19), sugiriendo que la regulación por EphrinB2 podría estabilizar los vasos de los tumores recurrentes después de una terapia anti-angiogénica utilizando anticuerpos contra el factor de crecimiento endotelio vascular (VEGF). Siguiendo este razonamiento, inhibir el sistema de Eph podría ser particularmente útil para terapias anti-angiogénicas, y posiblemente lograría superar la resistencia a las terapias anti VEGF.
Hasta la actualidad, se han identificado moléculas pequeñas que inhiben la actividad del dominio quinasa de Eph y dos de ellas, dasatinib y XL647, han sido evaluadas en ensayos clínicos. Dasatinib es un potente inhibidor de EphA2, estudiado hasta fase II en leucemia mie-loide crónica y en tumores sólidos, mientras que XL647, probado en cáncer de pulmón, es un inhibidor de EphB4 y de los receptores del factor de crecimiento epidérmico (EGF) y VEGF (http://clinicaltrials.gov). Otra estrategia de terapia anti-angiogénica para el cáncer ha consistido en inhibir las interacciones Eph/Ephrin y la señalización bidireccional. Para esto se han desarrollado moléculas pequeñas, péptidos, receptores solubles y anticuerpos monoclonales antagonistas (20) que han sido capaces de disminuir con el crecimiento tumoral y la angiogénesis asociada en diferentes modelos in vitro y en ratón. De manera interesante, existen también anticuerpos agonistas y ligandos que han sido utilizados exitosamente para reducir la progresión tumoral, a pesar de ser activadores de la señalización de Eph/Ephrin (17). La respuesta ante una terapia particular contra el sistema Eph/Ephrin dependerá del tipo de tumor, del estadío de avance y del microambiente tumoral. Seleccionar la estrategia óptima enfocada en interferir con las funciones de Eph como terapia contra el cáncer requiere un mejor entendimiento de los mecanismos de señalización en los diferentes compartimientos celulares del tumor.
Referencias bibliográficas
1. Wang HU., Chen Z.F., Anderson D.J. Molecular Wang HU, et al. Molecular distinction and angiogenic interaction between embryonic arteries and veins revealed by ephrinB2 and its receptor EphB4. Cell 1998; 93: 741-53.
2. Pasquale EB. Eph receptors and ephrins in cancer: bidirectional signaling and beyond. Nat Rev Cancer 2010; 10(3): 165-80.
3. Himanen JP, Nikolov DB. Eph signaling: a structural view. Trends Neurosci 2003; 26(1): 46-51.
4. Pasquale EB. Eph-ephrin bidirectional signaling in physiology and disease. Cell 2008; 133: 38-52.
5. Poliakov A, Cotrina M, Wilkinson DG. Diverse roles of eph receptors and ephrins in the regulation of cell migration and tissue assembly. Dev Cell 2004; 7: 465-80.
6. Hattori M, Osterfield M, Flanagan JG. Regulated cleavage of a contact-mediated axon repellent. Science 2000; 289: 1360-5.
7. Spacek J, Harris KM. Trans-endocytosis via spinules in adult rat hippocampus. J Neurosci 2004; 24: 4233-41.
8. Flanagan JG. Neural map specification by gradients. Curr Opin Neurobiol 2006; 16: 59-66.
9. Adams RH, Wilkinson GA, Weiss C, et al. Roles of ephrinB ligands and EphB receptors in cardiovascular development: Demarcation of arterial/venous domains, vascular morphogenesis, and sprouting angiogenesis. Genes Dev 1999; 13: 295-306.
10. Kim, Y. H., Hu H., et al. Artery and vein size is balanced by Notch and ephrin B2/EphB4 during angiogenesis. Development 2008; 135(22): 3755-64.
11. Katsu M. et al. Ex vivo gene delivery of ephrin-B2 induces development of functional vessels in a rabbit model of hind limb ischemia. Vasc Surg 2009; 49: 192.
12. Hirai H, Maru Y, Hagiwara K, Nishida J, Takaku F. A novel putative tyrosine kinase receptor encoded by the eph gene. Science 1987; 238: 1717-20.
13. Surawska, H., P. C. Ma, et al. (2004). The role of ephrins and Eph receptors in cancer. Cytokine Growth Factor Rev 15(6): 419-33.
14. Zelinski DP, Zantek ND, Stewart JC, Irizarry AR, Kinch MS. EphA2 overexpression causes tumorigenesis of mammary epithelial cells. Cancer Res 2001; 61:2301-2306.
15. Martiny-Baron, G., T. Korff, et al. Inhibition of tumor growth and angiogenesis by soluble EphB4. Neoplasia 2004; 6(3): 248-57.
16. Kertesz, N., V. Krasnoperov, et al. The soluble extracellular domain of EphB4 (sEphB4) antagonizes EphB4-EphrinB2 interaction, modulates angiogenesis, and inhibits tumor growth. Blood 2006; 107(6): 2330-8.
17. Noren, N. K., G. Foos, et al. The EphB4 receptor suppresses breast cancer cell tumorigenicity through an Abl-Crk pathway. Nat Cell Biol 2006; 8(8): 815-25.
18. Noren, N. K., M. Lu, et al. "Interplay between EphB4 on tumor cells and vascular ephrin-B2 regulates tumor growth." Proc Natl Acad Sci USA 2004; 101(15): 5583-8.
19. Salvucci O, et al. EphrinB reverse signaling contributes to endothelial and mural cell assembly into vascular structures. Blood 2009; 114: 1707-16.
20. Krasnoperov V, Kumar SR, Ley EJ, Scehnet JS, Liu R, Zozulya S, et al. Novel EphB4 Monoclonal antibodies modulate angiogenesis and inhibit tumor growth. Am J Pathol 2010; 76(4): 2029-38.
LABORATORIO DE INMUNOHEMATOLOGÍA
Importancia de las Células Madre Mesenquimales en el desarrollo del cáncer de mama
Importance of mesenchymal stem cells in breast cancer development
Importância das Células Tronco Mesenquimais no desenvolvimento do câncer de mama
Valeria Fernández Vallone, Vivian Labovsky, Leandro Martinez, Norma Chasseing
Resumen
La mayoría de las pacientes con cáncer de mama (PCM) avanzado desarrollan metástasis óseas, de tipo osteolíticas, como resultado de un desbalance entre los procesos de os-teogénesis, osteoclastogénesis y resorción ósea. Nosotros encontramos en la médula ósea (MO) de las PCM avanzado (carcinoma mamario ductal infiltrante, estadío clínico III y IV, sin metástasis en MO y hueso) una disminución de la eficiencia de clonado de las células madre mesenquimales (MSC), medida como el número de unidades formadoras de colonias fibroblásticas (CFU-F), así como una disminución en su capacidad de diferenciación osteogénica en comparación con las voluntarias sanas (VS). Además, observamos osteoclastogénesis espontánea en MO y sangre periférica de las PCM, mientras que no lo hicimos en las VS. Por último, consideramos importante la evaluación de la diferenciación osteogénica de las MSC de MO y del potencial osteoclasto-génico de los progenitores hematopoyéticos de MO y de los monocitos de sangre periférica, como posibles factores pronósticos de futuros desórdenes óseos que pueden favorecer la invasión de las células del CM en el hueso.
Palabras clave: células madre mesenquimales; cáncer de mama; médula ósea; hueso; osteogénesis; osteoclasto-génesis.
Summary
Most advanced breast cancer patients (BCP) develop oste-olytic bone metastasis as a result of the imbalance between osteogenesis, osteoclastogenesis and bone resorption processes.In bone marrow (BM) aspirates of untreated BCP (infiltrative ductal breast carcinoma, clinical stage III and IV, without bone and BM metastasis), a decrease in cloning efficiency of BM-mesenchymal stem cells (MSC), measured as number of colony forming unit-fibroblasts (CFU-F), and a decrease in its osteogenic differentiation capacity compared to healthy volunteers (HV) were found . Moreover, spontaneous osteoclastogenesis (SpOC) in BM and peripheral blood of BCP were observed, while SpOC was not observed in BM of HV. Finally, evaluation of the osteogenic differentiation of BM-MSC and osteoclastogenic potential of BM-hematopoi-etic progenitors as well as peripheral blood-monocytes are considered important as possible prognostic factors for future bone disorders that may favor the invasion of BC cells into bone.
Key words: mesenchymal stem cell; breast cancer; bone marrow; bone; osteogenesis; osteoclastogenesis.
Resumo
A maior parte das pacientes com câncer de mama (PCM) avançado desenvolve metástases ósseas, de tipo osteolíticas, como resultado de um desequilíbrio entre os processos de os-teogênese, osteoclastogênese e ressorção óssea. Nós encontramos na medula óssea (MO) das PCM avançado (carcinoma mamário ductal infiltrante, estágío clínico III e IV, sem metástase em MO e osso) uma diminuição da eficiên-cia de clonagem das células tronco mesenquimais (MSC), medida como o número de unidades formadoras de colônias fibroblásticas (CFU-F), bem como uma diminuição em sua capacidade de diferenciação osteogênica em comparação com as voluntárias saudáveis (VS). Além disso, observamos osteoclastogênese espontânea em MO e sangue periférica das PCM, enquanto que não o fizemos nas VS. Por último, consideramos importante a avaliação da diferenciação os-teogênica das MSC de MO e do potencial osteoclastogênico dos progenitores hematopoiéticos de MO e dos monócitos de sangue periférico, como possíveis fatores prognósticos de futuras desordens ósseas que possam favorecer a invasão das células do CM no osso.
Palavras chave: células tronco mesenquimais, câncer de mama, medula óssea, osso, osteogênese, osteoclastogênese.
El cáncer de mama, a pesar de ser tema de gran número de investigaciones, continúa siendo el tipo de cáncer más común entre las mujeres y la segunda causa de muerte particularmente en EE.UU. (1). Cada año, más de 44.000 mujeres mueren de cáncer de mama. La estadística indica que la mortalidad en el año 2000 fue de 24,2 y 26,7 en EE.UU. y Argentina, respectivamente (1). En ambos casos, se trata de cifras de mortalidad específica expresadas como número de muertes por año, por 100.000 habitantes. Y a pesar de los esfuerzos realizados para detectar el cáncer mama en estadíos tempranos, esto no garantiza la mejor sobrevida del paciente. Observación que indica la necesidad de contar con métodos más sensibles para detectar las células epiteliales tumorales mamarias (CEpTM) y/o las células madre tumorales (TSC) presentes en la mama, así como también la necesidad de continuar profundizando sobre la biología del cáncer de mama en sus estadíos iniciales y estudiando los mecanismos que llevan al desarrollo de las metástasis.
Por otra parte, el cáncer fue considerado durante mucho tiempo como un desorden constituido por células transformadas que adquirieron un alto grado de proliferación y autorrenovación, así como mayor capacidad de sobrevida e invasión a través de la activación de oncogenes e inactivación de genes supresores del tumor (2). Sin embargo, en los últimos años se demostró que la formación de un tumor clínicamente relevante depende de la composición y función del microambiente tumoral (MT) formado por células estromales y accesorias, matriz extracelular y factores solubles (2). Dentro de este MT se han encontrado fibroblastos, pericitos, leucocitos (linfocitos T y B, células naturalmente citotóxi-cas, neutrófilos, eosinófilos, monocitos-macrófagos, ba-sófilos y mastocitos), miofibroblastos, células dendríticas, células derivadas de médula ósea (MO) entre las cuales se encuentran las células madre mesenquimales (MSC) y los progenitores mesenquimales, células endoteliales vasculares linfáticas y de sangre (2). Numerosos estudios experimentales muestran una interacción activa y recíproca entre las CEpTM y las células estromales/ accesorias y demás componentes del MT, eventos críticos que determinan y promueven el crecimiento del tumor primitivo y su progresión hacia una futura metástasis (2). Por lo tanto, el análisis del MT, en particular la presencia y función de las MSC de MO, así como de los progenitores endoteliales y células endoteliales, fibroblastos asociados al tumor y macrófagos asociados al tumor de tipo M2, son actualmente tema de múltiples estudios destinados a comprender más sobre la biología del tumor y así poder desarrollar tratamientos terapéuticos que inhiban o retrasen el crecimiento del tumor primitivo y las metástasis (3)(4).
Por otro lado, el cerebro, hueso, hígado y pulmón son los sitios preferidos de metástasis en las pacientes con cáncer de mama (PCM). Ha sido reportado que las metástasis pueden ocurrir incluso en ausencia del tumor primario de mama y, en hueso, es el resultado de un desbalance fisiológico y físico como son la lesión lítica y la hipercalcemia (5). Es importante recordar que las metástasis óseas se expresan clínicamente por: 1)- Dolor óseo en el 60-70% de las PCM; 2)- Fractura patológica en el 30-40% de las PCM (68% en fémur y 28% en húmero); 3)- Síndrome de comprensión medular en el 20-30% de las PCM; 4)- Hipercalcemia en el 15% de las PCM y 5)- en los casos de afección vertebral, puede existir dolor local e irradiado, con o sin signos de déficit neu-rológico. Alteraciones que reducen la calidad de vida del paciente y se suman por lo tanto a la necesidad de profundizar sobre la compleja interacción entre las CEpTM y los componentes de MO y hueso (1)(5). Ambos tejidos proveen un microambiente favorable donde las células tumorales pueden proliferar y, así, la MO y el hueso se convierten en un reservorio de la enfermedad. Muchos avances recientes se han realizado en el tratamiento quimioterápico de las PCM avanzado (estadío clínico III y IV) pero la principal limitación es la falta de respuesta al tratamiento de las CEpTM quiescentes presentes en MO, así como la presencia de células madre tumorales. Hasta el momento, no se ha descrito en humanos, si anterior al desorden óseo que implica la invasión tumoral y desarrollo de la metástasis ósea (MTsO) existe una alteración en el potencial osteogénico de la MSC de MO para dar osteoblastos/osteocito y/o en su migración al hueso afectado. Y tampoco se estudió in vitro qué pasaba con la formación de osteoclastos a partir del progenitor hema-topoyético comprometido con el linaje monocítico de la MO en estas PCM avanzado sin MTsO. Sin embargo, lo que sí se encontró recientemente, es que la producción y actividad de los osteoclastos está regulada por los factores solubles liberados tanto por las MSC como por preosteo-blastos/ osteoblastos, así como por las CEpTM presentes en el hueso con metástasis [RANKL, M-CSF, TRAIL, OPG (receptor soluble de RANKL soluble o RANKL de membrana y TRAIL), IL-1β, IL-6, IL-11, IL-8, MIP-1α, PTHrP, TNF-α, TGF-β, PGE2, MMP-7, etc.], sin descartar un efecto indirecto por la liberación de estos factores desde el tumor primario en mama (6, 7). Los factores osteoclastogénicos pueden ser de acción directa como el RANKL, IL-11 o indirecta como la PTHrP, IL-6, IL-1, MIP-1α, PGE2, TNF-α, MMP-7 pues inducen la liberación de M-CSF y RANKL por parte del osteoblasto y MSC del microambiente de MO y hueso afectado (6, 7). En relación a la formación de oste-oclasto, el RANKL se une a su receptor el RANK presente en la membrana del preosteoclasto estimulando sucesivamente la diferenciación, la fusión a una célula multinu-cleada, la activación y la sobrevida del osteoclasto (8). Además, el M-CSF es un factor primordial en la osteoclas-togénesis pues incrementa directamente el pool de pre-osteoclastos en hueso y favorece la diferenciación a oste-oclasto pues al unirse a su receptor el c-fms presente en la membrana del preosteoclasto incrementa la expresión de RANK y su unión con RANKL (8).
En trabajos anteriores demostramos, por primera vez, una disminución significativa de la capacidad de clonado de las MSC para dar unidades formadoras de colonias fibroblásticas (CFU-F) en MO de PCM avanzado, libres de tratamiento y sin metástasis en MO y hueso, así como una disminución significativa del potencial osteogénico de las MSC de MO de estas PCM en comparación con las voluntarias sanas (VS) (9). Hechos ambos que se asocian posiblemente a una disminución de los niveles de Dkk-1 en los medios condicionados de los cultivos de CFU-F= MSC (Dkk-1 en medio de no diferenciación favorece la proliferación de la MSC y su sobrevida) y a un aumento de los niveles de Dkk-1 liberado en los medios condicionados de las MSC cultivadas en medio de diferenciación osteogénico (Dkk-1 inhibidor de la vía de las Wnt, factor este último inductor de la diferenciación osteogénica de la MSC), resultados estos últimos que encontramos en estas PCM (10). También cuantificamos un incremento significativo de Dkk-1 en plasma de sangre periférica (SP) de estas PCM avanzado en comparación con las VS (11).
Por otra lado, observamos osteoclastogénesis espontánea in vitro en estas PCM avanzado (libres de tratamiento y sin MTsO), independiente de que la diferenciación se hiciera a partir de precursores mielomono-cíticos de MO o de monocitos CD14+ de SP en comparación con las VS que presentaron una nula o mínima formación espontánea de osteoclastos. Los cultivos de las PCM tampoco respondieron in vitro a los factores os-teoclastogénicos conocidos (vitamina D3, RANKL y M-CSF). Mas aún, los medios condicionados de los cultivos de células mononucleares, no estimuladas, de MO de estas PCM avanzado fueron capaces de inducir la diferenciación osteoclástica de monocitos de SP de las VS a valores de % de osteoclasto semejantes al inducido con M-CSF + RANKL (11). Mas aún, se evaluó un incremento significativo de RANKL soluble y Dkk-1 (inhibidor de la osteogénesis e indirecto activador de la osteoclastogénesis por favorecer el pool de osteoblastos productores de RANKL) en SP de estas PCM; incremento significativo de ICAMs (activador de osteoclastos y factor que favorece la proliferación, migración y MTsO de la CEpTM) y disminución significativa de IL-10 (factor anti-osteoclasto-génico e inhibidor de algunos tumores) ambos en SP de estas PCM en comparación con las VS e incremento significativo de GM-CSF (factor que en exceso favorece la multinucleación de los preosteoclastos y su actividad) en los medios condicionados (7 días) de MSC de las PCM, así como un incremento en la expresión/ MSC de RANKL de membrana en estas pacientes (11). Todos los factores antes descriptos favorecen la osteoclastogénesis espontánea encontrada en MO y SP de estas PCM avanzado, pudiendo ser marcadores pronóstico de futuras MTsO.
Por último, encontramos que las MSC que quedan como reserva en la MO de las PCM avanzado, sin MTsO, poseen una disminución significativa de la capacidad de diferenciación no sólo osteogénica como se detalló anteriormente sino también adipogénica, a expensa del linaje condrogénico que está aumentado respecto a los valores de las VS. Esta deficiente plasticidad de la MSC de MO de estas PCM avanzado se relaciona con la disminución del % de la población de MSC con fenotipo CD146+ (marcador de MSC del nicho vascular) así como con una disminución del índice de fluorescencia relativa de CD146. Otros autores encontraron (12) que la mayor intensidad de fluorescencia relativa de CD146/ MSC corresponden a las MSC que presentan triple plasticidad y mayor autorrenovación, así como mayor capacidad de regular la hematopoyesis en comparación a las que expresan menos intensidad de fluorescencia relativa que corresponden a las MSC unipotenciales de baja eficiencia de clonado. De este último resultado y de nuestros estudios de años anteriores se desprende que en estas PCM avanzado previa aparición de las MTsO existe un menor reservorio de MSC con alta autorrenovación, sobrevida, migración y multipotencialidad, pues posiblemente al inicio del desarrollo tumoral hayan migrado las más efectivas al tumor primitivo como se describió en modelos mu-rinos y las que quedan en la MO en este momento del desarrollo tumoral tengan como función principal favorecer la osteoclastogénesis y resorción ósea, procesos ambos que favorecen el desarrollo de las MTOs.
Referencias bibliográficas
1. Patel SA, Heinrich AC, Reddy BY, Srinivas B, Heidaran N, Rameshwar P. Breast cancer biology: the multifac-eted roles of mesenchymal stem cells. J Oncol 2008: 425895.
2. Lorusso G, Rüegg C. The tumor microenvironment and its contribution to tumor evolution toward metastasis. Histochem Cell Biol 2008: 130: 1091-103.
3. Roorda BD, ter Elst A, Kamps WA, de Bont ES. Bone marrow-derived cells and tumor growth: contribution of bone marrow-derived cells to tumor micro-environments with special focus on mesenchymal stem cells. Crit Rev Oncol Hematol 2009: 69:187-98.
4. Arendt LM, Rudnick JA, Keller PJ, Kuperwasser C. Stroma in breast development and disease.
5. Rose AA, Pepin F, Russo C, Abou Khalil JE, Hallett M, Siegel PM. Osteoactivin promotes breast cancer metastasis to bone. Mol Cancer Res 2007: 5: 1001-14.
6. Wittrant Y, Théoleyre S, Chipoy C, Padrines M, Blan-chard F, Heymann D, et al. RANKL/RANK/OPG: new therapeutic targets in bone tumours and associated os-teolysis. Biochim Biophys Acta 2004: 1704: 49-57.
7. Rose AA, Siegel PM. Breast cancer-derived factors facilitate osteolytic bone metastasis. Bull Cancer 2006: 93: 931-43.
8. Khosla S. Minireview: the OPG/RANKL/RANK system. Endocrinology 2001: 142: 5050-55.
9. Hofer EL, Fernández Vallone VB, Labovsky V, Feldman L, Bordenave RH, LaRussa V, et al. Plasticity of mesenchy-mal stem cells from bone marrow of patients with lung and breast cancer. Libro del Congreso 5th Internacional Conference on Mesenchymal and Non Hematopoietic Stem Cells 2009, abst 23, pg 30; Austin, TX, EE.UU.
10. Hofer EL, Labovsky V, LaRussa VJ, Vallone VF, Honegger AE, Belloc CG, et al. Mesenchymal stromal cells, colony-forming unit fibroblasts, from bone marrow of untreated advanced breast and lung cancer patients suppress fi-broblast colony formation from healthy Marrow. Stem cells and development. 2010: 19: 359-70.
11. Fernández Vallone VB, Otaegui J, Dimase F, Batgelj E, Feldman L, Bordenave RH, Chasseing NA. Spontaneous osteoclastogenesis in bone marrow and peripheral blood of advanced breast cancer patients. Libro del Congreso 5th Internacional Conference on Mesenchymal and Non Hematopoietic Stem Cells; 2009, abst 48, pg 57. Austin, TX, EE.UU.
12. Russell KC, Phinney DG, Lacey MR, Barrilleaux BL, Mey-ertholen KE, O'Connor KC. In vitro high-capacity assay to wuantify the clonal heterogeneity in trilineage potential of mesenchymal Stem cells reveals a complex hierarchy of lineage commitment. Stem Cells 2010: 28: 788-98.
LABORATORIO DE INMUNOPATOLOGÍA
Glicómica de la respuesta inmune: el universo de glicanos y lectinas en microambientes inflamatorios y neoplásicos
Glycomics of the immune response: the universe of glycans and lectins in inflammatory and neoplasic microenvironments
Glicômica da resposta imune: o universo de glicanos e lectinas em microambientes inflamatórios e neoplásicos
Victoria Sundblad, Juan P. Cerliani, Daniel Compagno, Diego O Croci, Tomas Dalotto Moreno, L. Sebastián Dergan-Dylon, Santiago Di Lella, Claudia Gatto, Lucas Gentilini, Laura Giribaldi, Carlos M. Guardia, Juan M. Ilarregui, Diego J. Laderach, Verónica Martinez Alló, Iván D. Mascanfroni, Santiago Méndez Huergo, Mariana Salatino, Juan C. Stupirski, Marta A. Toscano, Gabriel A. Rabinovich
Resumen
Las galectinas, una familia de lectinas que reconocen glico-conjugados específicos en la superficie celular y la matriz, participan en diversos procesos biológicos como reguladores de la ho-meostasis de la respuesta inmune y de la progresión tumoral. Considerando el papel inmunomodulador de Galectina-1 (Gal-1) en modelos de inflamación crónica y su contribución a la creación de microambientes tolerogénicos, durante los últimos años exploramos el impacto de esta proteína sobre el balance de células T y la funcionalidad de células dendríticas (CDs). Mientras las células Th1 y Th17 poseen el repertorio de glicanos necesarios para la unión de Gal-1, los linfocitos Th2 son resistentes a la unión de esta proteína, lo cual explicaría el incremento en la susceptibilidad de los linfocitos Th1 y Th17 a la apoptosis inducida por Gal-1 y la consecuente desviación en el balance de la respuesta inmune hacia un perfil Th2. Además, identificamos un circuito tolerogénico en el que Gal‐1 induce la diferenciación de CDs tolerogénicas productoras de IL‐27, la consecuente expansión de células T regulatorias productoras de IL‐10 y la supresión de la inflamación mediada por células Th1 y Th17. Postulamos un nuevo mecanismo de regulación homeostática de la respuesta inmune basado en la interacción entre Gal‐1 y sus gli-canos específicos, el cual permite anticipar nuevos horizontes terapéuticos, en los que la modulación de la expresión de Gal‐1 o sus glicanos nos permitiría regular la respuesta inmune.
Palabras clave: galectina-1; células T; células dendríticas; tolerancia inmunológica.
Summary
Galectins, a family of endogenous glycan-binding proteins able to recognize specific glycoconjugates on cell surface and extracellular matrix, control critical immunological processes involved in immune homeostasis and tumor progression. Given the immunosuppressive role of Galectin-1 (Gal-1) in different models of chronic inflammation and its contribution to the creation of tolerogenic microenvironments in cancer and pregnancy models, the impact of this protein on T helper cell balance and dendritic cells (DCs) functionality was explored. A novel mechanism, based on the differential glycosylation of T helper cell subsets, by which Gal-1 preferentially eliminates antigen-specific Th1 and Th17 cells, leading to a shift toward a Th2 profile was identified. While Th1- and Th-17-differentiated cells expressed the repertoire of cell surface glycans that are critical for Gal-1-induced cell death, Th2 cells are protected from Gal-1 through differential sialylation of cell surface glycoproteins. More recently, the ability of Gal-1 to trigger the differentiation of tolerogenic dendritic cells (DCs), which promote resolution of autoimmune inflammation, was demonstrated. A tolerogenic circuit linking Gal-1 signaling, IL-27-producing DCs and IL-10-secreting T cells was identified. It can be postulated that molecular interactions between endogenous galectins and specific glycans constitute a novel mechanism of homeostatic regulation of immune responses. Understanding the role of protein-glycan interactions in the establishment of tolerogenic or inflammatory programs will enable the design of more rational immunotherapeutic strategies with broad biomedical implications.
Key words: galectin-1; T cells; dendritic cells; immune tolerance.
Resumo
As galectinas, uma família de lectinas que reconhecem gli-coconjugados específicos na superfície celular e a matriz, participam em diversos processos biológicos como reguladores da homeostase da resposta imune e da progressão tu-moral. Considerando o papel imunomodulador de Galec-tina-1 (Gal-1) em modelos de inflamação crônica e sua contribuição à criação de microambientes tolerogênicos, durante os últimos anos exploramos o impacto desta proteína sobre o balanço de células T e a funcionalidade de células dendríticas (CDs). Enquanto as células Th1 e Th17 possuem o repertório de glicanos necessários para a união de Gal-1, os linfócitos Th2 são resistentes à união desta proteína, o qual explicaria o incremento na suscetibilidade dos linfóci-tos Th1 e Th17 à apoptose induzida por Gal-1 e o conse-guinte desvio no balanço da resposta imune para um perfil Th2. Além disso, identificamos um circuito tolerogênico no qual Gal‐1 induz a diferenciação de CDs tolerogênicas pro-dutoras de IL‐27, a conseguinte expansão de células T re-gulatórias produtoras de IL‐10 e a supressão da inflamação mediada por células Th1 e Th17. Postulamos um novo mecanismo de regulação homeostática da resposta imune ba-seado na interação entre Gal‐1 e seus glicanos específicos, que permite antecipar novos horizontes terapêuticos, nos quais a modulação da expressão de Gal‐1 ou seus glicanos nos permitiria regular a resposta imune.
Palavras chave: galectina-1; células T; células dendríticas; tolerância imunológica.
Introducción
En los últimos años, el estudio de la glicosilación diferencial de proteínas de superficie celular ha cobrado renovado interés, debido a la posibilidad de descifrar información biológica clave codificada en sacáridos específicos (1). Una gran variedad de glicanos, producto de la acción secuencial de un amplio repertorio de enzimas denominadas glicosiltransferasas y glicosidasas, decora la superficie de las células de nuestro organismo (2). La gli-cosilación de proteínas de superficie de células del sistema inmune puede modificarse drásticamente en condiciones fisiológicas y patológicas, regulando de esta forma procesos críticos de la respuesta inmune, tales como la activación de células T, la migración linfocitaria y la síntesis de citoquinas (1). Es así que el repertorio de glicanos en la superficie celular codifica información fisiológica clave que regula la homeostasis del sistema inmune. La tarea de decodificar dicha información recae sobre un número limitado de proteínas de unión a gli-canos o lectinas endógenas (1)(3).
Las galectinas constituyen una familia de lectinas extremadamente conservadas a través de la evolución que reconocen y se unen a glicanos con configuración [Galβ1-4-NAcGlc] (4). Durante los últimos años se ha involucrado a esta familia en diversos procesos biológicos como reguladores de la homeostasis de la respuesta inmune (3) y de la progresión tumoral (6). Hasta el momento se han descripto 15 miembros de esta familia en diversos tejidos de distintas especies (4). A pesar de la similitud de secuencia y especificidad de interacción con carbohidratos, algunos miembros de la familia de galectinas se comportan como amplificadores de la respuesta inmune, mientras que otros regulan negativamente el desarrollo de procesos inflamatorios (3).
Gal-1: una lectina endógena con propiedades anti-inflamatorias
Numerosas evidencias asignan a galectina-1 (Gal-1), un miembro 'proto-tipo' de la familia de galectinas, una función crítica en la homeostasis de la respuesta inmune e inflamatoria (3)(4) (Figura 1). Esta proteína es capaz de inhibir la proliferación y expansión clonal de linfocitos T activados, mediante mecanismos que involucran bloqueo de la activación, arresto del ciclo celular e inducción de apoptosis (3)(4). Gal-1 se halla ausente en linfocitos T en reposo; sin embargo comienza a expresarse durante la activación de células T contribuyendo de este modo a la regulación negativa de la respuesta efectora. Más aún, se ha demostrado que Gal-1 se expresa en forma incrementada en células T regula-torias CD4+CD25+FoxP3+ contribuyendo a su potencial inmunosupresor (3)(4).
En diferentes modelos experimentales de inflamación crónica y autoinmunidad (incluidos modelos de artritis reumatoidea, enfermedad inflamatoria intestinal, uveitis autoinmune y diabetes), la administración exó-gena de Gal-1 logró suprimir la inflamación dependiente de citoquinas Th1, promoviendo un incremento en la apoptosis de linfocitos T patogénicos y un desvío de la respuesta inflamatoria hacia un perfil Th2 (4). Por otro lado, en un modelo murino de abortos inducidos por stress, observamos que Gal-1 logró reestablecer la tolerancia inmunológica, disminuyendo las tasas de rechazo fetal al incrementar la frecuencia de células T re-gulatorias y células dendríticas (DCs) tolerogénicas en la interfase materno-fetal (5).
Se ha observado que Gal-1 se expresa en forma abundante en diversos tipos de tumores tales como próstata, melanoma, ovario, y mama, y su expresión correlaciona con la malignidad de dichos tumores y su potencial metastásico (6). En este contexto, en nuestro laboratorio demostramos que Gal-1 juega un papel crítico en fenómenos inmunosupresores en el microambiente tu-moral. En el modelo experimental de melanoma B16 en ratones, demostramos previamente que Gal-1, sintetizada y secretada por células de melanoma, inhibe el desarrollo de una respuesta inmune Th1 antitumoral efectiva favoreciendo la progresión tumoral (7). El bloqueo de la actividad inmunosupresora de Gal-1 en el miEstructura: Galectina prototipo. Homodímero compuesto por dos subunidades de 14.5 kDa croambiente tumoral condujo a una respuesta mediada por células CD8 y Th1, lo cual resultó en un rechazo tu-moral. Este efecto lo confirmamos en linfoma Hodgkin demostrando el papel de Gal-1 como factor promotor del escape tumoral a través de un mecanismo dependiente del factor de transcripción AP1 (8). En conjunto, estos hallazgos sugieren fuertemente que la expresión de Gal-1 por células tumorales constituye un nuevo mecanismo de escape tumoral.

Figura 1. Propiedades inmunomoduladoras de Galectina-1 (Gal-1)
Teniendo en cuenta el papel de Gal-1 en diferentes modelos de inflamación crónica y su contribución a la creación de microambientes tolerógenicos, el estudio de los posibles mecanismos involucrados en estos efectos resulta de particular interés. Es así que en el laboratorio exploramos el impacto de Gal-1 sobre el balance de células T efectoras, y su efecto sobre la funcionalidad de DCs.
Impacto de la interacción entre Gal-1 y glicanos en la regulación de la fisiología de células T
Procesos como maduración tímica, activación, migración y apoptosis de linfocitos T constituyen algunos de los eventos de la fisiología linfocitaria que son regulados por interacciones entre proteínas y glicanos (9). Se ha demostrado que Gal-1 interacciona con alta avidez con gli-coconjugados que contienen residuos poli-LacNAc presentes en N- y O-glicanos (3)(4). La expresión y actividad de las glicosiltransferasas involucradas en la síntesis de secuencias de poli-LacNAc determinan la susceptibilidad a la apoptosis inducida por esta lectina in vivo. Además, la incorporación de ácido siálico en un enlace α(2→6) a ligandos poli-LacNAc en N-glicanos, por la enzima ST6Gal I, inhibe la unión de Gal-1 y reduce la susceptibilidad de linfocitos T a la acción de esta proteína (3). De este modo, el enmascaramiento de ligandos específicos en la superficie celular podría controlar la unión de Gal-1 y evitar la inducción de apoptosis de linfocitos T.
En este sentido, en el laboratorio demostramos que la interacción entre Gal‐1 y sus glicanos específicos constituye un paso clave en la regulación homeostática selectiva de las respuestas T. Notablemente, observamos que linfocitos Th1, Th2 y Th17 presentan una susceptibilidad diferencial a la apoptosis inducida por Gal-1. Al explorar los mecanismos involucrados, encontramos que, mientras las células Th1 y Th17 poseen el repertorio de glicanos necesarios para la unión de Gal-1, los linfocitos Th2 son resistentes a la unión de esta proteína ya que los residuos LacNAc se hallan decorados con acido siálico en posición α2,6 merced a la expresión de la sialiltransferasa ST6Gal I. In vivo, demostramos que la administración de Gal‐1 inhibe la inflamación mediada por células Th1 y Th17 durante la encefalo-mielitis autoinmune experimental (EAE). En este con-/-texto, ratones deficientes en el gen de Gal-1 (Lgals1 ) exhiben un incremento de la severidad de la respuesta inflamatoria frente al desafío con estímulos antigénicos en modelos experimentales de autoinmunidad (10).
Papel crítico de Gal-1 en la diferenciación de células dendríticas tolerogénicas
Las DCs son células presentadoras de antígeno altamente especializadas en reconocer, procesar y presentar antígenos a células T vírgenes. Tradicionalmente se ha identificado a las DCs como células capaces de promover la iniciación y amplificación de la respuesta inmune adaptativa. Sin embargo, evidencias recientes indican que las DCs poseen a su vez la facultad de promover tolerancia y silenciar la respuesta inmune favoreciendo la expansión de células T regulatorias con fenotipo CD4+CD25+Foxp3+ (Tregs) ó FoxP3- productoras de IL-10 (Tr1) (11). Se ha observado que citoquinas producidas por el estroma tumoral y mediadores anti-inflama-torios pueden favorecer la diferenciación de DCs capaces de silenciar la respuesta inmune (11). En búsqueda de posibles mecanismos responsables de la acción anti-inflamatoria de Gal-1 y considerando el papel crítico que cumplen las DCs en las decisiones entre tolerancia e inflamación, en nuestro laboratorio exploramos el impacto de Gal-1, tanto exógena como endógena, sobre la diferenciación, maduración, funcionalidad y capacidad regulatoria de DCs utilizando diferentes modelos experimentales in vitro e in vivo.
DCs derivadas de médula ósea diferenciadas en presencia de Gal-1 (DCGal-1) exhibieron un perfil regula-torio dependiente de la producción de IL-27 y de la activación del factor de transcripción STAT3, en comparación con DCs controles (12). La función tole-rogénica de DCGal-1 fue confirmada en cultivos alogé-nicos in vitro y desafíos antígeno-específicos in vivo. La relevancia fisiopatológica de DCs diferenciadas en presencia de Gal-1 fue demostrada en modelos experimentales de cáncer e inflamación crónica. DCGal-1 demostraron menor capacidad de proteger ratones singénicos frente al desafío con melanoma B16, favoreciendo la inducción de tolerancia en el microam-biente tumoral. En un abordaje terapéutico, observamos que la administración de DCGal-1 suprimió las manifestaciones clínicas de autoinmunidad e inhibió las respuestas patogénicas Th1 y Th17. Nuestros resultados revelaron la capacidad de Gal-1 de iniciar un circuito to-lerogénico al interaccionar con glicanos presentes en DCs inmaduras, y de esta forma generar DCs tolerogé-nicas productoras de IL-27 que inducen la diferenciación de células Tr1 productoras de IL-10 (12). Estos hallazgos sugieren un papel jerárquico clave para Gal-1 en la iniciación de circuitos inmunosupresores in vivo y en la generación de DCs regulatorias con potencial tole-rogénico en enfermedades inflamatorias y cáncer.
Conclusiones y Perspectivas Futuras
En conjunto estos resultados permiten postular un nuevo mecanismo de regulación homeostática de la respuesta inmune basado en la interacción entre Gal‐1 y sus glicanos específicos. La glicosilación diferencial de los linfocitos Th1, Th2 y Th17 explicaría el incremento en la susceptibilidad de los linfocitos Th1 y Th17 a la muerte celular inducida por activación y la consecuente desviación en el balance de la respuesta inmune hacia un perfil Th2, observados en modelos de inflamación crónica luego del tratamiento con esta lectina (Figura 2). Además, identificamos un circuito tolerogénico en el que la señalización vía Gal‐1 conduce a la diferenciación de DCs tolerogénicas productoras de IL‐27, con la consecuente expansión de células T regulatorias productoras de IL‐10 y la supresión de la inflamación mediada por células Th1 y Th17 (Figura 2). A la luz de estos resultados es posible anticipar nuevos horizontes terapéuticos en diferentes patologías, tales como procesos neoplásicos o infecciosos, en los que la inhibición de la expresión de Gal‐1 o sus glicanos nos permitiría potenciar la respuesta inmune. Por otro lado en procesos inflamatorios crónicos, enfermedades autoinmunes y en episodios de rechazo de transplantes, la inducción de DCs con capacidad tolerogénica por estimulación con Gal‐1 brindaría importantes beneficios terapéuticos generando efectos inmunomoduladores selectivos lo cual constituye EL MAYOR DESAFÍO DE LA INMUNOLOGÍA DE ESTE NUEVO MILENIO.

Figura 2. Galectinas: Un nuevo paradigma en la respuesta inmune. Acción selectiva de Gal-1 sobre células dendríticas (DC) y diferentes poblaciones de células T (Th1, Th17 y Th2).
AGRADECIMIENTOS
Los trabajos de nuestro equipo fueron financiados en los últimos 5 años por el CONICET (PIP 2008), la Agencia Nacional de Promoción Científica y Tecnológica (FONCYT; PICT 2006; PICT Bi-centenario 2010), la Universidad de Buenos Aires (UBACYT 2010-2012), la Fundación Florencio Fiorini (2007), la Fundación Sales (Programa Sales/CONICET 2000-presente), el Cancer Research Institute (New York 2006-2011), la Mizutani Foundation for Glycoscience (Tokio, Programa 2005 y Programa 2011), la Prostate Cancer Research Foundation (London; 2009-2012). Agradecemos a todos los miembros y colaboradores administrativos y técnicos del IBYME por su apoyo y colaboración desinteresada
Referencias bibliográficas
1. van Kooyk Y, Rabinovich GA. Protein-glycan interactions in the control of innate and adaptive immune responses. Nature Immunol 2008; 9: 593-601.
2. Ohtsubo K, Marth JD. Glycosylation in cellular mechanisms of health and disease. Cell 2006; 126: 855-67.
3. Rabinovich GA, Toscano MA. Turning 'sweet' on immunity: galectin-glycan interactions in immune tolerance and inflammation. Nature Rev. Immunol 2009; 9: 338-52.
4. Liu FT, Rabinovich GA. Galectins: regulators of acute and chronic inflammation. Ann. N.Y. Acad. Sci. 2010; 1183: 158-82.
5. Blois SM, Ilarregui JM, Tometten M, Garcia M, Orsal AS, Cordo-Russo R, et al. A pivotal role for galectin-1 in fe-tomaternal tolerance. Nat Med 2007; 13: 1450-7.
6. Liu F, Rabinovich G. Galectins as modulators of tu-mourprogression. Nature Rev Cancer 2005; 5: 29-41.
7. Rubinstein N, Alvarez M, Zwirner NW, Toscano MA, Ila-rregui JM, Bravo A, et al. Targeted inhibition of galectin-1 gene expression in tumor cells results in heightened T cell-mediated rejection; A potential mechanism of tumor-immune privilege. Cancer Cell 2004; 5: 241-51.
8. Juszczynski P, Ouyang J, Monti S, Rodig SJ, Takeyama K, Abramson J, et al. The AP1-dependent secretion of galectin-1 by Reed Sternberg cells fosters immune privilege in classical Hodgkin lymphoma. Proc Natl Acad Sci USA 2007; 104: 13134-9.
9. Lowe JB. Glycosylation, immunity, and autoimmunity. Cell 2001; 104: 809-12.
10. Toscano MA, Bianco GA, Ilarregui JM, Croci DO, Cor-reale J, Hernandez JD, et al. Differential glycosylation of TH1, TH2 and TH-17 effector cells selectively regulates susceptibility to cell death. Nature Immunol 2007; 8: 825-34.
11. Rabinovich GA, Gabrilovich D, Sotomayor EM. Im-munosuppressive strategies that are mediated by tumor cells. Annu. Rev Immunol 2007; 25: 267-96.
12. Ilarregui JM, Croci DO, Bianco GA, Toscano MA, Salatino M, Vermeulen ME, et al. Tolerogenic signals delivered by dendritic cells to T cells through a galectin-1-driven im-munoregulatory circuit involving interleukin 27 and in-terleukin 10. Nature Immunol 2009; 10: 981-91.
LABORATORIO DE INMUNOPATOLOGÍA
Células NK: una interfase entre la inmunidad innata y adaptativa con potencial inmunoterapéutico.
NK cells: an interphase between innate and adaptive immunity with immunotherapeutic potential
Células NK: uma interfase entre a imunidade inata e adaptativa com potencial imunoterapêutico
Norberto W. Zwirner, Mercedes B. Fuertes, Carolina I. Domaica, Lucas E. Rossi, Damián E. Ávila, Raúl G. Spallanzani, Andrea Ziblat, Ximena Raffo Iraolagoitía
Resumen
Las células citotóxicas naturales o NK juegan un rol crítico en la inmunovigilancia contra tumores y regulan la respuesta inmune a través de la secreción de citoquinas y la citotoxicidad. Los receptores NKG2D y NKp46 juegan un rol central en dichos procesos. No obstante, las células NK son blanco de mecanismos de escape tumoral tal como la retención intracelular de MICA (MHC class I chain-related protein A) en retículo endoplásmico de algunos melanomas humanos. Las células NK también se activan por citoqui-nas (IL-12 o IFN-α) y receptores de tipo Toll, efecto que es potenciado por tumores que promueven la microagre-gación de NKG2D. Asimismo, el contacto célula tumo-ral-linfocito T induce la secreción de IFN-α por células NK a través de la adquisición de ligandos de NKG2D y NKp46 de células tumorales por linfocitos T, los que subsecuentemente promueven la estimulación de las células NK a través de NKG2D y NKp46. Por consiguiente, células de la inmunidad adaptativa regulan a las células de la inmunidad innata, lo que podría tener relevancia en la inmunidad anti-tumoral. Además, determinadas drogas anti-neoplásicas comprometen la función de las células NK, lo que atenta contra su eficacia terapéutica. En resumen, las células NK poseen un gran potencial inmunoterapéutico para cuya explotación deberemos elucidar los mecanismos celulares y moleculares que gobiernan el desarrollo de sus funciones efectoras.
Palabras clave: células NK; receptores; tumores; inter-ferón; inmunoterapia.
Summary
Natural killer (NK) cells critically participate in the immune surveillance against tumors and are pivotal regulators of the adaptive immune through the secretion of cytokines and the cytotoxic function. NKG2D and NKp46 are two key receptors involved in these processes. Howeverr, NK cells are targets of tumor immune escape mechanisms such as ntracellular retention of MICA (MHC class I chain-related protein A) in the endoplasmic reticulum of certain human melanomas. NK cells also become activated in a cooperative manner by cytokines (IL-12 or IFN-α) and Toll like receptors, an effect that is potentiated by tumors that promote engagement of NKG2D. Moreover, tumor cell-T cell contact induce secretion of IFN-γ by NK cells through acquisition of tumor-derived NKG2D and NKp46 ligands by T cells, which subsequently promote NKG2D- and NKp46-dependent NK cell stimulation. Therefore, cells from the adaptive immune response regulate the activity of cells of the innate immune response, which may have relevance during anti-tumor immunity. Also, some anti-neoplastic drugs impair an NK cell function, which reduces their therapeutic efficacy. In summary, NK cells have a great immunotherapeutic potential but to fully exploit it, the cellular and molecular mechanisms that govern their effector function must be elucilated first.
Keywords: NK cells, receptors, tumors, interferon, immu-notherapy
Resumo
As células citotóxicas naturais ou NK têm um papel crítico na imunovigilância contra tumores e regulam a resposta imune através da secreção de citocinas e a citotoxicidade. Os receptores NKG2D e NKp46 têm um papel central em tais processos. Não obstante isso, as células NK são alvo de mecanismos de escape tumoral tal como a retenção intrace-lular de MICA (MHC class I chain-related protein A) em retículo endoplásmico de alguns melanomas humanos. As células NK também são ativadas por citocinas (IL-12 ou IFN-a) e receptores de tipo Toll, efeito que é potenciado por tumores que promovem a microagregação de NKG2D. Do mesmo modo, o contato célula tumoral-linfócito T induz a secreção de IFN-y por células NK através da aquisição de ligandos de NKG2D e NKp46 de células tumorais por linfócitos T, os que imediatamente promovem a estimulação das células NK através de NKG2D e NKp46. Por conseguinte, células da imu-nidade adaptativa regulam as células da imunidade inata, o que poderia ter relevância na imunidade antitumoral. Além disso, determinadas drogas antineoplásicas comprometem a função das células NK, o que atenta contra sua eficácia terapêutica. Em resumo, as células NK possuem um grande potencial imunoterapêutico para cuja exploração deveremos elucidar os mecanismos celulares e moleculares que gover-nam o desenvolvimento de suas funções efetoras.
Palavras chave: células NK; receptores; tumores; inter-feron; imunoterapia.
Introducción
Células NK, receptores y ligandos
Evidencias obtenidas en los últimos años han contribuido a una comprensión de los eventos celulares y moleculares que regulan la activación de las células citotóxicas naturales o células NK contra células tu-morales (1) y durante la respuesta inmune contra patógenos (2). La función primordial de las células NK es la secreción de citoquinas pro-inflamatorias (IFN-γ, TNF-α, TNF-β, GM-CSF e IL-10 (3), siendo el IFN-αcrítico para la polarización de la respuesta inmune hacia un perfil TH1 (4)(5). Además, las células NK estimulan la activación de macrófagos hacia perfiles clásicos o de tipo 1 (M1) y promueven la maduración de las células dendríticas (CDs) a través de un contacto célula-célula (6)(7).
El reconocimiento de las células blanco por las células NK es llevado a cabo por receptores activadores o inhibidores que regulan sus funciones efectoras (8)(9). Los receptores inhibidores reconocen moléculas de clase I del complejo mayor de histocompati-bilidad (CMH) y dentro de este grupo se destacan algunos miembros de la familia KIR (killer Ig-like receptors) en humanos y de la familia Ly49 en ratones. Los receptores activadores constituyen un grupo heterogéneo de moléculas de superficie entre las que se destacan la molécula CD16 (receptor para porción Fc de inmunoglobulinas de tipo IIIA), el receptor NKG2D (CD314), el receptor DNAM-1 (CD226), el receptor 2B4 (CD244) y los miembros de la familia de receptores de citotoxicidad natural (natural cytotoxicity receptors o NCRs), integrada por las moléculas NKp46 (CD335), NKp44 (CD336) y NKp30 (CD337). Los receptores NKG2D y NKp46 son críticos para la detección temprana y eliminación de tumores ya que ratones deficientes en NKG2D (10) o en NKp46 (11) muestran una mayor susceptibilidad a la generación de tumores, y el bloqueo in vivo de NKG2D mediante la administración de un anticuerpo monoclonal favorece la iniciación y crecimiento tumoral (12). En humanos, se conoce que existe una mayor incidencia de tumores de diferentes fenotipos en individuos que presentan una baja actividad citotóxica natural en células de sangre periférica (13). Este cúmulo de datos demuestra que las células NK censan la presencia de células tumorales a través de NKG2D y NKp46, y de esta manera protegen al individuo del desarrollo y progresión tumoral.
La mayoría de los receptores activadores reconocen ligandos inducibles en células infectadas o tumorales (8, 9). La identidad de los ligandos de los NCRs sobre células tumorales es aún desconocida aunque NKp30 reconoce a la molécula B7-H6 (14). Para NKG2D se han descripto cerca de 10 ligandos (NKG2DLs) diferentes (15, 16). DNAM-1 reconoce como ligandos al receptor del virus de la polio (PVR o CD155) y a la molécula nectina-2 (CD112) (17), y participa en la eliminación de células tumorales (18)(19).
Células NK, respuesta anti-tumoral y mecanismos de escape
El rol crítico de las células NK en la inmunidad antitumoral hace que no sea sorprendente que existan mecanismos de escape tumoral que involucran a ligandos reconocidos por diversos receptores activadores de células NK (20-22). En particular, MICA (MHC class I chain-related protein A) es un NKG2DL inducido por estímulos de estrés genotóxico que se expresa en superficie celular de diversos tumores y que promueve la activación de las células NK y de linfocitos T CD8 citotóxicos (16). Sin embargo, en nuestro laboratorio hemos observado que determinados melanomas humanos poseen la particularidad de promover una retención intracelular de la molécula MICA en retículo endoplásmico debido a la acumulación de formas inmaduras del polipéptido (21). Esta retención intracelular confiere resistencia a mecanismos efectores de las células NK y privilegio inmunológico (Fig. 1) por lo que constituye un novedoso mecanismo de escape tumoral cuya elucidación permitirá diseñar estrategias tendientes a restaurar la expresión de MICA en superficie de células tumorales con el fin de mejorar la calidad de la respuesta inmune anti-tumoral mediada por células NK.
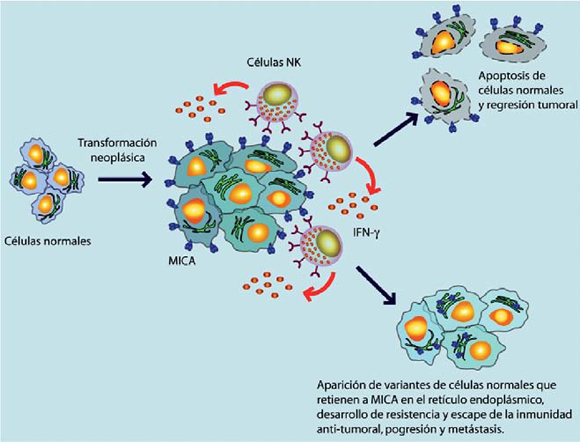
Figura 1. Mecanismo de escape tumoral en melanomas humanos basado en la retención intracelular de MICA. La expresión de MICA se inicia como consecuencia de la transformación maligna de melanocitos normales. Células de melanoma que expresan MICA en superficie son detectadas por células NK a través de NKG2D, lo que promueve la secreción de IFN-γ, la cito-toxicidad contra las células tumorales y, si el proceso es eficiente, contribuye con la regresión tumoral (parte superior de la figura). Células de melanoma que desarrollan el mecanismo de retención intracelular de MICA en el retículo endoplásmico adquieren la capacidad de prevenir el reconocimiento por células NK a través de NKG2D y consecuentemente, se favorece la aparición de variantes tumorales resistentes, lo que favorece el escape tumoral y la progresión (parte inferior de la figura).
Células NK y activación por citoquinas y receptores de tipo Toll (TLRs)
Las células NK también pueden activarse por cito-quinas tales como IL-2, IL-12, IL-15, IL-18, IL-21 e IFN-α(coincidentemente, estas citoquinas han mostrado resultados promisorios en protocolos de inmunoterapia del cáncer (23), y a través del reconocimiento de patrones moleculares asociados a patógenos ya que expresan diversos receptores de tipo Toll (TLRs) (24). En particular, IL-12, IL-15 e IL-18 son secretadas por CDs durante la respuesta inmune contra patógenos y tumores, lo que establece un diálogo recíproco entre CDs y células NK (2)(4)(5)(7). Además, la activación de las células NK se encuentra regulada negativamente por TGF-β producido por células T regulatorias (25). En nuestro laboratorio hemos demostrado la existencia de efectos cooperativos para la secreción de IFN-a por células NK desencadenados por agonistas de TLR3 o TLR7 en presencia de dosis subóptimas de IL-12 o IFN-α (24). Asimismo, observamos una secreción de IFN-7 mayor aún por células NK cuando fueron estimuladas con dichos agonistas e IL-12 en presencia de tumores que sobre-expresan MICA. Por lo tanto, la activación de células NK a través de diferentes tipos de receptores potencia notablemente la secreción de IFN-y (Fig. 2). Por ello, las estrategias terapéuticas con agonistas de TLR3 o TLR7 favorecerían no sólo la maduración de las CDs y la activación de la respuesta inmune adaptativa sino también el desarrollo de funciones efectoras mediadas por células NK, lo que podría ser más relevante aún en pacientes con tumores que expresan NKG2DL.
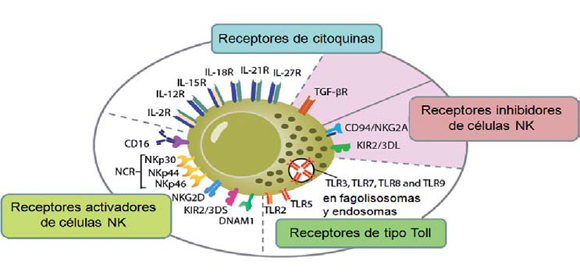
Figura 2. Efectos cooperativos de receptores de tipo Toll, receptores de citoquinas y receptores activadores (NKG2D) sobre la capacidad de secreción de IFN-γen células NK. La estimulación simultánea a través de estas categorías de receptores es un poderoso estímulo para la secreción de IFN-γ por parte de las células NK.
Células NK y regulación por linfocitos T CD4
Durante los últimos años se ha elucidado cómo es la intrincada relación entre los tumores y el huésped durante distintas etapas del crecimiento tumoral (26) y se han descubierto un gran número de mecanismos que regulan la respuesta inmune contra tumores y de escape tumoral (27). Sin embargo, poco es lo que se conoce acerca de la existencia de posibles mecanismos regula-torios entre células NK y linfocitos T CD4. En nuestro laboratorio hemos observamos que el contacto célula tu-moral-linfocito T promueve el desarrollo, por parte de estos últimos, de funciones estimuladoras para células NK, lo que gatilla la secreción de IFN-γ a través de un mecanismo que involucra la adquisición de moléculas de superficie de las células tumorales por parte de los linfocitos T durante el contacto mutuo (fenómeno conocido como trogocitosis)(28). Entre las moléculas adquiridas se destacan MICA y ligandos de NKp46, los que subsecuentemente promueven la estimulación de las células NK a través de NKG2D y NKp46 y el desarrollo de funciones efectoras (Fig. 3). Así, demostramos por primera vez que células de la inmunidad adaptativa (células T CD4) adquieren propiedades estimulatorias para células de la inmunidad innata (células NK) mediante un fenómeno de trogocitosis que podría tener relevancia en la respuesta anti-tumoral y en otras situaciones patológicas donde se observe alta expresión de ligandos de NKG2D y NKp46, y reclutamiento de células T CD4 y NK.

Figura 3. Estimulación de células NK por linfocitos T activador como consecuencia de la captura (trogocitosis) de MICA y ligandos de NKp46 desde la superficie tumoral. Cuando linfocitos T activados contactan células tumorales, capturan moléculas de la superficie de éstas, tales como MICA y ligandos de NKp46. Estas moléculas, ahora ubicadas en la superficie de los linfocitos T activados, promueven la secreción de IFN-γ por parte de las células NK por medio del reconocimiento a través de NKG2D y NKp46.
Células NK y terapias anti-tumorales
Aunque la radio- y la quimioterapia son las estrategias terapéuticas más efectivas para el tratamiento de las enfermedades neoplásicas en seres humanos, no están exentas de efectos secundarios indeseables. Esto ha movilizado el desarrollo de nuevas drogas anti-tumorales, muchas de las cuales han mostrado resultados promisorios. Sin embargo, en muchos casos se desconoce si estos compuestos ejercen efectos deletéreos sobre células del sistema inmune comprometidas en la inmunovigilancia, lo que atentaría contra la efectividad terapéutica de estas drogas. En los últimos años se ha puesto interés en el papel de las deacetilasas de histonas (HDACs), ya que existen evidencias que las vinculan con el desarrollo de tumores. Esto ha movilizado el desarrollo de inhibidores de HDACs (HDACi) y su empleo como drogas anti-tumorales (29-31). Aunque algunos HDACi aumentan la expresión de NKG2DLs haciendo a las células tumorales más susceptibles a los mecanismos efectores de las células NK in vitro (32), en nuestro laboratorio hemos observado que comprometen la actividad funcional de las células NK, lo que podría atentar contra su eficacia terapéutica.
Conclusiones generales
Las células NK, si bien son críticas en la inmunovi-gilancia contra tumores, no están exentas de padecer mecanismos de escape tumoral. Algunos melanomas humanos promueven una retención intracelular en el retículo endoplásmico de ligandos de NKG2D, lo que confiere resistencia a mecanismos efectores de las células NK y privilegio inmunológico. Asimismo, las células NK pueden activarse por citoquinas y a través de TLRs, efectos que se ven potenciados por estímulos a través de NKG2D, por lo que estrategias de inmunote-rapia con agonistas de TLRs podrían favorecer el desarrollo de funciones efectoras de las células NK, sobre todo en pacientes con tumores que expresan NKG2DL. Además, los linfocitos T CD4, a través de un fenómeno de trogocitosis de MICA y de ligandos de NKp46, adquieren la capacidad de promover la secreción de IFN-γ por células NK luego de haber contactado células tumorales, lo que indica que células de la inmunidad adaptativa pueden regular la actividad de células de la inmunidad innata.
Asimismo, el empleo de nuevas drogas para el tratamiento de enfermedades neoplásicas tales como los HDACi constituye un arma de doble filo ya que el efecto anti-tumoral de estas drogas va acompañado de efectos supresores de la actividad funcional de las células NK, lo que podría atentar contra su eficacia terapéutica. Por lo tanto, las células NK poseen un gran potencial in-munoterapéutico pero para explotar tales capacidades deberemos profundizar en el estudio de los mecanismos celulares y moleculares que gobiernan el desarrollo de sus funciones efectoras.
Referencias bibliográficas
1. Zwirner NW, Croci DO, Domaica CI, Rabinovich GA. Overcoming the hurdles of tumor immunity by targeting regulatory pathways in innate and adaptive immune cells. Curr Pharm Des 2010; 16: 255-67.
2. Newman KC, Riley EM. Whatever turns you on: accessory-cell-dependent activation of NK cells by pathogens. Nat Rev Immunol 2007; 7: 279-91.
3. Cooper MA, Fehniger TA, Turner SC, Chen KS, Ghaheri BA, Ghayur T, et al. Human natural killer cells: a unique innate immunoregulatory role for the CD56(bright) subset. Blood 2001; 97: 3146-51.
4. Ferlazzo G, Pack M, Thomas D, Paludan C, Schmid D, Strowig T, et al. Distinct roles of IL-12 and IL-15 in human natural killer cell activation by dendritic cells from secondary lymphoid organs. Proc Natl Acad Sci USA 2004; 101: 16606-11.
5. Martin-Fontecha A, Thomsen LL, Brett S, Gerard C, Lipp M, Lanzavecchia A, et al. Induced recruitment of NK cells to lymph nodes provides IFN-gamma for T(H)1 priming. Nat Immunol 2004; 5: 1260-5.
6. Ikeda H, Old LJ, Schreiber RD. The roles of IFN gamma in protection against tumor development and cancer im-munoediting. Cytokine & Growth Factor Rev 2002; 13: 95-109.
7. Mailliard RB, et al. (2003) Dendritic cells mediate NK cell help for Th1 and CTL responses: two-signal requirement for the induction of NK cell helper function. (Translated from eng) J Immunol 171(5): 2366-73 (in eng).
8. Lanier LL. NK cell recognition. Annu Rev Immunol 2005; 23: 225-74.
9. Moretta L, Bottino C, Pende D, Castriconi R, Mingari MC, Moretta A. Surface NK receptors and their ligands on tumor cells. Semin Immunol 2006; 18: 151-8.
10. Guerra N, Tan YX, Joncker NT, Choy A, Gallardo F, Xiong N, et al. NKG2D-deficient mice are defective in tumor surveillance in models of spontaneous malignancy. Immunity 2008; 28: 571-80.
11. Elboim M, Gazit R, Gur C, Ghadially H, Betser-Cohen G, Mandelboim O. Tumor immunoediting by NKp46. J Immunol 2010; 184: 5637-44.
12. Smyth MJ, Swann J, Cretney E, Zerafa N, Yokoyama WM, Hayakawa Y. NKG2D function protects the host from tumor initiation. J Exp Med 2005; 202: 583-8.
13. Imai K, Matsuyama S, Miyake S, Suga K, Nakachi K. Natural cytotoxic activity of peripheral-blood lymphocytes and cancer incidence: an 11-year follow-up study of a general population. Lancet 2000; 356: 1795-9.
14. Brandt CS, Baratin M, Yi EC, Kennedy J, Gao Z, Fox B, et al. The B7 family member B7-H6 is a tumor cell lig-and for the activating natural killer cell receptor NKp30 in humans. J Exp Med 2009; 206: 1495-503.
15. Eagle RA, Trowsdale J. Promiscuity and the single receptor: NKG2D. Nat Rev Immunol 2007; 7: 737-44.
16. Zwirner NW, Fuertes MB, Girart MV, Domaica CI, Rossi LE. Cytokine-driven regulation of NK cell functions in tumor immunity: role of the MICA-NKG2D system. Cy-tokine & Growth Factor Rev 2007; 18:159-70.
17. Pende D, Spaggiari GM, Marcenaro S, Martini S, Rivera P, Capobianco A, et al. Analysis of the receptor-ligand interactions in the natural killer-mediated lysis of freshly isolated myeloid or lymphoblastic leukemias: evidence for the involvement of the Poliovirus receptor (CD155) and Nectin-2 (CD112). Blood 2005; 105: 2066-73.
18. El-Sherbiny YM, Meade JL, Holmes TD, McGonagle D, Mackie SL, Morgan AW, et al. The requirement for DNAM-1, NKG2D, and NKp46 in the natural killer cell-mediated killing of myeloma cells. Cancer Res 2007; 67: 8444-9.
19. Iguchi-Manaka A, Kai H, Yamashita Y, Shibata K, Tahara-Hanaoka S, Honda S, et al. Accelerated tumor growth in mice deficient in DNAM-1 receptor. J Exp Med 2008; 205: 2959-64.
20. Groh V, Wu J, Yee C, Spies T. Tumour-derived soluble MIC ligands impair expression of NKG2D and T-cell activation. Nature 2002; 419: 734-8.
21. Fuertes MB, Girart MV, Molinero LL, Domaica CI, Rossi LE, Barrio MM, et al. Intracellular retention of the NKG2D ligand MHC class I chain-related gene A in human melanomas confers immune privilege and prevents NK cell-mediated cytotoxicity. J Immunol 2008; 180: 4606-14.
22. Carlsten M, Norell H, Bryceson YT, Poschke I, Sched-vins K, Ljunggren HG, et al. Primary human tumor cells expressing CD155 impair tumor targeting by down-regulating DNAM-1 on NK cells. J Immunol 2009; 183:4921-30.
23. Terme M, Ullrich E, Delahaye NF, Chaput N, Zitvogel L. Natural killer cell-directed therapies: moving from unexpected results to successful strategies. Nat Immunol 2008; 9: 486-94.
24. Girart MV, Fuertes MB, Domaica CI, Rossi LE, Zwirner NW. Engagement of TLR3, TLR7, and NKG2D regulate IFN-gamma secretion but not NKG2D-mediated cyto-toxicity by human NK cells stimulated with suboptimal doses of IL-12. J Immunol 2007; 179: 3472-9.
25. Ghiringhelli F, Menard C, Terme M, Flament C, Taieb J, Chaput N, et al. CD4+CD25+ regulatory T cells inhibit natural killer cell functions in a transforming growth factor-beta-dependent manner. J Exp Med 2005; 202: 1075-85.
26. Dunn GP, Bruce AT, Ikeda H, Old LJ, Schreiber RD. Cancer immunoediting: from immunosurveillance to tumor escape. Nat Immunol 2002; 3: 991-8.
27. Rabinovich GA, Sotomayor E, Gabrilovich D. Immuno-suppressive Strategies that Are Mediated by Tumor Cells. Ann Rev Immunol 2007; 25: 267-96.
28. Domaica CI, Fuertes MB, Rossi LE, Girart MV, Avila DE, Rabinovich GA, et al. Tumour-experienced T cells promote NK cell activity through trogocytosis of NKG2D and NKp46 ligands. EMBO Rep 2009; 10: 908-15.
29. Bolden JE, Peart MJ, Johnstone RW. Anticancer activities of histone deacetylase inhibitors. Nat Rev Drug Dis-cov 2006; 5: 769-84.
30. Lane AA, Chabner BA. Histone deacetylase inhibitors in cancer therapy. J Clin Oncol 2009; 27: 5459-68.
31. Minucci S, Pelicci PG. Histone deacetylase inhibitors and the promise of epigenetic (and more) treatments for cancer. Nat Rev Cancer 2006; 6: 38-51.
32. Kato N, Tanaka J, Sugita J, Toubai T, Miura Y, Ibata M, et al. Regulation of the expression of MHC class I-related chain A, B (MICA, MICB) via chromatin remodeling and its impact on the susceptibility of leukemic cells to the cytotoxicity of NKG2D-expressing cells. Leukemia 2007; 21: 2103-8.
LABORATORIO DE BIOQUÍMICA NEUROENDOCRINA
Desarrollo de estrategias terapéuticas basadas en esteroides neuroactivos y neuroesteroides para el tratamiento de neuropatologías experimentales
Development of therapies based on neuroactive steroids and neurosteroids for the treatment of experimental neuropathologies
Desenvolvimento de estratégias terapêuticas baseadas em esteroides neuroativos e neuroesteroides para o tratamento de neuropatologias experimentais
Alejandro F. De Nicola, Juan Beauquis, Florencia Coronel, Laura I. Garay, Maria Claudia Gonzalez Deniselle, Susana L. Gonzalez, Florencia Labombarda, Luciana Pietranera, Flavia E. Saravia; Maria Meyer, Gisella Gargiulo, Elvira Brocca, Lydia van Overveld, Analia Lima, Paulina Roig
Resumen
Los esteroides activos en el sistema nervioso ("neuroactivos") ejercen actividades neuroprotectoras o neurotóxicas, dependiendo de su estructura química, de las concentraciones circulantes o tisulares, del tipo de receptores intervinientes y de los mecanismos de señalización intracelular empleados. Estas propiedades han sido estudiadas en modelos animales de neuropatologías humanas. Bajo condiciones experimentales que remedan el traumatismo de la médula espinal, dolor neuropático, esclerosis múltiple y esclerosis lateral amiotrófica, el tratamiento con progesterona produjo beneficios terapéuticos relacionados con la neuroprotección, re-mielinización e inhibición de la neuroinflamación. Por otra parte, estudios realizados en animales hipertensos demuestran una pronunciada encefalopatía en cuya etiopatogenia interviene la hiperfunción del sistema mineralocorticoide, ya que similares anormalidades neuroquímicas aparecen en animales normales tratados con mineralocorticoides. Por consiguiente, la neurotoxicidad podría ser consecuencia de la hi-peractividad del sistema mineralocorticoide. La encefalopatía de la hipertensión es similar a la de la diabetes mellitus y a la del cerebro añoso. En los tres casos, los estrógenos actúan como agentes neuroprotectores, promoviendo la neurogéne-sis hipocampal, la expresión de factores neurotróficos y disminuyendo la astrogliosis, confirmándose la plasticidad del sistema nervioso al estímulo estrogénico. Por consiguiente, el empleo de esteroides neuroactivos en modelos animales hace factible la transferencia a corto plazo de los resultados experimentales a la clínica humana.
Palabras clave: diabetes mellitus; dolor neuropático; encefalopatía hipertensiva; esclerosis lateral amiotrófica; esclerosis múltiple; esteroides neuroactivos; neuroesteroides; trauma de médula espinal.
Summary
Steroids showing activity on the nervous system are known as "neuroactive steroids". They exert neuroprotective or neu-rotoxic activities, depending on their chemical structure, circulating or tissue concentrations, binding to different receptors and the mechanisms of intracellular signalling employed. In order to elucidate these properties, work was performed on animal models of human neuropathologies, including spinal cord injury, neuropathic pain, multiple sclerosis, and amy-otrophic lateral sclerosis. In these models, treatment with progesterone has shown great therapeutic effectiveness. In another set of studies, it was shown that hypertensive animals bear a pronounced encephalopathy, possibly caused by an overdrive of the mineralocorticoid system. It has been suggested that overdrive of the mineralocorticoid system plays a neurotoxic role, based on the development of similar brain abnormalities following mineralocorticoid treatment of otherwise normal animals. Hypertensive encephalopathy is similar to that developed by diabetes mellitus and aging animals. In the three cases, estrogen treatment provided strong neuroprotection, as shown by enhanced hippocampal neu-rogenesis, increased neurotrophic factor expression and decreased astrogliosis. Thus, the use of estrogens supports the regenerative capacity and plasticity of the nervous system. Therefore, animal models become useful tools to transfer experimental data to the human patient in the short-term.
Key words: diabetes mellitus; neuropathic pain; hypertensive encephalopathy; amyotrophic lateral sclerosis; multiple sclerosis; neuroactive steroids; neurosteroids; spinal cord trauma.
Resumo
Os esteroides ativos no sistema nervoso ("neuroativos") exercem atividades neuroprotetoras ou neurotóxicas, de-pendendo de sua estrutura química, das concentrações circulantes ou tissulares, do tipo de receptores intervenientes e dos mecanismos de sinalização intracelular utilizados. Estas propriedades têm sido estudadas em modelos animais de neuropatologias humanas. Sob condições experimentais que remedam o traumatismo da medula espinal, dor neuro-pática, esclerose múltipla e esclerose lateral amiotrófica, o tratamento com progesterona produziu benefícios terapêu-ticos relacionados com a neuroproteção, remielinização e ini-bição da neuroinflamação. Por outra parte, estudos realizados em animais hipertensos demonstram uma pronunciada encefalopatia em cuja etiopatogenia intervém a hiperfunção do sistema mineralocorticoide, visto que similares anormalidades neuroquímicas aparecem em animais normais tratados com mineralocorticoides. Por conseguinte, a neuroto-xicidade poderia ser consequência da hiperatividade do sistema mineralocorticoide. A encefalopatia da hipertensão é similar à da diabetes mellitus e à do cérebro idoso. Nos três casos, os estrogênios atuam como agentes neuroprotetores, promovendo a neurogênese hipocampal, a expressão de fa-tores neurotróficos e diminuindo a astrogliose, confirmando-se a plasticidade do sistema nervoso ao estímulo estrogênico. Por conseguinte, o emprego de esteroides neuroativos em modelos animais torna fatível a transferência em curto prazo dos resultados experimentais para a clínica humana.
Palavras chave: diabetes mellitus; dor neuropática; ence-falopatia hipertensiva; esclerose lateral amiotrófica; escle-rose múltipla; esteroides neuroativos; neuroesteroides; trauma de medula espinhal.
1) La progesterona ejerce efectos neuroprotectores en diversas enfermedades del sistema nervioso central y periférico:
Los estudios clásicos consideraron a la progesterona como una hormona relacionada con la ovulación, preñez y comportamiento sexual. Sin embargo, ya en 1941 Hans Selye había demostrado que poseía propiedades anestésicas, mientras finalmente Baulieu y colaboradores (1) describieron que además de actuar como un es-teroide neuroactivo, se producia localmente en el sistema nervioso, acuñando el término "neuroesteroide". Actualmente, la progesterona es reconocida por sus acciones mielinizantes y neuroprotectoras luego de la injuria del sistema nervioso central, en la neurodegene-ración, neuroinflamación y como calmante del dolor neuropático. La progesterona ejerce estas propiedades actuando sobre todas las poblaciones celulares del sistema nervioso central, es decir neuronas, oligodendro-citos, astrocitos y microglia.. Entre numerosos ejemplos, describiremos las acciones de la progesterona en la lesión de la medula espinal, en un modelo inducido de esclerosis múltiple, en un modelo genético de degeneración de motoneurona y en el dolor neuropático experimental (2).
Como resultado de una lesión de la médula espinal producida en la rata, las motoneuronas del asta ventral degeneran por un proceso denominado cromatólisis, por el cual la sustancia de Nissl (ribonucleoproteínas) se agolpa en la membrana plasmática dándole un aspecto atigrado a la neurona.. La cromatólisis, que es un proceso reversible al contrario de la apoptosis, cursa con disminución de la expresión de moléculas fundamentales para el funcionamiento neuronal, incluyendo factores neurotróficos, enzimas de la neurotransmisión y la bomba de sodio que mantienen el potencial de membrana. Asimismo, se descontrola la actividad de la glia (astrocitos, microglia ) y de los progenitores de oli-godendrocitos (OPC). La lesión medular produce des-mielinización con disminución de las proteinas centrales de la mielina y de los factores de transcripcion de la mielina central, mientras que los OPC proliferantes no se diferencian a oligodendrocitos maduros productores de mielina. Los astrocitos y microglia reactivos produced sustancias proinflamatorias y tóxicas para las neuronas, acentuando la desmielinización y neurodegene-ración.
Es altamente auspicioso comprobar que la administración in vivo de progesterona a ratas por períodos entre 3 a 21 dias revierte las anormalidades debidas a la lesión de la médula espinal. Por ejemplo, disminuye la cromatólisis neuronal, estimula la proliferación de los OPC e induce su diferenciación y maduración para sintetizar mielina. El tratamiento agudo con progesterona inhibe la proliferación de astrocitos y microglía, mientras que su continuación por 21 días inhibe la activación de estos tipos gliales. En conclusión, la administración de progesterona luego del trauma de la medula espinal inhibe la astrogliosis y microgliosis, ejerce efectos antiinflamatorios por inhibición de la microglia y de las ci-toquinas proinflamatorias, favorece la remielinización a partir de la proliferación de OPC y su diferenciación a células capaces de generar mielina; y previene la degeneración neuronal. Por consiguiente, la progeste-rona constituye un arma terapéutica importante para las lesiones de la médula espinal (3)( 4).
Las acciones anti-inflamatorias e inmunomodulatorias de la progesterone se han explorado con profundidad en modelos animales de enfermedades autoinmunes. Estos estudios se basaron en conocidas observaciones clínicas en mujeres embarazadas que padecían de esclerosis múltiple (EM). La EM es una enfermedad autoinmune que ataca la mielina, y en mujeres embarazadas los relapsos de la enfermedad remiten en el 3º trimestre, debido a los altos niveles de esteroides sexuales circulantes. Para explicar este hallazgo clínico, se ha empleado un modelo experimental denominado encefalomielitis autoinmune experimental (EAE), por el cual ratones son inmunizados con un péptido de la mielina llamado MOG (myelin oligodendrocyte glycoprotein). Estos ratones desarrollan signos clínicos tales como pérdida de la tonicidad de la cola, espasticidad, parálisis de miembros posteriores, etc. A nivel neuroquimico, la médula espinal sufre de infiltración linfocitaria y macrofágica, des-mielinización en focos con disminución de las proteínas centrales de la mielina : MBP (proteína básica de la mielina) y PLP (proteolípido proteína), se desarrolla as-trogliosis y aparecen lesiones y pérdida de axones además de cambios degenerativos de las neuronas. El pre-tratamiento con progesterona de estos animales produjo resultados espectaculares, tales como el retardo en la aparición de la enfermedad y la atenuación del grado clínico. A nivel de la médula espinal, la progesterona produjo marcado descenso de la desmielini-zación, demostrada por la mayor expresión de MBP y PLP, menor infiltración macrófagica y de células del sistema inmune, y disminución de la astrogliosis (5). Asimismo, la progesterona ejerce poderosos efectos antiinflamatorios locales, disminuyendo la expresión de los ARN mensajeros del factor de necrosis tumoral alfa (TNFα), interleuquina 1α y del marcador de microglia C11b determinados por reacción de la polimerasa en tiempo real (6). En la EAE, los efectos de la progeste-rona incluyen: neuroprotección y promielinización de la médula espinal, además de suprimir la respuesta inmune. Teniendo en cuenta que los efectos de proges-terona podrían ser sistémicos por supresión del sistema inmune periférico, se realizaron nuevos estudios empleando un modelo focal de desmielinización por inyección intraespinal de la gliotoxina lisolecitina. Los resultados fueron similares a los obtenidos con el modelo EAE, lo que sugiere que las acciones de la progesterona son en parte independientes del sistema inmune sisté-mico. Los datos resultan importantes por su aplicación la clínica. En este sentido, un estudio multicéntrico europeo (POPART-MUS) emplea actualmente la proges-terona, en agregado a estrógenos, para prevenir los relapsos post-parto de mujeres con EM.
En agregado a los ejemplos mencionados anteriormente, el rol protector de la progesterona se extiende también a un modelo de neurodegeneración de moto-neurona y a humanos que padecen de esclerosis lateral amiotrófica (ELA). La ELA es una enfermedad crónica que afecta las motoneuronas espinales y bulbares, siendo la sobrevida inferior a 5 años. Existen varios modelos de ELA, uno de ellos es el ratón Wobbler, que presenta una mutación de la proteína de tráfico intracelu-lar Vps54. En las motoneuronas espinales, se observa degeneración no apoptótica, con extensa vacuolización debida al aumento del estrés oxidativo. La expresión de moléculas tales como el factor neurotrofico derivado del cerebro (BDNF) se encuentra disminuída en Wobblers en estadio clíni co sintomático, mientras que la proges-terona corrige esta deficiencia (7). Estudios posteriores se desarrollaron en ratones Wobblers genotipificados wr/wr de 3 estadios: progresivo temprano (1-2 meses), establecido (5-8 meses) y tardio (12 meses) y controles NFR/NFR de edades similares. La mitad de cada grupo recibió progesterona por 3 semanas. Los estudios in-ciales evaluaron la vacuolización de motoneuronas, la expresión del ARNm para BDNF, y parámetros gliales tales como la densidad de astrocitos, la expresión de la enzima detoxificante del glutamato -glutamina sintetasa-y el número de oligodendrocitos en los diversos estadíos evolutivos de la enfermedad. El tratamiento con pro-gesterona de Wobblers disminuyó la degeneración va-cuolar en todos los estadios, elevó la expresión del BDNF en los estadios establecido y tardio, disminuyo la astrogliosis y aumentó la densidad de oligodendrocitos maduros y de células que expresaban glutamina sinte-tasa (8). Funcionalmente, el tratamiento prolongado con progesterona mejoró la fuerza muscular y la sobrevida de los Wobblers. Los resultados han sido extrapolados en cierta medida a humanos con ELA. Esta enfermedad es habitualmente tratada con riluzole, un fármaco antiglutamatérgico. Dados los datos que demostraban las acciones neuroprotectora de progeste-rona en el Wobbler, se evaluó la utilidad de la misma en pacientes con ELA. El dosaje de esteroides en sangre demostró que la sobrevida se asociaba positivamente a los niveles más elevados de progesterona, al contrario de lo que ocurría con el cortisol plasmático. Asimismo, en forma preliminar se ha podido demostramos que la terapia combinada con riluzole + progesterona mostró una tendencia a prolongar la sobrevida con baja probabilidad de efectos adversos (9).
Las acciones protectoras y antiinflamatorias de la progesterona no se circunscriben al sistema nervioso central sino que también abarcan al periférico. La Asociación Internacional para el Estudio del Dolor (IASP, por sus siglas en inglés), define al dolor neuropático como aquel dolor causado por una lesión o enfermedad del sistema nervioso, ya sea periférico o central. Es un dolor crónico, severo, y refractario a los tratamientos farmacológicos disponibles, lo que motiva el diseño de nuevas estrategias terapéuticas. Existen modelos experimentales de lesión espinal o de nervios periféricos, que reproducen las características principales de la condición clínica en humanos y permiten explorar las alteraciones neuroquímicas, celulares y moleculares del dolor neuropático. De hecho, más del 60% de los pacientes con trauma directo o disfunción espinal desarrolla dolor neuropático de difícil tratamiento. Asimismo, el modelo de compresión del nervio ciático representa la causa más frecuente de neuropatía periférica, generalmente debida a injuria física de los nervios, por caídas, accidentes automovilísticos, actividades deportivas, o hernia discal, que provocan atrapamiento o compresión de los nervios afectados. Si bien numerosos mecanismos participan en la génesis y el mantenimiento del dolor crónico, la activación sostenida de los sistemas nociceptivos espinales juega un rol crucial. Existen datos experimentales que describen las alteraciones temporales que ocurren en la expresión de moléculas clave en el proceso de sensibilización central a nivel espinal, entre ellas el receptor NMDA, la isoforma gamma de la proteína kinasa C (PKCγ), la dinorfina y el receptor kappa opioide. Se parte de la hipótesis que parte de estos mecanismos podrían ser un blanco de modulación por esteroides neuroactivos, abriendo la posibilidad de una nueva perspectiva terapéutica. Más recientemente, se ha demostrado que la progesterona previene el desarrollo de la conducta nociceptiva en los modelos experimentales, a la vez que modula la expresión de las moléculas antes mencionadas. El panorama molecular y celular observado luego de la administración de progesterona permitiría explicar, aunque sea en parte, las acciones analgésicas del esteroide luego de la injuria. Por consiguiente, se han conseguido avances en el conocimiento de los mecanismos involucrados en el desarrollo del dolor neu-ropático y en el valor de la administración de progesterona como posible modulador del dolor crónico, a fin de contribuir al diseño de nuevas estrategias terapéuticas (10).
Finalmente, es preciso mencionar que los efectos descritos en los distintos modelos experimentales pueden originarse en mecanismos genómicos, a través del receptor nuclear clásico para progesterona (PR) que actúa como un factor regulador de la transcripción de genes blanco. Existen dos isoformas de PR, llamadas PRA y PRB. Asimismo, existe la posibilidad de efectos no genómicos, a través de receptores de membrana alternativos (mPR) de los cuales se han descrito 3 variedades: α, β y γ acoplados a proteína G, y un cuarto receptor de membrana denominado 25 DX, fuertemente expresado en el asta dorsal de la medula espinal. Para complicar más el panorama, la progesterona puede reducirse a dos metabolitos, uno con capacidad de unión al RP, la 5-dihidroprogesterona, y otro que actúa como agonista del receptor GABAa, la tetrahidroprogeste-rona (alopregnanolona). Ambos ejercen acciones neu-roprotectoras. Como puede apreciarse, son múltiples los mecanismos e intermediarios de la acción de este esteroide pleiotrópico, la progesterona (2) a nivel de la médula espinal y nervios periféricos.
El empleo a nivel clínico de la progesterona, además de lo ya detallado para la ELA, se ha realizado en casos de injuria traumática del cerebro (TBI, traumatic brain injury). Los trabajos de Stein y colaboradores (11) mostraron que la progesterona mostraba efectos neuro-protectores en humanos con TBI. Mientras que al principio esto se demostró en ensayos clínicos en fase II, actualmente existen en fase III en los EE.UU., Europa y Asia.
1) Los estrógenos son reconocidos como agentes neuroprotectores para las enfermedades del sistema nervioso asociadas al envejecimiento: diabetes e hipertensión arterial
De manera similar a lo expresado para la progesterona, los trabajos iniciales que señalaban a los estrógenos como las hormonas típicas que regulaban los fenómenos reproductivos, fueron seguidos por una avalancha de evidencias sobre el rol fundamental que juegan los estrógenos para la neuroprotección. Desde tiempos inmemoriales, se asociaron los estrógenos a la terapia de reemplazo hormonal del climaterio, aunque ciertas dudas sembradas al respecto hicieron retroceder su generalización (12). Sin embargo, hoy dia se re-evalúa el papel de los estrógenos en sus diversas formas, ya sean naturales como sintéticos y a los reguladores selectivos del receptor estrogénico (SERM), como los agentes de elección para el tratamiento del cerebro senil y los cambios que aparecen durante el climaterio (13). La hipótesis de la protección cerebral por los estrógenos se ha extendido a varias enfermedades neurodegenerativas y síndrome psiquiatricos, entre ellos el accidente cerebovascular agudo, la isquemia cerebral, esquizofrenia, enfermedades de Parkinson y Alzheimer, trastornos cognitivos leves, etc. (14). Sin embargo, es necesario reconocer que no existe consenso generalizado sobre si el tratamiento estrogénico en humanos está libre de efectos indeseables y si realmente provee efectos beneficiosos para las enfermedades neurológicas.
Los estrógenos actúan de diversas maneras en el sistema nervioso. Existen dos subtipos de receptores es-trogénicos clásicos, denominados ERalfa y ERbeta, producto de dos genes diferentes, aunque con similitud aminoacídica en los diferentes dominios. ERα y ERβ muestran una distribución diferente en el sistema nervioso. Por ejemplo, ERα se expresa mayormente en el núcleo arcuato y ventromediano del hipotálamo, mientras que el ERβ se concentra en el hipocampo, núcleos paraventricular y ventromediano del hipotálamo y en el area preóptica. Se han descrito receptores de membrana que unen estrógenos, tales como el receptor unido a proteína G (GCR30) que está acoplado a la activación rápida de la proteína quinasa activada por mi-tógenos (MAPK/ERK), el ERX especifico para el 17 α estradiol, y la interacción proteína/proteína entre el ERα y el receptor para el factor de crecimiento insulina-simil (15). La intervención de uno o varios de estos mecanismos llevaa al control, a nivel cellular, de la neuro-génesis, prevención de la muerte neuronal, aumento de la supervivencia neuronal y crecimiento de neuritas, prevención de la excitotoxicidad glutamatérgica, la estimulación de la sinaptogénesis y a los efectos antioxidantes y anti-inflamatorios (14)(16 ).
Un tema de gran actualidad es el empleo de la neu-roprotección estrogénica para las enfermedades neurodegenerativas que aparecen durante el envejecimiento, entra las que se halla la encefalopatía de la hipertensión arterial. La hipertensión arterial en el humano es causante no solamente de accidentes cerebrovaculares, sino también se asocia a una importante encefalopatia, que afecta al hipocampo. El hipocampo es una región cerebral importante para la memoria de corta duración, aprendizaje y la génesis de nuevas neuronas en el cerebro adulto. Un modelo de elección es la rata espontáneamente hipertensa (SHR) de causa poligénica, cuya encefalopatía cursa con atrofia cerebral y del hipocampo, hidrocefalia y pérdida de sustancia blanca (17). Asimismo, las SHR presentan disminución de la génesis de nuevas neuronas en el giro dentado, proliferación de as-trocitos y pérdida neuronal en el hilio del giro dentado del hipocampo. Estos cambios revierten luego del tratamiento con estradiol administrado in vivo (18). Como se sabe que el cerebro fabrica sus propios "neuroesteroides" luego del descubrimiento de Baulieu, también investigamos la expresión de aromatasa, enzima responsable de la síntesis endógena (local) de estradiol, pensando que la síntesis de estrógenos endógenos podria estar defectuosa en las ratas SHR. Se sabía que la enzima aromatasa se expresa en el sistema nervioso particularmente en el hipocampo, está involucrada en la regulación de la plasticidad neuronal, se le reconoce un efecto neuroprotec-tor y su expresión aumenta en respuesta a la injuria. Lo que resultó una verdadera sorpresa, fue la observación que la expresión del gen de la aromatasa determinada por reacción en cadena de la polimerasa en tiempo real, y la determinación de la proteína por inmunohistoqui-mica, estaba aumentada en los animales SHR. Lo interesante fue comprobar que las SHR mostraban un aumento posterior de la aromatasa cuando se trataban con estradiol. Concluimos que los estrógenos exógenos y los localmente producidos por la aromatasa actuarían en conjunto ejerciendo efectos neuroprotectores sobre la encefalopatía hipertensiva, aumentando la génesis de nuevas neuronas necesarias para incorporar nuevas memorias y aprendizajes, y para el correcto funcionamiento neuroendócrino del hipocampo (19).
En forma similar a la hipertensión arterial, la diabetes mellitus afecta múltiples sistemas entre los que se encuentra el sistema nervioso central, siendo el hipocampo una de las estructuras más vulnerables. En forma semejante a lo descrito para los mineralocorticoides en ratas SHR, los glucocorticoides resultaron ser esteroides moduladores negativos (neurotóxicos) para la proliferación celular en el giro dentado del hipocampo. Esto se debía a que la corticosterona plasmática resultó elevada, el ritmo circadiano estaba ausente y la respuesta de la adrenal a la ACTH in vitro se encontraba aumentada, convirtiendo a la sobreactivación del sistema glucocor-ticoide en un factor responsable de la encefalopatía de la diabetes mellitus. Esta hipótesis se comprobó mediante la administración del antagonista del receptor para glucocorticoides (GR) conocido como RU486 o Mi-fepristone. Se determinó la proliferación celular en el giro dentado mediante inmunomarcación para Ki67 y se encontró una disminución en los animales diabéticos y una recuperación por el tratamiento con RU486. La diferenciación de las nuevas células hacia neuronas se estudió por inmunofluorescencia para bromodesoxiuri-dina y microscopía confocal. En los animales diabéticos se encontró una menor diferenciación y el RU486 logró una reversión hacia valores controles, lo cual apoyaba el papel neurotóxico de los glucocorticoides sobre la neu-rogénesis hipocampal (20). El sistema, sin embargo, resultó ser altamente plástico y con capacidad de recuperación por tratamiento estrogénico. Mediante el tratamiento con estradiol por un plazo de 10 dias, se revertió completamente la reducción de la proliferación celular del ratón diabético. Al mismo, tiempo, las neuronas del hilio del giro dentado volvieron a valores normales, asi como la densidad de los astrocitos volvió a niveles controles. Fue interesante constatar que la administración de estrógenos no alteró el estado hiperglicémico de los animales ni tampoco la tasa proliferativa neuronal en los controles. Por consiguiente, comprobamos el valor de los estrógenos como una herramienta adicional para el tratamiento de los trastornos cerebrales de la diabetes mellitus (21). Podemos concluir que la maquinaria celular puesta en marcha durante la protección estrogé-nica en las enfermedades asociadas al envejecimiento es intrinsicamente compleja y podría mostrar distintas modalidades dependientes de la patología pre-existente. A nivel celular, sin embargo, son varias las funciones deficitarias en el envejecimiento, hipertensión arterial y diabetes mellitus cuyo denominador común es la respuesta positiva a los esteroides neuroactivos con estructura es-trogénica.
RECONOCIMIENTOS
Los trabajos del Laboratorio de Bioquímica Neuroendocrina han recibido apoyo económico del CONICET (PIP # 112-200801-00542), Proyecto Santaló (CONICET/CSIC), Convenio de Cooperación Internacional INSERM/CONICET, Universidad de Buenos Aires (20020100100089 y M614), y PICT 2007 01044.
Referencias bibliográficas
1. Baulieu EE, Robel P, Schumacher M. Neurosteroids: beginning of the story. Int Rev Neurobiol 2001; 46: 1-32.
2. De Nicola AF, Labombarda F, Gonzalez Deniselle MC, Gonzalez SL, Garay L, Meyer M, Guennoun R, Schumacher M. Progesterone neuroprotection in traumatic CNS injury and motoneuron degeneration. Front Neu-roendocrinol 2009 ; 30: 173-187.
3. Labombarda F, González SL, Lima A, Roig P, Guennoun R, Schumacher M, De Nicola AF. Effects of progesterone on oligodendrocyte progenitors, oligodendrocyte transcription factors, and myelin proteins following spinal cord injury. Glia 2009; 57: 884-97.
4. Labombarda F, González S, Lima A, Roig P, Guennoun R, Schumacher M, De Nicola AF. Progesterone attenuates astro- and microgliosis and enhances oligodendro-cyte differentiation following spinal cord injury. Exp Neurol 2011; 231: 135-46.
5. Garay L, Gonzalez Deniselle MC, Meyer M, Costa JJ, Lima A, Roig P, et al. Protective effects of progesterone administration on axonal pathology in mice with experimental autoimmune encephalomyelitis. Brain Res 2009; 1283: 177-85.
6. Garay L, Tuengler V, Deniselle MC, Lima A, Roig P, De Nicola AF. Progesterone attenuates demyelination and microglial reaction in the lysolecithin-injured spinal cord. Neuroscience 2011; 192: 588-97.
7. Gonzalez Deniselle MC, Garay L, Gonzalez S, Saravia F, Labombarda F, Guennoun R, et al. Progesterone modulates brain-derived neurotrophic factor and choline acetyltransferase in degenerating Wobbler motoneu-rons. Exp Neurol 2007; 203: 406-14.
8. Meyer M, Gonzalez Deniselle MC, Garay LI, Monachelli GG, Lima A, Roig P, et al. Stage dependent effects of progesterone on motoneurons and glial cells of wobbler mouse spinal cord degeneration. Cell Mol Neurobiol 2010; 30: 123-35.
9. Gargiulo Monachelli G, Meyer M, Rodríguez GE, Garay LI, Sica RE, De Nicola AF, et al. Endogenous progesterone is associated to amyotrophic lateral sclerosis prognostic factors. Acta Neurol Scand 2011; 123: 60-7.
10. Coronel MF, Labombarda F, Villar MJ, De Nicola AF, González SL. Progesterone prevents allodynia after experimental spinal cord injury. J Pain 2011; 12: 71-83.
11. Stein DG. Progesterone exerts neuroprotective effects after brain injury. Brain Res Rev 2008; 57: 386-97.
12. Resnick SM, Coker LH, Maki PM, Rapp SR, Espeland MA, Shumaker SA. The Women's Health Initiative Study of Cognitive Aging (WHISCA): a randomized clinical trial of the effects of hormone therapy on age-associated cognitive decline. Clin Trials 2004; 1: 440-50.
13. Arevalo MA, Santos-Galindo M, Lagunas N, Azcoitia I, Garcia-Segura LM. Selective estrogen receptor modulators as brain therapeutic agents. J Mol Endocrinol 2011; 46: R1-R9.
14. Behl C. Oestrogen as a neuroprotective hormone. Nat. Rev Neurosci 2002; 3: 433-42.
15. Garcia-Segura LM, Azcoitia, I, Don Carlos LL. Neuropro-tection by estradiol. Prog Neurobiol 2001; 63: 29-60.
16. Manthey D, Behl C. From structural biochemistry to expression profiling: Neuroprotective activities of estrogen. Neuroscience 2006; 138: 845-50.
17. Amenta F, Tayebati SK, Tomassoni D. Spontaneously hypertensive rat neuroanatomy: applications to pharmacological research. Ital J Anat Embryol 2010; 115: 13-7.
18. Pietranera L, Lima A, Roig P, De Nicola AF. Involvement of brain-derived neurotrophic factor and neurogenesis in oestradiol neuroprotection of the hippocampus of hypertensive rats. J Neuroendocrinol 2010; 22 :1082-92.
19. Pietranera L, Bellini MJ, Arévalo MA, Goya R, Brocca ME, Garcia-Segura LM, et al. Increased aromatase expression in the hippocampus of spontaneously hypertensive rats: effects of estradiol administration. Neuro-science 2011; 174:151-9.
20. Revsin Y, Rekers NV, Louwe MC, Saravia FE, De Nicola AF, de Kloet ER, et al. Glucocorticoid receptor blockade normalizes hippocampal alterations and cognitive impairment in streptozotocin-induced type 1 diabetes mice. Neuropsychopharmacology 2009; 34: 747-58.
21. Saravia F, Beauquis J, Pietranera L, De Nicola AF. Neu-roprotective effects of estradiol in hippocampal neurons and glia of middle age mice. Psychoneuroendocrinology 2007; 32: 480-92.
LABORATORIO DE NEUROENDOCRINOLOGÍA
Alteraciones neuroendocrinas causadas por disruptores endocrinos: el ejemplo del Bisfenol A
Neuroendocrine alterations by endocrine disruptors: the example of Bisphenol A
Alterações neuroendócrinas causadas por disruptores endócrinos: o exemplo do Bisfenol A
Nadia Bourguignon1, Marina Fernández1,2, Victoria Lux-Lantos1, Carlos Libertun1,2
1 Instituto de Biología y Medicina Experimental, Consejo Nacional de Investigaciones Científicas y Técnicas, Buenos Aires, Argentina;
2 Facultad de Medicina, Universidad de Buenos Aires, Argentina
Resumen
Los contaminantes ambientales, como los disruptores endocrinos, podrían provocar profundos cambios en los seres vivos. Aquí se analizan las alteraciones neuroendocrinas y reproductivas en mamíferos, incluyendo las descriptas en humanos, causadas por una molécula de origen industrial, el Bisfenol A.
Palabras clave: xenoestrógenos; Bisfenol A; neuroendo-crinos; reproducción.
Summary
Exposure to endocrine disruptors may produce profound alterations in several species. As an example, the neuroen-docrine and reproductive alterations due to Bisphenol A in mammals are summarized here.
Key words: xenoestrogen; Bisphenol A; neuroendocrine; reproduction.
Resumo
Os contaminantes ambientais, como os disruptores endó-crinos, poderiam provocar profundas alterações nos seres vivos. Aqui são analisadas as alterações neuroendócrinas e re-produtivas em mamíferos, incluindo as descritas em humanos, causadas por uma molécula de origem industrial, o Bisfenol A.
Palavras chaves: xenoestrógenos; Bisfenol A; neuroendó-crinos; reprodução.
El conocimiento de las acciones que los contaminantes ambientales ejercen sobre los seres vivos es de importancia vital. Su estudio, en extensión y en profundidad, es crítico para la salud animal y vegetal, para conservar la biodiversidad y esencial para la salud humana. Aquellos que afectan al sistema hormonal se los conoce como disruptores endocrinos y se los define como "agentes exógenos que interfieren con la síntesis, secreción, transporte, unión, acción o eliminación de las hormonas naturales que son responsables de mantener la homeostasis, reproducción, desarrollo y/o conducta del individuo" (1)(2). Entre los disruptores endocrinos se hallan los xenoestrógenos, compuestos que mimetizan las acciones de los estrógenos naturales. Los Xenoestrógenos hallados naturalmente en vegetales como la soja y ciertas legumbres, fitoes-trógenos, son capaces de interferir con los estrógenos endógenos. Se les han atribuidos ciertos efectos benéficos para la salud humana a los fitoestrógenos, por ejemplo en ciertos estudios epidemiológicos, disminución de la sintomatología menopáusica o disminución de la incidencia de ciertos tumores. Existe un segundo grupo de xenoestrógenos, producto de actividad industrial humana, al que se le han atribuido acciones mayormente nocivas. El Bisfenol A (BPA) es producido en todo el mundo en grandes cantidades industriales, Es un constituyente de los plásticos poli-cabonatados y resinas epoxy utilizados en la industria y en odontología. Los polímeros se hidrolizan a alta temperatura y liberan BPA. Cantidades de BPA son ingeridas por humanos en sólidos y en el agua de bebida, ya que cantidades detectables del mismo fueron halladas en latas de alimentos, contenedores para mi-croondas, botellas y biberones plásticos, accesorios de uso médico de policarbonato, selladores dentales, entre otros objetos de uso diario y distribución universal. BPA fue encontrado en aguas de ríos, lagos y mares.
En humanos, cantidades claramente detectables de BPA fueron halladas en saliva, sangre, cordón umbilical, calostro y leche materna. Se estima que la exposición diaria de los recién nacidos e infantes de hasta 6 meses depende del esquemas de alimentación, siendo menor con alimentación natural que con alimentación por fórmulas comerciales en biberón plástico (3 - 5)
Los efectos del BPA, como los de otros xenoestró-genos, son condicionados por la especie, dosis y rutas de administración, tiempo de exposición y en gran medida por la edad del organismo expuesto, como lo indican estudios experimentales. Los adultos son en general más resistentes a ciertos efectos adversos y en algunos casos los mismos son reversibles al suspenderse la exposición (6). En cambio la exposición perinatal in útero, o neonatal, al actuar durante el periodo organizacional, puede provocar efectos profundos, persistentes e irreversibles en ratas (7-11).
En general, muchos de los efectos permanentes coinciden con aquellos descriptos para los estrógenos naturales cuando actúan durante el desarrollo sobre, por ejemplo, la diferenciación sexual encéfalo hipo-fisaria. Además de su actividad estrogénica, al BPA tiene otros efectos como antagonizar ciertas acciones de los propios estrógenos, andrógenos y hormonas tiroideas, actuar por vías no genómicas e influir sobre ciertas enzimas y expresión de algunos receptores (12).
En nuestros estudios, en el Instituto de Biología y Medicina Experimental, hallamos que el BPA actuando luego del nacimiento en la rata hembra, provoca cambios reproductivos e hipotálamo hipofisa-rios notorios a medida que el animal madura, tales como adelanto de la eclosión puberal, alteraciones del ciclo estral y de la pulsatilidad de la neurona GnRH, de la secreción gonadotrópica y de la respuesta de ciertos mensajeros intracelulares del gonadotropo en respuesta al GnRH (13). Más aún, en estas hembras expuesta al BPA al nacer, cuando llegan a la adultez hallamos en sangre testosterona y estrógenos elevados, baja progesterona, cambios en la estructura ová-rica, con múltiples quistes, y fertilidad disminuida remedando el sindrome de ovario poliquístico, patología de alta prevalencia en mujeres en edad reproductiva (14).
En resumen, el Bisfenol A es un xenostrógeno abundante en el medio ambiente, producto de la actividad humana, y cuyas acciones influyen grandemente sobre los seres vivos y la salud humana. Su efecto es más notorio cuando actúa a edades muy tempranas, el período organizativo perinatal, y persistentes a edades posteriores.
La importancia de este contaminante llevó a que recientemente varios países implementaran normas para restringir su uso y que los productos que contienen BPA lleven advertencias para los consumidores. De todas maneras los efectos de esta norma se considera que serán de utilidad en muchos años, por el alto contenido hoy presente de BPA en el hábitat y su lenta desaparición aún luego del cese de su producción. Su estudio podría ser guía sobre las investigaciones que imperiosamente debemos desarrollar sobre los contaminantes de nuestro ambiente.
Referencias bibliográficas
1. Daston GP, Cook JC, Kavlock RJ. Uncertainties for endocrine disrupters: our view on progress. Toxicol Sci 2003; 74: 245-52.
2. Diamanti-Kandarakis E, Bourguignon JP, Giudice LC, Hauser R, Prins GS, Soto AM, et al. Endocrine-disrupting chemicals: an Endocrine Society scientific statement. Endocr Rev 2009; 30: 293-342.
3. Calafat AM, Weuve J, Ye X, Jia LT, Hu H, Ringer S, et al. Exposure to bisphenol A and other phenols in neonatal intensive care unit premature infants. Environ Health Perspect 2009; 117: 639-44.
4. Edginton AN, Ritter L. Predicting plasma concentrations of bisphenol A in children younger than 2 years of age after typical feeding schedules, using a physiologically based toxicokinetic model. Environ Health Perspect 2009; 117: 645-52.
5. Vandenberg LN, Hauser R, Marcus M, Olea N, Welshons WV. Human exposure to bisphenol A (BPA). Reprod Tox-icol 2007; 24:139-77.
6. Richter CA, Birnbaum LS, Farabollini F, Newbold RR, Rubin BS, Talsness CE et al. In vivo effects of bisphe-nol A in laboratory rodent studies. Reprod Toxicol 2007; 24: 199-224.
7. Kato H, Ota T, Furuhashi T, Ohta Y, Iguchi T. Changes in reproductive organs of female rats treated with bisphenol A during the neonatal period. Reprod Toxicol 2003; 17: 283-8.
8. Moral R, Wang R, Russo IH, Lamartiniere CA, Pereira J, and Russo J. Effect of prenatal exposure to the endocrine disruptor bisphenol A on mammary gland morphology and gene expression signature. J Endocrinology 2008; 196: 101-12.
9. Patisaul HB, Fortino AE, Polston EK. Differential disruption of nuclear volume and neuronal phenotype in the preoptic area by neonatal exposure to genistein and bisphenol-A. Neurotoxicology 2007; 28: 1-12.
10. Ramos JG, Varayoud J, Kass L, Rodriguez H, Costabel L, Munoz-de-Toro M, et al. Bisphenol a induces both transient and permanent histofunctional alterations of the hypothalamic-pituitary-gonadal axis in prenatally exposed male rats. Endocrinology 2003; 144: 3206-15.
11. Khurana S, Ranmal S, Ben Jonathan N. Exposure of newborn male and female rats to environmental estrogens: delayed and sustained hyperprolactinemia and alterations in estrogen receptor expression. Endocrinology 2000; 141: 4512-7.
12. Wetherill YB, Akingbemi BT, Kanno J, McLachlan JA, Nadal A, Sonnenschein C et al. In vitro molecular mechanisms of bisphenol A action. Reprod Toxicol 2007; 24: 178-98.
13. Fernandez MO, Bianchi MS, Lux-Lantos VAR, Libertun C. Neonatal exposure to Bisphenol A alters reproductive parameters and Gonadotropin Releasing Hormone signaling in female rats. Environ Health Perspect 2009; 117(5): 757-62.
14. Fernandez MO, Bourguignon N, Lux-Lantos VAR, Li-bertun C. Neonatal exposure to bisphenol A and reproductive and endocrine alterations resembling the poly-cystic ovarian syndrome in adult rat. Environ Health Perspect 2010; 118(9): 1217-22.
LABORATORIO DE REGULACIÓN HIPOFISARIA
El receptor dopaminérgico D2: acciones endocrinas no clásicas
Non-conventional endocrine functions of dopamine type 2 receptor: new insights gained from transgenic mice
O receptor dopaminérgico D2: ações endócrinas não clássicas
Isabel Garcia Tornadú, María Victoria Recouvreux, Maria Cecilia Ramirez, María Guillermina Luque, Maria Ines Perez-Millan, Rodrigo Lorenzo, María Cristina Camilletti, Ana María Ornstein, Isabel Lacau-Mengido, Carolina Cristina, Graciela Diaz-Torga, Damasia Becu-Villalobos
Resumen
El receptor dopaminérgico D2 (RD2) participa en un complejo repertorio de funciones adaptativas para mejorar el desempeño del individuo, su éxito reproductivo y supervivencia. Utilizando estrategias combinadas de ensayos farmacológicos, líneas celulares y ratones transgénicos, nuestro laboratorio demostró la participación del RD2 no sólo en el desarrollo de prolactinomas, sino en el eje del crecimiento, la ingesta y el metabolismo de glucosa. Determinamos que el desarrollo de prolactinomas por ausencia de RD2 correlaciona con un aumento de VEGF y una disminución de TGFβ1 y su receptor TGFβ tipo II, po-sicionando estos factores como posible terapia complementaria en prolactinomas resistentes a agonistas dopa-minérgicos. En el eje de crecimiento, postulamos que la acción de RD2 facilita la liberación de GHRH, y la ausencia del receptor condiciona la población reducida de somatotropos, y produce enanismo. Respecto a la ingesta, los resultados indicaron que la ausencia de RD2 modula varios factores orexígenos y anorexígenos, revelando una mayor complejidad del sistema. Por último, demostramos que la dopamina a través del RD2 pancreático modula la liberación de insulina, esclareciendo en parte por qué el uso de antisicóticos conlleva a un desarrollo de diabetes tipo II. En conjunto nuestros resultados destacan la importancia de este receptor en acciones endocrinas no clásicas y su participación en forma integral en la fisiología del individuo.
Palabras clave: dopamina; prolactina; hormona del crecimiento; ingesta; glucosa; homeostasis.
Summary
Dopamine D2 receptors (D2R) participate in a complex system of adaptive functions to improve performance, reproductive success and survival of individuals.Using combined strategies with drug, cell lines and transgenic mice, our laboratory demonstrated that D2R take part, not only in the development of prolactinomas, but also in the regulation of the growth axis, food intake and glucose metabolism. It was determined that the development of prolactinomas due to the lack of D2R correlates with increased VEGF and decreased TGF β1 and TGF type II receptor, positioning these factors as potential targets in complementary therapies for dopamine agonist resistant prolactinomas. With regard to the growth axis, it was postulated that D2R facilitates the release of GHRH, and the absence of the receptor determines a decrease in the somatotroph population and produces dwarfism. Regarding food intake, it was demonstrated that the absence of D2R modulates several orexigenic and anorexigenic factors, pointing to a complexity of the system. Finally, it was shown that dopamine modulates insulin release through pancreatic D2R, partly clarifying why the use of antipsychotics leads to development of type II diabetes. Overall, our results highlight the importance of this receptor in non-classical endocrine actions and enable the understanding of the integral physiology of the D2R in homeostasis.
Key words: dopamine; prolactin; growth hormone; food intake; glucose; homeostasis.
Resumo
O receptor dopaminérgico D2 (RD2) participa num complexo repertório de funções adaptativas para melhorar o desem-penho do indivíduo, seu êxito reprodutivo e sobrevivência. Utilizando estratégias combinadas de ensaios farmacológicos, linhas celulares e camundongos transgênicos, nosso labora-tório demonstrou a participação do RD2 não só no desenvol-vimento de prolactinomas, mas no eixo do crescimento, a in-gestão e o metabolismo de glicose. Determinamos que o desenvolvimento de prolactinomas por ausência de RD2 correlaciona com um aumento de VEGF e uma diminuição de TGFβ1 e seu receptor TGFβtipo II, posicionando estes fa-tores como possível terapia complementar em prolactinomas resistentes a agonistas dopaminérgicos. No eixo de cresci-mento, postulamos que a ação de RD2 facilita a liberação de GHRH, e a ausência do receptor condiciona a população reduzida de somatotrofos, e produz nanismo. A respeito da ingestão, os resultados indicaram que a ausência de RD2 modula vários fatores orexígenos e anorexígenos, revelando uma maior complexidade do sistema. Por último, demonstramos que a dopamina através do RD2 pancreático modula a liberação de insulina, esclarecendo em parte por qué o uso de antipsicóticos leva a um desenvolvimento de diabetes tipo II. Em conjunto nossos resultados destacam a importância deste receptor em ações endócrinas não clássicas, e sua par-ticipação em forma integral na fisiologia do indivíduo.
Palavras chave: dopamina; prolactina; hormônio do cres-cimento; ingestão; glicose; homeostase.
A lo largo de la evolución el receptor dopaminérgico tipo 2 (RD2) ha participado en un complejo repertorio de funciones adaptativas para mejorar el desempeño del individuo, su éxito reproductivo y supervivencia. Diversos mecanismos que aumentan la probabilidad de consumir alimentos nutritivos y aparearse recurrentemente usan la estimulación de este subtipo de receptor. Los RD2 también son fundamentales en la coordinación motora, la actividad de locomoción, el planeamiento, la motivación o aversión y la dominancia social. La participación del RD2 en la función endocrina refuerza su papel en la reproducción y supervivencia.
Es bien conocido en la fisiología endocrina que el RD2 regula la hormona prolactina, pero su participación en el control de otras hormonas relacionadas al crecimiento, ingesta de alimentos o metabolismo de la glucosa no ha sido extensamente estudiada. En general, la relevancia del RD2 ha sido demostrada usando agentes farmacológicos con limitada especificidad in vivo, o en estudios in vitro que no permiten un análisis inte-grador fisiológico. Nosotros demostramos la participación de este receptor no sólo en el desarrollo de pro-lactinomas, sino también en el eje del crecimiento, la ingesta y el metabolismo de glucosa usando en forma combinada ensayos farmacológicos y ratones transgé-nicos con mutación nula del RD2 en todo el organismo.
La dopamina inhibe la síntesis, secreción de prolactina y la proliferación de lactotropos hipofisarios actuando a través del RD2. Nuestros primeros estudios se relacionaron a la tumorogénesis hipofisaria, sus mecanismos de control y las alteraciones producidas durante este proceso. En particular, los estudios se centralizaron en los prolactinomas, los tumores hipofisarios más frecuentes, dentro de los adenomas secretantes. Estos tumores se diferencian del resto de los tumores hipofisa-rios, pues en su mayoría son tratados exitosamente con agonistas dopaminérgicos logrando, en general, una rápida reducción del tamaño tumoral con liberación de los síntomas de compresión.
Sin embargo, en un 15% de los casos los prolactino-mas pueden ser resistentes a drogas dopaminérgicas y es necesario recurrir a la cirugía para su extirpación. La hiperprolactinemia producida por los prolactinomas afecta la reproducción, por lo que el abordaje terapéutico del prolactinoma tiene como objetivo revertir dichas manifestaciones, como así también las de tipo neurológico y/u oftalmológico provocadas por la expansión tumoral.
En pacientes con prolactinomas resistentes a drogas dopaminérgicas sigue abierta la búsqueda de nuevas terapéuticas.
Nosotros abordamos el estudio de prolactinomas resistentes desde varias perspectivas experimentales, analizando los posibles factores involucrados en el proceso de desarrollo y funcionalidad del tumor. Utilizamos diferentes modelos experimentales tales como líneas celulares tumorales, generación de tumores por tratamientos farmacológicos, y modelos de animales trans-génicos específicos. Por último, para tener una mayor comprensión del proceso patológico se realizaron estudios en tumores hipofisarios humanos.
Los ratones que carecen de la expresión del RD2, ratones Drd2-/- , desarrollan en forma espontánea hiper-prolactinemia seguida de hiperplasia de la hipófisis y finalmente un adenoma hipofisario. Este modelo experimental es útil para entender en parte lo que sucede en tumores hipofisarios resistentes a agentes do-paminérgicos (1).
Como ocurre para otros tipos de tumores, el crecimiento de los adenomas hipofisarios requiere de una adecuada vascularización una vez que el tumor sobrepasa unos pocos milímetros de tamaño. El factor de crecimiento del endotelio vascular, VEGF, es uno de los factores angiogénicos más potentes que se conocen. En ratones transgénicos Drd2-/- demostramos que existe un aumento de la expresión de VEGF en las hipófisis y que este aumento es regulado por la falta de acción dopami-nérgica (2). Por otro lado, no se vieron incrementados los factores angiogénicos PTTG [3] o FGF2 (4) (Fig. 1), lo que posiciona al sistema VEGF como blanco terapéutico en los adenomas hipofisarios secretores de prolactina y resistentes a agentes dopaminérgicos. En concordancia, tratamientos con terapia anti-VEGF resultaron en una inhibición del crecimiento tumoral y de la síntesis de prolactina en hipófisis Drd2-/- (5). Además, los bajos niveles de FGF2 y PTTG encontrados podrían relacionarse al crecimiento lento y la rareza de metástasis que acompañan a estos tumores de naturaleza benigna.

Figura 1. Efectos de la disrupción del RD2 en la hipófisis anterior. El aumento de prolactina por la falta del tono inhibitorio correlaciona con un aumento de VEGF y una disminución de TGFβ1. Otros factores angiogénicos como el PTTG y el FGF2 están disminuidos, quizás poniendo un freno a la angiogénesis inducida por VEGF.
Por otro lado, como sucede en el desarrollo de otros tumores, durante la tumorogénesis hipofisaria se producen profundos cambios en la estructura de los componentes de la matriz extracelular. Sin embargo, los pro-lactinomas rara vez producen metástasis. Por ello estudiamos los componentes de la matriz extracelular. Entre ellos, el factor de crecimiento transformante beta 1 (TGFβ1), una citoquina que se encuentra implicada en múltiples y potentes acciones locales, procesos biológicos como embriogénesis, desarrollo y homeostasis celular, proliferación y modificaciones de la matriz extracelular. El TGF-β1 y su receptor TGFβ tipo II (TβRII) están expresados en los lactotropos donde se ha descripto que ejercen un efecto inhibitorio sobre la proliferación celular y la secreción de prolactina. Nosotros demostramos que la expresión, activación y acción del TGFβ1 en hipófisis está disminuida en los ratones Drd2-/- (6). Estos resultados apuntan hacia la búsqueda de nuevas drogas para el tratamiento de tumores resistentes a drogas do-paminérgicas relacionadas con TGFβ1 y sus activadores locales.
Por último, en tumores hipofisarios humanos y en particular en prolactinomas resistentes al tratamiento con agonistas dopaminérgicos, determinamos un incremento de VEGF y su asociación con marcadores de vascularización como el CD31 y CD34 (7)(8). Estos hallazgos ponen de relevancia la vascularización del tumor hipofisario también en el humano, en oposición a trabajos que cuestionaban el aumento de vasculatura en estos adenomas.
El uso de antisicóticos en la clínica ha demostrado que además de la participación e importancia de la do-pamina como neurotrasmisor y neuromodulador en la regulación del sistema nervioso central los RD2 tienen funciones a nivel periférico que no son tan claras.
En particular, nosotros demostramos que la dopa-mina a través del RD2 modula el eje de crecimiento. Los animales transgénicos Drd2-/- presentaron un eje de crecimiento alterado, con una baja talla y un menor peso corporal. Esto se correlacionó con menores niveles de hormona de crecimiento secretados por la hipófisis, y menor IGF-I circulante (9)(10). Postulamos que la dopamina central a través del RD2 impediría la correcta liberación de GHRH del hipotálamo en la ventana temporal del período neonatal, y por ende el desarrollo de la población de somatotropos estaría alterado (Fig. 2). En concordancia, en humanos se ha observado que la L- DOPA puede acelerar el crecimiento en niños con deficiencia de GH, y que una población de niños con polimorfismos en el RD2 presentó deficiencias en el eje de crecimiento, con talla baja idiopática. Finalmente, en adultos bajo tratamiento crónico con antisicóticos se demostró una respuesta anormal de GH durante el sueño. En conjunto todos estos datos apuntan a una participación del RD2 en la regulación del eje GHRH-GH.
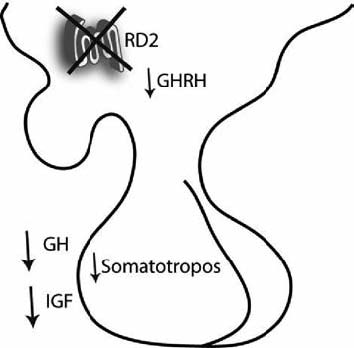
Figura 2. La falta de RD2 a nivel hipotalámico produce un descenso en la expresión de GHRH, y esta falla condiciona una inadecuada expansión del linaje somatotropo, con menor secreción de GH, y por ende de IGF-I circulante. En conjunto estas alteraciones producen una talla baja en roedores.
La dopamina regula el hambre y la saciedad actuando a nivel hipotalámico. Sin embargo, los efectos de la dopamina sobre la ingesta no son claros ya que interactúa con distintos núcleos hipotalámicos y estimula distintos subtipos de receptores.
En ratones mutantes nulos para el RD2 se observó un incremento en los gramos de alimento consumido por g de peso corporal. Sin embargo simultáneamente se describieron dos eventos anorexigénicos en estos ratones: un aumento en la α-MSH sérica e hipotalámica (la α-MSH es un potente anorexígeno), y una disminución del precursor de las orexinas (11). Estos eventos fueron compensados por el gran aumento de los niveles de prolactina que actúan como estímulo orexigénico (Fig. 3). Se ha descripto que la prolactina estimula la ingesta y la deposición de grasa en ratas hembras y que ratones deficientes del receptor de prolactina tienen una reducción progresiva en el peso corporal.
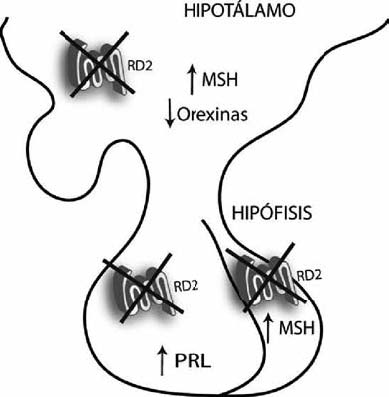
Figura 3. La disrupción del RD2 afecta distintos componentes reguladores de la ingesta. A nivel central se produce una disminución de las orexinas, y un aumento de αMSH. A nivel de la neurohipófi-sis se produce un aumento de secreción de αMSH por parte de los melanotropos, y en la hipófisis anterior un aumento de prolactina. El gran aumento de prolactina podría estar relacionado con el aumento de la ingesta del modelo, a pesar del descenso de orexinas y el incremento de αMSH (anorexígeno).
De nuestros resultados se destaca la compleja regulación del sistema de la ingesta, sistema primordial para la supervivencia. Múltiples factores actuarían en la regulación de la ingesta por el RD2, por un lado estos receptores tienen acciones orexigénicas estimulando las orexinas y la α-MSH, y por otro, anorexigénicas inhibiendo en forma constante la secreción de prolactina.
En humanos, la reducción de los RD2 se asocia con comportamientos adictivos, pero la evidencia sobre mutaciones en el RD2 y obesidad es escasa, aunque en general las mutaciones con pérdida de función se asocian a sobrepeso.
Recientemente se describió que existe una estrecha vinculación del uso de drogas antisicóticas y el desarrollo de diabetes tipo II. Nosotros demostramos que la dopamina también actúa a nivel del islote de Langerhans, regulando en forma inhibitoria la secreción de insulina. Utilizando los modelos animales de mutantes nulos, definimos que la ausencia de la acción dopaminér-gica sobre el islote (dada por ejemplo por el uso de drogas que antagonizan al RD2, o en forma constitutiva en los transgénicos), produce una secreción aumentada de insulina, lo que crónicamente conduce a un lento deterioro y agotamiento de las reservas insulínicas del islote (Figura 4) [12].
Figura 4. La falta de RD2 en el islote promueve la liberación de insulina, si esto se mantiene en forma crónica los islotes se agotan, y finalmente no descargan insulina en forma adecuada.
Este es un enfoque original, no presentado hasta ahora en la literatura, que resalta al páncreas como posible blanco no deseado de los tratamientos antisicóti-cos, y destaca la necesidad de desarrollar nuevos fármacos más específicos teniendo en consideración los posibles efectos negativos a este nivel.
Nuestros resultados en su conjunto, traen a la luz las complejas acciones endocrinas de los RD2 a distintos niveles del organismo, el hipotálamo, la hipófisis y el páncreas, destacando que el funcionamiento de estos receptores en forma orgánica y coordinada promueve el éxito reproductivo, el crecimiento, la ingesta y un metabolismo equilibrado.
Referencias bibliográficas
1. Cristina C, García-Tornadú I, Diaz-Torga G, et al. The do-paminergic D2 receptor knockout mouse: an animal model of prolactinoma. Front Horm Res 2006; 35: 50-63.
2. Cristina C, Diaz-Torga G, Baldi A, et al. Increased pituitary vascular endothelial growth factor-A in dopamin-ergic D2 receptor knockout female mice. Endocrinology 2005; 146: 2952-62.
3. Cristina C, Diaz-Torga GS, Goya RG, et al. PTTG expression in different experimental and human pro-lactinomas in relation to dopaminergic control of lac-totropes. Mol Cancer 2007; 6: 4.
4. Cristina C., Diaz-Torga G., Gongora A, et al. Fibroblast Growth Factor-2 in hyperplastic pituitaries of D2R knockout female mice. Am J Physiol Endocrinol Metab 2007; 293: E1341-51.
5. Luque GM, Perez-Millan MI, Ornstein AM, et al. Inhibitory effects of anti-VEGF strategies in experimental dopamine resistant prolactinomas. J Pharmacol Exp Ther 2011; 337: 766-74.
6. Recouvreux MV, Guida MC, Rifkin DB, et al. Active and Total Transforming Growth Factor-{beta}1 Are Differentially Regulated by Dopamine and Estradiol in the Pituitary. Endocrinology 2011; 152.
7. Cristina C, Perez-Millan MI, Luque G, et al. VEGF and CD31 association in pituitary adenomas. Endocr Pathol 2010; 21: 154-60.
8. Mallea-Gil MS, Cristina C, Perez-Millan MI, et al. Invasive giant prolactinoma with loss of therapeutic response to cabergoline: expression of angiogenic markers. Endocr Pathol 2009; 20: 35-50.
9. Diaz-Torga G, Feierstein C, Libertun C, et al. Disruption of the D2 dopamine receptor alters GH and IGF-I secretion and causes dwarfism in male mice. Endocrinology 2002; 143: 1270-9.
10. Garcia-Tornadu I, Rubinstein M, Gaylinn BD, et al. GH in the dwarf dopaminergic D2 receptor knockout mouse: somatotrope population, GH release, and responsiveness to GH-releasing factors and somatostatin. J Endocrinol 2006; 190: 611-9.
11. Garcia-Tornadu I, Diaz-Torga GS, Risso G, et al. Hypo-thalamic orexin, OX1, αMSH, NPY and MCRs expression in dopaminergic D2R knockout mice. Neuropeptides 2009; 43: 267-74.
12. Garcia-Tornadu I, Ornstein AM, Chamson-Reig A, et al. Disruption of the Dopamine D2 Receptor impairs insulin secretion and causes glucose intolerance. Endocrinology 2010; 151:1441-50.
LABORATORIO DE NEUROBIOLOGÍA
Eventos tempranos condicionantes de enfermedades neurodegenerativas
Early events as conditioning factors of neurodegenerative diseases
Eventos precoces condicionantes de doenças neurodegenerativas
Héctor Coirini, María Sol Kruse, Mariana Rey, Marina Roxana Di Pilla, María Cristina Vega
Resumen
Estudios clínicos sugieren que las complicaciones obstétricas están relacionadas con el desarrollo de alteraciones funcionales en el sistema nervioso central del individuo adulto. Una hipótesis establecida indica que las enfermedades neurodegenerativas estarían asociadas a un proceso iniciado por un estrés oxidativo temprano, y mediante distintos modelos experimentales tratamos de identificar cambios que pueden producirse durante la preñez, o al momento del nacimiento, relacionados con trastornos conductuales o cognitivos descriptos en enfermedades neurodegenerativas. De esta manera mediante una asfixia perinatal global que no afecta la sobrevida del individuo, hemos descripto alteraciones en las sinapsis de neoestriado e hipocampo, observando agregación proteica y ubiquitinación aumentada así como cambios en el contenido de actina, mientras que en retina describimos alteraciones en la actividad de la oxido nítrico sin-tasa. Resultados similares fueron reproducidos in vitro usando cultivos organotípicos, donde las estructuras del cerebro y las conexiones entre los diferentes núcleos se conservan. En un tercer modelo donde se induce una diabetes gestacional (DG) hemos evidenciado alteraciones importantes en las vías de señalización intracelular en cerebro embrionario involucradas en el proceso de muerte celular programada. En este mismo modelo estamos evaluando los efectos de la DG sobre la expresión de receptores hepáticos X y su relación con la expresión de la enfermedad de Alzheimer.
Palabras clave: estrés oxidativo; cultivos organotípicos; asfixia perinatal; óxido nítrico sintasa; enfermedad de Alzheimer; diabetes gestacional; retina.
Summary
Clinical studies suggest that obstetric complications are related to the development of functional alterations in the central nervous system of an adult. An established hypothesis suggests that neurodegenerative diseases would be associated
to a process initiated by early oxidative stress. Then, using different experimental models, early changes that may occur during pregnancy or at the perinatal period related to behavioral or cognitive disorders described in neurodegenera-tive diseases are identified. Using the model of perinatal asphyxia without affecting the survival of the individual, changes in neostriatum and hippocampus synapses, such as increased protein aggregation and ubiquitination as well as changes in the actin content have been described. On the other hand, in the retina, alterations of nitric oxide synthase were also observed. Similar results were reproduced in vitro using organotypic cultures where the brain structures and connections between different nuclei are preserved. In a third model, induction of gestational diabetes (GD) has shown significant alterations in the intracellular signaling pathways involved in the embryonic brain related to programmed cell death. In this model, we are currently evaluating the effects of GD on the levels of liver X receptors and their possible relationship with the expression of Alzheimer disease.
Key words: oxidative stress; organotypic cultures; perinatal asfixia; nitric oxide sintasa; Alzheimer disease; gestational diabetes; retina.
Resumo
Estudos clínicos sugerem que as complicações obstétricas estão relacionadas com o desenvolvimento de alterações funcionais no sistema nervoso central do indivíduo adulto. Una hipótese estabelecida indica que as doenças neurodegenerativas estariam associadas a um processo iniciado por um estresse oxidativo precoce, e através de diferentes modelos experimentais procuramos identificar alterações que podem ser produzidas durante a prenhez, ou no momento do nascimento, relacionados com transtornos de conduta ou cognitivos descritos em doenças neurodegenerativas. Deste modo, mediante uma asfixia perinatal global que não afeta a sobrevida do indivíduo, temos descrito alterações nas si-napses de neoestriado e hipocampo observando agregação proteica e ubiquitinação aumentada bem como alterações no conteúdo de actina, ao passo que em retina descrevemos al-terações na atividade da óxido nítrico sintase. Resultados similares foram reproduzidos in vitro usando culturas organo-típicas, onde as estruturas do cérebro e as conexões entre os diferentes núcleos se conservam. Num terceiro modelo onde se induz uma diabetes gestacional (DG) temos evidenciado alterações importantes nas vias de sinalização intracelular em cérebro embrionário envolvidas no processo de morte celular programada. Neste mesmo modelo estamos avaliando os efeitos da DG sobre a expressão de receptores hepáticos X e sua relação com a expressão da doença de Alzheimer.
Palavras chave: estresse oxidativo; culturas organotípicas; asfixia perinatal; óxido nítrico sintase; doença de Alzheimer; diabetes gestacional; retina.
Un gran número de estudios clínicos sugieren que las complicaciones obstétricas estarían relacionadas con el desarrollo de alteraciones funcionales en el sistema nervioso central (SNC) del individuo adulto. Procesos neurodegenerativos, tales como la espasticidad cerebro-espinal, una retinopatía proliferativa isquémica (RPI), el desencadenamiento de la esquizofrenia y hasta el riesgo de desarrollar la enfermedad de Alzheimer, tienen su origen en edad temprana, no solo en la expresión precoz de la disfunción sino por la presencia de un precondicionamiento del individuo a otros factores desencadenantes. Ciertas complicaciones que ocurren durante el desarrollo fetal o incluso en la etapa posnatal temprana, como una injuria cerebral, procesos inflamatorios o el desarrollo a una resistencia a insulina, además de alteraciones cromosómicas o genéticas, pueden generar una expresión clínica particular, la cual en principio no es deletérea pero que a largo plazo, se convierte en un importante factor de riesgo. La hipótesis general es que las enfermedades neurodegenerativas, estarían asociadas a un proceso iniciado por un estrés oxidativo temprano. El daño producido en el sistema nervioso central durante el período perinatal, afectaría principalmente el desarrollo neuronal y glial conduciendo a anormalidades en la respuesta celular o grupo de células involucradas, a corto, mediano y largo plazo. La evaluación de las alteraciones y su comparación entre sistemas similares, permitirá entonces establecer parámetros para la detección temprana de anomalías y plantear el desarrollo de posibles terapias paliativas.
En nuestro laboratorio se utilizan modelos experimentales relacionados, a fin de reproducir complicaciones que pueden producirse durante la preñez, o al momento del nacimiento, evaluando su efecto a largo plazo sobre cambios que se producen a nivel celular y bioquímico.
Asfixia perinatal
La asfixia perinatal es considerada como una de las más comunes de las complicaciones obstétricas, produce una injuria hipóxico-isquémica del sistema nervioso central, generalmente asociada con una cascada de eventos moleculares, que conducen a la muerte celular por apoptosis o necrosis. Entre los mecanismos nocivos implicados más importantes, se encontraría la liberación de aminoácidos excitatorios que generan un aumento del calcio intracelular con liberación de óxido nítrico (NO) y la producción de especies reactivas del oxígeno. En el modelo experimental utilizado se produce una asfixia global al momento del nacimiento y luego se evalúan cambios estructurales y ul-traestructurales, (1) así como alteraciones en la expresión de la óxido nítrico sintasa (NOS) en animales adultos o a edades tempranas, utilizándose también metodologías físicas y farmacológicas, a fin de prevenir o revertir la aparición de las anormalidades provocadas por la asfixia.
Alteraciones sinápticas en el cerebro
Las sinapsis de neoestriado e hipocampo, presentan características diferentes en cuanto a las densidades post-sinápticas (DPSs). Las alteraciones en estas estructuras durante un proceso hipóxico-isquémico, asociadas a la producción de NO, provocan alteraciones estructurales en las sinapsis que llevan a la muerte neuronal. Estos cambios así como el posible daño en las proteínas específicas que forman parte de estas estructuras, han sido vinculados con agregación proteica y ubi-quitinación sináptica. (2). Una de las posibles proteínas dañadas sería la F-actina, la cual está altamente concentrada en las espinas dendríticas, por lo que cambios en el contenido de actina podrían estar relacionados con la patogenia de la hipoxia (3).
Asfixia perinatal y retina
Un alto porcentaje de niños prematuros con algún grado de asfixia, desarrollan una RPI como consecuencia de la variación de los niveles de oxígeno durante el desarrollo de la vasculatura retiniana (4). Estudios realizados en el laboratorio han indicado que ratas sometidas a una asfixia perinatal en normotermia presentan RPI. Esta patología pudo ser evidenciada por fondo de ojo, en animales adultos y se encontró asociada a cambios en la expresión de la isoenzima in-ducible de la óxido nítrico sintasa (iNOS) a 21 y 30 días posteriores a la asfixia (5) con un marcado aumento en la inmunorreactividad para iNOS en la epi-rretina. Asímismo, la actividad de esta enzima determinada a 7, 15, 21, 30 y 60 días de edad presentó un aumento con la edad en ratas C con valores máximos a los 30 días de edad, mientras que los animales AP presentaron en cambio una actividad mayor que los controles a los 21 días de edad que se mantuvo en todas las edades (6).
Diabetes gestacional
Alteraciones en la progenie de madres diabéticas
En este modelo se induce una diabetes experimental no controlada en animales preñados, que conlleva alteraciones endocrino-metabólicas, un medio interno alterado para el desarrollo fetal y a un trabajo de parto complicado con riesgos perinatales. Estudios preliminares se enfocaron sobre posibles alteraciones en las vías de señalización intracelular en cerebro embrionario de madres diabéticas, utilizando técnicas de western blot para evaluar la expresión de p-Akt, Bax y Caspasa-3 a una edad embrionaria de 19 días, observándose una disminución de la p-Akt y de la proteína Bax indicando la existencia de múltiples alteraciones en las vías de señalización que conducen a un proceso defectuoso de muerte celular programada, lo cual podría estar relacionado con la susceptibilidad de la progenie de madres diabéticas a ciertas patología (7).
Asociación con enfermedad de Alzheimer
La progenie de madres con diabetes presenta un aumento en el riesgo a desarrollar obesidad y/o diabetes tipo II a edades tempranas. Estas complicaciones (obesidad y diabetes) han sido vinculadas con un aumento significativo en el riesgo de desarrollar la enfermedad de Alzheimer (AD). Tanto en la diabetes tipo II como en la AD existe una deficiencia en la respuesta a insulina y alteraciones en el metabolismo de colesterol. Los niveles de insulina y colesterol tienen papeles críticos en los procesos metabólicos básicos de los tejidos periféricos pero ambos actúan también como moléculas reguladoras de la función neuronal, teniendo una acción de importancia sobre los procesos de memoria y en las enfermedades neurodegenerativas. Los receptores hepáticos X (LXR) recientemente descrip-tos, se encuentran involucrados en el control del metabolismo energético interviniendo tanto en el metabolismo lipídico como en el de hidratos de carbono y ambos metabolismos están altamente correlacionados con las patologías descriptas anteriormente. Hemos iniciado estudios de caracterización y localiza-ción de los LXR en el cerebro de animales nacidos de madres con diabetes experimental a fin de evaluar si estas alteraciones pueden estar asociadas al riesgo de desarrollar AD (8).
Cultivos organotípicos
Con el fin de estudiar en detalle los procesos moleculares provocados por una asfixia global, iniciamos estudios con cultivos organotípicos, para ello se utilizan cortes de tejido cerebral, los cuales son mantenidos con vida, durante 21 días; esto permite evaluar cambios estructurales una semana después de provocarles una asfixia-hipoxia in vitro. Asimismo con este modelo podemos evaluar la acción de compuestos neuroprotec-tores a un proceso excitotóxico. Uno de los agentes evaluados fue alopregnanolona (Alo) utilizando cultivos organotípicos de estriado (St) e hipocampo (Hc). Luego de 1h de hipoxia todos los cultivos presentaron un aumento de LDH que fue mayor y significativo a las 24h post-hipoxia, provocando un aumento en las neuronas positivas para NADPH en St (38%) pero no en Hc. Ensayos con microscopía confocal mostraron un aumento de la señal de GFAP 24h después de la hipoxia. El pretratamiento con Alo provocó una disminución de la señal de GFAP que fue dosis dependiente (50nM y 5μM) en ambos tejidos siendo significativo en el hipocampo [9].
Otros proyectos
El laboratorio desarrolla proyectos en colaboración entre los que se destaca la evaluación de la interacción de diversos esteroides sintéticos, análogos de metaboli-tos reducidos de progesterona, producidos en el Departamento de Química Orgánica, FCEyN-UBA [10, 11], los cuales interactúan con el receptor para GABA tipo A. Seguida la caracterización del comportamiento de unión a los distintos sitios de ese receptor se realizan estudios sobre las características neuroprotectoras de estos, ante los eventos hipóxico-isquémico en cultivos or-ganotípicos, tejido fresco e in vivo.
Referencias bibliográficas
1. Cebral E, Capani F, Selvín-Testa A, Funes MR, Coirini H, Loidl CF. Neostriatal cytoskeleton changes following perinatal asphyxia: effect of hypothermia treatment. Int J Neurosci 2006; 116: 697-714.
2. Capani F, Saraceno GE, Botti V, Aon-Bertolino L, de Oli-veira DM, Barreto G, et al. Protein ubiquitination in post-synaptic densities after hypoxia in rat neostriatum is blocked by hypothermia. Exp Neurol 2009; 219: 404-13.
3. Capani F, Saraceno E, Boti VR, Aon-Bertolino L, Fernández JC, Gato F, et al., Ellisman MH, Coirini H. A tridimensional view of the organization of actin filaments in the central nervous system by use of fluorescent photooxidation. Biocell 2008; 32: 1-8.
4. Larrea P, Franco, P, Rey Funes M, Loidl CF, Capani F, Coirini H. Alteraciones en la retina de animales sometidos a asfixia perinatal detectados mediante métodos clínicos. I Congreso Nacional de Investigación en Visión y Oftalmología. 2005, Libro de resúmenes, 32.
5. Rey-Funes M, Ibarra ME, Dorfman VB, López EM, Ló-pez-Costa JJ, Coirini H, Loidl CF. Hypothermia prevents the development of ischemic proliferative retinopa-thy induced by severe perinatal asphyxia. Exp Eye Res 2010; 90: 113-20.
6. Rey-Funes M, Ibarra ME, Dorfman VB, Serrano J, Fernández AP, Martínez-Murillo R, et al. Hypothermia prevents nitric oxide system changes in retina induced by severe perinatal asphyxia. J Neurosci Res 2011; 89: 729-43.
7. Barutta J, Kruse MS, Coirini, H. Phospho-Akt and apop-totic proteins expression in the embryonic brains from diabetic rats (enviado a publicar).
8. Di Pilla MR, Vega MC, Bruno MA, Coirini H. Distribución de los receptores hepáticos X en el cerebro de animales nacidos de madres con diabetes experimental. III Jornada Interna de Investigación, Universidad Católica de Cuyo. Nov. 2010. Abstract CM06.
9. Kruse MS, Rey M, Barutta J, Coirini H. Allopregnanolone effects on astrogliosis induced by hypoxia in organ-otypic cultures of striatum, hippocampus, and neocor-tex. Brain Res 2009; 1303: 1-7.
10. Alvarez LD, Veleiro AS, Baggio RF, Garland MT, Edel-sztein VC, Coirini H, et al. Synthesis and GABA(A) receptor activity of oxygen-bridged neurosteroid analogs. Bioorg Med Chem 2008; 16: 3831-8.
11. Durán FJ, Edelsztein VC, Ghini AA, Rey M, Coirini H, Dauban P, et al. Synthesis and GABA(A) receptor activity of 2,19-sulfamoyl analogues of allopregnanolone. Bio-org Med Chem 2009; 17: 6526-33.
LABORATORIO DE BIOLOGÍA DEL COMPORTAMIENTO, INSTITUTO DE BIOLOGÍA Y MEDICINA
Un análisis integral del concepto de estrés
A comprehensive analysis of the concept of stress
Uma análise integral do conceito de estresse
Marcelo H. Cassini, Enrique T. Segura
Resumen
El concepto de estrés es utilizado en una gran diversidad de disciplinas biológicas, desde la biología molecular hasta la ecología de ecosistemas. Sin embargo, no existe una teoría universal del estrés y cada disciplina utiliza una definición de estrés que resulta funcional al proceso que está investigando pero que agrega confusión a la posibilidad de definir el estrés con criterio riguroso. Nuestro objetivo fue realizar un análisis exhaustivo del uso del concepto de estrés en las ciencias biológicas. No pretendimos realizar una revisión completa de la literatura sino poner énfasis en la diversidad de procesos en los que el estrés está involucrado. A partir del análisis de esa diversidad, surgieron patrones en el uso del término que permiten ir delimitando una definición única del estrés. El análisis que realizamos incluyó: (a) comparación de definiciones de la literatura; (b) identificación de siete componentes que conforman el proceso del estrés: estresor, contexto del estresor, efecto del estresor, mecanismo de reconocimiento del estresor, mecanismo de generación de respuesta, respuesta de estrés y consecuencia de la respuesta de estrés; (c) análisis de la intensidad y efecto del es-tresor y del tipo de resultado del estrés; (d) clasificación del tipo de consecuencias de la respuesta de estrés en reversibles o irreversibles y de corto, mediano o largo plazo; (e) reflexión sobre la especificidad de la respuesta y predictibili-dad del estresor. Concluimos que conviene restringir la noción de estrés al proceso que incluye la interacción entre
un estresor impredecible (en cierto grado) y un mecanismo individual de respuesta inespecífica (en cierto grado). Los efectos predecibles deberían quedar enmarcados dentro del contexto del estrés, y las respuestas poblacionales y de niveles superiores, dentro de las consecuencias ecológicas de la respuesta de estrés.
Palabras clave: condiciones ambientales adversas; estrés a nivel celular; fisiológico y ecológico; estresor; respuesta de estrés; consecuencias genéticas del estrés.
Summary
The concept of stress is used in a variety of biological disciplines, from molecular biology to ecosystem ecology. However, there is no universal theory of stress and each discipline uses a definition of stress that is functional to the process being investigated, but adds confusion to the possibility of defining stress using rigorous criteria. Our objective was to conduct a thorough analysis of the use of the concept of stress in the biological sciences. We did not attempt a full review of the literature but to emphasize the diversity of processes that stress involved. From the analysis of this diversity, patterns emerged in the use of the term that enabled a delimitation of a single definition of stress. The analysis performed includes: (a) comparison of definitions from the literature; (b) identification of seven components that make up the process of stress: stressor context, stressor, effect of the stressor, stressor recognition mechanism, a mechanism for response generation, stress response, and consequence of the stress response; (c) analysis of the intensity and effect of the stressor and type of result of stress; (d) classification of the type of consequences of the stress response in reversible or irreversible, and short, medium or long term; (e) analysis of the specificity of the response and predictability of the stressor. It can be concluded that it is advisable to restrict the notion of stress process to the interaction between a-to some degree-unpredictable stressor and a single-to some degree-non-specific response mechanism. The predictable effects should be framed within the context of stress, and population responses and higher levels within the ecological consequences of the stress response.
Key words: noxious environmental conditions; cellular; physiological and ecological stresses; stressor; genetic consequences of stress.
Resumo
O conceito de estresse é utilizado em uma grande diversidad de disciplinas biológicas, da biologia molecular até a ecolo-gia de ecossistemas. Entretanto, não existe uma teoria universal do estresse e cada disciplina utiliza uma definição de estresse que resulta funcional ao processo que está pesquisando mas que agrega confusão à possibilidade de definir o estresse com critério rigoroso. Nosso objetivo foi realizar uma análise exaustiva do uso do conceito de estresse nas ciên-cias biológicas. Não pretendemos realizar uma revisão completa da literatura mas colocar ênfase na diversidade de pro-cessos nos quais o estresse está envolvido. A partir da
análise dessa diversidade, surgiram padrões no uso do termo que permitem ir delimitando uma definção única do estresse. A análise que realizamos incluiu: (a) comparação de defini-ções da literatura; (b) identificação de sete componentes que conformam o processo do estresse: estressor, contexto do es-tressor, efeito do estressor, mecanismo de reconhecimento do estressor, mecanismo de geração de resposta, resposta de estresse e consequência da resposta de estresse; (c) análise da intensidade e efeito do estressor e do tipo de resultado do estresse; (d) classificação do tipo de consequências da resposta de estresse em reversíveis ou irreversíveis e de curto, médio ou longo prazo ; (e) reflexão sobre a especifi-cidade da resposta e preditibilidade do estressor. Concluímos que convém restringir a noção de estresse ao processo que inclui a interação entre um estressor impredizível (em certo grau) e um mecanismo individual de resposta inespecífica (em certo grau). Os efeitos predizíveis deveriam ficar en-quadrados dentro do contexto do estresse, e as respostas po-pulacionais e de níveis superiores, dentro das consequências ecológicas da resposta de estresse.
Palavras chave: condições ambientais adversas; estresse a nível celular; fisiológico e ecológico; estressor; resposta de estresse; consequências genéticas do estresse.
La noción de estrés es utilizada en diversas áreas de la ciencia, desde la física a la medicina. Además se aplica a diversas condiciones de la vida cotidiana. En esta revisión nos concentramos en el uso que se le brinda en el vasto campo de las ciencias biológicas. El concepto de estrés se aplica a numerosos fenómenos biológicos. Los especialistas que la usan en un campo de la biología frecuentemente no tienen la intención de extrapolar sus conclusiones acerca del estrés a otros campos, como si se trataran de fenómenos diferentes. Sin embargo, la entidad es por naturaleza inter-disciplina-ria porque relaciona diversos niveles de organización entre sí y con el medio ambiente. Tiene el atractivo teórico de ligar los mecanismos fisiológicos con los procesos ecológicos y la evolución. Los estímulos ambientales adversos disparan procesos a nivel molecular y celular y la respuesta del organismo al estrés refleja el rol de las fuerzas ambientales externas en determinar la distribución, la abundancia y los procesos evolutivos de las especies (1- 4).
La disciplina "madre" del concepto de estrés es la endocrinología de los vertebrados. El 'descubridor' del estrés, Hans Selye describió en 1935 las alteraciones fisiológicas en ratas de laboratorio sometidas a condiciones de estrés. la reactividad del eje hipotalá-mico-pituitario-adrenal es uno de los primeros y mejor comprendidos de los mecanismos fisiológicos asociados al estrés. El concepto de estrés fue rápidamente incorporado a la medicina y la psicología y se volvió un concepto popular para describir las alteraciones de salud provocadas por el frenesí de la vida moderna. La noción de estrés también se fue incorporando al léxico de diversas disciplinas científicas, desde la biología molecular a la ecología. Para evaluar la frecuencia y distribución del uso de este concepto en las ciencias biológicas actuales, realizamos una relevamiento de los artículos publicados en la revista PLoS Biology que contienen el término stress, desde el primer número publicado en el 2003 hasta junio 2011. Se cita la palabra estrés (sin incluir los casos en que el término "stress" se usa con el significado de "enfatizar") en 485 de 2780 artículos, es decir un 17,5%. La distribución de los porcentajes de mención del término es bastante pareja entre las primeras 9 disciplinas (Genética & Genómica, Biología celular, Biología molecular, Biología del Desarrollo, Neu-rociencias, Bioquímica, Microbiología, Biología computacional y Ecología), con un mínimo de 14,9% de citas con el término en ecología y un máximo de 27,2% en microbiología. El resultado de este rápido pa-neo sobre las publicaciones sugiere que es un concepto vigente en las ciencias biológicas modernas con una distribución amplia entre diversas disciplinas.
El objetivo de este trabajo es realizar un análisis exhaustivo del uso del concepto de estrés en las ciencias biológicas. Describimos diferencias y similitudes en el uso del concepto entre diferentes disciplinas y diferentes autores. Investigamos si es posible generar una definición universal de estrés. En caso de encontrar diferencias conceptuales insalvables entre diferentes aproximaciones al estrés, evaluamos la posibilidad de ser más cuidadosos en el uso del término, reemplazar su uso por términos más precisos o aceptar que el término estrés sea utilizado más como una metáfora de condiciones adversas que un concepto científico con una definición precisa.
Algunos usos actuales del concepto de estrés
Como ya dijimos, son muchas las disciplinas biológicas que utilizan el concepto de estrés. En esta sección se darán algunos ejemplos de su uso dentro de dos campos que tienen escalas de trabajo contrapuestas: la biología celular y la ecología. La biología celular ha tenido un enorme desarrollo en las últimas décadas. Buena parte de este crecimiento está asociado a cuestiones biomédicas y concomitantemente, al descubrimiento de los mecanismos celulares involucrados en diversas patologías en los humanos. Como veremos, la noción de enfermedad o disfunción está estrechamente relacionada al concepto de estrés. En este contexto, el concepto de estrés se incorpora como el medio ambiente anómalo que provoca la disfunción de algún mecanismo celular que precede al surgimiento del síntoma. Algunos de las condiciones y mecanismos de estrés más estudiados a nivel celular y molecular son: el estrés oxidativo, el estrés del retículo endoplasmático, el estrés genotóxico, el estrés osmótico, el estrés mecánico, el estrés de la replicación, las proteínas del estrés, las fibras del estrés y los gránulos del estrés. Cada uno de estos términos resumen un área completa de investigaciones con extensas referencias bibliográficas. Aquí sólo daremos breves definiciones extraídas de esa literatura como forma de ilustrar la diversidad de usos del concepto de estrés.
El estrés oxidativo es producido por un exceso de radicales libres que provocan daños en las proteínas celulares, en los lípidos de las membranas y en los ácidos nucleicos, y puede llevar eventualmente a la muerte celular (5). El estrés oxidativo se ha asociado al origen de diversas enfermedades como la aterosclerosis, la enfermedad de Parkinson y la enfermedad de Alzheimer. El retículo endoplasmático cumple múltiples funciones celulares que pueden ser alteradas por diversas perturbaciones externas tales como privación de glucosa, infecciones virales y obesidad (6)(7). El retículo endo-plasmático responde al estrés disparando una respuesta conservada evolutivamente, conocida con el nombre de 'respuesta a proteínas desdobladas', la cual involucra programas transcripcionales que inducen la expresión de genes específicos (7). El estrés genotóxico resulta de la exposición de las células a ciertos químicos que impactan sobre el ADN y producen alteraciones del material genético (8). Este fenómeno ha sido reconocido como uno de los factores asociados al desarrollo del cáncer en humanos (9). Para responder al daño celular provocado por este tipo de estrés, las células han desarrollado un repertorio de respuestas que involucra muchos factores celulares que forman un extensa red de transducción de señales (9). Las variaciones de osmo-ralidad del medio ambiente pueden provocar estrés celular particularmente en bacterias y plantas. Existen similitudes sorprendentes en la respuesta celular al estrés osmótico entre grupos taxonómicos diversos (10).
El estrés mecánico es una fuerza que opera sobre la superficie celular y que puede ser provocada por una compresión operando hacia el interior, una tracción o por cizallamiento (shear) en la superficie de los tejidos (11). La respuesta al estrés mecánico, como los canales de iones sensibles al estiramiento, está presente en bacterias, hongos, invertebrados y vertebrados (11). En humanos, ha sido intensamente investigada en relación al impacto del estrés por cizallamiento de la pared producido por variaciones en la presión sanguínea, las cuales resultan en enfermedades cardio-vasculares y la ateroesclerosis (11). Las proteínas del estrés (heat shock proteins) probablemente sean el mecanismo más famoso de defensa contra el estrés celular (12). Son universales y con diversos roles funcionales, de las cuales la más estudiada es la de 'chaperones' moleculares (13). Los gránulos del estrés son sitios citoplasmáticos dinámicos y transitorios que contienen agregados de ARNm (14). Estos gránulos son la consecuencia morfológica de la respuesta de estrés de proteínas involucradas en eventos normales de procesamiento del ARNm. Esta respuesta de estrés puede ser disparada por shocks de calor, exposición a oxidantes, proteínas desdobladas o ARN de doble cadena (14).
La ecología es una disciplina muy amplia que analiza las interacciones con el medio ambiente de varios niveles de organización, incluyendo individuos, poblaciones, comunidades y ecosistemas. Existen diversos estresores ambientales que afectan a los organismos vivos a esos distintos niveles. La depredación y las condiciones climáticas extremas son ejemplos típicos. Sin embargo, el uso del concepto de estrés en ecología se expandió a partir de los estudios del impacto de las actividades humanas sobre el medio ambiente natural (15). La contaminación, la degradación del hábitat y el cambio climático generan condiciones estresantes para la vida silvestre.
La ecología de poblaciones investiga la respuesta de especies individuales a variaciones temporales en las condiciones del ambiente. La medida más importante del efecto del ambiente sobre las poblaciones es la tasa de crecimiento poblacional y los parámetros que la afectan como las tasas de natalidad, mortalidad y fecundidad (16)(17). El efecto del estrés se mide sobre estas variables. Si bien los mecanismos de estrés operan a nivel individual, el impacto que tiene sobre una población depende de la proporción de individuos que tienen capacidad de responder adaptativamente al estrés, por lo que poblaciones aparentemente viables con fitness positivo bajo condiciones de estrés pueden encontrarse en el límite de la extinción (18). La ecología de poblaciones vegetales fue una de las primeras ramas de la ecología en estudiar el estrés, a punto tal de considerar la 'resistencia al estrés' como un propiedad de historia de vida de las especies, junto a características tales como tiempo y duración de la floración y la longevidad del banco de semillas (19). La ecología de comunidades estudia la estructura y dinámica de conjuntos de poblaciones. Se ha investigado profusamente el efecto que tiene el estrés sobre dos procesos fundamentales (y contrapuestos) de las comunidades: la competencia in-ter-específica y la facilitación. Una de las hipótesis en este campo plantea que la importancia relativa de estos dos procesos en las comunidades depende de la intensidad de estrés abiótico, siendo las interacciones positivas más frecuentes cuando la intensidad del estrés es más alta (20)(21).
El estrés que opera sobre la organización de los ecosistemas produce una gran diversidad de efectos, dependiendo de los componentes y procesos que se ven afectados. Estos efectos perturbadores son más evidentes cuando son producto del impacto antrópico. Por ejemplo, la contaminación biológica de los lagos produce una alteración en las bases de las tramas tróficas acuáticas, aumentando la productividad primaria, induciendo floraciones de algas con las consiguientes alteraciones sobre los consumidores; otro ejemplo en la dirección opuesta es la explotación pesquera que normalmente implica la remoción del los peces carnívoros 'tope' lo que provoca un efecto en cascada sobre la trama trófica (22). Un tercer ejemplo es la respuesta de los microorganismos del suelo a estresores tales como las sequías o las heladas tiene consecuencias sobre los nutrientes del suelo que afectan la productividad vegetal y los eslabones tróficos superiores (3).
Este rápido paneo realizado solamente dentro de dos áreas de la biología, sirve para ilustrar la diversidad y complejidad de condiciones en las que se aplica el concepto de estrés. Dada esta situación, es de esperar que existan numerosas y variadas definiciones de estrés.
Diversidad de definiciones de estrés
El término estrés ha sido uno de los más controvertidos de los términos biológicos. A continuación se enumera una serie de definiciones provenientes de distintos campos de la biología:
. Un estado de tensión no específica en organismos vivos (23)
. Una respuesta no específica del cuerpo a cualquier demanda de cambio (24)
. Una resultante fisiológica de demandas que exceden las capacidades regulatorias del organismo (25).
. Un factor ambiental que causa un cambio poten-cialmente nocivo en un sistema biológico (26).
. Un factor ambiental, usualmente uno físico, que tiene algún efecto sobre el fitness (2).
. Una condición externa que reduce el crecimiento, la supervivencia y/o la fecundidad de un organismo (21)
. Un contexto en el cual el fitness absoluto del tipo salvaje es reducido en comparación con el fitness absoluto en algún otro contexto de referencia (27)
. Un estado fisiológico de un animal en relación al estresor experimentado (1).
. Una reducción en la ganancia neta de recursos de un organismo relativa a su potencial máximo incluso luego de aclimatación o adaptación a una condición ambiental (28)
. Una amenaza crónica que impone costos fisiológicos (4)
. Una amenaza, real o implícita, a la homeostasis (29)
. El estado en el que la homeostasis ha sido perdida (30)
¿Cuáles son los componentes del estrés?
De lo anteriormente expuesto queda claro que el estrés es un concepto vigente que se utiliza con frecuencia para explicar numerosos fenómenos biológicos que tienen que ver con el impacto de factores ambientales adversos, pero que no existe una definición común que describa todos esos fenómenos. Con el objeto de ordenar la variedad de conceptos invocados en nombre del estrés y avanzar hacia una teoría unificada para este fenómeno, comenzamos por realizar una 'disección' del proceso involucrado en el estrés. Identificamos siete componentes en el estrés: estresor, contexto del estre-sor, efecto del estresor, mecanismo de reconocimiento del estresor, mecanismo de generación de respuesta, respuesta de estrés y consecuencia de la respuesta de estrés. A continuación se describe brevemente cada uno de esos componentes.
Los estresores son los factores del ambiente que afectan negativamente al organismo. Los estresores son variados dependiendo del tipo de organismo considerado. Por ejemplo, la labranza o la remoción completa de árboles producen alteraciones estructurales del suelo que son estresores para los micro-organismos del suelo (4) mientras que la fuerza de las corrientes de agua puede volverse estresante para un caracol que habita ambientes lóticos (31). Frecuentemente se distingue entre el efecto de estresores naturales y aquellos de origen antrópico. Otra forma de clasificación es la de estreso-res de corto término (fuego, tormentas, cosechas) y de largo término o crónicos (sequías, toxinas) (4). Para la ecología de sistemas, los primeros tienden a denominarse 'perturbaciones'. Algunos autores hablan de que el ambiente puede ser interno (genético o celular) o externo (ecológico). Ejemplos de estresores internos son la endogamia, las mutaciones deletéreas y el envejecimiento celular (32). Es importante no confundir el es-tresor con el contexto o ambiente donde opera el es-tresor.
El contexto del estresor son las condiciones físicas y psicológicas presentes cuando el estresor aparece (33). El ambiente social, las condiciones climáticas, la disponibilidad previa de recursos, el grado de control sobre el estresor, determinan un contexto que influye sobre la capacidad de respuesta frente al estresor. Más adelante se discutirá como algunos de los normales denominados estresores deberían ser considerados parte del contexto estresante. El contexto del estresor es una de las causas que determinan que diferentes individuos muestren distintas intensidades de respuesta frente al mismo efecto del estresor.
El efecto del estresor es el tipo de impacto negativo que provoca el estresor sobre el organismo. El efecto directo del estresor es siempre a nivel de organismos individuales, pudiendo afectar al individuo completo, alguno de sus sistemas o solo alguno tejidos. Puede tener consecuencias sobre poblaciones, comunidades y ecosistemas, pero el efecto directo es siempre sobre individuos.
El mecanismo de reconocimiento del efecto del estresor es un proceso fisiológico o uno molecular (dependiendo el tipo de efecto del estresor) que permite identificar la ocurrencia y el nivel del efecto del estresor. Es el segundo de los factores que determina el grado de variación de respuesta a un estresor, ya que el sistema de reconocimiento se seleccionaría en función del estresor. Esto determinaría que los mecanismos de reconocimiento puedan ser específicos pero, como veremos, la respuesta es inespecífica.
El mecanismo de generación de respuesta de estrés es el rasgo de diseño adaptativo disponible al organismo para responder al efecto del estresor. En micro-organismos, existen varios mecanismos que han sido considerados como respuestas de estrés. El entrar en estado de inactividad (dormancy) es considerado una respuesta a condiciones estresantes extremas (4). Las bacterias utilizan los mecanismos de transferencia horizontal de genes como una herramienta genética altamente eficiente para responder a condiciones adversas del medio ambiente. Su extendida capacidad para generar resistencia anti-biótica es una clara demostración de esta capacidad (34). En invertebrados, los mecanismos de respuesta a los tóxicos del ambiente son diversos y resultan en una disminución en la captación (v.g. disminuir permeabilidad en poliquetos), un aumento de la depuración (v.g. aumentar excreción en insectos), una mejoría de los procesos de desintoxicación, o mejorar los procesos reparación (vg. una mutación puntual que reduce el efecto del tóxico), entre otros (revisado por 3). En vertebrados, el mecanismo más reconocido de respuesta al estrés es el ya mencionado eje hipotálamo-hi-pofisiario-adrenal. También el sistema nervioso autonómico, particularmente la respuesta simpática de la médula adrenal y los nervios simpáticos (29). De acuerdo a la amplitud en la definición del concepto de estrés, se puede incluir al sistema inmune (27) y al repertorio de conductas de evitación (32) como mecanismos de estrés.
La respuesta de estrés es lo que produce el mecanismo frente al efecto del estrés. A la respuesta de estrés también se la llama "resistencia al estrés" (stress resistance). La respuesta de estrés en el caso del eje hipotá-lamo-hipofisiario-adrenal de los vertebrados incluye la movilización de glucosa a los músculos, la estimulación de la gluconeogénesis hepática, el incremento del tono cardiovascular, la estimulación de la función inmune y la inhibición de las conductas reproductora y alimentaria (35). La respuesta de estrés es, en la mayoría de los casos, inmediata al efecto del estrés.
La consecuencia de la respuesta de estrés es el efecto a mediano o largo plazo, reversible o irreversible que puede tener el estrés en un organismo, población, comunidad o ecosistema. Los mecanismos de estrés puede interaccionar con otros mecanismos fisiológicos o con-ductuales (v.g. eje con respuesta inmune) y ecológicos (competencia y facilitación), diversificando sus efectos. Un área muy investigada de las consecuencias de la respuesta de estrés es en el comportamiento social de los vertebrados, por ejemplo en las relaciones de dominancia dentro de los grupos sociales (v.g. 36) y en el valor de las asimetrías fluctuantes para la selección sexual (vg. 37). Para muchos autores, las consecuencias del estrés son consideradas respuestas de estrés pero, como discutiremos más adelante, la distinción facilita alcanzar una definición más estricta del estrés.
¿Puede haber estrés sin que haya respuesta adaptativa de estrés?
La mayor confusión que se ha generado en la literatura en relación al estrés radica en la respuesta a esta pregunta. Existe una considerable contradicción entre la definición originaria del estrés y muchas definiciones de estrés utilizadas por los biólogos en las últimas décadas.
Para los físicos que fueron quienes acuñaron el término, el estrés es una medida de las fuerzas que actúan sobre un cuerpo que puede ser deformado. El material que compone el cuerpo responde con un cambio de forma y tiene un límite de tolerancia a las fuerzas que operan sobre él. Superado ese umbral, ocurren fallas estructurales. Es decir que para los físicos, el estrés existe porque existe la respuesta de estrés. Si se aplica una fuerza sobre un cuerpo y este se rompe sin oponer resistencia, significa que no hay estrés. Bajo una condición estresante, un cuerpo puede responder 'adaptativa-mente' cuando el estímulo es de intensidad intermedia o puede sufrir un efecto negativo permanente, cuando esa intensidad supera un umbral.
H. Selye (23) fue el primero en aplicar el concepto a los seres vivos y lo definió como 'una respuesta no específica del cuerpo a cualquier demanda de cambio'. Es decir que para el 'descubridor' del estrés, es también la respuesta de estrés. Al igual que para los físicos, para los primeros fisiólogos el efecto negativo del estrés solo aparece cuando la respuesta del estrés no alcanza para compensarlo. En otras palabras, los primeros investigadores del estrés estaban especialmente interesados en los últimos dos componentes: mecanismos y respuestas.
Cuando el concepto de estrés se vuelve popular, lo hace con una connotación más negativa. El estrés es visto como un efecto que implica una disminución de funcionalidad del organismo, que puede producir enfermedad física o psíquica, sin que el individuo tenga posibilidad de responder adaptativamente al estresor. Cuando el concepto de estrés es adoptado por la ecología, lo hace influenciado por este concepto negativo del estrés, más cercano al concepto de distress de Selye (23). La mortalidad se vuelve una medida fácil para medir el estrés (2). En otras palabras, se produce un cambio en los componentes del estrés sobre los que se realiza el énfasis, hacia los primeros dos componentes: estresor y efecto del estresor, enfatizando los efectos cuando ya no es efectiva la respuesta de estrés.
En síntesis, a lo largo de la historia del concepto de estrés, se pasa de un período inicial en el que lo más importante era la respuesta de estrés, al concepto que puede haber estrés sin que haya una respuesta de estrés. En los últimos años, desde la biología celular se ha producido un reflorecimiento parcial del énfasis sobre los mecanismos de estrés, ya que esta disciplina hace foco en los procesos metabólicos y la funcionalidad celular que provocan los estresores.
¿Es el estímulo estresante intermedio entre lo normal y lo letal? ¿Hay efectos positivos del estrés?
Para muchos investigadores, la existencia de estrés depende de la intensidad del estímulo negativo. Estos autores asignan al estrés un efecto intermedio: el estímulo estresante debe encontrarse por debajo de los rangos 'normales' de tolerancia y por encima de los rangos 'letales' (2). Sin embargo, hay otros autores que consideran estresantes a estímulos negativos normales y otros que hacen lo mismo con estímulos letales.
Es fundamental diferenciar el efecto del estrés sin y con respuesta de estrés. Estrictamente hablando, el efecto que tiene el estresor debe siempre considerarse cuando no hay respuesta de estrés. Bajo esta definición, el efecto del estresor siempre es negativo. Lo que ocurre es que las respuestas de estrés pueden neutralizar el efecto del estresor y, en algunos casos, puede mejorar la condición del organismo. Un ejemplo sencillo es la aparición de un depredador. Gracias a la respuesta de estrés el organismo puede escapar, por lo que no habría ningún efecto negativo del estresor sobre la funcionalidad ni el fitness del organismo (quizás represente un pequeño costo metabólico). Pero el efecto del estresor es el daño potencial que produciría el es-tresor si no hubiera esa respuesta de estrés. De acuerdo a esto, el efecto directo del estrés es siempre negativo y hay efectos letales que deben ser considerados estresantes.
Cuando un factor ambiental tiene un efecto negativo dentro de los rangos 'normales' de una especie, entonces se dice que no hay estrés. La cuestión es definir 'normalidad'. En términos estrictos, un efecto normal sería aquel que no afecta el fitness sin necesidad que operen mecanismos de estrés. Dentro de este rango de 'normalidad' están las respuestas adaptativas específicas, es decir adaptaciones que no tienen relación con el estrés. Las respuestas adaptativas a estímulos negativos que no son respuestas de estrés son el producto de evolución frente a factores ambientales estables y predecibles. Este concepto será analizado en una sección posterior.
¿Cómo puede resultar la interacción entre el estresor y el organismo?
Como acabamos de analizar, por definición el estresor siempre tiene potencialmente un efecto inmediato negativo. Este efecto puede ser neutralizado por la respuesta de estrés o puede expresarse si la respuesta de estrés no existe o es débil en relación a la intensidad del estímulo. A nivel de los organismos, el estrés pueden tener cinco resultados diferentes, dependiendo de cómo interactúa el efecto del estresor con la respuesta de estrés: (1) puede ser letal, si el estresor es intenso y no hay respuesta de estrés o esta no es suficiente; (2) puede afectar directamente el fitness por efecto sobre la funcionalidad (v.g., enfermedad) o la reproducción, cuando la respuesta de estrés no es suficiente para anular un efecto no letal del estresor; (3) puede afectar indirectamente el fitness por efecto sobre el balance energético; (4) puede ser neutro si la respuesta de estrés es efectiva; y (5) puede ser positivo, si predispone al organismo a responder más eficientemente a exposiciones futuras al estresor.
El tercer tipo de efecto, que significa considerar el estrés como un 'costo' merece una explicación más amplia. Cuando se define al estrés como una respuesta 'adaptativa' o 'plástica', en realidad se puede aceptar que esa respuesta igual conlleva un efecto indirecto sobre el fitness. Como los recursos energéticos y de tiempo son finitos, la asignación de recursos a la respuesta de estrés inevitablemente implica un costo en términos de asignación de recursos, por más que no tenga un impacto directo sobre la funcionalidad que se refleja en la salud o en la reproducción. Si hay efecto indirecto, puede haber disminución del fitness, pero no por disminución de la funcionalidad sino por alteración del presupuesto energético (26)(29). Seria análogo a la diferencia entre alimentación y reposo. La alimentación es más costosa que el reposo y además frecuentemente es más riesgosa. Sin embargo, no se puede decir que la alimentación afecte la funcionalidad de un organismo. Es una actividad esencial como es esencial poder responder eficazmente a disminuciones temporales en la calidad del hábitat, que sería la definición 'adaptativa'.
Las consecuencias reversibles e irreversibles del estrés
Para un organismo, las consecuencias del estrés pueden ser reversibles o irreversibles. Cuando las consecuencias son reversibles, el impacto puede ser de corto término o de mediano término. En estas definiciones entra los conceptos clásicos de homeostasis y alostasis (29). Cuando las consecuencias son reversibles y de corto término, se puede decir que hay una perturbación momentánea del equilibrio interno del organismo que se restablece luego de superado el estado de estrés.
Ejemplo comunes de consecuencias reversibles de corto término son la huída de un depredador o la respuesta a una helada nocturna por los micro-organismos del suelo. Dado que las condiciones ambientales cambian continuamente en forma tanto predecible como im-predecible, muchas veces resulta conveniente cambiar de condición de equilibrio para ajustarse a una nueva condición ambiental. A este mantenimiento de la estabilidad interna a través del cambio se la conoce como alostasis (29). Cuando estas respuestas reversibles de cambio de estado estacionario ocurren como respuesta al efecto de un cambio negativo más o menos impre-decible, estamos frente a un tipo de consecuencia de respuestas de estrés. Un ejemplo para ilustrar una condición alostática cíclica y otra impredecible. Durante el estado de preñez para una hembra de mamífero, las demandas cambian de forma de pasar a un estado meta-bólico diferente que seguramente requerirá de un aumento de la ingesta de alimento. Si esta hembra hipotética debe gestar en un invierno inusualmente crudo, queda sometida a una condición estresante que implica un aumento todavía más elevado de las demandas energéticas. En algunas especies de mamíferos, condiciones climáticas adversas persistentes durante la preñez desencadenan una respuesta de estrés extrema cual es el aborto espontáneo.
Cuando son irreversibles, las consecuencias del estrés para un organismo pueden ser de mediano o de largo plazo. Los efectos de mediano plazo son cambios permanentes en la vida de un organismo, mientras que los de largo plazo son cambios genéticos que trascienden al organismo. Si bien el efecto potencial inmediato del es-tresor es siempre negativo, las consecuencias a mediano y largo plazo pueden ser neutras e inclusive positivas o beneficiosas. Esto se debe a que el organismo o la población responde al estresor y esta respuesta puede neutralizar el efecto del estrés o inclusive mejorar el estado del individuo o población. En otras palabras, es muy importante diferenciar entre el efecto del estresor y el efecto de las respuestas que provoca el estresor, es decir las consecuencias de la respuesta de estrés.
Todas las consecuencias descriptas hasta ahora en esta sección afectan a organismos individuales. Cuando el efecto es supra-individual, se habla de consecuencias ecológicas del estrés. Los estresores pueden afectar a muchos organismos simultáneamente, lo que trae consecuencias en las interacciones dentro y entre poblaciones. Como ya hemos visto, el estrés afecta la dinámica de las interacciones competitivas intra- e inter-específicas y las relaciones tróficas dentro de los ecosistemas.
¿Es la respuesta de estrés inespecífica y es el estresor impredecible?
La noción de especificidad del estrés ha ido cambiando a lo largo del tiempo. La definición original incluía esta noción. Para Selye, el estrés era inespecífico, en el sentido que la misma respuesta se evoca para una diversidad de estresores. Esta característica permite excluir de la definición de estrés a muchas respuestas adaptativas que sí son específicas. A medida que la definición de estrés se fue relajando, lo mismo ocurrió con su especificidad. En las definiciones más modernas de estrés, no se hace referencia al grado de especificidad de la respuesta. Implícitamente se incluyen las respuesta específicas e inclusive se hace innecesaria la existencia de respuesta para que se considere estrés, como fue descripto antes.
Si se analiza el concepto de estrés con una mirada evolutiva, se puede deducir que toda respuesta de estrés debería ser inespecífica, y que el estresor debe ser impredecible.
Existe una relación entre especificidad de la respuesta y predictibilidad del estresor, determinada por la manera en que opera la selección natural. La selección natural tiende a generar rasgos biológicos (diseños) que son eficientes bajo las condiciones naturales en que estos evolucionan (38). Esta es la noción básica de adaptación. Cuanto más estables son las condiciones ambientales, más específicos son los diseños producidos por la selección natural. En otras palabras, cuando hay un cambio en el ambiente, la selección di-reccional (positiva) tiende a producir un carácter adaptativo que luego es mantenido por selección esta-bilizadora (negativa) (39). Cuando un estresor ambiental se puede predecir, entonces la selección natural inevitablemente se orientará a generar respuestas específicas. Podríamos decir que existe entonces un rango de adaptaciones especie-específicas que están diseñadas para responder a cambios negativos pre-decibles del ambiente. Los ritmos biológicos probablemente sean el mejor ejemplo. Estas respuestas específicas han sido tradicionalmente consideradas fuera de la órbita del estrés, pero las definiciones más recientes y relajadas de estrés pueden incluirlas. La importancia de la predictibilidad del estresor ha sido enfatizada repetidamente en la literatura (v.g.: 1). Las condiciones adversas pero predecibles del ambiente, como las reducciones estacionales en la temperatura o la oferta de alimento puede afectar negativamente el balance energético pero no actúan en sí mismos como estresores. Este tipo de condiciones pueden ser parte del componente del estrés: 'contexto del estresor' y por lo tanto puede hacer al organismo más susceptible al estrés real, per no pueden ser descriptos como estresantes en sí mismos.
Las definiciones modernas más relajadas del estrés que no incluyen la existencia obligatoria de una respuesta de estrés, tienen el problema que confunden dos contextos evolutivos diferentes: una situación ambiental estable en la que existentes estímulos impre-decibles y una situación inestable en la que aparecen variables negativas nuevas en el ambiente. Ejemplos de esto serían el ataque de predadores y la contaminación de origen antropogénico, respectivamente. En la sección siguiente mostraremos cómo una definición demasiado amplia de estrés lleva a confusión respecto a las consecuencias evolutivas del estrés.
¿Cuáles son las consecuencias evolutivas del estrés?
Existe un concepto generalizado que establece que las condiciones estresantes pueden actuar como fuerzas evolutivas que fuerzan a las poblaciones a responder adaptativamente (32). En otras palabras, que la disminución en el fitness provocada por el estrés afecta la tasa de selección. Este concepto está muy difundido pero debe ser reflexionado. La validez de esta afirmación depende de la propia definición de estrés y solo se cumple cuando se considera estrés a cualquier efecto negativo de un estresor. Diferente es cuando se considera que hay estrés sólo cuando los organismos exhiben una respuesta adaptativa a estímulo impredecibles.
Cuando el ambiente es estable pero con cambios impredecibles dentro de un rango de posibles condiciones, entonces se espera que se favorezcan mecanismos inespecíficos de respuesta a esas condiciones que varían al azar. Bajo estas condiciones las condiciones estresantes no provocarán ningún cambio adap-tativo. Cuando el ambiente sufrió un cambio permanente estable recientemente y los organismos todavía no están adaptados, entonces los estímulos negativos seguramente van afectar la tasa de selección y las poblaciones van a tender a responder adaptativamente al cambio.
Agrawal & Whitlock (27) revisaron la información empírica alrededor de la idea que el estrés afecta la fuerza de la selección sobre nuevas mutaciones. Estos autores encontraron que diferentes tipos de estrés afectan la selección en forma diferente y concluyeron que esta idea que el estrés típicamente incrementa la selección, debe ser rechazada. Sin embargo, no pudieron encontrar un explicación clara acerca de los mecanismos subyacentes a esta variabilidad. Es probable que los diferentes resultados observados en este estudio estén relacionados con diferentes contextos evolutivos de estrés. Si las condiciones en las que se evaluó el estrés son estables y existían respuestas adaptativas previas, no se espera que haya un cambio en la tasa de mutaciones, porque la presencia de un estímulo negativo no es pre-condición obligatoria para un cambio evolutivo. Si por el contrario, los organismos fueron expuestos a es-tresores nuevos para los que no existe una respuesta de estrés previa, se establecen condiciones para que opere la selección natural.
Conclusiones
En este trabajo se han analizado dos categorías de definiciones de estrés. Las más amplias y modernas que definen al estrés en función del efecto negativo de los es-tresores y las más restrictivas y antiguas que relacionan el estrés con la respuesta positiva de los organismos a esos estresores.
Las definiciones generalistas del estrés presentan diversas vaguedades: (1) puede o no haber respuesta de estrés, (2) la respuesta de estrés puede ser inespecífica o específica, (3) el estresor puede ser predecible o im-predecible, (4) el efecto del estrés puede o no ser letal o benigno, y (5) el estrés puede o no tener efectos sobre la tasa de selección natural. En síntesis, la definición amplia del estrés incluye todas las condiciones adversas del ambiente y las respuestas individuales, poblacionales y ecosistémicas, de corto y largo plazo, a esas condiciones. Otra característica de la noción ge-neralista de estrés es que tiene una connotación negativa, ya que enfatiza el efecto directo del estresor que, como hemos visto, siempre es negativo. Desde un punto de vista fisiológico, esta visión negativa del estrés está entroncada con la idea de homeostasis, que a su vez se asocia con la idea de un equilibrio estático (29). Desde un punto de vista evolutivo, esta visión confiere al estrés un rol fundamental en el proceso evolutivo forzando a las poblaciones a responder adapta-tivamente.
La definición más restrictiva del estrés incluye la existencia de una respuesta de estrés y está respuesta es inespecífica y adaptativa. El estresor es impredecible y con un efecto entre lo letal y lo benigno. A niveles bajos de acción del estrés, la respuesta de estrés amortigua los efectos negativos o tiene un impacto solo sobre el balance de costos-beneficios, con un efecto débil sobre el fitness. A niveles altos del estímulo, la respuesta de estrés se vuelve ineficiente, por lo que hay un efecto sobre la funcionalidad y/o directamente sobre el fitness. Este efecto no impacta sobre la tasa de selección. Esta definición de estrés circunscribe al estrés a un rango de efectos de estresores y mecanismos fisiológicos concretos. Esta visión parcialmente positiva del estrés se acerca a una aproximación a los sistemas fisiológicos de equilibrio dinámicos y retroalimentación positivas.
En síntesis, hay dos definiciones diferentes del estrés. Enfatizando componentes distintos, difieren en aspectos substanciales en la concepción del funcionamiento de los sistemas fisiológicos y del rol del estrés en los procesos evolutivos. Mientras persistan estas dos concepciones básicamente diferentes, el uso del término estrés seguirá siendo confuso y convendría ser reemplazado por términos que describan mejor el fenómeno que se investiga. Nuestra opinión es que conviene restringir la noción de estrés al proceso que incluye la interacción entre un factor ambiental adverso impredecible (en cierto grado) y un mecanismo individual de respuesta inespecífica (en cierto grado). Los efectos predecibles deberían quedar enmarcados dentro del contexto del estrés, y las respuestas pobla-cionales y de niveles superiores, dentro de las consecuencias ecológicas de la respuesta de estrés. Este criterio permite acomodar fácilmente cada fenómeno que involucra el impacto de una factor ambiental negativo dentro o fuera de la órbita del estrés. Solo un par de ejemplos para ilustrar los beneficios de esta definición. ¿Los cambios genéticos pueden ser considerados respuestas de estrés? De acuerdo a nuestra definición, depende del tipo de proceso genético: la adquisición de resistencia a antibióticos por una bacteria a través de mecanismos de transferencia horizontal de genes entra dentro de la órbita del estrés, ya que es una respuesta relativamente inespecífica a un cambio impredecible del ambiente que opera a nivel de un individuo. Por el contrario, la resistencia a insecticidas producto exclusivamente de cambios en las frecuencias génicas dentro de una población de insectos no se corresponde con esta definición de estrés porque no es una respuesta individual. ¿Es la parición (el parto en humanos) una situación de estrés? Si bien la parición, como la gestación y el amamantamiento son costosas para la hembra, no pueden considerarse estrés ya que son estados predecibles. Sí pueden predisponer a la hembra a ser más susceptible al estrés y por ello estas etapas de la reproducción pueden ser incluidas dentro del contexto del estresor.
A modo de corolario, vale la pena volver a enfatizar que el análisis realizado en este trabajo también permitió confirmar que el concepto de estrés es fundamental por dos motivos. Primero, porque liga la ecología con la fisiología y segundo, porque enfatiza la noción de alostasis sobre la de homeostasis. Estas características le otorgan un grado de universalidad al estrés que pocos conceptos poseen en biología. Hemos citado una pequeñísima parte de la bibliografía disponible sobre estrés y hemos dado solo algunos ejemplos de casos de estrés de la gran cantidad de ellos que hay en la literatura. Pero el objetivo de este trabajo no fue el de realizar una revisión completa sino de navegar a través de la diversidad de usos y aplicaciones del concepto con la esperanza de arribar a una conclusión respecto al mejor destino que se le puede dar al uso del concepto de estrés.
AGRADECIMIENTOS
Agradecemos a la Lic. Claudia Marro por sus aportes en la discusión de conceptos analizados en este trabajo. Los autores de este trabajo son investigadores del CONICET. Este trabajo fue financiado con subsidios del CONICET (PIP Nº 11420090100367) y el MINCYT RES Nº383/10.
Referencias bibliográficas
1. Buchanan KL. Stress and the evolution of condition-dependent signals. TREE 2000; 15: 156-60.
2. Sorensen JG & Loeschcke V. Studying stress responses in the post-genomic era: its ecological and evolutionary role. J Biosc 2007; 32: 447-456.
3. Maltby L. Studying stress: the importance of organism-level responses. Ecol Appl 1999; 9: 431-40.
4. Schimel J, Balser TC, Wallenstein M. Microbial stress-response physiology and its implications for ecosystem function. Ecology 2007; 88: 1386-94.
5. Maritim AC, Sanders RA, Watkins III JB. Diabetes, ox-idative stress, and antioxidants: a review. J Biochem Molec Toxicol 2003; 17: 24-38.
6. Gregor MF, Hotamisligil GS. Adipocyte Stress: The en-doplasmic reticulum and metabolic disease. J Lipid Res 2007; 48: 1905-14.
7. Xu C, Bailly-Maitre B, Reed JC Endoplasmic reticulum stress: cell life and death decisions. J Clin Inv 2007; 115: 2656-64.
8. Ulm R, Revenkova E, di Sansebastiano G-P, Paszkowski J. Mitogen-activated protein kinase phosphatase is required for genotoxic stress relief in Arabidopsis. Genes De-vel 2001; 15: 699-709.
9. Yang J, Yu Y, Hamrik HE, Duerksen-Hughes PJ. ATM, ATR and DNA-PK: initiators of the cellular genotoxic stress responses. Carcinogenesis 2003; 24: 1571-80.
10. Csonka LN. Physiological and genetic responses of bacteria to osmotic stress. Microbioll Rev 1989; 53: 121-47.
11. Davies PF, Tripathi SC 1993. Mechanical stress mechanisms and the cell. An endothelial paradigm. Circul Res 72: 239-45
12. Kregel KC. Heat shock proteins: modifying factors in physiological stress responses and acquired thermotoler-ance. J App Physiol 2002; 92: 2177-86.
13. Feder ME, Hofmann GE. Heat-shock proteins, molecular chaperones, and the stress response: Evolutionary and ecological physiology. Ann Rev Phys 1999; 61: 243-81.
14. Anderson P, Kedersha N. RNA granules. J Cell Biol 2006; 172: 803-8.
15. Yunus M, Singh N, de Kok LJ Eds. Environmental stress: indication, mitigation and eco-conservation. Dordrecht, The Netherlands. Kluwer: Academic Publishers; 2000; .p. 465.
16. Sibly RM. Efficient experimental designs for studying stress and population density in animal productions. Ecol appl 1999; 9: 496-503.
17. Sibly RM, Hone J, Clutton-Brock TH. Wildlife population growth rates, Cambridge: Cambridge University Press; 2003. pp. 363.
18. Zani PA, Swanson SET, Corbin D, Cohnstaedt LW, Agotsch MD, Bradshaw WE, et al. Geographic Variation in Tolerance of Transient Thermal Stress in the Mosquito Wyeomyia smithii. Ecology 2005; 86: 1206-11.
19. Févrille Héléne, McConway K, Dodd M, Silvertown J. Prediction of extinction in plants: interaction of extrinsic threats and life history traits. Ecology 2007; 88: 2662-72.
20. Emery NC, Ewanchuk PJ, Bertness MD. Competition and salt-marsh plant zonation: stress tolerators may be dominant competitors. Ecology 2001; 82: 2471-85.
21. Maestre FT, Valladares F, Reynolds JF. Is the change of plant-plant interactions with abiotic stress predictable? A meta-analysis of field results in arid environments. J Ecol 2005; 93: 748-57.
22. Lenihan HS, Peterson CH, Byers JE, Grabowski JH, Thayer GW, Colby DR. Cascading of habitat degradation: oyster reefs invaded by refugee fishes escaping stress. Ecol Appl 2001; 11: 764-82.
23. Selye H. The stress of life. New York & London: Longmans, Green & Co; 1956.
24. Selye H. The general adaptation syndrome and the diseases of adaptation. J Clin Endoc Metab 1946; 6: 117-230.
25. Bradshaw D. Vertebrate ecophysiology: an introduction to its principles and applications. Cambridge, Cambridge University Press; 2003. pp. 287.
26. Parsons P A. The metabolic cost of multiple environmental stress: implications for climatic change and conservation. TREE 1990; 5: 315-7.
27. Agrawal AF, Whitlock MC. Environmental duress and epistasis: how does stress affect the strength of selection on new mutations. TREE 2010; 25: 450-8.
28. Dethier MN, Williams SL, Freeman A. Seaweeds under stress: manipulated stress and herbivory affect critical life-history functions. Ecol Monog 2005; 75: 403-18.
29. McEwen BS, Wingfield JC. The concept of allostasis in biology and biomedicine. Horm Behav 2003; 43: 2-15.
30. Reeder DM, Kramer KM. Stress in free-ranging mammals: integrating physiology, ecology and natural history. J Mammal 2005; 86: 225-35.
31. Lam PKS. Methods for distinguishing genetic and environmental variance in stress tolerance. Ecol Appl 1999; 9: 449-55..
32. Sorensen JG, Kristensen N, Loeschcke V. The evolutionary and ecological role of heat shock proteins. Ecol Lett 2003; 6: 1025-37.
33. Romero LM. Physiological stress in ecology: lessons from biomedical research. TREE 2004; 19: 249-55.
34. Michael CA, Gillings MR, Holmes AJ, Hughes L, Andrew NR, et al. 2004 Mobile gene cassettes: a fundamental resource for bacterial evolution. Am Nat 2004; 164: 1-12.
35. Boonstra R. Equipped for life: the adaptive role of the stress axis in male mammals. J Mammal 2005; 86: 236-47.
36. Beehner JC, Bergman TJ, Cheney DL, Seyfarth RM, Whitten PL. The effect of new alpha males on female stress in free-ranging baboons. Anim Behav 2005; 69: 1211-21.
37. Leamy LJ, Klingenberg P. The genetics and evolution of fluctuating asymmetry. Ann Rev Ecol Evol Syst 2005; 36: 1-21.
38. Stephens DW, Krebs JR. Foraging theory. Princeton, NJ: Princeton University Press; 1986.
39. Mayhew PJ. Discovering evolutionary ecology: bringing together ecology and evolution. Oxford: Oxford University Press; 2006. pp. 215.
LABORATORIO DE BIOLOGIA DEL COMPORTAMIENTO
Modelo experimental de lesión medular sacra en ratas: correlatos clínicos y electrofisiológicos del segmento metamérico afectado
Experimental model of spinal lesion in rats: clinical and electrophysiological correlates in the metameric affected segment.
Modelo experimental de lesão medular sacra em camundongos: correlatos clínico e eletrofisiológicos do segmento metamérico afetado.
Francisco Mannará1,2, Enrique Segura1, Silvina Figu-relli2, Héctor Coirini1, Alberto Yorio1,2
1. Hospital de Agudos Juan A. Fernández (GCABA).
2. Instituto de Biología y Medicina Experimental (CONICET).
Resumen
La lesión experimental de la médula espinal a nivel sacro en la rata produce un modelo animal con baja morbilidad respecto a los investigados con lesiones de la médula espinal a nivel torácico. La descripción y cuantificación de la es-pasticidad clínica en la cola de la rata causada por la lesión de la médula espinal sacra es escasa en la bibliografía. Por otro lado, no hay investigaciones acerca de las correlaciones entre el grado de espasticidad en la cola de rata y parámetros electrofisiológicos, por lo que nuestro objetivo es estudiar la espasticidad de la cola con estudios clínicos y electro-miográficos. Se realizaron cirugías espinales experimentales en 10 ratas Sprague Dawley. El nivel sacro fue elegido para producir la espasticidad sólo en la cola. En el tiempo postoperatorio se evaluó la cola buscando signos de espasticidad, como paresia e hipertonía, y el grado de espasticidad se ca-tegorizó utilizando una escala cuantitativa del tono muscular. Además, se realizaron estudios de electromiografía para obtener respuesta de los músculos de la cola por estimulación del nervio caudal (ondas M y F). Luego, los animales fueron sacrificados y perfundidos. Las lesiones de médula espinal fueron verificadas con histopatología. Todos los animales con lesión medular presentaron paresia de la cola. Los signos de espasticidad se iniciaron en la segunda semana del estudio. En relanción con la escala de tono muscular cinco ratas presentaron espasticidad de grado 2, tres ratas espasticidad de grado 4, y sólo una espasticidad de grado 3. La electrofi-siología mostró patrones de respuesta en relación con la evolución clínica y el grado de espasticidad. Los resultados obtenidos muestran la correspondencia entre el grado de es-pasticidad y los patrones electrofisiológicos causado por el grado de excitabilidad de las motoneuronas del segmento espinal afectado. Este modelo experimental que permite hacer una evaluación clínica y de la correspondencia con la elec-trofisiología con la menor morbilidad general provocada por la lesión de médula espinal.
Palabras clave: lesión espinal; espasticidad; electromiografía.
Summary
The experimental sacral spine lesion in the rat produce an animal model with low morbidity than those with toracic spinal lesions. The clinical spasticity quantification in the tail of the rat caused by sacral cord lesion was poorly described in the bibliography. Furthermore, there are no investigations about the relantionship between electrophysyological parameters and the grade of spasticity in the rat tail, so our purpose is to evaluate tail spasticity with clinical and elec-tromyographic studies. Experimental spinal surgeries were done in 10 Sprague Dawley rats. Sacral level was choosen to produce spasticity only in the tail. On the postoperatory time the tail was evaluated searching signs of spasticity, such as paresia and hypertonia, and then the grade of spasticity was categorizated using a muscular tone quantitative scale. On the other hand, electromyographic studies were done to obtain the muscular responses of the tail to the caudal nerve stimulation (M, F and waves). Then, the specimens were sacrificed and perfunded. Spinal cord lesions were verified with hystopathology. All the animals with spinal lesion presented paresia of the tail. The spasticity signs began at the second postoperative week. In relantionship with the muscular tone scale five rats presented grade 2 spasticity, three rats grade 4 spasticity, and only one grade 3 spastic-ity. The electrophysiology showed patterns of response in relation with the clinical evolution and the grade of spasticity. The results obtained showed correspondence between the grade of spasticity and the electrophysiological patterns caused by the grade of the motoneuron excitability. This experimental model allows to make a clinical evaluation and the correspondence with the electrophysiology, with the lowest general morbidity.
Key words: spinal injury; spasticity; electromyography.
Resumo
A lesão experimental da medula espinhal a nível sacro no camundongo produz um modelo animal com baixa morbilidade a respeito dos pesquisadores com lesões da medula espinhal a nível torácico. A descrição e quantificação da espasticidade clínica na cauda do rato causada pela lesão da medula es-pinhal sacra é escassa na bibliografia. Por outro lado, não há pesquisas acerca das correlações entre o grau de espastici-dade na cauda do rato e parâmetros eletrofisiológicos, por-tanto o nosso objetivo é estudar a espasticidade da cauda com estudos clínicos e eletromiográficos. Foram realizadas
cirurgias espinhais experimentais em 10 ratos Sprague Daw-ley. O nível sacro foi escolhido para produzir a espasticidade só no rabo. No tempo pós-operatório foi avaliado o rabo na procura de sinais de espasticidade, como paresia e hiperto-nia, e o grau de espasticidade se categorizou utilizando uma escala quantitativa do tom muscular. Além disso, foram realizados estudos de eletromiografia para obter resposta dos músculos da cauda por estimulação do nervo caudal (ondas M e F). Depois, os animais foram sacrificados e perfundidos. As lesões de medula espinhal foram verificadas com histo-patologia. Todos os animais com lesão medular apresenta-ram paresia da cauda. Os sinais de espasticidade foram iniciados na segunda semana do estudo. Em relação à escala de tom muscular cinco ratos apresentaram espasticidade de grau 2, três ratos espasticidade de grau 4, e só um espasti-cidade de grau 3. A eletrofisiologia mostrou padrões de res-posta com relação à evolução clínica e o grau de espastici-dade. Os resultados obtidos mostram a correspondência entre o grau de espasticidade e os padrões eletrofisiológicos causado pelo grau de excitabilidade dos motoneurônios do segmento espinhal afetado. Este modelo experimental permite fazer uma avaliação clínica e da correspondência com a eletrofisiologia com a menor morbilidade geral provocada pela lesão de medula espinhal.
Palavras chave: lesão espinhal; espasticidade; eletromiografia.
Introducción
Las alteraciones clínicas y fisiopatológicas provocadas por lesión traumática de la médula espinal son el resultado no sólo de la lesión primaria propiamente dicha, sino también de la conjunción de factores inflamatorios, necrosis hemorrágica progresiva, destrucción neuronal, proliferación glial y trastorno vascular, conocidas como lesiones secundarias y terciarias (1). Los modelos animales experimentales de lesión medular constituyen una herramienta útil para la investigación de los mecanismos fisiopatológicos involucrados y los posibles procedimientos terapéuticos. En la bibliografía se describen los efectos clínicos de la lesión medular experimental en ratas así como también hallazgos elec-trofisiológicos observados en los niveles afectados. Sin embargo, las descripciones se refieren generalmente a los efectos producidos por lesiones en el nivel torácico de la médula espinal y es infrecuente el estudio de las correlaciones entre los hallazgos clínicos y los electro-fisiológicos (2)(3).
En este estudio se utiliza un modelo experimental de lesión espinal en la rata albina Sprague Dawley a nivel del segmento medular sacro, porque en este modelo se puede observar los efectos clínicos de la lesión espinal a nivel de la cola del animal con menor morbilidad, ya que se evita el compromiso esfinteriano y de la locomoción. El objetivos es el de correlacionar los efectos clínicos y electrofisiológicos de la lesión medular.
Materiales y Métodos
Se utilizaron 14 ratas macho Sprague-Dawley (250-300 gramos), procedentes del bioterio del Instituto de Biología y Medicina Experimental (IBYME, CONICET). La lesión medular se realizó en 10 animales; las restantes correspondieron al grupo control: 1 rata con lesión falsa y 3 ratas sin lesión.
Procedimientos quirúrgicos
Las cirugías se realizaron con anestesia profunda con mezcla de ketamina (80 mg/kg, i.p.) y xylazina (10 mg/kg, i.p), manteniendo la temperatura corporal a 37 oC. El control del sangrado se efectuó con Gelfoam. En distintos animales se utilizaron dos procedimientos: a) Lesión falsa, en la se efectuó sección de tejidos blandos, laminectomía posterior sin apertura de la duramadre y sutura. b) Lesión de médula espinal (LME), utilizando microscopio quirúrgico, laminectomía posterior en nivel L1-2 (correspondiente a la metámera S1 de la médula espinal), apertura de la duramadre y transección de médula espinal con tijera de iridectomía, con posterior sutura de duramadre y tejidos blandos.
Estudios clínicos
El estado general y el tono muscular y la motilidad activa de la rata se examinaron en forma diaria. Se evaluó particularmente el segmento de la cola por medio de la inspección, la motilidad pasiva y la respuesta a estímulos táctiles. Para cuantificar el grado de compromiso del tono muscular de la cola se utilizó una escala diseñada por los investigadores (Tabla I).
Tabla I. Grados de alteración del tono muscular, en categorías según signos clínicos observados en el examen físico de la cola.
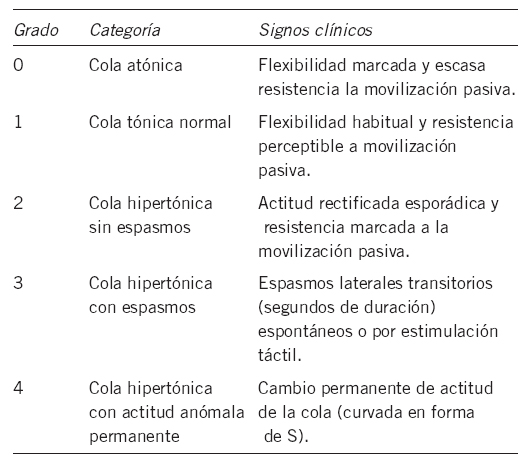
Estudios electrofisiológicos
Los registros se realizaron bajo anestesia ligera con ketamina (60 mg/kg), a la 1ª, 2ª, 3ª y 4ª semana de realizada la LME. En músculo de la cola mediante electrodo coaxial se registraron los potenciales compuestos de acción muscular provocados por estimulación con electrodos subcutáneos del nervio caudal. Se detectaron una onda de corta latencia (respuesta M) y una onda de latencia tardía (respuesta F). Se midieron latencia en milisegundos y amplitud en milivolts de ambas ondas. La estimulación del nervio caudal se efectuó a 1, 2, 4 y 8 hertz a fin de evaluar los efectos de la estimulación repetitiva sobre la excitabilidad del segmento de médula espinal sacro. Se computaron las amplitudes porcentuales de la respuesta H respecto a la amplitud máxima obtenida a frecuencias de estimulación de 0.25 hertz. Se confeccionaron curvas de amplitud porcentual en función de la frecuencia de estimulación.
Estudios histológicos
Los animales fueron sacrificados en forma incruenta en la cuarta semana posterior al inicio de las evaluaciones. La médula espinal fue removida y el segmento medular caudal a S1, disecado y fijado en formol al 10% durante 48 horas. Posteriormente se analizaron los resultados obtenidos para determinar el grado de lesión en los diferentes niveles de la médula espinal sacra, tanto proximales como distales al sitio de sección.
Resultados
Las 10 ratas con LME (100%) presentaron hipotonía y parálisis total de la cola inmediatamente distal a la lesión medular. La duración de la fase aguda o de hipo-tonía fue variable, entre 1 y 4 días después de la lesión. Además, en 3 ratas se observó una leve paresia en alguna de las extremidades posteriores, transitoria, con recuperación ad-integrum luego de la primera semana posoperatoria. Los hallazgos clínicos a nivel de la cola fueron marcadamente distintos de acuerdo al tiempo transcurrido posterior a la cirugía, por lo que se consideraron dos etapas desde el punto de vista clínico: la etapa aguda, correspondiente a la primera semana pos-quirúrgica, y la etapa crónica, correspondiente a la evolución a partir de la segunda semana posquirúrgica. Las exploraciones electrofisiológicas realizadas durante la fase aguda de la lesión medular permitieron observar que las respuestas electromiográficas de la cola a la estimulación del nervio caudal fueron en general respuestas M y F de incidencia, configuración y amplitud variables, con predominio de la disminución de las amplitudes. Una de las ratas con LME falleció dentro de la primera semana posquirúrgica.
Como se consignó previamente, luego de la segunda semana postoperatoria se manifestaron signos claros de incremento del tono muscular de la cola. De acuerdo con la escala de espasticidad utilizada, 5 ratas (55%) presentaron espasticidad grado 2, una (11%) grado 3 y las otras 3 restantes (33%) espasticidad grado 4. Los registros electrofisiológicos realizados en la fase crónica mostraron que los parámetros de la respuesta M fueron constantes. A diferencia de lo observado en los animales del grupo control, las curvas de amplitud porcentual respecto a la frecuencia de estimulación fueron menos pronunciadas en los animales con LME, por menor variación en la amplitud de la respuesta F. En las ratas con mayor grado de espasticidad (grados 3 y 4) las respuestas F prácticamente no presentaron variaciones de amplitud a las distintas frecuencias de estimulación.
La histología permitió corroborar la existencia de sección completa medular a nivel de S1 y varias anormalidades histológicas en los segmentos adyacentes a la zona lesionada: degeneración neuronal (vacuolización del neuropilo), y astrogliosis.
Discusión y Conclusiones
La lesión medular experimental en ratas se asocia a cambios clínicos y electrofisiológicos distintos según el tiempo transcurrido desde la lesión. En la primera semana posterior a la lesión existe un cuadro de parálisis fláccida, hipotonía y arreflexia de la cola, que se asocia a una disminución de las respuestas electromiográficas respecto a los animales controles. Luego de la segunda semana se pueden observar signos clínicos de hipertonía en los músculos de la cola de las ratas lesionadas y cambios correlativos en las respuestas electromiográficas a la estimulación. Estos resultados son coincidentes con lo reportado por otros autores, que describen parálisis muscular e hipotonía de la cola en el período temprano posterior a la lesión medular, asociadas a la ausencia o variabilidad de las respuestas electromiográficas, e hipertonía de la cola en relación a salvas de actividad elec-tromiográfica en los períodos posteriores (4).
Nuestros resultados también concuerdan con los de otros investigadores respecto a la posibilidad de evaluar en un modelo animal de lesión medular el grado de tono muscular del segmento corporal afectado por LME en forma cuantitativa por medio de una escala de espasticidad (5). En la bibliografía también se menciona que hay diferencias en la respuesta electromio-gráfica tardía de los animales con lesión medular respecto a los controles; esto se atribuye a un aumento de la excitabilidad de las motoneuronas, resultante de la sección de las vías descendentes en la médula espinal (11)(12). A diferencia de estos trabajos, que estudian la onda elec-tromiográfica tardía en la pata trasera en modelos de lesión medular en niveles más altos (6)(11)(13-16), nuestros resultados muestran efectos de la onda electromiográ-fica tardía en la cola del animal en un modelo de lesión medular sacra. Estos resultados sugieren la validez del modelo experimental propuesto, con menor morbi-mortidad e invasión sobre la integridad física y com-portamental del los animales.
Desde el punto de vista fisiopatológico, se considera que ambas fases clínicas (hipotonía y espasticidad), son el resultado de alteraciones del balance entre los mecanismos inhibitorios y excitatorios que normalmente actúan sobre las motoneuronas. En la fase aguda existe un evidente defecto de los mecanismos excitatorios sobre las motoneuronas ubicadas en el segmento medular distal a la lesión. En la fase crónica, la recuperación de los mecanismos excitatorios se expresa mediante la reaparición y aumento de la reactividad neuromuscular. Además, la lesión medular interrumpe las influencias inhibitorias que provienen del tronco cerebral proyectándose a través de los fascículos laterales de la médula espinal. De esta manera, los aminoácidos monoami-nérgicos no llegan a ejercer su influencia moduladora sobre las interneuronas y motoneuronas espinales. En estas condiciones, la desinhibición medular resulta en un aumento de la excitabilidad de las motoneuronas, que se presenta como un incremento de la descarga de los potenciales de acción de las fibras musculares en respuesta a la estimulación.
Referencias bibliográficas
1. Coutts M, Keirstead HS. Stem cells for the treatment of spinal cord injury. Exp Neurol; 2008; 209: 368-77.
2. Bennett DJ, Sanelli L, Cooke CL, Harvey PJ, Gorassini MA. Spastic longlasting reflexes in the awake rat after sacral spinal cord injury. J Neurophysiol 2004; 91: 2247-58.
3. Yorio A, Mannara F, Pennisi P, Figurelli S, Segura E. Changes in the F-wave of sacral segments by spinal cord injury in rats: clinical, histological and biochemical correlates. Clinical Neurophysiology 2008; 119: S172.
4. Li Y, Harvey PJ, Li X, Bennett DJ. Spastic long-lasting reflexes of the chronic spinal rat studied in vitro. Journal of Neurophysiol 2004; 91:2236-46.
5. Harris RL, Putman CT, Rank M, Sanelli L, Bennett DJ
Spastic tail muscles recover from myofiber atrophy and myosin heavy chain transformations in chronic spinal rats. J Neurophysiol 2007; 97: 1040-51.
6. Basso DM, Fisher LC, Anderson AJ, Jakeman LB, Mc-Tigue DM, Popovich PG. Basso Mouse Scale for locomotion detects differences in recovery after spinal cord injury in five common mouse strains. J Neurotrauma 2006; 23: 635-59.
7. Gelderd JB, Chopin SF. The vertebral level of origin of spinal nerves in the rat. Anatomical Record 1977; 188: 45-7.
8. Mannará F, Figurelli S, Pennisi P, Segura E, Yorio A. Lesión experimental de la médula espinal sacra en la rata y correlato clínicoelectrofisiológico. Medicina 2008; 68 Supl II: 146.
9. Kakinohana O, Hefferan MP, Nakamura S, Kakinohana M, Galik J, Tomori Z, et al. Development of GABA-sensitive spasticity and rigidity in rats after transient spinal cord ischemia: a qualitative and quantitative electrophysiologi-cal and histopathological study. Neuroscience 2006; 141: 1569-83.
10. Joynes RL, Janjua K, Grau JW. Instrumental learning within the spinal cord: VI. The NMDA receptor antagonist, AP5, disrupts the acquisition and maintenance of an acquired flexion response. Behavior Brain Res 2004; 154: 431-8.
11. Carp JS, Tennissen AM, Chen XY, Wolpaw JR. H-reflex op-erant conditioning in mice. J Neurophysiol 2006; 96: 1718-27.
12. Lee BH, Lee KH, Kim UJ, Yoon DH, Sohn JH, Choi SS, et al. Injury in the spinal cord may produce cell death in the brain. Brain Research 2004; 1020: 37-44.
13. Kim Y, Aoki T, Ito H. Evaluation of parameters of serially monitored F-wave in acute cervical spinal cord injury. J Nippon Med Sch 2007; 74: 106-13.
14. Gosgnach S, Lanuza GM, Butt SJ, Saueressig H, Zhang Y, Velasquez T, Riethmacher D, Callaway EM, Kiehn O, Goulding M. V1 spinal neurons regulate the speed of vertebrate locomotor outputs. Nature 2006; 440: 215-9.
15. Chen Y, Chen XY, Jakeman LB, Chen L, Stokes BT, Wol-paw JR. Operant conditioning of H-reflex can correct a locomotor abnormality after spinal cord injury in rats. J Neu-roscience 2006; 26: 12537-43.
16. Carp JS, Tennissen AM, Chen XY, Wolpaw JR. Diurnal H-reflex variation in mice. Experimental Brain Research 2006; 168: 517-28.















