Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Acta bioquímica clínica latinoamericana
versión impresa ISSN 0325-2957
Acta bioquím. clín. latinoam. vol.45 no.4 La Plata oct./dic. 2011
TRADUCCIONES SELECCIONADAS DEL CLINICAL CHEMISTRY
El Colesterol no-HDL demuestra una mejor exactitud en el score de la clasificación del riesgo cardiovascular comparado con el colesterol LDL, directo o calculado, en una población dislipémica
Non-HDL cholesterol shows improved accuracy for cardiovascular risk score classification compared to direct or calculated ldl cholesterol in a dyslipidemic population
Hendrick E. van Deventer1, W. Greg Miller2, Gary L Myers3, Ikunosuke Sakurabayashi4, Lorin M. Bachmann2, Samuel P. Caudill3, Andrzej Dziekonski2, Selvin Edwards3, Mary M. Kimberly3, William J. Korzun2, Elizabeth T. Leary5, Katsuyuki Nakajima6, Masakazu Nakamura7, Robert D. Shamburek1, George W. Vetrovec2, G. Russell Warnick8 y Alan T. Remaley1,*
1National Institutes of Health, Bethesda, MD;
2 Virginia Commonwealth University, Richmond, VA;
3Centers for Disease Control Prevention, Atlanta, GA;
4Jichi Medical University, Tochigi-ken, Japan;
5 Pacific Biomarkers and Pacific Biometrics Research Foundation, Seattle, WA;
6 Otsuka Pharmaceutical, Tokyo, Japan;
7 Osaka Medical Center for Health Science and Promotion, Osaka, Japan;
8 Health Diagnostics Laboratory, Richmond, VA.
Traducción: Diego Lucero y Laura Schreier.
Departamento de Bioquímica Clínica, Facultad de Farmacia y Bioquímica. Universidad de Buenos Aires.
Este artículo ha sido traducido con el permiso de la AACC. La AACC no es responsable de la exactitud de la traducción. Las opiniones expresadas son las de los autores y no necesariamente de la AACC o de la Revista. Tomado de Clin Chem, 2011 57(3):490-501, con el permiso del editor. Derechos de autor original © Asociación Americana de Química Clínica, Inc, 2011. Al citar este artículo, por favor recurra a la fuente original de publicación en la revista Clinical Chemistry.
This article has been translated with the permission of AACC. AACC is not responsible for the accuracy of the translation. The views presented are those of the authors and not necessarily those of the AACC or the Journal. Reprinted from Clin Chem, 2011 57(3):490-501, by permission of the publisher. Original copyright © 2011 American Association for Clinical Chemistry, Inc. When citing this article, please refer to the original publication source in the journal, Clinical Chemistry.
* Dirección de correspondencia de este autor: National Institutes of Health, Department of Laboratory Medicine, Building 10, Room 2C-433, 10 Center Drive, MSC 1508, Bethesda, MD 20892-1508. Fax 301-402-1885; e-mail aremaley1@cc.nih.gov.
Resumen
Antecedentes: Nuestro objetivo fue evaluar la exactitud en el score de la clasificación del riesgo de enfermedad cardiovascular (ECV) por parte de la medida directa de colesterol de LDL (dc-LDL), del cálculo del colesterol LDL (cc-LDL), y del colesterol no HDL (no-c-HDL) en comparación a la clasificación por los métodos de referencia (MR) realizados en el CDC. Métodos: Se estudiaron 175 pacientes, entre ellos 138 con ECV u otras condiciones que puedan afectar a la medición de c-LDL. Las mediciones de dc-LDL se realizaron con reactivos Denka, Kyowa, Sekisui, Serotec, Sysmex, UMA y Wako. Se calculó cc-LDL mediante la ecuación de Friedewald, usando la respectiva medida directa del colesterol de HDL de cada fabricante y las mediciones de colesterol total y triglicéridos medidas por Roche y Siemens (Advia), respectivamente. Resultados: Para los participantes con triglicéridos <2,26 mmol / L (<200 mg / dL), la tasa de errores de clasificación global en el score de riesgo de ECV fue de 5% a 17% con los métodos de cc-LDL, y del 8% al 26% para los métodos dc-LDL en comparación con los MR. Sólo el dc-LDL realizado por Wako presentó menos errores de clasificación que su método de cc-LDL correspondiente (8% vs 17%, p<0,05). El no-c-HDL clasificó erróneamente a un menor número de pacientes que dc-LDL en 4 de los 8 métodos (P <0,05). Para los pacientes con triglicéridos >2,26 mmol / L (>200 mg / dL) y <4,52 mmol / L (<400 mg / dL), los métodos de dc-LDL, en general, presentaron mejores resultados que los métodos cc-LDL, y los métodos de no-c-HDL mostraron una mejor correspondencia con el MR en el score de clasificación de riesgo de ECV que los métodos de dc-LDL como de cc-LDL. Conclusiones: A excepción de las personas hipertrigliceridémicas, 7 de los 8 métodos de dc-LDL fallaron en mejorar el score de clasificación de riesgo de ECV sobre los correspondientes métodos de cc-LDL. No-c-HDL mostró en general la mejor concordancia con el MR en el score de clasificación de riesgo de ECV en individuos normales y con hipertrigliceridemia.
Summary
Backgound: Our objective was to evaluate the accuracy of cardiovascular disease (CVD) risk score classification by direct LDL cholesterol (dLDL-C), calculated LDL cholesterol (cLDL-C), and non-HDL cholesterol (non-HDL-C) compared to classification by reference measurement procedures (RMPs) performed at the CDC. Methods: We examined 175 individuals, including 138 with CVD or conditions that may affect LDL-C measurement. dLDL-C measurements were performed using Denka, Kyowa, Sekisui, Serotec, Sysmex, UMA, and Wako reagents. cLDL-C was calculated by the Friedewald equation, using each manufacturer's direct HDL-C assay measurements, and total cholesterol and triglyceride measurements by Roche and Siemens (Advia) assays, respectively. Results: For participants with triglycerides <2.26 mmol/L (<200 mg/dL), the overall misclassification rate for the CVD risk score ranged from 5% to 17% for cLDL-C methods and 8% to 26% for dLDL-C methods when compared to the RMP. Only Wako dLDL-C had fewer misclassifications than its corresponding cLDL-C method (8% vs 17%; P < 0.05). Non-HDL-C assays misclassified fewer patients than dLDL-C for 4 of 8 methods (P < 0.05). For participants with triglycerides <2.26 mmol/L (200 mg/dL) and <4.52 mmol/L (<400 mg/dL), dLDL-C methods, in general, performed better than cLDL-C methods, and non-HDL-C methods showed better correspondence to the RMP for CVD risk score than either dLDL-C or cLDL-C methods. Conclusions: Except for hypertriglyceridemic individuals, 7 of 8 dLDL-C methods failed to show improved CVD risk score classification over the corresponding cLDL-C methods. Non-HDL-C showed overall the best concordance with the RMP for CVD risk score classification of both normal and hypertriglyceridemic individuals.
Introducción
El colesterol de LDL (c-LDL), factor de riesgo mayor para la enfermedad cardiovascular (ECV), es principal objetivo de las terapias hipolipemiantes y es utilizado para clasificar a los pacientes en varias categorías de riesgo de ECV (1). Las lipoproteínas son un grupo heterogéneo de partículas de diferente tamaño y composición lipídica y proteica (2), por lo tanto el desarrollo de métodos específicos para medir c-LDL son un desafío. El método de referencia (MR) para la medida de c-LDL (rc-LDL) y de colesterol de HDL (rc-HDL) es la ultracentrifugación, mediante la cual se realiza la remoción de la VLDL y los quilomicrones, seguida de una precipitación con heparina-magnesio para remover la LDL (3). Aunque el rc-LDL es poco práctico para el uso de rutina, ha sido validado como biomarcador de ECV en grandes estudios clínicos (4)(5) y es el patrón contra el cual son comparados todos los métodos de rutina (6). Hasta hace poco, el c-LDL no era medido directamente sino que era estimado desde el colesterol total (CT), colesterol de HDL (c-HDL) y triglicéridos (TG) usando la fórmula de Friedewald (7). Es sabido, sin embargo, que el c-LDL calculado (cc-LDL) se vuelve progresivamente menos exacto a medida que se elevan los niveles de TG, no es válido en la hiperlipoproteinemia de tipo III y requiere muestras en ayunas (7). Además, el sesgo y la imprecisión de las 3 medidas por separado utilizadas en el cálculo pueden afectar adversamente a la exactitud del cc-LDL (8).
Para superar estas limitaciones, se han desarrollado varios reactivos para la medición directa de c-LDL (dc-LDL) que actualmente son ampliamente adoptados (2). Una ventaja de estos métodos es que no dependen de la medida de TG y entonces son menos influenciados por las muestras sin ayuno. Otra ventaja es que son totalmente automatizados en varias plataformas y, por lo tanto, tienen una precisión relativamente buena (9). Aun así, estudios previos sobre dc-LDL han demostrado que no muestran una especificidad completa hacia el c-LDL y que no siempre ofrecen una ventaja significativa sobre el cc-LDL (2)(8)(10)(11). Estos estudios, sin embargo, a veces fueron limitados, porque algunos sólo estudiaban un único método directo, y muchos otros no estudiaban poblaciones dislipémicas o no comparaban los resultados contra el rc-LDL (2)(8)(10).
Recientemente, completamos un estudio comparando todos los métodos de dc-LDL del mercado contra el rc-LDL (9). Observamos que los métodos dc-LDL frecuentemente fallan en cumplir con los objetivos de calidad del National Cholesterol Education Program (NCEP) para muestras dislipémicas cuando fueron comparados con el MR de beta-cuantificación por ultracentrifugación para c-LDL. En este estudio, usando la misma población, analizamos la concordancia del score de la clasificación del riesgo de ECV, por varios métodos de dc-LDL y cc-LDL, usando el método directo de c-HDL (dc-HDL) de cada fabricante para realizar el cálculo, respecto al score de riesgo cardiovascular obtenido por el MR para c-LDL. Adicionalmente, para realizar score de riesgo de ECV, también se midieron apolipoproteína (apo)-B y apo-A-I, principales componentes proteicos estructurales de las LDL y HDL respectivamente, así también como colesterol no-HDL (no-c-HDL).
Materiales y Métodos
MUESTRAS DE PACIENTES
Los pacientes fueron reclutados del Virginia Commonwealth University Medical Center y NIH (National Institute of Health de Estados Unidos), con la aprobación de los comités revisores institucionales. La población (n=175), cuyos detalles fueron previamente descriptos (9), incluyó 37 controles sanos y el resto de los participantes, en su mayoría, fueron reclutados de una clínica de lípidos o ECV. Un total de 104 participantes ayunaron más de 12 h, 10-12 tuvieron 24 h de ayuno, 11 ayunaron de 8 a 10 h y 36 ayunaron menos de 8 h. Los sueros fueron almacenados a 4 °C, y todas las mediciones se realizaron dentro de las 48 h desde la extracción.
ANÁLISIS DE LÍPIDOS Y LIPOPROTEÍNAS
Fueron utilizados los resultados de rc-LDL, rc-HDL, dc-LDL, dc-HDL, TG y CT de un estudio anterior (9). Las mediciones por el MR para c-LDL y c-HDL, por ultracentri-fugación, fueron realizados en el CDC. Los métodos para la medida directa de c-LDL y de c-HDL [Denka Seiken, Kyowa Medex, Sekisui Médica (antes Daiichi), Serotec, Reactivos Sysmex Internacional, UMA, Industrias Wako Pure Chemical, y Roche Diagnostics (distribuidora de reactivos Kyowa Medex con calibrador y controles Roche)] se realizaron en un analizador Hitachi 917 (Roche Diagnostics) utilizando los parámetros recomendados por cada fabricante. CT se midió mediante reactivos de Roche adaptados para un analizador Siemens ADVIA 1650. TG totales se midieron, sin blanco de glicerol, utilizando reactivos de Siemens Advia en un autoanalizador ADVIA 1650. Los rendimientos de los métodos de CT y TG se verificaron por la participación en el Programa de Estandarización de Lípidos del CDC (12), y la media de sesgos en comparación al MR del CDC fueron del 0,2% (rango de -0,3% a 0,8%) de CT y -0,1% (rango -3,0% a 2,5%) para TG.
El cc-LDL se calculó mediante la fórmula de Friedewald: [cc-LDL (mmol / L) = CT (mmol / L) - c-HDL (mmol / L) - TG (mmol / L) / 2,22] (7), utilizando el dc-HDL de cada fabricante y el CT y TG, como se describió anteriormente. El no-c-HDL se calculó mediante la siguiente ecuación: (no-c-HDL = CT - c-HDL), usando dc-HDL de cada fabricante o rc-HDL y CT como se describió anteriormente. Los valores de referencia para el colesterol VLDL (rc-VLDL) se calcularon mediante la siguiente ecuación, usando CT y métodos de referencia para el c-LDL y el c-HDL: (rc-VLDL = CT - rc-LDL - rc-HDL). Para valores de dc-LDL <0,08 mmol / L (3 mg / dL) o cuando cc-LDL <0, se le asignó un valor de 0,05 mmol / L (2 mg / dL).
Las medidas de apoA-I y apoB se realizaron en muestras congeladas almacenadas a -70 ° C (entre 6 y 12 meses) y en una misma corrida utilizando un método de nefelometría, Dimensión Vista ® System (Siemens Healthcare Diagnostics). Para verificar la trazabilidad de los resultados se midieron en cuadriplicado, apoB IFCC/estándar de la OMS (SP3-08) y la apoA-I IFCC/estándar de la OMS (SP1-01), arrojando resultados cercanos a sus respectivos valores asignados [SP3 apoB-08: 118 mg / dL vs. media (DE) 117 (2.2) mg / dl; SP1-01 apoA-1: 150 mg / dL vs. 155 (3,7) mg / dL].
ANÁLISIS ESTADÍSTICO
Se utilizaron los programas estadísticos JMP Statistical Software (SAS Institute) y Analyze-it de Microsoft Excel (Analyze-it Software). El rendimiento de dc-LDL y cc-LDL en comparación con rc-LDL se evaluó mediante el uso de coeficientes de determinación y análisis ponderado de regresión de Deming. Se evaluó el rendimiento de los métodos para c-LDL en los participantes con concentraciones de TG <2,26 mmol / L (200 mg / dL) y entre 2,26 y 4,52 mmol / L (200 y 400 mg / dL) e incluyó tanto a los individuos enfermos como a los no enfermos. Los participantes fueron clasificados en categorías de riesgo de ECV en base a los criterios del NCEP (1) como se describe en el Suplemento de Datos que acompaña a la versión online de este artículo en http://www.clinchem.org/content/vol57/issue3. Se utilizó el test de McNemar para evaluar si la tasa de errores en la clasificación de los participantes con dc-LDL o cc-LDL, difiere significativamente de los medidos con el MR. Los datos nominales que se utilizan para el análisis fueron las tasas de clasificación errónea de McNemar para dc-LDL, cc-LDL, y no-c-HDL en comparación con sus MR. Para cada método, las tasas de errores de clasificación se compararon con sus métodos de referencia, como se describió previamente (13). Por ejemplo, consideramos una hipótesis nula planteando que cualquier método de dc-LDL dado no clasificaba erróneamente a los pacientes ni más ni menos frecuentemente que el cc-LDL correspondiente para cada método. Si las dos partes de esta hipótesis son rechazadas, se puede afirmar que hay equivalencia en la tasa de errores de clasificación.
Resultados
COMPARACIÓN DE LOS MÉTODOS DE c-LDL, DIRECTOS Y CALCULADO, PARA LAS MUESTRAS CON TG < 2,26 mmol/L (200 mg / dL)
Los coeficientes de determinación (R2) con rc-LDL variaron desde 0,85 hasta 0,99 para los ensayos de dc-LDLy0,96 a 0,98 para los ensayos de cc-LDL (Tabla I). Todos los ensayos también mostraron un sesgo relativamente pequeño, proporcional y fijo. Los resultados de dc-LDL y de cc-LDL de cada método se usaron para calcular el scorede clasificación de riesgo de ECV, de acuerdo con las categorías de riesgo del NCEP y compararlas con el score de clasificación de riesgo obtenido usando rc-LDL. La tasa de errores de clasificación de riesgo de ECV general osciló entre 5% y 17% para los métodos de cc-LDL y fue menor que lo observado para 5 de los 8 métodos correspondientes de dc-LDL, que tuvieron tasas de errores de clasificación entre 8% y 26%. Estadísticamente, los errores de clasificación obtenidos con Roche y Serotec fueron significativamente mayores con los métodos de dc-LDL comparando con sus correspondientes cc-LDL (p <0,05) (Roche: dc-LDL 20% vs cc-LDL 6%; Serotec dc-LDL 27% vs cc-LDL 7%). Sólo el cc-LDL calculado con el método de Wako mostró errores de clasificación mayores que su correspondiente método de dc-LDL (17% vs 8%) (p<0,05).
El porcentaje de individuos clasificados por los métodos dc-LDL en una categoría menor de riesgo en comparación con rc-LDL osciló entre el 3% y 26%, mientras que sólo 1% a 8% de los individuos fueron clasificados erróneamente en una categoría de mayor riesgo (Fig. 1). A excepción de los métodos dc-LDL de Denka y Wako, los métodos de dc-LDL clasificaron erróneamente más pacientes en un menor en lugar de una categoría de mayor riesgo. Sólo en dos casos, ambos ocurrieron con el método de UMA para dc-LDL, un individuo fue mal clasificado en más de 2 categorías de riesgo. En el caso de métodos de cc-LDL, no se observó un patrón consistente en cuanto a la dirección de los errores de clasificación (Fig. 1), tres métodos cc-LDL tuvieron un sesgo positivo y 4 tuvieron un sesgo negativo.
Tabla I. Métodos directo de colesterol LDL (dc-LDL) y cálculo de colesterol LDL (cc-LDL) en comparación con el método de referencia de colesterol LDL (rc-LDL).

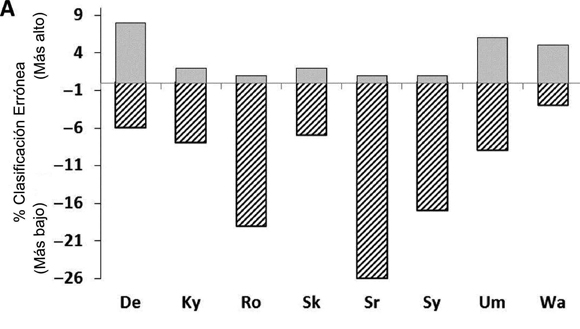


Figura 1. Tasa de clasificaciones erróneas de riesgo de ECV en los participantes con niveles de TG <2,26 mmol / L (200 mg / dL), n = 145. Se muestran los porcentaje de los resultados de los test que clasificaron tanto por encima (barra sombreada) o por debajo (barra entramada) de la categoría de riesgo, comparándolos con los MR, dc-LDL (A), cc-LDL (B), o no-c-HDL (C). De, Denka; Ky, Kyowa; Ro, Roche; Sr, Serotec; Sk, Sekisui, Sy, Sysmex; Um, UMA; Wa, Wako.
COMPARACIÓN DE LOS MÉTODOS DE c-LDL, DIRECTO Y CALCULADO, EN MUESTRAS HIPERTRIGLICERIDEMICAS
Este análisis (Tabla I) se limita a 20 individuos con concentraciones de TG entre 2,26 mmol/L (200 mg / dL) y 4,52 mmol/L (400 mg/dL), debido a la limitación conocida de la ecuación de Friedewald para las muestras hipertrigliceridémicas. En general, los métodos dc-LDL se desempeñaron mejor que sus correspondientes métodos de cc-LDL en esta población, evaluado por el error total o el porcentaje observado de acuerdo con la clasificación de puntuación de riesgo de ECV realizada con rc-LDL. Los métodos de cc-LDL también parecen mostrar un sesgo en la categorización de individuos en categorías de menor riesgo, en comparación con los métodos para dc-LDL (Tabla I y Suplemento online Fig. 1).
EVALUACIÓN DE LOS FACTORES QUE CONTRIBUYEN AL ERROR EN cc-LDL
En la Tabla II se presentan los datos de la contribución de los errores de métodos de dc-HDL en el cálculo de c-LDL. Para los pacientes con concentraciones de TG <2,26 mmol / L (200 mg / dL), los desvíos estándares residuales (Sy | x) para dc-HDL fueron relativamente bajos [rango 0,06-0,08 mmol / L (2,3 a 3,1 mg / dL)], excepto para el método de UMA (0,22 mmol / L, 8,5 mg / dL). Entre el 6% y el 20% de los valores para los métodos de dc-HDL superaron las metas de error total en pacientes con concentraciones de TG <2,26 mmol / L (200 mg / dL). Cuando se compara con rc-HDL para la clasificación de puntuación de riesgo de ECV, se observó un menor número de clasificaciones erróneas durante los ensayos de dc-HDL (Tabla II) que los que se observaron con los ensayos de dc-LDL (Tabla I). Sin embargo, todos los ensayos dc-HDL, con excepción de Sekisui, mostraron un incremento sustancial en el número de resultados que superaron las metas de error total, en pacientes con concentraciones de TG ≥2,26 mmol / L (200 mg / dL). El término TG (mmol / L) / 2,22, utilizado en la fórmula de Friedewald, proporciona una estimación del colesterol de VLDL y es otra fuente de error para el cc-LDL. Parte del error se debe a la imprecisión y el sesgo de la medición de TG, incluso si se resta el glicerol endógeno. Además, TG tiene una variabilidad biológica relativamente grande de aproximadamente el 20% CV, lo que también contribuye a los errores en el cálculo de c-LDL (14). En nuestra población, TG (mmol / L) / 2,22 y el colesterol de VLDL (n = 144, tras la exclusión de un valor atípico) mostraron una relación relativamente débil (R2 = 0,65) y una DE residual relativamente grande (Sy/x) [0,12 mmol / L (4,9 mg / dL)], incluso para aquellas personas con TG <2,26 mmol / L (<200 mg / dL) (Fig. 2 en el suplemento online), que es aproximadamente dos veces la cantidad de errores que contribuyeron los métodos de dc-HDL.
EL NO-c-HDL EN LA CLASIFICACIÓN DEL SCORE DE ECV
El no-c-HDL, que es una medida de colesterol asociado a todas las partículas que contienen apoB, fue examinado como una alternativa para la clasificación de score de riesgo de ECV (Tabla III y consultar la Tabla II en el suplemento online). El no-c-HDL no se ve afectado por los errores relacionados con la estimación de colesterol de VLDL, ni tampoco es afectado por la especificidad de los métodos para dc-LDL hacia otras lipoproteínas que contienen apo-B. Para los pacientes con concentraciones de TG <2,26 mmol / L (200 mg / dL), el no-c-HDL calculado utilizando métodos dc-HDL mostró una fuerte asociación (R2≥0,97) con el no-c-HDL calculado utilizando rc-HDL. El porcentaje de personas clasificadas usando los métodos no-c-HDL en una categoría de menor riesgo en comparación con el método de referencia para no-c-HDL osciló entre 0% y 11%, mientras que un 1% -8% fueron mal clasificados en una categoría de mayor riesgo. A excepción de método Wako para dc-LDL, los métodos de no-c-HDL mostraron en general menores errores de clasificación que los métodos de dc-LDL o los métodos de cc-LDL (Fig. 1). Para los pacientes con concentraciones de TG ≥2,26 mmol / L (200 mg / dL) y <4,52 mmol / L (400 mg / dL), los métodos no-c-HDL, en general, presentaron una mejor correspondencia con su MR que los métodos dc-LDL o cc-LDL (Suplemento online Fig. 1). El porcentaje de individuos mal clasificados en una categoría de menor riesgo osciló entre 0% y 7%, mientras que el 0% -18% fueron clasificados erróneamente en una categoría de mayor riesgo, lo cual fue mejor que lo observado, ya sea tanto para los métodos de dc-LDL como para los métodos de cc-LDL.
Tabla II. Método directo de colesterol HDL (dc-HDL) en comparación con el método de referencia de colesterol HDL (rc-HDL).
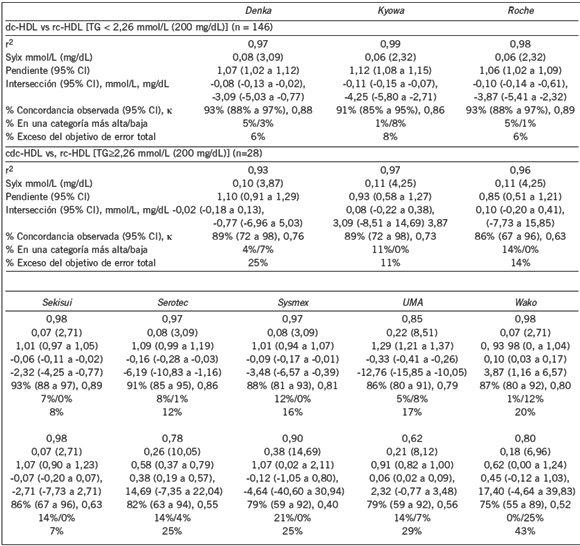
Tabla III. Comparación de los resultados y clasificación basados en colesterol no HDL (no-c-HDL) directo vs. no-c-HDL por el método de referencia (MR).

APOB Y APOA-I PARA LA CLASIFICACIÓN DEL SCOREDE ECV
Los valores de apoB correlacionaron débilmente con todos los métodos dc-LDL, y los coeficientes de determinación (R2) oscilaron entre 0,47 y 0,61 (Tabla III del Suplemento online). Los coeficientes de determinación entre apoB y rc-LDL fueron también relativamente bajos (R2 = 0,56). Sin embargo, el coeficiente de determinación entre apoB y no-c-HDL fue mejor, y osciló entre 0,83 y 0,84 (Tabla IV del Suplemento online). Cuando el no-c-HDL de referencia se comparó con la medida de apoB, el coeficiente de determinación fue de 0,86 (ver figura online 3A). La relación entre la apoA-I y rc-HDL fue bastante fuerte (R2 = 0,81) (Fig. online 3B). Sin embargo, las relaciones entre la apoA-I y los diversos métodos dc-HDL fueron muy variables, con coeficientes de determinación que oscilan entre 0,66 y 0,83 (Tabla V del Suplemento online).
Discusión
Una de las principales conclusiones de este estudio es que los métodos dc-LDL, en general, no ofrecen ventajas sobre cc-LDL en clasificar a los pacientes en categorías de riesgo según el NCEP en una población con dis-lipidemia, en comparación con rc-LDL. De hecho, para los pacientes con concentraciones de TG <2,26 mmol / L (200 mg / dL), los valores de cc-LDL basados en los métodos de Roche y Serotec para dc-HDL se acercan más al score del rc-LDL que sus correspondientes métodos dc-LDL. Los métodos de dc-LDL, sin embargo, parecen ser ventajosos sobre cc-LDL en el score de clasificación de riesgo de ECV para los pacientes con concentraciones de TG>2,26 mmol / L (200 mg / dL) (Tabla I y Tabla I online), debido al pobre desempeño de los métodos dc-HDL en muestras hipertrigliceridemicas (Tabla II) y las imprecisiones en la estimación del colesterol VLDL (Figura 2 online). Estos resultados sugieren que, desde un punto de vista práctico y económico, puede ser mejor usar cc-LDL para la clasificación en el subgrupo de pacientes con concentraciones de TG <2,26 mmol / L (200 mg / dl), debido a que no implican realizar la medición adicional de dc-LDL. Los métodos dc-LDL pueden reservarse para personas con concentraciones de TG≥ 2,26 mmol / L (200 mg / dL), en los que estos métodos por lo general mostraron una ventaja para la correcta clasificación de los pacientes.
Otros factores a tener en cuenta al momento de evaluar los métodos de dc-LDL y de cc-LDL para la clasificación de riesgo de ECV, es la variabilidad biológica intraindividual y además, la necesidad de ayuno antes de la toma de muestras. A pesar de la variabilidad biológica de las 3 variables, es decir, CT, TG y c-HDL, que afectan al cálculo de c-LDL, se ha demostrado que la variación intraindividual de cc-LDL es similar a la de dc-LDL [7,3% (0,6%) para cc-LDL y el 6,8% (0,5%) para dc-LDL] (8). Una medida precisa de cc-LDL también requiere que el paciente ayune antes de la toma de muestra (15)(16). Una ventaja potencial, por lo tanto, de los métodos de dc-LDL es su uso con muestras sin ayuno. Sin embargo, un estudio reciente de un método dc-LDL (autoanalizador Hitachi 917, Roche Diagnostics), mostró una falta de asociación del dc-LDL sin ayuno con el riesgo de ECV, lo que plantea dudas sobre la utilidad clínica de por lo menos este método de dc-LDL en pacientes sin ayuno (17)(18). Otro estudio que evaluó un método de dc-LDL (Sigma Diagnostics) también mostró tener un desempeño relativamente pobre en los pacientes sin ayuno (19). Otros estudios también revelaron en algunos pacientes una disminución fisiológica de los valores de c-LDL postprandial (15)(20)(21).
El tercer Panel de Tratamiento de Adultos de NCEP (ATPIII) recomienda actualmente el uso de no-c-HDL, que incluye el colesterol de todas las lipoproteínas que contienen apoB, como objetivo secundario de la reducción de lípidos para las personas con concentraciones de TG≥ 2,26 mmol / L (200 mg / dL) (1). En este estudio, no-c-HDL clasificó menos casos en forma errónea, independientemente de la concentración de TG, con respecto a lo que hicieron dc-LDL o cc-LDL, cuando se compararon con sus respectivos MR (Figura 1). Esta reducción en la tasa de errores de clasificación fue más pronunciada en los pacientes con concentraciones de TG> 2,26 mmol / L (200 mg / dL), en el que ambos métodos de dc-LDL y de cc-LDL mostraron un desempeño menos eficiente (Fig. online 1). También, el no-c-HDL requiere la medición de sólo dos analitos, en lugar de las 3 utilizadas para cc-LDL, reduciendo así los costos. Antes de que el no-c-HDL pueda ser recomendado como una prueba de screening primaria, sería importante establecer, no sólo una correspondencia superior con sus propios MR, sino también que el no-c-HDL es por lo menos equivalente al c-LDL para la predicción de ECV. En los pacientes diabéticos con aumento de TG, no-c-HDL ha demostrado en varios estudios ser efectivamente superior al c-LDL en la predicción de riesgo de ECV (22-24). Esto puede ser cierto porque las otras li-poproteínas que contienen apoB, que no sean LDL, como las lipoproteínas remanentes, también contribuyen significativamente a la patogénesis de la ateroscle-rosis en pacientes diabéticos. Varios estudios epidemiológicos también han demostrado que no-c-HDL, en la población general, es al menos equivalente o mejor que el c-LDL y apoB en la predicción de riesgo de ECV (25-B, 27, 28). En el Framingham Heart Study, se encontró que el no-c-HDL era superior al c-LDL en personas que tenían TG incrementados o dentro del intervalo de referencia (29)(30). Por otra parte, no-c-HDL es predictor de ECV aún en personas sin ayuno (29)(30). Un metaanálisis reciente de 68 estudios que incluyeron a más de 300 000 individuos encontró que los hazard ratio para ECV fueron equivalente para no-c-HDL y c-LDL, siendo el c-LDL calculado o medido directamente por diferentes métodos (31).
Las recientes guías de la American Diabetes Association y American College of Cardiology sugieren que la apo B puede ser superior al c-LDL como objetivo para el tratamiento de colesterol (32). También se ha demostrado, en algunos estudios, que la medida de apoA-I es equivalente o superior a la de c-HDL en la evaluación de riesgo de ECV (33)(34). Nuestros datos muestran que la apoB y apoA-I han reclasificado el 17% y el 13%, respectivamente, en una categoría de menor riesgo de ECV y el 22% y el 5%, respectivamente, en una categoría de mayor riesgo de ECV, en comparación con rc-LDL y rc-HDL (Tablas suplementarias online 3 y 5). Dado que en este estudio no estuvieron disponibles datos de resultados clínicos no se pudo evaluar la precisión clínica de la reclasificación por los dos métodos de apoproteínas. Otra limitación de este estudio fue que se utilizó sólo un método de apoB y de apoA-I, aunque estos métodos alcanzaron los valores estándar de la apoB (SP3-08) y apoA-I (SP1-01) de la IFCC/OMS. Un estudio prospectivo reciente, con objetivos finales clínicos, reveló que la apoB y apoA-I (Behring Nephelometer, BNII) no mejoró significativamente la reclasificación del riesgo, más que el basado en cc-LDL o c-HDL (autoanalizador RA-1000, Bayer Diagnostics) (35).
Es importante señalar que este estudio tiene varias limitaciones. El procedimiento de β-cuantificación para medir rc-LDL también puede ser sensible al colesterol de las lipoproteínas de densidad intermedia y de la lipoproteína (a) (2). Los métodos dc-LDL que son verdaderamente específicos para LDL pueden, por tanto, mostrar una tendencia negativa en comparación con rc-LDL realizado por β-cuantificación, como se observa en la mayoría de los métodos dc-LDL de este estudio. Sin embargo, esas otras lipoproteínas que contienen apoB que son también pro-aterogénicas (36, 37), contribuirían a los valores de cc-LDL y no-c-HDL, lo que puede explicar, al menos en parte, el mejor desempeño observado en el score de calificación de riesgo cardiovascular de estos marcadores. Otra limitación de este estudio fue que no todos los pacientes estaban en ayunas (71 participantes con ayuno <12 h), aunque un análisis por separado de esta población no mostró una diferencia significativa con los individuos en ayunas en cuanto a la exactitud de la calificación de riesgo de ECV por los distintos métodos (Tabla 6 de consulta online). Además, CT y TG se midieron utilizando sólo un método de rutina para cada uno, aunque la precisión de los métodos utilizados fue verificada por el Programa de Estandarización de Lípidos del CDC. Debido a que aproximadamente el 80% de las muestras en este estudio provienen de pacientes con dislipidemias, los resultados de este estudio pueden no ser aplicables a otras poblaciones, sin embargo, estos son los tipos de personas para las que una medida exacta de lípidos y lipoproteínas es más importante. Por último, el tamaño de la población estudiada fue relativamente pequeño (n = 175), en particular para el subconjunto de individuos con TG> 2,26 mmol / L (200 mg / dl) y <4,52 mmol / L (400 mg / dL) (n = 20).
En resumen, salvo para muestras hipertrigliceridémi-cas, 7 de los 8 métodos de dc-LDL no mejoran la precisión del score de clasificación de riesgo de ECV más que el cc-LDL. Esto es atribuible, al menos en parte, al hecho de que los métodos dc-HDL, en general, mostraron una mayor concordancia con su MR que los métodos dc-LDL. En general, el no-c-HDL, usando resultados de dc-HDL, mostró la mejor correspondencia con sus MR y una mejor concordancia en la clasificación de riesgo de ECV respecto a los métodos de dc-LDL y cc-LDL, tanto en muestras con TG bajos como altos. Deben realizarse futuros estudios estableciendo puntos finales clínicos para evaluar la utilidad clínica de los diversos métodos de medición directa de c-LDL y c-HDL y para resolver la in-certidumbre del significado clínico de las fracciones de las lipoproteínas que están siendo excluidas o medidas en esos ensayos directos en comparación con el MR por ul-tracentrifugación.
AGRADECIMIENTOS
Damos las gracias a Tonya Mallory por organizar el apoyo de los distribuidores en EE.UU.. Agradecemos también, la asistencia de los Dres. Todd Gehr, Daniel Carl, Vinnikova Anna, y Velimir Luketic y Carol Sargeant por el reclutamiento de pacientes en Virginia Commonwealth University. También agradecemos a Kara Dobbin del CDC por la realización de las mediciones del MR de colesterol.
Descargo de responsabilidad: Los resultados y conclusiones de este manuscrito son las del autor (es) y no necesariamente representan las opiniones de CDC/Agency for Toxic Substances and Disease Registry
9 abreviaturas no estándar: el c-LDL, colesterol LDL; ECV, enfermedades cardiovasculares; MR, el procedimiento de medición de referencia; rc-LDL, procedimientos de medición de referencia para el c-LDL; rc-HDL, procedimientos de medición de referencia para c-HDL; CT, colesterol total; c-HDL, colesterol de HDL; TG, triglicéri-dos; cc-LDL, colesterol de LDL calculado; dc-LDL, medición directa de colesterol LDL; NCEP, National Cholesterol Education Program; dc-HDL, medición directa de colesterol HDL; apo, apolipoproteína.
Contribuciones de los autores: Todos los autores confirmaron que han contribuido al contenido intelectual de este documento y han cumplido con los siguientes tres requisitos: (a) contribuciones significativas a la concepción y diseño, adquisición de datos, o análisis e interpretación de datos, (b) la elaboración o la revisión del artículo de contenido intelectual, y (c) la aprobación final del artículo publicado.
Revelaciones de los autores o potenciales conflictos de interés: Tras la presentación del manuscrito, todos los autores completaron el formulario la divulgación de los conflictos potenciales de interés. Posibles conflictos de interés:
Empleo o liderazgo: GT Miller, Clinical Chemistry, AACC; GL Myers, AACC.
Rol de consultor o Asesor: Ninguno declarado.
Propiedad de archivo: Ninguno declarado.
Honorarios: Ninguno declarado.
Financiación de la Investigación: G. Miller, investigador principal del proyecto: Denka Seiken, Kyowa Medex, Sekisui Medical, Serotec, Sysmex Internacional Reagents, UMA, y Wako Pure Chemical Industries donaron reactivos, calibradores y controles y han contribuido financieramente al Pacific Biometrics Research Foundation.
Genzyme y Ciencia Pointe aportó apoyo financiero a Pacific Biometrics Research Foundation. Pacific Biometrics Research Foundation concedió una subvención a la Virginia Commonwealth University (financiado por las contribuciones que se señalaron anteriormente). Roche Diagnostics donó reactivos, calibradores, controles, y un equipo Hitachi 917. H.E. Van Deventer, Warren Grant Magnuson Clinical Center, Programa de Investigación Intramural del National Institute of Health. A.T. Remaley, Warren Grant Mag-nuson Clinical Center, Programa de Investigación Intramural del National Institute of Health.
Testimonio experto: Ninguno declarado.
Papel del patrocinador: Las organizaciones financiadoras no jugaron ningún papel en el diseño del estudio, la elección de los pacientes reclutados, revisión e interpretación de datos, o la preparación o aprobación del manuscrito.
1. Executive Summary of the Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III). JAMA 2001; 285: 2486-97. [ Links ]
2. Nauck M, Warnick GR, Rifai N. Methods for measurement of LDL-cholesterol: a critical assessment of direct measurement by homogeneous assays versus calculation. Clin Chem 2002; 48: 236-54. [ Links ]
3. Nauck M, Wiebe D, Warnick GR. Measurement of high-density-lipoprotein cholesterol. In: N Rifai, GR Warnick, MH Dominiczak eds. Handbook of lipoprotein testing. 2nd ed. Washington, DC: AACC Press; 2000: 227-30. [ Links ]
4. Gordon T, Kannel WB, Castelli WP, Dawber TR. Lipoproteins, cardiovascular disease, and death. The Framingham study. Arch Intern Med 1981; 141: 1128-31. [ Links ]
5. Castelli WP, Doyle JT, Gordon T, Hames CG, Hjortland MC, Hulley SB, et al. HDL cholesterol and other lipids in coronary heart disease. The cooperative lipoprotein phenotyping study. Circulation 1977; 55: 767-72. [ Links ]
6. Myers GL, Kimberly MM, Waymack PP, Smith SJ, Cooper GR, Sampson EJ. A reference method laboratory network for cholesterol: a model for standardization and improvement of clinical laboratory measurements. Clin Chem 2000; 46: 1762-72. [ Links ]
7. Friedewald WT, Levy RI, Fredrickson DS. Estimation of the concentration of low-density lipoprotein cholesterol in plasma, without use of the preparative ultracentrifuge. Clin Chem 1972; 18: 499-502. [ Links ]
8. Schectman G, Patsches M, Sasse EA. Variability in cholesterol measurements: comparison of calculated and direct LDL cholesterol determinations. Clin Chem 1996; 42: 732-7. [ Links ]
9. Miller WG, Myers GL, Sakurabayashi I, Bachman LM, Caudill SP, Dziekonski A, et al. Seven direct methods for measuring HDL and LDL cholesterol compared with ultracentrifugation reference measurement procedures. Clin Chem 2010; 56: 977-86. [ Links ]
10. Sahu S, Chawla R, Uppal B. Comparison of two methods of estimation of low density lipoprotein cholesterol, the direct versus Friedewald estimation. Indian J Clin Biochem 2005; 20: 54-61. [ Links ]
11. Miller WG, Waymack PP, Anderson FP, Ethridge SF, Jayne EC. Performance of four homogeneous direct methods for LDL-cholesterol. Clin Chem 2002; 48: 489-98. [ Links ]
12. Warnick GR, Kimberly MM, Waymack PP, Leary ET, Myers GL. Standardization of measurements for cholesterol, triglycerides, and major lipoproteins. Lab Med 2008; 39: 481-90. [ Links ]
13. Lachenbruch PA, Lynch CJ. Assessing screening tests: extensions of McNemar's test. Stat Med 1998; 17: 2207-17. [ Links ]
14. Ricos C, Alvarez V, Cava F, Garcia-Lario J, Hernandez A, Jimenez CM, J, et al. Current databases on biological variation: pros, cons and progress. Scand J Clin Lab Invest 1999; 59: 491-500. [ Links ]
15. Cohn JS, McNamara JR, Schaefer EJ. Lipoprotein cholesterol concentrations in the plasma of human subjects as measured in the fed and fasted states. Clin Chem 1988; 34: 2456-9. [ Links ]
16. Rifai N, Merrill JR, Holly RG. Postprandial effect of a high fat meal on plasma lipid, lipoprotein cholesterol and apolipoprotein measurements. Ann Clin Biochem 1990; 27(Pt 5): 489-93. [ Links ]
17. Mora S, Rifai N, Buring JE, Ridker PM. Fasting compared with nonfasting lipids and apolipoproteins for predicting incident cardiovascular events. Circulation 2008; 118: 993-1001. [ Links ]
18. Mora S, Rifai N, Buring JE, Ridker PM. Comparison of LDL cholesterol concentrations by Friedewald calculation and direct measurement in relation to cardiovascular events in 27,331 women. Clin Chem 2009; 55: 888-94. [ Links ]
19. Yu HH, Ginsburg GS, Harris N, Rifai N. Evaluation and clinical application of a direct low-density lipoprotein cholesterol assay in normolipidemic and hyperlipidemic adults. Am J Cardiol 1997; 80: 1295-9. [ Links ]
20. Cohn JS, McNamara JR, Cohn SD, Ordovas JM, Schaefer EJ. Postprandial plasma lipoprotein changes in human subjects of different ages. J Lipid Res 1988; 29: 469-79. [ Links ]
21. Lund SS, Petersen M, Frandsen M, Smidt UM, Parving HH, Vaag AA, Jensen T. Sustained postprandial decrease in plasma levels of LDL cholesterol in patients with type-2 diabetes mellitus. Scand J Clin Lab Invest 2008; 68: 628-40. [ Links ]
22. Liu J, Sempos C, Donahue RP, Dorn J, Trevisan M, Grundy SM. Joint distribution of non-HDL and LDL cholesterol and coronary heart disease risk prediction among individuals with and without diabetes. Diabetes Care 2005; 28: 1916-21. [ Links ]
23. Lu W, Resnick HE, Jablonski KA, Jones KL, Jain AK, Howard WJ, et al. Non-HDL cholesterol as a predictor of cardiovascular disease in type 2 diabetes: the strong heart study. Diabetes Care 2003; 26: 16-23. [ Links ]
24. Jiang R, Schulze MB, Li T, Rifai N, Stampfer MJ, Rimm EB, Hu FB. Non-HDL cholesterol and apolipoprotein B predict cardiovascular disease events among men with type 2 diabetes. Diabetes Care 2004; 27: 1991-7. [ Links ]
25. Ingelsson E, Schaefer EJ, Contois JH, McNamara JR, Sullivan L, Keyes MJ, et al. Clinical utility of different lipid measures for prediction of coronary heart disease in men and women. JAMA 2007; 298: 776-85. [ Links ]
26. Ridker PM, Rifai N, Cook NR, Bradwin G, Buring JE. Non-HDL cholesterol, apolipoproteins A-I and B100, standard lipid measures, lipid ratios, and CRP as risk factors for cardiovascular disease in women. JAMA 2005; 294: 326-33. [ Links ]
27. Bittner V, Hardison R, Kelsey SF, Weiner BH, Jacobs AK, Sopko G. Non-high-density lipoprotein cholesterol levels predict five-year outcome in the Bypass Angio-plasty Revascularization Investigation (BARI). Circulation 2002; 106: 2537-42. [ Links ]
28. Cui Y, Blumenthal RS, Flaws JA, Whiteman MK, Langenberg P, Bachorik PS, Bush TL. Non-high-density lipoprotein cholesterol level as a predictor of cardiovascular disease mortality. Arch Intern Med 2001; 161: 1413-9. [ Links ]
29. Miller M, Ginsberg HN, Schaefer EJ. Relative athero-genicity and predictive value of non-high-density lipopro-tein cholesterol for coronary heart disease. Am J Cardiol 2008; 101: 1003-8. [ Links ]
30. Liu J, Sempos CT, Donahue RP, Dorn J, Trevisan M, Grundy SM. Non-high-density lipoprotein and very-low-density lipoprotein cholesterol and their risk predictive values in coronary heart disease. Am J Cardiol 2006; 98: 1363-8. [ Links ]
31. Di Angelantonio E, Sarwar N, Perry P, Kaptoge S, Ray KK, Thompson A, et al. Major lipids, apolipoproteins, and risk of vascular disease. JAMA 2009; 302: 1993-2000. [ Links ]
32. Brunzell JD, Davidson M, Furberg CD, Goldberg RB, Howard BV, Stein JH, Witztum JL. Lipoprotein management in patients with cardiometabolic risk: consensus statement from the American Diabetes Association and the American College of Cardiology Foundation. Diabetes Care 2008; 31: 811-22. [ Links ]
33. Kukita H, Hiwada K, Kokubu T. Serum apolipoprotein A-I, A-II and B levels and their discriminative values in relatives of patients with coronary artery disease. Atherosclerosis 1984; 51: 261-7. [ Links ]
34. Maciejko JJ, Holmes DR, Kottke BA, Zinsmeister AR, Dinh DM, Mao SJ. Apolipoprotein A-I as a marker of angiographically assessed coronary-artery disease. N Engl J Med 1983; 309: 385-9. [ Links ]
35. van der Steeg WA, Boekholdt SM, Stein EA, El-Harchaoui K, Stroes ES, Sandhu MS, et al. Role of the apolipoprotein B-apolipoprotein A-I ratio in cardiovascular risk assessment: a case-control analysis in EPIC-Norfolk. Ann Intern Med 2007; 146: 640-8. [ Links ]
36. Hackam DG, Anand SS. Emerging risk factors for atherosclerotic vascular disease: a critical review of the evidence. JAMA 2003; 290: 932-40. [ Links ]
37. Carmena R, Duriez P, Fruchart JC. Atherogenic lipoprotein particles in atherosclerosis. Circulation 2004; 109(23 Suppl 1): III2-7. [ Links ]














