Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Acta bioquímica clínica latinoamericana
Print version ISSN 0325-2957
Acta bioquím. clín. latinoam. vol.46 no.1 La Plata Jan./Mar. 2012
BIOQUÍMICA CLÍNICA
Investigación en Química de Productos Naturales en Argentina: Vinculación con la Bioquímica
Development and Research Trends in Chemistry of Natural Products in Argentina: Connection with Biochemistry and Clinical Biochemistry
Pesquisa em Química de Produtos Naturais na Argentina: Vinculagáo com a Bioquímica
Alicia Beatriz Pomilio1a
1. Doctora de la Universidad de Buenos Aires. Investigadora Superior de CONICET.
a. PRALIB-CONICET, Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires, Junín 956, C1113AAD Ciudad Autónoma de Buenos Aires, Argentina. e-mail: pomilio@ffyb.uba.ar
Resumen
En este trabajo se detallan las características y objetivos de la especialidad de Química de Productos Naturales, analizando los conocimientos requeridos de otras especialidades para realizar investigación en la misma. A través de un breve desarrollo histórico se puede observar la vinculación con varias ramas de la Química, como Química Orgánica, Química Biológica y Química Bioanalítica, así como Bioquímica Clínica, entre otras. Se brindan las perspectivas de esta especialidad, mostrando las tendencias en la investigación y en la industria química internacional. El trabajo multidisciplinario se evidencia en las aplicaciones presentadas en investigación.
Palabras clave: Productos naturales; Historia; Vinculación; Perspectivas
Summary
This article is focused on the characteristics and aims of the Chemistry of Natural Products analyzing the required knowledge from other fields to carry out research. Through a brief historical development, it can be observed that it is related with various branches of Chemistry, including Organic Chemistry, Biological Chemistry and Bioanalytical Chemistry as well as Clinical Biochemistry, among others. Prospects in this field are provided, showing trends in research and in the international chemical industry. A multidisciplinar approach is evident in the research projects shown herein.
Key Words: Natural products; History; Links; Prospects
Resumo
Neste trabalho sáo detalhadas as características e objetivos da especialidade de Química de Produtos Naturais, analisando os conhecimentos requeridos de outras especialidades para realizar pesquisa na mesma. Através de um breve desenvolvimento histórico é possível observar a vinculagáo com vários ramos da Química, como Química Orgánica, Química Biológica e Química Bioanalítica, bem como Bioquímica Clínica, dentre outras. Sáo oferecidas as perspectivas desta especialidade, mostrando as tendencias na pesquisa e na indústria química internacional. O trabalho multidisciplinar se evidencia nas aplicagóes apresentadas em pesquisa.
Palavras chave: Produtos naturais; Historia; Vinculagáo; Perspectivas
1. Características y objetivos de la especialidad
La Química de los Productos Naturales se refiere a la investigación en metabolitos secundarios o "metabolitos especiales" de fuentes naturales de origen vegetal, animal, marino, fúngico y bacteriano.
Se consideran Productos Naturales a todos los compuestos orgánicos provenientes del metabolismo secundario o también llamado metabolismo especial que, independientemente del peso molecular (PM), se producen en ese organismo vivo como respuesta ante las condiciones externas, ya sea: estrés hídrico, térmico, de superpoblación y radiante, siendo en general señales químicas frente a herbivoría, plagas, patógenos y simbiosis con otros organismos (1-4). Estos son justamente compuestos de interés porque poseen en su estructura química algunas subestructuras que son bioactivas en organismos animales, incluido el hombre.
La mayoría de estos compuestos orgánicos poseen PM bajo o intermedio y están representados por terpenoides y sus glicósidos, alcaloides, agliconas naturales, O y C-glicósidos de flavonoides, o bien, Oglicósidos acilados en distintas posiciones, biflavonoides, proantocianas diméricas y oligoméricas, principalmente. También se incluyen compuestos de alto PM, como por ejemplo: glico-péptidos, péptidos y proteínas que se forman bajo circunstancias determinadas y que no son consecuencia del metabolismo de base o primario. Por ejemplo: glicopéptidos por presencia de endofitos en plantas vasculares (5-8) o en ectoendomicorrizas de hongos superiores con árboles (9-12).
Las etapas requeridas para obtener los compuestos orgánicos de interés de la fuente natural adecuadamente identificada, consisten en: 1) Extracción, 2) Aislamiento, 3) Purificación, 4) Determinación estructural.
Diversas técnicas extractivas y cromatográficas están involucradas en cada una de estas etapas, en particular en las tres primeras. En cuanto a la cuarta etapa, ha dado lugar al desarrollo de la llamada Química Estructural, Química Orgánica Estructural, Química Orgánica Molecular, así como también Química Molecular Medicinal cuando se incluye la bioactividad y su relación con la estructura.
El siglo XIX correspondió al desarrollo de la Química Orgánica pura, mientras que el siglo XX fue el de la Biología y ramas relacionadas. Asimismo, en el siglo XX se desarrolló la Química Estructural, con tecnologías como: resonancia magnética nuclear (RMN), espectrometría de masas (EM) y técnicas cromatográficas como: cromatografía líquida de alta resolución (en inglés: high performance liquid chromatography: HPLC), cromatografía gas-líquido (CGL) y electroforesis capilar (EC).
Con esta integración de diversas ramas del conocimiento, que incluyen a la Bioquímica Clínica, Química Biológica, Química Orgánica, Físico-Química, Química Bioanalítica, Química Medicinal, Biología y Medicina, en el siglo XXI se produce el desarrollo de las "ómicas": Genómica, Proteómica, Metabolómica y Transcriptómica. Se produce la integración de la Biología, la Genética y el Comportamiento con la Química y además, con altas tecnologías: electroforesis capilar acoplada a espectrometría de masas (EC-EM), electroforesis capilar acoplada a resonancia magnética nuclear (EC-RMN), cromatografía líquida de alta resolución acoplada a espectrometría de masas tándem (HPLC-EM/EM), dentro de la disciplina de la Química de los Productos Naturales, que lleva en algunos casos al reemplazo del nombre original por los términos mencionados.
Ya elucidadas las estructuras químicas, en el caso de ser nuevas es deseable confirmarlas mediante síntesis o hemisíntesis, es decir prepararlas en el laboratorio con la estereoquímica correcta y proceder a la comparación del producto sintético y del producto natural.
A veces, el análisis conformacional requiere un estudio aparte y específico.
Si no se conoce la actividad biológica del o de los compuestos obtenidos, se puede proceder a realizar un screening farmacológico. Habiendo establecido la bioactividad se puede estudiar la relación experimental de estructura-actividad (modificación química del producto natural y observación de la respuesta biológica obtenida), lo cual permite determinar qué partes, o subestructuras, de la molécula son las responsables de la actividad observada.
A partir de este conocimiento y si la actividad lo justificara, se puede hacer el estudio de compuestos químicos equivalentes y/o análogos químicos, así como también el estudio de relación cuantitativa de estructura-actividad, conocido por la sigla QSAR del inglés quantitative structuCAICYTtivity relationship, sobre la familia o subfamilia de compuestos. También se pueden efectuar investigaciones con vistas a ahondar en su estructura electrónica.
En la Fig. 1 se resumen las diferentes etapas de la Química de los Productos Naturales conducentes a la obtención de un compuesto de aplicación biotecnológica.
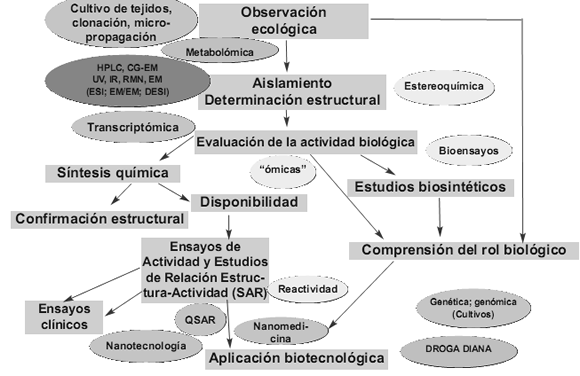
Figura 1. Etapas de la Química de los Productos Naturales conducentes a la obtención de un compuesto de aplicación biotecnológica.
2. Conocimientos requeridos de otras disciplinas
De acuerdo al ítem anterior, y ejemplificando el tema con los productos naturales de origen vegetal, se requieren conocimientos previos de Taxonomía, Botánica, Biología
General y Ecología para comprender las interacciones entre organismos y las señales químicas como respuesta al estrés. No obstante, el material vegetal en estudio es identificado por taxónomos especialistas, siendo necesario guardar ejemplares de herbario en instituciones reconocidas internacionalmente. En las publicaciones se detalla el nombre del taxónomo y el número de depósito del material de herbario y en qué institución se ha depositado.
La etapa de extracción y los distintos tipos de técnicas extractivas son objeto de estudio en Química Analítica, Química Orgánica y Química Biológica. Lo más común es el uso de extracción sólido-líquido tipo Soxhlet, pero también pueden usarse: extracción líquido-líquido, extracción líquido-líquido a gota a presión, extracción con fluidos supercríticos, entre otras.
Las etapas de aislamiento y purificación involucran la utilización de técnicas cromatográficas y electroforéticas, cromatografía líquida a presión atmosférica y a mediana presión, HPLC, CGL, EC y control de las fracciones obtenidas mediante cromatografía en capa delgada (del inglés thin-layer chromatography: TLC), CGL y HPLC. Se estudian en Química Analítica y Química Orgánica y algunas en Química Biológica. Estos procesos en mayor escala o en escala industrial se estudian en Química Industrial y en Ingeniería Química.
La elucidación estructural se puede realizar por métodos químicos y por técnicas espectroscópicas como 1H- y 13C-RMN mono y bidimensional (2D), EM de impacto electrónico (IE-EM), EM por bombardeo de átomos rápidos, conocido con la sigla FAB del inglés fast atom bombardment (FAB positivo y negativo), espectrometría de masas en condiciones ambientales con ionización por desorción con electrospray (DESI-EM; DESI: desorption electrospray ionization) (13), ultravioleta (UV), infrarrojo (IR), que se estudian y provienen de Química Orgánica, pero que se han extendido a Química Biológica y Bioquímica Clínica.
Bioactividades estudiadas
Las bioactividades de interés han sido: antitumoral (14), antiviral, antimicrobiana, antioxidante, anti-inflamatoria y antimicobacteriana (14), así como la quimioprevención (15).
La Farmacología y la Química Biológica están involucradas en las búsquedas sistemáticas de bioactividad y en los bioensayos que se realizan con los compuestos, así como en la relación entre la estructura química y la actividad biológica.
Los estudios de Estructura Electrónica y los estudios QSAR están vinculados con la Física, la Físico-Química y la Química Teórica.
Otras especialidades relacionadas
Fitoquímica, Farmacognosia, Desarrollo de Fármacos, Estudios Farmacocinéticos, de Farmacodinamia y de Fitoterápicos.
3. Origen de la especialidad: Relación con la Historia de la Ciencia en Argentina
La especialidad está directamente entroncada con la Química y en particular con la Química Orgánica y la Química Biológica. Asimismo, en la determinación de la bioactividad y estudios relacionados, importa la Clínica Médica y en especial la Bioquímica Clínica.
Sin duda que realizar estudios de Estructura Electrónica, Análisis Conformacional y aplicación de QSAR requiere conocimientos de Físico-Química, Física, Química Teórica y/o Química Computacional.
Si bien el desarrollo de la Ciencia en Argentina se remonta al siglo XVII en las órdenes religiosas, en particular los jesuitas, responsables de fundar la Universidad de Córdoba y el Colegio de Montserrat (1687), la contribución realizada en el siglo XX por Bernardo Houssay (primer Premio Nobel en Ciencias de Argentina) y Enrique Gaviola (primer astrofísico argentino de renombre internacional) (16) en el diseño de una política científica fue decisiva para el desarrollo de la Ciencia en Argentina (17).
En el siglo XVIII, una vez creado el Virreinato del Río de La Plata (1776), el segundo virrey Vértiz fundó el Protomedicato del Río de la Plata (1779), cuyo primer Protomédico fue el irlandés Miguel O'Gorman, que dio lugar a la primera Escuela de Medicina (1801) cuyos estudios seguían un plan similar al de la Universidad de Edimburgo. Cosme Argerich, médico y examinador del Protomedicato, fue el mentor y director del Instituto Médico Militar que luego pasaría a formar parte del Departamento de Medicina de la Universidad de Buenos Aires. En el siglo XIX se destacan los gobiernos de Bernardino Rivadavia y de Domingo Faustino Sarmiento en el desarrollo de la Ciencia de Argentina (18).
El desarrollo de la Medicina, la Bioquímica, Farmacia y Análisis Clínicos está intensamente relacionado con la especialidad de los Productos Naturales.
Se puede decir que el padre de la Química Orgánica en Argentina es Venancio Deulofeu, quien habiendo realizado la carrera de Química, llevó a cabo su Tesis Doctoral bajo la dirección del Dr. Alfredo Sordelli, un químico destacado en Química Biológica y Medicina. Al Dr. Deulofeu se debe el desarrollo de la especialidad en Productos Naturales en Argentina y gran parte de Iberoamérica.
La Bioquímica Clínica surgió a partir de dos grandes fuentes: el desarrollo de la investigación científica en Medicina y la aparición de disciplinas químicas como Química Orgánica y Química Fisiológica.
La introducción de la Química en las Ciencias Biológicas, el aislamiento, la purificación y la identificación de los Productos Naturales y la investigación de su metabolismo, favorecieron el establecimiento de la Bioquímica Clínica a fines del siglo XIX, como bien lo señala la Federación Bioquímica de la Provincia de Buenos Aires (www.faba.org.ar). Mientras los investigadores se interesaban por los fundamentos de la Química Fisiológica, los laboratoristas clínicos se orientaban a la aplicación con propósitos de diagnóstico.
La Bioquímica Clínica surgió luego como disciplina independiente, con objetivos claros de proporcionar información al médico para la preservación de la salud y el diagnóstico, prognosis y tratamiento de la enfermedad. Esta disciplina requiere no sólo la aplicación de fundamentos de Química y Medicina, sino también de Biología, Física, Matemática, Fisiología, Farmacología y Toxicología.
La primera Sociedad de Bioquímica Clínica fue la SociétéFrancaise de Biologie Clinique que surgió en Francia en 1942. Luego siguieron sociedades similares en otros países, pero, en realidad, tomó fuerza internacional la fundación de la Comisión de Química Clínica de la Sección de Bioquímica de la International Union of Pure and Applied Chemistry (IUPAC) en 1952, que finalmente dio lugar en 1964 a la cCAICYTión de la Federación Internacional de Química Clínica ( Internacional Federation of Clinical Chemistry: IFCC) afiliada a IUPAC.
Los países del continente americano poseen especialistas en Química/Bioquímica Clínica que forman parte de Asociaciones, Sociedades y Federaciones sólidas que contribuyen al desarrollo y permanencia de esta especialidad. Así por ejemplo, la Federación Bioquímica de la Provincia de Buenos Aires nuclea a los Bioquímicos/ Químicos Clínicos desde 1960, en que surgió como Federación de Especialistas de Análisis Biológicos de la Provincia de Buenos Aires. Posteriormente surgieron organizaciones vinculadas a la Federación, como la Confederación Unificada Bioquímica Clínica de la República Argentina (CUBRA) fundada en 1982 (www.faba.org.ar/pInformacionOrganizaciones.asp). CUBRA posee un Comité Ejecutivo constituido por representantes de las Sociedades Provinciales del país y es la entidad nacional representante de Argentina ante la Confederación Latinoamericana de Bioquímica Clínica (COLABIOCLI) y la IFCC.
El profesional dedicado a la Bioquímica Clínica además de desempeñarse en el laboratorio de diagnóstico clínico, puede desarrollar investigación científica en el área de bioquímica animal y vegetal, en farmacología molecular y bioquímica, en clínica orientada a la salud humana y animal y en problemas medio ambientales. También se desempeña en laboratorios de desarrollo e investigación de industrias relacionadas con productos químicos o productos naturales: fermentación, proteínas, hormonas, etc. y lleva a cabo el estudio nutricional de productos naturales y elaborados (19).
Entre los alcances del Título (anteriormente incumbencias) de la Bioquímica Clínica, además de realizar e interpretar análisis clínicos que contribuyan a la prevención, diagnóstico y tratamiento de las enfermedades de los seres humanos y a la preservación de su salud, se encuentran el desarrollo e interpretación de análisis de productos biológicos, como hormonas, enzimas y vacunas; la realización de estudios farmacológicos y toxicológicos; la posibilidad de trabajar con materiales radiactivos, infecciosos y tóxicos. Un profesional de esta especialidad estudia y desarrolla las metodologías para resolver los problemas tanto de la estructura como del funcionamiento de la materia viva, desde una perspectiva químico-biológica; además, posee conocimientos de fisiología animal y vegetal como para poder interpretar el funcionamiento de los procesos que regulan la vida normal y patológica, macro y microscópica (19). Gracias a esta disciplina, se efectúa la búsqueda y desarrollo de nuevos fármacos a partir de diversas fuentes naturales; de ahí su vinculación con la Química de los Productos Naturales.
En cuanto al desarrollo del conocimiento en el país, la ciencia continúa siendo objeto de orgullo del mismo. Según la revista Nature es uno de los 19 países que lideran proyectos y aumentaron sus presupuestos del área en 2006, y sigue siendo un líder regional, respaldado por su tradición científica (20) (21).
Su capacidad actual es relevante en Biomedicina, Nanotecnología, Energía Nuclear, Ciencias Agrarias, Desarrollo de Satélites, Biotecnología e Informática, así como en los proyectos de investigación subsidiados se incluyen Química Estructural, Bioquímica Clínica, Metabolómica, Genómica, Transcriptómica, Proteómica, QSAR, Estructura Electrónica y Bioinformática.
4. Perspectivas de la especialidad
Tendencias en investigación:
. Integración de trabajos interdisciplinarios en grupos multidisciplinarios de investigación.
Con el objeto de:
. Responder los interrogantes vinculados con la Biología y/o la Bioquímica: Explicar el mecanismo de acción o mostrar cuál es el comportamiento de un Producto Natural aislado de una planta, hongo, alga, animal marino o bacteria, a nivel celular o en otro organismo.
. Realizar estudios "holísticos" para evitar etapas de separación. Ejemplos: Espectros RMN y EM de extractos completos y analizarlos comparativamente y estadísticamente por análisis de componentes principales (principal component analysis: PCA), entre otros.
. Combinar técnicas separativas con detección espectral de alta resolución. Ejemplos: HPLC-EM/EM; EC-RMN.
Tendencias en la industria química internacional:
. Uso de la llamada Biotecnología Blanca (BB) que es considerada sustentable ya que utiliza materias primas renovables, es independiente del petróleo y del gas, se basa en reducir las emisiones de CO2 e involucra bajo potencial de riesgo o de peligro (22). Varias industrias internacionales utilizan BB con productos naturales de alto PM, en:
. Obtención de compuestos químicos vía biocatálisis: Nuevos procesos y productos catalizados por enzimas, como las lipasas. Ejemplos: nuevos monómeros, intermediarios quirales.
. Biopolímeros: Polímeros producidos por fermentación o síntesis biocatalítica. Ejemplos: polímeros renovables, polímeros especiales.
. Productos químicos vía fermentación: Compuestos químicos/monómeros producidos por microorganismos en base a materiales renovables. Ejemplo: ácido succínico.
. Productos biológicos eficientes: Nuevos productos basados en proteínas, enzimas y microorganismos. Ejemplos: modificación de superficies, ingredientes de cosméticos.
5. Resultados en el campo biomédico
Los Productos Naturales, en realidad compuestos químicos bioacticos provenientes de fuentes naturales, han dado origen a varios medicamentos alopáticos de relevancia internacional y continúan siendo una fuente invalorable de estructuras activas novedosas (23).
Todos los compuestos activos nuevos aprobados desde 1/1981 al 6/2006 para ser usados en medicamentos, y desde 1950 a 6/2006 para todas las drogas antitumorales aprobadas en el mundo correspondieron a 1184 (24), siendo un 56% productos naturales, análogos derivados o compuestos sintéticos derivados de productos naturales.
Así, en el área de cáncer, desde alrededor de la década de 1940 hasta la fecha, de las 155 moléculas pequeñas, el 73% no son de origen sintético, sino que provienen de o están inspiradas en estructuras de productos naturales, con un 47% que en realidad son productos naturales puros o derivados directamente de los mismos. En otras áreas, la influencia de las estructuras de productos naturales es muy marcada, como en los agentes antiinfecciosos. Aunque las técnicas de química combinatoria han tenido éxito como métodos de optimización de estructuras de muchos agentes aprobados, sólo se pudo identificar un único compuesto combinatorial de novo (Nexavar, Bayer) aprobado en este período de más de 25 años. Un número importante de medicamentos provenientes de productos naturales son producidos por microbios y/o interacciones microbianas con el "huésped de donde fue aislado".
De los productos naturales bioactivos de origen marino en el período 1965-2003, la fuente más importante provino de esponjas (31%) y corales (24%), seguidos por microorganismos (15%), ascidias (6%), moluscos (6%), algas marrones (5%), algas rojas (4%), algas verdes (1%) y otros (8%) (25) (26).
Asimismo, son fuente de medicamentos fitoterápicos o fitomedicamentos. La Organización Mundial de la Salud (OMS) estima que el 80% de la población mundial utiliza la medicina tradicional con fines terapéuticos (27). Pero, en realidad, los fitomedicamentos contemplan el uso de extractos o fracciones bioactivas, destacando la importancia de la sinergia de los compuestos en la acción terapéutica, mientras que la Química de los Productos Naturales se dedica más a la búsqueda, aislamiento e identificación estructural de los compuestos más activos para lograr un medicamento de uso alopático. Asimismo, es de interés modificar químicamente la estructura activa para lograr mayor acción farmacológica y menores efectos secundarios.
Algunas aplicaciones en el campo de los productos naturales
1. Estudios qsar en base a datos sobre la bioactividad de una serie de compuestos.
Ejemplo: Estudio QSAR de flavonoides y biflavonoides como inhibidores de neuraminidasa del virus H1N1 de influenza.
Se determinó recientemente un modelo QSAR y se realizó un análisis predictivo para la inhibición (IC50) de esta enzima por flavonoides y biflavonoides que podría servir como una guía para el diseño racional de nuevos inhibidores potentes y selectivos de esta familia de compuestos (28). Este estudio fue el primero realizado en este campo.
2. Estudio de las funciones metabolitos secundarios en la planta
Los metabolitos secundarios de origen vegetal se encuentran generalmente como mezclas de compuestos en compartimientos. Suelen variar en su concentración y presencia en las distintas partes de la planta y según la etapa de desarrollo. Algunos de ellos, ya presentes en la planta de origen, suelen activarse como compuestos de defensa o aumentar en su concentración, ante estímulos externos. También se producirán otros nuevos como mecanismo de defensa de la planta.
Los metabolitos secundarios actúan en los mecanismos de defensa, atracción y protección UV de la planta, así como en los fenómenos de alelopatía y como señalización de estrés (Fig. 2). Al ubicar el tipo de compuestos que actúan como defensa de la planta ante diferentes agentes y factores externos, se pueden obtener compuestos con esa actividad frente a los agentes determinados pero de acción externa a la planta, como por ejemplo: compuestos repelentes de insectos, antimicrobianos, de inhibición de germinación y de crecimiento (Fig. 2).

Figura 2. Función de los metabolitos secundarios en las plantas.
3. Hoy y hacia el futuro: transcriptómica y metabolómica
Las etapas de la transcriptómica son: análisis de datos por micromatrices: selección, normalización, escalado; encontrar los genes clave: hacer agrupamientos jerárquicos; análisis estadístico; verificación de los genes encontrados por qPCR; experimentos. Ejemplos: La variación natural explica la mayor parte de los cambios transcriptómicos entre las plantas transgénicas de maíz y las variedades que no han sido genéticamente modificadas, sometidas a dos prácticas agrícolas de fertilización nitrogenada (29). Se realizó transcriptómica epitelial nasal a distintos tiempos durante la exposición al polen natural de abedul en sujetos sanos y pacientes alérgicos (30).
El objetivo de la metabolómica es la identificación y cuantificación de todos los metabolitos en un organismo. La metabolómica basada en RMN tiene muchas aplicaciones en la ciencia vegetal. Se puede utilizar en la genómica funcional y para diferenciar plantas de diferente origen, o bien, después de diversos tratamientos. Recientemente se publicó un protocolo con los pasos siguientes de metabolómica vegetal utilizando espectroscopía RMN: preparación de la muestra (secado por congelación seguido por extracción por ultrasonido con CD3OD: bufferKH2PO4 (1:1) en D2O), análisis por RMN (1H-RMN estándar, espectro J-resuelto, espectroscopía de correlación 1H-1H (1H-1H correlation spectroscopy: COSY) y correlación heteronuclear de enlaces múltiples ( heteronuclear multiple bond correlation: HMBC) y métodos quimiométricos. La principal ventaja que presenta el análisis metabolómico por RMN es la posibilidad de identificar metabolitos mediante la comparación de los datos de RMN con referencias o por elucidación estructural mediante RMN bidimensional. Este protocolo es especialmente adecuado para el análisis de metabolitos secundarios, como compuestos fenólicos y para metabolitos primarios, como azúcares y aminoácidos (31).
La metabolómica también se usa para la diferenciación de especies cercanas de plantas medicinales. Choi et al. (32) compararon diez especies de Ilex con Ilex paraguariensis; 256 señales de RMN se redujeron a 10 CPs (componentes principales) y a análisis jerárquicos.
4. Nuevas estructuras más complejas en el mismo tipo de organismos
Ejemplo: Proantocianas diméricas y oligoméricas en plantas. Síntesis de las estructuras nuevas.
Se encontraron marcadores del tipo de fermentación y características de las cervezas que permitieron establecer estudios QSAR para su caracterización, con poder predictivo (33). Asimismo, en la cerveza se encuentran proantocianas diméricas del tipo B, que son antioxidantes, inmunomoduladores y antiinflamatorios. En cambio, las proantocianidinas oligoméricas (OPC: Oligomeric Proanthocyanidin Complexes) son abundantes en las uvas y el vino y son antioxidantes 20 veces más fuertes que la vitamina C y 50 veces más fuertes que la vitamina E. Se estudiaron también marcadores en jugos y concentrados cítricos (34).
5. Estudio de la estructura electrónica y análisis conformacional. Estudios topológicos
Las proantocianidinas diméricas del tipo A fueron sintetizadas hace un tiempo (35) (36). Recientemente, se calcularon los correspondientes mapas del potencial electrostático molecular (MEP: molecular electrostaticpotential) con los valores en unidades atómicas (u.a.) para los rotámeros Z-1 y Z-2 de la estructura central de estos compuestos (37). También se determinaron las interacciones entre los sustituyentes y la correspondiente CAICYTtividad (38)
6. Estudiar estructuras más complejas: ciclopéptidos
Los péptidos cíclicos o ciclopéptidos se encuentran en hongos superiores, plantas superiores, mamíferos, bacterias, arañas, entre otros. Pueden actuar como antibióticos, toxinas, reguladores del transporte iónico, inhibidores de la fijación de proteínas, inhibidores enzimáticos e inmunosupresores. Presentan las siguientes bioactividades: antimicrobiana, anti-inflamatoria, insecticida y acaricida, hepatotóxica, antineoplásica, uterotónica, estrogénica, sedante, antimalárica, nematicida, inmunosupresora e inhibitoria de la enzima de conversión de angiotensina I. Poseen efectos inhibitorios sobre tirosinasa y formación de melanina. Son inhibidores de proteinasas e instrumentos de investigación.
Se llevó a cabo el aislamiento y la detección de ciclopéptidos en distintos géneros y especies de hongos superiores (Basidiomicetes). También se hizo la determinación conformacional de los mismos y la relación de MEPs y momentos dipolares con la toxicidad (9-12) (39).
7. Interacción entre familiasIias de compuestos
Se estudió la interacción proteína-proteína y proteína-péptido a través de la CAICYTtividad cruzada de amanitinas y venenos de abejas y serpientes (8).
8. Determinación de amanitina en orina por electroforesis cailar de alta resolución (ECAR)
Se desarrolló un método para detectar amanitina en orina por electroforesis capilar automatizada de alta resolución con valor diagnóstico para intoxicaciones (40).
9. Ciclopéptidos en plantas superiores
Se estudiaron las estructuras de nonapéptidos cíclicos provenientes de plantas superiores, como por ejemplo: ciclolinopéptidos de semillas de Linum usitatissimum (Familia: Linaceae) (41) (42). Algunos presentaron actividad inmunosupresora. Recientemente, se lograron establecer las estructuras secundarias y terciarias de algunos de ellos (42).
10. Proteínas circulares o ciclótidos
Se conocen también ciclopéptidos que poseen de 14 a 70 aminoácidos (43). Ejemplos: Microcina J25 (21 aminoácidos): excretada por Escherichia coli AY25. Antibiótico. Bacteriocina AS-48 (70 aminoácidos): proveniente de Enterococcus faecalis subsp. liquefaciens S-48. Antibiótico (contra bacterias Gram positivas y negativas). SFTI- I (sunflower trypsin inhibitor-1) (14 aminoácidos): ciclopéptido de las semillas de girasol (Helianthus annuus). Presenta una unión disulfuro. Inhibidor de tripsina más potente que cualquier otro péptido natural. Es la proteína circular más pequeña encontrada hasta ahora. Posee
una secuencia y conformación similares a los inhibidores de Bowman-Birk (Bowman-Birk inhibitors: BBIs) que son inhibidores de serínproteasas de semillas de Fabaceae y otras, que están involucrados en los mecanismos de defensa de las plantas y también tienen potencial como agentes quimiopreventivos del cáncer. RTD-1 (Rhesus theta defensin) (18 aminoácidos): de leucocitos de Macaca mulatta (mono Rhesus). Presenta tres uniones disulfuro (arreglo tipo escalera). Antibiótico. Los 3 RTD representan el primer ejemplo de un nuevo tipo de defensinas de mamíferos.
Como SFTI-1 imita el loop inhibidor de tripsina de los bien estudiados BBIs resultó de interés examinar sus importantes características estructurales y funcionales. SFTI-1 posee un bucle de enlace ( binding loop) que se une con un puente disulfuro y con un bucle de péptido secundario ( secondary peptide loop) conforman el esqueleto circular. El bucle secundario estabiliza el bucle de unión como consecuencia de las variaciones de la secuencia (44). El análisis mutacional de SFTI-1 define claramente la naturaleza optimizada del esqueleto de SFTI-1 y demuestra la importancia del bucle o circuito secundario ( secondary loop) para mantener la conformación activa del bucle de unión (binding loop) (44).
11. Diversas bioactividades de los compuestos en estudio. Si se contraponen, modificar la estructura para que prevalezca la actividad deseada
En los péptidos antimicrobianos existen actividad hemolítica y actividad antimicrobiana. Por lo tanto, para su uso clínico se deben modificar, mediante la formación de análogos, para disminuir la actividad hemolítica.
Los péptidos antimicrobianos son un antiguo sistema inmunológico, constituido por pequeñas proteínas de carga catiónica, que participan en la defensa inmune innata del huésped. Ejemplos: lisozima; fosfolipasa A; catepsinas. Son compuestos catiónicos y anfipáticos que permeabilizan las membranas mediante adhesión e inserción en las mismas. Las aplicaciones que actualmente se conocen de estos péptidos antimicrobianos se pueden resumir en: a) Antifúngicos (contra Candida, Cryptococcus, Aspergillus); b) antiparasitarios (contra Malaria, Leishmania, Trypanosoma); c) antivirales (contra virus del Herpes, virus de la influenza, HIV); d) antibacterianos (contra bacterias Gram positivas y negativas. Ejemplo: Indolicidina cíclica. Aplicación Clínica: para el tratamiento de Acné, Candidiasis (12).
12. Estudiar metabolismo de productos naturales in vivo
Se realizan estudios metabólicos mediante imágenes en cámara gamma y SPECT. De esta manera se estudian: a) Vías metábolicas in vivo. Biodistribución; b) pasaje de la Barrera Hemato-Encefálica (BHE). Se utilizan 99m-Tc (t1/2: 6 h), 131-I (t1/2: 7 días), entre otros radionucleídos.
Se puede ver cuánto tarda en ser eliminado el compuesto en estudio de cada región de interés. Ejemplos: cerebro, hígado y riñones, estableciendo la cinética del compuesto in vivo sin sacrificar animales (45-49).
Los péptidos antimicrobianos marcados pueden ser candidatos promisorios para discriminar entre infecciones e inflamaciones, ya que estos compuestos suelen mostrar preferencia de unión a microorganismos.
AGRADECIMIENTOS
La autora agradece a sus colaboradores actuales: Dr. Andrew Mercader, Dra. Elvira Falzoni, Dr. Víctor Szewczuk, Méd. Farm. Stella M. Battista, Ing. Agr. Eduardo Bernatené, Méd. Jorge O. Ciprian Ollivier, Lic. Pablo Outumuro, Dra. Rosana Lobayan, Dr. Miguel Giraudo, Dra. Marta Vacchino. Las marcaciones se realizan en colaboración con: Prof. Dr. Arturo A. Vitale (Química Orgánica Sintética) y Dr. Carlos Cañellas (Radiofarmacia). Se agradece el apoyo financiero de CONICET (Argentina), Universidad de Buenos Aires (UBA) (Argentina) y Fundación Alexander von Humboldt (Humboldt-Stiftung, Alemania).
CORRESPONDENCIA
Prof. Dra. Alicia B. Pomilio
Directora del Area Química Estructural y Espectroscopía RMN
Del PRALIB (UBA y CONICET)
pomilio@ffyb.uba.ar
abpomilio@sinectis.com.ar
Tel.: (011) 4814-3952
1. Fontana JD, Lancas FM, Passos M, Noseda M, Pomilio AB, Vitale A, et al. Selective polarity- and adsorption-guided extraction/purification of Annona sp. polar acetogenins and biological assay against agricultural pests. Appl Biochem Biotechnol 1998; 70/72 (1): 67-76. [ Links ]
2. Pomilio AB, Leicach S, Yaber Grass M, Ghersa C, Santoro M, Vitale A. Constituents of the root exudate of Avena fatua grown under farinfrared-enriched light. Phytochem Anal 2000; 11: 304-8. [ Links ]
3. Malec L, Pomilio AB. Herbivory effects on the chemical constituents of Bromus pictus. Mol Med Chem 2003; 1: 30-8. [ Links ]
4. Leicach SR, Yaber Grass MA, Corbino GB, Pomilio AB, Vitale AA. Nonpolar lipid composition of Chenopodium album grown incontinously cultivated and nondisturbed soils. Lipids 2003; 38 (5): 567- 72. [ Links ]
5. Pomilio AB, Rofi RD, Gambino MP, Mazzini CA, Debenedetti de Langenheim RT. The lethal principle of Poa huecu (Coiron Blanco): A plant indigenous to Argentina. Toxicon 1989; 27 (12): 1251-62. [ Links ]
6. Casabuono AC, Pomilio AB. Festuca argentina and Festuca hieronymi: Chemical relationships between non-polar constituents. Biochem Syst Ecol 1996; 24 (3): 247-54. [ Links ]
7. Casabuono AC, Pomilio AB. Alkaloids from endophyte-infected Festuca argentina. J Ethnopharmacol 1997; 57 (1): 1-9. [ Links ]
8. Battista M, Rodríguez R, Vitale A, Pomilio AB, Albonico A, Alonso A. CAICYTtividad cruzada entre los venenos de serpiente, de abeja y las toxinas del hongo Amanita phalloides. Medicina-Buenos Aires 2004; 64 (1): 66-7. [ Links ]
9. Battista M, Vitale A, Pomilio AB. Relationship between the conformation of the cyclopeptides isolated from the fungus Amanita phalloides (Vaill. Ex Fr.) Secr. and its toxicity. Molecules 2000; 5 (3): 489-90. [ Links ]
10. Pomilio AB, Battista M, Vitale A. Semiempirical AM1 and ab initio parameters of the lethal cyclopeptides alpha-amanitin and its related thioether, S-sulphoxide, sulphone, and O-methyl derivative. J Mol Struct Theochem 2001; 536 (2-3): 243-62. [ Links ]
11. Pomilio AB, Battista ME, Vitale AA. Naturally occurring cyclopeptides: Structures and bioactivity. Curr Org Chem 2006; 10 (16): 2075-121. [ Links ]
12. Pomilio AB, Battista SM, Vitale AA. I. Quantitative structure-activity relationship (QSAR) studies on bioactive cyclopeptides. En: Castro EA, chief editor. QSPR-QSAR Studies on Desired Properties for Drug Design. Kerala, India: Research Signpost. Pandalai SG, Managing Editor; 2010. Chapter 1, p. 1-34.
13. Pomilio AB, Bernatené EA, Vitale AA. Desorption electrospray ionization ambient mass spectrometry. Espectrometría de masas en condiciones ambientales con ionización por desorción con electrospray. Acta Bioquím Clín Latinoam 2011; 45: 47-79.
14. Pomilio AB, Vacchino MN, Vitale AA. Antimycobacterial and antitumoral activities of argentine plants belonging to the Amaranthaceae family. En: Martino VS, Muschietti LV, editores. South American Medicinal Plants as a Potential Source of Bioactive Compounds. Kerala, India: Transworld Research Network, General Manager: Sudarsan NJ, distributed by American Technical Publishers Ltd., Herts, Hitchin, Inglaterra; 2008. Chapter 5, p. 73-113.
15. Vitale AA, Bernatené EA, Pomilio AB. Carotenoids in chemoprevention: Lycopene. Carotenoides en quimioprevención: Licopeno. Acta Bioquím Clín Latinoam 2010; 44 (2): 195-238.
16. Bernaola O. Enrique Gaviola y el Observatorio Astronómico de Córdoba. Su impacto en el desarrollo de la ciencia argentina. Buenos Aires: Saber y Tiempo; 2001.
17. Bunge M. Ciencia e ideología en el mundo hispánico. Buenos Aires: Interciencia; 2001. 11:3, p. 120-5.
18. Orione J. Historia crítica de la Ciencia Argentina (del proyecto de Sarmiento al reino del pensamiento mágico). Buenos Aires: Capital Intelectual (CI); 2008.
19. Arca MA. El ejercicio profesional bioquímico en Latinoamérica y en Argentina. Acta Bioquím Clín Latinoam 2008; 42 (3): 339-59.
20. Nature [News in Brief]. Argentina sets up a ministry of science. Nature 2007; 450 (7170): 598.
21. Dalton R. Argentina: The come back. Argentina's government has pledged to reverse a decadeslong scientific brain drain. Nature 2008; 456 (7221): 441-2. [ Links ]
22. Frazzetto G. White biotechnology. EMBO reports 2003; 4 (9): 835-7. [ Links ]
23. Mongelli ER, Pomilio AB. Nuevos medicamentos y et-nomedicina: Del uso popular a la industria farmacéutica. Ciencia Hoy 2002; 12 (68): 52-66. [ Links ]
24. Newman DJ, Cragg GM. Natural products as sources of new drugs over the last 25 years. J Nat Prod 2007; 70 (3): 461-77. [ Links ]
25. Blunt JW, Copp BR, Munro MHG, Northcote PT, Prinsep MR. Marine natural products. Nat Prod Rep 2005; 22 (1): 15-61.
26. Blunt JW, Copp BR, Hu WP, Munro MHG, Northcote PT, Prinsep MR. Marine natural products. Nat Prod Rep 2008; 25 (1): 35-94.
27. Medicina Tradicional -Necesidades Crecientes y Potencial. Perspectivas políticas sobre medicamentos de la OMS. Documento No. 2: pág. 1-6, Mayo de 2002, 1-6, Organización Mundial de la Salud (OMS), Ginebra, Suiza.
28. Mercader AG, Pomilio AB. QSAR study of flavonoids and biflavonoids as influenza H1N1 virus neuraminidase inhibitors. Eur J Med Chem 2010; 45 (5): 1724-30.
29. Coll A, Nadal A, Collado R, Capellades G, Kubista M, Messeguer J, et al. Natural variation explains most transcriptomic changes among maize plants of MON810 and comparable non-GM varieties subjected to two N-fertilization farming practices. Plant Mol Biol 2010; 73 (3) : 349-62. [ Links ]
30. Mattila P, Renkonen J, Toppila-Salmi S, Parviainen V, Joenvaara S, Alff-Tuomala S, et al. Time-series nasal epithelial transcriptomics during natural pollen exposure in healthy subjects and allergic patients. Allergy 2010; 65 (2): 175-83.
31. Kim HK, Choi YH, Verpoorte R. NMR-based metabolomic analysis of plants. Nature Protocols 2010; 5 (3): 536-49.
32. Choi YH, Sertic S, Kim HK, Wilson EG, Michopoulos F, Lefeber AWM, et al. Classification of Ilex species based on metabolomic fingerprinting using nuclear magnetic resonance and multivariate data analysis. J Agric Food Chem 2005; 53 (4): 1237-45.
33. Pomilio AB, Duchowicz PR, Giraudo MA, Castro EA. Amino acid profiles and quantitative structure-property relationships for malts and beers. Food Res Int 2010; 43 (4) : 965-71. [ Links ]
34. Pomilio AB, Giraudo MA, Duchowicz PR, Castro EA. QSPR Analyses for aminograms in food: Citrus juices and concentrates. Food Chemistry 2010; 123 (3): 917-27.
35. Pomilio A, Müller O, Schilling G, Weinges K. Zur Kenntnis der Proanthocyanidine, XXII. Über die Konstitution der Kondensationsprodukte von Phenolen mit Flavylium-salzen. Justus Liebigs Ann Chem 1977; 597-601.
36. Pomilio A, Ellmann B, Künstler K, Schilling G, Weinges K. Naturstoffe aus Arzneipflanzen, XXI. 13C-NMR-spek-troskopische Untersuchungen an Flavanoiden. Justus Liebigs Ann Chem 1977; 588-96.
37. Lobayan RM, Jubert AH, Vitale MG, Pomilio AB. Conformational and electronic (AIM/NBO) study of unsubstituted A-type dimeric proanthocyanidin. J Mol Model 2009; 15 (5): 537-50.
38. Bentz EN, Jubert AH, Pomilio AB, Lobayan RM. Theoretical study of Z isomers of A-type dimeric proanthocyanidins substituted with R=H, OH and OCH3: stability and CAICYTtivity properties. J Mol Model 2010; 16 (12): 1895-909.
39. Pomilio AB, Battista ME, Vitale AA. Estructuras de las toxinas de hongos superiores. Industria y Química 2006; (352): 19-27.
40. Battista SM, Pomilio AB, Vitale AA. Detección y cuantificación de ciclopéptidos tóxicos de Basidiomicetes por electroforesis capilar de alta resolución, para evaluación temprana de intoxicaciones. VI Congreso Argentino de la Calidad en el Laboratorio Clínico. IV Jornada Latinoamericana de la Calidad en el Laboratorio Clínico. CALILAB 2010. Puerto Madero, Buenos Aires, 3 al 5 de noviembre de 2010.
41. Morita H, Shishido A, Matsumoto T, Takeya K, Itokawa H, Hirano T, et al. A new immunosuppressive cyclic nonapeptide, cyclolinopeptide B from Linum usitatissimum. Bioorg Med Chem Lett 1997; 7 (10): 1269-72.
42. Battista SM, Pomilio AB. Estudios conformacionales y configuracionales de ciclolinopéptidos en muestras de semillas de Linum usitatissimum. XXVIII Congreso Argentino de Química y 4o. Workshop de Química Medicinal "Bicentenario de Mayo", Lanús, Pcia. de Buenos Aires, 13 al 16 de septiembre de 2010.
43. Craik DJ, Mylne JS, Daly NL. Cyclotides: macrocyclic peptides with applications in drug design and agriculture. Cell Mol Life Sci 2010; 67 (1): 9-16.
44. Daly NL, Chen Y-K, Foley FM, Bansal PS, Bharathi R, Clark RJ, et al. The absolute structural requirement for a proline in the P3'-position of Bowman-Birk protease inhibitors is surmounted in the minimized SFTI-1 scaffold. J Biol Chem 2006; 281 (33): 23668-75.
45. Argüelles MG, Rutty Solá GA, Cañellas CO, Viaggi ME, Vitale AA, Pomilio AB et al. HM-PAO-Tc-99m and other lipophilic agents for brain visualization (Part 1). Rev Argent Nuclear 1990; 4: 42-9.
46. Argüelles MG, Rutty Solá GA, Cañellas CO, Viaggi ME, Vitale AA, Pomilio AB, et al. HM-PAO-Tc-99m and other lipophilic agents for brain visualization (Part 2). Rev Argent Nuclear 1990; 4: 53-62.
47. Adonaylo VN, Stahl A, Cañellas CO, Pomilio AB, Vitale AA. Technetium-99m-dimethylglyoxime (99mTc-DMG) as renal imaging agent. J Labelled Compnds Radiopharm 1993; 33 (6): 443-53.
48. Vitale AA, Calviño MA, Ferrari CC, Stahl A, Pomilio AB. Preparation and biological evaluation of Technetium-99m-phenylethylamine complexes. J Labelled Compnds Radiopharm 1995; 36 (6): 509-19.
49. Vitale AA, Pomilio AB, Cañellas CO, Vitale MG, Putz EM, et al. In vivo long-term kinetics of /V,/V-dimethyltryptamine and tryptamine in brain by radioiodination planar imaging. J Nucl Med 2011; 52 (6): 970-7.
Aceptado para su publicación el 12 de agosto de 2011














