Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista argentina de microbiología
versión impresa ISSN 0325-7541versión On-line ISSN 1851-7617
Rev. argent. microbiol. v.38 n.3 Ciudad Autónoma de Buenos Aires jul./sep. 2006
M. A. López1*, G. F. Kusznierz1, M. S. Imaz1, R. Cociglio2, F. A. Tedeschi3, F. E. Zalazar3
1Instituto Nacional de Enfermedades Respiratorias "Emilio Coni", Blas Parera 8260 (3000) Santa Fe; 2Hospital de Niños "Dr. Orlando Alassia", Mendoza 4151, (3000) Santa Fe; 3Práctica Profesional, Facultad de Bioquímica y Ciencias Biológicas, Universidad Nacional del Litoral, Avda. Freyre 2150 (3000) Santa Fe, Argentina.
*Correspondencia. E-mail: marandlopez@hotmail.com
RESUMEN
El metapneumovirus humano (hMPV) es un nuevo agente causal de infección aguda del tracto respiratorio, recientemente reportado tras su hallazgo en niños, jóvenes, adultos y ancianos. Las manifestaciones clínicas producidas por el hMPV son indistinguibles de aquellas provocadas por los virus respiratorios clásicamente conocidos, y varían desde infección asintomática hasta neumonía complicada. Por otro lado, se han descrito casos de exacerbación de asma bronquial asociados a la infección con hMPV. En este trabajo se describe el caso de un niño hospitalizado que presentó una crisis asmática bronquial severa con sospecha de una infección viral asociada. Por el test de inmunofluorescencia indirecta no se detectaron virus sincicial respiratorio (VSR), adenovirus, virus influenza a - b ni virus parainfluenza 1, 2 y 3. En un intento por detectar la presencia de hMPV, se realizó una RT-PCR para la amplificación de los genes N y F con resultado positivo. Conforme a nuestro conocimiento, esta sería la primera descripción de un caso de exacerbación de asma asociado a hMPV en nuestra región. Los resultados de este estudio serían similares a los reportados por otros autores, quienes postulan que, a semejanza de lo que ocurre con el VSR, una infección por hMPV puede gatillar una enfermedad respiratoria crónica, como el asma.
Palabras clave: hMPV, RT-PCR, crisis asmática bronquial severa
ABSTRACT
Human Metapneumovirus (hMPV) associated to severe bronchial asthmatic crisis. Human Metapneumovirus (hMPV) is a recently reported agent of acute infection in the respiratory tract. It has been found in children as well as in young adults and elders. The clinical manifestations produced by hMPV are indistinguishable from those by common respiratory virus, and can evolve from asymptomatic infection into severe pneumonia. On the other hand, some authors have described cases of bronchial asthma exacerbation associated with hMPV infection. In this work we report a case of a child who presented a severe bronchial asthmatic crisis with a suspected viral associated infection. Immunofluorescence tests yielded negative results for sincitial respiratory virus, adenovirus, a-b influenza virus and parainfluenza 1, 2, 3, virus. In an attempt to detect the presence of hMPV, a RT-PCR was carried out to amplify sequences from both N and F genes. Using this approach, a positive result for hMPV was obtained. To our knowledge, this is the first description of a case of asthma exacerbation associated to hMPV in our region. In addition, these results are similar to previous reports where it was hypothesized that, like RSV, hMPV can trigger a respiratory chronic disease as asthma.
Key words: hMPV, RT-PCR, severe bronchial asthmatic crisis
El metapneumovirus humano (hMPV) se ha descrito recientemente como un nuevo agente causal de infección aguda del tracto respiratorio (IRA), tras su hallazgo en niños, jóvenes, adultos y ancianos. En Holanda un grupo de investigadores (11) reveló la presencia del virus en niños con infección respiratoria, en los que estudios destinados a detectar otros virus respiratorios fueron negativos. Análisis serológicos retrospectivos revelaron que niños menores de 5 años de edad han sido infectados por este virus, que ha estado circulando durante más de 43 años en algunas poblaciones (11).
El hMPV pertenece a la familia Paramyxoviridae, subfamilia Pneumovirinae, género Metapneumovirus. Posee un ARN de cadena simple de polaridad negativa, no segmentado, y carece de los genes que codifican para las proteínas no estructurales NS1 y NS2, lo que lo diferencia del virus sincicial respiratorio o VSR (11). Análisis filogenéticos han demostrado la presencia de dos grupos genéticos predominantes, reconocidos como A y B, los que a su vez se subdividen en dos subgrupos, 1 y 2 (12, 13). El virus descrito en Holanda en el 2001 se ha encontrado además en otros países, como Australia, Canadá, Estados Unidos, Francia, Reino Unido, España y Japón, y también en diversas regiones de Latinoamérica (14). En Buenos Aires (Argentina), Galiano et al. (2004) comunicaron las primeras evidencias de la presencia de hMPV en niños con infecciones respiratorias agudas bajas (3). La presentación del hMPV ocurre principalmente en los meses de invierno y a principios de primavera, con similitud epidemiológica al VSR. Las manifestaciones clínicas de los niños infectados son indistinguibles de aquellas provocadas por los virus respiratorios clásicamente conocidos, y varían desde una infección asintomática hasta neumonía complicada. Los intentos de diagnóstico de infección por hMPV mediante cultivo celular, serología, inmunofluorescencia y microscopía electrónica revelaron baja sensibilidad y especificidad, mientras que las técnicas moleculares para la detección de ácidos nucleicos parecen ser el método de elección. En este sentido y como ocurre con otros patógenos, la reacción en cadena de la polimerasa (PCR) acoplada a una transcripción reversa (RT-PCR) sería de utilidad para el diagnóstico (14). Dado que recientemente se han publicado cuadros de exacerbación de asma asociados a la infección por hMPV (8, 15), en este trabajo describimos el caso de un paciente pediátrico que tuvo que ser hospitalizado por un episodio agudo de asma bronquial con sospecha de una infección viral concomitante, negativo para los virus habitualmente responsables de IRA pero positivo para hMPV.
El paciente estudiado fue un niño de 4 años y 6 meses, admitido en el Hospital de Niños de Santa Fe "Dr. Orlando Alassia" a causa de un cuadro de crisis asmática aguda, con fiebre, accesos de tos catarral y agitación. Debido a los síntomas clínicos que presentó el paciente, compatibles con una infección respiratoria viral concomitante, una muestra de aspirado nasofaríngeo (HOA465) fue obtenida al día siguiente de la admisión por el Servicio de Guardia del Hospital. Una alícuota de la muestra fue conservada a –20 °C hasta la purificación de ARN y el resto se utilizó para la búsqueda inicial de virus respiratorio sincicial, adenovirus, virus influenza a y b y virus parainfluenza 1, 2 y 3 por inmunofluorescencia indirecta, empleando anticuerpos monoclonales con un revelado mediante la adición de una IgG de cabra anti IgG de ratón, conjugada a isotiocianato de fluoresceína (Chemicon International, CA, USA).
Para la búsqueda de hMPV, el ARN fue extraído a partir de 500 µl del aspirado, utilizando el reactivo comercial Trizol® y siguiendo las instrucciones del fabricante (Invitrogen Life Tech, Carlsbad, CA, USA). En el ensayo de transcripción reversa, en un primer paso se incubó el ARN a 65 °C durante 5 min, a fin de eliminar estructuras secundarias. Luego se agregaron 200 U de la enzima M-MLV (Promega, Madison, WI, USA); 100 pmol de primers arbitrarios; dNTPs 0,4 mM; Tris-HCl pH 8,3 50 mM; KCl 75 mM; MgCl2 3 mM y DTT 10 mM, en un volumen final de 25 µl, y se incubó a 37 °C durante 1 h. Finalizada esta incubación, las muestras fueron sometidas a 95 °C a fin de inactivar la enzima transcriptasa reversa.
Luego, para realizar la amplificación de los segmentos correspondientes a los genes N y F del hMPV, se trabajó con un volumen final de 25 µl y se utilizaron reactivos comerciales. La reacción se llevó a cabo en un medio que contenía buffer termofílico (Tris-HCl pH 9,0 10 mM, NaCl 50 mM y Tritón X-100); mezcla de dNTPs a una concentración equimolecular de 0,1 mM; MgCl2 en una concentración de 2 mM; 0,5 U de GoTaq® ADN polimerasa (Promega, Madison, WI, USA); 0,4 µM de cada uno de los primers y 2,5 µl de ADNc.
La siguiente es la descripción de las secuencias de primers utilizados:
hMPV -Nf: 5- TATATTCATGCAAGCTTACGG-3 (777-797, Gen Bank acceso Nº 371337)
hMPV-Nr: 5- CCCAACTTTGCAAGTGTTGTTC-3 (994-1013, Gen Bank acceso Nº371337)
hMPV-Ff: 5- GAGCAAATTGAAAATCCCAGACA-3 (3328-3350, Gen Bank acceso Nº371337) (2)
hMPV-Fr: 5-GAAAACTGCCGCACAACATTTAG-3 (3652-3674, Gen Bank acceso Nº371337) (2)
Se utilizó un termociclador marca Eppendorf Master-cycler® Personal (Wesseling-Berzdorf, Alemania), con las siguientes condiciones de ciclado: incubación inicial a 94 °C durante 10 min, hibridación a 55 °C por 5 min y extensión a 72 °C durante 2 min, seguida de 30 ciclos de 30 seg a 94 °C, 30 seg a 55 °C y 1 min a 72 °C. El último ciclo consistió en una incubación a 94 °C por 30 seg, a 55 °C durante 30 seg y una extensión final de 5 min a 72 °C.
Los productos de amplificación in vitro fueron resueltos en un gel de agarosa al 2% en presencia de bromuro de etidio (0,5 µg/ml) y visualizados bajo luz UV.
En cada reacción, desde el paso de transcripción reversa, se incluyeron los siguientes controles: un control de reactivos con agua en lugar de muestra, un control positivo (ARN obtenido a partir de un cultivo viral en células LLC-MK2) y un control negativo compuesto de un ARN no relacionado, purificado de células mononu-cleares de sangre periférica humana.
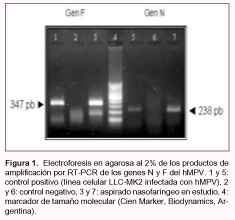
Al momento del ingreso hospitalario, el paciente presentaba, además de fiebre, tos catarral en accesos y agitación. A través de una radiografía se comprobó atrapamiento aéreo e infiltrado intersticial, por lo cual se procedió a su internación, que se prolongó por cuatro días. Durante este período se le suministraron corticoides, broncodilatadores y oxígeno. Posteriormente se le otorgó el alta clínica con buen estado general. Todos los ensayos para virus respiratorios que se le practicaron dieron resultados negativos. Al mismo tiempo, la búsqueda del hMPV se realizó en otra alícuota del aspirado nasofaríngeo por RT-PCR. Los blancos de amplificación fueron regiones conservadas dentro del genoma del hMPV (genes N y F). Cuando se utilizaron el par de primers correspondientes al gen N, se obtuvo una banda de 238 pb. De la misma forma, se visualizó una banda de 347 pb cuando se usó el par de primers seleccionados para amplificar un fragmento del gen F (Figura1). Estos resultados son similares a los comunicados en un caso de exacerbación de un cuadro asmático debido a hMPV en un paciente pediátrico. Se postula que, a semejanza de lo que ocurre con el VSR, una infección por hMPV puede gatillar una enfermedad respiratoria crónica como el asma (8, 15). Además, se ha comunicado recientemente que la infección por hMPV juega un rol decisivo en las exacerbaciones de asma agudo en adultos, lo que frecuentemente lleva a la hospitalización de los pacientes afectados (1, 4, 7, 10).
En el hemisferio sur, aun cuando se ha descrito que entre los niños hospitalizados con diagnóstico de IRA el porcentaje de detección de hMPV oscilaría entre el 5,4% y el 17% (3), no se conocen datos acerca de la asociación de este virus con la exacerbación de casos de asma. En consecuencia, esta sería la primera descripción en nuestra región de detección molecular de hMPV, asociada a un cuadro de crisis asmática. La definición de la importancia local del hMPV como causa de distintos síndromes clínicos, adquiriría fundamental importancia si se tiene en cuenta la hipótesis propuesta acerca de la existencia de diferentes subgrupos virales que podrían estar asociados a síndromes de variada gravedad (5, 6, 9). Así, la presencia y la intensidad de la circulación local de distintos subgrupos podrían determinar la importancia relativa del virus en los distintos cuadros clínicos.
Finalmente, acordamos con otros autores en que la aplicación de procedimientos de análisis molecular por RT-PCR permitirá una estimación más aproximada de la prevalencia e incidencia de infecciones por hMPV y, a la vez, aportará información adicional en la evaluación de las manifestaciones clínicas de estas infecciones respiratorias virales. Por otra parte, la implementación en forma rutinaria de la detección del hMPV disminuiría los casos de IRA de origen desconocido, lo que permitiría establecer en forma más acabada el papel que desempeña este virus en nuestro medio y facilitaría la elección de las conductas terapéuticas más apropiadas, orientadas a las subpoblaciones susceptibles.
Agradecimientos: a la Dra. Cristina Videla (CEMIC, Buenos Aires, Argentina), quien facilitó gentilmente una muestra de células LLC-MK2 infectadas con hMPV para la preparación de los controles positivos en las reacciones de PCR. A la Bioq. Alejandra Millán, División Inmunología y Banco de Sangre, Hospital de Niños "Dr. Orlando Alassia", Mendoza 4151, (3000) Santa Fe de la Vera Cruz, Pcia. de Santa Fe, Argentina.
BIBLIOGRAFÍA
1. Boivin G, Abed Y, Pelletier G, Ruel L, Moisan D, Cote S, et al. Virological features and clinical manifestations associated with human metapneumovirus: a new paramyxovirus res-ponsible for acute respiratory-tract infections in all age groups. J Infec Dis 2002; 186: 1330-4. [ Links ]
2. Falsey AR, Erdman D, Anderson LJ, Walsh EE. Human metapneumovirus infections in young and elderly adults. J Infect Dis 2003; 187: 785-90. [ Links ]
3. Galiano M, Videla C, Sánchez Puch S, Martínez A, Echavarría M,Carballal G. Evidence of human metapneumovirus in children in Argentina. J Med Virol 2004; 72: 299-303. [ Links ]
4. Maertzdorf J, Wang CK, Brown JB, Quinto JD, Chu M, de Graaf M, et al. Realtime reverse transcriptase PCR assay for detection of human metapneumoviruses from all known genetic lineages. J Clin Microbiol 2004; 42: 981-6. [ Links ]
5. Peiris JS, Tang WH, Chan KH, Khong PL, Guang Y, Lau YL, et al. Children with respiratory disease associated with metapneumovirus in Hong Kong. Emerg Infect Dis 2003; 9: 628-33. [ Links ]
6. Peret TC, Boivin G, Li Y, Couillard M, Humphrey C, Osterhaus ADME, et al. Characterization of human meta-pneumoviruses isolated from patients in North America. J Infect Dis 2002; 185: 1660-3. [ Links ]
7. Rawlinson WD, Waliuzzaman Z, Carter IW, Belessis YC, Gilbert KM, Morton JR. Asthma exacerbations in children associated with rhinovirus but not human metapneumovirus infection. J Infect Dis 2003; 187: 1314-8. [ Links ]
8. Schildgena O, Geikowskia T, Glatzela T, Simonb A, Wilkesmannb A, Roggendorfc M. New variant of the human metapneumovirus (hMPV) associated with an acute and severe exacerbation of asthma bronchiale. J Clin Virol 2004; 31: 283-8. [ Links ]
9. Stockton J, Stephenson I, Fleming D, Zambon M. Human metapneumovirus as a cause of community-acquired respiratory illness. Emerg Infect Dis 2002; 8: 897-901. [ Links ]
10. Van den Hoogen BG, van Doornum GJ, Fockens JC, Cornelissen JJ, Beyer WE, de Groot R, et al. Prevalence and clinical symptoms of human metapneumovirus infection in hospitalized patients. J Infect Dis 2003; 188: 1571-7. [ Links ]
11. Van den Hoogen BG, de Jong JC, Groen J, Kuiken T, De groot R, Fouchier RAM, et al. A newly discovered human pneumovirus isolated from young children with respiratory tract disease. Nat Med 2001; 7: 719-24. [ Links ]
12. Van Den Hoogen BG, Osterhaus ADME, Fouchier R. Clinical impact and diagnosis of human metapneumovirus infection. Pediatr Infect Dis J 2004; 23: S25-S32. [ Links ]
13. Van den Hoogen BG, Bestebroer TM, Osterhaus A, Fouchier RAM. Analysis of the genomic sequence of a human meta-pneumovirus. Virology 2002; 295: 119-32. [ Links ]
14. Williams JV. Human metapneumovirus: an important cause of respiratory disease in children and adults. Curr Infect Dis Rep 2005; 7: 204-10. [ Links ]
15. Williams JV, Crowe JE Jr, Enriquez R, Minton P, Peebles RS Jr, Hamilton RG, et al. Human metapneumovirus infection plays an etiologic role in acute asthma exacerbations requiring hospitalization in adults. J Infect Dis 2005; 192: 1149-53. [ Links ]
Recibido: 30/01/06
Aceptado: 14/08/06














