Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista argentina de microbiología
versión impresa ISSN 0325-7541versión On-line ISSN 1851-7617
Rev. argent. microbiol. v.39 n.2 Ciudad Autónoma de Buenos Aires abr./jun. 2007
Investigación de Trichomonas vaginalis durante el embarazo mediante diferentes metodologías
B. Perazzi1*, C. Menghi2, E. Coppolillo3, C. Gatta2, M. Cora Eliseht3, C. Vay1, O. Méndez2, H. Malamud De Rudavega3, R. De Torres4, A. Famiglietti1
1 Laboratorio de Bacteriología Clínica, y
2 Laboratorio de Parasitología, Departamento de Bioquímica Clínica, Hospital de Clínicas, Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires. Av. Córdoba 2351 (1120) Ciudad Autónoma de Buenos Aires, Argentina;
3 Sección del Tracto Genital Inferior, Primera Cátedra de Obstetricia, Hospital de Clínicas, Universidad de Buenos Aires. Av. Córdoba 2351 (1120) Ciudad Autónoma de Buenos Aires, Argentina;
4 Carrera de Especialización en Bacteriología Clínica, Facultad de Farmacia y Bioquímica, Universidad de Buenos Aires. Junín 956 (1113) Ciudad Autónoma de Buenos Aires, Argentina.
*Correspondencia. E-mail: hugodandrea@ciudad.com.ar
RESUMEN
Los objetivos del trabajo fueron conocer la prevalencia de tricomonosis en pacientes embarazadas y evaluar la utilidad de diferentes metodologías para su diagnóstico. Se estudiaron prospectivamente 223 mujeres embarazadas. Trichomonas vaginalis se investigó utilizando distintos exámenes microscópicos, cultivo en medio sólido y medio líquido. Se evaluó la sensibilidad y especificidad de la microscopía considerando a los cultivos en ambos medios como método de referencia. La prevalencia del parásito obtenida por cultivo (medio líquido más medio sólido) fue de 4,5% (10/223) siendo la detección por examen en fresco, coloración de May-Grunwald Giemsa, fresco con solución acética formolada (SAF)/azul de metileno y por cultivo en medio sólido y líquido de 1,3%, 1,8%, 1,8% y 4,5% respectivamente. La sensibilidad del examen en fresco fue 30%, para el May-Grunwald Giemsa y el SAF/azul de metileno fue 40%. Utilizando conjuntamente los tres exámenes microscópicos, la sensibilidad se elevó al 50% y la especificidad fue 100% para todos los exámenes microscópicos. El cultivo en medio líquido detectó el 100% de los casos positivos , mientras que el medio sólido sólo el 50%. Por la baja sensibilidad de la microscopía para T. vaginalis, en embarazadas asintomáticas recomendamos la utilización del cultivo en medio líquido durante el embarazo, para instaurar un tratamiento precoz.
Palabras clave: Investigación; Trichomonas vaginalis; Embarazo
ABSTRACT
Investigation of Trichomonas vaginalis through different methodologies during pregnancy. The aim of this study was to conduct a survey regarding the prevalence of trichomoniasis in pregnant patients and to evaluate the utility of different diagnostic methods. Two hundred and twenty three vaginal swab specimens from pregnant women were prospectively examined. Trichomonas vaginalis was investigated by various microscopic examinations, solid culture medium and liquid culture medium. The sensitivity and specificity of microscopy were evaluated by considering both culture media as the "gold standards". The prevalence of T. vaginalis obtained by both culture media (liquid plus solid media) was 4.5% (10/223). The prevalence of T. vaginalis obtained by direct smear, May-Grunwald Giemsa staining, sodium acetate-acetic acid-formalin (SAF)/Methylene blue staining-fixing technique, solid medium and liquid medium was 1.3%, 1.8%, 1.8% and 4.5%, respectively. The sensitivity of the direct smear was 30 %, but for the May- Grunwald Giemsa staining and the SAF/Methylene blue staining-fixing technique was 40%. Considering the three microscopic examinations altogether, the sensitivity rose to 50% and the specificity was 100% for all of them. The solid medium detected only 50% of the positive cases; the liquid medium detected 100%. Due to the low sensitivity obtained with microscopy in asymptomatic pregnant patients, we recommend the use of the liquid medium during pregnancy, in order to provide an early treatment.
Key words: Diagnosis; Trichomonas vaginalis; Pregnancy
INTRODUCCIÓN
Los cambios hormonales que se producen durante el embarazo predisponen a una mayor incidencia de infecciones del tracto genital inferior, lo que conlleva a complicaciones maternas y perinatológicas. El diagnóstico de la infección por Trichomonas vaginalis durante el embarazo reviste gran importancia ya que dicha infección predispone a rotura prematura de membrana, labor pretérmino y bajo peso al nacer (6, 17).
La tricomonosis es una enfermedad de transmisión sexual asociada con uretritis, vaginitis, cervicitis, enfermedad inflamatoria pélvica e infertilidad tubárica (3, 11, 12, 23, 25). Puede presentarse en forma asintomática en un 10 a un 50% de los casos, de los cuales un 50% podrían presentar síntomas de infección dentro de los 6 meses posteriores (8, 28). La mujer suele reinfectarse por contacto sexual con el hombre, que suele actuar como portador asintomático (13).
El diagnóstico de laboratorio por examen microscópico presenta baja sensibilidad (35-80%), sobre todo en pacientes asintomáticas, motivo por el cual es necesario implementar metodologías más sensibles (12, 15, 28). Tanto es así que, en el caso de las observaciones microscópicas en fresco, la detección de T. vaginalis depende de la experiencia del observador y de la rapidez en el transporte y procesamiento de la muestra, pues se debe evitar la pérdida de la movilidad del parásito (12). En consecuencia, el cultivo en medio líquido de T. vaginalis es considerado el método de mayor precisión (método de referencia) para el diagnóstico de tricomonosis (8, 9, 14, 20, 21, 26, 27).
Teniendo en cuenta la importancia de la detección de T. vaginalis durante el embarazo, los objetivos de este trabajo fueron:
1) Conocer la prevalencia de infección en mujeres embarazadas sintomáticas y asintomáticas.
2) Evaluar la utilidad de diferentes metodologías microscópicas directas en comparación con el cultivo, para el diagnóstico de tricomonosis en dichas mujeres.
3) Establecer asociaciones entre T. vaginalis y otros gérmenes.
MATERIALES Y MÉTODOS
Se analizaron 223 contenidos vaginales de pacientes embarazadas que concurrieron en forma consecutiva a la Sección del Tracto Genital Inferior de la Primera Cátedra de Obstetricia del Hospital de Clínicas en el período comprendido entre el 1 de agosto de 2005 y el 15 de enero de 2006 inclusive. A todas las pacientes se les realizó, además, examen clínico y colposcópico.
Este estudio fue aprobado por el Comité de Ética del Hospital de Clínicas.
El estudio microbiológico del contenido vaginal para el diagnóstico de tricomonosis y su asociación con otros gérmenes incluyó los siguientes exámenes:
1. Extendidos para coloración de Gram y May-Grunwald Giemsa prolongado. La coloración de May-Grunwald Giemsa se efectuó de la siguiente forma: a cada extendido se lo cubrió con colorante May-Grunwald puro durante 3 minutos, luego se lo enjuagó con agua destilada 1 minuto, y se lo cubrió con colorante de Giemsa diluido al décimo en agua destilada durante 90 minutos y finalmente se lo enjuagó con agua destilada.
2. Observación en fresco con 1 ml de solución fisiológica (SF).
3. Observación en fresco con solución acética formolada (SAF)/ azul de metileno (0,5 ml de azul de metileno y 0,5 ml de solución fijadora SAF) (5).
4. Determinación de pH de la secreción vaginal.
5. Observación en fresco con 1 ml de KOH al 10% y prueba de aminas. Ésta consistió en contactar el hisopo con la secreción vaginal con 1 ml de KOH al 10% e inmediatamente después percibir el olor desprendido. Se consideró dicha prueba positiva cuando se percibía un olor desagradable, producto de la volatilización de aminas.
6. Cultivo en medio líquido (tioglicolato modificado) para T. vaginalis, con incubación durante 7 dias a 37 °C en atmósfera de 5% de CO2 (21). Este medio contiene cada 1000 ml: peptona de caseína digerida (Laboratorios Britania, Bs. As., Argentina), 15 g; extracto de levadura (Oxoid Ltd., Hampshire, England), 12 g; glucosa (Merck, Darnstadt, Germany), 5,5 g; cloruro de sodio (Biopack, Bs. As., Argentina), 2,5 g; L-cystina (Biochemical BDH, Poole, England), 0,5 g; tioglicolato de sodio (Biochemical BDH, Poole, England), 0,5 g; agar (Biokar Diagnostic, Zac de Ther, Allonne, France), 0,75 g; y resazurina (Sigma Chemical Co., St. Louis, USA), 1 mg. El medio se autoclava y posteriormente se le agregan asépticamente 120 ml de suero equino inactivado (Laboratorio Gutiérrez, Bs. As., Argentina), 2 mg de anfotericina B (Gibco BRL Life Technologies, Paisley, Scotland), 1.000.000 U de penicilina G (Gibco BRL Life Technologies, Paisley, Scotland) y 80 mg de gentamicina (Gibco BRL Life Technologies, Paisley, Scotland). Se ajusta a pH de 7 ± 0,2. Se colocan 5 ml de medio en tubos de hemólisis con tapa a rosca.
7. Cultivo en medio sólido (agar Columbia modificado) para T. vaginalis, con incubación durante 7 días a 37 °C en atmósfera de anaerobiosis (27). Para la preparación de 400 ml de este medio, 13 g de agar Columbia (Oxoid Ltd., Hampshire, England), 4 g de dextrosa (Mallinkrodt, St. Louis, USA) y 4 g de extracto de malta (Laboratorios Britania, Bs. As., Argentina) se disuelven en 345 ml de agua destilada, se ajusta a pH 6,0 y se autoclava. Luego se agregan asépticamente 50 ml de suero ovino inactivado (Laboratorio Gutiérrez, Bs. As., Argentina), 0,8 mg de anfotericina B (Gibco BRL Life Technologies, Paisley, Scotland), 4 ml de una solución con 10 mg/ml de penicilina G (Gibco BRL Life Technologies, Paisley, Scotland), y 4 ml de una solución con 10 mg/ml de gentamicina (Gibco BRL Life Technologies, Paisley, Scotland). Se colocan 10 ml de medio en placas de Petri de 6 cm de diámetro.
8. Cultivo en agar base Columbia (Laboratorios Britania, Bs. As., Argentina) con 5% de sangre humana con incubación durante 48 h a 37 °C en atmósfera de 5% de CO2, conservando la muestra en medio de Stuart.
La investigación de T. vaginalis se realizó a través de la observación microscópica directa con SF y con SAF/azul de metileno, la coloración de May-Grunwald Giemsa prolongado, el cultivo en tioglicolato modificado y en agar Columbia modificado. El medio líquido se examinó mediante observación microscópica directa diaria y el medio sólido mediante observación microscópica directa al séptimo día, en busca de parásitos móviles.
La detección de candidiasis se realizó a través de la observación en fresco con KOH al 10% y por cultivo en agar Sabouraud y agar sangre. La identificación de las especies de Candida se realizó utilizando el agar cromogénico.
El diagnóstico de vaginosis bacteriana (VB) se realizó utilizando el criterio de Nugent, cuando el score fue ³ 7 (18) y también por el criterio de Amsel, es decir, la presencia de 3 o más de los siguientes criterios (1):
- Observación de clue-cells en la coloración de Gram.
- pH > 4,5.
- Prueba de aminas positiva.
- Descarga vaginal fina y homogénea.
Análisis estadístico
Se compararon los distintos exámenes microscópicos (fresco con SF, May-Grunwald Giemsa y SAF/ azul de metileno) con el cultivo (medio líquido más medio sólido) considerado los cultivos en ambos medios como método de referencia. Se efectuó la valoración de cada examen microscópico mediante el cálculo de sensibilidad, especificidad, valor predictivo positivo y negativo y los correspondientes intervalos de confianza (IC) del 95 % (EPI INFO 6.0).
RESULTADOS
Se diagnosticó la presencia de T. vaginalis en 10/ 223 pacientes embarazadas (4,5%) con un IC de 2,3- 8,3 por cultivo (desarrollo en medio líquido más medio sólido).
En la Tabla 1 se observan los porcentajes de positividad para T. vaginalis con los diferentes métodos de diagnóstico ensayados. En la Tabla 2 se muestran la sensibilidad, la especificidad y los valores predictivos positivo y negativo de cada metodología utilizada.
Tabla 1. Prevalencia de T. vaginalis en 223 pacientes embarazadas según diferentes métodos de diagnóstico

Tabla 2. Sensibilidad, especificidad y valores predictivos positivos y negativos de los diferentes métodos de diagnóstico de T. vaginalis en pacientes embarazadas

El examen en fresco con SF detectó el parásito en 3/ 223 pacientes (1,3%), (sensibilidad 30% y especificidad 100%). Tanto la coloración de May-Grunwald Giemsa como el examen en fresco con SAF/azul de metileno lo detectaron en 4 de 223 pacientes (1,8%) (sensibilidad 40% y especificidad 100%). Al considerar la suma de los tres exámenes microscópicos (fresco con SF, coloración de May-Grunwald Giemsa y fresco con SAF/azul de metileno), se diagnosticó el parásito en 5/223 pacientes (2,2%) (sensibilidad 50% y especificidad 100%). En las Fotos 1, 2 y 3 se observa el parásito en fresco con SF, en la coloración de May-Grunwald Giemsa y en fresco con SAF/azul de metileno respectivamente.

Foto 1. Trichomonas vaginalis: observación en fresco con solución fisiológica (400X).

Foto 2. Trichomonas vaginalis: coloración de May-Grunwald Giemsa prolongado (1000X).

Foto 3. Trichomonas vaginalis: observación en fresco con solución acética formolada/azul de metileno (400X).
El cultivo en medio sólido detectó el parásito en 5/223 pacientes (2,2%), mientras que el medio líquido detectó 10/223 (4,5%). El cultivo en medio sólido detectó sólo 5 de las 10 pacientes positivas para T. vaginalis (50%) con un IC de 18,7-81,3, mientras que el medio líquido detectó la totalidad de casos positivos (100%) con un IC de 69,2-100.
En la Tabla 3 se resumen las características de las pacientes con tricomonosis y los hallazgos microbiológicos.
Tabla 3. Características de las pacientes con tricomonosis y hallazgos microbiológicos
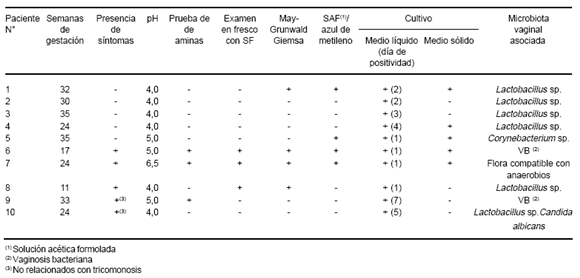
De 10 pacientes con tricomonosis, 5 no presentaban sintomatología y la colposcopía fue normal. En estas pacientes la flora asociada fue Lactobacillus spp. (4) y Corynebacterium sp. (1). Los exámenes microscópicos resultaron negativos para T. vaginalis en 3/5 y positivos en escasa cantidad en los 2 restantes. Por otro lado, 3/ 10 manifestaron cervicocolpitis y presentaron sintomatología compatible con tricomonosis (secreción purulenta abundante, prurito, flujo maloliente). De estos 3 casos, uno estuvo asociado a VB, otro a flora compatible con anaerobios. Estos dos presentaron exámenes microscópicos positivos para T. vaginalis en abundante cantidad; mientras que el restante se asoció con Lactobacillus sp. y mostró examen microscópico positivo para T. vaginalis solamente en escasa cantidad. Las otras 2 pacientes manifestaron síntomas relacionados con VB (1) y vulvovaginitis por Candida albicans (1) y los exámenes microscópicos resultaron negativos para T. vaginalis en ambos casos.
DISCUSIÓN
En este trabajo se observó una prevalencia de 4,5% de T. vaginalis por cultivo, tanto en embarazadas sintomáticas como asintomáticas. Estos valores de prevalencia de T. vaginalis durante el embarazo varían en la literatura de acuerdo con las poblaciones estudiadas. Es así como Cotch et al. obtuvieron también por cultivo una prevalencia de T. vaginalis, tanto en embarazadas sintomáticas como asintomáticas de 6,1% en mujeres caucásicas y de 6,6% en mujeres latinas, mientras que en mujeres de población negra fue de 22,8%, debido a que las mujeres de esta población presentan un pH del contenido vaginal normal mayor que las de población blanca (5,3 ± 0,7) (6). Asimismo, Germain et al. relataron una prevalencia por cultivo de 14,9% en embarazadas de todas las razas con síntomas y sin ellos (10). Sin embargo, Blackwell et al. describieron prevalencias mucho menores (0,75%) también por cultivo, en embarazadas sintomáticas y asintomáticas (2). Hasta el presente no fueron documentados en nuestro país datos de prevalencia de T. vaginalis utilizando cultivos.
Por otra parte, las prevalencias de T. vaginalis varían de acuerdo a la metodología empleada. En la literatura, al igual que en este trabajo, se describen prevalencias menores por exámenes microscópicos que por cultivo, aunque con variaciones según la población analizada. Es así como Meis et al. relataron prevalencias en embarazadas sintomáticas y asintomáticas de diferentes razas de 3,3% y 2,7% a las 24 y 28 semanas de gestación respectivamente, utilizando examen en fresco con SF (16). En Brasil, Simoes et al. describieron prevalencias similares a las de nuestro trabajo, 2,1% por exámenes microscópicos en embarazadas con síntomas y sin ellos (24). Por otra parte, Coppolillo et al. describieron en un trabajo previo realizado en el Hospital de Clínicas, mayores prevalencias de T. vaginalis (4,7%) por exámenes microscópicos (fresco con SF y coloración de May-Grunwald Giemsa) en embarazadas sintomáticas y asintomáticas (4). Di Bartolomeo et al. documentaron también en Argentina prevalencias mayores (3,5%) por exámenes en fresco con SF y por coloración de May-Grunwald Giemsa, aunque se trataba de embarazadas sintomáticas (7).
Cabe aclarar que los intervalos de confianza del 95% en lo que respecta a la prevalencia de positivos para T. vaginalis con los diferentes métodos son amplios, dado que la prevalencia de infección por este parásito es baja en la población estudiada, en relación con otras infecciones genitales como la candidiasis vaginal (24,3%) y la VB (19,5%) (4).
Tal como lo describe la literatura, donde se informa que la sensibilidad del examen microscópico oscila entre 35 y 80%, en nuestro trabajo la sensibilidad de los diferentes exámenes microscópicos osciló entre 30 y 40% y ascendió a 50% al considerar la suma de los tres exámenes microscópicos, probablemente debido al escaso número de parásitos presentes en la población de mujeres embarazadas asintomáticas estudiada (12, 19, 28). Krieger et al. describieron un 60% de sensibilidad en el diagnóstico de T. vaginalis a través del examen en fresco con SF en mujeres pertenecientes a una población de alto riesgo (14). Asimismo, Radonjic et al. relataron un 66,7% de sensibilidad para este mismo examen y un 52,4% para la coloración de May-Grunwald Giemsa en pacientes con complicaciones ginecológicas (22). También Wiese et al. describieron un 58% de sensibilidad y un 99,8% de especificidad del examen en fresco con SF en un estudio realizado en forma consecutiva y prospectiva, donde los resultados de los exámenes microscópicos no estaban influenciados por el cultivo (29). Asimismo, Costamagna relató un 58,3% de sensibilidad del examen en fresco con SF y además describió un mayor rendimiento para el examen en fresco con SAF/azul de metileno (5).
Sin embargo, la especificidad de los distintos exámenes microscópicos fue elevada (100%), tal como lo describe la literatura (19, 29). Cabe aclarar también que los intervalos de confianza del 95% de la sensibilidad de los diferentes métodos resultaron amplios, mientras que los correspondientes a la especificidad fueron acotados, en gran parte debido a que la mayoría de las mujeres no tuvieron infección por T. vaginalis. Estos rangos podrían ser más acotados, probablemente con un mayor número de pacientes positivas para dicha infección.
El cultivo en medio sólido (agar Columbia modificado) solo detectó la mitad de los casos positivos para T. vaginalis, con lo que demostró su escasa utilidad. Estos resultados difieren de los relatados por Stary et al. quienes describieron un 100% de sensibilidad de este medio para pacientes asintomáticas y un 97,3% para sintomáticas (27). Estas diferencias podrían deberse a la distinta composición de los medios de cultivo utilizados. La mayor concentración de agar en el medio sólido podría dificultar el desarrollo y la movilidad del parásito, ya que en este medio se los observó en escaso número y además presentaban alteraciones morfológicas (formas redondeadas y presencia de vacuolas en su interior). Hasta el momento no se han documentado otras publicaciones que pudieran reproducir los resultados observados por Stary et al. Sin embargo, para evaluar la real utilidad de este medio sólido se deberían estudiar un mayor número de pacientes con tricomonosis.
El cultivo en medio líquido (tioglicolato modificado) detectó la totalidad de los casos positivos para T. vaginalis y además resulta accesible para los laboratorios de mediana complejidad, tal como lo describieron Poch et al. (21). Sin embargo, la investigación del parásito mediante este medio requiere de una exhaustiva y laboriosa observación microscópica diaria durante 7 días, ya que el parásito desarrolla entre el segundo y el séptimo día en aquellas pacientes con exámenes microscópicos negativos.
Cabe destacar que en la mayoría de las embarazadas asintomáticas con tricomonosis, el diagnóstico de T. vaginalis fue realizado solo por cultivo en medio líquido ya que los exámenes microscópicos resultaron frecuentemente negativos. En estas pacientes, el pH del contenido vaginal fue £ 4,5 y la prueba de aminas negativa, y el parásito se asoció con la presencia de Lactobacillus spp. Por otra parte, en aquellas pacientes con Candida albicans y/o VB, pero que no presentaban síntomas y/o secreción compatibles con tricomonosis los exámenes directos también resultaron negativos. Por lo expuesto, recomendamos la utilización del medio de cultivo líquido (tioglicolato modificado) en el diagnóstico de T. vaginalis durante el embarazo, especialmente cuando los exámenes microscópicos resultan negativos, con el objeto de incrementar la sensibilidad para instaurar un tratamiento precoz y adecuado y así prevenir posibles complicaciones maternas y perinatológicas.
Agradecimientos: Este trabajo fue realizado con el aporte del proyecto UBACyT B049
BIBLIOGRAFÍA
1. Amsel R, Totten PA, Spiegel CA, Chen KC, Eschenbach D, Holmes KK. Nonspecific vaginitis: Diagnosis criteria and microbial and epidemiologic associations. Am J Med 1983; 74: 14-22.
2. Blackwell AL, Thomas PD, Wareham K, Emery SJ. Health gains from screening for infection of the lower genital tract in women attending for termination of pregnancy. Lancet 1993; 342: 206-10.
3. Cates W, Joesoef MR, Goldman MB. Atypical pelvis inflammatory disease: can we identify clinical predictors? Am J Obstet Gynecol 1993; 169: 341-6.
4. Coppolillo E, Perazzi B, Vay C, Cora Eliseht M, Tauscher P, Barata A et al. Metodología diagnóstica para las infecciones del tracto genital inferior durante el embarazo. Ginecol Reprod 2000; 7: 76-81.
5. Costamagna SR. Trichomonas vaginalis. En: Costamagna SR, editores. Parasitosis regionales, un estudio referido a las principales parasitosis de Bahía Blanca, provincia de Buenos Aires, Argentina. Bahía Blanca, Editorial de la Universidad Nacional del Sur, 2004, p.197-217.
6. Cotch MF, Pastorek JG, Nugent RP, Hillier SL, Gibbs RS, Martin DH et al. Trichomonas vaginalis associated with low birth weight and preterm delivery. The vaginal infections and prematurity study group. Sex Transm Dis 1997; 24: 353-60.
7. Di Bartolomeo S, Rodríguez M, Sauka D, de Torres RA. Perfil microbiológico en secreciones genitales de embarazadas sintomáticas, en el Gran Buenos Aires, Argentina. Enferm Infecc Microbiol Clin 2001; 19: 99-102.
8. Fouts AC, Kraus SJ. Trichomonas vaginalis: re-evaluation of its clinical presentations and laboratory diagnosis. J Infect Dis 1980; 141: 137-43.
9. Garber GE, Sibau L, Ma R, Proctor EM, Shaw CE, Bowie WR. Cell culture compared with broth for detection Trichomonas vaginalis. J Clin Microbiol 1987; 25: 1275-9.
10. Germain M, Krohn MA., Hillier SL, Eschenbach DA. Genital flora in pregnancy and its association with intrauterine growth retardation. J Clin Microbiol 1994; 32: 2162-8.
11. Grodstein F, Goldman MB, Cramer DW. Relation of tubal infertility to a history of sexually transmitted disease. Am J Epidemiol 1993; 137: 577-84.
12. Heine P, Mc Gregor JA. Trichomonas vaginalis: a reemerging pathogen. Clin Obstet Gynecol 1993; 36: 137-44.
13. Krieger JN. Trichomoniasis in men: old issues and new data. Sex Transm Dis 1995; 22: 83-96.
14. Krieger JN, Tam MR, Stevens CE, Nielsen IO, Hale J, Kiviat NB et al. Diagnosis of trichomoniasis. Comparison of conventional wet-mount examination with cytologic studies, cultures and monoclonal antibody staining of direct specimens. JAMA 1988; 259: 1223-7.
15. McCann JS. Comparison of direct microscopy and culture in the diagnosis of trichomoniasis. Br J Vener Dis 1974; 50: 450-2.
16. Meis PJ, Goldenberg RL, Mercer B, Moawad A, Das A, Mc Nellis D et al. The preterm prediction study: significance of vaginal infections. Am J Obstet Gynecol 1995; 173: 1231-5.
17. Minkoff H, Grunebaum AN, Schwarz RH, Feldman J, Cummings MC, Crombleholme W et al. Risk factors for prematurity and premature rupture of membranes: prospective study of the vaginal flora in pregnancy. Am J Obstet Gynecol 1984; 150: 965-72.
18. Nugent RP, Krohn MA, Hillier SL. Reliability of diagnosing bacterial vaginosis is improved by a standardized method of Gram stain interpretation. J Clin Microbiol 1991; 29: 279- 301.
19. Patel SR, Wiese W, Patel SC, Ohl C, Byrd JC, Estrada CA. Systematic review of diagnostic tests for vaginal trichomoniasis. Infect Dis Obstet Gynecol 2000; 8: 248-57.
20. Petrin D, Delgaty K, Bhatt R, Garber G. Clinical and microbiological aspects of Trichomonas vaginalis. Clin Microbiol Rev 1998; 11: 300-17.
21. Poch F, Levin D, Levin S, Dan M. Modified thioglycolate medium: a simple and reliable means for detection of Trichomonas vaginalis. J Clin Microbiol 1996; 34: 2630-1.
22. Radonjic IV, Dzamic AM, Mitrovic SM, Arsic Arsenijevic VS, Popadic DM, Kranjcic Zec IF. Diagnosis of Trichomonas vaginalis infection: The sensitivities and specificities of microscopy, culture and PCR assay. Eur J Obstet Gynecol Reprod Biol 2006; 126: 116-20.
23. Rein MF, Holmes KK. ¨Non-specific vaginitis¨, vulvovaginal candidiasis and trichomoniasis: clinical features, diagnosis and management. En: Remington J, Swartz M N, editors. Current clinical topics in infectious diseases. New York, NY, Mc Graw-Hill Book Co., 1983, p. 281-315.
24. Simoes JA, Giraldo PC, Faundes A. Prevalence of cervicovaginal infections during gestation and accuracy of clinical diagnosis. Infect Dis Obstet Gynecol 1998; 6: 129-33.
25. Sobel JD. Vaginitis. N Engl J Med 1997; 337: 1896-903.
26. Spence MR, Hollander DH, Smith J, Mc Gaig L, Sewell P, Brockman M. The Clinical and laboratory diagnosis of Trichomonas vaginalis infection. Sex Transm Dis 1980; 7: 168-71.
27. Stary A, Kuchinka-Koch A, Teodorowicz L. Detection of Trichomonas vaginalis on modified Columbia agar in the routine laboratory. J Clin Microbiol 2002; 40: 3277-80.
28. Swygard H, Sena AC, Hobbs MM, Cohen NS. Trichomoniasis: clinical manifestations, diagnosis and management. Sex Transm Infect 2004; 80: 91-5.
29. Wiese W, Patel SR, Patel SC, Ohl CA, Estrada CA. A metaanalysis of the Papanicolaou smear and wet mount for the diagnosis of vaginal trichomoniasis. Am J Med 2000; 108: 301-8. [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ] [ Links ]
Recibido: 24/07/06
Aceptado: 15/05/07














