Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
Revista argentina de microbiología
versión impresa ISSN 0325-7541versión On-line ISSN 1851-7617
Rev. argent. microbiol. v.40 n.2 Ciudad Autónoma de Buenos Aires abr./jun. 2008
Bacillus thuringiensis: generalidades. Un acercamiento a su empleo en el biocontrol de insectos lepidópteros que son plagas agrícolas
Diego H. Sauka*, Graciela B. Benintende
Área Bioinsumos Microbianos, Instituto de Microbiología y Zoología Agrícola (IMYZA), Instituto Nacional de Tecnología Agropecuaria (INTA), De los Reseros y Las Cabañas s/nro. C.C. 25 (1712) Castelar, Buenos Aires, Argentina
*Correspondencia. E-mail: dsauka@cnia.inta.gov.ar
RESUMEN
Bacillus thuringiensis es el insecticida biológico más aplicado en el mundo y se utiliza para controlar diversos insectos que afectan la agricultura, la actividad forestal y que transmiten patógenos humanos y animales. B. thuringiensis constituyó durante las últimas décadas un tema de investigación intensiva. Estos esfuerzos brindaron datos importantes sobre las relaciones entre la estructura, el mecanismo de acción y la genética de sus proteínas cristalinas pesticidas, y una visión más clara y coherente sobre estas relaciones ha emergido gracias a ellos. Otros estudios se centraron en el rol ecológico de las proteínas cristalinas de B. thuringiensis, su funcionamiento en sistemas agrícolas y en otros sistemas naturales. Teniendo como base todo el conocimiento generado y las herramientas de la biotecnología, los investigadores están ahora divulgando resultados prometedores sobre el desarrollo de toxinas más útiles, bacterias recombinantes, formulaciones nuevas y plantas transgénicas que expresan actividad pesticida, con el objetivo de asegurar que estos productos sean utilizados con un mayor beneficio y eficacia. Este artículo constituye una tentativa de integrar todos estos progresos recientes sobre el estudio de B. thuringiensis en un contexto de control biológico de plagas de insectos lepidópteros de importancia agrícola.
Palabras clave: Bacillus thuringiensis; Bioinsecticida; Insectos lepidópteros
ABSTRACT
Bacillus thuringiensis: general aspects. An approach to its use in the biological control of lepidopteran insects behaving as agricultural pests. Bacillus thuringiensis is the most widely applied biological pesticide used to control insects that affect agriculture and forestry and which transmit human and animal pathogens. During the past decades B. thuringiensis has been the subject of intensive research. These efforts have yielded considerable data about the relationships between the structure, mechanism of action, and genetics of their pesticidal crystal proteins. As a result, a coherent picture of these relationships has emerged. Other studies have focused on the ecological role of the B. thuringiensis crystal proteins and their performance in agricultural and other natural settings. With this knowledge as background and the help of biotechnological tools, researchers are now reporting promising results in the development of more useful toxins, recombinant bacteria, new formulations and transgenic plants that express pesticidal activity, in order to assure that these products are utilized with the best efficiency and benefit. This article is an attempt to integrate all these recent developments in the study of B. thuringiensis into a context of biological control of lepidopteran insect pest of agricultural importance.
Key words: Bacillus thuringiensis; Bioinsecticide; Lepidopteran insect pest
INTRODUCCIÓN
Hoy en día existe una necesidad crítica de contar con herramientas seguras y efectivas para el control de plagas, alternativas a los insecticidas químicos. Esto estimula considerablemente el interés en usar patógenos como agentes de biocontrol. El patógeno más exitoso en cumplir este objetivo, que además mantiene potencial para seguir desarrollándose, es la bacteria con cualidades insecticidas Bacillus thuringiensis. Esta posee una toxicidad selectiva alta debido a su estrecho rango de especificidad y gracias a ello genera en el ambiente un impacto muy bajo.
Esta actualización es un intento de integrar los desarrollos recientes de la biología y la genética molecular en el estudio de esta bacteria entomopatógena dentro de un contexto de control biológico de insectos lepidópteros que son plagas de cultivos de interés agronómico.
Algunas revisiones generales sobre este tema fueron publicadas hace un tiempo atrás en idioma inglés y sobre ellas basaremos parte de nuestra discusión (20, 107). Sin embargo, creemos necesario retomar el tema teniendo en cuenta resultados recientes y nuestras propias observaciones.
CARACTERÍSTICAS GENERALES
Bacillus thuringiensis es un bacilo gram positivo, de flagelación perítrica, que mide de 3 a 5 µm de largo por 1 a 1,2 µm de ancho y que posee la característica de desarrollar esporas de resistencia elipsoidales que no provocan el hinchamiento del perfil bacilar (Figura 1) (49). Es un microorganismo anaerobio facultativo, quimioorganótrofo y con actividad de catalasa (117). Los distintos aislamientos de B. thuringiensis presentan en general características bioquímicas comunes. Poseen la capacidad de fermentar glucosa, fructosa, trealosa, maltosa y ribosa, y de hidrolizar gelatina, almidón, glucógeno, esculina y N-acetil-glucosamina. Sin embargo, la característica principal de B. thuringiensis es que durante el proceso de esporulación produce una inclusión parasporal formada por uno o más cuerpos cristalinos de naturaleza proteica que son tóxicos para distintos invertebrados, especialmente larvas de insectos (Figura 1) (107). Estas proteínas se llaman Cry (del inglés, Crystal) y constituyen la base del insecticida biológico más difundido a nivel mundial.

Figura 1. Imagen de microscopía electrónica de transmisión de una cepa de B. thuringiensis en estado de esporangio. C: cristal parasporal; E: espora. Barra, 0,5 mm.
SITUACIÓN TAXONÓMICA Y CLASIFICACIÓN
B. thuringiensis pertenece a la familia Bacillaceae y se ubica dentro del grupo 1 del género Bacillus; forma parte del grupo de Bacillus cereus, el que incluye a B. anthracis, B. cereus, B. mycoides, así como también a los más recientemente descritos B. pseudomycoides (93) y B. weihenstephanensis (77). Se encuentra estrechamente relacionado con los dos primeros, de los que no logra distinguirse por completo debido a que no existen suficientes diferencias en sus características morfológicas y bioquímicas, por lo que la designación de B. thuringiensis como especie ha estado sometida a discusión (107). A pesar de esto, el Bergey´s Manual of Determinative Bacteriology reconoce la individualidad de estas especies basándose sobre todo en dos características diferenciales: la presencia de la inclusión o cristal parasporal y sus propiedades insecticidas (117).
B. thuringiensis se clasifica en 84 serovares mediante serología del antígeno flagelar H (Tabla 1). Se trató de establecer relaciones entre estos serovares y su actividad insecticida o la presencia de algún tipo de cristal en particular pero no se tuvo éxito, por lo que su significado biológico no está claro. Por ejemplo, el serovar morrisoni agrupa cepas que son tóxicas para lepidópteros, dípteros y coleópteros; no todas las cepas de B. thuringiensis svar aizawai son tóxicas para Spodoptera littoralis (Lepidoptera). Existen, además, cepas de B. thuringiensis que no pueden clasificarse utilizando esta metodología, ya que no pueden formar flagelos. Todas estas cepas se agruparon en un serovar, actualmente desaparecido de la literatura (76).
Tabla 1. Clasificación de B. thuringiensis de acuerdo con el antígeno H.

CRISTALES PARASPORALES
Desde el instante en el que ocurre el englobamiento de la pre-espora hasta su maduración, en simultaneidad con la formación de la espora, tiene lugar en B. thuringiensis la síntesis de uno o varios cristales parasporales, que pueden representar hasta un 30% del peso seco del esporangio (18). Estos cristales pueden presentar distintas morfologías y pueden clasificarse en bipiramidales, cúbicos, cuadrados aplanados, esféricos y otras formas atípicas menos frecuentes (69).
Se logró en muchos casos establecer asociaciones entre la morfología del cristal, sus proteínas Cry constituyentes, el peso molecular de éstas y su espectro de actividad insecticida (Tabla 2) (83). Sin embargo, existen trabajos en los que se describieron cristales parasporales que, a pesar de tener morfologías asociadas a una toxicidad específica, no parecen poseer actividad insecticida alguna (6, 83).
Tabla 2. Asociaciones entre los principales tipos de cristales de B. thuringiensis, proteínas Cry y su espectro de actividad insecticida.

Los cristales de B. thuringiensis pueden ser degradados por la acción de los microorganismos del suelo (134) y, al igual que sus esporas, también pueden ser inactivados por la acción de la luz ultravioleta (81, 97).
El cristal parasporal se ubica en el interior del esporangio y, por lo general, fuera del exosporio de la espora, y ambos son finalmente liberados tras la lisis celular. Existen algunos casos donde se describieron cristales dentro del exosporio, por lo que estos continúan junto a las esporas tras la lisis (61, 83). En otro caso muy atípico, se pudo observar que los cristales se forman fuera del exosporio, pero ambos permanecen indefinidamente dentro de un esporangio que no se lisa, preservándolos de una rápida degradación (Figura 2) (104).

Figura 2. Imagen de microscopía electrónica de transmisión de una cepa atípica de B. thuringiensis que permanece ininterrumpidamente en forma de esporangio. A: espora; B: cristal ovoide; C: borde del esporangio que no se lisa. Sauka y Benintende (104). Barra, 1 mm.
Cada cuerpo de inclusión cristalino puede estar constituido por proteínas Cry de una o varias clases (62, 87) que se agrupan entre sí mediante puentes disulfuro (73). La estabilidad de estas uniones condiciona el pH de solubilización del cristal (ver "Mecanismo de acción"). Particularmente en el caso de los cristales bipiramidales, cuando estos puentes están distorsionados, estos cristales son solubles a pH mayor de 9,5; mientras que si permanecen en su estado más estable necesitan un pH superior a 12 para lograrlo (84).
MECANISMO DE ACCIÓN
El mecanismo de acción de las proteínas Cry se describió principalmente en lepidópteros como un proceso de múltiples etapas. Los cristales de B. thuringiensis son ingeridos y luego solubilizados en el intestino medio del insecto, tras lo cual se liberan las proteínas cristalinas en forma de protoxinas. Estas no producirán el daño per se, sino que deberán ser procesadas por proteasas intestinales para generar las toxinas activas que llevarán a la muerte de la larva (14). Bajo su forma monomérica, las toxinas atraviesan la membrana peritrófica y se unen de forma univalente a la caderina, con gran afinidad en la cara apical de la membrana epitelial (14, 50). Luego, de acuerdo con estudios realizados en cultivos de células de insectos, se inicia una cascada de señalización dependiente del ion magnesio que sería responsable de l muerte celular (138). Además, el inicio de esa cascada de señalización estimula la exocitosis de caderina desde vesículas intracelulares hacia la membrana apical de la célula y aumenta el número de receptores; por ende, recluta un número mayor de toxinas libres que amplificarían la señal inicial (139). Por otro lado, con base en experimentos in vitro y bioensayos, se propone que la unión de los monómeros a caderina facilita el clivaje proteolítico sobre el extremo N-terminal de la toxina (46, 64). Este último clivaje induce el ensamble de los monómeros y se establece una forma oligomérica pre-poro. Esta estructura incrementa la afinidad por un receptor secundario como puede ser la aminopeptidasa N o la fosfatasa alcalina (14, 67). Por último, la unión a ese segundo receptor facilita la formación de un poro en el epitelio del intestino medio, esto provoca un desequilibrio osmótico y la consecuente lisis celular (Figura 3) (14). El tejido intestinal resulta dañado gravemente, lo que impide la asimilación y retención de compuestos vitales para la larva y lleva a la muerte del insecto. La muerte puede acelerarse al germinar las esporas y proliferar las células vegetativas en el hemocele del insecto (32, 107). Broderick et al. (16) descartaron estas posibilidades y demostraron que la mortalidad inducida por B. thuringiensis dependería en esencia de ciertas bacterias entéricas que son parte de la microbiota normal del intestino del insecto susceptible, ya que sólo B. thuringiensis no sería suficiente. Estas bacterias serían responsables de causar la septicemia en el insecto luego de que B. thuringiensis les permite alcanzar el hemocele tras dañar el epitelio intestinal.
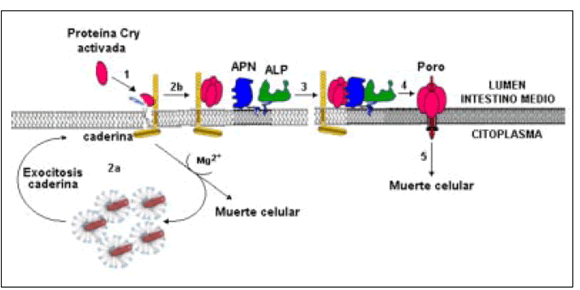
Figura 3. Mecanismo de acción de proteínas Cry en insectos lepidópteros. 1) Unión de la toxina a caderina y clivaje desde su extremo C-terminal para generar la forma monomérica activa; 2a) inicio de la cascada de señalización dependiente de Mg2+, estimulación de exocitosis de caderina desde vesículas intracelulares hacia la membrana apical y consiguiente muerte celular; 2b) formación de la estructura oligomérica pre-poro; 3) unión del oligómero a la aminopeptidasa N (APN) y/o fosfatasa alcalina (ALP) y migración a zonas específicas de la membrana; 4) formación del poro; 5) desequilibrio osmótico y consiguiente muerte celular. Adaptado de Bravo et al. (15) y Zhang et al. (138).
GENES CODIFICANTES DE PROTEÍNAS INSECTICIDAS Cry
Existen 376 genes cry distintos que se clasificaron sobre la base de su similitud de secuencias en 54 grupos divididos en diferentes clases y subclases (25, 26). Una lista actualizada de todos estos genes cry, cuyo número aumenta día a día, se encuentra disponible con acceso libre en Internet (26).
Los genes cry poseen una secuencia codificante de entre 1900 pares de bases (pb) ( cry2Ab) y unos 3600 pb ( cry1Aa, cry1Ab, cry1Ac, etc.) (25). Las proteínas que codifican presentan una identidad aminoacídica que puede variar desde más de un 90% hasta menos de un 20%, y el intervalo de masas moleculares oscila entre 50 y 140 kDa. Más adelante se discutirá en detalle sobre las características generales y específicas de estas proteínas.
Las cepas de B. thuringiensis pueden portar un único gen cry, como por ejemplo B. thuringiensis svar. kurstaki HD-73, que posee solamente un gen cry1Ac (48), o bien presentar perfiles génicos muy complejos, con hasta ocho genes cry diferentes (2, 7, 15, 65, 100, 125, 129).
En general, es posible correlacionar el tipo de gen cry presente en una determinada cepa o aislamiento con su actividad insecticida. Por lo tanto, la identificación del contenido génico cry de una cepa de B. thuringiensis puede utilizarse para efectuar dicha predicción (96).
Existe la idea generalizada de que los genes cry siempre se localizan en plásmidos de peso molecular elevado que se replican mediante un mecanismo específico conocido como de tipo "theta" (5). A pesar de esto, un reporte reciente informa la detección de un gen cry en un plásmido de bajo peso molecular que se replica mediante un mecanismo de círculo rodante (82). También se informó la existencia de genes cry insertados en el cromosoma de B. thuringiensis (71, 72, 101).
Genes cry que codifican proteínas tóxicas para insectos lepidópteros
Genes cry1
Los genes cry1 codifican proteínas de aproximadamente 130 kDa que se agrupan durante la esporulación en inclusiones cristalinas bipiramidales. Como ya fue mencionado, estas proteínas son sintetizadas como protoxinas que se solubilizan en las condiciones alcalinas del intestino medio del insecto y se activan por proteólisis en toxinas -en este caso de aproximadamente 65 kDa- mediante proteasas asociadas al cristal o al intestino medio de la larva. Esta activación proteolítica puede ser llevada a cabo in vitro utilizando una gran variedad de proteasas (135).
La gran mayoría de los genes cry que se conocen pertenecen al grupo cry1, y estos son sin duda los más estudiados. Se han informado hasta hoy 150 genes cry1 distintos, los que han sido clasificados en 12 clases (A a L) (26). Estos genes fueron los primeros en ser caracterizados (109), así como también en ser modificados genéticamente (92). Hace poco, nuestro grupo publicó una estrategia nueva para la amplificación y secuenciación de genes cry1A en forma completa; en esa comunicación se detalla una lista de cebadores que fueron diseñados para tal fin (103). Se lograron identificar dos genes cry1A a partir de un aislamiento nativo de B. thuringiensis como fruto de este trabajo, que fueron aceptados por el Bt Pesticidal Crystal Protein Nomenclature Committee como variantes naturales nuevas (26, 103).
La frecuencia de detección de los distintos genes cry1 varía en forma marcada. Algunos genes, como los cry1A, se detectan con más frecuencia que otros -de hecho, se han presentado en más de la mitad de las cepas analizadas-; mientras que otros como los cry1H, cry1K o los cry1L son muy raros. Luego de los de la clase cry1A, los genes más comunes de encontrar son los de las clases cry1C y cry1D. En cambio, los genes cry1B, cry1E, cry1F y cry1G se detectan con una frecuencia menor, a pesar de existir excepciones (7, 15, 22, 125). Un ejemplo de ello es la importante presencia de genes cry1E en una colección china de B. thuringiensis (59). También se encontró una presencia elevada (30% de los aislamientos), pero de genes cry1B, en otro estudio de tamizaje (23). Los genes cry1I son otra clase bastante común de hallar. Mediante diversas técnicas de biología molecular se confirmó la amplia distribución de estos genes en cepas de B. thuringiensis (106, 113). Esta clase de genes cry1 presenta una serie de características distintivas con respecto al resto de los miembros de este grupo. Se sugirió la naturaleza críptica de estos genes, ya que a sus proteínas no se las encontró formando parte de los cristales parasporales (43, 120). Los genes cry1I están localizados generalmente 500 pb "corriente abajo" de los genes cry1A, y se cree que no se expresan debido a la ausencia de una región promotora (113, 120). Otro grupo comunicó que estos genes se expresan y secretan en una fase temprana de la esporulación (74). El clonado y la expresión de esta clase de genes en Escherichia coli reveló que codifican proteínas de 81 kDa, sólo tóxicas para larvas de lepidópteros (29, 43, 113). Sin embargo, Tailor et al. ya habían informado con anterioridad (120) que estas poseían una toxicidad dual para larvas de lepidópteros y coleópteros. En la actualidad existen otros trabajos que verifican esa actividad insecticida dual (52, 86, 99), por lo que serían necesarios más estudios para dilucidar esta cuestión.
En estudios de distribución de genes cry se reveló la existencia de distintas asociaciones que involucran genes cry1 en una misma cepa de B. thuringiensis. Es muy común que se encuentren genes cry1I cuando otro gen cry1 está presente, y esto sería consistente con la ubicación física de los genes cry1I en el genoma de B. thuringiensis próximos a otros genes cry1 (129). Recientemente se halló que esta asociación tan fuerte entre ambas clases de genes cry1 se debe sobre todo a la relación entre los genes cry1Aa, cry1Ab y/o cry1Ac con cry1Ia en especial (102). Otra combinación frecuente de encontrar es la de los genes cry1C y cry1D (15, 28, 125, 129). La asociación entre estos dos genes puede ser explicada por su ubicación en el mismo replicón en una cepa de B. thuringiensis svar. aizawai, en la que ambos genes están separados por tan sólo 3 kb (101). Sin embargo, la combinación más frecuentemente detectada es la de genes cry1Aa, cry1Ab y cry1Ac, ya sea los tres juntos o de a pares (7, 15, 22, 56, 65, 70, 102, 125). Estos tres genes cry1 forman parte de B. thuringiensis svar. kurstaki HD-1; cry1Aa y cry1Ac se localizan juntos en un plásmido de 110 MDa y cry1Ab dentro de otro más pequeño e inestable de 44 MDa (21).
Genes cry2
Los genes del grupo cry2 poseen marcos de lectura abiertos ( orf; del inglés, open reading frames) de unas 1900 pb, ya que carecen del gran fragmento C-terminal presente en otros genes cry. Estos codifican proteínas de 65 kDa que se agrupan en inclusiones cuboidales. Los genes cry2 están presentes en cepas de distintos serovares: B. thuringiensis svar. kurstaki HD-1, B. thuringiensis svar. thuringiensis Berliner, B. thuringiensis svar. kenyae, B. thuringiensis svar. tolworthi, etc. Las proteínas codificadas por estos genes fueron previamente designadas como proteínas P2, en oposición a las inclusiones cristalinas P1 de 130 kDa presentes en las mismas cepas (58). Existen descriptos en la actualidad 43 genes cry2 distintos clasificados en sólo una clase (A) (26).
Los genes cry2Aa tendrían la peculiaridad de estar ubicados en la región más distal de un operón del cual formarían parte. Este consistiría de tres marcos abiertos de lectura (orf1, orf2 y cry2Aa) (58). La proteína Cry2Aa requiere de la proteína que corresponde al segundo gen de este operón (Orf2) para la formación del cristal. Esta última se encontraría ausente en el cristal, a pesar de ser indispensable para su formación (24). Por otro lado, no está claro si los productos del orf1 y de cry2Ab estarían presentes en el cristal. Los cristales de algunas de las cepas que contienen cry2Ab presentan poca o nada de la correspondiente proteína (30, 87). Si se inserta a este gen tras un promotor fuerte se alcanza un nivel elevado de expresión, lo que indicaría que la expresión deficiente de cry2Ab es resultado de un promotor débil.
Los genes cry2 también se encuentran de manera frecuente en B. thuringiensis (105), sobre todo entre aquellas cepas que poseen genes cry1 (7, 102, 125). Es muy común que se encuentren los genes cry2Aa y cry2Ab simultáneamente o el gen cry2Ab solo, pero no el cry2Aa en forma aislada (7, 105). Sólo existe un trabajo donde se describió el hallazgo atípico de un aislamiento de B. thuringiensis con sólo el gen cry2Aa (105).
Genes cry9
Los genes cry9 son de los menos estudiados entre aquellos que codifican proteínas tóxicas para lepidópteros. No obstante, son considerados herramientas muy promisorias para el control eficiente y el manejo de la resistencia de muchas especies de lepidópteros que son importantes desde el punto de vista agronómico (63, 90, 127). Existen actualmente 15 genes cry9 distintos clasificados en 5 clases (A, B, C, D y E) (26), que codifican para protoxinas de 130 kDa. Estas proteínas producidas por los genes de las clases cry9A, cry9B, cry9C y cry9E se agruparían en inclusiones cristalinas bipiramidales. Por otra parte, los genes cry9D lo harían dentro de inclusiones esféricas que no presentarían ninguna relación con las inclusiones bipiramidales y cuboidales típicas de cepas de B. thuringiensis tóxicas para lepidópteros (132, 133). La subclase cry9Aa (antes denominada cryIg) fue el primer gen de este grupo en ser descubierto a partir de una cepa de B. thuringiensis svar. galleriae (116). Posteriormente, el gen críptico cry9Ba (antes denominado cryX) se informó "corriente arriba" de cry9Aa (112). La falta de un codón de iniciación en su secuencia nucleotídica le brindaría su naturaleza críptica, por lo cual no podría expresarse in vivo (112).
Si bien se sabe que los genes cry1 y cry2 tienden a hallarse juntos en B. thuringiensis, no existiría una asociación clara entre ellos y los genes cry9 (102).
Genes cry15
Este grupo está formado por sólo un integrante que es el gen cry15Aa (26). Este gen codifica para una protoxina de aproximadamente 40 kDa que se agrupa en una inclusión cristalina cuboidal, la cual resulta tóxica para Manduca sexta (17). Es muy poca la información disponible acerca de este grupo. Parecería ser que su presencia se restringe sólo a cepas de B. thuringiensis svar. thompsoni (17, 35).
OTROS FACTORES DE VIRULENCIA PRODUCIDOS POR B. THURINGIENSIS
Además de las proteínas Cry, B. thuringiensis posee otros factores de virulencia que le permitirían sobrevivir y multiplicarse dentro del huésped, evadir su sistema inmune y producir septicemia. Algunos de estos factores de virulencia, como fosfolipasas (111), enterotoxinas (111), b-exotoxinas (37), y quitinasas (3, 4, 122), no tienen especificidad por el orden de insectos que afectan y se encuentran ampliamente distribuidos dentro de los distintos serovares de B. thuringiensis y otros miembros del grupo B. cereus (55). Por otro lado, algunos B. thuringiensis poseen otros factores de virulencia que sí tienen especificidad por el orden de insectos que afectan. Tal es el caso de las proteínas Cyt que se encuentran formando parte principalmente de los cristales de cepas mosquitocidas de B. thuringiensis (ej. svar. israelensis, kyushuensis, darmstadiensis, medellin, etc.), aunque también se pueden llegar a encontrar rara vez en alguna cepa tóxica para lepidópteros (ej. svar. morrisoni HD-12) (53, 54, 66). Estas proteínas son hemolíticas y citolíticas in vitro y son especialmente tóxicas para larvas de dípteros in vivo (54). Otro caso de factores de virulencia que tienen especificidad por el orden de insectos que afecta lo constituye el grupo de proteínas llamado Vip ( vegetative insecticidal proteins). Las Vip son proteínas insecticidas no relacionadas con las Cry que no forman inclusiones cristalinas y que se secretan al medio durante el crecimiento vegetativo de la bacteria (36). Incluyen la toxina binaria Vip1 y Vip2 con especificidad para coleópteros y la toxina Vip3 con especificidad para lepidópteros (36, 130, 131). Existen en la actualidad 40 genes vip3 distintos clasificados en 2 clases (A y B), que codifican para proteínas de aproximadamente 88 kDa (26, 36). Si bien las Vip3 compartirían algunas etapas en el modo de acción con las Cry, utilizarían distintos receptores (78). Otras proteínas llamadas Sip ( secreted insecticidal proteins) fueron recientemente descritas, pero muy poco se conoce de ellas (34). Sólo se conoce un miembro de este grupo: la proteína Sip1A, que también es producida y secretada por B. thuringiensis durante su etapa de crecimiento vegetativo y que posee propiedades insecticidas para coleópteros (34).
ESTRUCTURA DE LAS PROTEÍNAS Cry
Las estructuras tridimensionales de las proteínas Cry1Aa y Cry1Ac (tóxicas para lepidópteros), Cry3Aa y Cry3Bb (tóxicas para coleópteros), Cry2Aa (toxicidad dual para lepidópteros y dípteros), y Cry4Aa y Cry4Ba (tóxicas para dípteros) fueron dilucidadas a través de cristalografía de rayos X (9, 10, 31, 39, 51, 79, 80, 91). Las estructuras de estas proteínas muestran, a pesar de poseer distinto espectro de acción, una topología común compuesta por 3 dominios. En general, el dominio I de estas proteínas Cry está formado por 7 estructuras a-hélice, donde una hélice central está rodeada por las otras 6. Este dominio participaría en la formación del poro en la membrana de las células intestinales del insecto susceptible (ver "Mecanismo de acción") (79, 95, 110). El dominio II está formado por 3 láminas de estructura b en antiparalelo y participaría en la interacción con el receptor, por lo que sería determinante en la especificidad (41, 45, 57, 79, 98, 108, 114). El dominio III es un b- sandwich en antiparalelo que parecería ser importante para la estabilidad de la toxina (79, 88), como así también para su especificidad (19, 33, 45, 57, 80) y en la modulación de la actividad de canales iónicos en el intestino medio de los insectos susceptibles (27, 137).
La estructura primaria de las proteínas Cry presenta en general 5 bloques conservados que originalmente fueron descritos por Höfte y Whiteley (58) entre las proteínas Cry conocidas por entonces. Estas observaciones fueron más tarde confirmadas por Schnepf et al. (107) en la gran mayoría de las proteínas Cry (Figura 4). Estos 5 bloques conservados están localizados en regiones importantes dentro de la estructura tridimensional, ya que corresponden a regiones internas de los dominios o limítrofes entre ellos. El bloque 1 está constituido por la a- hélice central del dominio I; el límite entre los dominios I y II constituye el bloque 2; el bloque 3 abarca la última lámina b del dominio II y la primera del III. Los bloques 4 y 5 corresponden a las láminas b centrales del dominio III (51, 79). La localización estratégica de estas regiones sugiere que por lo menos las proteínas Cry de B. thuringiensis que las contienen pueden tener un plegamiento similar y, por lo tanto, un mecanismo de acción semejante.

Figura 4. Posiciones de los distintos bloques conservados entre las proteínas Cry. Los bloques conservados se representan en color negro, mientras que aquellos de color gris indican una similitud un poco más baja con respecto a la secuencia consenso. Adaptado de Schnepf et al. (107).
Proteínas Cry y Vip tóxicas para insectos lepidópteros
Las proteínas de la clase Cry1 y las Vip3 son las consideradas tradicionalmente tóxicas para las larvas del orden Lepidoptera. Las diferencias aminoacídicas que presentan se traducen comúnmente en variaciones de toxicidad y especificidad (8, 124). En general, las proteínas Cry y Vip muestran espectros de actividad reducidos y muchas veces acotados a unas cuantas especies de insectos pertenecientes a un mismo orden. No obstante, la toxicidad de las proteínas Cry1 no se restringe sólo a los lepidópteros. Por ejemplo, las proteínas Cry1Ba y Cry1Ia demostraron poseer también toxicidad para coleópteros (12, 52, 86, 99, 120) y la proteína Cry1Ca para dípteros (115). Sucede algo similar con la proteína Cry2Aa, que es tóxica para dípteros también (136). En la Tabla 3 se presentan en forma detallada las proteínas Cry y Vip tóxicas para lepidópteros, como así también las familias y especies de insectos susceptibles.
Tabla 3. Toxicidad de proteínas Cry y Vip para insectos lepidópteros.


BIOINSECTICIDAS A BASE DE B. THURINGIENSIS
Los bioinsecticidas desarrollados en los inicios y muchos otros usados en la actualidad incluyen en su formulación como ingrediente activo una mezcla de cristales y esporas de B. thuringiensis. Estos productos tienen como limitación que presentan una especificidad restringida a ciertos órdenes de insectos, potencia baja y toxicidad residual corta. A pesar de ello, han sido los agentes de control biológico más populares (13). A partir de la entrada al mercado del primer producto comercial a base de B. thuringiensis llamado "Sporoine", en Francia en 1938, existió un interés creciente, que sigue aún hoy, en desarrollar productos más avanzados, como se verá en los párrafos subsiguientes.
B. thuringiensis svar. kurstaki HD-1 es por excelencia la cepa utilizada para el control de insectos lepidópteros, plagas agrícolas y forestales. Esta cepa fue aislada originalmente por Dulmage en 1970, lo que constituye un hito en la historia del uso de B. thuringiensis como larvicida, ya que fue la responsable de que los productos a base de B. thuringiensis puedan competir con los insecticidas químicos en términos de eficiencia. Esta cepa resultó ser hasta 200 veces más tóxica para algunas especies de lepidópteros que las otras cepas utilizadas en los productos de aquella época.
B. thuringiensis svar. kurstaki HD-1 es una de las cepas de B. thuringiensis mejor estudiadas y se caracteriza por la portación de los siguientes genes cry antilepidópteros: cry1Aa, cry1Ab, cry1Ac, cry2Aa, cry2Ab y cry1Ia (58, 102). El descubrimiento de B. thuringiensis svar. israelensis (44), para el control de larvas de mosquitos y jejenes, expandió el uso de B. thuringiensis como bioinsecticida. La mayoría de los bioinsecticidas a base de B. thuringiensis se producen empleando un número reducido de cepas y utilizan sólo una pequeña proporción de las proteínas Cry conocidas. En los laboratorios del IMYZA-INTA, contamos con una colección de más de 300 cepas nativas que hemos aislado de suelo, filoplano de plantas, residuos de la molienda de granos, larvas de insectos muertos y telarañas, a partir de muestras provenientes de regiones agroecológicas diversas de nuestro país. La mayoría de los cristales de estas cepas están caracterizados mediante microscopía de contraste de fases, SDSPAGE, PCR con cebadores generales y específicos para diversos genes cry y mediante ensayos biológicos de toxicidad frente a miembros de los órdenes Lepidoptera, Diptera y Coleoptera, y constituyen una fuente de recursos biológicos y genéticos muy rica.
El uso de este tipo de insecticidas biológicos en Argentina es limitado debido, en gran parte, a que los productos comerciales registrados y disponibles en el mercado son importados y caros, en comparación con los insecticidas químicos. El INTA cuenta actualmente con un bioinsecticida de primera generación a base de una cepa nativa de B. thuringiensis dirigido al control de larvas de insectos lepidópteros, totalmente desarrollado por nuestro grupo, que pronto será registrado y que tenderá a superar las limitaciones mencionadas.
Bioinsecticidas de primera generación
Son aquellos cuya formulación incluye como ingrediente activo una mezcla de cristales y esporas de B. thuringiensis. Constituyen la mayor proporción de los productos comerciales que se utilizan en el mundo (Tabla 4). Estos productos se encuentran disponibles en diferentes tipos de formulaciones, tanto líquidas como sólidas. Estas formulaciones satisfacen en el presente los requerimientos de distintos ámbitos, desde la agricultura hasta la salud pública (85, 89).
Tabla 4. Bioinsecticidas de primera generación tóxicos para lepidópteros disponibles en el mundo.

Estos productos se utilizan en el sector agrícola, principalmente para el control de plagas lepidópteras en cultivos de maíz, trigo, sorgo, soja, algodón y frutales. Aunque su uso es limitado en comparación con los insecticidas convencionales, existe un interés creciente en el manejo integrado de plagas (según la FAO: " cuidadosa consideración de todas las técnicas disponibles para combatir las plagas y la posterior integración de medidas apropiadas que disminuyen el desarrollo de las mismas y mantienen el empleo de plaguicidas y otras intervenciones a niveles económicamente justificados y que reducen al mínimo los riesgos para la salud humana y el ambiente"). Dicho interés se debe al menor riesgo de desarrollo de resistencia, a políticas nacionales sobre el uso de los pesticidas convencionales y a los costos altos del desarrollo de insecticidas químicos nuevos. Todas estas observaciones sugieren que los agentes de control biológico, en general, incrementarían su uso e importancia en los próximos años.
Bioinsecticidas de segunda generación
Son aquellos constituidos por una mezcla de esporas y cristales provenientes de una cepa de B. thuringiensis a la cual se le introdujo mediante algún mecanismo de transferencia de genes, ya sea transformación, transducción y/o conjugación, genes cry presentes en otras cepas de B. thuringiensis y no en la receptora, lo que permite ampliar su espectro de actividad hacia otros insectos plaga o aumentar su toxicidad mediante un efecto sinérgico o aditivo. Los productos a base de B. thuringiensis modificados genéticamente pueden involucrar otras manipulaciones, como la recombinación específica de sitio, curación de plásmidos, mutagénesis in vitro y construcción de proteínas Cry híbridas.
El uso de B. thuringiensis como huésped de otros genes distintos de los que poseía la cepa original ofrece una serie de ventajas. Las cepas de B. thuringiensis pueden mantener de manera estable y expresar eficientemente varios genes cry; esto les permite aumentar la toxicidad para un insecto plaga determinado en forma aditiva o sinérgica. Distintos genes cry con diferentes modos de acción o diferentes propiedades de unión al receptor pueden reducir la posibilidad de desarrollo de resistencia (119).
Existen productos a base de cepas de B. thuringiensis transconjugantes, como es el caso de los productos Condor® y Cutglass®. Para su obtención, un plásmido autotransferible que porta un gen cry1A de una cepa del svar aizawai fue transferido por conjugación a una cepa receptora del svar kurstaki, y un plásmido que contiene un gen cry1 de una cepa del svar kurstaki fue transferido por conjugación a una cepa receptora del svar aizawai, respectivamente. El ingrediente activo del producto Foil® OF produce las proteínas Cry1Ac y Cry3A, y presenta toxicidad para plagas de lepidópteros y coleópteros. Esta ampliación en el rango de huéspedes fue lograda mediante la transferencia de un plásmido portador del gen cry3A de B. thuringiensis svar. morrisoni a una cepa del svar. kurstaki (40).
Existen otros desarrollos con el objeto de obtener este tipo de productos que no han sido registrados. Un ejemplo de estos fue detallado por Kalman et al. (68). Desarrollaron una cepa a la que se le introdujo de manera estable el gen cry1C de B. thuringiensis svar. aizawai (gen con actividad tóxica para Spodoptera, que no se encuentra en B. thuringiensis svar. kurstaki) dentro de B. thuringiensis svar. kurstaki HD-73 (que sólo contiene cry1Ac), de esta forma se logró ampliar el rango de huéspedes susceptibles.
Bioinsecticidas de tercera generación
Son aquellos cuya formulación contiene bacterias recombinantes que han sido modificadas genéticamente con genes cry o cepas de B. thuringiensis modificadas con otros genes que codifican otros factores de virulencia distintos de las d-endotoxinas. Estos productos se desarrollaron con el objetivo de resolver la limitación de la toxicidad residual corta que poseen los productos de primera generación, o simplemente de aumentar la toxicidad hacia los insectos. Una estrategia que permitió obtener un tipo de estos productos consistió en el uso de bacterias recombinantes muertas, con el objeto de obtener un sistema nuevo de utilización de las proteínas Cry (38). La compañía Mycogen desarrolló una estrategia que implica el encapsulamiento de varias proteínas Cry dentro de células de Pseudomonas fluorescens. A este sistema se lo llamó CellCap® y consiste en matar las células transformadas durante la fase estacionaria de crecimiento mediante un tratamiento físico o químico. La ventaja que brinda este sistema sobre los convencionales sería que la célula de Pseudomonas fluorescens protege a las proteínas Cry de B. thuringiensis de la degradación causada por el medio ambiente, y otorga una actividad insecticida residual más prolongada.
Existen otros bioinsecticidas que no fueron registrados aún, que se obtuvieron insertando genes cry de B. thuringiensis en otros microorganismos. Estos fueron seleccionados teniendo en cuenta su capacidad de colonizar el habitat del insecto blanco del tratamiento, con la idea de que los organismos transformados puedan sintetizar de forma continua cantidades suficientes de proteína Cry para evitar el daño causado por el insecto (42). Se llevaron a cabo varios estudios en los cuales se insertaron genes específicos con toxicidad para lepidópteros en bacterias que colonizan externamente la superficie de hojas y raíces de plantas, tales como Pseudomonas cepacia (118), Pseudomonas fluorescens (94, 128) y Bacillus megaterium (11), o internamente, tales como Clavibacter xyly (75).
El inconveniente que acarrea la introducción de genes cry en otras bacterias distintas de B. thuringiensis es que involucra la liberación de microorganismos recombinantes, los que presentan muchas restricciones de regulación en su uso. Una de ellas se relaciona con la posible inestabilidad de la característica que se introduce, como por ejemplo, que los genes insertados se transfieran a otras especies bacterianas (123). No obstante, se han utilizado distintas estrategias para minimizar este problema. Con este objeto se utilizaron derivados del transposón Tn5 transposasa negativos (94) o "vectores suicidas", cuya integración es dependiente de la recombinación entre secuencias de ADN homólogas (128).
Existen también otros bioinsecticidas de tercera generación -ninguno de ellos registrado-, en los que su principio activo son cepas de B. thuringiensis modificadas genéticamente mediante la inserción de genes que codifican para otros factores de virulencia distintos de las d-endotoxinas. Estos bioinsecticidas también poseen restricciones en cuanto a su regulación de uso.
Vale la pena destacar los desarrollos informados por Thamthiankul et al. (121) y Zhu et al. (141), realizados con el objetivo de controlar insectos lepidópteros. En el primero de ellos lograron una cepa recombinante de B. thuringiensis svar. aizawai que demostró una toxicidad mejorada para Spodoptera exigua con respecto a la cepa salvaje, mediante la expresión cromosomal de un gen de quitinasa durante la etapa de esporulación; ese gen no se encontraba en la cepa salvaje (recordar que los genes cry se expresan durante la esporulación). La actividad de quitinasa puede hidrolizar la quitina de la membrana peritrófica del insecto blanco, lo que forma poros y permite que una mayor cantidad de toxina Cry alcance las células epiteliales del intestino medio del insecto (61). En el segundo trabajo, a partir de una cepa comercial de B. thuringiensis muy tóxica para Helicoverpa armigera y Plutella xylostella obtuvieron una bacteria recombinante que expresa de manera estable el gen vip3Aa7. De esta forma se logró aumentar la toxicidad para los insectos mencionados, y además, ampliar su rango de toxicidad a Spodoptera exigua, un insecto plaga que era naturalmente resistente a la cepa salvaje.
PLANTAS TRANSGÉNICAS Bt
La ingeniería genética desarrolló muchas especies de plantas que expresan genes cry de B. thuringiensis y las convirtió así en "plantas insecticidas". Comúnmente se hace referencia a este tipo de plantas como "plantas o cultivos Bt" (por ejemplo, maíz Bt, algodón Bt, etc.). El primer informe de una planta transgénica con un gen cry de B. thuringiensis data de 1987 (126). Se desarrollaron plantas de tabaco ( Nicotiana tabacum) que producían cantidades suficientes de proteína Cry para controlar larvas de primer estadio de Manduca sexta. Desde entonces, al menos diez tipos de genes cry distintos se introdujeron en 26 especies vegetales: cry1Aa, cry1Ab, cry1Ac, cry1Ba, cry1Ca, cry1H, cry2Aa, cry3A, cry6A y cry9C.
El empleo de este tipo de plantas posee la ventaja de reducir la necesidad de aplicar insecticidas y de proveer una protección duradera a lo largo de la temporada de cultivo. Otra característica muy importante que poseen es que los únicos insectos expuestos a la toxina son aquellos que se encuentran alimentándose de los cultivos y no otros. No obstante, la mayor ventaja de estas plantas Bt es que brindan a los agricultores una alternativa al uso de pesticidas químicos tradicionales y constituyen una herramienta para el control de plagas de importancia económica que son difíciles de controlar por los primeros. Todas estas ventajas se verían reflejadas finalmente en beneficios enormes para la producción de alimentos y en una calidad medioambiental mejor en todo el mundo (60, 69).
Por otro lado, las plantas Bt poseen la gran desventaja que radica en la posible generación de resistencia en ciertas poblaciones naturales de insectos que se alimentan de ellas. Este fenómeno determinaría la inutilización de determinadas proteínas Cry para su control, ya sea mediante su empleo en plantas transgénicas o con los bioinsecticidas que los contengan (47).
En el año 2002 se aprobó en los Estados Unidos de América y en Australia el uso comercial de una planta transgénica de algodón que produce de manera simultánea las proteínas Cry1Ac y Cry2Ab (140). Los modelos teóricos actuales sugieren que las plantas que expresan dos genes cry diferentes (o un gen cry y otro de distinto tipo, como uno vip), que son reconocidos por al menos un receptor distinto son más efectivos en el control de insectos plaga y tendrían el potencial de demorar la aparición de resistencia (140).
Hasta el presente, existen autorizadas para su cultivo y comercialización una línea transgénica de algodón Bt y seis de maíz Bt (Tabla 5) (1).
Tabla 5. Plantas transgénicas Bt aprobadas para su comercialización en Argentina (1).

1. AGBIOS (Agriculture & Biotechnology Strategies, Inc.). GMO Database. 2008; http://www.agbios.com/dbase.php. [ Links ]
2. Armengol G, Escobar M, Maldonado M, Ordúz S. Diversity of Colombian strains of Bacillus thuringiensis with insecticidal activity against dipteran and lepidopteran insects. J Appl Microbiol 2007; 102: 77-88. [ Links ]
3. Barboza-Corona J, Nieto-Mazzocco E, Velázquez-Robledo R, Salcedo-Hernández R, Bautista M, Jiménez B, Ibarra J. Cloning, sequencing, and expression of the chitinase gene chiA74 from Bacillus thuringiensis. Appl Environ Microbiol 2003; 69: 1023-9. [ Links ]
4. Barboza-Corona J, Reyes-Ríos D, Salcedo-Hernández R, Bideshi D. Molecular and Biochemical Characterization of an Endochitinase (ChiA-HD73) from Bacillus thuringiensis subsp. kurstaki HD-73. Mol Biotechnol 2008; 39: 29-37. [ Links ]
5. Baum J, González J. Mode of replication, size and distribution of naturally occurring plasmids in Bacillus thuringiensis. FEMS Microbiol Lett 1992; 96: 143-8. [ Links ]
6. Benintende G, López-Meza J, Cozzi J, Ibarra J. Novel nontoxic isolates of Bacillus thuringiensis. Lett Appl Microbiol 1999; 29: 151-5. [ Links ]
7. Ben-Dov E, Zaritsky A, Dahan E, Barak Z, Sinai R, Manashherob R, et al. Extended screening by PCR for seven cry-group genes from field-collected strains of Bacillus thuringiensis. Appl Environ Microbiol 1997; 63: 4883-90. [ Links ]
8. Bhalla R, Dalal M, Panguluri S, Jagadish B, Mandaokar A, Singh A, et al. Isolation, characterization and expression of a novel vegetative insecticidal protein gene of Bacillus thuringiensis. FEMS Microbiol Lett 2005; 243: 467-72. [ Links ]
9. Boonserm P, Davis P, Ellar D, Li J. Crystal structure of the mosquito-larvicidal toxin Cry4Ba and its biological implications. J Mol Biol 2005; 348: 363-82. [ Links ]
10. Boonserm P, Mo M, Angsuthanasombat C, Lescar J. Structure of the functional form of the mosquito larvicidal Cry4Aa toxin from Bacillus thuringiensis at a 2.8-Å resolution. J Bacteriol 2006; 188: 3391-401. [ Links ]
11. Bora R, Murty M, Shenbargarathai R, Sekar V. Introduction of Lepidopteran-specific insecticidal crystal protein gene of Bacillus thuringiensis subsp. kurstaki by conjugal transfer into a Bacillus megaterium strain that persists in the cotton phylloplane. Appl Environ Microbiol 1994; 60: 214-22. [ Links ]
12. Bradley D, Harkey M, Kim M, Biever K, Bauer L. The insecticidal CryIB crystal protein of Bacillus thuringiensis ssp. thuringiensis has dual specificity to coleopteran and lepidopteran larvae. J Invertebr Pathol 1995; 65: 162-73. [ Links ]
13. Brar S, Verma M, Tyagi R, Valéro J. Recent advances in downstream processing and formulations of Bacillus thuringiensis based biopesticides. Process Biochem 2006; 41: 323-42. [ Links ]
14. Bravo A, Gómez I, Conde J, Muñoz-Garay C, Sánchez J, Miranda R, et al. Oligomerization triggers binding of a Bacillus thuringiensis Cry1Ab pore-forming toxin to aminopeptidase N receptor leading to insertion into membrane microdomains. Biochim Biophys Acta 2004; 1667: 38-46. [ Links ]
15. Bravo A, Sarabia S, López L, Ontiveros H, Abarca C, Ortiz A, et al. Characterization of cry genes in a Mexican Bacillus thuringiensis strain collection. Appl Environ Microbiol 1998; 64: 4965-72. [ Links ]
16. Broderick N, Raffa K, Handelsman J. Midgut bacteria required for Bacillus thuringiensis insecticidal activity. Proc Natl Acad Sci USA 2006; 103: 15196-9. [ Links ]
17. Brown K, Whiteley H. Molecular characterization of two novel crystal protein genes from Bacillus thuringiensis subsp. thompsoni. J Bacteriol 1992; 174: 549-57. [ Links ]
18. Bulla L, Bechtel D, Kramer K, Shethna Y, Aronson A, Fitz- James P. Ultrastructure, physiology, and biochemistry of Bacillus thuringiensis. CRC Crit Rev Microbiol 1980; 8: 147-204. [ Links ]
19. Burton S, Ellar D, Li J, Derbyshire D. N-acetylgalactosamine on the putative insect receptor aminopeptidase N is recognised by a site on the domain III lectin-like fold of a Bacillus thuringiensis insecticidal toxin. J Mol Biol 1999; 287: 1011-22. [ Links ]
20. Cannon R. Bacillus thuringiensis use in agriculture: a molecular perspective. Biol Rev 1996; 71: 561-636. [ Links ]
21. Carlton BC, González JM. The genetics and molecular biology of Bacillus thuringiensis. En: Dudnan, editors. The molecular biology of the bacilli. 1985, p. 211-49. [ Links ]
22. Cerón J, Covarrubias L, Quintero R, Ortiz A, Ortiz M, Aranda E, et al. PCR analysis of the cryI insecticidal crystal family genes from Bacillus thuringiensis. Appl Environ Microbiol 1994; 60: 353-6. [ Links ]
23. Cerón J, Ortiz A, Quintero R, Guereca L, Bravo A. Specific PCR primers directed to identify cryI and cryIII genes within a Bacillus thuringiensis strain collection. Appl Environ Microbiol 1995; 61: 3826-31. [ Links ]
24. Crickmore N, Ellar D. Involvement of a possible chaperonin in the efficient expression of a cloned CryIIA deltaendotoxin gene in Bacillus thuringiensis. Mol Microbiol 1992; 6: 1533-7. [ Links ]
25. Crickmore N, Zeigler D, Feitelson J, Schnepf E, Van Rie J, Lereclus D, et al. Revision of the nomenclature for the Bacillus thuringiensis pesticidal crystal proteins. Microbiol Mol Biol Rev 1998; 62: 807-13. [ Links ]
26. Crickmore N, Zeigler D, Schnepf E, Van Rie J, Lereclus D, Baum J, et al. Bacillus thuringiensis toxin nomenclature. 2008; http://www.lifesci.sussex.ac.uk/Home/Neil_Crickmore/Bt/ [ Links ]
27. Chen X, Lee M, Dean D. Site-directed mutations in a highly conserved region of Bacillus thuringiensis delta-endotoxin affect inhibition of short circuit current across Bombyx mori midguts. Proc Natl Acad Sci USA 1993; 90: 9041-5. [ Links ]
28. Chen F, Tsai M, Peng C, Chak K. Dissection of cry gene profiles of Bacillus thuringiensis isolates in Taiwan. Curr Microbiol 2004; 48: 270-5. [ Links ]
29. Choi S, Shin B, Kong E, Rho H, Park S. Cloning of a new Bacillus thuringiensis cry1I-type crystal protein gene. Curr Microbiol 2000; 41: 65-9. [ Links ]
30. Dankocsik C, Donovan W, Jany C. Activation of a cryptic crystal protein gene of Bacillus thuringiensis subspecies kurstaki by gene fusion and determination of the crystal protein insecticidal specificity. Mol Microbiol 1990; 4: 2087- 94. [ Links ]
31. Derbyshire D, Ellar D, Li J. Crystallization of the Bacillus thuringiensis toxin Cry1Ac and its complex with the receptor ligand N-acetyl-D-galactosamine. Acta Crystallog sect D 2001; 57: 1938-44. [ Links ]
32. de Maagd R, Bravo A, Crickmore N. How Bacillus thuringiensis has evolved specific toxins to colonize the insect world. Trends Genet 2001; 17: 193-9. [ Links ]
33. de Maagd R, Kwa M, van der Klei H, Yamamoto T, Schipper B, Vlak J, et al. Domain III substitution in Bacillus thuringiensis delta-endotoxin CryIA(b) results in superior toxicity for Spodoptera exigua and altered membrane protein recognition. Appl Environ Microbiol 1996; 62: 1537-43. [ Links ]
34. Donovan W, Donovan W, Engleman J, Donovan J, Baum J, Bunkers G, et al. Discovery and characterization of Sip1A: A novel secreted protein from Bacillus thuringiensis with activity against coleopteran larvae. Appl Microbiol Biotechnol 2006; 72: 713-9. [ Links ]
35. Ejiofor A, Johnson T. Physiological and molecular detection of crystalliferous Bacillus thuringiensis strains from habitats in the South Central United States. J Ind Microbiol Biotechnol 2002; 28: 284-90. [ Links ]
36. Estruch J, Warren G, Mullins M, Nye G, Craig J, Koziel M. Vip3A, a novel Bacillus thuringiensis vegetative insecticidal protein with a wide spectrum of activities against lepidopteran insects. Proc Natl Acad Sci USA 1996; 93: 5389-94. [ Links ]
37. Farkas J, Sebesta K, Horska K, Samek Z, Dollijs J, Storm F. The structure of exotoxin of Bacillus thuringiensis var. gelechiae. Coll Czech Chem Com 1969; 34:1118-20. [ Links ]
38. Gaertner F, Quick T, Thompson M. CellCap: an encapsulation system for insecticidal biotoxin proteins. En: Kim, L, editor. Advanced engineered pesticides. Marcer Dekker, 1993, p. 73-83. [ Links ]
39. Galitsky N, Cody V, Wojtczak A, Ghosh D, Luft JR, Pangborn W, et al. Structure of the insecticidal bacterial deltaendotoxin Cry3Bb1 of Bacillus thuringiensis. Acta Crystallogr D Biol Crystallogr 2001; 57: 1101-9. [ Links ]
40. Gawron-Burke C, Baum J. Genetic manipulation of Bacillus thuringiensis insecticidal crystal protein genes in bacteria. Genet Eng (NY) 1991; 13: 237-63. [ Links ]
41. Ge A, Shivarova N, Dean D. Location of the Bombyx mori specificity domain on a Bacillus thuringiensis delta-endotoxin protein. Proc Natl Acad Sci USA 1989; 86: 4037-41. [ Links ]
42. Gelernter W. Targeting insectice-resistance markers: new developments in microbial based product. Managing resistance to agrochemicals: from fundamental research to practical strategies. American Chemical Society - USA 1990; 4221: 105-17. [ Links ]
43. Gleave A, Williams R, Hedges R. Screening by polymerase chain reaction of Bacillus thuringiensis serotypes for the presence of cryV-like insecticidal protein genes and characterization of a cryV gene cloned from B. thuringiensis subsp. kurstaki. Appl Environ Microbiol 1993; 59: 1683-7. [ Links ]
44. Goldberg L, Margalit J. A bacterial spore demonstrating rapid larvicidal activity against Anopheles sergentie, Uranotaenia unguiculata, Culex univitattus, Aedes aegypti and Culex pipiens. Mosq News 1977; 37: 355-8. [ Links ]
45. Gómez I, Arenas I, Benítez I, Miranda-Ríos J, Becerril B, Grande R, et al. Specific epitopes of domains II and III of Bacillus thuringiensis Cry1Ab toxin involved in the sequential interaction with cadherin and aminopeptidase-N receptors in Manduca sexta. J Biol Chem 2006; 281: 34032-9. [ Links ]
46. Gómez I, Sánchez J, Miranda R, Bravo A, Soberón M. Cadherin-like receptor binding facilitates proteolytic cleavage of helix alpha-1 in domain I and oligomer pre-pore formation of Bacillus thuringiensis Cry1Ab toxin. FEBS Lett 2002; 513: 242-6. [ Links ]
47. González-Cabrera J. Plantas transgénicas con la capacidad insecticida de Bacillus thuringiensis. En: Caballero P, Ferré J, editores. Bioinsecticidas: fundamentos y aplicaciones de Bacillus thuringiensis en el Control Integrado de Plagas, 2001, p. 169-87. [ Links ]
48. González J, Dulmage H, Carlton B. Correlation between specific plasmids and delta-endotoxin production in Bacillus thuringiensis. Plasmid 1981; 5: 352-65. [ Links ]
49. Gordon R, Haynes W, Pang C. The genus Bacillus. En: US Department of Agriculture handbook N° 427. Washington DC., USDA, 1973, p. 109-26. [ Links ]
50. Griko N, Rose-Young L, Zhang X, Carpenter L, Candas M, Ibrahim MA, et al. Univalent binding of the Cry1Ab toxin of Bacillus thuringiensis to a conserved structural motif in the cadherin receptor BT-R1. Biochemistry 2007; 46: 10001-7. [ Links ]
51. Grochulsky P, Masson L, Borisova S, Pusztai-Carey M, Schwartz L, Brousseau R, et al. Bacillus thuringiensis Cry1A(a) insecticidal toxin: crystal structure and channel formation. J Mol Biol 1995; 254: 447-64. [ Links ]
52. Grossi-de-Sa M, Quezado de Magalhaes M, Silva M, Silva S, Dias S, Nakasu E, et al. Susceptibility of Anthonomus grandis (cotton boll weevil) and Spodoptera frugiperda (fall armyworm) to a Cry1Ia-type toxin from a Brazilian Bacillus thuringiensis strain. J Biochem Mol Biol 2007; 40: 773-82. [ Links ]
53. Guerchicoff A, Delécluse A, Rubinstein C. The Bacillus thuringiensis cyt genes for hemolytic endotoxins constitute a gene family. Appl Environ Microbiol 2001; 67: 1090-6. [ Links ]
54. Guerchicoff A, Ugalde R, Rubinstein C. Identification and characterization of a previously undescribed cyt gene in Bacillus thuringiensis subsp. israelensis. Appl Environ Microbiol 1997; 63: 2716-21. [ Links ]
55. Guttman D, Ellar D. Phenotypic and genotypic comparisons of 23 strains from the Bacillus cereus complex for a selection of known and putative B. thuringiensis virulence factors. FEMS Microbiol Lett 2000; 188: 7-13. [ Links ]
56. Hernández C, Andrew R, Bel Y, Ferré F. Isolation and toxicity of Bacillus thuringiensis from potato-growing areas in Bolivia. J Invertebr Pathol 2005; 88: 8-16. [ Links ]
57. Herrero S, González-Cabrera J, Ferré J, Bakker P, de Maagd R. Mutations in the Bacillus thuringiensis Cry1Ca toxin demonstrate the role of domains II and III in specificity towards Spodoptera exigua larvae. Biochem J 2004; 384: 507-13. [ Links ]
58. Höfte H, Whiteley H. Insecticidal crystal proteins of Bacillus thuringiensis. Microbiol Rev 1989; 53: 242-55. [ Links ]
59. Hongyu Z, Ziniu Y, Wangxi D. Composition and ecological distribution of cry proteins and their genotypes of Bacillus thuringiensis isolates from warehouses in China. J Invertebr Pathol 2000; 76: 191-7. [ Links ]
60. Hossain F, Pray C, Lu Y, Huang J, Fan C, Hu R. Genetically modified cotton and farmers' health in China. Int J Occup Environ Health 2004; 10: 296-303. [ Links ]
61. Huber H, Lüthy P. Bacillus thuringiensis d-endotoxin: composition and activation. Davidson editor. Pathogenesis of invertebrate microbial diseases. New Jersey, U.S.A., 1981. [ Links ]
62. Ibarra J, Federici, B. Isolation of a relatively nontoxic 65- kilodalton protein inclusion from the parasporal body of Bacillus thuringiensis subsp. israelensis. J Bacteriol 1986; 165: 527-33. [ Links ]
63. Jansens S, van Vliet A, Dickburt C, Buysse L, Piens C, Saey B, et al. Transgenic corn expressing a Cry9C insecticidal protein from Bacillus thuringiensis protected from European corn borer damage. Crop Sci 1997; 37: 1616-24. [ Links ]
64. Jiménez-Juárez N, Muñoz-Garay C, Gómez I, Saab-Rincón G, Damián-Almazo J, Gill S, et al. Bacillus thuringiensis Cry1Ab mutants affecting oligomer formation are non-toxic to Manduca sexta larvae. J Biol Chem 2007; 282: 21222-9. [ Links ]
65. Juárez-Pérez V, Ferrandis M, Frutos R. PCR-based approach for detection of novel Bacillus thuringiensis cry genes. Appl Environ Microbiol 1997; 63: 2997-3002. [ Links ]
66. Juárez-Pérez V, Guerchicoff A, Rubinstein C, Delécluse A. Characterization of Cyt2Bc toxin from Bacillus thuringiensis subsp. medellin. Appl Environ Microbiol 2002; 68: 2997-3002. [ Links ]
67. Jurat-Fuentes J, Adang M. Characterization of a Cry1Acreceptor alkaline phosphatase in susceptible and resistant Heliothis virescens larvae. Eur J Biochem 2004; 271: 3127- 35. [ Links ]
68. Kalman S, Kiehne K, Cooper N, Reynoso M, Yamamoto T. Enhanced production of insecticidal proteins in Bacillus thuringiensis strains carrying an additional crystal protein gene in their chromosomes. Appl Environ Microbiol 1995; 61: 3063-8. [ Links ]
69. Khetan S. Bacterial Insecticide: Bacillus thuringiensis. En: Khetan editor. Microbial Pest Control, 2001, p. 14. [ Links ]
70. Kim H. Comparative study of the frequency, flagellar serotype, crystal shape, toxicity, and cry gene contents of Bacillus thuringiensis from three environments. Curr Microbiol 2000; 41: 250-6. [ Links ]
71. Klier A, Fargette F, Ribier J, Rapoport G. Cloning and expression of the crystal protein genes from Bacillus thuringiensis strain Berliner 1715. EMBO J 1982; 1: 791-9. [ Links ]
72. Klier A, Rapoport G. Cloning and heterospecific expression of the crystal protein genes from Bacillus thuringiensis. EMBO J. En: Alout J, Fehrenbach F, Free J, Jalljaszenice J, editors. Bacterial protein toxins, 1984, p. 65-72. [ Links ]
73. Knowles B. Mechanism of action of Bacillus thuringiensis insecticidal d-endotoxins. Advan Insect Physiol 1994; 24: 175-308. [ Links ]
74. Kostichka K, Warren G, Mullins M, Mullins A, Palekar N, Craig J, et al. Cloning of a cryV-type insecticidal protein gene from Bacillus thuringiensis: the cryV-encoded protein is expressed early in stationary phase. J Bacteriol 1996; 178: 2141-4. [ Links ]
75. Lampel J, Canter G, Dumock M, Kelly J, Anderson J, Uratani B, et al. Integrative cloning, expression and stability of the cryIA(c) gene from Bacillus thuringiensis subsp. kurstaki in a recombinant strain of Clavibacter xyli subsp. cynodontis. Appl Environ Microbiol 1994; 60: 501-8. [ Links ]
76. Lecadet M. Collection of Bacillus thuringiensis and Bacillus sphaericus. Classified by H serotypes. 1998. Institut Pasteur. Paris. [ Links ]
77. Lechner S, Mayr R, Francis K, Pruss B, Kaplan T, Wiessner- Gunkel E, et al. Bacillus weihenstephanensis sp. nov. is a new psychrotolerant species of the Bacillus cereus group. Int J Syst Bacteriol 1998; 48: 1373-82. [ Links ]
78. Lee M, Walters F, Hart H, Palekar N, Chen J. The mode of action of the Bacillus thuringiensis vegetative insecticidal protein Vip3A differs from that of Cry1Ab delta-endotoxin. Appl Environ Microbiol 2003; 69: 4648-57. [ Links ]
79. Li J, Carroll J, Ellar D. Crystal structure of insecticidal d- endotoxin from Bacillus thuringiensis at 2.5 Å resolution. Nature 1991; 353: 815-21. [ Links ]
80. Li J, Derbyshire D, Promdonkoy B, Ellar D. Structural implications for the transformation of the Bacillus thuringiensis delta-endotoxins from water-soluble to membrane-inserted forms. Biochem Soc Trans 2001; 29: 571-7. [ Links ]
81. Liu Y, Sui M, Ji D, Wu I, Chou C, Chen C. Protection from ultraviolet irradiation by melanin of mosquitocidal activity of Bacillus thuringiensis var. israelensis. J Invertebr Pathol 1993; 62: 131-6. [ Links ]
82. Loeza-Lara P, Benintende G, Cozzi J, Ochoa-Zarzosa A, Baizabal-Aguirre V, Valdez-Alarcón J, et al. The plasmid pBMBt1 from Bacillus thuringiensis subsp. darmstadiensis (INTA Mo14-4) replicates by the rolling-circle mechanism and encodes a novel insecticidal crystal protein-like gene. Plasmid 2005; 54: 229-40. [ Links ]
83. López-Meza J, Ibarra J. Characterization of a Novel Strain of Bacillus thuringiensis. Appl Environ Microbiol 1996; 62: 1306-10. [ Links ]
84. Lu H, Rajamohan F, Dean D. Identification of amino acid residues of Bacillus thuringiensis d-endotoxin CryIAa associated with membrane binding and toxicity to Bombyx mori. J Bacteriol 1994; 176: 5554-9. [ Links ]
85. Mahilum M, Ludwig M, Madon M, Becker N. Evaluation of the present dengue situation and control strategies against Aedes aegypti in Cebu City, Philippines. J Vector Ecol 2005; 30: 277-83. 86. Martins E, Aguiar R, Martins N, Melatti V, Falcão R, Gomes A, et al. Recombinant Cry1Ia protein is highly toxic to cotton boll weevil ( Anthonomus grandis Boheman) and fall armyworm ( Spodoptera frugiperda). J Appl Microbiol 2008 104: 1363-71. [ Links ] [ Links ]
87. Masson L, Erlandson M, Puzstai-Carey M, Brousseau R, Juárez-Pérez V, Frutos R. A holistic approach for determining the entomopathogenic potential of Bacillus thuringiensis strains. Appl Environ Microbiol 1998; 64: 4782-8. [ Links ]
88. Masson L, Tabashnik B, Mazza A, Préfontaine G, Potvin L, Brousseau R, et al. Mutagenic analysis of a conserved region of domain III in the Cry1Ac toxin of Bacillus thuringiensis. Appl Environ Microbiol 2002; 68: 194-200. [ Links ]
89. Maxwell E, Fadamiro H, McLaughlin J. Suppression of Plutella xylostella and Trichoplusia ni in cole crops with attracticide formulations. J Econ Entomol 2006; 99: 1334- 44. [ Links ]
90. McGaughey W, Whalon M. Managing insect resistance to Bacillus thuringiensis toxins. Science 1992; 258: 1451-5. [ Links ]
91. Morse R, Yamamoto T, Stroud R. Structure of Cry2Aa suggests an unexpected receptor binding epitope. Structure 2001; 9: 409-17. [ Links ]
92. Nakamura K, Oshie K, Shimizu M, Takada Y, Oeda K, Ohkawa H. Construction of chimeric insecticidal proteins between the 130-kDa and 135-kDa proteins of Bacillus thuringiensis subsp. aizawai for analysis of structure-function relationship. Agric Biol Chem 1990; 54: 715-24. [ Links ]
93. Nakamura L. Bacillus pseudomycoides sp. nov. Int J Syst Bacteriol 1998; 48: 1031-5. [ Links ]
94. Obukowicz M, Perlak F, Kusano-Kretzmer K, Mayer E, Bolten S, Watrud L. Tn5-mediated integration of the deltaendotoxin gene from Bacillus thuringiensis into the chromosome of root-colonizing pseudomonads. J Bacteriol 1986; 168: 982-9. [ Links ]
95. Pardo-López L, Gómez I, Muñoz-Garay C, Jiménez-Juárez N, Soberón M, Bravo A. Structural and functional analysis of the pre-pore and membrane-inserted pore of Cry1Ab toxin. J Invertebr Pathol 2006; 92: 172-7. [ Links ]
96. Porcar M, Juárez-Pérez V. PCR-based identification of Bacillus thuringiensis pesticidal crystal genes. FEMS Microbiol Rev 2003; 26: 419-32. [ Links ]
97. Pusztai M, Fast P, Gringorten L, Kaplan H, Lessard T, Carey P. The mechanism of sunlight-mediated inactivation of Bacillus thuringiensis crystals. Biochem J 1991; 273: 43-7. [ Links ]
98. Rajamohan F, Hussain S, Cotrill J, Gould F, Dean D. Mutations at domain II, loop 3, of Bacillus thuringiensis CryIAa and CryIAb delta-endotoxins suggest loop 3 is involved in initial binding to lepidopteran midguts. J Biol Chem 1996; 271: 25220-6. [ Links ]
99. Ruiz de Escudero I, Estela A, Porcar M, Martínez C, Oguiza J, Escriche B, et al. Molecular and insecticidal characterization of a Cry1I protein toxic to insects of the families Noctuidae, Tortricidae, Plutellidae, and Chrysomelidae. Appl Environ Microbiol 2006; 72: 4796-804. [ Links ]
100. Salehi Jouzani G, Pourjan Abad A, Seifinejad A, Marzban R, Kariman K, Maleki B. Distribution and diversity of dipteranspecific cry and cyt genes in native Bacillus thuringiensis strains obtained from different ecosystems of Iran. J Ind Microbiol Biotechnol 2008; 35: 83-94. [ Links ]
101. Sanchis V, Lereclus D, Menou G, Chaufaux J, Lecadet M. Multiplicity of delta-endotoxin genes with different insecticidal specificities in Bacillus thuringiensis aizawai 7.29. Mol Microbiol 1988; 2: 393-404. [ Links ]
102. Sauka D. Estudio de genes y proteínas insecticidas de aislamientos nativos de Bacillus thuringiensis. Aportes al conocimiento de su distribución y toxicidad en plagas agrícolas. Tesis Doctoral. UBA. Director: Benintende G. 2007. [ Links ]
103. Sauka D, Amadio A, Zandomeni R, Benintende G. Strategy for amplification and sequencing of insecticidal cry1A genes from Bacillus thuringiensis. Antonie van Leeuwenhoek 2007; 91: 423-30. [ Links ]
104. Sauka D, Benintende G. (Comunicación personal). [ Links ]
105. Sauka D, Cozzi J, Benintende G. Screening of cry2 genes in Bacillus thuringiensis isolates from Argentina. Antonie van Leeuwenhoek 2005; 88: 163-5. [ Links ]
106. Sauka D, Cozzi J, Benintende G. Detection and identification of cry1I genes in Bacillus thuringiensis using polymerase chain reaction and restriction fragment length polymorphism analysis. Curr Microbiol 2006; 52: 60-3. [ Links ]
107. Schnepf E, Crickmore N, Van Rie J, Lereclus D, Baum J, Feitelson J, et al. Bacillus thuringiensis and its pesticidal crystal proteins. Microbiol Mol Biol Rev 1998; 62: 775-806. [ Links ]
108. Schnepf H, Tomczak K, Ortega J, Whiteley H. Specificitydetermining regions of a lepidopteran-specific insecticidal protein produced by Bacillus thuringiensis. J Biol Chem 1990; 265: 20923-30. [ Links ]
109. Schnepf H, Wong H, Whiteley H. The amino acid sequence of a crystal protein from Bacillus thuringiensis deduced from the DNA base sequence. J Biol Chem 1985; 260: 6264-72. [ Links ]
110. Schwartz J, Potvin L, Chen X, Brousseau R, Laprade R, Dean D. Single-site mutations in the conserved alternatingarginine region affect ionic channels formed by CryIAa, a Bacillus thuringiensis toxin. Appl Environ Microbiol 1997; 63: 3978-84. [ Links ]
111. Sergeev N, Distler M, Vargas M, Chizhikov V, Herold K, Rasooly A. Microarray analysis of Bacillus cereus group virulence factors. J Microbiol Methods 2006; 65: 488-502. [ Links ]
112. Shevelev A, Svarinsky M, Karasin A, Kogan Y, Chestukhina G, Stepanov V. Primary structure of cryX**, the novel delta- endotoxin-related gene from Bacillus thuringiensis spp. galleriae. FEBS Lett 1993; 336: 79-82. [ Links ]
113. Shin B, Park S, Choi S, Koo B, Lee S, Kim J. Distribution of cryV-type insecticidal protein genes in Bacillus thuringiensis and cloning of cryV-type genes from Bacillus thuringiensis subsp. kurstaki and Bacillus thuringiensis subsp. entomocidus. Appl Environ Microbiol 1995; 61: 2402-7. [ Links ]
114. Smedley D, Ellar D. Mutagenesis of three surface-exposed loops of a Bacillus thuringiensis insecticidal toxin reveals residues important for toxicity, receptor recognition and possibly membrane insertion. Microbiology 1996; 142: 1617- 24. [ Links ]
115. Smith G, Merrick J, Bone E, Ellar D. Mosquitocidal activity of the CryIC delta-endotoxin from Bacillus thuringiensis subsp. aizawai. Appl Environ Microbiol 1996; 62: 680-4. [ Links ]
116. Smulevitch S, Osterman A, Shevelev A, Kaluger S, Karasin A, Kadyrov R, et al. Nucleotide sequence of a novel deltaendotoxin gene cryIg of Bacillus thuringiensis ssp. galleriae. FEBS Lett 1991; 293: 25-8. [ Links ]
117. Sneath P. Spore forming gram-positive rods and cocci. En: Butler J, editor. Bergey's Manual of Systematic Bacteriology, 1986, p. 1104-207. [ Links ]
118. Stock C, McLoughlin T, Klein J, Adang M. Expression of Bacillus thuringiensis crystal protein gene in Pseudomonas cepacia 526. Can J Microbiol 1990; 396: 879-84. [ Links ]
119. Tabashnik B. Evolution of resistance to Bacillus thuringiensis toxins. Ann Rev Entomol 1994; 39: 47-79. [ Links ]
120. Tailor R, Tippett J, Gibb G, Pells S, Pike D, Jordan L, et al. Identification and characterization of a novel Bacillus thuringiensis delta-endotoxin entomocidal to coleopteran and lepidopteran larvae. Mol Microbiol 1992; 6: 1211-7. [ Links ]
121. Thamthiankul S, Moar W, Miller M, Panbangred W. Improving the insecticidal activity of Bacillus thuringiensis subsp. aizawai against Spodoptera exigua by chromosomal expression of a chitinase gene. Appl Microbiol Biotechnol 2004; 65: 183-92. [ Links ]
122. Thamthiankul S, Suan-Ngay S, Tantimavanich S, Panbangred W. Chitinase from Bacillus thuringiensis subsp. pakistani. Appl Microbiol Biotechnol 2001; 56: 395-401. [ Links ]
123. Tiedje J, Colwell R, Grossman Y, Hodson R, Lenski R, Mack R, et al. The planned introduction of genetically engineered organisms: ecological considerations and recommendations. Ecology 1989; 70: 298-315. [ Links ]
124. Tounsi S, J'Mal A, Zouari N, Jaoua S. Cloning and nucleotide sequence of a novel cry1Aa-type gene from Bacillus thuringiensis subsp. kurstaki. Biotechnol Lett 1999; 21: 771-5. [ Links ]
125. Uribe D, Martínez W, Cerón J. Distribution and diversity of cry genes in native strains of Bacillus thuringiensis obtained from different ecosystems from Colombia. J Invertebr Pathol 2003; 82: 119-27. [ Links ]
126. Vaeck M, Reynaerts A, Höfte H, Jansens S, De Beuckeleer M, Dean D, et al. Transgenic plants protected from insect attack. Nature 1987; 328: 33-7. [ Links ]
127. van Frankenhuyzen K, Gringorten L, Gauthier D. Cry9Ca1 Toxin, a Bacillus thuringiensis Insecticidal Crystal Protein with High Activity against the Spruce Budworm ( Choristoneura fumiferana). Appl Environ Microbiol 1997; 63: 4132-4. [ Links ]
128. Waalwijk C, Dullemans A, Maat C. Construction of a bioinsecticidal rhizosphere isolate of Pseudomonas fluorescens. FEMS Microbiol Lett 1991; 77: 257-64. [ Links ]
129. Wang J, Boets A, Van Rie J, Ren G. Characterization of cry1, cry2 and cry9 genes in Bacillus thuringiensis isolates from China. J Invertebr Pathol 2003; 82: 63-71. [ Links ]
130. Warren G. Vegetative insecticidal proteins: novel proteins for control of corn pests. En: Carozzi N, Koziel M. (Ed.). Advances in insect control, the role of transgenic plants. Taylor & Francis Ltd, London. 1997; 109-21. [ Links ]
131. Warren G, Koziel M, Mullins M. Auxiliary proteins for enhancing the insecticidal activity of pesticidal proteins. Novartis, US patent 5770696. 1998. [ Links ]
132. Wasano N, Ohba M. Assignment of delta-endotoxin genes of the four lepidoptera-specific Bacillus thuringiensis strains that produce spherical parasporal inclusions. Curr Microbiol 1998; 37: 408-11. [ Links ]
133. Wasano N, Ohba M, Miyamoto K. Two delta-endotoxin genes, cry9Da and a novel related gene, commonly occurring in Lepidoptera-specific Bacillus thuringiensis Japanese isolates that produce spherical parasporal inclusions. Curr Microbiol 2001; 42: 129-33. [ Links ]
134. West A, Burges H, White R, Wyborn C. Persistence of Bacillus thuringiensis parasporal crystal insecticidal activity in soil. J Invertebr Pathol 1984; 44: 128-33. [ Links ]
135. Whiteley H, Schnepf H. The molecular biology of parasporal crystal body formation in Bacillus thuringiensis. Annu Rev Microbiol 1986; 40: 549-76. [ Links ]
136. Widner W, Whiteley H. Two highly related insecticidal crystal proteins of Bacillus thuringiensis subsp. kurstaki possess different host range specificities. J Bacteriol 1989; 171: 965-74. [ Links ]
137. Wolfersberger M, Luthy A, Maure P, Pareti F, Sacchi B, Giordana M, et al. Preparation and partial characterization of aminoacid transporting brush border membrane vesicles from the larval midgut of the cabbage butterfly ( Pieris brassicae). Comp Biochem Physiol 1987; 86: 301-8. [ Links ]
138. Zhang X, Candas M, Griko N, Taussig R, Bulla L Jr. A mechanism of cell death involving an adenylyl cyclase/PKA signaling pathway is induced by the Cry1Ab toxin of Bacillus thuringiensis. Proc Natl Acad Sci USA 2006; 103: 9897-902. [ Links ]
139. Zhang X, Griko N, Corona S, Bulla L Jr. Enhanced exocytosis of the receptor BT-R(1) induced by the Cry1Ab toxin of Bacillus thuringiensis directly correlates to the execution of cell death. Comp Biochem Physiol B Biochem Mol Biol 2008; 149: 581-8. [ Links ]
140. Zhao J, Cao J, Li Y, Collins H, Roush R, Earle E, et al. Transgenic plants expressing two Bacillus thuringiensis toxins delay insect resistance evolution. Nat Biotechnol 2003; 21: 1493-7. [ Links ]
141. Zhu C, Ruan L, Peng D, Yu Z, Sun M. Vegetative insecticidal protein enhancing the toxicity of Bacillus thuringiensis subsp kurstaki against Spodoptera exigua. Lett Appl Microbiol 2006; 42: 109-14. [ Links ]
Recibido: 28/08/07
Aceptado: 14/03/08














