Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO  uBio
uBio
Compartilhar
Revista argentina de microbiología
versão impressa ISSN 0325-7541
Rev. argent. microbiol. vol.44 no.2 Ciudad Autónoma de Buenos Aires abr./jun. 2012
INFORME BREVE
Dos aislamientos de Salmonella Infantis multirresistentes se comportan como hipoinvasivos pero con elevada proliferación intracelular
José A. Di Conza1'2* , Marta E. Mollerach1, Gabriel O. Gutkind1, Juan A. Ayala3,1
1 Facultad de Farmacia y Bioquímica - Universidad de Buenos Aires, Junín 956(1113) Ciudad Autónoma de Buenos Aires;
2 Facultad de Bioquímica y Ciencias Biológicas - Universidad Nacional del Litoral, Paraje el Pozo (3000) Santa Fe, Argentina;
3Centro de Biología Molecular "Severo Ochoa". Consejo Superior de Investigaciones Científicas, (28049) Madrid, España.
*Correspondencia. E-mail: jdiconza@fbcb.unl.edu.ar
RESUMEN
En este trabajo se investigó la presencia de determinantes característicos de plásmidos de virulencia en dos aislamientos clínicos de Salmonella Infantis portadores de plásmidos de multirresistencia. Además, se estudió la capacidad de invasión y proliferación en células eucariotas no fagocíticas. Ninguno de los aislamientos de S. Infantis mostró los determinantes genéticos que caracterizan a los plásmidos de virulencia para este género (operón spv). Los ensayos de invasión sobre líneas celulares eucariotas mostraron que los aislamientos de S. Infantis presentan una capacidad de invasión disminuida pero persisten y proliferan en el citoplasma, independientemente de utilizar una línea celular permisiva (HeLa) o no permisiva (NRK) para tal fin. Finalmente, no se observaron indicios microscópicos que podrían hacer sospechar un efecto bactericida de estas líneas celulares sobre los aislamientos estudiados.
Palabras clave: Salmonella Infantis; Multirresistencia; Capacidad de invasión; Proliferación intracelular
ABSTRACT
Two multidrug-resistant Salmonella Infantis isolates behave like hypo-invasive strains but have high intracellular proliferation. In this work, plasmid-encoded virulence factors in two Salmonella Infantis isolates carrying multiresistance plasmids were investigated. In addition, their invasion and proliferative ability in non-phagocytic cells was studied. None of them showed the typical determinants of virulence plasmids (spv operon). The invasion assays of S. Infantis isolates on eukaryotic cells showed a decreased ability to Invade but they remained and proliferated In the cytoplasm regardless of having used a permissive (HeLa) or non-permissive (NRK) cell line. Finally, there was no microscopic evidence suggesting a bactericidal effect of these eukaryotic cell lines on the Isolates tested.
Key words: Salmonella Infantis; Multiresistance; Invasion ability; Intracellular proliferation
Las especies de Salmonella son patógenos intracelulares facultativos y generalmente colonizan mamíferos, aves y reptiles. En la mayoría de las infecciones producidas en humanos, se desarrolla una gastroenteritis autolimitada que cursa con multiplicación bacteriana dentro de la submucosa intestinal y diarrea (9,10). En algunos casos, la invasión del microorganismo puede causar septicemia; el patógeno puede persistir en sangre y provocar infecciones crónicas (10).
Algunos genes que codifican los factores de virulencia residen dentro de grandes plásmidos de virulencia. Estos plásmidos se han encontrado solo en unas pocas serovariedades de Salmonella entérica: Salmonella Enteritidis, Salmonella Typhimurium, Salmonella Dublin y Salmonella Choleraesuis (2).
Hasta el momento, no ha habido comunicación de estos plásmidos en Salmonella Infantis.
Se cree que la presencia de estos plásmidos es necesaria durante la fase sistèmica de la enfermedad causada por Salmonella spp. no tifoideas. Los plásmidos de virulencia contienen una región altamente conservada de 7,8 kb denominada spv (Salmonella plasmid virulence). El operón spv está formado por cinco genes designados spvRABCD. A su vez, se han caracterizado dos replicones independientes, repB y repC. Ambos son funcionales y pueden coexistir o estar presentes en forma independiente (14, 15).
El efecto de los plásmidos de virulencia en la proliferación de Salmonella en macrófagos es controvertido (11, 15). Existen evidencias de que los genes spv capacitan a la cepa para infectar bazo e hígado, por aumento en la replicación bacteriana dentro de la célula del hospedador. Cuando S. enterica infecta otros sitios diferentes del intestino y causa una enfermedad sistèmica, se requiere una terapia rápida y adecuada. El cuadro se complica aún más si la cepa aislada es resistente a múltiples drogas. Desde un principio se ha pensado que estos plásmidos de virulencia están poco relacionados con la resistencia a los antibióticos, pero en la actualidad existen informes sobre la presencia de grandes plásmidos híbridos de virulencia/resistencia (2, 3) en las serovariedades Typhimurium y Choleraesuis, y se postula que estos surgieron como resultado de eventos de recombinación entre diferentes plásmidos (12, 14). Poco se sabe sobre la presencia simultánea de determinantes de virulencia en plásmidos de resistencia en otras serovariedades.
El objetivo de este trabajo fue investigar la presencia de determinantes característicos de plásmidos de virulencia en dos aislamientos clínicos de Salmonella Infantis multirresistentes, y comparar el comportamiento de invasión y proliferación intracelular de dichos aislamientos en distintas líneas de células eucariotas.
Los dos aislamientos clínicos de Salmonella enterica serovar Infantis fueron recuperados de pacientes pediátricos internados en el Hospital de Niños "Ricardo Gutiérrez" de la ciudad de Santa Fe, en los años 1996 y 1997. Estos aislamientos (denominados S07 y S21) presentan, al menos, un plásmido conjugativo que codifica múltiples mecanismos de resistencia. El perfil de resistencia a los antibióticos y los determinantes genéticos asociados se resumen en la Tabla 1 (5, 6).
TABLA 1. Patrón de resistencia y determinantes genéticos asociados en los aislamientos clínicos de Salmonella

Para identificar plásmidos de virulencia, se investigó por PCR e hibridación sobre colonias la presencia del gen de virulencia plasmídico spvC (por ser el más conservado entre las distintas serovariedades dentro de la región spv) y de los replicones característicos repB y repC. Las condiciones de PCR, los cebadores empleados y el tamaño de los fragmentos esperados fueron los descritos por Chu et al. (4). Como control de amplificación e hibridación se utilizó la cepa S. Typhimurium OU5045, cepa de laboratorio C5, cedida gentilmente por el grupo de trabajo responsable de la publicación recién citada.
Además de los aislamientos clínicos de Salmonella S07 y S21, se incluyó también la cepa de S. Typhimurium SL1344, portadora del plásmido de virulencia; esta cepa fue utilizada como referente para los ensayos de invasión y proliferación bacteriana en células eucariotas (7, 13).
Los aislamientos de S. Infantis S07 y S21 no presentaron ninguno de los marcadores genéticos evaluados, lo cual indica que estas cepas no portarían un plásmido de virulencia característico. Estos resultados concuerdan con los publicados por otros autores (2,15), quienes destacan que estos plásmidos, al parecer específicos de serovariedad, se encuentran con mayor frecuencia en las serovariedades Typhimurium, Choleraesuis y Enteritidis, y hasta el presente, no se describió ningún caso en la serovariedad Infantis. La cepa de referencia S. Typhimurium SL1344 mostró la presencia del gen spvC y solo uno de los replicones, repB.
Si bien los aislamientos de S. Infantis estudiados no presentan el gen spvC, no puede descartarse la presencia de otros genes del operón spv o de marcadores de virulencia no conocidos en el plásmido de resistencia.
Posteriormente, se efectuaron estudios in vitro de invasión y proliferación intracelular con los aislamientos S21 y S07 en cultivos de células eucariotas no fagocíticas (línea epitelial HeLa, ATCC CCL2, y fibroblastos NRK, ATCC CRL1570). Los ensayos de infección bacteriana de células eucariotas se realizaron aplicando algunas modificaciones a la metodología utilizada por Martinez-Moya et al. (13). Brevemente, las monocapas de células eucariotas se obtuvieron en una placa de 24 pocilios, a una densidad entre 5 y 8 x 104 células/pocilio. Antes de proceder a la infección, estas células se lavaron con buffer fosfato salino (PBS) pH = 7,4 y se añadió medio fresco MEM o DMEM, más 10 % de suero fetal bovino (Gibco) (SFB). Luego se añadió un volumen conocido de bacterias (crecidas en medio LB durante 14 a 16 h, a 37 °C y sin agitación), a razón de 10 bacterias/células, aproximadamente, y se incubó a 37 °C en atmósfera de C02al 5 % durante 30 minutos. Las células infectadas se lavaron con PBS (3 veces) y se incubaron durante 2 h en MEM o DMEM con 10 % de SFB, el cual contenía 300 mg/ml de amicacina (Sigma Ch. Co., EE.UU.). Este antibiótico mata a las bacterias extracelulares sin afectar la viabilidad de las bacterias intracelulares, ya que no penetra la membrana citoplasmàtica eucariota. A las 2 h posinfección, las células se lavaron con PBS (3 veces) y se añadió MEM o DMEM con 10 % de SFB adicionado con 200 mg/ml de amicacina. Se incubó en las mismas condiciones hasta cumplir las 24 h de infección. Para determinar el número de bacterias viables intracelulares a las 2 y a las 24 h de infección, las células contenidas en 2 pocilios diferentes se lavaron 3 veces con PBS, se añadió Tritón X-1001 % (100 mi) y se incubó 5 minutos a 37 °C.Tras añadir 400 mi de PBS y agitar, se realizaron diluciones seriadas en PBS para su posterior recuento en placas de LB. Los resultados de estos ensayos fueron comparados con los obtenidos con cepas de referencia: S. Typhimurium SL1344, portadora de plásmido de virulencia, y la cepa isogénica curada de plásmido SV4277 (gentileza del Dr. David Cano, Sevilla, España). Además, se incluyó a la cepa SV21 obtenida mediante transformación de la cepa SV4277 con el plásmido de multirresistencia de S21 (5).
Se realizaron entre 3 y 5 ensayos de infección por cepa bacteriana. La capacidad de invasión (Cinv) se calculó dividiendo el número de bacterias intracelulares viables a las 2 h posinfección por el número de bacterias extracelulares añadidas para infectar, y el índice de proliferación (Ipro) se calculó dividiendo el número de bacterias viables intracelulares a largo tiempo (24 h) por el número de bacterias viables intracelulares obtenido a las 2 h. Los resultados se trataron estadísticamente efectuando el análisis de la varianza de un factor fijo (ANOVA) y realizando el test a posteriori (test de Dunnett) con el programa "GraphPad InStat tm" v2.02.
Sobre las células HeLa, la cepa virulenta SL1344 presentó una Cinv de 0,15 y el número de bacterias viables intracelulares (Ipro) aumentó 4,8 veces a las 24 h de infección. La cepa isogénica SV4277 mostró resultados similares. Sin embargo, los aislamientos clínicos S07 y S21 mostraron una Cinv al menos 5 veces menor, y el Ipro fue hasta 10 veces mayor que en las cepas controles (Tabla 2). Resultados similares se observaron con la cepa SV21. El análisis de la varianza reveló que existen diferencias significativas en la capacidad de invasión (p < 0,0001) y en el índice de proliferación (p = 0,0361) entre los distintos grupos bacterianos. Al realizar el test a posteriori, se observaron diferencias significativas en cada una de las cepas con plásmidos de multirresistencia frente a ambos controles, tanto en la capacidad de invasión (p < 0,01), como en la de proliferación intracelular (p < 0,05).
TABLA 2. Capacidad de Invasión e índice de proliferación obtenidos en las líneas HeLa y NRK
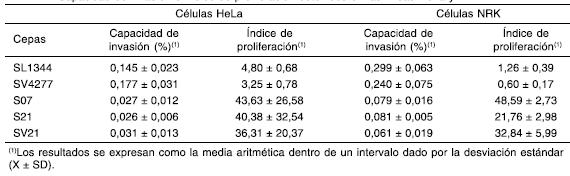
El notorio aumento en el Ipro de las cepas clínicas en células HeLa motivó el estudio de infección sobre la línea celular NRK, considerada como no permisiva para la proliferación intracelular de la cepa SL1344 (13). Los resultados del ensayo corroboraron la falta de proliferación de la cepa SL1344 en esta línea celular. La variante SV4277 presenta un Ipro < 1, lo que estaría indicando no solo la falta de proliferación, sino también la menor persistencia intracelular. Pese a esto, los aislamientos S07 y S21 mostraron una Cinv menor (igual que lo observado en células HeLa) y un Ipro entre 20-50 veces mayor que la cepa SL1344 (Tabla 2). El análisis de la varianza de un factor fijo para ambos parámetros mostró que existen diferencias altamente significativas (p < 0,0001) entre los distintos grupos bacterianos. Al realizar el test a posteriori, se observaron diferencias altamente significativas (p < 0,01) de los aislamientos clínicos frente a los controles en ambas determinaciones.
Carlson et al. (1) clasifican a las cepas como hipoinvasivas si existe una reducción de la invasión relativa de al menos un 50 % respecto de lo observado con las cepas controles. Si respetamos este criterio, se puede considerar a los aislamientos clínicos analizados como hipoinvasivos, independientemente de la línea celular empleada. Esta característica ya ha sido descrita en algunos aislamientos clínicos multirresistentes de S. Typhimurium DT104 (y otros fagotipos) estudiados sobre la línea celular Hep-2.
Los estudios de virulencia sobre modelos murinos mostraron que las cepas hipoinvasivas presentan una leve disminución en la capacidad de causar letalidad (1).
Por otro lado, en este trabajo se advirtió un aumento de la proliferación intracelular de los aislamientos de Salmonella Infantis, inclusive en la línea eucariota previamente descrita como no permisiva para tal fin. In vitro se ha observado que las células epiteliales, a diferencia de determinadas líneas de fibroblastos, han resultado ser más permisivas para el crecimiento intracelular bacteriano. Hay evidencias que sugieren que tanto factores del huésped como del patógeno contribuyen a un ajuste fino de la tasa de crecimiento intracelular (8); de qué modo estos factores se interrelacionan para este ajuste es un tema aún poco conocido.
Para profundizar sobre el comportamiento de los aislamientos internalizados en ambas líneas celulares, se analizó por microscopía de inmunofluorescencia confocal la integridad, la morfología y el número de bacterias intracelulares a las 24 h posinfección. Las bacterias se detectaron por fluorescencia mediante tinción del ADN con DAPI (que también tiñe el núcleo celular) y con anticuerpo de conejo anti-LPS específico (Difco Laboratories, EE.UU.), donde la reacción inmunológica se completa con un segundo anticuerpo de cabra anti-lgG de conejo, marcado con isotiocianato de fluoresceína (FITC) (Sigma). El ensayo fue realizado como se describió previamente (6, 13).
En el interior de las células HeLa, S. Typhimurium SL1344 prolifera activamente manteniendo su morfología bacilar normal, mientras que en las células NRK no se aprecia crecimiento bacteriano y la bacteria altera su morfología de bacilar a cocoide. Estas mismas observaciones fueron señaladas por otros autores como Martínez-Moya etal. (13), al ensayar esta cepa frente a las mismas líneas celulares. Además, dichos autores han advertido, mediante microscopía electrónica de transmisión, claros signos de degradación y lisis bacteriana dentro de las células no permisivas NRK y 3T3 (efecto bactericida de las líneas celulares).
Sin embargo, S. Infantis S21 se encuentra proliferando activamente tanto en el citoplasma de HeLa como de NRK (Figura 1). A su vez, las bacterias intracelulares mantienen su morfología bacilar en ambas líneas. La ausencia de estructuras filamentosas o redondeadas dentro del citoplasma celular sugiere una falta de actividad bactericida de la célula NRK sobre S21.
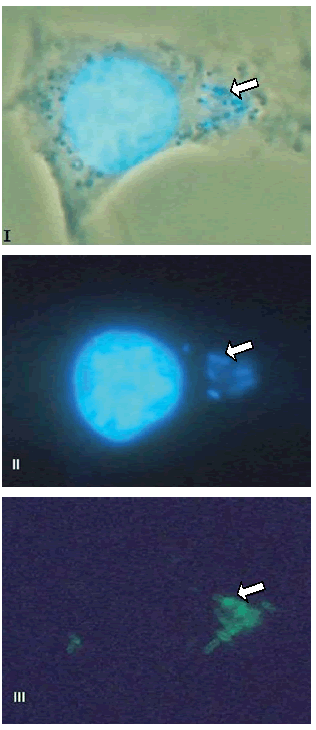
Figura 1. Microscopía de inmunofluorescencia. Las flechas marcan la morfología bacilar de S. Infantis S21 en células no permisivas NRK (aumento 600X) procesadas 24 h posinfección. Imagen obtenida con: (I) contraste de fase y tinción con DAPI (mareaje de ADN tanto de las células eucarlotas como de las bacterias); (II) tinción con DAPI; (III) inmunofluorescencia empleando un anticuerpo primario antl-LPS de Salmonella y un anticuerpo secundarlo antl-lgG de conejo marcado con FITC.
Un paso esencial en el proceso de patogenicidad de Salmonella spp. está sujeto a la capacidad del microorganismo para inducir su absorción por las células epiteliales en el intestino. Evaluando los valores de Cinv obtenidos, los aislamientos de S. Infantis parecen menos agresivos que las cepas controles. Sin embargo, sabiendo que se requiere de la proliferación intracelular para poder manifestar la máxima capacidad de virulencia, los resultados observados en los valores de Ipro marcan la tendencia opuesta.
En principio, estas características podrían estar ligadas a factores desconocidos presentes en el plásmido de multirresistencia de S21, ya que los resultados de invasión y proliferación se repitieron al realizar los ensayos de infección con la cepa transformante SV21.
En la actualidad, se considera la secuenciación total de este plásmido para evaluar la presencia de secuencias comunes o nuevos factores bacterianos que podrían influir en los eventos de invasión, proliferación o persistencia intracelular al infectar células eucariotas no fagocíticas.
Agradecimientos: este trabajo fue financiado con subsidios ANPCyT y UBA otorgados a GG; con proyecto BFU2009-9200 del MICINN, Gobierno de España, otorgado a JAA, y con fondos de la UNL otorgados a JDC. GG, MM y JDC son miembros de la carrera de investigador científico de CONICET.
1. Carlson SA, Browning M, Ferris KE, Jones BD. Identification of diminished tissue culture invasiveness among multiple antibiotic resistant Salmonella typhimurium DT104. Microb Pathog 2000; 28: 37-44. [ Links ]
2. Chu C, Chlu CH. Evolution of the virulence plasmids of non-typhoid Salmonella and Its association with antimicrobial resistance. Microbes Infect 2006; 8: 1931-6. [ Links ]
3. Chu C, Chiu CH, Wu WY, Chu CH, Liu TP, Ou JT. Large drug resistance virulence plasmids of clinical Isolates of Salmonella entérica serovar Choleraesuis. Antlmicrob Agents Chemother 2001; 45: 2299-303. [ Links ]
4. Chu C, Hong S, Tsai C, Lin W, liu T, Ou JT. Comparative physical and genetic maps of the virulence plasmids of Salmonella entérica serovars Typhimurium, Enteritidis, Choleraesuis, and Dublin. Infect Immun 1999; 67: 2611-4. [ Links ]
5. Di Conza J, Ayala J, Power P, Mollerach M, Gutklnd G. Novel class 1 integran (lnS21) carrying the bla^^ gene In Salmonella entérica serovar Infantis. Antlmicrob Agents Chemother 2002; 46: 2257-61. [ Links ]
6. Dl Conza JA. Caracterización de -lactamasas asociadas a ¡ntegrón de clase 1 y evaluación de factores de virulencia en plásmidos de salmonelas. Tesis Doctoral 2004. Universidad de Buenos Aires.
7. García del Portillo F, Jungnltz H, Rohde M, Guzmán CA. Interaction of Salmonella entérica serotype Typhimurium with dendritic cells Is defined by targeting to compartments lacking lysosomal membrane glycoproteins. Infect Immun 2000; 68: 2985-91. [ Links ]
8. Garcia del Portillo F. Salmonella Intracellular proliferation: where, when and how? Microbes Infect 2001; 3: 1305-11.
9. Grolsman EA, Blanc-Potard AB, Uchiya K. Pathogenicity islands and the evolution of Salmonella virulence. En: Hacker JBK, editor. Pathogenicity Islands and other mobile virulence elements. Washington D.C., ASM Press, 1999, p. 127-50.
10. Groisman EA, Ochman H. The Path to Salmonella. ASM News 2000; 66: 21-7. [ Links ]
11. Guiney DG, Fang FC, Krause M, Libby S. Plasmid-mediated virulence genes in non-typhoid Salmonella serovars. FEMS Microbiol Lett 1994; 124: 1-10. [ Links ]
12. Herrero A, Mendoza MC, Threlfall EJ, Rodiclo MR. Detection of Salmonella entérica serovar Typhimurium with pUO-StVR2-like virulence-resistance hybrid plasmlds in the United Kingdom. Eur J Clin Microbiol Infect Dis 2009; 28: 1087-93. [ Links ]
13. Martlnez-Moya M, de-Pedro MA, Schwarz H, Garcia del Portillo F. Inhibition of Salmonella intracellular proliferation by non-phagocytic eucariotic cells. Res Microbiol 1998; 149: 309-18. [ Links ]
14. Mendoza M del C, Herrero A, Rodiclo MR. Evolutionary engineering in Salmonella: emergence of hybrid virulence-resistance plasmids In non-typhoid serotypes. Enferm Infecc Microbiol Clin 2009; 27: 37-43. [ Links ]
15. Rotger R, Casadesüs J.The virulence plasmlds of Salmonella. Int Microbiol 1999; 2:177-84. [ Links ]
Recibido:8/11/2011 - Aceptado:12/2/2012














