Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO
Related links
-
 Similars in
SciELO
Similars in
SciELO  uBio
uBio
Share
Revista de la Sociedad Entomológica Argentina
Print version ISSN 0373-5680
Rev. Soc. Entomol. Argent. vol.70 no.3-4 Mendoza July/Dec. 2011
TRABAJOS CIENTÍFICOS
Efectos de la competencia larval en los mosquitos de contenedores artificiales, Aedes aegypti y Culex pipiens (Diptera: Culicidae) en condiciones semi-controladas
Effects of larval competition between the container mosquitoes, Aedes aegypti and Culex pipiens (Diptera: Culicidae) in semi-controlled conditions
Francia, Analía* y Arnaldo Maciá**
Centro de Estudios Parasitológicos y de Vectores, CEPAVE (CCT-La Plata- CONICET- UNLP), 2 Nº 584, 1900 La Plata, Argentina
* Dirección actual: Centro de Ecología Aplicada del Litoral, CECOAL (CONICET), Ruta 5 km 2,5, 3400 Corrientes, Argentina; e-mail: analiafrancia@yahoo.com.ar
** Dirección actual: División Entomología, Museo de La Plata, Paseo del Bosque s/n, 1900 La Plata, Argentina; e-mail: arnaldo_macia@yahoo.com.ar
Recibido: 9-V-2011
Aceptado: 12-X-2011
RESUMEN. Las larvas de los mosquitos Aedes aegypti (Linneo) y Culex pipiens Linneo pueden criar conjuntamente en pequeños contenedores artificiales de agua, se genera así una competencia interespecífica y/o intraespecífica. El objetivo de este trabajo fue comparar la magnitud relativa de la competencia intra e interespecífica en A. aegypti y C. pipiens, generada durante el desarrollo larval en contenedores artifi ciales. Las variables medidas como respuesta fueron la supervivencia y el tiempo de desarrollo larval, y la biomasa total producida en estado de pupa. Se criaron larvas de ambos mosquitos en neumáticos de automóvil con agua declorinada y hojarasca. Se introdujeron larvas recién eclosionadas de acuerdo a la densidad (5) estimada según un censo previo de A. aegypti y C. pipiens. Serealizaron los siguientes tratamientos agregando larvas de: (1) A. aegypti hasta alcanzar δ A. aegypti determinada según el censo previo, (2) C. pipiens hasta δ C. pipiens del censo previo, (3) A. aegypti hasta alcanzar la suma de δ A. aegypti y δ C. pipiens del censo previo, (4) C. pipiens hasta alcanzar la suma de δ A. aegypti y δ C. pipiens del censo previo y (5) A. aegypti y C. pipiens hasta δ A. aegypti y δ C. pipiens del censo previo. Las tres variables medidas fueron afectadas por los tratamientos, excepto la supervivencia y la biomasa producida por C. pipiens. Aedes aegypti fue más alterada por la competencia intraespecífica que por la competencia interespecífica. En C. pipiens, la competencia interespecífica superó en sus efectos a la competencia intraespecífica. Existió asimetría competitiva, ya que C. pipiens fue más afectada por A. aegypti que lo contrario.
PALABRAS CLAVE: Mosquitos; Competencia; Tiempo de desarrollo; Biomasa; Supervivencia.
ABSTRACT. Larvae of Aedes aegypti (Linneo) and Culex pipiens Linneo may develop together in small artificial water containers, promoting inter- and/or intra-specific competition. Our aim was to compare the relative importance of interspecific and intraspecific competition in both species during larval development in artificial containers. Larvae were bred outdoors in automobile tires with leaf litteras the nutrient source. The number of experimental larvae was set after an assessment of densities (5) from wild populations. We established the treatments: 1: A. aegypti alone at the 5 of A. aegypti in the census; 2: C. pipiens alone at the 5 of C. pipiens in the census; 3: A. aegypti alone at the 5 of A. aegypti + C. pipiens in the census; 4: C. pipiens alone at the 5 A. aegypti + 5 C. pipiens in the census; and 5: A. aegypti at the 5 of A. aegypti in the census + C. pipiens at the 5 of C. pipiens in the census. Survivorship, development time and total biomass were affected by treatments, except for survivorship and biomass of C. pipiens. Intraspecific competition outweighed interspecific competiton in A. aegypti, while the opposite trend was detected in C. pipiens. Competition was asymmetric, as C. pipiens was more affected by A. aegypti.
KEY WORDS. Mosquitoes; Competition; Development time; Biomass; Survivorship.
INTRODUCCIÓN
Los géneros Aedes Meigen y Culex Linneo de la familia Culicidae incluyen los insectos que poseen la máxima importancia médica junto con las especies de Anopheles Meigen, ya que son vectores de enfermedades humanas que provocan millones de muertes anualmente. Los tres géneros están presentes en la Argentina y están implicados en la transmisión de enfermedades infecciosas como algunas arbovirosis, filariasis y malaria.
El mosquito Aedes aegypti (Linneo) es el único vector de la fiebre amarilla urbana y del dengue en Argentina, siendo esta una enfermedad que se manifestó en forma de epidemia en 2008 y 2009, cuando se registraron casi 26.000 casos confirmados en el país (Ministerio de Salud de la Nación, 2009). El dengue es la arbovirosis más importante del mundo, ya que se estima que cada año unos 50 millones de personas se infectan en todo el planeta. Con respecto a la fiebre amarilla, si bien es una enfermedad que se puede controlar a través de la vacunación, se ha observado una reemergencia de la misma, ya que se han registrado tres casos fatales en 2008 en nuestro país (OPS, 2009).
Culex pipiens Linneo constituye un complejo de especies (Vinogradova, 2000) y es el mosquito doméstico común. Es transmisor primario de la filariasis linfática, que afecta alrededor de 120 millones de personas en el mundo (Michael et al., 1996). En Argentina, se han detectado recientemente casos de encefalitis por los virus Encefalitis de San Luis y del Nilo del Oeste, en cuya transmisión está implicado ese mosquito (Ministerio de Salud de la Nación, 2011).
Los mosquitos de ambas especies son antropofílicos y frecuentes en cementerios y viviendas humanas, y los estados preimaginales suelen encontrarse en recipientes artificiales que contienen agua. En nuestro país, varios estudios señalaron la coexistencia de larvas de ambos mosquitos en ambientes urbanos (Vezzani et al., 2001; García et al., 2002; Stein & Oria, 2002; Rossi & Almirón, 2004; Micieli et al., 2006).
La comparación de las fuerzas relativas de la competencia intra e interespecífica permite entender los procesos implicados en la organización de las comunidades. En teoría, el aumento en la competencia intraespecífica expandiría el nicho de una especie, mientras que el aumento de la competencia interespecífica lo reduciría (Connell, 1983). Algunos organismos pueden cohabitar en hábitats pequeños y restringidos (en los cuales se agudizaría la competencia), cuando existen adaptaciones que separan sus nichos e impiden la extinción del competidor. Los mosquitos A. aegypti y C. pipiens brindan una oportunidad para estudiar estos procesos porque frecuentemente comparten los ambientes de cría en el estado larval. Se han realizado numerosos estudios sobre la competencia entre los mosquitos que crían en contenedores, pero son escasos los que consideran en particular, la interacción entre Culex y Aedes, ya sea en el laboratorio (Ríos et al., 1978) o en condiciones de campo (Carrieri et al., 2003; Costanzo et al., 2005). Si bien el impacto de la competencia sobre la biología de especies de Culex y Aedes ha sido estudiado, no lo ha sido en el caso particular de las interacciones entre C. pipiens y A. aegypti, a pesar de su presencia en todos los continentes y su importancia médico-veterinaria. Probablemente, esto es debido a que los procesos de competencia generados entre Aedes albopictus (Skuse) y A. aegypti han congregado más la atención de los investigadores, sobre la base de la relativamente reciente bioinvasión en Estados Unidos de la primera especie, y porque se ha observado un desplazamiento de A. aegypti por A. albopictus en ciertos escenarios (Hobbs et al. 1991, O' Meara et al., 1995).
La importancia de analizar la competencia entre dos especies vectoras radica en que la dinámica de una de ellas puede alterarse como consecuencia de la reducción competitiva i. e. cualquier disminución en las poblaciones como consecuencia de la competencia intraespecífica, cuando esa disminución es menor que la extinción local (Lounibos, 2007). Por otro lado, puede ocurrir que al añadir una fuente de mortalidad (por ejemplo, un agente de control) se reduzca la mortalidad denso-dependiente (como en el caso de la que está asociada a la competencia). Si la población está sometida a la sobrecompensación, entonces el efecto final podría ser la menor mortalidad total y el mayor tamaño poblacional luego de los esfuerzos de control (Service, 1985; Juliano, 2007). Tal fenómeno fue corroborado experimentalmente en el laboratorio por Agudelo-Silva y Spielman (1984). Dichos autores simularon el uso de larvicidas contra A. aegypti en contenedores con cantidades subóptimas de alimento y verificaron que la cantidad de adultos producida era mayor que en los controles, sin mortalidad añadida. En síntesis, como consecuencia de la implementación de medidas de control vectorial, la eliminación de uno de los competidores podría liberar la otra especie de las presiones de competencia a que está normalmente sometida. De esta manera, el efecto podría ser la expansión más veloz de uno de los dos vectores, al aumentar su potencial reproductivo o un incremento en su capacidad vectorial.
En mosquitos, los rasgos de historia de vida que pueden alterarse como consecuencia de la acción de la competencia a nivel del estado de larva, son el peso corporal en estado de pupa, la supervivencia, el tamaño de los adultos, la fecundidad y la longevidad de las hembras (Steinswascher, 1982; Reisen et al., 1984; Fisher et al. 1990). En general, una especie se ve perjudicada cuando debe competir con otra por los recursos, aunque también es posible que ambas especies resulten beneficiadas luego de compartir el hábitat larval (Bradshaw & Creelman, 1984).
El objetivo de este trabajo fue comparar la magnitud relativa de las competencias intraespecífica e interespecífica en A. aegypti y C. pipiens, generada durante el desarrollo larval en contenedores artificiales sometidos a condiciones semi-controladas. La hipótesis que se pone a prueba es que la interacción entre A. aegypti y C. pipiens produce resultados similares a lo que observaron Carrieri et al. (2003) y Costanzo et al. (2005) entre C. pipiens y A. albopictus, en condiciones de laboratorio. Dichos autores demostraron que ambos mosquitos, cuando sus larvas se desarrollan conjuntamente en el ambiente acuático, compiten en forma asimétrica, ya que A. albopictus es superior a C. pipiens.
En la aproximación experimental de este trabajo, se utilizaron neumáticos como ambiente de cría larval porque son rutinariamente utilizados como larvitrampas en todo el mundo (OPS, 1995). Esto permitiría la comparación con los resultados de estudios similares, y además, porque son microhábitats naturalmente explotados por mosquitos urbanos que crían en contenedores, los cuales pueden actuar como dispersores pasivos de huevos de especies invasivas de Aedes, al ser transportados inadvertidamente por el hombre.
MATERIAL Y MÉTODOS
Censo preliminar. El objetivo de esta fase fue estimar la abundancia de las larvas de A. aegypti y C. pipiens que se desarrollan en neumáticos en condiciones naturales, en la zona templada de la Argentina hacia fines del verano y comienzos del otoño, período en que la abundancia de los mosquitos alcanza niveles altos (Schweigmann et al, 2002; Vezzani et al., 2004). Se realizaron muestreos en neumáticos colocados ad hoc en el predio del Jardín Zoológico Municipal entre octubre de 2007 y marzo de 2008. Simultáneamente, se tomaron muestras de larvas en gomerías de La Plata (34 55'17"S, 57 57'16"O) y se compararon con las del Zoológico para corroborar que las muestras de este último sitio eran representativas de la dinámica de A. aegypti y C. pipiens de la zona. Un total de 36 neumáticos del Zoológico estuvieron expuestos a la intemperie durante un mínimo de seis meses y fueron colonizados naturalmente por ambas especies. En marzo de 2008, se seleccionaron 12 neumáticos en los cuales se había detectado la presencia de larvas de A. aegypti y de C. pipiens. Se midió el volumen de agua y el contenido fue trasladado al laboratorio, donde se contaron las larvas de 1º a 4º estadio y de pupas. El muestreo se realizó sin reposición de los individuos. Se calculó la densidad media (δ) para cada especie, expresada como δ= Σ número de larvas/ Σ volumen (litros) de agua retenida en los neumáticos. No se analizaron las diferencias en la composición por estadios larvales entre ambas especies, a fines de simplificar el diseño experimental.
De los otros 14 neumáticos provenientes exclusivamente del Zoológico, se extrajo el contenido sólido y líquido, y se filtró con una malla de apertura 1 mm. Los fragmentos > 1 cm fueron cortados en trozos más pequeños. Todos los detritos fueron mezclados y secados en una estufa a 60º C por 72 h. De esta manera, se obtuvieron 254 g (peso seco) de materia orgánica, consistentes en una mezcla de restos vegetales como hojarasca, semillas y fragmentos de corteza, y restos de origen animal (adultos y larvas de insectos). La hojarasca correspondió mayormente a hojas de "tilo", Tilia x moltkei Späth ex C. K. Schneid. (Malvales: Tiliaceae). Los detritos se dividieron en 15 partes de 16 g cada una y se conservaron en bolsas plásticas numeradas. Dichos detritos fueron destinados a servir como fuente de nutrientes para las larvas en el transcurso del experimento. Esta metodología permitió una aproximación realista de las condiciones que enfrentan las larvas en condiciones naturales. Si bien se sacrifica parte de la repetibilidad en el método, los experimentos que usan hojarasca como fuente de nutrientes para larvas de mosquitos de contenedores tienen menos sesgo que cuando se usa alimento artificial (Reiskind et al., 2009).
Colecta y cría de los mosquitos. Las larvas de C. pipiens se obtuvieron de balsas de huevos colectadas en zanjas, en la periferia de La Plata. Las balsas se trasladaron al laboratorio en cajas de plástico revestidas interiormente con algodón embebido en agua. En el laboratorio, las balsas se mantuvieron en agua declorinada a temperatura ambiente hasta la eclosión.
Las larvas de A. aegypti provinieron de una colonia mantenida en el insectario del CEPAVE por menos de 10 generaciones. La colonia fue originada a partir de larvas colectadas en los alrededores de La Plata. Los adultos fueron mantenidos en una jaula, con acceso ad libitum a pasas de uva como fuente de carbohidratos, bajo un fotoperíodo de 16:8 luz: oscuridad y a 26º C. Las hembras fueron alimentadas con sangre de gallina y para la postura de huevos se colocó en la jaula un recipiente negro parcialmente lleno de agua declorinada y revestido interiormente con papel. El papel en donde fueron puestos los huevos se mantuvo mojado, hasta completar el período embrionario (dos días) y luego se almacenó en bolsas plásticas con alta humedad. El día anterior al inicio del experimento se forzó la eclosión de los huevos, sumergiendo el papel en agua.
Las larvas de A. aegypti y C. pipiens tenían menos de 24 horas desde el nacimiento al inicio del experimento y fueron enjuagadas antes de organizar las cohortes.
Diseño experimental. En esta etapa, se manipularon cohortes experimentales de larvas para lograr la cría aislada o conjunta de las especies. Quince mitades de neumáticos cortados diametralmente (= réplicas) se colocaron a la intemperie en el CEPAVE y se agregó a cada una de ellas tres litros de agua declorinada y el contenido de una bolsa de detrito (16 g), asignado con una tabla de números al azar. Para reconstituir la microflora y microfauna adherida a superficies y en suspensión en cada réplica, se añadieron 100 ml de agua proveniente de otros neumáticos del Zoológico en los que se encontraron larvas de mosquito (cinco litros provenientes de cuatro neumáticos, mezclados y filtrados a través de una tela con trama de 0,3 mm de apertura). Las réplicas permanecieron en estas condiciones por siete días para la estabilización del hábitat y el crecimiento de los microorganismos. Para impedir nuevas oviposiciones durante el período que duró el experimento, cada neumático fue cubierto con una malla (1 mm de apertura) fijada con bandas elásticas, a fin de evitar el acceso de hembras grávidas.
El volumen de agua de cada réplica fue mantenido en forma constante, añadiendo agua destilada cuando se advirtió alguna disminución del volumen.
Tres neumáticos fueron asignados al azar (utilizando una tabla de números al azar) a cada uno de los siguientes tratamientos:
Tratamiento 1: larvas de ler estadio (LI) de A. aegypti hasta alcanzar δ A. aegypti determinada según el censo preliminar. n= 213 LI.
Tratamiento 2: LI de C. pipiens hasta alcanzar δ C. pipiens determinada según el censo preliminar. n= 330 LI.
Tratamiento 3: LI de A. aegypti hasta alcanzar la suma de δ A. aegypti y δ C. pipiens determinadas según el censo preliminar. n= 543 LI.
Tratamiento 4: LI de C. pipiens hasta alcanzar la suma de δ A. aegypti y δ C. pipiens determinadas según el censo preliminar. n= 543 LI.
Tratamiento 5 (control): LI de A. aegypti y de C. pipiens hasta alcanzar δ A. aegypti y δ C. pipiens determinadas según el censo preliminar. n= 213 LI de A. aegypti y 330 LI de C. pipiens.
Los tratamientos 1 y 2 excluyeron los efectos negativos generados por la competencia interespecífica en A. aegypti y C. pipiens, respectivamente; los tratamientos 3 y 4 se utilizaron para medir la acción forzada de la competencia intraespecífica en cada especie; y el tratamiento 5 se utilizó para medir la acción de la competencia interespecífica según ocurre en condiciones naturales.
Durante el transcurso del experimento una réplica del tratamiento 5 fue eliminada debido a un error en la manipulación. Cada dos días se extrajeron las pupas de cada réplica, se registraron su especie y sexo y se pesaron in vivo con una precisión de 0,1 mg con una balanza electrónica.
El día de inicio del experimento (agregado de LI a todas las réplicas) fue el 19/3/2008 y la extracción de la última pupa se realizó el 7/5/2008. Entre esos días, el fotoperíodo varió entre 13:11 y 11,5:12,5 h (luz:oscuridad) (Servicio de Hidrografía Naval, comunicación personal). Las temperaturas oscilaron entre un valor mínimo de 4,6 ºC y uno máximo de 29,2 ºC, con una temperatura media de 17,5 ºC (DE= 3,79) (Departamento de Sismología e Información Meteorológica, Facultad de Ciencias Astronómicas y Geofísicas, UNLP, comunicación personal).
Análisis estadístico. Las variables respuesta del experimento fueron la supervivencia larval, medida como el porcentaje de individuos de la cohorte original (=añadidos a las réplicas en LI) que alcanzó el estado de pupa; el tiempo de desarrollo larval, medido como el número de días transcurridos desde el inicio del experimento hasta la pupación; y la biomasa, calculada como la suma de los pesos individuales de las pupas en cada tratamiento. Los datos de la biomasa pupal se transformaron a log (peso+1) mientras que los datos de supervivencia larval fueron transformados a arco seno. La homogeneidad de varianzas fue analizada con la prueba de Bartlett. La supervivencia larval y el tiempo de desarrollo fueron analizados con ANOVA, con los Tratamientos, Sexo y su interacción como factores de variación, y la variación entre las réplicas como error experimental. La biomasa acumulada de pupas (sexos mezclados) se analizó con ANOVA con los Tratamientos como factor principal. Se realizaron ANOVA independientemente para cada especie. La comparación de medias a posteriori (entre tratamientos) se realizó con la prueba de Tukey (HSD), con α =0,05.
RESULTADOS
Tiempo de desarrollo larval. Los tiempos de desarrollo mínimos y máximos fueron de 9 y 42, y 9 y 49 días en machos y hembras de A. aegypti respectivamente, y 12 y 47, y 15 y 47 días en machos y hembras de C. pipiens, respectivamente. En ambas especies, los machos se desarrollaron más rápido que las hembras (Fig. 1). Tanto en A. aegypti como en C. pipiens el efecto del Tratamiento fue significativo (A. aegypti: F= 4,955, g.l.= 2, 12, p= 0,027; C. pipiens: F= 5,727, g.l.= 2, 6, p= 0,040), no así el efecto del Sexo ni la interacción Tratamiento x Sexo.
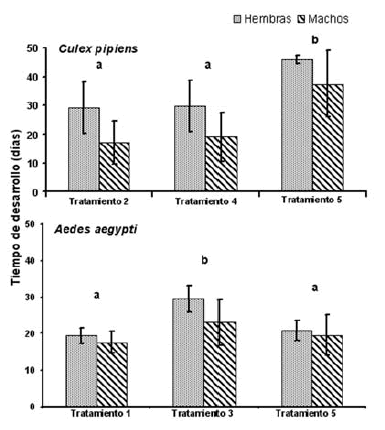
Fig. 1. Promedios 2 desvíos estándar del tiempo de desarrollo larval (días) de machos y hembras de Aedes aegypti y Culex pipiens en los Tratamientos 1 a 5, que consistieron en el agregado de los siguientes números de larvas I (LI): T1: 213 LI de A. aegypti; T2: 330 LI de C. pipiens; T3: 543 LI de A. aegypti; T4: 543 LI de C. pipiens; y T5: 213 LI de A. aegypti y 330 LI de C. pipiens. Las letras diferentes denotan diferencias significativas entre tratamientos (Prueba HSD: p<0,05).
Las larvas de C. pipiens tardaron significativamente más tiempo en empupar cuando compartían el hábitat con A. aegypti (Tratamiento 5) que cuando criaban solas (Tratamientos 2 y 4). El tiempo de desarrollo larval de C. pipiens en los Tratamientos 2 y 4 fue el mismo, es decir fue independiente de la densidad inicial.
Las larvas de A. aegypti tardaron más en desarrollarse en el Tratamiento 3, en el que lo hicieron sin la presencia de C. pipiens y en densidad alta. La respuesta del tiempo de desarrollo larval de A. aegypti fue la misma en los Tratamientos 1 y 5, por lo que no fue afectado por la presencia de C. pipiens en el hábitat (Fig. 1).
Supervivencia larval. Un total de 440 individuos de A. aegypti y 93 de C. pipiens alcanzaron el estado de pupa, esto representó el 16 y el 3% de las cohortes.
En C. pipiens, el efecto del Tratamiento no fue significativo (p=0,056), ni tampoco los efectos del Sexo y de la interacción Tratamiento x Sexo (p>0,05). Hubo mayor número de supervivientes en el Tratamiento 2 que en los Tratamientos 4 y 5, los cuales generaron una respuesta similar.
En A. aegypti, el efecto del Tratamiento fue significativo (F= 4,727, g.l.= 2, 12, p= 0,031), mientras que los efectos del Sexo y de la interacción Tratamiento x Sexo no fueron significativos. El menor número de sobrevivientes de esta especie se produjo sin la presencia de la especie competidora y cuando el desarrollo se produjo en densidad alta (Tratamiento 3), y el máximo, en competencia con C. pipiens y ante densidad baja de coespecíficos (Tratamiento 5); mientras que el Tratamiento 1 provocó una respuesta intermedia (Fig. 2). Por lo tanto, la mayor mortalidad en A. aegypti se produjo ante la alta densidad de larvas de su propia especie.

Fig. 2. Promedios + desvío estándar del porcentaje de supervivencia larval de machos y hembras de Aedes aegypti y Culex pipiens en los Tratamientos 1 a 5. Para A. aegypti, las letras diferentes denotan diferencias significativas entre tratamientos (Prueba HSD: p<0,05); en C. pipiens el efecto de los tratamientos no fue significativo (p>0,05). Referencias de los Tratamientos como en la Fig. 1.
Biomasa pupal. No se detectaron diferencias estadísticamente significativas entre Tratamientos para C. pipiens. La máxima acumulación de biomasa de C. pipiens se produjo cuando las larvas se desarrollaron en baja densidad y sin la especie competidora (Tratamiento 1), la mínima en situación de competencia con A. aegypti (Tratamiento 5) e intermedia cuando las larvas se desarrollaron en alta densidad y sin la especie competidora (Tratamiento 4) (Fig. 3).
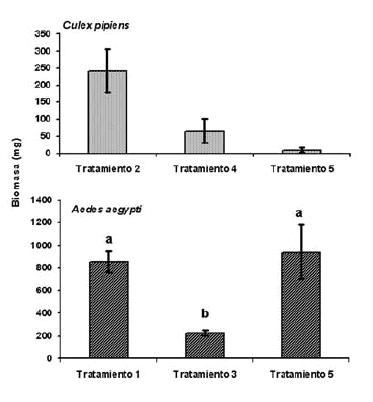
Fig. 3. Promedios +2 desvíos estándar de la biomasa (mg) de las pupas de Aedes aegypti y Culex pipiens en los Tratamientos 1 a 5. Para A aegypti, las letras diferentes denotan diferencias significativas entre tratamientos (Prueba HSD: p<0,05); en C. pipiens el efecto de los tratamientos no fue significativo (p>0,05). Referencias de los Tratamientos como en la Fig. 1.
En cambio, la biomasa de A. aegypti fue significantemente diferente entre los Tratamientos (F= 28,93, g.l.= 2, 6, p< 0,001). En el Tratamiento 3, se produjo la menor acumulación de biomasa como consecuencia de la alta densidad de individuos coespecíficos, mientras que no se observaron diferencias significativas entre los Tratamientos 1 y 5 (Fig. 3).
DISCUSIÓN
Este experimento demostró que cuando dos de las especies más comunes de mosquitos de ambientes urbanos, A aegypti y C. pipiens, comparten el mismo micro-hábitat durante el estado de larva, se modifican algunos rasgos de historia de vida como resultado de la competencia entre los individuos. Otros estudios señalaron que el número de días transcurridos en la etapa de larva es mayor en situación de competencia, ya sea en el seno de la especie (Reisen et al. 1984; Broadie & Bradshaw, 1991) o con otra especie (Chambers, 1985; Smith et al., 1995), lo que redunda en un efecto negativo para la población, porque los individuos estarían expuestos a depredadores o patógenos por más tiempo. El aumento en la mortalidad asociado a la competencia intraespecífica también fue comprobado en mosquitos de inundación como Ochlerotatus cantans (Meigen) (Renshaw et al., 1993) y Ochlerotatus albifasciatus Macquart (Gleiser et al., 2000), mosquitos de huecos de árbol como Ochlerotatus sierrensis (Ludlow) (Hawley, 1985) y Ochlerotatus triseriatus (Say) (Fisher et al., 1990), y en A. aegypti (Bèdhomme et al., 2003, 2005). También se observó una disminución en la supervivencia ante la competencia interespecífica (Barrera, 1996; Braks et al., 2004; Juliano et al., 2004; Costanzo et al., 2005). La biomasa total en la metamorfosis es afectada ya que el peso individual de las pupas también disminuye como respuesta a la competencia intraespecífica (Maciá, 2009) y el tamaño corporal de los adultos, como respuesta a la competencia interespecífica (Carrieri et al., 2003). Como el peso de las pupas es un estimador de la fecundidad de las hembras (Armbruster & Hutchinson, 2002), se puede considerar que una mayor biomasa producida se traduce en un aumento de la fecundidad.
Aedes aegypti fue más afectada por la competencia intraespecífica que por la interespecífica. La supervivencia de las larvas fue menor, su tiempo de desarrollo fue más prolongado y la biomasa pupal producida fue menor cuando la cantidad de larvas de la propia especie se aumentó experimentalmente 2,5 veces, manteniendo constantes el volumen de agua y la cantidad de alimento en los neumáticos (Tratamiento 1 vs. 3). Por otro lado, la presencia de C. pipiens no se asoció a un aumento de la mortalidad, no prolongó el tiempo de desarrollo ni disminuyó la biomasa de A. aegypti, a pesar de que la cantidad total de individuos en el hábitat también fue 2,5 veces mayor (Tratamiento 1 vs. 5).
En C. pipiens, la competencia interespecífica superó en sus efectos a la intraespecífica. El tiempo de desarrollo larval no fue alterado sustancialmente ante un aumento de individuos coespecíficos en una magnitud de 1,6 veces, pero aumentó drásticamente cuando en el hábitat existió una densidad de larvas 1,5 veces mayor, pero de individuos de A. aegypti. Una situación similar se observó en las respuestas de la supervivencia larval y la biomasa pupal, que fueron reducidas drásticamente (Tratamiento 2 vs. 5); aunque dicha reducción no pudo corroborarse estadísticamente (Figs. 2 y 3).
En general, se comprobó la existencia de asimetría competitiva, producto de la cual C. pipiens fue más afectada por A. aegypti que lo contrario. Dicha asimetría sería la manifestación de una desigualdad en el reparto de recursos en el hábitat entre ambas especies, o bien a que A. aegypti es más eficiente en el aprovechamiento de esos recursos que C. pipiens, al menos cuando crían en neumáticos. Existen diferencias evolutivas en cuanto a los mecanismos de explotación de los recursos por parte de ambas especies y que actuarían a nivel genérico. Las hembras de C. pipiens, como las de la mayoría de las especies de ese género, depositan los huevos en la superficie del agua en forma de balsas, cada una de ellas representa la totalidad de huevos desarrollada en un ciclo gonadotrófico; en cambio, A. aegypti utiliza más de un receptáculo de agua para repartir los huevos de un mismo ciclo (OPS, 1995). Como consecuencia, en algunos criaderos larvales, la presencia de una gran cantidad de larvas coespecíficas sería una situación común para C. pipiens. Por lo tanto, sería más frecuente enfrentar una situación de competencia intraespecífica entre larvas de C. pipiens que de A. aegypti, particularmente en pequeños recipientes. Como resultado, a lo largo de su historia evolutiva, C. pipiens podría haber desarrollado algunos mecanismos para contrarrestar los efectos negativos de la competencia intraespecífica. La expansión de la distribución geográfica de A. aegypti desde África tropical al resto de los continentes es relativamente reciente (Lounibos, 2002). Ello habría redundado en menores oportunidades para el desarrollo de mecanismos que eviten la competencia interespecífica con A. aegypti por parte de C. pipiens, además, ésta usa también criaderos naturales y de tamaño variable no usados por A. aegypti.
La alta mortalidad observada en general en este experimento podría relacionarse con la calidad del hábitat. Maciá (2006) señaló que el desempeño de A. aegypti es superior en larvitrampas que en ovitrampas, si aquel se mide en términos de peso en la metamorfosis, pero inferior si la respuesta medida es la mortalidad. La comparación de rasgos de historia de vida de C. pipiens en diferente tipo de habitat no se ha estudiado. Por otro lado, la alta mortalidad podría explicar al menos parcialmente la falta de validación estadística de los efectos de los tratamientos sobre la supervivencia larval y la biomasa pupal de C. pipiens.
La competencia interespecífica puede resultar en la coexistencia de las especies implicadas o en el desplazamiento e incluso la extinción de una de ellas. La posibilidad de desplazamiento o extinción no se produciría en el par A. aegypti/C. pipiens porque ambas especies pueden mantenerse en hábitas alternativos. Sin embargo, existirían consecuencias para la dinámica de poblaciones en aquellas localidades en que se lleven a cabo maniobras de control por parte del hombre. Por ejemplo, el control en cuerpos de agua utilizados por C. pipiens en los que no se encuentra A. aegypti (como lagunas, estanques, charcos permanentes y zanjas y canales con agua estancada) o ésta está presente en bajas densidades (como piscinas en desuso) (Maciá, observaciones personales), o podría desplazar al menos parte de las poblaciones hacia ambientes más favorables para A. aegypti como floreros, neumáticos u otros pequeños contenedores; en esa situación, la competencia afectaría poco a A. aegypti. Por otro lado, la eliminación de hábitats típicos de A. aegypti tampoco incidiría en gran medida sobre la abundancia de C. pipiens, ya que la competencia intraespecífica en esta especie no resultó tener consecuencias severas en el tipo de hábitat estudiado.
Carrieri et al. (2003) y Costanzo et al. (2005) analizaron la competencia entre A. albopictus y C. pipiens en recipientes de bajo volumen (>1 l), en un entorno de temperatura y fotoperíodo controlados en el interior de las cámaras de cría. Carrieri et al. (2003) demostraron que bajo una temperatura óptima y constante (25ºC) A. albopictus es un competidor superior a C. pipiens, y que el impacto de la asimetría competitiva fue más evidente sobre la supervivencia larval, además C. pipiens fue drásticamente afectada tanto por la competencia intra como interespecífica. Por otro lado, Costanzo et al. (2005) mostraron que A. albopictus se desempeña mejor que C. pipiens ante una situación de escasez de alimentos durante la etapa de larva. Ambos estudios, si bien difieren de este trabajo que fue realizado en un régimen de temperatura natural, en recipientes de mayor volumen y con A. aegypti como competidor de C. pipiens, demostraron las mismas tendencias generales en cuanto a las consecuencias de la competencia (asimetría en detrimento de C. pipiens), y por lo tanto, son de gran valor predictivo.
En conclusión, aunque existe competencia intensa entre A. aegypti y C. pipiens durante el desarrollo larval, no habría desplazamiento o extinción de ésta por parte de A. aegypti, la cual es competitivamente superior. Ambas especies tendrían refugios temporales o espaciales que impiden la superposición de sus nichos. El presente estudio debería compararse con futuras investigaciones en que se consideren otros factores de variación, por ejemplo, la contribución diferencial de los distintos estadios larvales a los resultados de la competencia, la estacionalidad de la competencia, el tipo de ambiente acuático en el que se produce, y la calidad del recurso alimenticio disponible para las larvas, ya que las hojas son una fuente de nutrientes que favorece al desempeño de C. pipiens sólo a corto plazo (días) (Maciá, 2011). Asimismo, el monitoreo de los efectos de las prácticas de control orientado a una de las especies del par podría evidenciar si la disminución local de una especie produce algún impacto sobre su interacción con la otra.
AGRADECIMIENTOS
A las autoridades y personal del Jardín Zoológico de La Plata, por permitir y facilitar parte de las tareas de campo. A Olga Deriu del Depto. Observatorio del Servicio de Hidrografía Naval, por proveer los datos de fotoperíodos. A Néstor Rossi del Departamento de Sismología e Información Meteorológica, Facultad de Ciencias Astronómicas y Geofísicas, UNLP, por proveer los datos de temperaturas. A Ana M. Marino de Remes Lenicov y Raúl E. Campos, por la lectura crítica del manuscrito. AF se desempeñó como pasante de la Facultad de Ciencias Naturales y Museo, UNLP, durante el desarrollo de este estudio. AM es Profesional de Apoyo de la Comisión de Investigaciones Científicas de la provincia de Buenos Aires (CIC).
BIBLIOGRAFÍA CITADA
1. AGUDELO-SILVA, F. & A. SPIELMAN. 1984. Paradoxical effects of simulated larviciding on production of adult mosquitoes. Am. J. Trop. Med. Hyg. 33: 1267-1269. [ Links ]
2. ARMBRUSTER, P. & R. A. HUTCHINSON. 2002. Pupal mass and wing length as indicators of fecundity in Aedes albopictus and Aedes geniculatus (Diptera: Culicidae). J. Med. Entomol. 39: 699-704. [ Links ]
3. BARRERA, R. 1996. Competition and resistance to starvation in larvae of container-inhabiting Aedes mosquitoes. Ecol. Entomol. 21: 117-127. [ Links ]
4. BEDHOMME, S., P. AGNEW, C. SIDOBLE & Y. MICHALAKIS. 2003. Sex-specific reaction norms to intraspecific larval competition in the mosquito Aedes aegypti. J. Evol. Biol. 16: 721-730. [ Links ]
5. BEDHOMME, S., P. AGNEW, C. SIDOBLE & Y. MICHALAKIS. 2005. Pollution by conspecifics as a component of intraspecific competition among Aedes aegypti larvae. Ecol. Entomol. 30: 1-7. [ Links ]
6. BRADSHAW, W. E. & R. E. CREELMAN. 1984. Mutualism between the carnivorous purple pitcher plant and its inhabitants. Am. Midland Nat. 112 (2): 294-304. [ Links ]
7. BRAKS, M. A., N. A. HONÓRIO, L. P. LOUNIBOS, R. L. OLIVEIRA & S. A. JULIANO. 2004. Interspecific competition between two invasive species of container mosquitoes in Brazil. Ann. Entomol. Soc. Am. 97: 130-139. [ Links ]
8. BROADIE, K. S. & W. E. BRADSHAW. 1991. Mechanisms of interference competition in the western tree-hole mosquito, Aedes sierrensis. Ecol. Entomol. 16: 145-154. [ Links ]
9. CARRIERI M., M. BACCHI, R. BELLINI & S. MAINI. 2003. On the competition occurring between Aedes albopictus and Culex pipiens (Diptera: Culicidae) in Italy. Environ. Entomol. 32: 1313-1321. [ Links ]
10. CHAMBERS, R. C. 1985. Competition and predation among larvae of three species of treehole-breeding mosquitoes. En: Lounibos, L. P., J. R. Rey & J. H. Frank (eds.), Ecology of mosquitoes: proceedings of a workshop. Florida Medical Entomology Laboratory, Vero Beach, pp. 25-53. [ Links ]
11. CONNELL, J. H. 1983. On the prevalence and relative importance of interspecific competition: evidence from field experiments. Am. Natur. 122 (5): 661-696. [ Links ]
12. COSTANZO, K. M., K. MORMANN & S. A. JULIANO. 2005. Asymmetrical competition and patterns of abundance of Aedes albopictus and Culex pipiens (Diptera: Culicidae). J. Med. Entomol. 42 (4): 559-570. [ Links ]
13. FISHER, I. J., W. E. BRADSHAW & C. KAMMEYER. 1990. Fitness and its correlates assessed by intra- and interspecific interactions among tree-hole mosquitoes. J. Animal Ecol. 59: 819-829. [ Links ]
14. GARCÍA J. J., M. V. MICIELI, M. F. ACHINELLY & G. A. MARTI. 2002. Establecimiento de una población de Aedes aegypti L. en La Plata, Argentina. En: Salomón, O. D. (ed.), Actualización en artropodología sanitaria argentina. Fundación Mundo Sano. Buenos Aires, pp. 149-153. [ Links ]
15. GLEISER, R. M., J. URRUTIA & D. E. GORLA. 2000. Effects of crowding on larval populations of Aedes albifasciatus (Diptera: Culicidae), under laboratory conditions. Ent. Exp. Appl. 95: 135-140. [ Links ]
16. HAWLEY, W. A. 1985. The effect of larval density on adult longevity of a mosquito, Aedes sierrensis: epidemiological consequences. J. Animal Ecol. 54: 955-964. [ Links ]
17. HOBBS, J. H., E. A. HUGHES & B. H. EICHOLD. 1991. Replacement of Aedes aegypti by Aedes albopictus in Mobile, Alabama. J. Am. Mosq. Control Assoc. 7 (3): 488-489. [ Links ]
18. JULIANO, S. A. 2007. Population dynamics. J. Am. Mosq.Control Assoc. 23 (2 Supl.): 265-275. [ Links ]
19. JULIANO, S. A., L. P. LOUNIBOS & G. F. O'MEARA. 2004. A field test for competitive effects of Aedes albopictus on A. aegypti in South Florida: differences between sites of coexistence and exclusion? Oecologia 139 (4): 583-593. [ Links ]
20. LOUNIBOS, L. P. 2002. Invasions by insect vectors of human disease. Annu. Rev. Entomol. 47: 233-266. [ Links ]
21. LOUNIBOS, L. P. 2007. Competitive displacement and reduction. J. Am. Mosq. Control Assoc. 23 (2 Supl): 276-282. [ Links ]
22. MACIÁ, A. 2006. Differences in performance of Aedes aegypti larvae raised at different densities in tires and ovitraps under field conditions in Argentina. J. Vector Ecol. 31 (2): 371-377. [ Links ]
23. MACIÁ, A. 2009. Effect of larval crowding on development time, survival and weight at metamorphosis in Aedes aegypti (Diptera: Culicidae). Rev. Soc. Entomol. Argent. 68 (1-2): 107-114. [ Links ]
24. MACIÁ, A. 2011. Degradación de las hojas de "tilo" y "fresno" y la utilización de recursos por las larvas del mosquito Culex pipiens (Diptera: Culicidae) en contenedores artificiales de agua. Ciencia Crítica 2 (2): 12-18. [ Links ]
25. MICHAEL, E., D. A. P. BUNDY & B. T. GRENFELL. 1996. Re-assessing the global prevalence and distribution of lymphatic filariasis. Parasitology 112: 409-428. [ Links ]
26. MICIELI, M. V., J. J. GARCÍA, M. F. ACHINELLY & G. A. MARTÍ. 2006. Dinámica poblacional de los estadios inmaduros del vector del dengue Aedes aegypti (Diptera: Culicidae): un estudio longitudinal (1996-2000). Rev. Biol. Trop. 54 (3): 979-983. [ Links ]
27. MINISTERIO DE SALUD DE LA NACIÓN. 2009. Situación del dengue en Argentina. Primer semestre del 2009. Boletín Epidemiológico Periódico. Edición Especial. Disponible en: http://www.msal.gov.ar/htm/site/pdf/BEP_dengue_int.pdf (Acceso 18/2/2011). [ Links ]
28. MINISTERIO DE SALUD DE LA NACIÓN. 2011. Alerta epidemiológico Nº 7. Boletín Epidemiológico Periódico. Disponible en: http://www.msal.gov.ar/ htm/site/pdf/epidemiologia/alerta-casos-encefalitis-san-luis.pdf (Acceso 14/4/2011). [ Links ]
29. O' MEARA, G. E., L. F. EVANS, A. D. GETTMAN & J. P. CUDA. 1995. Spread of Aedes albopictus and decline of Ae. aegypti (Diptera: Culicidae) in Florida. J. Med. Entomol. 32 (4): 554-562. [ Links ]
30. OPS. 1995. Dengue y dengue hemorrágico en las Américas: guías para su prevención y control. Organización Panamericana de la Salud. Publ. Cient. Nº 548, Washington. [ Links ]
31. OPS. 2009. Situación de la Salud en las Américas. Indicadores Básicos 2009. Disponible en: http://new.paho.org/hq/dmdocuments/2009/IB_SPA_2009.pdf (Acceso 29/4/2011). [ Links ]
32. REISEN, W. K., M. M. MILBY & M. E. BOCK. 1984. The effects of immature stress on selected events in the life history of Culex tarsalis. Mosq. News 44: 385-395. [ Links ]
33. REISKIND, M. H., K. L. GREENE & L. P. LOUNIBOS. 2009. Leaf species identity and combination affect performance and oviposition choice of two container mosquito species. Ecol. Entomol. 34: 447-456. [ Links ]
34. RENSHAW, M., M. W. SERVICE & M. H. BIRLEY. 1993. Density-dependent regulation of Aedes cantans (Diptera: Culicidae) in natural and artificial populations. Ecol. Entomol. 18: 223-233. [ Links ]
35. RÍOS, A. A., C. E. MACHADO-ALLISON, J. E. RABINOVICH & D. J. RODRÍGUEZ. 1978. Competencia intra e interespecífica en Aedes aegypti (L.) y Culex fatigans (Wiedemann) (Diptera: Culicidae) en condiciones de laboratorio. Acta Cient. Venezolana 29 (6): 467-472. [ Links ]
36. ROSSI, G. C. & W. R. ALMIRÓN. 2004. Clave ilustrada para la identificación de larvas de mosquitos de interés sanitario encontradas en criaderos artificiales en la Argentina. Serie Enfermedades Transmisibles, Publicación Monográfica 5, Fundación Mundo Sano, Buenos Aires. [ Links ]
37. SCHWEIGMANN, N., P. ORELLANO, J. KURUC, V. M. TERESA, D. VEZZANI & A. MÉNDEZ. 2002. Distribución y abundancia de Aedes aegypti (Diptera: Culicidae) en la ciudad de Buenos Aires. En: Salomón, O. D. (ed.), Actualizaciones en Artropodología Sanitaria Argentina, Publicación Monográfica 2, Buenos Aires, pp. 155-160. [ Links ]
38. SERVICE, M. W. 1985. Population dynamics and mortalities of mosquito preadults. En: Lounibos, L. P. , J. R. Rey & J. H. Frank (eds.), Ecology of mosquitoes: Proceedings of a workshop. Florida Medical Entomology Laboratory, Vero Beach, pp. 185-201. [ Links ]
39. SMITH, P. T., W. K. REISEN & D. A. COWLES. 1995. Interspecific competition between Culex tarsalis and Culex quinquefasciatus. J. Vector Ecol. 20: 139-146. [ Links ]
40. STEIN, M. & G. I. ORIA. 2002. Identificación de criaderos de Aedes aegypti (Diptera: Culicidae) y cálculo de índices de infestación en la provincia del Chaco. En: Salomón, O. D. (ed.), Actualización en artropodología sanitaria argentina. Fundación Mundo Sano. Buenos Aires, pp. 161-166. [ Links ]
41. STEINSWASCHER, K. 1982. Relation between pupal mass and adult survivorship and fecundity for Aedes aegypti. Environ. Entomol. 11: 150-153. [ Links ]
42. VEZZANI, D., S. M. VELÁZQUEZ & N. J. SCHWEIGMANN. 2004. Seasonal pattern of abundance of Aedes aegypti (Diptera: Culicidae) in Buenos Aires City, Argentina. Mem. Inst. Oswaldo Cruz 99 (4): 351-356. [ Links ]
43. VEZZANI, D., S. M. VELÁZQUEZ, S. SOTO & N. J. SCHWEIGMANN. 2001. Environmental characteristics of the cemeteries of Buenos Aires City (Argentina) and infestation levels of Aedes aegypti (Diptera: Culicidae). Mem. Inst. Oswaldo Cruz 96 (4): 467-471. [ Links ]
44. VINOGRADOVA, E. B. 2000. Culex pipiens pipiens mosquitoes: taxonomy, distribution, ecology, physiology, genetics, applied importance and control. Pensoft, Moscú [ Links ].














