Introducción
La contaminación por metales pesados es seguramente uno de los problemas ambientales más serios. Industrias como la minería, la fundición de metales, la producción de combustible y energía a partir de petróleo, la industria de fertilizantes y pesticidas y sus aplicaciones, entre otras, producen residuos que contienen metales pesados y éstos terminan transfiriéndose al medio ambiente debido a un incorrecto tratamiento o disposición final (Londoño et al, 2016). El plomo es un metal que se encuentra de forma natural en el medio ambiente, generalmente formando parte de algunos minerales como la galena (sulfuro de plomo, PbS) siendo un metal bioacumulable muy tóxico y sin función biológica conocida (Wiwid et al, 2014) como parte de la remediación de sitios contaminados, la biosorción resulta ser una de las tecnologías más prometedoras, ya que se trata de un proceso que permite tratar grandes volúmenes de efluentes con bajas concentraciones del metal (Das y Das, 2013; Gupta et al, 2019). Por otra parte, segúnEsmaeili y Beni (2020) el concepto biosorción de metales pesados, se refiere básicamente a la captación pasiva de iones metálicos por medio de una biomasa viva o muerta a través de mecanismos fisicoquímicos como la adsorción o el intercambio iónico. La biosorción involucra una fase sólida como la biomasa (biosorbente) y una fase líquida (solvente, generalmente es agua) en la cual están la(s) especie(s) metálica(s) a ser biosorbida(s) (adsorbato). Si el adsorbente posee grupos funcionales afines al adsorbato, la biosorción es eficiente. Numerosos materiales biológicos han sido estudiados con el fin de evaluar su potencial para la adsorción de metales pesados. Entre estos materiales, la biomasa bacteriana, hongos y algas marinas, constituyen el conjunto más estudiados hasta el momento (Chung et al, 2013; Holanda et al, 2016).
La capacidad de adsorción de las diferentes biomasas puede ser mejorada con pretratamientos, físicos o químicos, también denominado etapa de activación. Esta etapa aumenta el número de sitios de unión, sin embargo, se debe tener en cuenta que puede encarecer el proceso dependiendo de las condiciones de activación (Castellón et al, 2014; Giese y Jordáo, 2019).
El objetivo de la presente contribución es aislar una cepa nativa de microorganismo de las pilas de lixiviación de la Mina Hualilán (Provincia de San Juan, Argentina) con el fin de ser utilizada como biosorbente para captar iones metálicos de plomo (II), además estudiar el proceso de adsorción mediante modelos cinéticos y de equilibrio.
Marco geológico
El yacimiento metalífero Hualilán se encuentra ubicado en el borde occidental de la Precordillera Central en el ámbito del bolsón de Hualilán, a unos 120 km de la ciudad de San Juan en el departamento Ullúm (Figura 1). En esta área afloran sucesiones carbonáticas y sili-coclásticas del Paleozoico Inferior y rocas intrusivas del Mioceno.
La Formación San Juan es una unidad clásica de la Precordillera de San Juan, la cual está compuesta en términos generales por wac-kestone, packstoney grainstone bioclásticos e intra-bioclasticos. Esta formación contiene una rica fauna fósil característica de ambiente carbo-nático de plataforma abierta según Benedetto (2003); de edad tremadociana-darriwilina (Or-dovícico Inferior-Medio) basado en su contenido de conodontes (Lehnert, 1995; Mestre y Heredia, 2013, 2020; Heredia etal., 2017). Sobre la Formación San Juan se apoya de forma paraconcordante las unidades silicoclásticas que componen el Grupo Tucunúco (Ordovícico Superior-Devónico) (Figura 1).
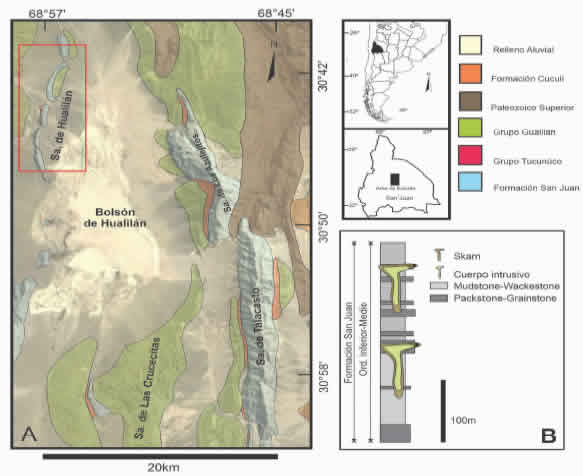
Figura 1: A- Mapa geológico del sector central de la Precordillera Central y Bolsón de Hualilán. B- Sección estratigráfica esquemática de La Formación San Juan con los intrusivos y mineralización en skarn del distrito minero de Hualilán. / Figure 1. A- Geological map of the central sector of the Central Precordillera and Bolsón de Hualilán. B- Schematic stratigraphic section of the San Juan Formation with the intrusives and mineralization in skarns of the Hualilán mining district.
Las calizas de la Formación San Juan se encuentran instruida principalmente por andesitas basálticas y pórfidos andesíticos y dacíticos de color gris a gris verdoso, las cuales fueron asignadas al Mioceno (Leveratto, 1976), (Figura 1). La intrusión de estos cuerpos ígneos causó una mineralización de tipo skarn en las rocas carbonáticas de la Formación San Juan (Taruá et al, 2000), (Figura 1). Dicho skarn ha sido objeto de explotación para Zn, Cu y Au desde principios del siglo XX hasta la década del 50, y actualmente se encuentra en exploración debido a su potencial como yacimiento de oro.
Los cuerpos mineralizados más importantes se alojan en las calizas y son concordantes con ellas. Constituyen dos corridas una situada en las minas del sur de más de 500 m y otra en las del norte. En general los cuerpos mineralizados son lenticulares (clavos) y profundos y suelen adelgazarse horizontalmente en cuña en sus extremos. El mineral fue explotado mediante laboreos subterráneos, contabilizando 23 laboreos que suman 6.500 m de desarrollo. Además, hay trabajos superficiales, como niveles y chiflones internos en varias minas (Furque et al., 2003). El método de recuperación que fue utilizado en esta mina fue la lixiviación en pilas mediante el uso de cianuro, sobre las cuales se ha realizado el muestro para los análisis llevados a cabo en la presente contribución.
Materiales y métodos
Muestreo de desechos mineros y caracterización fisicoquímica del sólido
El trabajo se llevó a cabo con muestras sólidas de la mina Hualilán. Las muestras fueron tomadas de 10 puntos diferentes de la pila de lixiviación (material de desecho) (Figura 2). La toma de muestras se realizó en forma manual excavando con pala retirando aproximadamente 500 g de muestra de cada punto seleccionado. El material utilizado fue previamente esterilizado y las muestras se almacenaron en envases plásticos estériles y se conservaron a temperatura ambiente hasta su procesamiento (Castro, 2017).
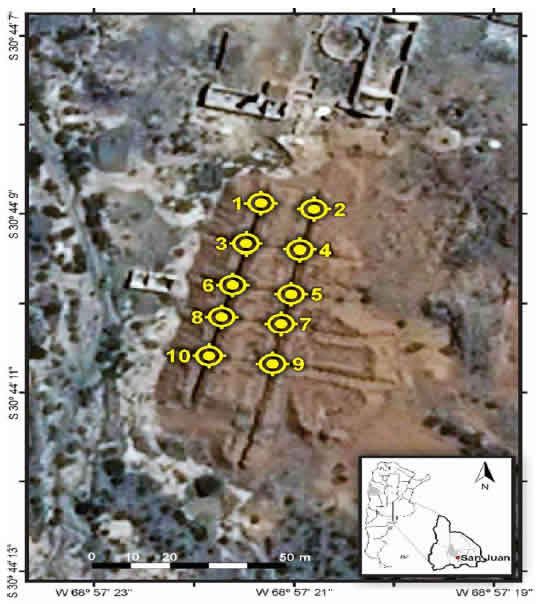
Figura 2: Foto satelital con referencias de coordenadas de los puntos de muestro en la pila de lixiviación en Mina Hualilán, San Juan, Argentina. / Figure 2. Satellitephoto with coordínate references of the samplingpoints in the heap leach at Mina Hualilán, San Juan, Argentina.
El análisis físico-químico de una muestra representativa del material de la pila de lixiviación fue realizado por el laboratorio de análisis instrumental del Instituto de Investigaciones Mineras (IIM) de la Universidad Nacional de San Juan según metodología estándar.
Aislamiento, identificación y obtención del biosorbente
Se utilizó Sabouraud glucosado agarizado Biopack comercial como medio de cultivo, con la siguiente composición: tejido de digestión pancreática de animales (5.00 g/L); digestión pancreática de caseína (5.00 g/L); dextrosa anhidra (36.40 g/L) y agar bacteriológico (15.00 g/L).
Se pesó 1 g de desecho minero y se agregó agua destilada estéril hasta un volumen final de 10 ml en tubo de ensayo y luego se agitó para homogeneizar la muestra. A partir de la suspensión, se realizaron diluciones decimales seriadas sembrando 0,10 ml de cada dilución, por triplicado. Se usaron placas de Petri con medio Dextrosa Sabouraud con antibióticos (cloranfenicol 0.05 g/l) a modo de control. Se incubaron en cajas de Petri a 28°C durante 7 días. A partir de las placas con crecimiento, se seleccionaron aquellas colonias de hongos filamentosos que presentaron diferentes morfotipos (color, tamaño, aspecto, etc.). El hongo aislado fue identificado molecularmente. La extracción de ADN se hizo según el protocolo de CTAB (Cetyl Tri-methyl Ammonium Bromide). Se realizó la PCR (Polymerase chain reaction) de la extracción utilizando los primers ITS1-ITS4 y Bt2a-Bt2b. La amplificación de la muestra se comprobó por electroforesis en gel de agarosa 1.50 % a 90 amperes por 30 minutos. La amplificación fue enviada a Macrogen para su secuenciación. Para el análisis de las secuencias, se eliminaron los extremos en los que la identificación de las bases no es fiable, se utilizó el programa Chromas Pro 1.5. Luego se cargaron los resultados en la base de datos BLAST.
Para la generación de biomasa, en primer lugar, se inoculó la cepa en medio líquido en estufa de cultivo a una temperatura de 28°C hasta su máximo crecimiento desarrollado en un tiempo total de 15 días. El medio de cultivo utilizado fue Sabouraud Glucosado caldo a volúmenes crecientes. Como el objetivo es generar una biomasa inerte, una vez que la cepa llegó a su máximo desarrollo, se esterilizó en autoclave a 121°C durante 15 minutos. Después se procedió a lavar la biomasa repetidamente con agua destilada y por último se secó en estufa a 80° C hasta peso constante.
Activación con Etanol y ensayo preliminar de adsorción
Se suspendieron 5 gramos de biomasa seca en 100 ml de etanol (solución 70%) durante 1 hora a temperatura ambiente. Luego se filtró y se secó en estufa a 80°C hasta peso constante (Ezzouhri et al, 2010). Para los ensayos preliminares de biosorción, se pesó 0.10 gramos de biomasa con y sin activación en 100 ml de solución de nitrato de plomo 25 ppm a un pH=5.00, con agitación y a temperatura ambiente. Después de 6 horas de incubación la solución se centrifugó, filtró y se envió a analizar por espectroscopia de absorción atómica.
Aplicación de un diseño compuesto central en la capacidad de absorción del plomo
Los factores evaluados de la capacidad de adsorción de HR-SA (sin activación) y HR-E (con activación) fueron: pH, concentración de bioma-sa, concentración metálica y tiempo en un diseño experimental central compuesto rotable (DCCR) con 4 puntos centrales, esto último permitió analizar la falta de ajuste. Los ensayos consistieron en poner en contacto la biomasa fúngica durante un intervalo de tiempo determinado, con soluciones de nitrato de plomo a distintas concentraciones, pH y concentración de adsorbente. En total fueron 28 corridas del diseño experimental realizado con las muestras en estudio como se evidencia en la tabla 1.

Tabla 1: Diseño experimental para optimizar los factores principales que influyen en la capacidad de adsorción. / Table 1. Experimental design to optimize the main factors that influence the adsofpúon capaáty.
A partir del estudio experimental se obtuvieron modelos cuadráticos para cada adsorbente, que relacionaron la capacidad de adsorción con los factores evaluados, además se pudo determinar las condiciones que maximizan la adsorción de plomo. En todos los casos se llevaron a cabo las validaciones experimentales de los modelos estadísticos. En la tabla 2 se muestra los niveles empleados en las variables independientes (factores) y las respuestas tanto para las bio-masas HR-SA y HR-E del diseño experimental. Se utilizó como software Statgraphics Centurion tanto para la generación del diseño y el análisis estadístico de datos.
La capacidad de adsorción (mg/g) “qe”, que se observa en la tabla 2, se calcula como se muestra en la siguiente ecuación
qe=(c-cf )*V/m
Donde “ci” y “cf ” son las concentraciones de la disolución metálica inicial y final, “V” es el volumen de la solución y “m” es la cantidad de adsorbente en gramos.
Modelos Cinéticos y de equilibrio de adsorción
Para evaluar la cinética de adsorción se realizaron ensayos discontinuos para metal plomo a dos concentraciones metálicas 75 y 25 ppm, 1 g/l de concentración biomasa, pH-5.80, durante 8 horas. Los resultados se ajustaron a modelos de Pseudo-primer y Pseudo-segundo orden de reacción.

Tabla 2: Factores y niveles del diseño experimental (qe capacidad de adsorción, mg/g). / Table 2. Factors andkvels of the experimental design (qe= adsotpñon capadty, mgjg).
Los ensayos de equilibrio se realizaron considerando el tiempo de equilibrio determinado por el estudio cinético y tres concentraciones metálicas 25, 50 y 75 ppm. Estos datos experimentales, se ajustaron a los modelos de Langmuir y Freundlich (Ramya et al., 2016) lo que permitió determinar parámetros que describen la eficacia del proceso, como la capacidad máxima de adsorción de un metal por la biomasa (qm), y la afinidad de los iones metálicos y los sitios activos.
Modelo de Langmuir:
qe-qm* K* Ce + K* C
Donde Ce es la concentración de equilibrio de iones metálicos (mg/L), qe es la capacidad de adsorción en el equilibrio (mg/g), KL es la constante de Langmuir (L/mg) y qm es la adsorción máxima en monocapa (mg/g).
Modelo de Freundlich: qe - K + Ce Vn Donde Ce es la concentración de equilibrio de iones metálicos (mg/l), qe es la capacidad de adsorción en el equilibrio (mg/g), n es la constante característica relativa a la intensidad de la adsorción y K constante característica relacionada con la capacidad de adsorción (mg/g). Cabe aclarar que estos cálculos se ven aplicados y reflejados tanto en tabla 6 y Figura 5 del presente artículo.
Resultados y discusión
La asociación mineralógica que caracteriza a las muestras extraídas de la pila de lixiviación es: pirita (Py), cuarzo (Qz), arcillas, mica, clastos líticos y óxidos (Figura 3). En la muestra se observó fuerte reacción al agregado de HCl (ácido clorhídrico) en frio, esto demuestra también, la presencia de carbonatos de calcio. Como resultado de la composición química del material de la pila (tabla 3), se evidencia la presencia de hierro como componente mayoritario mientras que calcio, manganeso, aluminio, potasio y sodio como secundarios. En cuanto a la presencia de metales pesados, en primer lugar, se encuentra zinc, seguido del plomo y cobre; en tanto el cadmio y la plata están presentes en pequeña proporción. Además, los minerales de la pila arrojaron un lixiviado con un pH de pasta ligeramente básico debido esencialmente a la presencia de carbonatos en su composición. Estos desechos mineros son el resultado de la acumulación de rocas mineralizadas que han sido sometidas a un proceso de alcalinización con lechada de cal y posterior lixiviación con cianuro de sodio para la extracción de los elementos valiosos.

Figura 3: A-B- Imágenes de las especies mineralógicas que caracteriza la pila de lixiviación, mediante Microscopio estereoscópico Leica S6D, escala 0.30 mm. / Figure 3. A-B- Images of the minerak§cdspecies that charactai%e the leachingpile, using a Leica S6D stereomicroscope, scale 0.30 mm.
Por esto, la caracterización mineralógica y química se corresponde con minerales de una pila de lixiviación, donde la alcalinidad protectora a pH mayor a 10, se consigue con agregados de cantidades medidas de álcalis; típica de un proceso de lixiviación con cianuro para la disolución del oro y plata.
Como resultado del aislamiento se obtuvo un total de 10 cepas que mediante la determinación del Índice de Tolerancia (IT) permitió seleccionar una de las cepas más tolerantes al plomo (Muñoz et al, 2012). Este ensayo consistió en poner en contacto todas las cepas aisladas con medio de cultivo al cual se le adicionó soluciones de plomo a distintas concentraciones de 25 a 800 ppm. Luego el crecimiento micelial en cada placa fue observado durante un período de total desarrollo del hongo comparado con la placa control, midiendo diámetros de crecimiento en cada placa en centímetros y por último se calculó el PICR (Porcentaje de Inhibición de Crecimiento Radial), (Samaniego Fernández et al, 2018), se calcula como se muestra en la siguiente ecuación:
PICR= ((R1-R2)) /R1*100
Donde:
R1 = es el diámetro de crecimiento de la muestra de control.
R2= es el diámetro de crecimiento de la cepa de estudio.
La cepa más tolerante denominada HR fue identificada como Pemilium clumiae cuyo número de acceso de GenBank es GQ221866 con un 99.82 % de identidad. Cabe resaltar la importancia de que la biomasa sea de origen autóctono, reside en que representan poblaciones tolerantes y/o resistentes, capaces de sobrevivir y crecer en ambientes altamente contaminados, pudiendo ser reutilizados como agentes biorremediadores (Cárdenas et al, 2013).

Tabla 3: Composición química de un compósito de los 10 puntos diferentes de la pila de lixiviación analizada mediante ICP (Unidades de concentración en g/g N/D= no detecta el equipo). / Table 3. ChemicalcomposHon of a composite the 10 different points of from heap leach analyzed by ICP (Units of concentration in g/g N/D = does not detect the equipment).
En el ensayo preliminar de adsorción se obtuvieron capacidades de adsorción de 2.80 mg/g y 4.00 mg/g para HR-SA y HR-E respectivamente. Se concluye que la biomasa HR activada con etanol tiene una mayor capacidad de adsorción comparada con la biomasa sin activar.
Los coeficientes de correlación (R2) de los diseños experimentales aplicados fueron de 82.00 y 84.14 para la adsorción de las biomasas fúngicas HR-SA y HR-E respectivamente.
En ambos casos los factores y todas las interacciones tuvieron un valor p menor que el nivel de significancia a=0.05, indicando que tienen influencia estadisticamente significativa sobre la variación de la capacidad de adsorción de plomo en los dos adsorbentes evaluados con un nivel de confianza del 95.00%. De la aplicación del diseño experimental se obtuvo un modelo de segundo orden que se muestra en la siguiente ecuación. En este modelo empírico se introdujeron los términos estadísticamente significativos.
q = β0 + β1 pH + β2 Conc.ad + β3 Conc.Met. + β4 t +β11 pH2 + β22 Conc ad.2 +β33 Conc met.2 + β44 t 2+ β12 pH Conc ad. + β13 pH concmet. + β14 pH t + β23 Concad.ConcMet + β24 Conc ad.t + β34 Conc.met.
Donde q es la capacidad de adsorción en el equilibrio (mg metal por g biomasa seca); β0 es el coeficiente de intercepción; β1, β2 y β3 son los términos lineales; β11, β22, β33 y β44 son los términos cuadráticos; y β12, β13, β14, β24, β23 y β34 son los términos de interacción.
La bondad del ajuste del modelo fue determinada evaluando la falta de ajuste, el coeficiente de correlación (R2) y el valor de la prueba de Fisher (Miller y Miller, 1993; Nour et al, 2016), obtenidos mediante el análisis de varianza (ANOVA). La significancia estadística del modelo y sus términos por separado fueron determinados para un nivel de significancia del 5 % (p=0.05). A partir del modelo se obtuvieron las condiciones que maximizaron la capacidad de adsorción (qe), las que son presentadas en la tabla 4.
El efecto del factor “concentración de biomasa” es negativo a la variable respuesta, esto expresa que para un aumento de la concentración de biomasa la capacidad de biosorción disminuye, como se puede apreciar en los gráficos de superficies de respuesta para HR-SA (Figura 4-A) y HR-E (Figura 4-B).
QR= qe=capacidad de adsorción de HR-SA; analizada como variable respuesta.
QR act=capacidad de adsorción de HR-E; analizada como variable respuesta.
Conc biom=concentración biomasa analizada como factor.
Conc meta=concentración metálica analizada como factor.
Para la validación de los modelos estadísticos se ensayaron las condiciones de la Tabla 4 y se compararon los valores de capacidad de adsorción experimental y los predichos, mediante un “Test t de Student de muestras apareadas” según Miller y Miller (1993). El cual demostró que no hubo diferencias significativas, denotando la validez al modelo empírico obtenido. Para el caso de HR-SA los valores obtenidos tanto de qe óptimo y qe experimental fueron 60.01 mg/g y 72.59 mg/g respectivamente; mientras que para HR-E los valores obtenidos tanto de qe óptimo y qe experimental fueron de 77.95 mg/g y 65.33 mg/g. Otros autores han reportado que la capacidad de adsorción de plomo de diferentes biomasas tales como Penicillum sp. y de R arrhicus (Gottfried Ehrenberg, 1818) fueron de 60.77 mg/g y 48.70 respectivamente (Aftab et al, 2013; Muñoz et al, 2019). Una comparación directa entre diferentes biosorbentes es difícil debido a las diferentes condiciones experimentales empleadas, sin embargo, se puede evidenciar que la cepa en estudio Penicillum cluniae exhibe una comparable y eficiente capacidad de adsorción frente a este metal.
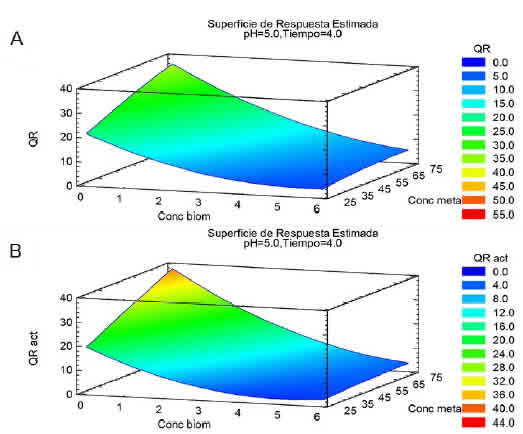
Tabla 4: Valores óptimos de los factores para la máxima capacidad de adsorción de todos los adsorbentes empleados para plomo. HR-SA=Penicillium chímate sin activar, H'R-E=Penicillium duniae activado con etanol (Donde qe óptimo= capacidad de adsorción óptimo obtenida del diseño (mg/g); qe exper. = capacidad de adsorción experimental obtenida a partir de los valores óptimos (mg/g); Conc. Biomasa = concentración de biomasa (g/l); Conc. Metálica= concentración Pb (ppm). / Table 4. Optimd valúes of thefactars for the máximum adsorption capacity of al adsorbents used for lead. HR-SA = Penicillium cluniae not acivated, HR-E = Penicillium cluniae activated with etanol (Where optimal qe = opimd adsorption capacity obtained from the design (mg/g); qe exper. = experimental adsorption capacity obtained from the optimd valúes (mg/g); Biomass Conc = biomass concentration (g/l); Metdlic Conc = Pb concentrañon (ppm)).

Figura 4: A- Gráfico de superficie de respuesta para HR-SA. B- Gráfico de superficie de respuesta para HR-E. / Figure 4. A. Response surfaceplot for HR-SA. B- Response surfaceplotfor HR-E.
En este trabajo la aplicación de los diseños experimentales en el estudio de adsorción de plomo con las dos biomasas fúngicas HR-SA y HR-E fue llevada a cabo con buenos valores de los parámetros estadísticos, y además permitió encontrar la región óptima de factores para alcanzar la máxima capacidad de adsorción de plomo. En la literatura no hay reportes de procesos similares con biosorbentes fúngicos que hayan sido evaluados mediante esta herramienta estadística, sin embargo, Muñoz et al. (2015) reportaron el uso de un diseño estadístico para estudiar el comportamiento de adsorción de una bacteria Klebsiella sp. 3S1 en soluciones acuosas de Pb.
Estudio cinético y de equilibrio
Tanto para la biomasa HR-SA como para la HR-E, el modelo de pseudo-segundo orden es el que mejor se ajusta a los datos experimentales, esto se puede ver en la
.
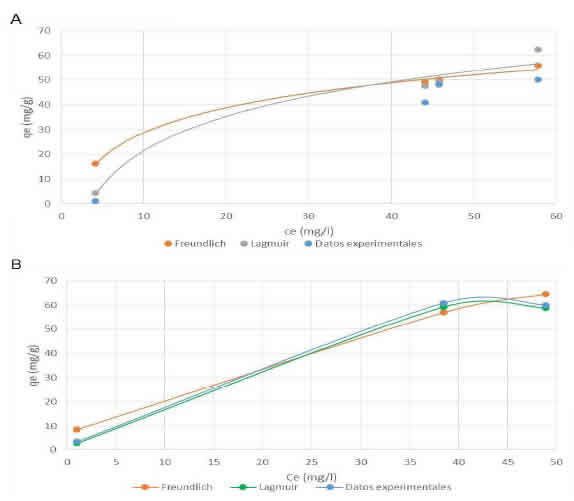
Tabla 5: Valores de los parámetros de los modelos cinéticos. Dónde: qe=capacidad de adsorción en el equilibrio.; K1 y K2= constantes de velocidad de Pseudo primer orden y Pseudo segundo orden; R2= R-cuadrada, coeficiente de determinación. / Table 5. Parameter valúes of the kinetic model. Where: qe = adsorption capacity at equilibrium; K1 and K2 = Pseudo first order and Pseudo second arder rate constants; R2 = R-squared, cofficient of determinañon.
Los procesos de adsorción de las dos bio-masas HR-SA y HR-E son bien descriptos por el modelo de Langmuir, indicando un recubrimiento en monocapa, esto se puede corroborar con los coeficientes de correlación detallados en la tabla 6.
En la figura 5 se muestran los datos experimentales de la capacidad de adsorción en el equilibrio y el ajuste según los modelos de Langmuir y Freundlich, tanto para las biomasas HR-SA (Figura 5-A) y HR-E (Figura 5-B).
Cabe destacar que los microorganismos aislados de desechos de minas son una importante fuente de biosorbentes para captar metales pesados en la remediación ambiental, dada la tolerancia que tienen por haber crecido en condiciones extremas como es una pila de lixiviación (desecho minero). De tal manera se puede afirmar que uno de los métodos más reconocidos para la obtención de materiales biosorbentes es a través del aislamiento de desechos contaminados de minas, debido a que exhiben, por un lado, altas capacidades de recuperación de metales pesados, y por el otro brinda una herramienta como solución a la remediación ambiental.

Figura 5: A- Ajuste de datos experimentales de HR-SA. B- Ajuste de datos experimentales de HR-E. / Figure 5. A. Fittingof HR-SA experimental data. B- Fitdng of HR-E experimental data.
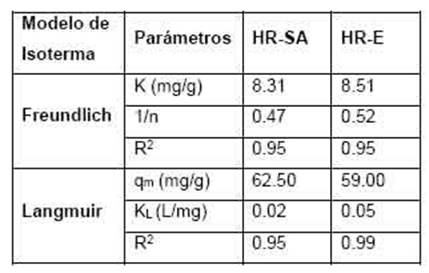
Tabla 6: Parámetros del modelo de Freundlich y Lagmuir para todos los biosorbentes. Dónde: K constante característica relacionada con la capacidad de adsorción (mg/g); n es la constante característica relativa a la intensidad de la adsorción; qm es la adsorción máxima en monocapa (mg/g); KL es la constante de Langmuir (L/mg). / Table 6. Parameters of the Freundlich andLagmuir modelfor cü biosorbents. Where: K charactmsñc mnstant related to the adsorption capacity (mg/g); n is the characteristic constant related to the intensity of the adsorption; qm is the maximum monolayer adsorption (mg/g); KL is Lamgmuirs constant (L/mg).
Agradecimientos
A la institución a las que pertenecen los autores y sus respectivas Direcciones de Investigación por el apoyo otorgado para la realización de la presente investigación.
Conclusión
De acuerdo a los objetivos planteados en este estudio, se aisló una cepa fúngica (Penicillium cluniae) a partir de desechos mineros y se evaluó el proceso de adsorción de Pb (II) mediante la aplicación de un diseño experimental central compuesto rotable (DCCR), logrando encontrar las condiciones que maximizan la capacidad de adsorción. Las capacidades de adsorción máxima fueron 60.01 mg/g para la biomasa sin activación y 77.95 mg/g para la biomasa activada. Ambos procesos de adsorción mostraron un comportamiento cinético de pseudo segundo orden, y en el equilibrio fueron bien representados por el modelo de Langmuir.
Los resultados indican que los hongos aislados de suelos de minas, podrían ser utilizados como biosorbentes, mejorando su capacidad de remoción del ión metal Pb (II) mediante técnicas simples y poco costosas.














