Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
InVet
versión On-line ISSN 1668-3498
InVet vol.13 no.1 Ciudad Autónoma de Buenos Aires ene./jun. 2011
ARTÍCULO DE INVESTIGACIÓN
Efecto de la infección de Mycobacterium avium paratuberculosis en la producción de anticuerpos bovinos
Fernández, B. 1.; Jolly, A.1; Colavecchia, S.1; Fernández, E.2; Mundo S.L.*1
1Cátedra de Inmunología,
2Cátedra de Clínica de Rumiantes, Facultad de Ciencias Veterinarias. Universidad de Buenos Aires. Chorroarín 280 (1427) Buenos Aires.
* Premio "Estímulo a la Investigación Científica 2010" en la categoría graduados de la Facultad de Ciencias Veterinarias, Universidad de Buenos Aires. Correspondencia e-mail: Silvia Mundo smundo@fvet.uba.ar
Recibido: 26/05/2011
Aceptado: 20/07/2011
Resumen
La paratuberculosis es una enfermedad granulomatosa crónica intestinal, causada por Mycobacterium avium subespecie paratuberculosis, que afecta a los rumiantes. El objetivo del trabajo fue caracterizar la respuesta inmune humoral sistémica y local de bovinos infectados. Se estudiaron once bovinos, seis infectados (asintomáticos, sintomáticos y terminales) y cinco controles. Se determinaron los niveles de inmunoglobulinas totales y se cuantificaron los subisotipos de IgG específicos a paratuberculosis en suero y materia fecal por ELISA. Los niveles de inmunoglobulinas totales en sueros fueron similares. Sin embargo, se evidenciaron aumentos significativos de IgM e IgG totales, e IgG-específica en materia fecal de los sintomáticos. La IgG1 específica fue predominante en sueros de bovinos sintomáticos y terminales. La IgG3 fue la inmunoglobulina específica de mayor cantidad detectada tanto en suero como en materia fecal de los asintomáticos. Nuestros resultados muestran que la infección no afecta la producción de inmunoglobulinas totales. El aumento de inmunoglobulinas en materia fecal podría relacionarse con la lesión de la mucosa intestinal. El predominio de IgG1 se corresponde con el cambio de perfil a Th2 en el periodo sintomático. El hallazgo de incrementos de IgG3 específica en asintomáticos sugiere el estudio de este isotipo para poder mejorar su identificación.
Palabras clave: Paratuberculosis; Bovino; Anticuerpos.
Effect of the infection with Mycobacterium avium paratuberculosis on the production of bovine antibodies
Summary
Paratuberculosis, caused by Mycobacterium avium subspecies paratuberculosis, is a chronic granulomatous enteric disease affecting ruminants. Our aim was to characterize systemic and local humoral responses of infected cows. Eleven cows were studied: six naturally infected (asymptomatic, symptomatic and terminal) and five control. Total IgM and IgG and paratuberculosis-specific IgG subisotypes, from feces and serum, were assessed by ELISA. No differences were detected on the levels of total immunoglobulins in sera. Symptomatic cows showed significative higher level of totals IgM and IgG, and specific-IgG in feces. IgG1 was the highest from sera of symptomatic and terminal. IgG3 was the highest specific immunoglobulin in sera and feces of asymptomatic. Our results showed total immunoglobulins levels in serum are not modified by the infection. The increment of immunoglobulins in feces could be caused by the lesions of intestinal mucosa. The predominance of IgG1 in symptomatic period is related to the change toward Th2 profile. The use of anti-IgG3 could improve the identification of asymptomatic cows.
Key words: Paratuberculosis; Bovine; Antibodies
Introducción
La paratuberculosis es una patología crónica intestinal que afecta a los rumiantes y es causada por el Mycobacterium avium subsp. paratuberculosis (Map)10. La enfermedad causa notables pérdidas económicas en la producción agropecuaria19; 20.
La infección se produce por ingestión de calostro, leche o materia fecal de animales eliminadores de bacterias.
Los animales infectados atraviesan un largo estadio subclínico durante el cual eliminan pequeñas cantidades de Map por leche y heces en forma intermitente. Su identificación es dificultosa, se utilizan principalmente kits que evalúan la producción de inteferón gamma por linfocitos en cultivo22. En algunos bovinos, por causas todavía inciertas, la forma subclínica avanza hacia el período clínico, que se caracteriza por la aparición de diarrea profusa, mala absorción de nutrientes y pérdidas de proteínas. En ese momento hay un cambio de perfil de la respuesta inmune de Th1 (celular) a Th2 (humoral)1;6;7, lo que conlleva a un aumento de inmunoglobulinas (Ig) circulantes facilitando el diagnóstico serológico de la enfermedad.
En la especie bovina, al perfil Th1 se lo relaciona con las IgM e IgG2, mientras que al Th2 se lo asocia con IgG1 e IgA8. Sin embargo, el papel funcional de los isotipos de anticuerpos (Ac) aún no ha sido totalmente dilucidado. Se describe al isotipo IgG1 como crítico para bloquear bacterias y toxinas en el sitio de infección, y al IgG2 se lo relaciona principalmente con el incremento de la fagocitosis mediada por neutrófilos frente a las infecciones bacterianas agudas.
El papel de los Ac en la protección frente a micobacterias ha sido reevaluado, demostrando que los Ac juegan un rol importante en la respuesta inmune frente a micobacterias2;11;24. Nuestro grupo ha demostrado un incremento en la asociación del Map con la célula blanco de la infección (el macrófago bovino) luego de la opsonización con IgG1 específica frente a la bacteria entera o a la proteína p34 recombinante. Además, se detectó un incremento en la activación celular y la formación del granuloma17.
En este contexto, se plantean como objetivos del presente trabajo la evaluación de la respuesta inmune humoral local y sistémica de bovinos en distintos estadios de paratuberculosis.
Materiales y métodos
Animales y muestras
Se estudiaron 11 bovinos adultos: 6 provenientes de rodeos infectados con paratuberculosis y 5 bovinos controles (C) provenientes de campos libres de paratuberculosis y tuberculosis de la provincia de Buenos Aires. De cada bovino se obtuvo 10 ml de sangre sin anticoagulante y materia fecal (MF). El suero se fraccionó y congeló a -20ºC hasta el momento de utilización. Las MFs fueron fraccionadas para realizar el cultivo y los ELISAs (se homogenizó 10 gr de MF y 10 ml de PBS Tween 20 al 0,05%, se centrifugaron varias veces a fin de obtener las muestras lo más límpida posible15. Luego fueron fraccionadas y congeladas a -20ºC hasta el momento de uso).
Los bovinos fueron clasificados según: rodeo de origen; presencia de signos clásicos de la enfermedad; niveles de proteínas séricas (evaluados por refractometría); detección de anticuerpos específicos en sueros frente al Antígeno Protoplasmático de Map (PPA); aislamiento e identificación de Map a partir de materia fecal.
Detección de anticuerpos específicos en sueros frente al PPA por ELISA
Se utilizaron placas de 96 hoyos sensibilizadas con 2µg/hoyo PPA (Allied Monitor Inc., Missouri, USA). Para evitar reacciones cruzadas con otras micobacterias, se pre-adsorbieron los sueros con Mycobacterium phlei (M. phlei) inactivada por calor (crecida en nuestro laboratorio). El sistema de revelado empleado fue un anticuerpo anti-IgG bovina en conejo conjugado a peroxidasa (Cappel, Fountain, USA) (anti-IgG-HRP). Para interpretar los valores de densidad óptica (DO) obtenidos se calculó el valor de corte (VC) sumando al promedio de los sueros controles negativos, dos desvíos estándares. A partir de los resultados se clasificó cada suero como: negativo (menor al VC), sospechoso (con densidades ópticas entre el VC y 1,5 el VC) y positivo (mayor a 1,5 el VC).
Aislamiento e identificación de Map a partir de materia fecal
Se cultivó la MF de los bovinos problema en medio Herrold con huevo, piruvato y micobactina (Allied Monitor Inc., Missouri, USA), a fin de confirmar el diagnóstico12;16. Se observaron todos los cultivos una vez por semana durante 18 semanas. En aquellos casos que crecieron colonias de bacterias con las características esperadas, se identificó el IS900 por PCR9. Para ello se utilizaron las secuencias de primers diseñadas por Mundo18 y Collins5. Map ATCC 19698 y M. phlei ATCC 11758 fueron utilizadas como cepas controles.
Producción de IgG3 bovina recombinante
Para obtener la IgG3 bovina recombinante (IgG3r) se cultivaron21 las E. coli BL21 pLysS transformadas con un plásmido obtenido en nuestro laboratorio17. Se realizó la purificación parcial de las proteínas a través de una columna de Níquel (His*Bind® Resin, Novagen, Darmstadt, Germany). Posteriormente se realizó la diálisis de las proteínas purificadas. Las bacterias E. coli BL21 (BL21-pRSET A) transformadas con el plásmido pRSET A sin inserto fueron procesadas y denominadas como extracto de E. coli (EEc).
Caracterización de los anti-isotipos de IgG.
Para el estudio de IgG1 e IgG2 se utilizaron reactivos comerciales: anti-IgG1 bovina en ovino conjugado a peroxidasa (Bethyl inc., Montgomery, USA), anti-IgG2 bovina monoclonal en ratón (Sigma-Aldrich Co., USA.), anti-IgG de ratón conjugado a peroxidasa (Jackson Immuno Research Laboratories, Inc., Pennsylvania, USA). Mientras que para evaluar la IgG3 se utilizó el suero de conejo anti-IgG3r obtenido previamente en nuestro laboratorio17, y el anti-IgG de conejo en cabra conjugado a peroxidasa (Kirkegaard & Perry Laboratorios, inc. Maryland, USA).
El suero de conejo anti-IgG3r fue preadsorbido con BL21-pRSET A en medio líquido (a una densidad óptica660nm de 2) y EEc en medio sólido (en placas de 96 hoyos) con el fin de disminuir la cantidad de Ac anti-E.coli. La determinación de las reacciones cruzadas se realizó por Inmunoblot y ELISA, utilizando los patrones comerciales IgG1 e IgG2 (Bethyl inc., Montgomery, USA), IgG3r, suero de un bovino normal y EEc.
Isotipos de inmunoglobulinas por ELISA
Niveles de Igs totales. Se sensibilizaron hoyos con 50µl de los sueros diluidos 1/6000 (IgM) y 1/20000 (IgG), y de las MFs sin diluir (IgM) y 1/100 (IgG). Se utilizaron los siguientes Ac conjugados a peroxidasa: anti-IgM bovina en ovino (Bethyl inc., Montgomery, USA) y anti-IgG-HRP.
Niveles de Igs específicas a Map. Los hoyos fueron sensibilizados con una cepa de referencia de origen bovino totalmente caracterizada y secuenciada denominada K1014 (gentilmente cedida por el Dr. Raul Barletta). Esta cepa se cultivó en medio 7H9 líquido y fue inactivada por calor en nuestro laboratorio. Se utilizaron 50µl de K10 a una DO660nm de 0,4..
Análisis Estadístico
Para analizar los resultados se utilizó el software estadístico Stastistix 8.0 (Analitical Software, Tallahasee, USA). Para la comparación de los niveles (DO) o cantidad de isotipos (µg/ ml) entre grupos, se realizó el análisis de varianza (ANOVA). Los niveles de significación fueron fijados en un 5%. Se determinó la homogeneidad de varianza y se realizó el Test de Dunet como análisis post-ANOVA.
Resultados
Clasificación de los grupos de animales infectados
El origen, sinología y los resultados de niveles de proteínas séricas, de reactividad frente a PPA en suero y el aislamiento e identificación de Map en materia fecal se muestran en la Tabla 1. Estos resultados permitieron clasificar a este grupo en infectados asintomáticos (IA), infectados sintomáticos (IS) e infectados terminales (IT).
Tabla 1. Clasificación de los grupos de bovinos. Grupo C (control), IA (infectado asintomático), IS (infectado sintomático), e IT (infectado terminal).
Producción de IgG3r y caracterización de los anti-isotipos de IgG bovinos
La purificación permitió obtener la IgG3r acompañada de una pequeña cantidad de proteínas contaminantes provenientes de la E. coli (Figura 1A). La pre-adsorción del suero de conejo anti-IgG3r disminuyó notablemente la cantidad de Ac anti-E. coli (Figura 1B). La evaluación del reconocimiento de E. coli por el anti-IgG3r mediante ELISA demostró que, al pre-adsorber el suero, la DO obtenida pasó de 1.01 (suero sin pre-adsorber) a 0.16 (suero pre-absorbido).
La lectura de los Inmunoblots reveló la existencia de reacciones cruzadas entre IgG3r con IgG1 e IgG2, ya que el anti-IgG3r preadsorbido reconoce a las tres subclases de IgG bovina (Figura 1B). Por otro lado, los antiisotipos comerciales (anti-IgG1 y anti-IgG2) sólo reconocieron el patrón correspondiente (IgG1 e IgG2 respectivamente, resultados no mostrados).
Por la técnica de ELISA se observó que el reactivo comercial anti-IgG2 reconoce la IgG3r y el antisuero anti-IgG3r pre-adsorbido reconoce IgG2 (patrón comercial). Sin embargo, estas reacciones cruzadas son siempre con menor intensidad que al reactivo correspondiente (Figura 1C).

Figura 1. Producción de IgG3r y caracterización de los anti-isotipos de IgG bovinos. A. Producción de IgG3r. SDS-PAGE al 12%. Calle 1 IgG3r expresada por Clon 36; Calle 2 IgG3r purificada; Calle 3 E. coli BL21 transformadas con el plásmido pRSET A sin inserto (EEc). B. Caracterización del anti-IgG3r. Inmunoblot. Antígenos: Calle 1 IgG2; Calle 2 IgG1; Calle 3 suero bovino; Calle 4 EEc; Calle 5 IgG3r. Se utilizó el anti-IgG3r como anticuerpo primario. C. Reacciones cruzadas de los anti-isotipos de IgG. ELISA.
Isotipos de inmunoglobulinas totales y específicas a Map en sueros y MFs
Niveles de IgM. Los resultados se muestran en Figura 2. Se detectó un leve aumento de IgMs totales y específicas a Map en los sueros de los infectados, especialmente en los IS en relación al C, aunque el análisis estadístico no permitió identificar estas diferencias como significativas. En MF los niveles fueron bajos en relación a los del suero. Sin embargo, el comportamiento fue similar al del suero. Se evidenció un incremento en los niveles de IgMs totales en IS e IT, siendo sólo significativa la diferencia entre los C y el IS.

Figura 2. Niveles de IgM e IgG totales y Map-específicas en sueros y materias fecales evaluados por ELISA.
Niveles de IgG. Los resultados se muestran en la Figura 2. Se determinaron niveles similares de IgG totales en sueros de los distintos grupos. Se observó un incremento estadísticamente significativo en los niveles de IgG Map específica en los sueros de los bovinos IS e IT. Llamativamente, la cantidad de IgG específica a Map en sueros de IA fue menor que en los C. En MFs se evidenciaron comportamientos similares entre IgG totales y específicas. Así mismo se detectaron altos niveles en IS e IT (IgG total y específica), siendo significativa la diferencia entre el IS y el C.
Isotipos de IgG específicas a Map: Los resultados se muestran en Tabla 2.
Tabla 2. Análisis de isotipos de IgG en sueros y materias fecales, expresados en μg/ml.
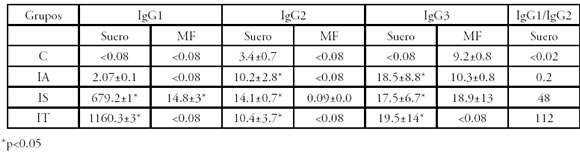
Niveles de IgG1:
Se observaron incrementos significativos en los niveles de IgG1 de sueros de IS e IT. Mientras que sólo se detectó IgG1 específica en MF del grupo sintomático (14,8± 3 µg/ml).
Niveles de IgG2.
Se identificó un aumento significativo en los sueros de todos los animales infectados (IA, IS e IT). En MF sólo pudo ser detectado en el grupo sintomático y en baja concentración (0,09±0.0 µg/ml). Mientras que en el resto de los bovinos los niveles fueron menores a 0.08 µg por ml correspondiente al límite de detección de la técnica.
Niveles de IgG3.
Se determinó un incremento significativo en los sueros de los bovinos infectados mostrando además cantidades similares entre ellos. En MF, los infectados IA e IS mostraron niveles similares a los detectados en suero.
Discusión
Nuestros resultados muestran que la infección con Map afecta los niveles de proteínas séricas sin modificar la producción de anticuerpos totales en suero, en contraposición al estudio realizado en pequeños rumiantes3. Por otro lado, se pudo observar un incremento de los niveles de IgM e IgG totales en materia fecal coincidiendo con el periodo clínico sintomático (IS). La IgM es el isotipo indicador de respuesta activa, sólo esperable en infecciones agudas o re-agudizaciones de infecciones crónicas. Este aumento de IgM en MF podría ser posible por la lesión intestinal y la re-estimulación de nuevos clonos de linfocitos B como respuesta a la re-infección endógena característica de éste periodo.
La IgM es una inmunoglobulina pentamérica que posee alta avidez pero poca afinidad. Por lo tanto, los altos niveles de IgM obtenidos en los bovinos controles podrían deberse a reacciones cruzadas con otras micobacterias25. Estos resultados coinciden con trabajos nuestros previos sobre bovinos infectados18.
El aumento de IgG específica a Map en sueros de bovinos sintomáticos y terminales está acompañado de incrementos de todas las sub-clases de IgG, principalmente de IgG1. Esta última parecería ser la Ig predominante en suero en estas etapas de la enfermedad tal como se han descripto previamente13;17.
Los animales asintomáticos presentaron niveles basales de IgGs Map-específicas en sueros. Esto podría deberse al tipo de respuesta inmune que predomina en esta etapa (celular).
Los altos niveles de IgG1 específicos encontrados en materias fecales de bovinos sintomáticos coinciden el predominio de este isotipo en la mucosa intestinal en bovinos normales4.
La respuesta de tipo Th2 no es tan clara dado que la IgG2 específica en suero aumentó en todos los bovinos infectados y los niveles son similares. Sin embargo, al analizar la relación IgG1/IgG2 se observa un incremento de dicha relación, coincidente con el avance de la patología (asintomáticos, sintomáticos, terminales). Estos resultados concuerdan con los expresados por Estes y Brown (2002) y Vanden Bush (2003).
Son pocos los trabajos que estudiaron la IgG3 en bovinos infectados con Map17. Y a nuestro entender, este es el primer trabajo que describe a la IgG3 bovina en mucosas. Se encontró un aumento de este isotipo en sueros de todos los bovinos infectados. Los niveles fueron levemente superiores a los hallados para IgG2 y parecería tener una cinética similar a la de IgG2. La detección de IgG3 Map-específica en MF del grupo control podría deberse a reacciones cruzadas con micobacterias intestinales no patógenas.
La IgG2 e IgG3 poseen cadenas pesadas similares; razón por la cual Butler4 las clasificó como IgG2a e IgG2b. La IgG3r producida para este trabajo, incluye regiones compartidas, lo que justifica las reacciones cruzadas encontradas. Sin embargo, se han encontrado diferencias entre los niveles de IgG2 e IgG3 en sueros y MFs estudiados, mostrando el poder de discriminación del reactivo (anti-IgG3r).
Es de destacar el predominio de la IgG3 específica en los animales asintomáticos. Dado que el diagnóstico serológico utilizado de rutina falla en la identificación de este grupo, se sugiere la utilización de un reactivo específico anti-IgG3 para mejorar su detección. En este sentido, nuestro próximo objetivo será desarrollar un ELISA diagnóstico utilizando PPA como antígeno y antisuero frente a IgG3 bovina recombinante.
Conclusiones
En el presente trabajo se determinó que la infección con Map no modifica los niveles de Igs totales séricas. Se corroboró el predominio de IgG1 en sueros de bovinos sintomáticos y terminales.
Se identificó IgG1 específica en materia fecal de los sintomáticos.
Se detectó IgG3 en sueros y materias fecales de animales asintomáticos y sintomáticos.
Se demostró que los reactivos desarrollados en nuestro laboratorio permitieron ampliar el conocimiento de la respuesta inmune humoral específica a paratuberculosis.
Agradecimientos
Se agradece a los veterinarios L. Gilardoni y L. Goldman por su apoyo técnico, y al doctor F. Paolicchi por sus aportes teóricos en el presente trabajo. Esta investigación fue financiada por los subsidios UBA-SeCyT v038 y v023.
1. Abbas B., Riemann H.P. IgG, IgM and IgA in the serum of cattle naturally infected with Mycobacterium paratuberculosis. Comp. Immunol. Microbiol. Infect. Dis. 1988; 11:171-175. [ Links ]
2. Abebe F. y Bjune G. The protective role of antibody responses during Mycobacterium tuberculosis infection.Clin. And Experimental Immunology. 2009; 157: 235-243. [ Links ]
3. Begara-McGorum I.; Wildblood L.A.; Clarke C.J. Early immunophatological events in experimental ovine paratuberculosis. Vet. Immunol. Immunophatol.. 1998; 63: 265-287. [ Links ]
4. Butler J.E.; Kehrli M.E. Immunocytes and immunoglobulins in milk. In Mucosal Immnology 3rd edition Ogra PL;Mesteckyme J; Lamm ME; Strober W; McGhee JR; Bienenstock J,. Academic Press, New York. 2004. [ Links ]
5. Collins D.M., Stephens D.M., de Lisle G.W. Comparison of polymerase chain reaction tests and faecal culture for detecting Mycobacterium paratuberculosis in bovine faeces. Vet Microbiol. 1993; 36(3-4):289-99. [ Links ]
6. Coussens P.M., Verman N., Coussens M.A., Elftman M.D., McNulty A.M. Cytokine gene expression in peripheral blood mononuclear cells and tissues of cattle infected with Mycobacterium avium subsp. paratuberculosis: evidence for an inherent proinflammatory gene expression pattern. Infect Immun. 2004; 72(3):1409-22. [ Links ]
7. Coussens P.M. Model for immune responses to Mycobacterium avium subsp. paratuberculosis in cattle. Infect Immun. 2004; 72(6):3089-96. [ Links ]
8. Estes D.M., Brown W.C. Type 1 and type 2 responses in regulation of Ig isotype expression in cattle. Vet. Inmunol. and Inmunop. 2002; 90: 1-10. [ Links ]
9. Green E., Tizard M., Moss M., et al. Sequence and characteristics of IS900, an insertion element identified in a human Crohn`s disease isolate of Mycobacterium paratuberculosis. Nucleid Acids Res. 1989; 17:9063-9073. [ Links ]
10. Harris N.B., Barletta R.G. Mycobacterium avium subsp. paratuberculosis in veterinary medicine. Clin. Microbiol. Rev. 2001; 14 (3):489-512. [ Links ]
11.Jolly A., Colavecchia S.B., Fernández B., et al. Antibodies induced by lipoarabinomannan in bovines: characterization and effects on the interaction between Mycobacterium avium subsp. paratuberculosis and macrophages in vitro. Vet. Med. Int. 2011: 1-8. [ Links ]
12. Jorgensen JB. 1982. An improved medium for culture of Mycobacterium paratuberculosis from bovine faeces. Acta Vet Scand. 23(3):325-35. [ Links ]
13. Koets A.P., Rutten V.P., de Boer M., Bakker D., Valentin-Weigand P., van Eden W. Differential changes in heat shock protein-, lipoarabinomannan-, and purified protein derivative-specific immunoglobulin G1 and G2 isotype responses during bovine Mycobacterium avium subsp. paratuberculosis infection. Infect. Immun. 2001; 69, 3:1492-1498. [ Links ]
14. Li L. Bannantine JP, Zhang Q, Amonsin A, May BJ, Alt D, Banerji N, Kanjilal S, Kapur V. The complete genome sequence of Mycobacterium avium subsp. paratuberculosis. Proc Natl Acad Sci U S A. 2005; 102(35):12344-9. [ Links ]
15. Marcoppido, G.A. Anticuerpos pasivos lactogénicos: moduación de la respuesta inmune y capacidad protectora frente a la diarrea por Rotavirus en un modelo ternero. Tesis Doctoral. Facultad de Ciencias Veterinarias. Universidad de Buenos Aires. 2007. [ Links ]
16. Merkal R.S., Richards W.D. Inhibition of fungal growth in the cultural isolation of mycobacteria. Appl Microbiol. 1972; 24(2):205-7. [ Links ]
17. Mundo, S.L., Fontanals A.M., García M., et al. Bovine IgG1 antibodies against Mycobacterium avium subsp. paratuberculosis protein p34-cx improve association of bacteria and macrophages. Vet Res. 2008; 39(1):6. [ Links ]
18. Mundo S.L. Tesis Doctoral. Facultad de Farmacia y Bioquímica. Universidad de Buenos Aires. 2005. [ Links ]
19. Paolicchi F. Paratuberculosis: aspectos clínicopatológicos y su impacto en la producción (Parte 1). XXXII Jornadas Uruguayas de Buiatría, 2004, p. 127, Paysandú, Uruguay. [ Links ]
20. Passucci JA y col. Análisis económico del saneamiento de paratuberculosis en un rodeo de cría bovina. Revista Argentina de Producción Animal. 2007; 27(supl. 1): 337-8. [ Links ]
21. Sambrook J., Fritsch E.F., Maniatis T., Molecular cloning: a laboratory manual. Cold Spring Harbor Laboratory, Nueva YorK, USA. 1989. [ Links ]
22. Stabel J.R. Cytokine secretion by peripheral blood mononuclear cells from cows infected with Mycobacterium paratuberculosis. Am. J. Vet. Res. 2000; 61:754-760. [ Links ]
23. Vanden Bush, Rosenbusch R.F. Characterization of the immune response to Mycoplasma bovis lung infection. Veterinary Immunology and Immunopathology. 2003: 94: 23-33. [ Links ]
24. Williams A., Reljic R., Naylor I., et al. Passive protection with immunoglobulin A antibodies against tuberculous early infection of the lungs. Immunology. 2004; 111:328-333. [ Links ]
25. Yokomizo Y., Merkal R.S., Lyle P.A., Enzymelinked immunosorbent assay for detection of bovine immunoglobulin G1 antibody to a protoplasmic antigen of Mycobacterium paratuberculosis, Am. J. Vet. Res. 1983; 44:2205-2207. [ Links ]














