Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO  uBio
uBio
Compartir
InVet
versión On-line ISSN 1668-3498
InVet vol.17 no.1 Ciudad Autónoma de Buenos Aires jun. 2015
ARTÍCULO DE INVESTIGACIÓN
Farmacocinética comparativa de una preparación de duración prolongada de amoxicilina luego de su administración por vía subcutánea e intramuscular a caninos
Porta, N.1; Prados, AP.1; Kreil, V.1; Tarragona, L.1; Monfrinotti, A.1; Rebuelto, M.1
1Cátedra de Farmacología, Facultad de Ciencias Veterinarias, UBA. Chorroarín 280 (1427) CABA.
Correspondencia e-mail: Porta Nicolás porta.nicolas@gmail.com
Recibido: 28/11/2014
Aceptado: 01/09/2015
Resumen
Se investigó la influencia de la vía de administración en la farmacocinética de la amoxicilina en caninos, luego de la administración por las vías subcutánea e intramuscular de 15 mg/kg de amoxicilina formulada como una suspensión acuosa de larga acción. Se tomaron muestras de sangre en tiempos predeterminados, y se calcularon los parámetros farmacocinéticos de las curvas de disposición para cada animal y para cada vía de administración. Se observaron diferencias significativas para los parámetros área bajo la curva (73.8 ± 13.1 mg.h/ml versus 88.3 ± 17.0 mg.h/ml) y tiempo medio de residencia (6.9 ± 2.8 h versus 10.3 ± 6.1 h) luego de las inyecciones intramuscular y subcutánea, respectivamente. La administración subcutánea mostró un mayor efecto depot que la intramuscular. No se observaron diferencias significativas para el tiempo sobre la concentración inhibitoria mínima para bacterias de baja (4 mg/ml) y alta (0.250 mg/ml) susceptibilidad a la amoxicilina. Nuestros datos sugieren que la formulación probada puede ser utilizada con un intervalo posológico prolongado de 48 h para bacterias muy susceptibles, y que ambas vías de administración proveen perfiles cinéticos similares, y por ende, similares resultados clínicos.
Palabras clave: Farmacocinética; Antibióticos; Betalactámicos; Aminopenicilinas; Perros.
Comparative pharmacokinetics of a long-acting amoxicillin formulation following its subcutaneous and intramuscular administration to dogs
Summary
The influence of the route of administration on the amoxicillin pharmacokinetics in dogs was investigated following the subcutaneous or intramuscular administration of 15 mg/kg amoxicillin formulated as a long-acting aqueous suspension. Serial blood samples were collected at predetermined times. Pharmacokinetic parameters were calculated from the disposition curves for both routes for each animal. Significant differences were observed for the parameters area under the curve (73.8 ± 13.1 mg.h/ml versus 88.3 ± 17.0 mg.h/ml) and mean residence time (6.9 ± 2.8 h versus 10.3 ± 6.1 h) following the intramuscular and subcutaneous injections, respectively. The subcutaneous administration exhibited higher depot effect than the intramuscular administration. No significant differences were observed for the time above the minimun inhibitory concentrations for bacteria of low (4 mg/ml) and high (0.250 mg/ml) amoxicillin sensitivity. Our data suggest that the tested formulation can be used with a prolonged interval of 48 h for high sensitivity bacteria, and that both routes of administration provide similar kinetic profiles and thus, similar clinical outcomes.
Key words: Pharmacokinetics; Antibiotics; Betalactams; Aminopenicillins; Dogs.
Introducción
La amoxicilina es frecuentemente utilizada en la clínica de los animales de compañía dado su espectro favorable, facilidad de administración y falta de toxicidad. Pertenece al grupo de los beta-lactámicos, y es activa contra algunas enterobacterias, como Escherichia coli, Proteus mirabilis y Salmonella spp.; y Haemophilus influenzae; contra algunos cocos gram positivos como estreptococos betahemolíticos y Staphylococcus aureus no productores de betalactamasa, y contra patógenos anaerobios como Clostridium perfringens. No presenta actividad antibacteriana sobre Pseudomonas aeruginosa1.
Estudios previos de eficacia antimicrobiana de antibióticos beta-lactámicos han demostrado que la persistencia de concentraciones séricas en niveles superiores a la concentración inhibitoria mínima (CIM) del patógeno causal está directamente relacionada a su eficacia clínica, dado que estos antibióticos ejercen una actividad bactericida tiempo-dependiente.2,3 El índice farmacocinético/farmacodinámico que predice mejor dicha eficacia es el tiempo durante el cual las concentraciones del antibiótico superan la concentración inhibitoria mínima de referencia (T>CIM). 2,3
Las características físico-químicas de la amoxicilina permiten la absorción de la droga tanto por la vía oral como parenteral, lo cual facilita su administración. En el mercado se encuentran distintas presentaciones (comprimidos, suspensiones orales, preparaciones inyectables convencionales y de larga acción), para poder satisfacer las necesidades de cada tratamiento clínico en particular.
Las preparaciones denominadas de larga acción, liberación prolongada o depot son muy importantes en medicina veterinaria ya que permiten alargar el intervalo entre aplicaciones, fundamental a la hora de proyectar un tratamiento y facilitar su cumplimiento. Así mismo, constituyen una vía segura de administración de la medicación, ya que las preparaciones orales no siempre resultan una vía accesible, sobre todo en animales indóciles. Como desventaja, estas preparaciones pueden causar dolor o generar reacciones tisulares en el punto de inyección, así como producir concentraciones plasmáticas de menor magnitud que los inyectables convencionales.4 En nuestro medio hay un preparado comercial de amoxicilina formulado como de liberación prolongada, para cuya administración en caninos y felinos se indican tanto la vía intramuscular como la subcutánea. Esto lleva a generar la duda, por parte del clínico, de si la vía de administración afectará la disposición del antibiótico en el organismo, ya que diversas situaciones de la práctica clínica pueden favorecer la administración por una u otra vía. Por ello, los objetivos de este estudio fueron describir y comparar en caninos sanos los perfiles farmacocinéticos y la eficacia clínica predicha, medida en T>CIM, de la amoxicilina, luego de la administración por vía intramuscular y subcutánea de un preparado comercial formulado para larga duración.
Materiales y métodos
Animales
En este estudio se incluyeron seis caninos adultos de raza Beagle, dos machos y cuatro hembras, con un peso de (media ± DE) 13,5 ± 1,5 kg, obtenidos de los caniles de la Facultad de Ciencias Veterinarias, Universidad de Buenos Aires. Los animales se encontraban en buen estado de salud determinado por exámenes físicos, análisis sanguíneos y urinarios. Ninguno de los caninos tenía antecedentes de alergia a betalactámicos. Este trabajo fue evaluado y aprobado por el Comité Institucional de Cuidado y Uso de Animales de Laboratorio (CICUAL) de la Facultad de Ciencias Veterinarias, UBA.
Protocolo
En ambas experiencias los tratamientos fueron administrados entre las 8.30 y las 9.30 h, y cada animal fue pesado para el cálculo de la dosis. La droga administrada fue amoxicilina trihidrato 15 mg/kg (suspensión acuosa, 150 mg/ml; Duphamox LA, Fort Dodge, Buenos Aires, Argentina) por vía subcutánea (s.c.), en parrilla costal (experiencia 1), y por vía intramuscular, en músculos dorsales (experiencia 2), con un período de lavado de 2 semanas entre cada experiencia. Se extrajeron muestras de sangre (2 ml) de las venas yugulares en tubos heparinizados en los siguientes tiempos: 0.16, 0.33, 0.50, 0.75, 1.00, 2.00, 4.00, 6.00, 8.00, 11.00, 24.00, 28.00 y 30.00 h luego de la administración de la amoxicilina. Las muestras fueron inmediatamente centrifugadas y el plasma fue conservado a -20ºC hasta su procesamiento dentro de las 48 h de obtenido.
Método analítico
Las concentraciones plasmáticas de la amoxicilina se midieron por triplicado mediante el método microbiológico previamente descripto por Bennet et al.5 utilizando Bacillus subtilis ATCC 6633 como cepa patrón. La curva estándar se realizó en un pool de plasma canino libre de antibiótico, y fue lineal para el rango de concentraciones 50.0 - 0.39 mg/ml (r= 0.9976). Las muestras incógnitas se sembraron simultáneamente con la curva estándar. El límite de cuantificación y de detección fue 0.39 mg/ml. El coeficiente de variación intra e inter-día y la exactitud, medida como desvío, del método fueron <10% en el rango de concentraciones estudiadas.
Análisis farmacocinético
Se utilizó el programa PCNONLIN (SCI Software, Lexington, KY, USA) para calcular los parámetros farmacocinéticos de la amoxicilina a partir de la curva concentración plasmática - tiempo mediante un análisis no compartimental y de acuerdo a las ecuaciones clásicas.6 La vida media de eliminación (t1/2λ) se obtuvo del cociente ln2/ λ, donde λ es la pendiente de la fase terminal de eliminación determinada por la regresión lineal de los últimos 4-5 puntos de la fase terminal de la curva de disposición. El área bajo la curva desde el tiempo 0 hasta la última concentración medida (ABC0-last) se calculó por la regla de los trapezoides lineales y fue extrapolada al infinito (ABC0-∞) de acuerdo a ABC0-last1 + Ct /λ, donde Ct es la última concentración medida. El tiempo medio de residencia (TMR) se calculó como ABCM/ ABC0/∞ donde ABCM es el área bajo la curva del producto del tiempo y concentración plasmática de la droga versus el tiempo desde el tiempo cero a infinito. Los valores calculados se expresan en media ± desvío estándar (DE).
El T>CIM se calculó gráficamente en horas para cada individuo y cada vía, tomando los valores de referencia de las CIM de 0.250 μg/ml como la CIM que incluye el 90% de bacterias susceptibles como los estreptococos beta-hemolíticos, Staphylococcus aureus no productores de beta-lactamasa, Clostridium perfringens y Haemophilus influenzae y 4.0 μg/ ml como la CIM representativa de bacterias de moderada susceptibilidad como Escherichia coli, Proteus mirabilis y Salmonella spp.1
Análisis estadístico
Los parámetros farmacocinéticos t1/2 λ, tmax, y TMR∞ y el T>CIM obtenidos luego de cada experiencia se compararon mediante el test de Wilcoxon. Para la comparación de Cmax, ABC0- last y ABC0-∞ se utilizó el test pareado, previa transformación logarítmica. Los cálculos se efectuaron mediante el programa GraphPad Prism (GraphPad Prism 3.0; GraphPad Software Inc., La Jolla, CA, EEUU). Se tomó p<0.05 como nivel de significación.
Resultados
La administración de la solución no ocasionó dolor en el sitio de inyección. No se observaron efectos adversos que se pudieran relacionar con el tratamiento.
Las curvas de concentraciones plasmáticas medias versus tiempo de administración para ambas experiencias se presentan en la Figura 1.
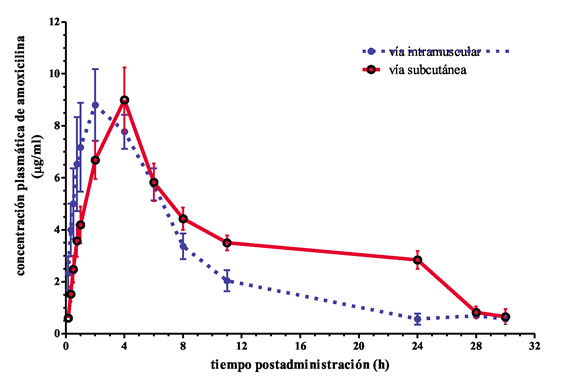
Figura 1. Concentraciones plasmáticas medias (± DE)obtenidas luego de la administración intramuscular (i.m.) y subcutánea (s.c.) de una dosis de amoxicilina (15mg/kg) a 6 caninos
Los valores de los parámetros farmacocinéticos se muestran en la Tabla 1, y los valores del T>CIM se observan en la Tabla 2. De los parámetros farmacocinéticos, solo se observaron diferencias significativas en el área bajo la curva y el tiempo medio de residencia. No se observaron diferencias significativas en los valores del T>CIM.
Tabla 1. Parámetros farmacocinéticos (media ± DE) calculados mediante el análisis no compartimental luego de la inyección intramuscular (i.m.) y subcutánea (s.c.) de 15 mg/kg de amoxicilina a seis caninos.

Diferentes superíndices indican diferencias significativas (p<0.05)
Tabla 2. Valores del tiempo sobre la concentración inhibitoria mínima (T>CIM) (media DE, coeficiente de variación) calculados luego de la inyección intramuscular (i.m.) y subcutánea (s.c.) de 15 mg/kg de amoxicilina a seis caninos

ns diferencias no significativas
Discusión
En este trabajo hemos estudiado la farmacocinética de la amoxicilina formulada como preparación de liberación retardada, luego de su administración por las vías i.m. y s.c. a caninos adultos. La dosis utilizada en ambas experiencias fue la indicada por el fabricante en el prospecto. El método microbiológico es apropiado para calcular las concentraciones plasmáticas de amoxicilina, ya que carece de metabolitos con actividad antibacteriana que puedan interferir con los valores de concentración de la droga madre7, y se ha determinado previamente una buena correlación entre los resultados obtenidos en la determinación de concentraciones de amoxicilina en fluidos biológicos mediante HPLC y el método microbiológico.8,9
La farmacocinética de la amoxicilina administrada por vía oral y parenteral ha sido previamente descripta en caninos.10-13 Sin embargo, hemos considerado útil realizar este estudio con un preparado comercial disponible en nuestro medio, ya que factores como la formulación y la vía y sitio de administración, pueden afectar la absorción y disposición de las drogas10,14,15. Esto es especialmente importante en los preparados de liberación retardada, ya que su absorción, al estar diseñados para liberación sostenida, suele ser más variable que la de los preparados convencionales. Dada la relación entre las concentraciones plasmáticas del antibiótico y su eficacia en la curación de infecciones en la clínica, variaciones en su perfil farmacocinético pueden comprometer el resultado de los tratamientos en la práctica clínica.
En nuestro estudio, el análisis de los valores de parámetros farmacocinéticos calculados para ambas vías mostró que este preparado comercial tiene una disposición similar cuando se da por vía i.m. y s.c., ya que no hubo diferencias significativas entre ellos, a excepción de las detectadas para el área bajo la curva y tiempo medio de residencia. La diferencia entre las áreas bajo la curva calculada para cada vía estuvo determinada por las mayores y más persistentes concentraciones plasmáticas obtenidas luego de la administración s.c. en la fase de eliminación del preparado. Los mayores valores de vida media de nuestros resultados en comparación con los previamente obtenidos en la administración intravenosa (1.2 ± 0.13 h,10) y oral (1.0 h11; 1.52 ± 0.2 h12; 1.2 ± 0.13 h13) indican un posible efecto flip-flop, característico de una prolongada fase de absorción (efecto depot de la formulación), y son similares a los reportados para una suspensión de trihidrato de amoxicilina en etiloleato administrada por vías s.c. e i.m. (rango 6.9 -11.1 h) 10.
Comparando nuestros parámetros indicativos de absorción con los obtenidos en un estudio previo que investigó la farmacocinética de la amoxicilina administrada por vía i.m. y s.c. con diferentes sitos de inyección, se observa que los valores de Cmax y área bajo la curva son similares, mientras que los tmax calculados en nuestro estudio son ligeramente menores a los reportados por estos autores. 10
El análisis de los parámetros indicativos de eficacia T>CIM demuestra que no hay diferencias entre ambas vías de administración, sin embargo cabe destacar que las concentraciones plasmáticas de amoxicilina son más altas y más variables para la vía s.c. Teniendo en cuenta que con el fin de obtener resultados clínicos exitosos se necesitan valores de T>CIM de al menos el 60% de la duración del intervalo posológico, aplicando nuestros datos podríamos sugerir que para bacterias de alta susceptibilidad como los cocos gram positivos (CIM = 0.250 mg/ml) sería indicado administrar este preparado cada 48 h, según lo indicado en el prospecto. Por el contrario, para bacterias poco susceptibles como los bacilos gram negativos (CIM = 4.0 mg /ml), el intervalo posológico indicado sería de 12 h para ambas vías. Esta recomendación, sin embargo, tiene la limitación de que nuestra experiencia fue desarrollada en animales sanos. En un estudio se determinó que la fiebre inducida mediante la administración de dosis diferentes de lipopolisacárido de E. coli afectaba la eliminación de la amoxicilina, aumentando la vida media en forma significativa (1.02 h en caninos control versus 1.51 h en caninos febriles) cuando la dosis de endotoxina era de 20 mg/kg, pero no cuando era de 2 mg/kg.11
Las referencias7,16 citan 10-20 mg/kg cada 8-12 h como la posología indicada para la administración de amoxicilina en caninos por vía oral e inyectable. Hemos demostrado que el preparado en estudio cumple en permitir un intervalo posológico prolongado de 48 hs para bacterias de alta susceptibilidad, siendo recomendable disminuir el intervalo para bacterias de menor susceptibilidad, y que ambas vías de administración recomendadas pueden ser utilizadas indistintamente, si bien se favorecería la vía subcutánea.
Agradecimientos: Este estudio fue realizado en el marco de los proyectos UBACYT 2011-2014, Proyecto 20020100100698, SCyT, Universidad de Buenos Aires.
Agradecemos a Pamela Quaine, Luis Ambros, Laura Montoya y al personal de los Caniles de la Facultad de Ciencias Veterinarias, UBA, la colaboración en la toma de muestras.
1. Prescott, J.F. Beta-lactam Antibiotics: Penam Penicillins. En Giguère, S.; Prescott, J.F.; Baggot, J.D.; Walker, R.D.; Dowling, P.M. (eds) Antimicrobial Therapy in Veterinary Medicine. 4th edn. Blackwell Publishing, Ames, Iowa, USA, 2006: pp 121-139 [ Links ]
2. Drusano, G.L. Antimicrobial pharmacodynamics: critical interactions of “bug and drug”. Nat Rev Microbiol. 2004; 2:289-300
3. Toutain, P.L.; Lees, P. Integration and modelling of pharmacokinetic and pharmacodynamic data to optimize dosage regimens in veterinary medicine. J Vet Pharmacol Ther, 2004; 27:467-477 [ Links ]
4. Delis, G.; Batzias, G.; Theodosiadou, E.; Kounenis, G.; Koutsoviti-Papadopoulou, M. Influence of the injection site on the pharmacokinetics of amoxicillin after intramuscular administration of a conventional and a long-acting formulation in sheep. J Vet Pharmacol Ther. 2009;32:457-464 [ Links ]
5. Bennet, J.V.; Brodie, J.L.; Benner, E.J.; Kirby, W.M.M. Simplified, accurate method for antibiotic assay of clinical specimens. Appl. Microbiol. 1966; 14:170-177 [ Links ]
6. Gibaldi, M.; Perrier, D. Farmacocinética. Editorial Reverté S.A., Barcelona, España. 1982: pp. 182-184 [ Links ]
7. Papich, M.G.; Riviere, J.E. β-lactam antibiotics: penicillins, cephalosporins, and related drugs. En: Riviere, J.E.; Papich, M.G.; Adams, H.R. (ed) Veterinary Pharmacology and Therapeutics. 9th ed. Willey-Blackwell, USA, 2009; pp 866-888
8. Foulstone, M.; Reading ,C. Assay of amoxicillin and clavulanic acid, the components of Augmentin, in biological fluids with high-performance liquid chromatography. Antimicrob Agents Chemother. 1982; 22:753-762 [ Links ]
9. Leroy, P.; Gavriloff, C.; Nicolas, A.; Archimbault, P.; Ambroggi, G. Comparative assay of amoxicillin by highperformance liquid chromatography and microbiological methods for pharmacokinetic studies in calves. Int. J Pharm, 1992; 82: 157-164 [ Links ]
10. ten Voorde, G.; Broeze, J.; Hartman, E. G.; van Gogh, H. The influence of the injection site on the bioavailability of ampicillin and amoxycillin in beagles, Vet Q, 1990; 12: 73-79 [ Links ]
11. Marier, J.F.; Beaudry, F.; Ducharme, M.P.; Fortin, D.; Moreau, J.P.; Massé, R.; Vachon, P. A pharmacokinetic study of amoxycillin in febrile beagle dogs following repeated administrations of endotoxin. J Vet Pharmacol Ther. 2001;24:379-383 [ Links ]
12. Vree, T.B.; Dammers, E.; Van Duuren E. Variable absorption of clavulanic acid after an oral dose of 25 mg/kg of Clavubactin and Synulox in healthy dogs. J Vet Pharmacol Ther. 2003;26:165-171 [ Links ]
13. Rebuelto, M.; Montoya, L.; Prados, A.P.; Kreil, V.; Quaine, P.; Monfrinotti, A.; Tarragona, L.; Hallu, R. Lack of interaction of metoclopramide on oral amoxicillin kinetics in dogs. J Vet Pharmacol Ther, 2011; 34:621-624 [ Links ]
14. Waxman Dova, S.; Albarellos, G.; Kreil, V.; Montoya, L.; Ambros, L.; Hallu, R.; Rebuelto, M. Comparative pharmacokinetics of an injectable cephalexin suspension in beef cattle. Res Vet Sci, 2008; 85:570-574 [ Links ]
15. Modric, S.; Martinez, M. Patient variation in veterinary medicine - Part II - Influence of physiological variables J Vet Pharmacol Ther, 2011; 34: 209-223 [ Links ]
16. Plumb, D.C. Manual de Farmacología Veterinaria. 6ª ed. Editorial Intermédica. Buenos Aires, Argentina. 2010, pp 64-66 [ Links ]














