Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de neurocirugía
versión On-line ISSN 1850-1532
Rev. argent. neurocir. v.23 n.1 Ciudad Autónoma de Buenos Aires ene./mar. 2009
Tratamiento endovascular de aneurismas cerebrales asintomáticos. Análisis de una serie de 118 casos
Miguel Robles, Luis Lemme-Plaghos, Silvia Garbugino, Walter Casagrande, Julio Fernández
Centro Endovascular Neurológico de Buenos Aires. Buenos Aires, Argentina
Correspondencia: roblesneuro@hotmail.com
Recibido: enero 2009;
aceptado: febrero 2009
RESUMEN
Objetivo. Analizar los resultados de una serie de aneurismas cerebrales asintomáticos tratados mediante técnica endovascular y discutir las indicaciones del tratamiento.
Material y método. Se realizó un análisis retrospectivo descriptivo de una serie de 96 pacientes con 118 aneurismas de hallazgo incidental que fueron abordados por vía endovascular para la embolización del aneurisma con espirales ("coils") o con técnica de "coils" asistida por encamisado ("stent"), en un período de cuatro y medio años.
Resultados. Ciento quince aneurismas pudieron ser tratados con una tasa de oclusión suficiente para prevenir el sangrado del 78%, observándose en 15 (12.7%) de los procedimientos complicaciones que causaron morbilidad definitiva en 3 (3.1%) pacientes y mortalidad en dos (2.1%). Uno (0.8%) de los aneurismas sangró a la hora post procedimiento.
Conclusión. La embolización de aneurismas no rotos esta asociada a baja morbilidad y mortalidad en comparación con comunicaciones recientes referidas a historia natural y resultados de la cirugía convencional. De todas maneras la decisión de tratar un aneurisma incidental dependerá de cada caso en particular y habrá que tener en cuenta los factores dependientes del paciente, (edad, estado clínico y la perspectiva de vida del mismo), factores inherentes al aneurisma (tamaño, forma, localización y crecimiento del mismo) así como también factores inherentes al equipo tratante (experiencia y resultados)
Palabras clave: Aneurismas cerebrales; Aneurismas incidentales; Embolización.
ABSTRACT
Objective. To analyze results in a series of unruptured aneurysms treated with endovascular technique and discuss the indication for treatment.
Material and methods. Retrospective analysis of a series of 118 unruptured aneurysms in 96 patients treated by embolization with coils or stent assisted coils during four and a half year period.
Results. One hundred and fifteen aneurysms were successfully embolized with 78% of total or almost total occlusion rate. Fifteen procedural (12.7%) complications occurred causing definite mobidity in 3 (3.1%) patients and two (2.1%) deaths. One of the embolized aneurysms (0.8%) bled one hour after the precedure.
Conclusion. Embolization of unruptured aneurysms is associated to low morbidity and mortality rates in comparison with most recent reports on natural history and open surgery results. Anyhow treatment indication will depend on the analysis of patient qualification (age, clinical status, life expectancy), aneurysm characteristics (size, shape, location and growth rate) as well as surgical team experience.
Key words: Cerebral aneurysms; Embolization; Incident aneurysms
INTRODUCCIÓN
La incidencia de aneurismas intracraneales no rotos (ANR) en adultos oscila entre el 1 y el 4% de la población1 y su diagnóstico cobra importancia ya que la complicación más temida es la hemorragia subaracnoidea (HSA), la cual está asociada a un 40 a 50% de mortalidad2.
Su diagnóstico se ha incrementado debido a los estudios neurorradiológicos no invasivos con los que se cuenta en la actualidad como son la angioTC y la angioRM, planteando un dilema en cuanto a su indicación terapéutica3.
La indicación de su tratamiento preventivo deberá efectuarse sólo luego de la evaluación de los riegos de morbimortalidad, que deberán ser menores a los de su historia natural2.
El tratamiento endovascular de los aneurismas con "coils" y la reconstrucción arterial con "stent" en aneurismas de cuello ancho, es una alternativa terapéutica valiosa para los aneurismas intracraneales4; con respecto a ella los resultados del estudio ISAT5 ya demostraron que en aneurismas rotos, posibles de ser tratados tanto por cirugía como por embolización, esta última ofrece mayores posibilidades de supervivencia libre de incapacidad a un año.
MATERIAL Y MÉTODOS
De una serie de 575 aneurismas consecutivos tratados por el equipo del Centro Endovascular Neurológico Buenos Aires entre mayo del 2003 y diciembre del 2007 se tomaron los 209 ANR, los cuales se clasificaron siguiendo a E. Spagnuolo6 en: a) incidentales (diagnóstico casual); b) testigos (presentes en HSA de otro aneurisma sin ser causantes de la misma) y c) sintomáticos (sintomatología y/o signología neurológica no hemorrágica). Estos últimos fueron excluidos de nuestro análisis por no ser causa de discusión de tratamiento ya que, como sabemos, para todo aneurisma sintomático sería recomendable el tratamiento1.
La muestra de este análisis quedó integrada entonces por aquellos aneurismas incidentales y aquellos aneurismas testigos asociados a HSA que fueran tratados con posterioridad a los 6 meses de producida la hemorragia del otro aneurisma. Se tomó como parámetro este lapso de espera posthemorragia teniendo en cuenta que las condiciones clínicas difieren de un cerebro sano al de uno que cursa concomitantemente con una HSA, la cual aumenta la morbimortalidad tanto por la historia natural de la enfermedad como por los fenómenos trombóticos asociados a la hemorragia, que juegan un papel en contra de la técnica de embolización endovascular.
Se excluyeron de la muestra los aneurismas intracavernosos por ser los mismos extradurales, lo que hace que la histología de su pared y su ubicación anatómica difiera de los aneurismas subaracnoideos y por consiguiente también su comportamiento y conducta terapéutica, y los aneurismas gigantes por ser el objetivo de este trabajo los aneurismas saculares asintomáticos y los gigantes en su mayoría son sintomáticos, además de presentar características fisiopatológicas que llevan a una conducta de tratamiento diferente.
El análisis retrospectivo descriptivo efectuado fue realizado sobre el abordaje de 118 aneurismas en 96 pacientes, de los cuales 73% fueron de sexo femenino y 27% masculino, con edad promedio de 53,1 años.
El 78,8% de los 118 aneurismas fueron incidentales siendo el motivo de consulta más frecuente la cefalea inespecífica no relacionada con la existencia del aneurisma y el 21,2% fueron aneurismas testigos asociados a HSA de más de 6 meses de evolución y sin secuelas neurológicas al momento del tratamiento. El 6,7% de los aneurismas estaban asociados a malformación arteriovenosa, siendo dos de los aneurismas por hiperflujo y cuatro sin relación con el eje vascular de la misma. El 27,1% de los casos fueron aneurismas múltiples.
A los fines del análisis se consideró cada aneurisma individualmente como un caso para establecer efectividad y complicaciones del método, mientras que la morbilidad y mortalidad fueron relacionadas con el número de pacientes.
De acuerdo con su localización, el 91,5% de los aneurismas se localizaba en el circuito anterior y el 8,5% en el circuito posterior (Tabla 1)
Tabla 1. Topografía de los aneurismas de circulación anterior y circulación posterior

Morfológicamente los aneurismas fueron clasificados siguiendo el estudio de ISAT5 en: a) pequeños (tamaño menor a 10 mm) y b) grandes (entre 10 mm y 25 mm) La relación entre las medidas del saco y del cuello aneurismático se clasificó tomando como límite 4 mm el diámetro del cuello en: a) saco pequeño con cuello pequeño, b) saco grande con cuello pequeño, c) saco pequeño con cuello grande, d) saco grande con cuello grande (Tabla 2).
Tabla 2. Relación entre saco y cuello aneurismático

La oclusión obtenida por embolización se clasificó en: Grado A) total (sin evidencia angiográfica de opacificación de aneurisma); Grado B) subtotal (opacificación del cuello ocupado por "coils" en un 95 al 99%); Grado C) incompleta (superior al 90%) y Grado D) parcial (menor al 90%)5. Se consideró oclusión suficiente para prevenir el sangrado a los grados A y B.
Se realizaron controles angiográficos diferidos a los 3 y 12 meses postembolización en el 76% de los casos, los que permitieron observar la evolución de la oclusión inicial.
RESULTADOS
Se realizaron 118 procedimientos de los cuales 3 (2,5%) fueron discontinuados: 2 por incontinencia del cuello sin factibilidad de colocación de "stent" y uno por originarse del saco aneurismático un ramo silviano derivándose el caso a cirugía. Por lo tanto, la efectividad del abordaje endovascular fue del 97,5%.
De los 115 aneurismas tratados el 81% fueron embolizados exclusivamente con "coils" y en el 19% se utilizó la técnica de "stent" en la arteria portadora debido a la incontinencia del cuello aneurismático seguido de "coils" intrasaculares.
La oclusión inicial de los 115 casos fue: grado A (total) en el 34,8% de los casos, grado B (subtotal) en el 43,5% de los casos, grado C (parcial) en el 17,4% de los casos y grado D (incompleta) en el 4,3% de los casos. Por lo tanto se consideró que la oclusión inicial suficiente para prevenir el sangrado fue del 78,3%.
Se realizaron controles angiográficos a los 3 y 12 meses en 87 aneurismas, observándose oclusión estable en un 42,5%, progresión de la oclusión en un 38% y compactación en un 19,5% (Tabla 3). En estos estudios de control angiográfico la oclusión suficiente para prevenir un sangrado fue del 78% (Figs. 1, 2 y 3). Los casos retratados fueron 12 (10,1%), por presentar oclusión C y D consideradas insuficientes para prevenir el sangrado (Fig. 4).
Tabla 3. Resultados de seguimiento angiográfico diferido (3 a 12 meses)

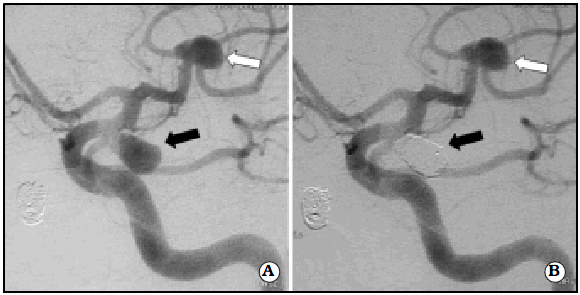
Fig. 1. A. Aneurismas cerebrales múltiples, aneurisma comunicante posterior sacular izquierdo (flecha negra) y aneurisma displásico de la trifurcación silviana con origen de ramas en el cuello del mismo (flecha blanca). B. Control angiográfico diferido muestra oclusión completa estable del aneurisma embolizado (flecha negra). El aneurisma silviano no fue tratado por riesgos de oclusión de ramas.
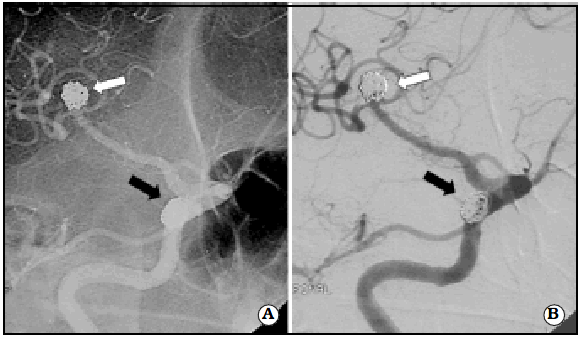
Fig. 2. Angiografía digital no sustraída de control angiográfico diferido de aneurismas cerebrales múltiples. A. Aneurisma comunicante posterior sacular derecho (flecha negra) y aneurisma sacular de la trifurcación silviana (flecha blanca). B. Mismo control angiográfico con imágenes sustraídas confirma la oclusión completa del aneurisma comunicante posterior (flecha negra) y mínima entrada de contraste en el cuello del aneurisma silviano (flecha blanca).
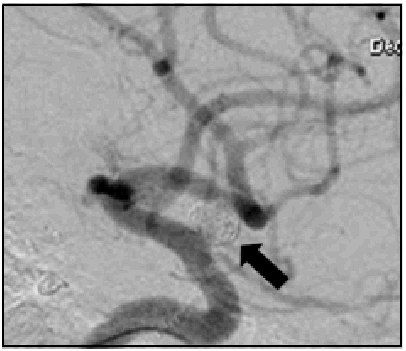
Fig. 3. Angiografía digital de control angiográfico diferido de aneurisma sacular del segmento oftálmico de la a. carótida interna derecha: se observa mínima compactación de los "coils" con ligera irregularidad en la pared de implantación del saco (flecha).
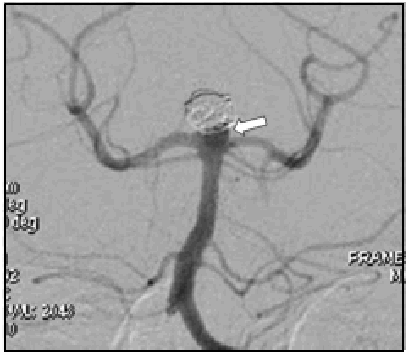
Fig. 4. Angiografía digital en incidencia frente para control angiográfico diferido de aneurisma sacular del tope de la arteria basilar: se observa persistencia de cuello aneurismático por compactación de los "coils" hacia el fondo del saco (flecha).
De los 118 procedimientos realizados hubo 15 (12,7%) en los cuales se presentaron complicaciones durante el mismo (Tabla. 4). Estas fueron:
Tabla 4. Complicaciones durante los procedimientos

a) Ruptura aneurismática: 4 casos (3 con hemorragia controlada por embolización sin repercusión clínica, 1 caso en el cual la ruptura de la punta del microcatéter dañó el cuello del aneurisma provocando una hemorragia masiva la cual fue controlada con la oclusión del vaso portador falleciendo el paciente a los 4 días).
b) Trombosis: 2 casos de oclusión del vaso portador (1 caso donde por movilización el cast de coils ocluyó la luz carotídea lo que provocó la trombosis de la misma con infarto hemisférico derecho falleciendo la paciente a las 48 hs; el otro caso por trombosis de ramo calcarino de arteria cerebral posterior izquierda quedando el paciente con hemianopsia definitiva) y 6 casos de oclusión de ramos distales (sin repercusión clínica).
c) Disección de vaso durante el abordaje: 2 casos (1 carotídeo y 1 femoral sin repercusión clínica).
d) Luxación del stent en boca del aneurisma: 1 caso (sin repercusión clínica).
Las complicaciones postprocedimiento se observaron en 8 casos (6,7%) (Tabla 5).
Tabla 5. Complicaciones postprocedimientos

a) Isquemia confirmada por TAC: 5 casos (3 casos cursaron con hemiparesia y afasia transitorias y 2 casos sin repercusión clínica)
b) Sangrado: 1 caso (paciente con deterioro del sensorio una hora postembolización que se realiza TAC de cerebro que muestra HSA en cisterna perimesencefálica; la angiografía no evidenció causa de sangrado y la paciente quedó con parafasia definitiva)
c) Hematoma en el sitio de punción: 1 caso en el músculo psoas sin repercusión clínica.
d) Estenosis de segmento supraclinoideo carotídeo derecho asociado en respuesta a la colocación de Stent sin repercusión clínica.
Por tanto la morbilidad total inherente al procedimiento considerando la muestra de 96 pacientes fue de 8 (8,3 %) casos dividiéndose en:
a) Transitoria: 5 (5,2%) casos (3 hemiparesia y afasia y 2 casos de hemiparesia).
b) Definitiva: 3 (3,1 %) casos (1 caso de hemiparesia, 1 caso de hemianopsia y 1 caso de parafasia).
La mortalidad en esta serie de 96 pacientes fue de 2 (2,1%) casos: uno por la ruptura aneurismática durante el procedimiento y otro secundario a luxación de coils con trombosis carotídea ya referidos. Si estimamos la mortalidad por número total de aneurismas tratados la misma es de 1,7%.
DISCUSIÓN
La incidencia de aneurismas cerebrales es relativamente alta: estudios clínicos y de autopsias indican que entre el 1 y el 4%1 de la población es portadora de ANR y su diagnóstico casual va en incremento con las nuevas técnicas neurorradiológicas disponibles como la tomografía computada (TAC), la resonancia magnética (IRM) y los estudios angiográficos no invasivos como son la angioRM y la AngioTAC. Este aumento de casos en la consulta diaria motiva actualmente la búsqueda de respuestas en cuanto a la conducta a seguir. Por este motivo diferentes estudios clínicos han abordado el tema, tanto para el mejor conocimiento de la historia natural de los aneurismas como para definir con mayor exactitud cuáles serían los niveles aceptables de morbilidad y mortalidad de su tratamiento quirúrgico en la actualidad.
Si bien se ha publicado que el riesgo de sangrado de estos aneurismas es de 0,15 a 8,6 % anual1 difiriendo según el tamaño y localización (Tabla 6), y a pesar de que la morbimortalidad por ruptura aneurismática es elevada, la indicación de un tratamiento preventivo en ANR aún sigue siendo tema de controversia, debido a que los resultados de un tratamiento quirúrgico no siempre son satisfactorios.
Tabla 6. Riesgo de ruptura al año en ANR (ISUIA: 2003). Se han excluido los aneurismas intracavernosos

En el año 1998, se publicó el trabajo conocido como ISUIA (International Study of Unruptured Intracraneal Aneurysms, Componente retrospectivo 1970-1991)7, efectuado por un grupo multicéntrico de investigadores referido a la evolución de los aneurismas intracraneales sin ruptura, los riesgos de ruptura y los riesgos de la intervención quirúrgica que incluía 2.621 pacientes de 53 centros con un seguimiento de 7,5 años. De acuerdo a los resultados del ISUIA, el riesgo de ruptura de aneurismas menores a 10 mm sin antecedentes de HSA previa era de 0,05% y se incrementaba diez veces (0,5%) en pacientes con historia de HSA por ruptura de otro aneurisma coincidente. Estas cifras se incrementaban significativamente para los aneurismas mayores a 10 mm que presentarían un riesgo de ruptura anual de 1%. El ISUIA también concluye que era improbable que la cirugía convencional redujera las tasas de incapacidad y muerte en pacientes portadores de ANR menores a 10 mm y sin antecedentes de HSA previa.
Su publicación generó importantes debates como el de J. Ausman8 cuando criticó estas conclusiones haciendo referencia que en el estudio no se había tenido en cuenta que no todos los ANR son iguales en cuanto a forma, tamaño y localización, por consiguiente el riesgo de ruptura debía diferir entre estos aneurismas.
Por otro lado era obvio que el estudio retrospectivo del ISUIA no había incluido a la embolización como una tercera alternativa, ya que la misma no era una práctica existente en los años 70 y 80, lo que hacía que sus conclusiones con respecto a los resultados del tratamiento activo de los ANR perdiera vigencia al momento de la publicación. Para ese momento esta nueva alternativa de tratamiento endovascular, había adquirido gran auge y se había demostrado un 98% de efectividad en evitar el sangrado cuando se lograba la exclusión del saco aneurismático3.
Otros estudios publicados posteriormente comunicaron cifras aún mayores. Rinkel9 en 1998 informó que la incidencia de ruptura en pacientes portadores de aneurismas coincidentes (testigos) era aún mayor llegando al 1 a 2% anual, siendo la hipertensión arterial y la multiplicidad aneurismática factores que aumentarían el riesgo de ruptura mientras que Juvela et al10, en el año 2000 publicaron una tasa promedio anual de ruptura de 1,3% en 181 ANR seguidos por una media de 19,7 años. Estas series con cifras de riesgo mucho más elevadas en comparación con las informadas por el ISUA motivaron los comentarios de J. Ausman.
A fines del 2003 se comunicaron los resultados de la segunda parte del estudio ISUIA (componente prospectivo 1991-1998)11, el cual trabajó sobre dos cohortes: la primera que incluyó los ANR no tratados por ser de bajo riesgo (localización anterior, tamaño aneurismático menor a 12 mm) y la segunda cohorte los ANR que por ser de alto riesgo (localización posterior, tamaño mayor a 12 mm) habían sido tratados ya fuere por cirugía convencional o por vía endovascular. A su vez se subdividió a esta última cohorte de aneurismas tratados en ANR con historia previa de HSA (por ruptura de aneurisma coincidente) y en ANR sin historia previa de HSA, esto teniendo en cuenta que el riesgo de ruptura para un aneurisma testigo como mencionáramos previamente, es mucho mayor que para un aneurisma incidental.
Este nuevo informe arrojó porcentajes de riesgos de ruptura mucho más elevados que en la primera fase cuyo riesgo de ruptura para aneurismas sin historia previa de HSA era de 0,05% mientras que en la segunda fase el riesgo de ruptura para aneurisma sin historia previa de HSA aumentaba al 0,4 % (Tablas 6 y 7). Con estos resultados el ISUA prospectivo varió las conclusiones previas diciendo que la indicación de tratar un ANR se debía tomar teniendo en cuenta cada caso en particular, sugiriendo conducta conservadora en aquellos aneurismas menores a 7 mm de circuito anterior no asociados a HSA por su baja tasa de probabilidad de sangrado, y que los pacientes de 50 años o menos con aneurismas de circuito posterior de un tamaño entre 7 y 24 mm se beneficiarían con el tratamiento del mismo ya fuere por cirugía convencional o cirugía endovascular.
Tabla 7. Riesgo de ruptura a los 5 años en ANR (ISUIA: 2003). Se han excluidos los aneurismas intracavernosos por ser extradurales

La idea que dejó la segunda comunicación del ISUIA es que la tasa de ruptura de los ANR, si bien mayor que en la primera, aún es baja, pero un detenido análisis efectuado por H. Fontana12 sobre el grupo de historia natural de ANR no tratados observó que en la evolución de estos ANR el riesgo de HSA acumulativo a los 4,1 años era del 5% (1,21% anual) y la mortalidad por esta causa era del 3,2% (0,78% anual). También observó que casi el 36% de este grupo recibió tratamiento no especificándose los motivos por los cuales se decidió dicha conducta. El análisis de este grupo de historia natural de ANR no tratados nos lleva a la conclusión de que, aunque se los quiera dejar evolucionar sin tratamiento, casi la tercera parte de ellos recibirán tratamiento, con un riesgo de sufrir una HSA del 5% acumulativo a los 4,1 años, con una mortalidad acumulativa anual del 3,2%12.
Una vez adoptado el criterio de llevar a cabo el tratamiento se deberá elegir si el mismo se debe efectuar por vía convencional a cielo abierto para el clipado del aneurisma o bien la vía endovascular para la embolización del saco malformativo: la elección deberá surgir fundamentalmente en base a la evidencia científica existente acerca de los resultados de cada una y de la capacidad del equipo neuroquirúrgico actuante en llevarla a cabo.
Con respecto a las alternativas terapéuticas, la Asociación Americana del Corazón (American Heart Association) en su comunicación "Recomendaciones para tratamiento endovascular de aneurisma intracraneanos" ya concluyó que la tasa combinada de morbimortalidad del tratamiento quirúrgico de ANR es de 15,2% a un año o 9% si se limita a incapacidad moderada, mientras que para aquéllos tratados mediante técnicas endovasculares es de 8,1% o 2,8% si se limita a incapacidad moderada13. Estos resultados de la vía endovascular coinciden con series publicadas por Goddard2, Johnston14, Roy15 y Garbugino3 sobre el tratamiento de ANR.
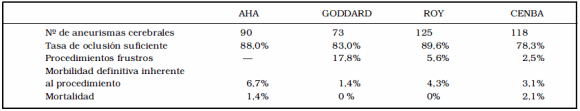
Comparando los beneficios de las dos alternativas terapéuticas el trabajo cooperativo de California13, donde se analizan los resultados de 2.069 pacientes portadores de ARN tratados mediante cirugía o embolización, observó una incidencia de evoluciones adversas del 25% en los pacientes operados en contraposición al 10% de los pacientes embolizados y las tasas de mortalidad fueron 3,5% y 0,5% para el grupo quirúrgico y endovascular respectivamente. En nuestra serie la tasa de morbilidad definitiva y mortalidad inherente al procedimiento fue del 3% y 1,7% respectivamente, semejantes a las informadas en el ISUIA (Componente Prospectivo) que arrojó una tasa de mortalidad del 1,7% y una tasa de morbilidad del 2,2% en los aneurismas tratados por técnica endovascular. En lo referente al grado de oclusión para prevenir ruptura aneurismática nuestra tasa fue del 78,3% (Tabla 8).
Tabla 8. Resultados comparativos de nuestra serie con otras del tratamiento endovascular de aneurismas no rotos
En base al análisis de nuestros resultados, coincidimos con las pautas terapéuticas propuestas por R. Komotar1 para el manejo de los ANR quien propone:
1) aneurismas incidentales menores de 5 mm deberían ser manejados conservadoramente;
2) aneurismas incidentales mayores de 5 mm en pacientes de hasta 60 años de edad debería considerarse seriamente el tratamiento del mismo;
3) aneurismas incidentales mayores de 10 mm en pacientes de hasta 70 años de edad deberían ser tratados.
Además el autor propone tener en cuenta que el crecimiento (menor 1 mm), forma (multilobulado), condiciones genéticas previas (poliquistosis renal, Marfan, Ehlen Danlos) y antecedentes de HSA (por ruptura de otro aneurisma asociado), incrementan el riesgo de ruptura. Otros autores consultados coinciden con esta postura observándose similitud con nuestras indicaciones respecto al manejo de los ANR16-19.
CONCLUSIONES
La bibliografía consultada y nuestra propia experiencia nos indican que el manejo de los ANR es un tema muy especial dentro de la neurocirugía ya que si bien se trata de pacientes con una patología potencialmente letal, se encuentran asintomáticos, lo que hace más desafiante la indicación de su tratamiento, así como controvertida la técnica a utilizar para este último.
Teniendo en cuenta la alta morbilidad y mortalidad que genera la HSA aneurismática y el riesgo anual y acumulativo de sangrar que tienen estos aneurismas con la consiguiente disminución de expectativa de vida en el portador de esta malformación vascular, coincidimos con la bibliografía actual que la mayoría de los aneurismas no rotos deberían ser tratados en forma preventiva, aun conociendo los riesgos de dicho tratamiento por menos invasivos que sean éstos.
De todas maneras recalcamos que la decisión de tratar un ANR dependerá de cada caso en particular y al momento de tomarla habrá que tener en cuenta por un lado factores dependientes del paciente como son su edad, estado clínico y su perspectiva de vida. Por otro lado están los factores inherentes al aneurisma como son tamaño, forma, localización y crecimiento del mismo, ya que el riesgo de ruptura difiere para cada caso en particular. Cabe aclarar que el factor psicológico del paciente al saber la gravedad de su patología, puede influir en la conducta a favor del tratamiento.
La experiencia y los resultados del equipo tratante también deben ser tenidos en cuenta al momento de optar por una conducta en la que los riesgos de morbimortalidad inherentes al tratamiento por este equipo deben ser menores que los propios de la historia natural de la enfermedad.
COMENTARIOS
Estos son resultados de un grupo que trabaja seriamente en nuestro medio y que presenta sus números reales en forma meticulosa y merece nuestro reconocimiento tanto por la calidad del trabajo asistencial y la honestidad científica, como por la envidiable experiencia que exponen a nuestra consideración.
Los autores analizan retrospectivamente los resultados del tratamiento endovascular de los aneurismas no rotos de su serie, luego de descartar aquellos que eran sintomáticos y los intracavernosos. Quedaron de esta manera, para el análisis, 118 aneurismas en 96 pacientes, encontrándose aneurismas múltiples en el 10% de dicha población.
El procedimiento fracasó en tres casos (2,5%), dos por incontinencia del cuello y uno por salida de un ramo silviano del saco aneurismático.
La oclusión total del aneurisma se alcanzó en casi el 35% de los casos, y la subtotal en el 43,5%, lo que hace que en el 78,5% el resultado haya sido considerado seguro en cuanto a la supresión del riesgo de sangrado. En el 17,4% se obtuvo un relleno parcial y en 4,3%, incompleto. En 24 pacientes (20%) no se pudo realizar ningún control post embolización.
En los que fueron controlados (72 pacientes con 87 aneurismas), la incidencia de retratamiento fue del 10,1% luego de controles angiográficos realizados entre los 3 y 12 meses después del tratamiento inicial.
La mortalidad del procedimiento fue del 2,1% si se analiza por número de pacientes y del 1,7% si se analiza por número de aneurismas tratados.
La morbilidad transitoria fue del 5,2% y la definitiva del 3,1 %. Entre estos pacientes los autores mencionan uno con parafasia.
Parafasia es un síntoma lingüístico dentro del complejo sintomático de las afasias que consiste en cambiar una palabra o denominación por otra, fonológica o semánticamente parecida. Es decir, el paciente presenta una afasia (quizá anómica en el caso comentado).
Respecto a sus resultados, los autores reconocen honestamente que en tres pacientes no se pudo realizar el procedimiento y en aproximadamente el 20 % del total, el tipo de relleno obtenido no fue considerado suficiente para impedir el sangrado, no pudiéndose resolver el problema por el cual el paciente fue intervenido.
Es posible que un análisis previo más profundo de las angiografías en relación a la geometría propia del aneurisma así como su relación con el vaso portador, sea la clave para tomar la decisión de hacer el tratamiento por vía endovascular o por microcirugía. Este debería ser un precepto tanto para el neurocirujano general antes de enviar el paciente a ser tratado por vía endovascular, como un motivo de modestia para el endovascular que quisiera tratar todo por la vía que maneja. Según las cifras presentadas por los autores, alrededor de una cuarta parte de los aneurismas intracraneanos no rotos, no deberían ser tratados por esta vía, si la selección de los pacientes se hace correctamente. Es posible, a su vez, que algunos de estos, sean también los más complejos para tratar por abordaje microquirúrgico.
La aparición de una estenosis carotídea a nivel del stent, aunque asintomática, nos hace pensar que es posible que estos dispositivos alteren en forma nada despreciable la hemodinamia no sólo del aneurisma, sino de la misma arteria portadora y de su territorio distal. Investigaciones profundas tanto clínicas como experimentales podrán determinar en un futuro, cuáles son las mejores condiciones para un encamisado arterial cerebral más allá del tamaño del cuello del aneurisma y su relación con el del saco.
Coincidimos con los autores acerca de la conducta de operar la mayoría de los aneurismas no rotos de más de 4 mm de diámetro, según nuestro criterio. En caso de duda o aumento del riesgo por padecimientos concomitantes, nuestra clasificación1 según el aspecto, en aneurismas quiescentes, en crecimiento o en degeneración, podría ayudar en la toma de decisión.
Por último, debemos preguntarnos si un período de control de 1 año, es suficiente para asegurarnos el resultado final de la embolización aneurismática. En el seguimiento del ISAT2, se observó que aneurismas totalmente ocluidos con coils, pueden recanalizarse tardíamente y requerir re tratamiento en un nada despreciable 5,8%, dentro de un período de tres años. La garantía de durabilidad del tratamiento en una terapia preventiva, adquiere especial trascendencia. Se sugiere a los autores revisar la estabilidad de la oclusión a largo plazo, en esta importante serie.
Héctor M. Belziti.
Horacio J. Fontana
Hospital Central de San Isidro
1. Fontana H, Belziti, H, Requejo, F, Buratti, S, Recchia, M. La circulación cerebral en condiciones patológicas. El aneurisma. Rev Argent Neuroc 2008; 22: 35-46.
2. Campi A, Ramzi, N, Molyneux, AJ, Summers, PE, Kerr, RSC, Sneade, M, Yarnold, JA, Rischmiller, J, Byrne, JV. Retreatment of ruptured cerebral aneurysms in patients randomized by coiling or clipping in the International Subarachnoid Aneurysm Trial (ISAT). Stroke 2007; 38: 1538-44.
En este excelente trabajo de Robles et al se presentan los resultados del tratamiento endovascular de una serie de 96 pacientes portadores de 118 aneurismas no rotos y asintomáticos.
En 81% el tratamiento consistió en el relleno del saco mediante coils mientras que en el 19% restante se hizo con coils asistidos con stents.
El resultado fue evaluado con arteriografias efectuadas a los 3 y 12 meses posteriores. En 78,3% de los pacientes se encontró una obliteración parcial o completa lo que fue considerado suficiente para prevenir la posibilidad de sangrado futuro.
La mortalidad fue de 2 pacientes; 8 pacientes (8,3%) tuvieron complicaciones de diferente gravedad que fueron transitorias en 5 de ellos y 3 pacientes quedaron con una hemiparesia, una hemianopsia o un trastorno del lenguaje en forma definitiva.
Todas las cifras presentadas son comparables con las de la mayoría de las series actuales de la bibliografía.
Creo que sería de gran utilidad para los neurocirujanos que en esa muestra tan importante de pacientes se hiciera una correlación mayor entre sus datos, por ejemplo, relación entre geometría y ubicación del saco, edad vs. morbilidad, presencia de comorbilidades o enfermedades familiares. Asimismo me interesaría conocer si hubo diferentes comportamientos entre los pacientes tratados con coils o con coils más stents.
Con relación al seguimiento postoperatorio es evidente que éste es muy breve, teniendo en cuenta que no debería ser menor de 3 años1.
Este trabajo demuestra una vez más que el tratamiento de los aneurismas debe ser centralizado en instituciones donde se encuentren los medios técnicos y el equipo médico entrenado para tal fin.
Juan A. Guevara
1. Campi A, Ramzi N, Molyneux AJ, Summers PE, Kerr RSC, Sneade M et al. Retreatment of ruptured cerebral aneurysms in patients randomized by coiling or clipping in the International Subarachnoid Aneurysm Trial (ISAT). Stroke, 2007; 38: 1538-44.
1. Komotar RJ, Mocco J, Solomon RA. Guidelines for the surgical treatment of unruptured intracranial aneurysms: the first annual J. Lawrence pool memorial research symposium-controversies in the management of cerebral aneurysms. Neurosurgery 2008; 62:183-93. [ Links ]
2. Goddard AJ, Annesley-Williams D, Gholkar A. Endovascular management of unruptured intracranial aneurysms: does outcome justify treatment?. J Neurol Neurosurg Psychiatry 2002; 72: 485-90. [ Links ]
3. Garbugino S, Casagrande W, Van Ooteghem M, Lemme-Plaghos L. Tratamiento Endovascular de Aneurismas Incidentales con Espirales GDC. Rev Argent Neurocir 2003; 17: 129-32. [ Links ]
4. Pierot L, Spelle L, Vitry F. Immediate Clinical Outcome of Patients Harbouring Unruptured Intracranial Aneurysms Treated by Endovascular Approach. Results of the ATENA Study. Stroke 2008; 39: 2497-504. [ Links ]
5. International Subarachnoid Aneurysm Trial Collaborative Group. International Subarachnoid Aneurysm Trial (ISAT) of neurosurgical clipping vs. endovascular coiling in 2143 patients with ruptured intracranial aneurysms: a randomized trial. Lancet 2002; 360: 1267-74. [ Links ]
6. Spagnuolo E, Tarigo A, Villar A, Peredta P, Hayek G, Rial M. Aneurismas no rotos. Clasificación. Rev. De Neurocirugía de Uruguay 2006; 8: 74-84. [ Links ]
7. The International Study of Unruptured Intracranial Aneurysm Investigators,Unruptured Intracranial aneurysms-risk of rupture and risks of surgical intervention. N Engl J Med 1998; 339: 1725- 33 [ Links ]
8. Ausman JI, Roitberg B. A response from the ISUIA. International Study on Unruptured Intracranial Aneurysms. Surg Neurol 1999; 52: 428-30. [ Links ]
9. Rinkel G J, Djibuti M, Algra A, van Gijn J. Prevalence and Risk of Rupture of Intracranial Aneurysms : A Systematic Review. Stroke 1998; 29: 251-256. [ Links ]
10. Juvela S, Porras M, Poussa K. Natural history of unruptured intracraneal aneurysms: probability and risk factors for aneurysms rupture. J Neurosurg 2000; 93: 379-87. [ Links ]
11. Unruptured Intracranial Aneurysms. Natural History, Clinical Outcome, and Risks of Surgical and Endovascular Treatment. New Eng J Med 2003; 362: 103-10. [ Links ]
12. Fontana H. La Evolución Natural de los Aneurismas no Rotos. Rev Argent Neurocir 2007; 21: IX-X (Editorial). [ Links ]
13. Claiborne J, Zhao S, Dudley A, Mitchell F, Berman D, Gress R. Treatment of Unruptured Cerebral Aneurysms in California. Stroke 2001; 32: 597. [ Links ]
14. Claiborne J, Randall T, Higashida DL, Barrow LR, Caplan JE, Dion G. Recommendations for the Endovascular Treatment of Intracranial Aneurysms. Stroke 2002; 33: 25-36. [ Links ]
15. Roy D, Milot G, Raymond J. Endovascular treatment of Unruptured Aneurysms. Stroke 2001; 32:1998. [ Links ]
16. Krisht AF, Gomez J, Partington S. Outcome of surgical clipping of unruptured aneurysms as it compares with a 10-year nonclipping survival period. Neurosurgery 2006; 58: 207-16. [ Links ]
17. Carter BS, Sheth S, Chang E, Sethl M, Ogilvy CS. Epidemiology of the size distribution of intracranial bifurcation aneurysms: smaller size of distal aneurysms and increasing size of unruptured aneurysms with age. Neurosurgery. 2006; 58: 217-23. [ Links ]
18. Chang HS. Simulation of the natural history of cerebral aneurysms based on data from International Study of Unruptured Intracranial Aneurysms. J Neurosurgery 2006; 104: 188-94. [ Links ]
19. Da Costa LB, Gunnarsson T, Wallace MC. Unruptured intracranial aneurysms: natural history and management decisions. Neurosurg Focus 2004; 17(5): E6. [ Links ]














