Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Ciencia del suelo
versión On-line ISSN 1850-2067
Cienc. suelo vol.27 no.1 Ciudad Autónoma de Buenos Aires ene./jun. 2009
TRABAJOS
Variación en la producción de alcaloides en inflorescencias de Senecio Grisebachii por deficiencia de nutrientes
Margarita A Yaber Grass; Marina Ciancia & Silvia R Leicach
Cátedra de Química Orgánica. Facultad de Agronomía, UBA. Av. San Martín 4453, Bs. As., Argentina. Correo electrónico: yaber@agro.uba.ar
Recibido: 20-06-08
Aceptado: 12-02-09
RESUMEN
Senecio grisebachii Baker es una maleza que invade pasturas naturales y cultivos en el sur de Brasil, Uruguay, y provincias mesopotámicas y Buenos Aires en la Argentina y es considerada tóxica debido a la presencia de alcaloides pirrolizidínicos (APs) en sus tejidos. Se evaluó el efecto de la deficiencia de nitrógeno y de fósforo sobre el perfil de APs en inflorescencias de esta maleza. Se realizó un ensayo utilizando un diseño completamente aleatorizado con 10 repeticiones, en el cual las plantas, que crecieron en hidroponia desde mayo hasta octubre, fueron regadas con solución de nutrientes en las que las concentraciones de N o de P reducidas en un 50% respecto del control. La cuantificación de APs en las inflorescencias de S. grisebachii por CG y CG-EM, demuestra un aumento significativo en el contenido total de APs, en los tratamientos con déficit en N o P (1,33 y 1,34 mg g-1 de materia seca, respectivamente, comparados con el control 0,35 mg g-1). Se identificaron siete APs y sus concentraciones variaron entre tratamientos. Senecionina resultó el alcaloide mayoritario en el tratamiento déficit de N, mientras senecifilina resultó más abundante en los tratamientos control y con déficit de P, seguidos en todos los casos por integerrimina y cantidades menores de espartiodina, jacobina, jacozina y retrorsina.
Palabras clave. Alcaloides pirrolizidínicos; Senecio; Déficit de nitrógeno; Déficit de fósforo.
Alkaloid production changes due to nutrient deficiencies in Senecio Grisebachii inflorescences
ABSTRACT
Senecio grisebachii Baker is a weed that invades natural pastures and crops in southern Brazil, Uruguay, the mesopotamic provinces and Buenos Aires in Argentina, and is considered to be toxic because of the presence of pyrrolizidine alkaloids (PAs) in its tissues. The effects of nitrogen and phosphorus deficiency was evaluated on the APs patterns of the weed inflorescences. A completely randomized design with 10 repetitions was used in an experiment where plants growing in hydroponics from May to October were irrigated with a nutrient solution containing 50% P or N concentrations with respect to the control treatment. PAs quantification on S. grisebachii inflorescences by GC and GCMS showed a significant increase in total PAs content in treatments with N or P deficiencies (1,33 and 1,34 mg gr-1 dry weight, respectively, compared to the control with 0,35 mg g-1). Seven PAs were identified with relative concentrations that varied according to treatments. Senecionine was the mayor alkaloid in treatments with N deficiency, while senecifiline was the most abundant in the control and in P- deficient treatments, followed in all cases by integerrimine and minor amounts of spartiodine, jacobine, jacozine and retrorsine. Agricultural intensification during the last decades, in addition to the introduction of soybean cropping in Argentina, resulted in soil degradation of the agroecosystems. This is evidenced by a decline in soil organic matter and nutrient (nitrogen, phosphorous) contents, among other factors. Moreover, new weed communities appeared, Senecio grisebachii Baker among them. Our results demonstrate that this invasive weed increases its toxicity when grown in continuously cropped lands, and its presence in crops and forage lands should be considered as an threat to human and cattle health.
Key words. Pyrrolizidine alkaloids; Senecio; Nitrogen deficiency; Phosphorus deficiency.
INTRODUCCIÓN
Senecio L. (Asteraceae, Senecioneae) es un género cosmopolita que incluye 3.000 especies, concentradas en su mayoría en regiones montañosas de América, Asia y África. La explotación continua en nuestro país ha producido cambios en los agroecosistemas, siendo notoria la degradación del suelo con pérdidas significativas del horizonte A y reducción de la materia orgánica, el nitrógeno total y el fósforo disponible (Michelena et al., 1989; Urricarriet & Lavado, 1999). El cultivo de soja es uno de los principales responsables de esta realidad que incluye además la aparición de nuevas comunidades de malezas. Un estudio de las especies malezas en las provincias de Buenos Aires y Santa Fe realizado en el período 2002-2003, indicó la presencia de Senecio grisebachii entre las nuevas comunidades de malezas (Leguizamón et al., 2003).
Las especies de este género se caracterizan por producir alcaloides pirrolizidínicos (APs) (Hartmann & Witte, 1995), los cuales han probado ser dañinos para el hombre y el ganado a través de actividades hepatotóxica (Mattocks, 1986) y neumotóxica (Wilson, 1992), entre otras. Estos compuestos presentan potencial mutagénico y carcinogénico además de ser débilmente virustáticos (Schmeller, 1997).
Los APs no son tóxicos por sí mismos sino a través de sus productos metabólicos, ya que son transformados por las enzimas hepáticas citocromo P-450 en pirroles que causan daño a nivel cromosómico. En Senecio riddellii Torr. & Cray, por ejemplo, la concentración de APs puede alcanzar hasta un 18% de su peso seco y se han encontrado valores de DL50 en ratas de 50 y 77 mg kg-1 para los alcaloides senecionina y senecifilina, respectivamente (Mattocks, 1986).
Dado que presentan efectos antialimentarios sobre insectos herbívoros no especializados (Brown, 1995), se considera que son parte de las estrategias defensivas de las especies vegetales que los producen (Bopprè, 1990). Varios insectos han desarrollado, sin embargo, mecanismos a través de los cuales secuestran APs utilizándolos para su propia defensa porque también actúan como fago repelentes frente a polillas, mariposas y escarabajos, sus potenciales depredadores (Hartmann, 1995). Los APs pueden contaminar alimentos como miel, leche, huevos (Culvenor, 1980) y derivados de granos como las harinas, debido a que varias especies del género Senecio invaden cultivos como el maíz y la soja.
Durante epidemias causadas por intoxicación con APs fueron detectados casos de lactantes en animales y humanos, con síntomas de la enfermedad debido a que también están presentes en la leche. Casos de enfermedades en lactantes y población infantil producidas por oclusión de las venas hepáticas, fueron relacionados a la presencia de APs en la leche materna y de vaca (Roulet, 1988).
Los APs son el resultado de diferentes formas de unión entre un amino alcohol, la necina, y el ácido nécico (Fig. 1).

Figura 1. Senecionina N-óxido.
Figure 1. Senecionine N-oxide.
A través de la taxonomía química y la biogenética se ha demostrado que existen en realidad tres clases de APs, que son biosintetizados como N-óxidos: diésteres macrocíclicos, como los del género Senecio, diésteres de cadena abierta y monoésteres (Hartmann & Witte, 1995). Los diésteres cíclicos, como la retrorsina son los derivados más tóxicos (DL50 en ratas: 34 mg kg-1, Mattocks, 1986), seguidos por los diésteres acíclicos y finalmente los monoésteres (Fig. 2). Los primeros son agentes alquilantes bifuncionales que se unen covalentemente al ADN impidiendo su duplicación y por ende la división celular.
La biosíntesis de los APs en las Asteraceae es un proceso coordinado y controlado que ocurre en las raíces. El N-óxido de senecionina (Fig. 1) es sintetizado en las raíces y trasladado vía floema a los sitios preferenciales de acumulación, las vacuolas de las células de inflorescencias y tejidos periféricos de hojas y tallos, lo cual confirmaría su rol como estrategia de defensa química. De los 26 diferentes APs descriptos en la literatura en S. jacobaea (Trigo et al., 2003), con la excepción de senecivernina, todos son derivados de la senecionina, a partir de la cual se obtienen a través de transformaciones metabólicas simples (Fig. 3).
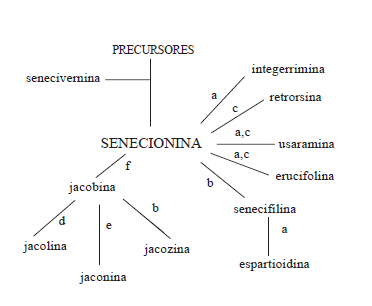
Figura 3. Reacciones involucradas en la biosíntesis de alcaloides pirrolizidínicos en Senecio. (a) isomerización Z/E en el C20; (b) deshidrogenación entre C13 y C19; (c) hidroxilación en C18; (d) hidrólisis de epóxido entre C15 y C20; (e) clorólisis de epóxido entre C15 y C20; (f) epoxidación entre C15 y C20.
Figure 3. Reactions involved in pyrrolizydine alkaloids synthesis in Senecio. (a) Z/E isomerization at C20; (b) C13 - C19 dehydrogenation; (c) hydroxylation at C18; (d) C15 - C20 epoxide hydrolysis; (e) C15 - C20 epoxide chlorolysis; (f) C15 - C20 epoxidation.
El desarrollo de las plantas ocurre a través de procesos de división, crecimiento y diferenciación celular, que requieren luz, agua y minerales para la producción de los metabolitos primarios necesarios. Además de los compuestos químicos relacionados a la adquisición de biomasa (proteínas, carbohidratos, lípidos y ácidos nucleicos) las plantas producen una serie de compuestos llamados metabolitos secundarios, los cuales parecen no ser esenciales para el crecimiento básico (Leicach, 2006). Independientemente de las características genéticas de una planta, la proporción relativa en que los recursos son utilizados en rutas metabólicas secundarias está fuertemente afectada por factores ambientales. Diferentes formas de estrés asociadas a la acción de animales (herbivoría) y patógenos (enfermedad), la presencia de competidores (competencia y/o alelopatía), además de factores abióticos (radiaciones, temperaturas extremas, las deficiencias nutricionales y de agua), influyen sobre la producción de los metabolitos secundarios (Einhellig, 1989) y en muchos casos tienden a incrementar la misma (Leicach, 2003; Pomilio et al., 2000; Vilariño et al., 2005).
Varias teorías han tratado de explicar el compromiso entre las funciones de defensa (metabolismo secundario) y el crecimiento y/o reproducción (metabolismo primario) (van der Meijden et al., 1988; Simms & Fritz, 1990). Un factor fundamental en ellas es el balance entre beneficios y costos en la producción de metabolitos secundarios. Se podría pensar que un incremento en la producción de metabolitos secundarios, derivados de los mismos precursores metabólicos de metabolitos primarios, disminuirá el crecimiento de la planta, y en algunas especies ocurre. Sin embargo, en otros casos se ha encontrado una falta de correlación o incluso una correlación positiva entre ambos (van Noordwijk, 1986).
Algunos autores sugieren que plantas que crecen con suministros limitados de energía o nutrientes deben optar entre crecer y defenderse (Herms & Mattson, 1992). El transporte, almacenamiento y los mecanismos de autodetoxificación y reciclado de los metabolitos secundarios implican costos que podrían conducir a una reducción en el crecimiento. Una hipótesis postulada para predecir los efectos del entorno sobre la expresión fenotípica del metabolismo secundario es la de Balance de la relación Carbono- Nutriente (BCN) (Reichardt et al., 1991). Esta teoría predice que una moderada deficiencia de nutrientes (valor alto de la relación C/N) limita más el crecimiento que la tasa de fotosíntesis, acumulándose carbohidratos que exceden los requeridos por la planta para el metabolismo primario. Ese exceso será asignado a la producción de metabolitos secundarios con C, H y O en su estructura química. Por otro lado, en suelos fértiles, la disminución de la relación C/N, impulsaría una mayor producción de compuestos nitrogenados, como los alcaloides, empleando el nitrógeno asimilado en exceso.
El presente bioensayo se realizó utilizado la técnica de hidroponía con el fin de evaluar el efecto causado sobre la producción y el perfil de alcaloides pirrolizidínicos en inflorescencias de Senecio grisebachii Baker, al variar los niveles de nitrógeno y fósforo en la solución nutritiva. La elección de las soluciones de riego, que de ella dependerá el desarrollo de la planta, se realizó siguiendo a Vrieling & Wijk (1994), quienes estudiaron otra especie de Senecio (jacobaea L.).
MATERIALES Y MÉTODOS
Se recolectaron al azar trozos de vástago en una población de Senecio grisebachii Baker en el campo experimental de la Estación INTA San Pedro, provincia de Buenos Aires. Los esquejes se hicieron enraizar en terrinas con arena estéril y perlita y las plantas obtenidas se trasplantaron a macetas a fines de julio de 2005. De las plantas obtenidas a partir de los esquejes se eligieron en forma aleatoria veinte para realizar los tres tratamientos que se detallan a continuación:
I) N1P1K1: control. Solución de riego: N 222,3 mg L-1, P 40,2 mg L-1, K 341,8 mg L-1, S 73,2 mg L-1, Ca 149,3 mg L-1, Mg 24,6 mg L-1 y micronutrientes (Arnon & Hoagland, 1940).
II) N2P1K1: déficit en N. Solución de riego: N 111,1 mg L-1 y los demás nutrientes ídem N1P1K1.
III) N1P2K1: déficit en P. Solución de riego: P 20,1 mg L-1 y los demás nutrientes ídem N1P1K1.
Los experimentos se llevaron a cabo en un invernáculo de la Facultad de Agronomía de la Universidad de Buenos Aires, en ambiente no controlado, manteniendo el contenido de agua a su máxima capacidad de retención. Las malezas e insectos fueron controlados manualmente, sin utilizar agroquímicos. A fines de octubre se retiraron las plantas y se separaron las inflorescencias.
La extracción, cuantificación e identificación de los APs se realizaron de acuerdo a técnicas previamente descriptas (Witte et al., 1993; Pelser et al., 2005). La cromatografía gaseosa (CG) permitió la separación de los distintos alcaloides, y su posterior acoplamiento a un Espectrómetro de Masa (CG-EM), la identificación de los mismos. Estos datos relacionados con el peso seco de cada muestra, permitieron la evaluación de las abundancias relativas de cada alcaloide. La Cromatografía Gaseosa permite separar compuestos en función de la intensidad diferencial con que son retenidos en una columna cromatográfica. Como la intensidad con que la fase fija de una columna, adecuadamente elegida, retiene a cada compuesto depende de su estructura química, los diferentes compuestos son arrastrados a tiempos (tiempos de retención, TR) diferentes por el gas portador.
La Espectrometría de Masa permite identificar compuestos por los fragmentos que resultan de su bombardeo electrónico. El espectro de masa presenta líneas verticales como señales correspondientes a los fragmentos iónicos positivos en los que puede fragmentarse una sustancia en esas condiciones. La altura relativa de cada línea indica la abundancia relativa de ese pico. Tanto la masa (m/z) de cada fragmento como la abundancia relativa que aparece a su lado entre paréntesis, están determinados por la estructura de cada compuesto, cuyo peso molecular coincide con M+.
Las inflorescencias fueron secadas en estufa con corriente de aire a 40 ºC inmediatamente después de su recolección. Muestras secas de 2 gramos fueron molidas y extraídas en forma continua durante 4 horas utilizando un equipo Soxhlet con metanol (250 mL) como solvente. El extracto metanólico fue evaporado a sequedad bajo presión reducida y el residuo disuelto por agregado de HCl 5% hasta alcanzar un pH =1. A la solución ácida, previamente particionada con cloroformo (3 x 30 mL) para eliminar los compuestos no polares, se agregó un exceso de zinc en polvo, manteniendo el sistema a temperatura ambiente durante 4 h con agitación constante para convertir los N-óxidos en las bases terciarias volátiles. La solución conteniendo los productos de reacción se filtró, llevó a pH =11 con NH4OH 25% y se extrajo con cloroformo (3 x 30 mL). El extracto clorofórmico se secó con Na2SO4 anhidro y evaporó a presión reducida hasta sequedad. Se mantuvo en desecador al vacío hasta constancia de peso. Se obtuvieron de esta manera las fracciones conteniendo todos los alcaloides (bases libres de APs + N-óxidos de AP), además de compuestos básicos como aminas, que pueden también ser extraídos en estas condiciones. Los extractos secados al vacío, fueron pesados y reservados a -18 ºC hasta su cuantificación por CG.
Para la cromatografía gaseosa se utilizó un cromatógrafo gaseoso Hewlett Packard 5890A (Avondale PA, USA) con columna capilar HP-Ultra 2 (50 m x 0,32 mm d. i.) y nitrógeno como gas portador. Programa de temperatura: de 150 a 260 ºC con rampa de 4 ºC minuto-1, luego isotérmico (260 ºC). Se utilizó un detector de ionización de llama (FID). Estándar interno: tetradecano.
Muestra (A): cada una de las muestras pesadas se disolvió en metanol en una relación de 5 mg por 50 μL de solvente.
Estándar interno (B): 25 μL de tetradecano (C14H30, δ= 0,765 gr mL-1) se disolvió en 3 ml de cloroformo.
Preparación de la muestra cromatográfica: Se mezclaron y homogeneizaron 10 μL de A y 10 μL de B. La cantidad inyectada en el cromatógrafo fue de 1 μL.
El análisis por CG-EM fue llevado a cabo en un cromatógrafo gas-líquido Shimadzu GC-17A, acoplado a un espectrómetro de masa CMS-QP 5050A (Kyoto, Japón) trabajando a 70 eV, con idénticas columna capilar y programa de temperatura utilizando helio como gas portador. La identificación de alcaloides se realizó por comparación de los correspondientes EM con los de bases de datos del software del espectrómetro. Las asignaciones se confirmaron por comparación con espectros de masa previamente publicados y/o los de testigos comerciales.
Para el análisis estadístico se utilizó el programa InfoStat/ Profesional, Versión 1.1 (2002). El diseño experimental completamente aleatorizado se analizó mediante ANOVA. La prueba de Tukey (P<0,05) se realizó para determinar diferencias entre las medias de los tratamientos, y el análisis multivariado de componentes principales (P<0,05) para los porcentajes de alcaloides en las muestras.
RESULTADOS
Los tiempos de retención (TR), los valores de masa del ión molecular (M+), los patrones de fragmentación característicos de cada compuesto se compararon con espectros de masa obtenidos de la literatura. En las inflorescencias de S. grisebachii se identificaron siete alcaloides, que resultaron ser diésteres cíclicos de necina y habían sido descriptos previamente por Trigo et al. (2003) para la especie jacobaea. Los patrones de fragmentación mostraron iones a m/z 246, 220, 136 y 120 provenientes de la necina y a 95, 94 y 93 debidos a las rupturas del ácido nécico. Entre ellos, cuatro resultaron ser dos pares de isómeros geométricos Z-E, senecionina-integerrimina y senecifilina-espartioidina.
Los datos correspondientes a los espectros de masa se presentan en la Tabla 1.
Tabla 1. Espectros de masa de alcaloides pirrolizidínicos: ión molecular M+, tiempos de retención TR y fragmentación.
Table 1. Mass spectral data of pyrrolizidine alkaloids: molecular ions M+, retention times TR and fragmentation.
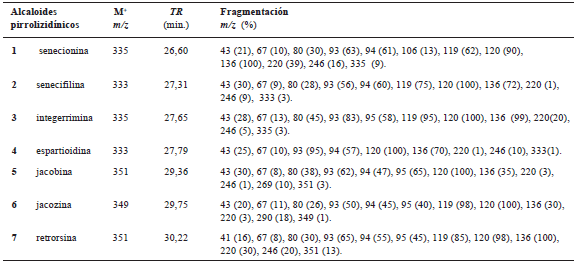
La identificación de los alcaloides pirrolizidínicos se realizó utilizando datos obtenidos de la bibliografía (Asres, 2004; El-Shazly, 1998, 2002; Hartmann & Dierich, 1998; Klitzke & Trigo, 2000; Pelser, 2005; Trigo et al., 2003: Vrieling, 2006).
El contenido total de APs (mg por gramo de materia seca) se incrementó significativamente en los tratamientos con déficit en N o P con valores de 1,33 y 1,34 mg g-1 respectivamente, frente a 0,35 mg g-1 para el control. En los tratamientos en los cuales las soluciones de riego aportaron la mitad de las concentraciones de N o P respecto del control, ninguno de los dos macronutrientes actuó como limitante de la producción de APs (Tabla 2).
Tabla 2. Medias de APs totales en mg g-1 materia seca ± D.E. y porcentaje de alcaloides individuales ± D.E. en inflorescencias de S. grisebachii Baker.
Table 2. Mean values of total APs in mg g-1 dry matter ± S.D. and individual alkaloids percentage ± S.D. in S. grisebachii Baker inflorescences.
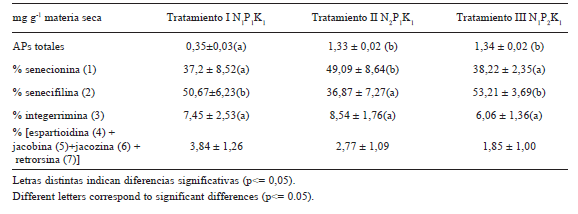
Los patrones de distribución de la composición de alcaloides de los tres tratamientos se obtuvieron a través del análisis multivariado de componentes principales (PCA) utilizando una matriz de varianza/covarianza para datos continuos, en que las variables, alcaloides, contribuyen al análisis en proporción a sus varianzas (Fig. 4 y Tabla 3). El Componente 1, que explica el 84% de la variabilidad, permite separar los tratamientos N1P1K1 (1) y N1P2K1 (3) del tratamiento N2P1K1 (2) señalando a senecionina y senecifilina como los alcaloides responsables de estas diferencias. La senecifilina recibe el peso positivo más alto y la senecionina, el peso negativo más alto, es decir, se relacionan en forma negativa. Los tratamientos control y con déficit de P, en los cuales el alcaloide principal es senecifilina se oponen al tratamiento con déficit de N donde senecionina es mayoritario. El Componente 2 sólo explica el 12% de la variabilidad, está asociado fundamentalmente a senecionina, senecifilina y jacozina.
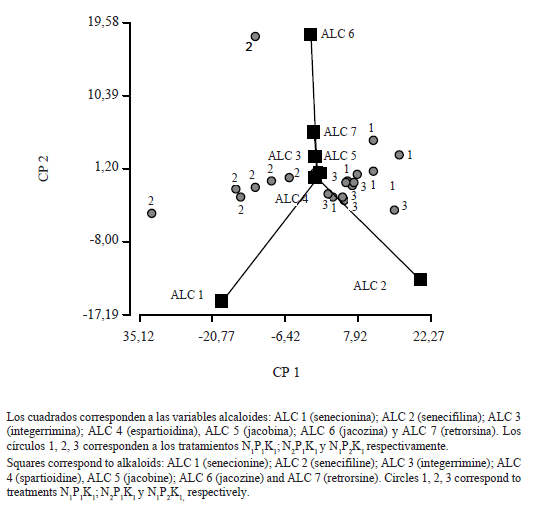
Figura 4. Análisis multivariado de componentes principales. Representación gráfica del primer y segundo componente.
Figure 4. Principal Component Multivariate Analysis. First and second component graphic representation.
Tabla 3. Análisis multivariado de componentes principales.
Table 3. Principal components multivariate analysis.

Estos resultados corroboran los presentados en la Tabla 1 donde el porcentaje de senecionina es significativamente mayor (49,09%) en el tratamiento con déficit de N respecto de los tratamientos control y déficit de P (37,2% y 38,22%, respectivamente). El valor de senecifilina es significativamente mayor en los tratamientos control y con déficit de P (50,67% y 53,21%) respecto del tratamiento con déficit de N (36,87%). El valor correspondiente a integerrimina no presentó diferencias significativas entre tratamientos (Tabla 2).
DISCUSIÓN
Los resultados señalan a senecionina, y senecifilina como los alcaloides presentes en mayor concentración, en inflorescencias de S. grisebachii, seguidos por integerrimina. Retrorsina aparece como uno de los alcaloides minoritarios. La comparación entre los porcentajes individuales de los alcaloides mayoritarios en las repeticiones de cada tratamiento y el análisis multivariado de componentes principales evidenciaron una dispersión mayor de datos en los tratamientos N1P1K1 y N2P1K1 (Fig. 4), que puede explicarse en parte teniendo en cuenta que en general existe variabilidad entre individuos de una determinada población, en la producción de aleloquímicos estructuralmente relacionados.
La mayor dispersión de datos en N1P1K1 se debe a que en una repetición cambia el alcaloide mayoritario, siendo senecionina en lugar de senecifilina, y en otras dos la abundancia de jacobina y retrorsina es notablemente superior al correspondiente valor medio.
En el tratamiento N2P1K1 senecionina, siempre mayoritario, presentó una abundancia mucho mayor que la media en una repetición, produciendo un aumento en la variabilidad a la que también contribuyeron los valores de jacozina y retrorsina que se disparan mucho más allá de la media en otra repetición.
Las desviaciones estándar de los alcaloides minoritarios espartoidina, jacobina, jacozina y retrorsina son relativamente altas ya que están presentes en proporciones muy bajas, alrededor del 1%, apenas por encima del ruido del cromatógrafo.
La alta concentración de senecionina y senecifilina, y la mayor producción de APs en situaciones de déficit de N o P, confirmarían lo postulado por algunos autores respecto de un aumento en el metabolismo secundario en condiciones de estrés (Einhellig, 1989).
En condiciones de déficit de nitrógeno, las inflorescencias presentaron cambios en el perfil de los alcaloides respecto del control, presentando un aumento en la abundancia relativa de senecionina, acompañado de la disminución en la de senecifilina. Dado que la primera es precursora de la segunda en la biosíntesis de APs, se podría especular que de esta manera se ahorra un paso biosintético, lo cual redundaría en un menor costo metabólico.
En el presente trabajo, los resultados difieren de los predichos por la hipótesis de Balance de la relación Carbono/ Nutriente (BCN), ya que la producción de alcaloides se incrementó significativamente en los tratamientos donde la disponibilidad de N o P había sido disminuida a la mitad respecto del control. Aunque estudios previos relacionados en general con la producción de metabolitos secundarios no nitrogenados revalidaron dicha hipótesis para ese tipo de compuestos, existen discrepancias en cuanto a variaciones en la concentración de metabolitos secundarios nitrogenados. Algunos ensayos señalan aumentos en su concentración por fertilización, por ejemplo se demostró un incremento en la concentración de alcaloides en Tabernaemontana pachysiphon Staff., en estudios con suplementación de N (Höft et al., 1996). Resultados inversos a los anteriores se encontraron en trabajos con Nicotiana sylvestris Speg. & Comes, que acumuló nicotina como respuesta a la deficiencia de N (Baldwin et al., 1993). En cambio, un experimento también llevado a cabo en condiciones de hidroponía, demostró que la especie S. jacobaea, no evidenciaba diferencias significativas en la producción de APs en la parte aérea y raíces en condiciones de estrés por deficiencia de N o P (Vrieling & van Wijk, 1994). Estos autores tampoco encontraron cambios significativos al analizar los efectos de la deficiencia de P sobre la producción de APs, sugiriendo que la producción de APs en S. jacobaea no se vería afectada por la deficiencia de fósforo, porque éste no es incorporado como tal en los alcaloides.
Cabe mencionar, sin embargo, que aún cuando el P no esté presente en la estructura de los alcaloides, podría afectar la producción de ATP, una de las formas de energía necesarias para la mayoría de las rutas biosintéticas, constituyendo así una forma de estrés para la planta.
Estos resultados confirman que el estrés por falta de macronutrientes aumenta la producción de metabolitos secundarios, ya que demuestran que la proporción de alcaloides pirrolizidínicos en inflorescencias de S. grisebachii se cuadruplica cuando se reduce a la mitad, tanto la disponibilidad de fósforo como la de nitrógeno.
En el marco del fuerte impacto ambiental resultante del manejo agrícola, nuestros resultados demuestran en principio que S. grisebachii, una maleza común, aumenta su toxicidad cuando crece con baja disponibilidad de N o P, característica de suelos sometidos a cultivo continuo. Esto puede ser un llamado de atención sobre el potencial problema relacionado con la presencia, en aumento, de esta especie en cultivos y pastizales argentinos.
AGRADECIMIENTOS
Los autores agradecen a la Universidad de Buenos Aires por financiar este trabajo (UBACYT G055).
BIBLIOGRAFÍA
1. Asres, K; F Sporer & M Wink. 2004. Patterns of pyrrolizidine alkaloids in 12 Ethiopian Crotalaria species. Biochem. Syst. Ecol. 32: 915-930. [ Links ]
2. Baldwin, IT; RC Oesch; PM Merhige & K Hayes. 1993. Damageinduced root nitrogen metabolism in Nicotiana sylvestris: Testing CN predictions for alkaloid production. J. Chem. Ecol. 19: 3029-3043. [ Links ]
3. Bopprè, M. 1990. Lepidoptera and pyrrolizidine alkaloids: exemplification of complexity in chemical ecology. J. Chem. Ecol. 16: 1-20. [ Links ]
4. Brown, KS & JR Trigo. 1995. The ecological activity of alkaloids. Pp. 227-354. In: Cordell, GA, (ed.). The Alkaloids. Vol.47. Academic Press, New York. [ Links ]
5. Culvenor, CCJ; M Clarke; JA Edgar; JL Frahn; MV Jago; et al. 1980. Structure and toxicity of the alkaloids of Russian comfrey (symphytum x uplandicum Nyman), a medicinal herb and item of human diet. Experientia 36: 377-381. [ Links ]
6. Einhellig, FA. 1989. Interactive effects of allelochemicals and environmental stress. Pp 101-117, en Phytochemical Ecology: allelochemicals, mycotoxins and insect pheromones and allomones. Chou, CH & Waller, GR (eds.), Institute of Botany, Academia Sinica Monograph Series Nº9, Taipei, ROC. [ Links ]
7. El-Shazly, A. 2002. Pyrrolizidine Alkaloid Profiles of Some Senecio Species from Egypt. Z. Naturforsch. 57: 429-433. [ Links ]
8. Hartmann, T & B Dierich. 1998. Chemical diversity and variation of pyrrolizidine alkaloids of the senecionine type: biological need or coincidence? Planta 206: 443-451. [ Links ]
9. Hartmann, T & L Witte. 1995. Pyrrolizidine alkaloids: chemical, biological and chemoecological aspects. Pp 155-233. In: Pelletier, SW (ed.) Alkaloids: Chemical and Biological Perspectives, vol. 9. Pergamon Press, Oxford. [ Links ]
10. Herms, AD & WJ Mattson. 1992. The Dilemma of Plants: to Grow or Defend, Q. Rev. Biol. 67: 283-335. [ Links ]
11. Klitzke, CF & JR Trigo JR. 2000. New records of pyrrolizidine alkaloid-feeding insects Hemiptera and Coleoptera on Senecio brasiliensis. Biochem. Syst. Ecol. 28: 313-318. [ Links ]
12. Höft, M; R Verpoorte & E Beck. 1996. Growth and alkaloid contents in leaves of Tabernaemontana pachysiphon Stapf (Apocynaceae) as influenced by light intensity, water and nutrient supply. Oecologia 107: 160-169. [ Links ]
13. Leguizamón, ES; G Ferrari & A Contigiani. 2003. Estudio del efecto de la presión de selección del sistema de siembra directa- glifosato en las comunidades de malezas de cultivos de soja: dos aproximaciones. Pp. 84-88. En: XI Congreso de la Sociedad Española de Malherbología (SEMh), Barcelona. [ Links ]
14. Leicach, SR; MA Yaber Grass; GB Corbino; AB Pomilio & AA Vitale. 2003. Nonpolar lipid composition of Chenopodium album grown in intensively-cultivated and non-disturbed soils. Lipids 38: 567-572. [ Links ]
15. Leicach, SR. 2006. Producción e impacto de los aleloquímicos [6] Pp. 97-106. En: EUDEBA Alelopatía. Interacciones químicas en la comunicación y defensa de plantas. 1ra edición. Buenos Aires, Argentina, 208 pág. [ Links ]
16. Mattocks, AR. 1986. Chemistry and Toxicology of Pyrrolizidine Alkaloids. Academic Press, London. [ Links ]
17. Michelena, RO; CB Irurtia; FA Vavruska; R Mon & A Pittaluga. 1989. Degradación de suelos en el Norte de la Región Pampeana. INTA Publ. Técnica 6.0 Instituto Nacional de Tecnología Agropecuaria, Centros regionales de Buenos Aires Norte, Córdoba, Entre Ríos y Santa Fe. Proyecto de Agricultura Conservacionista, Buenos Aires, Argentina. [ Links ]
18. Pelser, PB; H de Vos; C Theuring; T Beuerle; K Vrieling et al. 2005. Frequent gain and loss of pyrrolizidine alkaloids in the evolution of Senecio section Jacobaea (Asteraceae). Phytochemistry 66: 1285-1295. [ Links ]
19. Pomilio, AB; SR Leicach; MA Yaber Grass; M Ghersa; M Santoro & A Vitale. 2000. Constituents of the Root exudate of Avena fatua Grown under Far Infrared- Enriched Light. Phytochem. Anal. 11: 304-308. [ Links ]
20. Reichardt, PB; FS Chapin III; JP Bryant; BR Mattes & TP Clausen. 1991. Carbon/nutrient balance as a predictor of plant defense in Alaskan balsam poplar: potential important of metabolic turnover. Oecología 88: 401-406. [ Links ]
21. Roulet, M; R Laurine; L Rivier, & A Calame. 1988. Hepatic venoocclusive disease in newborn infant of a woman drinking herbal tea. J. Pediatr. 112: 433-436. [ Links ]
22. Schmeller, T; A El-Shazly & M Wink. 1997. Allelochemical activities of pyrrolizidine alkaloids. Interaccions with neuroreceptors and acetylcholine related enzymes. J. Chem. Ecol. 23: 399-416. [ Links ]
23. Simms EL & RS Fritz. 1990. The ecology and evolution of host plant resistance to insects. Trends in Ecology and Evolution. 5: 356-360. [ Links ]
24. Trigo, JR; IR Leal; NI Matzenbacher; TM Lewinsohn. 2003. Chemotaxonomic value of pyrrolizidine alkaloids in southern Brazil Senecio (Senecioneae: Asteraceae). Biochem. Syst. Ecol 31: 1011-1022. [ Links ]
25. Urricarriet, S & RS Lavado. 1999. Indicadores de deterioro en suelos de la Pampa Ondulada. Ciencia del Suelo. 17(1): 37-44. [ Links ]
26. van der Meijden, E; M Wijn & HJ Verkaar. 1988. Defence and regrowth, alternative plants stretegies in the struggle against herbivores. Oikos. 51: 355-363. [ Links ]
27. van Noordwijk, AJ & G de Jong. 1986. Acquisition and allocation of resources: their influence on variation in life history tactics. American Naturalist 128: 137-142. [ Links ]
28. Vilariño, MP; G Mareggiani; M Yaber Grass; SR Leicach & D Ravetta. 2005. Post-damage alkaloid concentration in sweet and bitter lupin varieties and its effect on subsequent herbivory. J. Appl. Entomology 129(5): 233-238. [ Links ]
29. Vrieling K & CAM van Wijk. 1994. Cost assessment of the production of pyrrolizidine alkaloids in ragwort (Senecio jacobaea L.). Oecologia 97: 541-546. [ Links ]
30. Wilson, DW; HP Segall; LC Pan; MW Lame; JE Estep et al. 1992. Mechanisms and pathology of monocrotaline pulmonary toxicity, Crit. Rev. Toxicol. 22: 307-325. [ Links ]
31. Witte, L; P Rubiolo; C Bicchi & T Hartmann. 1993. Comparative analysis of pyrrolizidine alkaloids from natural sources by gas chromatography-mass spectrometry. Phytochemistry 32 (1): 187-196. [ Links ]














