Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Ciencia del suelo
versión On-line ISSN 1850-2067
Cienc. suelo vol.29 no.2 Ciudad Autónoma de Buenos Aires jul./dic. 2011
TRABAJO
Absorción de nitrógeno y rendimiento de arroz con diferentes formas de nitrógeno aplicado previo al riego
Nitrogen uptake and rice yield with different forms of nitrogen applied before irrigation
César Eugenio Quintero1; Fabio Prats2; María de los Ángeles Zamero1; Edgardo Santiago Arévalo1; Nicolás Blas Spinelli3 & Graciela Norma Boschetti1
1Facultad de Ciencias Agropecuarias, UNER, CC24 Paraná ER (3100).
2Profesional Independiente, Schweitzer 9356, Rosario (2000).
3Grupo de Investigación y Desarrollo Agropecuario Independiente, Pte. Perón 17, Paraná ER (3100). Autor para correspondencia: cquinter@fca.uner.edu.ar
Recibido: 06-06-11
Recibido con revisiones: 16-09-11
Aceptado: 19-09-11
Resumen
En la Argentina el arroz se siembra sobre suelo seco con maquinaria y luego se lo riega por inundación desde inicios del macollaje hasta la madurez. Esto determina condiciones especiales donde el nitrógeno puede perderse tanto por volatilización como por desnitrificación. Las fuentes de N más recomendadas en arroz son las amoniacales o amídicas; sin embargo, las fuentes nítricas podrían presentar ventajas importantes. Se realizó un ensayo a campo con el objetivo de evaluar la respuesta y eficiencia de absorción de distintas fuentes y formas de nitrógeno. Se utilizó: urea, sulfato de amonio (SA), nitrato de calcio (CN), solución de urea-nitrato de amonio-tiosulfato (UAN+ATS) y nitrato de amonio calcáreo (CAN). Se aplicó una dosis de N 60 kg/ha previo al riego para todas las fuentes, incluyendo un tratamiento testigo. Se evaluó la absorción de N y el rendimiento. El rendimiento en grano del tratamiento control fue de 9.756 kg/ha y su absorción total de N fue de 137 kg/ha; mientras que los fertilizados absorbieron de 164 a 185 kg/ ha. Las fuentes puras (urea, SA y CN) mostraron una alta tasa de absorción del N inicial, con una recuperación aparente del N del fertilizante de 80 al 100% en diferenciación de panícula. La mayor respuesta se observó con el CN, con una alta eficiencia de uso del fertilizante. Las fuentes mixtas (UAN+ATS y CAN) mostraron menor absorción y recuperación del N proveniente del fertilizante. Los resultados de este ensayo indican que las pérdidas por desnitrificación no fueron importantes y que las fuentes nítricas podrían ser utilizadas en fertilización de arroz.
Palabras clave. Arroz; Nitrógeno; Desnitrificación; Fuentes.
Abstract
In Argentina, rice is mechanically sowed on dry soil and is then flooded from early tillering to maturity. This practice gives rise to conditions that promote nitrogen losses by volatilization and denitrification. The most recommended N fertilizers for rice have N in the form of ammonium or amides; however, nitric sources have shown advantages. A field trial was conducted to evaluate the responsiveness and absorption efficiency of different sources and forms of nitrogen. Urea, ammonium sulfate (AS), calcium nitrate (CN), solution of urea-ammonium nitrate-thiosulfate (UAN + ATS) and calcium ammonium nitrate (CAN) were tested. A fertilizer rate of 60 kg N/ha was applied before irrigation and a control treatment with no N was included. Rice N uptake and yield was measured. The control treatment yielded 9756 kg/ha and total N uptake was 137 kg/ha, while the fertilized treatments absorbed from 164 to 185 kg N/ha. Pure fertilizer sources (urea, SA, CN) showed a high rate of initial N uptake, with an 80 to 100% apparent recovery of N fertilizer at the panicle differentiation stage. Surprisingly, the greatest response was observed in the treatment with CN, presenting a high fertilizer use efficiency. The mixed sources (UAN+ATS, CAN) showed a lower N uptake and fertilizer recovery. The results of this field trial indicate that denitrification losses were not significant and nitric sources could be used in rice fertilization.
Key words. Rice; Nitrogen; Denitrification; Sources.
INTRODUCCIÓN
El arroz se cultiva principalmente en las provincias de Corrientes y Entre Ríos, teniendo las otras provincias una participación menor. La superficie implantada anualmente en la Argentina es de unas 200.000 hectáreas. El arroz se siembra en condiciones de secano y es regado por inundación con una lámina de agua de 5 a 10 cm de espesor desde los veinte a treinta días después de la emergencia hasta unos días previos a la cosecha. Una de las características distintivas del cultivo de arroz es que permanece parte del ciclo de desarrollo con el suelo saturado con agua, lo que produce modificaciones en el ambiente edáfico. En general, hay una mayor disponibilidad de nitrógeno para el cultivo que en suelos aireados (Dobermann & Fairhurst, 2000); pero debido a condiciones físico-químicas favorables, el nitrógeno tiene un gran potencial para perderse por desnitrificación, volatilización o lixiviación (Norman et al., 2003). En estas condiciones, los nitratos adicionados al suelo como fertilizantes o los que se generan en las zonas aeróbicas cerca de las raíces o en la superficie del suelo, tienden a perderse por desnitrificación dado que la mayor parte del suelo se encuentra en condiciones anóxicas. Por esta razón se asume generalmente que el arroz y otras plantas hidrófilas absorben poco N como nitrato. Sin embargo, muchos experiencias muestran que el arroz es excepcionalmente eficiente en absorber y asimilar NO3- en comparación con el NH4+ (Kira & Kronzucker, 2005; Duan, et al., 2007; Wang, et al., 2010). La planta de arroz es capaz de transportar O2 por el aerénquima hacia las raíces en cantidades tales que puede oxidar el NH4+ a NO3- en la rizósfera, lo que reduce la toxicidad del amonio y determina una nutrición parcial con nitratos (Kirk & Kronzucker, 2005). Una nutrición parcial de N con NO3- ha mostrado mayor crecimiento de raíces, más producción de ácido indol acético, mayor actividad fotosintética y mayor producción de biomasa (Zhang et al., 2011; Song et al., 2011), mientras que una exclusiva con N- NH4+ ha mostrado hasta toxicidad (Holzschunh et al., 2009).
La fuente nitrogenada más utilizada en fertilización de arroz es la urea. En numerosos trabajos se muestra la conveniencia de utilizar esta fuente dado que tiene el N en forma amídica y no se vería afectado significativamente por la desnitrificación en un ambiente reductor como el del arroz. Algo similar ocurre con fuentes amoniacales como el sulfato de amónio. La estrategia para reducir las pérdidas en forma de amoníaco por volatilización, es inundar dentro de los 5 días de aplicado en N. Las fuentes nítricas no están recomendadas, dado que al inundar se perdería gran parte del N por desnitrificación (Norman, et al., 2003). La desnitrificación implica la pérdida de N por un proceso biológico que produce gases de nitrógeno reducido (NO, N2O, N2) que pasan a la atmósfera. El proceso es favorecido fundamentalmente por condiciones de anaerobiosis o excesos de humedad y altas temperaturas, pero deben encontrase NO3- disponibles junto con una fuente carbonada como substrato. Luego de la inundación, el oxígeno presente en el suelo es consumido rápidamente por los microorganismos, el resultado es la disminución del potencial redox que trae aparejada la reducción de los nitratos a N2 y N2O. De Datta (1986) informó pérdidas por desnitrificación de 30 a 40% del nitrógeno aplicado entre los 7 y 12 días después de la aplicación de nitrógeno de fertilizante en forma nítrica.
Para las nuevas variedades de porte bajo y resistentes al vuelco, una sola aplicación de N puede ser tan o más eficiente que aplicaciones divididas. La bibliografía internacional indica que lo más conveniente es hacer una única aplicación pre riego o aplicar un 50 a 65% de la dosis en pre riego y el resto en diferenciación de primordio. Sheehy et al. (2004) encontraron que un 30% del N presente en los granos de arroz es absorbido antes de diferenciación, las hojas actúan como reservorio y luego el N es removilizado. Las recomendaciones que surgen a partir de las investigaciones en Estados Unidos, muestran que la fertilización previo a la inundación es la más efectiva, si se realiza sobre suelo seco y se inunda antes de los 5 días de aplicado el N. El arroz debe mantenerse inundado y en anaerobiosis para reducir las pérdidas de N por desnitrificación (Norman et al., 2003).
En Entre Ríos, la disponibilidad de herbicidas selectivos y residuales, junto con la introducción de variedades resistentes a herbicidas del grupo imidazolinonas, permite un mejor control de malezas, retrazar el ingreso del agua y reduce la necesidad de una lámina de agua profunda. Podría esperarse entonces, que las condiciones que favorecen la desnitrificación sean menores, lo que permitiría la posibilidad de utilizar fuentes distintas a la urea. De hecho, algunas experiencias han mostrado buenos resultados fertilizando con sulfonitrato de amonio, nitrato de amonio calcáreo y UAN (Wilson et al., 1994; Spinelli et al., 2007; Quintero et al., 2008). Por lo cual el objetivo del trabajo fue evaluar el rendimiento del cultivo, la absorción de nitrógeno y la eficiencia de utilización de diferentes formas de nitrógeno bajo condiciones locales.
MATERIALES Y MÉTODOS
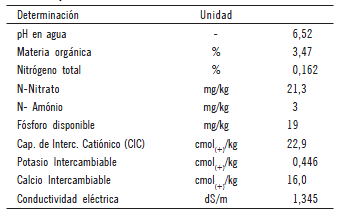
Durante la campaña 2006/07, se realizó un ensayo en un establecimiento comercial de la provincia de Entre Ríos (Argentina), sobre un suelo vertisol de la zona centro, cerca de la localidad de Villaguay, las principales características del suelo pueden verse en la Tabla 1.
Tabla 1. Características físico-químicas del suelo (0-15 cm).
Table 1. Physico-chemical soil features (0-15 cm).
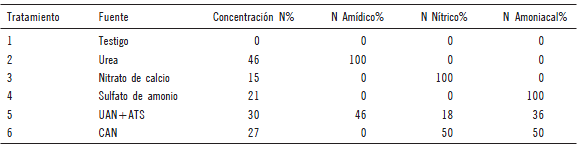
El ensayo se realizó en parcelas de 100 m2 por tratamiento, en un diseño experimental en bloques completos aleatorizados, con tres repeticiones. Los tratamientos fueron fuentes con diferentes formas de nitrógeno: 100% amídico (Urea), 100 % nítrico (Nitrato de calcio), 100% amónico (Sulfato de amonio), y combinando: Urea+Nitrato de amonio+Tiosulfato de amonio (UAN+ATS), Nitrato de amonio calcáreo (CAN) y un testigo sin N. La Tabla 2 muestra los tratamientos y las formas de nitrógeno para las distintas fuentes utilizadas. La fertilización nitrogenada se realizó previo al riego, el 14 de noviembre, en inicio de macollaje, con una dosis de 60 kg/ha de N.
Tabla 2. Tratamientos y características de las fuentes utilizadas.
Table 2. Treatment and characteristics of the sources used.
La variedad utilizada fue Puitá INTA-CL, en siembra directa sobre taipas con laboreo de verano. La fecha de siembra fue el 11 de octubre, sobre cultivo antecesor arroz. El riego por inundación se inició el 20 de noviembre. Todas las parcelas experimentales recibieron una fertilización NPK a la siembraque consistió en 160 kg/ha de una mezcla 10-29-5, más una dosis de 122 L/ha de Tiosulfato de K, para aportar 29 S y 43 K. Las semillas fueron tratadas con Zn en forma de quelato al 4%, en una dosis de 1 L cada 100 kg de semilla.
En tres oportunidades durante el ciclo de cultivo, se determinó el potencial redox y el pH del suelo a campo, a una profundidad de 5 cm, con electrodos de platino y de calomel respectivamente, tomando 5 lecturas en el ensayo. En los mismos momentos se tomaron muestras de suelo de cada parcela (0-15 cm), se mantuvieron refrigeradas para el traslado al laboratorio y el mismo día se determinó la concentración de N de nitratos y de amonio (extracción con KCl 1N y determinación de N por destilación con MgO y aleación Devarda (Heredia, 2005).
Se efectuó un seguimiento del N absorbido por la planta, mediante cortes de la biomasa aérea por parcela en una superficie de 0,6 m2 al inicio del ciclo a 0,1 m2 en floración. Se determinó la concentración de N total en planta sobre muestra seca a estufa, mediante una digestión con ácido sulfúrico, destilación y titulación (Jackson, 1976). Los momentos de corte fueron: cuatro hojas, macollaje, diferenciación, floración y madurez (grano y rastrojo). Se calculó la tasa de absorción de N para cada período como la diferencia entre la cantidad de N absorbida al final de la etapa y el inicio de la misma, sobre los días transcurridos. Se estimó la recuperación aparente del N proveniente del fertilizante como la diferencia entre el N absorbido para una determinada fuente y el N absorbido por el testigo en el mismo tiempo.
Se avaluó el rendimiento de granos y rastrojo en 1 m2 por parcela. El rendimiento se corrigió a 14% de humedad. Se realizó un análisis de varianza y un test de comparación de medias. (LSD Fisher. p<= 0,05).
RESULTADOS Y DISCUSIÓN
En la Tabla 3 se presenta la información del seguimiento de la variación del Potencial Redox en suelo, para las tres fechas evaluadas. La primera se realizó antes del riego cuando se aplicó el nitrógeno, y los otros dos momentos fueron medidos con suelo inundado en diferenciación y floración. El suelo evolucionó de una condición moderadamente reducida hacia una reducida, pero no llegó a una condición altamente reducida (< -100 mV). El pH del suelo tendió a aumentar ligeramente en el período evaluado.
Tabla 3. Variación del pH de suelo y el Potencial Redox desde inicio del riego hasta floración.
Table 3. Variation of soil pH and redox potential since the beginning of irrigation until flowering.

El seguimiento del N-NH4+ y el N-NO3- en el suelo, mostró resultados con alta variabilidad. El N-NO3- disminuyó con el tiempo encontrándose los valores más altos con la fuente Nitrato de Ca, sin diferencias significativas. De un valor inicial de 21 mg/kg, el N-NO3-, descendió a 13 mg/kg en pleno macollaje y a 6 mg/kg en diferenciación (promedio de todos los tratamientos). Por otro lado, el N-NH4+ se incrementó desde 3 mg/kg al momento de la siembra a 8 mg/kg en pleno macollaje; solamente la urea aumentó significativamente a 12 mg/kg, mientras que el testigo permaneció sin variación en 3 mg/kg. Hacia la diferenciación, todas las fuentes disminuyeron a 5 mg/kg sin diferencias significativas.
El tratamiento testigo presentó una gran absorción de N, ligada a una buena fertilidad natural y disponibilidad de N en el suelo, junto con una adecuada fertilización a la siembra. A pesar de esto, el cultivo respondió significativamente al N aplicado con las distintas fuentes. Tanto la producción de biomasa aérea, como la concentración de N en tejidos se incrementaron con las distintas fuentes, lo que determinó una mayor absorción de N (Tabla 4). A las 6 semanas de aplicado el N, tanto la fuente nítrica como en la amoniacal mostraban una absorción aparente del N aplicado de alrededor de 100%.
Tabla 4. Absorción de N en la biomasa aérea. Valores en kg de N por ha.
Table 4. N uptake in aboveground biomass. Values in kg N per ha.
Las tasas de absorción de N fueron significativamente más altas en los tratamientos con Urea, Nitrato de Ca y Sulfato de amonio entre macollaje y diferenciación. Luego de la diferenciación y hasta la madurez, la tasa de absorción de N disminuyó en todos los tratamientos sin diferentas con el testigo (Fig. 1). Es de destacar que el ritmo de absorción de N en las panojas fue mayor a 2 kg/ha/día, muy superior a la tasa de absorción de la planta completa en ese momento (<1 kg/ha/día). Esto estaría indicando una importante translocación del N absorbido en etapas vegetativas (almacenado en las hojas y tallos) hacia los granos, en coincidencia con informado por Sheehy et al. (2004).
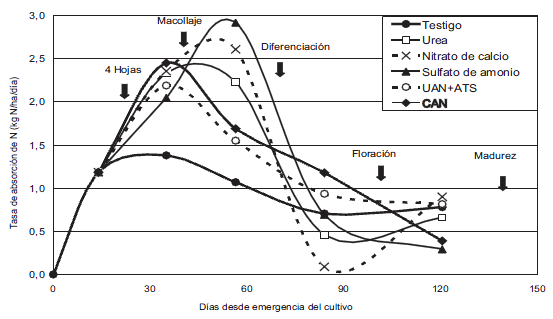
Figura 1. Tasa de absorción de N en el ciclo de cultivo.
Figure 1. N uptake rate during the crop cycle.
El rendimiento final de grano mostró una buena respuesta y eficiencia a pesar de la alta fertilidad del suelo. La fuente Nitrato de Ca se destacó sobre el resto con una elevada eficiencia de uso del N (Tabla 5). La eficiencia de absorción del N fue cercana al 80 % para el Nitrato de Ca y alrededor del 60% para las otras fuentes, indicando pérdidas de N relativamente bajas a muy bajas. El Nitrato de amonio calcáreo mostró una menor respuesta, con una baja eficiencia como resultado.
Tabla 5. Rendimiento y respuesta del cultivo. Eficiencia de uso de N.
Table 5. Yield and crop response. Nitrogen use efficiency.

Las fuentes puras como el nitrato de Ca , el Sulfato de amonio y la urea mostraron una alta tasa de absorción en los días siguientes a su aplicación. Una alta proporción del N aplicado fue absorbido por el cultivo con el inicio del riego en los 45 días siguientes a su aplicación, cuando las condiciones reductoras no eran muy marcadas, los potenciales redox se hicieron francamente negativos recién luego de la diferenciación. La hidrólisis de la urea incrementa el pH del suelo lo que podría favorecer la volatilización del amonio y, por lo tanto, explicaría la menor recuperación aparente del N ureico en un suelo de reacción neutra como lo indica Norman et al. (2003). Las fuentes mixtas (UAN+ATS y CAN) mostraron una menor respuesta y absorción de N (Tabla 3, Fig. 2).

Figura 2. Absorción aparente del N proveniente del fertilizante para las distintas fuentes evaluadas.
Figure 2. Apparent N uptake from the fertilizer for the different sources evaluated.
Un suelo bien aireado y oxidado presenta valores de potencial redox en el rango de +400 a +700 mV, mientras que las mayores emisiones de N2O por desnitrificación se dan entre +250 y +120 mV. A medida que se reduce el suelo, más N se pierde como gas producto de la desnitrificación, pero a 0 mV es mayormente como N2 (Yu et al., 2001; Masscheleyn, 1993). Bajo las condiciones de producción de los sistemas arroceros como el evaluado, el suelo permanece saturado menos tiempo que en otras partes del mundo. Además, se utiliza una lámina de agua delgada durante el período de inundación, y no se alcanza una condición fuertemente reductora. Sin embargo, los potenciales redox medidos fueron suficientes como para que el NO3-sea reducido y se pierda como N2O y N2.
Contrariamente a lo esperado, los resultados de este experimento mostraron que la fuente nítrica no presentó diferencias importantes con las fuentes recomendadas como la urea y el sulfato de amonio. Esto podría deberse en parte a que si bien se dieron las condiciones de reducción, no se establecieron otras condiciones apropiadas para la actividad microbiológica de desnitrificación y a que el N pudo ser absorbido rápidamente por el arroz antes de que se pierda. Existen numerosas evidencias de que el arroz absorbe mas eficientemente el NO3- que el NH4+ (Kron-zucker et al., 1999; 2000). Además el NO3- estimula la absorción de N en arroz, especialmente en variedades índicas como la utilizada en este ensayo (Duan et al., 2007). Esto se debe a que aumenta significativamente la absorción de NH4+ dado que se incrementa el número de transportadores de NH4+ en las membranas celulares (Duan et al., 2007; Wang et al., 2010). En nuestro ensayo podría tratarse de una mayor absorción del N-NH4+ del suelo estimulada por la adición de NO3- que enmascaró las pérdidas por desnitrificación y dio como resultado una alta recuperación aparente del fertilizante.
Las fuentes con proporciones intermedias entre NO3-y NH4+ como el UAN+ATS y el CAN presentaron una menor respuesta y eficiencia de uso del nitrógeno. Según Youngdahl et al. (1982), la existencia simultanea de NO3- y NH4+ en la superficie de la raíz, podría llevar a un uso ineficiente del N debido a una reducida absorción del N-NO3- que es deprimida por la presencia del NH4+. El efecto depresivo del NH4+ en la absorción de NO3- puede haberse evidenciado en nuestro ensayo en las fuentes mixtas, especialmente en el tratamiento con nitrato de amonio calcáreo.
Este trabajo ha sido útil para mostrar que en las condiciones actuales de producción de arroz en Entre Ríos, podría esperarse una alta eficiencia de utilización del N tanto de fuentes nítricas como amoniacales, con bajas pérdidas de N en aplicaciones previas al riego. Sin embargo, sería conveniente la realización de otros ensayos que permitan confirmar los resultados obtenidos en esta investigación.
AGRADECIMIENTOS
AM Sordelli, a O Henderson, a San Cristóbal S.A. y a Petrobras Energía por la financiación del trabajo. Este trabajo formó parte de la tesis para obtener el grado de Especialista FA-UBA de Fabio Prats.
BIBLIOGRAFÍA
1. De Datta, SK. 1986. Producción de arroz. Fundamentos y Prácticas. Ed. Limusa. México, D.F. p. 515-572. [ Links ]
2. Dobermann, A & T Fairhurst. 2000. Rice: Nutrient Disorders and Nutrient Management. Potash and Phosphate Institute and International Rice Research Institute. [ Links ]
3. Duan, YH; XM Yin; YL Zhang & QR Shen. 2007. Mechanisms of enhanced rice growth and nitrogen uptake by nitrate. Pedosphere 17(6): 697-705. [ Links ]
4. Heredia, O. 2005. Métodos de extracción y determinación de nitratos en suelos. Parte (I). En: Tecnologías en análisis de suelos. (eds. Marbán & Ratto). AACS. Buenos Aires. P:123-130. [ Links ]
5. Holzschunh, MJ; H Bohnen; I Anghinoni; EJ Meurer; F Campos & SE Valadao. 2009 Resposta do arroz irrigado ao suprimento de amonio e nitrato.R. Brás- Ci. Solo 33: 1323-1331. [ Links ]
6. Jackson, ML. 1976. Determinación de nitrógeno en los suelos y tejidos vegetales. p.254-281. En: Análisis químico de suelos. Ediciones Omega S.A. Barcelona. 662 p. [ Links ]
7. Kirk, GJR & HJ Kronzucker. 2005. The potential for nitrification and nitrate uptake in the rhizosphere of wetland plants: a modeling study. Annals of Botany 96: 639-646. [ Links ]
8. Kronzucker, HJ; MY Siddiqi; ADM Glass & GJD Kirk. 1999. Nitrate-ammonium synergism in rice: a subcellular flux analysis. Plan Physiology 119: 1041-1045. [ Links ]
9. Kronzucker, HJ; MY Siddiqi; ADM Glass & GJD Kirk. 2000. Comparative kinetic analysis of ammonium and nitrate acquisition by tropical lowland rice: implications for rice cultivation and yield potential. New Phytologist 145: 471-476. [ Links ]
10. Norman, R.; C Wilson & N Slaton. 2003. Soil Fertilization and Mineral Nutrition in U.S. Mechanized Rice Culture. In: Rice: Origin, History, Technology, and Production. Smith, CW and Dilday RH. Ed. P331-411. [ Links ]
11. Quintero, C. ; M Zamero; NG Boschetti; M Befani; E Arévalo & N Spinelli. 2008. Ensayos de Fuentes Nitrogenadas en Arroz. En: Resultados experimentales 2007-2008 Fundación Proarroz. Volumen XVII. Publicación editada por INTA E.E. A. C. Del Uruguay y Fundación Proarroz. P:89. [ Links ]
12. Sheehy, SH; M Mnzava; KG Cassman; PL Mitchell & P Pablico. 2004. Temporal origin of nitrogen in the grain of irrigated rice in the dry season: The outcome of uptake, cycling, senecense and competition studied using 15N- placement technique. Field Crop Research 89: 337-34. [ Links ]
13. Song W; K Makeen; D Wang; C Zang; Y Xu, H Zhao; E Tu; Y Zang; Q Shen & G Xu. 2011. Nitrate supply affects roots growth differentially in two rice cultivars differing in nitrogen use efficiency. Plant and Soil 343: 357-348. [ Links ]
14. Spinelli, N; F Prats & CE Quintero. 2007. Evaluación de fertilizantes líquidos como fuentes de nitrógeno en el cultivo de arroz. P. 83-85. En: Resultados experimentales 2006-2007 Fundación Proarroz. Volumen XVI. Publicación editada por INTA E.E. A. C. Del Uruguay y Fundación Proarroz. 121 p. [ Links ]
15. Wilson CE; BR Wells & RJ Norman. 1994. Fertilizer nitrogen uptake by rice from urea-ammonium nitrate solution vs. Granular urea. Soil Sci. Soc. Am. J. 58: 1825-1828. [ Links ]
16. Youngdahl, LJ; R Pacheco; JJ Street & PLG Vlek. 1982. The kinetics of ammonium and nitrate uptake by young rice plants. Plant and Soil 69(2): 225-232. [ Links ]
17. Zhang Y; H Lv; D Wang; J Deng; W Song; K Makeen; Q Shen & G Xu. 2011. Partial nitrate nutrition amends photosynthetic characteristic in rice (Oriza sativa J cv japonica) differing in nitrogen use efficiency. Plant Growth Regul 63: 235-242. 43. [ Links ]














