Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista argentina de cardiología
versión On-line ISSN 1850-3748
Rev. argent. cardiol. v.74 n.3 Buenos Aires mayo/jun. 2006
Doce años de extracciones de catéteres endocavitarios de marcapasos y desfibriladores en la Argentina
Héctor A. Mazzetti, Osvaldo Mascheroni
División Cardiología, Hospital Juan A. Fernández, Buenos Aires
Dirección para separatas: Héctor A. Mazzetti Santiago del Estero 1620 (1824) Lanús Oeste, Provincia de Buenos Aires
Recibido: 03/11/2005
Aceptado: 22/12/2005
RESUMEN
La extracción de catéteres de marcapasos fue una práctica habitual desde que se implantó el primer marcapasos en 1958. Se presenta la experiencia sobre extracciones de catéteres por vía percutánea de 609 catéteres de marcapasos y desfibriladores, desde julio de 1993 hasta julio de 2005. La indicación más frecuente fue por infección (decúbitos y endocarditis bacteriana asociada con marcapasos). Se utilizaron distintas vías de abordaje: vena cava superior (la más frecuente), vena cava inferior, transyugular interna y transauricular. Los catéteres con mayor tiempo de implantados necesitaron del sistema de extracción con más frecuencia que los catéteres más nuevos. Los catéteres de desfibrilador tuvieron menos tiempo de implantados y requirieron el material de extracción un número mayor de veces. La eficacia fue superior al 99%. El procedimiento tiene riesgos de complicaciones que incluyen la muerte. Sin embargo, con un entrenamiento apropiado, material adecuado y experiencia en el procedimiento se puede llevar a cabo con una excelente tasa de éxito.
Palabras clave: Extracción de catéteres; Infección de bolsillo; Endocarditis bacteriana; Marcapasos; Desfibriladores.
Abreviaturas:
TS Tracción simple
CCCA Cirugía cardíaca a cielo abierto
EB Endocarditis bacteriana
FA Fijación activa
FP Fijación pasiva
SUMMARY
Twelve Years of Experience in Pacemaker and Defibrillator Lead Extraction in Argentina
Lead extraction has been a common practice since the first pacemaker was implanted in 1958. This study presents our experience in 609 pacemaker and defibrillator lead extractions, from July 1993 to July 2005. Infection (by erosions and pacemaker endocarditis) was the most frequent indication. Several approaches were employed: superior vena cava, inferior vena cava, transjugular and transatrial approaches. Older leads needed lead extraction tools more frequently than newer leads. Defibrillator leads had shorter implant duration than pacemaker leads, but needed extraction tools more frequently. The efficacy was more than 99%. The procedure has several risks including death, albeit with proper training, adequate tools and procedural experience, an excellent success rate can be obtained.
Key words: Lead extraction; Pocket infection; Endocarditis; Pacemaker; Defibrillator.
INTRODUCCIÓN
La extracción de catéteres de marcapasos fue una práctica habitual desde que se implantó el primer marcapasos en 1958.
Las primeras indicaciones solamente eran para los catéteres infectados y la tracción simple (TS) era el modo habitual de extracción. Luego se agregó la tracción continua con pesas. En años posteriores se introdujeron otros instrumentos como canastillas, pigtails, pinzas de biopsia, etc.
Cuando todo lo anterior fracasaba y el paciente tenía una septicemia/endocarditis, el catéter debía extraerse por cirugía cardíaca a cielo abierto (CCCA), con la morbimortalidad que este procedimiento tenía en aquellos tiempos. Dussaut, en 1980, presentó su experiencia en el tratamiento de la endocarditis bacteriana (EB) asociada con marcapasos, que mostraba la alta mortalidad de los que no eran operados. (1, 2)
En 1985, Melboim presentó la primera técnica de extracción endocavitaria, con un sistema compuesto por un estilete fijador y vainas.
Posteriormente, distintos autores desarrollaron nuevos sistemas de extracción hasta llegar a los que se utilizan actualmente. (3-12)
En la Argentina, la primera extracción con esta técnica se realizó en 1993*, en el Hospital Pirovano. (13)
La extracción de catéteres es un componente importante y necesario del tratamiento de las complicaciones relacionadas con dispositivos implantables. (14)
Con el avance de la tecnología para la extracción intravascular y de la seguridad del procedimiento, el número de indicaciones se incrementó. En 2000, la NASPE (15) publicó las recomendaciones para indicaciones de extracción.
El presente trabajo se llevó a cabo con el objetivo de mostrar la experiencia de doce años con la técnica de extracción de catéteres endocavitarios de marcapasos y desfibriladores.
MATERIAL Y MÉTODOS
Desde el 20 de julio de 1993 hasta el 20 de julio de 2005 se trataron 364 pacientes a quienes se les extrajeron 609 catéteres endocavitarios de marcapasos o desfibriladores. Se analizaron las indicaciones, los abordajes, los sistemas de extracción y los resultados.
Los criterios de eficacia utilizados se basaron en las recomendaciones de la NASPE; se definió completa a la extracción de todo el catéter del sistema vascular, parcial al retiro de todo el catéter menos una pequeña porción < 4 cm del conductor y/o aislante y fracaso al abandono de una longitud importante del catéter después de un intento de extracción.
También en base a las recomendaciones de la NASPE, las complicaciones del procedimiento se clasificaron en mayores cuando requirieron intervención quirúrgica o transfusión para prevenir la muerte o había riesgo de vida o el resultado fue muerte o serio daño a la salud.
Se clasificaron como complicaciones menores aquellas que requirieron procedimientos quirúrgicos menores o tratamiento médico o prolongación de la internación o que limitaron la capacidad funcional del paciente, pero no pusieron en riesgo su vida ni causaron su muerte ni serio daño a su salud.
RESULTADOS
La población estudiada estuvo compuesta por 227 hombres (62,3%) y 137 mujeres (37,6%), con una edad promedio de 62,3 años, (rango 7-102), DE 18,15, mediana 66 años.
Se extrajeron 609 catéteres (1,67 catéteres por paciente), de los cuales 210 eran auriculares y 399, ventriculares. Entre los catéteres extraídos hubo 67 de cardiodesfibrilador, 4 de ellos de vena cava superior.
Con respecto al tipo de fijación, 220 eran de fijación activa (FA) y 389 de fijación pasiva (FP). Los catéteres auriculares fueron 186 de FA y 24 de FP. Los catéteres ventriculares fueron 35 de FA y 364 de FP.
El tiempo promedio de implantados de todos los catéteres fue de 63 meses (rango 1-354), DE 59,6, mediana 44.
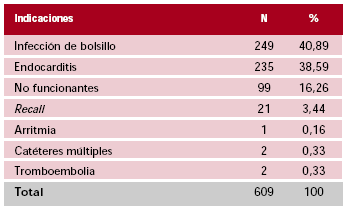
Las indicaciones para extracción de catéteres se resumen en la Tabla 1. Algunos de los pacientes con EB tenían bolsillos sanos y el origen de su infección se halló con punto de partida de otro foco (bucal, urinario, biliar, etc.).
Tabla 1. Indicaciones para la extracción de catéteres
Las vías de abordaje empleadas para efectuar la extracción de catéteres se detallan en la Tabla 2.
Tabla 2. Vías de abordaje para la extracción

Para los catéteres de desfibriladores, las indicaciones para extracción se enumeran en la Tabla 3 y las vías de abordaje empleadas se detallan en la Tabla 4.
Tabla 3. Indicaciones para la extracción de catéteres de desfibriladores

Tabla 4. Vías de abordaje para la extracción de catéteres de desfibriladores

Del total de 609 catéteres, 166 (27,2%) se extrajeron por TS. Su tiempo medio de implantados fue de 20,4 meses (rango 1-174), DE 25,5 meses, mediana 10 meses.
Los restantes 443 (72,7%) requirieron empleo de sistemas de extracción. Su longevidad media fue de 79,0 meses (rango 1-354, DE 61 meses, mediana 63 meses).
Los catéteres con FA (n = 220), 106 de ellos fueron extraídos por TS y 114 mediante extractores. Los catéteres con FP (n = 389), 62 se extrajeron por TS y 327 con extractores.
Catéteres de marcapasos
Se extrajeron 542 catéteres, con un tiempo de implantados de 65,1 meses (rango 1 a 354 meses). Por tracción simple se extrajeron 160 catéteres, con un tiempo de implantados de 20,7 meses (rango 1 a 174 meses). Los extractores se utilizaron en 382 catéteres con un tiempo de implantados de 83,8 meses.
Catéteres de cardiodesfibriladores
Si bien los catéteres de cardiodesfibrilador están incluidos en el total, algunos datos se presentan aquí en forma separada.
Se realizó la extracción de un total de 67 catéteres de cardiodesfibrilador de 56 pacientes (1,2 catéteres por paciente) con edades entre 21 y 83 años, promedio de 59,3 años, DE 14,6 años, mediana 63 años. La longevidad media de los cables fue de 45,7 meses (rango 1-137 meses), DE 29,2 meses, con una mediana de 42 meses.
Respecto del tipo de fijación, de los 67 electrodos de cardiodesfibrilador, 18 tenían FA y todos se retiraron mediante el extractor. Los restantes 49 eran de FP y solamente 6 se extrajeron mediante TS, con un tiempo de implantados de 12,6 meses. Se abordaron con extractores 61 catéteres, con un tiempo de implantados de 49 meses.
El diagrama de columnas de la Figura 1 muestra comparativamente el tiempo de implante y el método de extracción para el total de catéteres. Para los catéteres con pocos meses de implantados fue frecuente la utilización de la TS, pero a medida que los catéteres tenían una antigüedad mayor se utilizaron estiletes fijadores y vainas telescópicas con mayor frecuencia. Para la mayoría de los cables se utilizaron ambos instrumentos. Las vainas telescópicas se utilizaron"solas" en aquellos casos en que no fue posible introducir un estilete fijador.

Fig. 1. Tiempo desde el implante del catéter y método de extracción.
De un total de 609 catéteres, la extracción fue completa en 591 de 609 catéteres (97%), de los cuales en 166 (27,2%) fue mediante TS y 443 (72,7%) con el uso de sistemas de extracción. La extracción fue parcial en 14 de 609 catéteres (2,3%) aunque con éxito clínico. Hubo fracaso para la extracción de los cables en 4 de 609 (0,66%). Considerando el éxito clínico de la extracción parcial, la eficacia global es del 99,3%.
A pesar del menor tiempo de implantados, los catéteres de desfibrilador presentaron más dificultad para su retiro y en un porcentaje alto de ellos se requirieron los extractores. Ello puede deberse al grosor de los cables, sobre todo a nivel de las bobinas (coils), ya que éstas son invadidas más frecuentemente por el tejido fibroso.
El 85,1% de todos los pacientes necesitaron del sistema de extracción.
En el 83,1% de los pacientes con marcapasos fue necesario el sistema de extracción.
El 96,4% de los pacientes con cardiodesfibrilador requirieron el extractor.
Las complicaciones fueron:
a) Muerte: esta complicación mayor se produjo en tres pacientes. En un paciente, con catéter de cardiodesfibrilador de 128 meses, fue atribuible al procedimiento y en dos ocurrió por complicaciones anestésicas.
b) Se observó fístula entre arteria pulmonar derecha y bronquio en un paciente.
c) Las complicaciones menores fueron: hematomas de bolsillo en 5 casos, trombosis de subclavia en 3, hemopericardio en 2, fibrilación auricular en 1 (revirtió con cardioversión eléctrica), fibrilación ventricular en 3 (revirtieron con cardioversión eléctrica), embolia de pulmón en 2 (tratamiento médico) y desplazamiento de catéter funcionante en 1.
Con respecto al tiempo de internación posoperatorio, la mayoría de los pacientes fueron dados de alta entre las 24 y 48 horas de operados. Su tiempo de internación no dependió del procedimiento, sino del tratamiento antibiótico por su endocarditis.
DISCUSIÓN
La infección posimplante de marcapasos, una de las complicaciones más graves en los pacientes portadores de marcapasos y cardiodesfibriladores, es poco frecuente (1% a 7%). (16)
Furman (17) describió en 1991 que "la infección es la complicación más letal de los implantes de marcapasos". Refirió que la mayoría de las infecciones son causadas por Staphylococcus aureus o epidermidis y que aún no hay un tratamiento adecuado y exitoso para estas infecciones, lo cual hace imprescindible la extracción de todo el material.
Desde hace más de 10 años se documenta la necesidad de retirar todo el sistema de estimulación infectado. (18, 19) El no hacerlo puede derivar en complicaciones como fístulas crónicas, empiemas, fístula broncopleural, tromboflebitis, bacteriemia, endocarditis y pericarditis, para finalizar en sepsis, con una mortalidad de hasta el 66%. (20)
Se comunicaron casos aislados de aparentes curas de infecciones de catéteres o por lo menos supresión de la infección con tratamiento antibiótico asociado con diferentes procedimientos quirúrgicos (recolocación retropectoral del bolsillo o procedimientos para la preservación de los catéteres), (21-23) a fin de no realizar la extracción de los catéteres, con seguimientos de entre 5 y 11 meses. Estos casos deberían considerarse con reserva, porque la mayoría de las infecciones recidivan tarde o temprano.
Choo y colaboradores (24) trataron en forma conservadora a 23 pacientes infectados, enviados de otros centros, con los antibióticos endovenosos apropiados, sin extraer el sistema de estimulación. Este tratamiento fracasó en todos los casos y la recuperación de los pacientes se logró con la extracción completa del sistema. Esta misma opinión es sostenida por del Río y colaboradores, (25) quienes trataron médicamente a 7 pacientes que se negaron a la cirugía y en todos ellos la infección recidivó.
El mecanismo por el que el tratamiento antibiótico no es eficaz se debe a la colonización de las bacterias en el catéter, que forman un biofilm en el metal del tip, sobre el aislante, en el conductor interno, que parece protegerlas de los antibióticos y de las defensas del organismo. (26-28)
Klug y colaboradores (29) demostraron que el cultivo de la porción intravascular de los catéteres extraídos por infecciones del bolsillo fue positivo en el 79,3%.
Furman menciona las distintas posibilidades para extracción (nosotros, en algún paciente, hemos utilizado la tracción con pesas hasta 1993). En la actualidad las vías posibles son: 1) CCCA, 2) técnicas percutáneas con pig tails, lazos, canastillas, graspings, pinzas de biopsia, estiletes fijadores y vainas.
Lo importante es el retiro de los elementos intracavitarios, con el procedimiento que esté accesible en la institución en la que esté internado el paciente.
Con respecto a la extracción con estiletes y vainas, hay que tener en cuenta el tiempo de implante de los catéteres que se han de extraer. (30) El tejido fibroso puede ser suficiente como para obstruir las venas y, si supera los 8 años, puede tener bandas circunferenciales de tejido calcificado.
El otro elemento para tener en cuenta es la morbimortalidad de este procedimiento. Styrbys (31) comunicó en 1991 las posibles complicaciones de las extracciones: sangrado, hemopericardio, hemotórax, neumotórax, hemoneumotórax, trombosis de subclavia y vena cava superior, desgarro auricular, avulsión miocárdica, lesión de válvula tricúspide, rotura cardíaca, embolia de pulmón, arritmias ventriculares graves y muerte súbita, por lo que este procedimiento siempre debe realizarse con cirugía cardíaca stand-by.
A pesar de la gravedad de las complicaciones, éstas son poco frecuentes; las mayores no superan el 1,9% y la mortalidad es inferior al 1%, según la US Dabase. (32)
La mayoría de nuestros pacientes fueron enviados de otros centros, con indicación de extracción, después del fracaso de varios intentos de salvar el implante mediante distintas plásticas, tratamiento antibiótico prolongado, intentos infructuosos de extracción, catéteres cortados y/o embolizados, etc.
En coincidencia con la US Database, los factores más importantes que influyen en el éxito o el fracaso de la extracción son: el tiempo de implante, paciente joven, catéteres ventriculares versus auriculares y la experiencia del equipo médico.
Estadísticas de estudios comparativos
Al cierre de la US Database 1999 se habían operado 7.823 pacientes, a quienes se les extrajeron 12.833 catéteres (1,64 catéteres/paciente). Las indicaciones para el período 1998/1999 fueron: 30% infección de bolsillo, 5% endocarditis, casi 50% no funcionantes, 12% catéteres Accufix y 4% otros diagnósticos.
En la experiencia de Jarwe y colaboradores en 1999, (33) las extracciones se debieron 14% a recall de catéteres Accufix, 12% a no funcionantes, 32% a endocarditis y 41% a decúbitos más infecciones de bolsillo.
Las vías de extracción en los Estados Unidos fueron: 95% vía superior, 2% vía inferior, 3% vía combinada. En la US Database, la eficacia para los catéteres auriculares fue completa en el 95%, parcial en el 3% y fracasó en el 2%. Para los ventriculares fue completa en el 91%, parcial en el 7% y fracasó en el 2%.
Las complicaciones mayores para el período 1998/ 1999 fueron del 1,9%.
Según sexo y número de catéteres fue:
Pacientes con 1 catéter (50% de los pacientes): 2% las mujeres, 1% los hombres.
Pacientes con 2 catéteres (40% de los pacientes): 2% las mujeres, 1,5% los hombres.
Pacientes con 3 a 6 catéteres (10% de los pacientes): 6% las mujeres, 2% los hombres.
En nuestro país, la mayor cantidad de indicaciones se debe a infección/decúbito de bolsillo y/o catéteres o por EB.
En el caso de la EB y ante la presencia de vegetaciones, cabe la pregunta: ¿qué vía se debe utilizar, percutánea o CCCA? Hay discusiones al respecto y el punto de inflexión pasaría por el tamaño de la vegetación. Algunos autores opinan que si supera los 15 mm debería indicarse CCCA. (34) Otros prefieren la eventual complicación de una embolia bacteriana de pulmón a las complicaciones de la bomba. (35, 36)
En nuestra experiencia, ninguno fue derivado a CCCA como consecuencia de su endocarditis. Hubo vegetaciones de hasta 40 mm y dos embolias de pulmón tuvieron buena evolución con tratamiento médico.
La posibilidad de utilizar la TS fue inversamente proporcional al tiempo de implantado el catéter. Para catéteres con menos de 6 meses, la TS fue eficaz en el 88,3% (fracasó en el 11,7%), mientras que para los catéteres de entre 6 y 12 meses el fracaso fue del 44%. Para catéteres de entre 12 y 24 meses, el fracaso fue del 64% y para los de entre 24 y 36 meses fue del 73%. Sobre 186 catéteres con más de 60 meses de implantados, solamente 7 (3,7%) se extrajeron mediante TS. Estas cifras son similares a las de la US Database.
CONCLUSIÓN
Sobre la experiencia de doce años en la extracción de catéteres de marcapasos y desfibriladores por vía percutánea, puede concluirse que esta técnica ha venido a reemplazar a la CCCA, con muy baja mortalidad atribuible al método, bajo índice de complicaciones y alto porcentaje de eficacia. Aun así, este procedimiento debe realizarse con cirugía cardíaca stand-by. En caso de complicaciones graves o ante la imposibilidad de una extracción exitosa en un paciente con una patología que comprometa su vida (EB o arritmias graves) se debe convertir en cirugía a cielo abierto.
La evolución posoperatoria de los pacientes con extracción percutánea fue buena, su tiempo de internación no dependió del procedimiento, sino del tiempo de tratamiento antibiótico por su endocarditis. El resto de los pacientes fueron dados de alta entre las 24 y las 48 horas.
Para finalizar, nos parece válido el concepto expresado por Tyers: "Donde existen centros con esta subespecialidad, para la extracción de catéteres crónicamente implantados no puede considerarse la conducta de "tirar y mirar qué pasa". Particularmente, tirar de los catéteres, cortarlos y permitir que se retraigan y embolicen en el lecho vascular es una práctica inaceptable que pone en riesgo al paciente y a futuros extraccionistas". (37)
* El equipo estaba formado por los Dres. Héctor Mazzetti, María Cristina Tentori y Eduardo Dussaut
1. Dussaut A, Vedoya R, Lozada B, Oglietti R, Mazzetti H. Tratamiento quirúrgico de la endocarditis bacteriana, en pacientes con marcapasos endocavitarios. Academia Argentina de Cirugía. Buenos Aires, 1980. Rev Argent Cirug 1980; 39:167-73. [ Links ]
2. Dussaut A, Lozada B, Mazzetti H, Tentori M, Dussaut E. Iatrogenia y marcapasos implantables. Academia Argentina de Cirugía, 1985. Rev Argent Cirug 1985;49:35-8. [ Links ]
3. Alt E, Neuzner J, Binner L, Gohl K, Res JC, Knabe UH, et al. Three-year experience with a stylet for lead extraction: a multicenter study. Pacing Clin Electrophysiol 1996;19:18-25. [ Links ]
4. Brodell GK, Castle LW, Maloney JD, Wilkoff BL. Chronic transvenous pacemaker lead removal using a unique, sequential transvenous system. Am J Cardiol 1990;66:964-6. [ Links ]
5. Byrd CL. Extracting chronically implanted pacing clin electrophysiolmaker leads using the spectranetics excimer laser; initial clinical experience. Pacing Clin Electrophysiol 1996;19:567 (Abstract). [ Links ]
6. Alt E, Theres H, Reinhardt J. First clinical use of a new extraction stylet for removal of infected leads. Pacing Clin Electrophysiol 1992;15:572 (Abstract). [ Links ]
7. Goode LB, Byrd CL, Wilkoff BL, Clarke JM, Fontaine JM, Fearnot NE, et al. Development of a new technique for explantation of chronic transvenous pacemaker leads: five initial case studies. Biomed Instrum Technol 1991;25:50-3. [ Links ]
8. Reinhardt J, Höcheri M, Babczynski K. Removal of chronic implanted leads using a new technology in 25 cases. European J Cardiac Pacing and Electrophysiology 1992;2:A77 (Abstract). [ Links ]
9. Fearnot NE, Smith HJ, Goode LB, Byrd CL, Wilkoff BL, Sellers TD. Intravascular lead extraction using locking stylets, sheaths, and other techniques. Pacing Clin Electrophysiol 1990;13:1864-70. [ Links ]
10. Byrd CL, Schwartz SJ, Hedin NB, Goode LB, Fearnot NE, Smith HJ. Intravascular lead extraction using locking stylets and sheaths. Pacing Clin Electrophysiol 1990;13:1871-5. [ Links ]
11. Byrd CL. Extracting chronically implanted pacing clin electrophysiolmaker leads using the spectranetics excimer laser; initial clinical experience. Pacing Clin Electrophysiol 1996;19:567 (Abstract). [ Links ]
12. Wilkoff B, Byrd C, Love C, Goode L, Norlander B, Heise H, et al. A bipolar electrosurgical dissection sheath for lead extraction: results of the multicenter feasibility study. Pacing Clin Electrophysiol 2000; 23:679 (Abstract). [ Links ]
13. Mazzetti H, Tentori C, Dussaut E, Lázzari J. Técnica alternativa de extracción de catéteres endocavitarios atrapados. Rev Argent Cirug 1996;70: 61-3. [ Links ]
14. De Rosa AF, Tentori MC, Mascheroni O, Mazzetti H. Endocarditis infecciosa asociada con marcapasos y cardiodesfibriladores. Formas de presentación, tratamiento y comparación con el resto de las endocarditis. Rev Argent Cardiol 2004;72:203-7. [ Links ]
15. Love CJ, Wilkoff BL, Byrd CL, Belott PH, Brinker JA, Fearnot NE, et al. Recommendations for extraction of chronically implanted transvenous pacing and defibrillator leads: indications, facilities, training. North American Society of Pacing and Electrophysiology Lead Extraction Conference Faculty. Pacing Clin Electrophysiol 2000;23:544-51. [ Links ]
16. Myers MR, Parsonnet V, Bernstein AD. Extraction of implanted transvenous pacing leads: a review of a persistent clinical problem. Am Heart J 1991;121:881-8. [ Links ]
17. Furman S. Removal of implanted hardware. Pacing Clin Electrophysiol 1991;14:735 (Editorial). [ Links ]
18. Byrd C, Schwartz S, Hedin N, Saunkeak B. Experience with 234 Pocket Infections: What Works? Pacing Clin Electrophysiol 1992; 15:510. [ Links ]
19. Vogt PR, Sagdic K, Lachat M, Candinas R, von Segesser LK, Turina MI. Surgical management of infected permanent transvenous pacemaker systems: ten year experience. J Card Surg 1996;11:180-6. [ Links ]
20. Rettig G, Doenecke P, Sen S, Volkmer I, Bette L. Complications with retained transvenous pacing clin electrophysiolmaker electrodes. Am Heart J 1979;48:587-94. [ Links ]
21. Chait LA, Ritchie B. A method of treating the exposed cardiac pacemaker. Br J Plast Surg 1979;32:281-4. [ Links ]
22. Yamada M, Takeuchi S, Shiojiri Y, Maruta K, Oki A, Iyano K, et al. Surgical lead-preserving procedures for pacemaker pocket infection. Ann Thorac Surg 2002;74:1494-9. [ Links ]
23. Valente A, Pochini M, Pinto AM. Subpectoral Pacing Clin Electrophysiolmaker implantation technique for treatment of generador pocket infection: inicial study. Rev Bras Cir Cardiovasc 2001;16:49-52. [ Links ]
24. Choo MH, Holmes DR Jr, Gersh BJ, Maloney JD, Merideth J, Pluth JR, et al. Permanent pacemaker infections: characterization and management. Am J Cardiol 1981;48:559-64. [ Links ]
25. del Rio A, Anguera I, Miro JM, Mont L, Fowler VG Jr, Azqueta M, et al; Hospital Clinic Endocarditis Study Group. Surgical treatment of pacemaker and defibrillator lead endocarditis: the impact of electrode lead extraction on outcome. Chest 2003;124:1451-9. [ Links ]
26. Peters G, Saborowski F, Locci R, Pulverer G. Investigations on staphylococcal infection of transvenous endocardial pacemaker electrodes. Am Heart J 1984;108:359-65. [ Links ]
27. Peters G, Locci R, Pulverer G. Adherence and growth of coagulase- negative staphylococci on surfaces of intravenous catheters. J Infect Dis 1982;146:479-82. [ Links ]
28. Baddour LM, Bettmann MA, Bolger AF, Epstein AE, Ferrieri P, Gerber MA, et al; AHA. Nonvalvular cardiovascular device-related infections. Circulation 2003;108:2015-31. [ Links ]
29. Klug D, Wallet F, Lacroix D, Marquie C, Kouakam C, Kacet S, Courcol R. Local symptoms at the site of pacemaker implantation indicate latent systemic infection. Heart 2004;90:882-6. [ Links ]
30. Byrd CL, Schwartz SJ, Hedin NB, Goode LB, Fearnot NE, Smith HJ. Intravascular lead extraction using locking stylets and sheaths. Pacing Clin Electrophysiol 1990;13:1871-5. [ Links ]
31. Stirbys P. Removable or nonremovable endocardial electrodes: do not accept erroneous conclusions. Pacing Clin Electrophysiol 1991; 14:858-9. [ Links ]
32. Wilkoff B. Whats New in Lead Extraction. Pacing Clin Electrophysiol 2000;1:D2 (Abstract). [ Links ]
33. Jarwe M, Klug D, Beregi JP, Le Franc P, Lacroix D, Kouakam C, et al. Single center experience with femoral extraction of permanent endocardial pacing leads. Pacing Clin Electrophysiol 1999;22:1202-9. [ Links ]
34. Chiu WS, Nguyen D. Pacemaker lead extraction in pacemaker endocarditis with lead vegetation: usefulness of transesophageal echocardiography. Can J Cardiol 1998;14:87-9. [ Links ]
35. Nguyen KT, Neese P, Kessler DJ. Successful laser-assisted percutaneous extraction of four pacemaker leads associated with large vegetations. Pacing Clin Electrophysiol 2000;23:1260-2. [ Links ]
36. Meier-Ewert HK, Gray ME, John RM. Endocardial pacemaker or defibrillator leads with infected vegetations: a single-center experience and consequences of transvenous extraction. Am Heart J 2003;146:339-44. [ Links ]
37. Tyers GF. Similar indications but different methods: should there be a consensus on optimal lead extraction techniques? Pacing Clin Electrophysiol 2002;25:1019-22. [ Links ]














